鲁教版_九年级化学__第三单元第一节第一课时_溶液的形成(上课用)
- 格式:ppt
- 大小:1.68 MB
- 文档页数:28

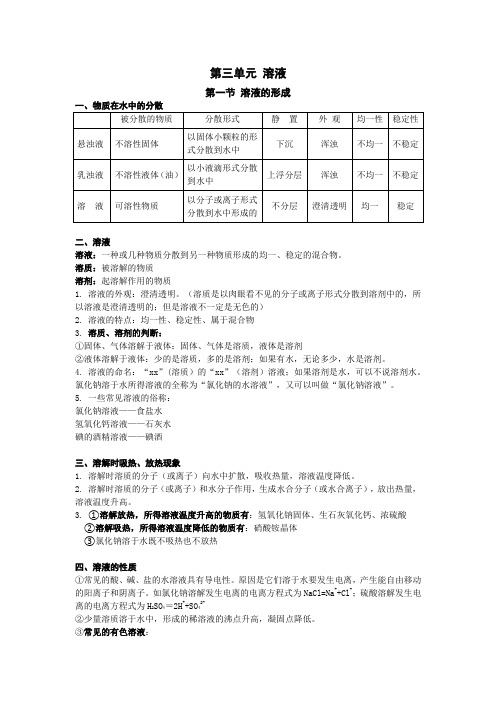
第三单元溶液第一节溶液的形成一、物质在水中的分散二、溶液溶液:一种或几种物质分散到另一种物质形成的均一、稳定的混合物。
溶质:被溶解的物质溶剂:起溶解作用的物质1.溶液的外观:澄清透明。
(溶质是以肉眼看不见的分子或离子形式分散到溶剂中的,所以溶液是澄清透明的;但是溶液不一定是无色的)2.溶液的特点:均一性、稳定性、属于混合物3.溶质、溶剂的判断:①固体、气体溶解于液体:固体、气体是溶质,液体是溶剂②液体溶解于液体:少的是溶质,多的是溶剂;如果有水,无论多少,水是溶剂。
4.溶液的命名:“xx”(溶质)的“xx”(溶剂)溶液;如果溶剂是水,可以不说溶剂水。
氯化钠溶于水所得溶液的全称为“氯化钠的水溶液”,又可以叫做“氯化钠溶液”。
5.一些常见溶液的俗称:氯化钠溶液——食盐水氢氧化钙溶液——石灰水碘的酒精溶液——碘酒三、溶解时吸热、放热现象1.溶解时溶质的分子(或离子)向水中扩散,吸收热量,溶液温度降低。
2.溶解时溶质的分子(或离子)和水分子作用,生成水合分子(或水合离子),放出热量,溶液温度升高。
3.①溶解放热,所得溶液温度升高的物质有:氢氧化钠固体、生石灰氧化钙、浓硫酸②溶解吸热,所得溶液温度降低的物质有:硝酸铵晶体③氯化钠溶于水既不吸热也不放热四、溶液的性质①常见的酸、碱、盐的水溶液具有导电性。
原因是它们溶于水要发生电离,产生能自由移动的阳离子和阴离子。
如氯化钠溶解发生电离的电离方程式为NaCl=Na++Cl-;硫酸溶解发生电离的电离方程式为H2SO4=2H++SO42-②少量溶质溶于水中,形成的稀溶液的沸点升高,凝固点降低。
③常见的有色溶液:蓝色溶液(含Cu 2+):硫酸铜溶液,氯化铜溶液,硝酸铜溶液浅绿色溶液(含Fe 2+):硫酸亚铁溶液,氯化亚铁溶液,硝酸亚铁溶液黄色溶液(含Fe 3+):硫酸铁溶液,氯化铁溶液,硝酸铁溶液 紫红色溶液:高锰酸钾溶液 紫色溶液:石蕊溶液五、饱和溶液与不饱和溶液1. 定义:在一定温度下,一定量的溶剂里,不能再继续溶解某种溶质的溶液,就是该溶质的饱和溶液。



溶液的形成教案课时1[教学目标]1.了解溶液、溶质、溶剂的概念,2.初步了解溶液的重要应用。
3.能识别常见溶液中的溶质和溶剂。
4.知道乳浊液及乳化现象。
[教学重点] 溶液、溶质、溶剂的概念[教学难点]1.溶液概念的建立。
2.溶解与乳化的区别。
[教学方法]实验探究法。
[教学用品] 实验仪器、药品、用品,教学媒体等[教学过程]一、新课导入由海水切入课题,引入新课(板书:课题1 溶液的形成)。
二、探究活动1(探究溶液的形成过程)1.学生实验:向实验桌上盛有50mL水的小烧杯中,加入一药匙食盐,用玻璃棒搅拌(教师巡回指导)。
2.师生活动1(建立溶液的概念):(1)学生描述实验现象。
(2)引导学生分析两种物质“消失”的原因。
(3)协助学生分析(体验)溶液的特征。
(4)建立溶液的初步概念并板书。
3.师生活动2(建立溶质、溶剂的概念): (1)溶质:被溶解的物质溶剂 (2)能溶解其它物质的物质。
(3)总结出溶质、溶剂三者之间的关系。
4.师生活动3(填写表格,让学生掌握溶质溶剂判断的一般方法):5.师生活动4:引导学生发现——溶质能够是固体、液体或气体;水是常见的溶剂;两种液体(不包括水在内)互溶时,将量多作为溶剂,量少的作为溶质。
6.师生活动5:探究物质溶解时的温度变化三、探究活动2(乳浊液及乳化现象)1.学生实验:观察步骤1试管中的液体振荡前、振荡后、静置后的现象。
2.学生实验:向步骤1试管中滴加2-3滴洗涤剂,按照振荡前、振荡后,静置后的顺序仔细观察实验现象。
3.建立乳浊液的概念:小液滴分散到液体里形成的混合物叫做乳浊液。
4.分析洗涤剂的去污原理教学反思:一、这节课的研究问题不是由我生硬地提出而是创设情景以演示实验和谈话的方式让学生根据自己生活中的经验主动的去发现问题,想要亲自动手研究的问题,这样有效的激发了学生学习的积极性、主动性。
二、其实让学生真正科学地经历过程并非易事,学生在课堂热热闹闹地活动起来,并不等同于真正的科学探究过程,有形无神的活动不是我们所倡导的,关键是看你的教学设计是否有利于学生在活动中自主发挥作用,并清楚地意识到自己是自身行为的主导者、科学探究活动的主人,无论得到的答案是对或错,都理应是调查研究的结果。

第一节溶液的形成
第1课时
一、教学目标
1.认识溶液溶解的本质和溶液的特征。
2.知道溶液、溶剂、溶质的概念;知道水是常见的溶剂,酒精、汽油等也是常见的溶剂。
3.了解溶液、浊液的区别以及它们在实际生活和生产中的应用。
4.进一步体会宏观现象和微观世界的联系,形成化学学科独特的观点—微粒观。
二、教学重难点
重点:溶液、溶剂、溶质的概念;知道水是常见的溶剂,酒精、汽油等也是常见的溶剂。
难点:溶液、浊液的区别以及它们在实际生活和生产中的应用。
三、教学准备
食盐、烧杯、蒸馏水、少量汽油、植物油、试管、酒精、碘粒等、教学资源动画氯化钠溶解等。
四、教学过程
五、板书设计
第一节溶液的形成
第1课时
一、氯化钠的溶解
实验操作:
现象:
微观解释:
二、溶液
概念:种或几种物质分散到另一种物质里,形成均一、稳定的混合物。
组成:由溶质和溶剂组成
命名:“溶质的名称+的+溶剂的名称+溶液”
用途:溶液在日常生活、工农业生产和科学研究中具有广泛的用途。