配位化学发展简史与现状
- 格式:ppt
- 大小:383.50 KB
- 文档页数:34

第1章配位化学导论配位化学(coordination chemistry)是无机化学的一个重要分支学科。
配位化合物(coordination compounds)(有时称络合物complex)是无机化学研究的主要对象之一。
配位化学的研究虽有近二百年的历史,但仅在近几十年来,由于现代分离技术、配位催化及化学模拟生物固氮等方面的应用,极大地推动了配位化学的发展。
它已广泛渗透到有机化学、分析化学、物理化学、高分子化学、催化化学、生物化学等领域,而且与材料科学、生命科学以及医学等其他科学的关系越来越密切。
目前,配位化合物广泛应用于工业、农业、医药、国防和航天等领域。
1.1 配位化学发展简史历史上记载的第一个配合物是普鲁士蓝。
它是1704年由柏林的普鲁士人迪斯巴赫(Diesbach)制得,它是一种无机颜料,其化学组成为Fe4[Fe(CN)6]3·nH2O。
但是对配位化学的了解和研究的开始一般认为是1798年法国化学家塔萨厄尔(B.M.Tassaert)报道的化合物CoCl3·6NH3,他随后又发现了CoCl3·5NH3、CoCl3·5NH3·H2O、CoCl3·4NH3以及其他铬、铁、钴、镍、铂等元素的其他许多配合物,这些化合物的形成,在当时难于理解。
因为根据经典的化合价理论,两个独立存在而且都稳定的分子化合物CoCl3和NH3为什么可以按一定的比例相互结合生成更为稳定的“复杂化合物”无法解释,于是科学家们先后提出多种理论,例如,布隆斯特兰德(W.Blomstrand)在1869年、约尔更生(S.M.Jørgensen)在1885年分别对“复杂化合物”的结构提出了不同的假设(如“链式理论”等),但由于这些假设均不能圆满地说明实验事实而失败。
1893年,年仅27岁的瑞士科学家维尔纳(A.Werner)发表了一篇研究分子加合物的论文“关于无机化合物的结构问题”,改变了此前人们一直从平面角度认识配合物结构的思路,首次从立体角度系统地分析了配合物的结构,提出了配位学说,常称Werner配位理论,其基本要点如下:(1) 大多数元素表现有两种形式的价,即主价和副价;(2) 每一元素倾向于既要满足它的主价又要满足它的副价;(3) 副价具有方向性,指向空间的确定位置。

无机化学中的配位化学理论是研究配合物形成、结构和性质的学科。
配合物是指由两个或多个离子或分子间的配位键结合而成的复合物,其中一个离子或分子起着配位中心的作用,其他则作为配体。
配位键一般由金属离子或原子与一个或多个配体的配位作用形成。
配位化学理论是无机化学领域一个重要的分支,它能够解释许多无机化学现象和化学反应。
一、配位化学的历史配位化学是早期化学家研究无机化合物所产生的。
18世纪末,Bergman首次提出了“配位”的概念,认为金属离子可以和一些特定的分子或离子发生化学反应,在这种反应中所产生的化合物称为配合物。
19世纪中叶,水合物和铜酰胺的合成让配合物变得更加重要。
20世纪初,单位配合数的概念被提出,并在1930年代得到广泛应用。
1952年,Jørgensen首次提出了“配位键”的概念,为配位化学理论的快速发展奠定了基础。
此后,人们逐渐深入研究了配合物的结构和性质,配位化学理论也得到了更为深刻的认识。
二、配位键的形成配位化学的核心是配位键的形成。
配位键可以分为共价性和离子性两种。
共价式键通常存在于过渡金属配合物中,它由金属离子的未满足配位电子对与配体的配位电子对相互重叠形成。
而离子式键则通常存在于铜、银和金等含d10电子的金属配合物中,它由金属离子的正电荷和配体的负电荷静电作用形成。
此外,还有一种类似氢键的键,即氢键型配位键,它主要存在于氢氧根、氨、水和羟基等配体中。
三、配位环境的影响配合物的结构和性质取决于配位环境,即最内层的配体、次内层的离子和周围溶剂的影响。
其中,配体的种类、数量和配位位置是影响配合物结构的关键因素。
次内层的离子通过配位作用能够改变配合物的电荷和几何构型。
而溶剂分子也能与金属离子配位形成溶剂合金属离子,并影响配合物的物理化学性质。
此外,温度、压力、电场等外部因素也会影响配合物的性质。
四、配合物的分类配合物可以根据金属离子的性质、配体的性质和功能进行分类。
根据金属离子的性质,配合物可以分为过渡金属配合物、主族金属配合物和内过渡金属配合物。

化学反应中的配位化学化学反应中的配位化学是一门研究化学反应中配位物质的反应性质和化学变化的学科。
它在化学领域中具有重要的地位和作用,涉及到化学、物理、材料等多个领域。
本文将从配位化学的基础知识、应用现状和未来展望三个方面来探讨化学反应中的配位化学。
一、配位化学的基础知识1. 配位化学的概念配位化学是指利用有机或配位物与金属离子之间的化学反应,形成络合物(配合物)的一门化学学科。
配合物是指由中心离子(金属离子)和一定数量的配体(有机物或无机物)通过共价键或配位键形成的化合物,具有明确的化学性质和结构特征。
2. 配位化学的基本结构配位化学中离子的配位方式分为三种:线性型、分支型和环状型。
其中,线性型是指配体在金属离子周围形成的一条直线,如[Co(NH3)6]2+;分支型是指配体在金属离子周围形成的一条分支结构,如[Cr(edta)]-;环状型是指配体在金属离子周围形成的一个环结构,如[Mn(H2O)6]2+。
3. 配位化学的反应机制配位化学反应机制主要包括化学键的形成和断裂过程。
在形成化学键的过程中,配体发生了配位键形成的反应,即配体的一个或多个可供给位点上出现一个共价或配位键,形成配合物。
在断裂化学键的过程中,反应产物的配体发生了离去或转移反应,即配合物中的一个或多个配体由于其它反应的作用而离去或被替代。
二、配位化学的应用现状1. 金属配合物在催化反应中的应用金属配合物在催化反应中起到了至关重要的作用。
它可以加速反应速率、提高产率、减少副产物、改善反应条件等多种效果。
如:铂催化剂可以帮助丙烷的氧化反应,使其转化为丙酮。
另外,其他金属如镍、铁、钒、铬等也可以用作催化剂。
2. 金属配合物在材料领域中的应用金属配合物在材料领域中有广泛的应用,可以制备出多种性质优异的材料。
如:可溶于水的金属离子与各种溶液中的有机物反应,可以制备出具有吸附性、交换性和载体性的离子交换树脂。
此外,配位化学也可以用于制备与生物有关的材料,如透明质酸等。


无机化学中的配位化学研究配位化学是无机化学的一个重要分支领域,也是一门非常重要的交叉学科。
研究配位化学可以帮助我们更深入地理解化学世界中的各种现象和规律,同时也为人类社会的发展做出了重要的贡献。
在无机化学中,配位化学是一个十分广泛的领域,它与许多领域有联系:有机化学、生物化学以及材料科学等等。
下面将对配位化学的研究进行探讨,探究它对于化学学科的贡献以及现今配位化学研究所涉及到的一些重要领域。
配位化学的概念和历史所谓配位化学,即研究有机或无机物中金属离子形成的配合物的性质、构造及反应规律的一门学科。
自19世纪以来,配位化学就在逐渐发展着,经过不断的努力,我们可以逐渐深入地了解其本质及应用。
最早对配位化学的研究是由一位名叫阙步达的荷兰人在19世纪时提出的,他研究了一些由无机化合物和有机化合物组成的复合物的性质,标志着配位化学这个学科首次被正式提出。
配位化学的重要性配位化学是无机化学中一个非常重要的分支,它主要研究的是由金属离子和配体组成的化合物,这些化合物具有不同的性质和功能。
人们通过研究配位化学,可以更好地理解生命过程、原子化学结构、催化反应等领域的现象,同时也可以帮助人们开发出新的材料和催化剂,从而推动化学技术的不断发展。
配位化学在生命科学中的应用生命科学是配位化学的重要应用领域之一。
在生物体内,各种配合物的形成与解除都是通过生物分子之间的相互作用实现的。
例如,在人体中,血液中的铁原子与血红蛋白中的组氨酸、组氨酸的酸化与去质子化作用就是一个配位反应。
此外,研究配位化学还可以帮助我们更好地理解一些生化过程,比如红细胞运输氧的过程和生物体中的金属离子的代谢过程。
配位化学在物质科学中的应用近些年来,金属有机框架化合物(MOF)引起了物质科学领域的广泛关注。
MOF是由金属离子和有机骨架组成的开放式结构化合物,在气体吸附、化学催化、分子识别、药物输送等方面都具有巨大的潜力。
例如,通过调整金属离子和有机配体的种类和比例,可以调节金属有机框架材料的结构和性质,进而实现吸附和分离气体、催化反应等功能。

配位化学史
配位化学是化学的一个分支,研究形成有机和无机化合物中的中心金属离子(称为配位中心)和周围配体之间的结构、性质和反应。
配位化学起源于18世纪末和19世纪初的化学研究,当时化学家开始注意到一些化合物中金属离子与其他分子之间的特殊相互作用。
然而,直到19世纪中叶,配位化学的独立分支才开
始发展起来。
在19世纪,研究人员开始注意到一些群体非常稳定地与金属
离子结合,并且能够形成命名化合物。
这些分子或离子被称为配体,可以通过与金属离子形成配位键。
在19世纪中叶,法
国化学家亨利·卡斯规定了一组基本的配位化合物形成规则,
为配位化学奠定了基础。
随着对配位化学的研究的不断深入,越来越多的配体和配位化合物被发现。
在20世纪初,研究人员开始提出有关配位键的
理论模型。
对于有机金属化合物,研究人员提出了茂金属的结构和反应机理。
随着X射线晶体学的发展,研究人员能够解
析配位化合物的结构,从而揭示了它们的空间构型和键的类型。
在20世纪50年代和60年代,配位化学得到了广泛的发展和
应用。
研究人员发展了许多用于合成和控制配位化合物性质的方法。
此外,他们还研究了配位化合物在催化、光化学和磁性材料方面的应用。
现代配位化学也与生物无机化学及其在药物设计和生物催化等领域的应用有着密切的关联。
总的来说,配位化学的发展经历了几个关键的阶段,包括发现和命名配体、提出配位键的理论模型以及应用于不同领域的研究。
该领域的研究为我们对金属离子和配位化合物性质的理解提供了重要的基础,也为材料科学和生物无机化学方面的研究提供了重要的支持。

配位化学现状及发展第一篇:配位化学现状及发展配位化学的现状及发展专业班级:化学(师范类)一班姓名:刘楠楠课程名称:配位化学摘要:配位化学已成为当代化学的前沿领域之一。
它的发展打破了传统的有机化学和无机化学之间的界线。
其新奇的特殊性能在生产实际中得到了重大的应用,花样繁多的价健理论及空间结构引起了结构化学和理论化学家的深切关注。
它和物理化学、有机化学、生物化学、固体化学、环境化学相互渗透,使其成为贯通众多学科的交叉点。
本文将介绍配位化学在近几年的现状和发展。
关键词:配位化学;现状;发展配位化学是在无机化学基础上发展起来的一门交叉学科,50年代以来配位化学以其与有机合成化学和结构化学相结合为特点,开始了无机化学的复兴时期,从而在实际上打破了传统的无机、有机和物理化学间的界限,进而成为各化学分支的结合点。
配合物以其花样繁多的价键和空间结构促进了基础化学的发展,又以其特殊的性质在生产实践和科学实验中取得了重大的应用。
配位化学是化学学科中最活跃的,具有很多生长点的前沿学科之一,它的近期发展趋势如下。
1.具有特殊性质和特殊结构配合物的合成、结构及性能的研究各种大环、夹心、多核、簇状、非常氧化态、非常配位数、混合价态及各种罕见构型配合物的合成、结构、热力学、动力学和反应性的研究正在深入。
其中巨型原子簇的研究已成为阐明金属原子化学和固体金属化学异同的桥梁;新型球型大环,聚邻苯酚脂大环配体对某些金属离子具有特殊高的选择性;在CO,CO2,H2和CH4等小分子配合物及活化方面,已发现用Co+,Li+ 双核配合物不仅可与CO2配位,并使其活化,而形成C—C键;此外H2的配合物研究及H2的活化亦在深入。
配合物合成、结构和性能研究方面,近年来的一个引人注目的动向是配位化学和固体化学的交叉[1]。
一系列具有链状、层片状和层柱状特殊结构的配合物已经合成。
对它们的性质和结构,正在进行系统研究。
2.溶液配位化学研究溶液配位化学研究正在继续深入,但已具有新的内容。


化学中的配位化学理论化学是一门非常重要的科学领域,而配位化学则是化学中的一个非常重要的分支。
配位化学主要研究的是金属离子和配体形成配合物的化学原理。
在配合物中,金属离子与配体之间形成了化学键,而这种化学键的形成与配合物的性质密切相关。
因此,探讨配位化学理论对于了解配合物的性质,开发新型配位剂等具有极其重要的意义。
一、配位化学的历史配位化学是一门历史悠久的学科,最早可以追溯到十九世纪末期。
当时的化学家们发现,金属离子在水溶液中可以与其他分子形成配合物。
这些配合物在物理性质上与单纯的金属离子有了很大的不同,如颜色发生变化、熔点降低等。
因此,化学家们开始思考:这些变化是由什么原因引起的?如何解释这些现象?在接下来的几十年里,化学家们逐渐摸索出了配位化学的一些基本原理。
他们发现,配合物的物理性质与其电荷、配位数、配位形式等因素有关。
于是,配位化学作为一门独立的学科开始逐渐成形。
二、配位化学的基本概念在配位化学中,配体是指与金属离子形成复合物的分子或离子,而金属离子则是中心原子。
而金属离子和配体之间形成的化学键则是配位键。
配位键是通过配体上的配位原子与金属离子之间的电子云重叠形成的。
金属离子和配体之间的配位数是一个非常重要的概念。
配位数是指与金属离子相邻的配位原子数,它可以决定配合物的稳定性。
通常情况下,金属离子的配位数在2-6之间。
除此之外,配位化学中还有一些非常重要的概念,如络合物、配合物、低自旋态、高自旋态等。
三、配位化学理论的发展在配位化学的发展过程中,出现了许多重要的理论。
这些理论不仅可以解释已知的化学现象,而且还可以指导开发新型的配位剂,用于各种重要的工业应用。
(一)丙二酮孪生体理论丙二酮孪生体理论是指配位化合物的中心离子周围的配体可被视为由, 配体中存在着两个互为孪生体的化学键。
这种情况下,配位合物中的中心离子会被包围在一个对称的分子构型中。
该理论最早由瑞典化学家保罗·克鲁特·沙曼在1925年提出。

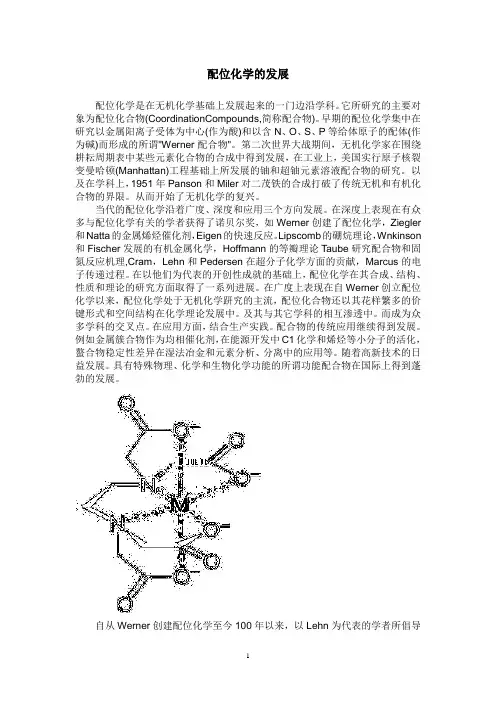
配位化学的发展配位化学是在无机化学基础上发展起来的一门边沿学科。
它所研究的主要对象为配位化合物(CoordinationCompounds,简称配合物)。
早期的配位化学集中在研究以金属阳离子受体为中心(作为酸)和以含N、O、S、P等给体原子的配体(作为碱)而形成的所谓"Werner配合物"。
第二次世界大战期间,无机化学家在围绕耕耘周期表中某些元素化合物的合成中得到发展,在工业上,美国实行原子核裂变曼哈顿(Manhattan)工程基础上所发展的铀和超铀元素溶液配合物的研究。
以及在学科上,1951年Panson和Miler对二茂铁的合成打破了传统无机和有机化合物的界限。
从而开始了无机化学的复兴。
当代的配位化学沿着广度、深度和应用三个方向发展。
在深度上表现在有众多与配位化学有关的学者获得了诺贝尔奖,如Werner创建了配位化学,Ziegler 和Natta的金属烯烃催化剂,Eigen的快速反应。
Lipscomb的硼烷理论,Wnkinson 和Fischer发展的有机金属化学,Hoffmann的等瓣理论Taube研究配合物和固氮反应机理,Cram,Lehn和Pedersen在超分子化学方面的贡献,Marcus的电子传递过程。
在以他们为代表的开创性成就的基础上,配位化学在其合成、结构、性质和理论的研究方面取得了一系列进展。
在广度上表现在自Werner创立配位化学以来,配位化学处于无机化学趼究的主流,配位化合物还以其花样繁多的价键形式和空间结构在化学理论发展中。
及其与其它学科的相互渗透中。
而成为众多学科的交叉点。
在应用方面,结合生产实践。
配合物的传统应用继续得到发展。
例如金属簇合物作为均相催化剂,在能源开发中C1化学和烯烃等小分子的活化,螯合物稳定性差异在湿法冶金和元素分析、分离中的应用等。
随着高新技术的日益发展。
具有特殊物理、化学和生物化学功能的所谓功能配合物在国际上得到蓬勃的发展。
自从Werner创建配位化学至今100年以来,以Lehn为代表的学者所倡导的超分子化学将成为今后配位化学发展的另一个主要领域。
配位化学的发展史摘要自从1893年瑞士化学家维尔纳创立配位化学已来,配位化学理论得到不断发展,逐渐完善。
经过化学家们100多年的努力,由传统经典的配合物,发展到今天的配位超分子化合物,并显示出结构和功能上的优越特性,成为现代无机化学的一个发展方向。
关键词配位化学晶体工程配位超分子化学自从1893年瑞士化学家维尔纳(Werner)在德国《Journal of Inorganic Chemistry》上发表了题为“对于无机化合物结构的贡献”的配位化学方面的第一篇经典著作之后[1],原本作为无机化学分支的配位化学发展极为迅速,并始终处于无机化学研究的主流。
配位化学的发展打破了传统的有机化学和无机化学之间的界限,在众多配合物中金属离子和有机配体形成的配合物以其花样繁多的价键形式和空间结构,在化学键理论发展、配合物性能等多样性方面引起了人们广泛的研究兴趣。
1 经典配位化学的产生和发展配合物的记载在很早就有,国外文献[2]最早记录的配合物—普鲁士蓝(Prussian Blue)是在1704年,其化学结构是FeIII4[FeII(CN)6]3,距今已有300年历史了。
我国《诗经》记载“缟衣茹藘”,“茹藘在阪”,实际上是二羟基蒽醌和铝钙离子生成红色配合物(比普鲁士蓝发现早2000多年)。
最早关于配合物的研究是1798年法国塔索尔特(Tassert)关于黄色氯化钴([Co(NH3)6]Cl3)的研究,他在CoCl2溶液中加入NH3•H2O 后没有得到Co(OH)3,而是得到了桔黄色结晶,起初认为是一种复合物(CoCl3•6NH3),但他在该桔黄色结晶的溶液中加碱后得不到NH3,也检查不出Co3+离子的存在,可见Co3+与NH3是紧密结合在一起的,而加AgNO3后却得到了AgCl沉淀,证明Cl-是游离的。
塔索尔特的报道使一些化学家开始研究这类化合物,因为当时的原子价理论不能解释这类化合物,故称之为复杂化合物,即络合物。
配位化合物结构理论发展简史1.配合物结构的早期理论配合物(coordination compound),早期也称为络合物(complex compound)。
配合物的早期发现与性质的研究,主要得益于17世纪末18世纪初欧洲染料工业发展的需求。
第一个金属配合物—普鲁士兰KFeFe(CN)6或KCN·Fe(CN)2·Fe(CN)3,即是由一个德国柏林的颜料工人Diesbach于1704年制得的。
但是配位化学的真正开端,是以1799年Tassert发现六氨合钴(Ⅱ)氯化物CoCl3·6NH3为标志的。
因为CoCl3和NH3都是价饱和的稳定化合物,它们又以何种形式而结合成另一种很稳定的化合物呢?这对当时的化学家来说是一道难题,因此引起了进一步研究的极大兴趣。
在科学实验中,化学家们制得了许多这类化合物,并且认真地研究了它们的性质。
如对三价钴盐与氨的化合物的性质研究表明,化合物不仅因氨分子的数目不同而有不同的颜色,而且钴络盐中氯的行为也有所不同,即化合物颜色酸性AgNO3实验CoCl3·6NH3橙黄色用AgNO3可沉淀出3C1—CoCl3·5NH3红紫色用AgNO3可沉淀出2C1—Co Cl3·5NH3·H2O 玫红色用AgNO3可沉淀出3C1—CoCl3·4NH3绿色用AgNO3可沉淀出lCl—为了解释这些实验事实,不少人都曾企图采用扩大原子价规则的办法。
但这方面的尝试均未成功。
2.Werner的配位理论1893年仅26岁化学家Werner(1913年获得诺贝尔化学奖),提出了他的配位学说,认为:(1)一些金属的原子价除主价外,还可以有副价,而且,元素倾向于既满足它的主价又要满足它的副价。
例如在CoCl 3 4NH 3中,钻的主价为三,副价为四,即三个氯离子满足了钻的主价,与氨分手的结合使用了副价。
(2)络合物分为“内界”和“外界”。
配位化学史配位化学史是化学史中的一部分,是研究金属离子与配体之间的相互作用、配位化合物的合成与性质的发展历程。
配位化学的起源可以追溯到古代,但其独立学科的形成要归功于19世纪的科学家们。
早在古代,人们就已经开始使用金属离子与配体形成配位化合物。
例如,古希腊人就发现了黄铜(由铜和锌组成)的存在。
然而,对于这些化合物的形成原理以及性质的理解非常有限。
在18和19世纪,科学家们开始逐步深入研究配位化学。
路易斯·布朗斯特德和约翰·纽贝里发现了金属离子在水中的溶解性以及它们与水分子的相互作用。
同时,弗里德里希·克劳斯提出了配位化合物的概念,即由中心金属离子与周围的配体形成稳定结构。
19世纪末和20世纪初,阿尔弗雷德·维纳成为配位化学的奠基人。
他提出了现代配位化学的基本原理,并系统地研究了金属离子和配体之间的配位键。
维纳的工作使得配位化学能够被视为一个独立的学科,并为后来的研究奠定了基础。
随着时间的推移,配位化学研究得到了广泛的发展。
托马斯·沃尔特·查尔斯·布尔特利特发现了金属配合物的立体化学特性,并提出了配合物的光、磁性质与内电荷转移等性质之间的关系。
此外,欧文·费舍尔和弗雷德里克·克罗都发现了很多重要的金属配合物,并对它们的结构和性质进行了详细研究。
近年来,配位化学的研究不断取得突破。
金属配合物在无机领域、有机领域和生物领域的应用得到了广泛关注。
许多金属配合物具有重要的实际应用,例如医药、材料科学和环境保护等领域。
同时,配位化学的发展也推动了其他学科的进步,如光化学、电化学和核化学等。
综上所述,配位化学史是一部充满着创新和发展的历史。
从古代人们对黄铜的发现,到维纳将其发展为独立学科,再到近年来的突破性研究,配位化学为我们揭示了金属离子与配体间的奇妙相互作用。
理解和掌握配位化学对于进一步开发新的材料和提高生活质量具有重要意义。