九年级化学二氧化碳制取的研究
- 格式:docx
- 大小:37.07 KB
- 文档页数:2

自学材料课题2 二氧化碳制取的研究知识点1 实验室制取二氧化碳的药品,反应原理1、药品:大理石或石灰石与稀盐酸。
2、反应原理:CaCO3 +2HCl ====CaCl2+H2O+CO2↑易错易混点:(1)不能用浓盐酸代替稀盐酸,因为浓盐酸易挥发,使制取的CO2不纯(混有氯化氢气体)。
(2)不能用稀硫酸代替稀盐酸,因为稀硫酸与碳酸钙反应生成微溶于水的硫酸钙覆盖在大理石或石灰石的表面,阻止反应的继续进行。
(3)不能用Na2CO3或 CaCO3粉末代替大理石(或石灰石),因为Na2CO3或CaCO3粉末与稀盐酸的反应速度太快,不便于收集。
由以上可知,确定实验室制取气体的反应原理,我们要就以下因素加以综合考虑:制得的气体较纯,反应条件易满足,反应速率适中等。
知识点2 实验室里制取气体的装置确定1、实验室里制取气体的装置包括发生装置和收集装置两部分。
确定气体发生装置和收集装置时考虑的因素。
(见教材110页)由以上条件可以确定实验室制取二氧化碳的发生装置有:实验室制取二氧化碳的收集装置为:动手试一试:利用教材P111提供的仪器,同学们还能组装出哪些制取二氧化碳的发生装置和收集装置。
并比较各装置的优缺点。
知识点3 二氧化碳的制取、检验和验满1、探究实验室制取二氧化碳的主要操作步骤2、讨论检查装置气密性的方法3、二氧化碳的检验和验满检验:将气体通入石灰水,石灰水变浑浊,则表明气体是二氧化碳。
CO2+Ca(OH)2====CaCO3↓+H2O验满:用燃着的木条放在集气瓶口,若木条熄灭,则表明气体已经集满知识点4 实验室制取气体的一般设计思路和方法1、选择药品:原理可行,反应速度适中,价格便宜,来源广泛,污染少,实验安全,所制气体纯净的药品。
2 、设计实验装置:根据药品的状态和反应原理,以及反应条件、设计实验装置;装置设计要简单,便于控制和操作。
3、制定操作步骤:合理有序。
知识点5 二氧化碳的工业制法在工业上,我们可以利用高温煅烧石灰石的方法来制备大量的二氧化碳,其反应原理为:CaCO3=高温=CaO+CO2↑。


第六单元碳和碳的氧化物课题2 二氧化碳制取的研究课标定位1、了解实验室中制取二氧化碳的反应原理2、探究实验室中制取二氧化碳的装置,并利用设计的装置制取二氧化碳3、了解实验室中制取气体的思路和方法知识梳理核心知识归纳1.实验室制取气体的装置包括发生装置和收集装置两部分。
确定气体发生装置时应考虑的因素有反应物的状态和反应条件;确定气体收集装置时应考虑的因素是气体的性质,包括气体的密度和溶解性。
2.密度比空气大的气体可用向上排空气法收集,密度比空气小的气体可用向下排空气法收集,不易溶于水且不与水发生反应的气体可用排水法收集。
3.实验室制取二氧化碳常用大理石(或石灰石)与稀盐酸,反应的化学方程式为CaCO3+2HClCaCl2+H2O+CO2↑。
4.二氧化碳的检验方法为向集气瓶中倒入澄清石灰水,振荡,看石灰水是否变浑浊;验满方法为将燃着的木条放在集气瓶口处,如果木条熄灭,证明已满。
知识点一、制取二氧化碳知识在线1.实验药品:大理石(或石灰石)和稀盐酸。
2.实验仪器和其他用品:锥形瓶(或试管、广口瓶等)、双孔橡皮塞(或单孔橡皮塞)、导管、长颈漏斗(或分液漏斗)、集气瓶、玻璃片、火柴、澄清石灰水。
3.实验原理:CaCO3+2HCl CaCl2+H2O+CO2↑。
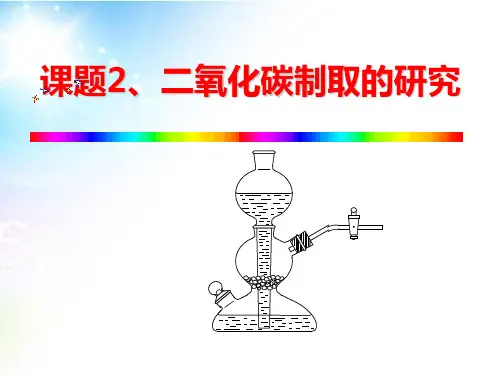
4.实验装置(如图所示)。
5.实验步骤:①组装仪器装置(如图所示);②检验装置的气密性;③向锥形瓶中加入石灰石,然后堵上橡皮塞;④从长颈漏斗倒入适量的稀盐酸;⑤收集二氧化碳;⑥验满二氧化碳。
6.收集方法: 向上排空气法(二氧化碳密度比空气大,且能溶于水)。
7.检验方法:倒入澄清石灰水,振荡,看石灰水是否变浑浊。
8.验满方法:将燃着的木条放在集气瓶口处,如果木条熄灭,证明已满。
9.放置方法:盖上玻璃片,然后瓶口向上正放在桌面上。
易错警示(1)不能用稀硫酸,因为稀硫酸与石灰石反应会生成微溶于水的硫酸钙,覆盖在大理石表面,阻碍反应继续进行。
(2)不能用浓盐酸,因为浓盐酸具有强烈挥发性,会挥发出大量的氯化氢气体,使制得的二氧化碳气体不纯净。


第六单元碳和碳的氧化物课题2二氧化碳制取的研究知识点一实验室制取二氧化碳的反应原理一、药品大理石(或石灰石)和稀盐酸大理石或石灰石的主要成分是碳酸钙,化学式是CaCO3。
二、反应原理CaCO3+2HCl===CaCl2+H2CO3碳酸钙盐酸氯化钙碳酸碳酸不稳定,容易分解生成二氧化碳和水。
H2CO3===H2O+CO2↑总的化学方程式是:CaCO3+2HCl===CaCl2+H2O+CO2↑理解辨析1、为什么实验室制取CO2时不用稀硫酸、浓盐酸?①实验室制取二氧化碳不用稀硫酸,因为稀硫酸与石灰石反应生成的硫酸钙微溶于水,覆盖在石灰石表面,阻碍石灰石与硫酸接触,使反应中断。
②不用浓盐酸。
浓盐酸易挥发出氯化氢气体,导致二氧化碳不纯。
例题1、在实验室里制取二氧化碳气体,可选择的药品是( D)A.碳酸钠粉末与浓盐酸B.块状石灰石与稀硫酸C.石灰石D.块状大理石和稀盐酸例题2、为什么实验室制取二氧化碳不用块状石灰石与稀硫酸反应(B)A.石灰石与硫酸不反应B.石灰石与稀硫酸反应的产物阻碍反应进行C.反应操作很麻烦D.石灰石与稀硫酸反应生成有杂气练习题1、实验室制取二氧化碳用稀盐酸而不用浓盐酸的原因为(D)A.浓盐酸反应太快了B.浓盐酸与石灰石的产物阻碍反应进行C.浓盐酸反应不完全造成浪费D.制取得到的气体混有氯化氢杂气2、反应得到二氧化碳的反应很多,其中用于实验室制取二氧化碳的方法是(B)A.块状石灰石与稀硫酸B.块状大理石和稀盐酸C.石灰石煅烧D.木炭与氧气反应知识点二 制取气体的一般思路一、制取装置的选择实验室制取气体的装置包括反应装置和 收集装置 。
反应装置 主要由反应物的状态、反应条件决定,收集装置主要考虑生成气体的物理性质( 密度 、 溶解性 )。
二、发生装置的选择三、收集装置的选择理解辨析1、判断气体的密度比空气的大还是小的方法是什么?空气的平均相对分子质量为29。
如果某气体的相对分子质量大于29,则这种气体的密度比空气大;如果小于29,则密度比空气小。




二氧化碳制取研究教学设计(通用14篇)(实用版)编制人:__________________审核人:__________________审批人:__________________编制单位:__________________编制时间:____年____月____日序言下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!并且,本店铺为大家提供各种类型的实用资料,如工作总结、工作报告、党团范文、工作计划、演讲稿、活动总结、行政公文、文秘知识、作文大全、其他资料等等,想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor.I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you!Moreover, our store provides various types of practical materials for everyone, such as work summaries, work reports, Party and Youth League model essays, work plans, speeches, activity summaries, administrative documents, secretarial knowledge, essay summaries, and other materials. If you want to learn about different data formats and writing methods, please stay tuned!二氧化碳制取研究教学设计(通用14篇)教学计划不仅是教师的一种工作规划,也是学生学习的规划,对于提高教学效果和学生成绩具有重要意义。
最新二氧化碳制取的研究课程标准二氧化碳制取的研究说课稿(优秀5篇)二氧化碳制取的研究课程标准篇一本单元是初中化学最为完整的学习元素和化合物知识体系的一个单元,而二氧化碳又是本单元的一个非常重要的内容,二氧化碳制取的研究这节课在本书乃至整个初中化学学习过程中都占据十分重要的地位。
本节课学习的重点是能力训练。
学生在前面学习了氧气的实验室制法,具备了一些气体制备的实践经验,各项实验技术也已经具备,此时,在课堂教学中体现学生为主体,让学生真正参与到教学过程中来正是时机。
1、知识与技能:(1)了解实验室制取二氧化碳的反应原理,探究实验室制取二氧化碳的装置,并利用设计的装置制取二氧化碳。
(2)了解实验室制取气体的方法和设计思路。
2、过程与方法:通过实验室里制取氧气的方法和设计思路,探索实验室制取二氧化碳实验装置,让学生初步学习科学探究的基本过程(提出假设,实验探究,获得结论)和方法,体验化学实验的方法的科学性;能进行初步的科学探究活动。
3、情感态度与价值观:通过实验、问题讨论,培养学生求实、创新、合作的科学品质。
通过师生间、学生间合作学习,研究性学习,体验探究成功的乐趣,激发学生探究欲。
教法分析1、探究式实验教学法:教师根据目标提问,学生动手实验,体验实验的过程。
教给学生通过实验、观察、探究得出科学结论教学方法。
2、互动式教学法:教师讲解过程中,学生去猜想,讨论、抢答,在学生的实验过程中有教师的指导、答疑,师生间不断的进行信息交流,有助于学生注意力的集中和学习积极性的提高。
3、竞赛教学法:根据初中生集体荣誉感强,好胜心强的特点,采用分组竞赛的方法,在竞赛中,提高学生自主参与的积极性,有利于知识的巩固和应用。
通过以上教学方法的使用,充分体现“教师为主导,学生为主体”的教学原则。
学法分析1、探究学习:学生通过实验来探究实验室制取二氧化碳为何不能使用其它药品,通过研究发生装置,选择其它仪器制取二氧化碳,来培养学生的观察能力,语言表达能力和分析能力,培养开拓创新的精神。
二氧化碳(CO2)是一种重要的化学物质,在地球大气中起着重要的
作用。
然而,由于人类的活动,如工厂排放、车辆尾气等,大量的二氧化
碳被释放到大气中,导致全球变暖的问题日益严重。
因此,对二氧化碳的
制取和利用进行深入研究,变得至关重要。
二氧化碳制取是指将二氧化碳从大气、地下或者工业废气中分离出来
的过程。
在工业生产中,常用的方法是利用尾气、发电厂烟气或工厂排放
的废气中的二氧化碳。
以下将介绍几种常见的CO2制取的方法。
第一种方法是吸收法。
这种方法的基本原理是利用溶液对二氧化碳进
行吸收。
其中最常用的溶液为氨溶液(氨水)。
在吸收法中,首先,将含
有二氧化碳的气体通入大气中,然后通过氨溶液中的气体鼓泡。
二氧化碳
气体与氨水反应,生成碳酸氢氨(NH4HCO3)溶液。
接下来,将溶液进行
加热,即可分解碳酸氢铵,产生了二氧化碳气体。
第二种方法是冷却法。
这种方法是通过将含有二氧化碳的气体冷却至
低温,使二氧化碳转化为液态。
然后,利用液态二氧化碳的密度差异进行
分离。
冷却法的主要过程包括压缩、冷却和蒸发。
首先,将气体进行压缩,使其体积减小。
然后,通过冷却气体,使其达到液态的温度。
最后,利用
蒸发将液态二氧化碳蒸发出来,从而得到纯净的二氧化碳。
第三种方法是植物吸收法。
植物通过光合作用将二氧化碳转化为氧气
和有机物质,可以将二氧化碳吸收到根部,并通过树木的呼吸作用排出。
因此植物吸收法在自然界中起着重要的角色。
在人工条件下,可以通过建
立大规模的植物园,采取植物种植等方法,有效地吸收和削减大气中的二
氧化碳含量。
除了以上几种常见的方法,还有一些其他方法也被应用于二氧化碳的制取,如化学吸附法、分子筛法等,它们基于二氧化碳与其他物质的化学吸附或分子筛效应。
总结起来,二氧化碳制取是一项重要的化学研究,目标是有效地从大气、地下或者工业废气中分离出二氧化碳。
吸收法、冷却法和植物吸收法是常见的二氧化碳制取方法。
这些方法在实践中已经得到了广泛应用,对于减少大气中的二氧化碳含量,减缓全球变暖的问题具有重要的意义。