苯扎溴铵溶液中间产品检验操作规程
- 格式:doc
- 大小:29.00 KB
- 文档页数:2

氨水检验操作规程一、实验目的对氨水进行检验,了解其化学性质和纯度,并对其是否符合质量标准进行评价。
二、实验仪器和试剂1.仪器:比色皿、试管、分液漏斗、滴管、万能架等。
2.试剂:氨水、硫酸铜溶液、硝酸银溶液、硼酸溶液、硝酸盐溶液等。
三、实验步骤及操作要点1.取一定量的氨水,加入硫酸铜溶液,观察是否产生深蓝色沉淀。
如果出现沉淀,说明氨水中可能含有铜离子。
2.取一定量的氨水,加入硝酸银溶液,并放置一段时间,观察是否产生白色沉淀。
如果出现沉淀,说明氨水中可能含有银离子。
3.取一定量的氨水,加入硼酸溶液,并滴加几滴酚酞指示剂,进行滴定。
记录滴定时所需的硼酸溶液体积,并计算氨水中氨的质量浓度。
4.取一定量的氨水,加入硝酸盐溶液,并加热至沸腾,观察有无气泡产生。
如果有气泡产生,则说明氨水中可能含有氮气。
四、实验结果记录与分析1.记录每次实验所用试剂的种类和用量。
2.记录实验现象的观察结果,如是否有沉淀产生、有无气泡产生等。
3.根据实验结果,评价氨水的纯度和化学性质是否符合质量标准。
例如,如果氨水中含有铜离子或银离子,说明其纯度较低;如果氨水中有氮气产生,则说明其可能含有杂质。
五、实验安全注意事项1.在操作过程中要佩戴实验手套和安全眼镜,避免与试剂直接接触眼睛或皮肤。
2.操作时要注意用量和保存试剂,确保实验的准确性和安全性。
3.氨水具有刺激性气味,操作时要保持通风良好。
4.严禁将试剂或废液倒入排水口,应按照相关规定处理。
六、实验心得体会通过这次实验,我对氨水的检验方法和操作规程有了更深入的了解。
同时,也加强了我对实验安全的关注,提高了实验操作的技能。
这对于今后的实验工作具有重要意义。

品质检验的操作规程品质检验是产品生产过程中非常重要的一环,其目的是为了确保产品的质量达到预设的标准并满足客户的需求。
为了提高检验的效率和准确性,制定一份操作规程对于品质检验的工作是至关重要的。
以下是品质检验的操作规程。
一、前期准备1.1 准备检验工具和设备。
根据产品的特点和检验要求,准备相应的检验工具和设备,例如量具、试验设备、仪器等。
1.2 校准检验设备。
在进行品质检验之前,应对检验设备进行校准,确保其准确性和可靠性。
1.3 确定检验样本。
根据产品的特点和生产批次,确定需要进行检验的样本数量和抽样方法。
二、检验操作流程2.1 样品接收。
在检验前,对接收到的样品进行核对和记录,确保样品的完整性和准确性。
2.2 检验项目确认。
根据产品的特点和技术要求,确认需要进行的检验项目和标准。
2.3 进行检验操作。
按照检验项目和标准,进行相应的检验操作和测量,记录检验结果。
2.4 处理异常样品。
在检验过程中,如发现样品不符合标准要求,应及时记录异常情况,并根据公司的流程进行处理。
2.5 结果评定。
根据检验结果和标准要求,对样品进行合格与否的评定,并记录结果。
2.6 检验报告。
根据检验结果和要求,编制检验报告,并将报告提交相关部门。
三、仪器设备的保养和维护3.1 定期保养。
对检验所使用的仪器设备进行定期保养和维护,确保其正常运行和准确度。
3.2 校准和维修。
定期对检验设备进行校准,并及时维修和更换不合格的设备,确保仪器的准确性和可靠性。
四、文件和记录管理4.1 检验记录。
对每次检验的样品和结果进行详细记录,包括样品的接收情况、检验项目和结果。
4.2 检验报告。
根据检验结果,编制检验报告并妥善保存,作为产品质量认证和追溯的重要依据。
4.3 文件管理。
建立健全的文件管理制度,包括文件的编号、索引和归档等,确保文件的准确和完整性。
五、持续改进5.1 定期评估。
定期对品质检验的标准、流程和操作进行评估,发现问题并及时进行改进。

第1篇一、目的为确保产品质量,防止微生物污染,保障消费者健康,特制定本操作规程。
二、适用范围本规程适用于所有需要进行无菌检测的产品。
三、操作步骤1. 准备工作(1)确保实验室环境符合无菌要求,温度保持在20-24℃,湿度保持在45-60%。
(2)检查无菌操作间、超净台、接种箱等设备的清洁度,确保符合100级洁净度。
(3)准备无菌操作所需的物品,如无菌试管、无菌培养皿、无菌移液器、无菌棉签、无菌酒精、无菌生理盐水等。
2. 产品取样(1)严格按照产品说明书要求,从不同部位、不同批次的产品中取样。
(2)取样时,使用无菌棉签擦拭取样部位,确保取样过程中不引入污染。
(3)将取样部位放入无菌试管中,密封后送检。
3. 培养基制备(1)按照培养基说明书要求,称取适量的培养基粉末,加入无菌生理盐水溶解。
(2)将溶解后的培养基分装至无菌培养皿中,放入培养箱中预培养。
4. 接种(1)将待检产品样品与无菌培养基进行平板划线接种。
(2)接种后,将培养皿放入培养箱中培养。
5. 检测(1)在培养过程中,观察培养基上是否有菌落生长。
(2)根据菌落特征,判断是否为微生物污染。
6. 记录与报告(1)详细记录实验过程,包括取样时间、接种时间、培养时间等。
(2)根据检测结果,出具无菌检测报告。
四、注意事项1. 实验室环境应保持清洁、无菌,操作人员应穿戴无菌工作服、口罩、手套等。
2. 操作过程中,严格遵循无菌操作原则,避免交叉污染。
3. 使用无菌物品时,确保其密封完好,防止污染。
4. 实验过程中,如发现异常情况,应立即停止操作,查找原因,采取相应措施。
5. 实验结束后,及时清理实验台,消毒处理使用过的物品。
五、附则1. 本规程由质量管理部负责解释。
2. 本规程自发布之日起实施。
第2篇一、目的为确保产品生产过程中的无菌质量,防止微生物污染,保障消费者健康,特制定本操作规程。
二、适用范围本规程适用于公司所有生产无菌产品的无菌检测工作。
三、职责1. 质量部负责制定和实施本规程;2. 生产部门负责按照规程执行无菌检测;3. 检验部门负责对无菌检测结果进行审核和判定。

注射剂检验操作规程注射剂检验操作规程一、目的与范围:本操作规程是为了规范注射剂检验工作流程,保证注射剂产品的质量,以及确保注射剂符合相关标准和法规的要求。
本操作规程适用于所有注射剂检验工作,包括原辅材料检验、半成品检验、成品检验等。
二、检验设备及仪器:1. 显微镜:用于对样品进行微观检查,检测是否存在异物、杂质等。
2. 压力计:用于检测注射剂容器的密封性和耐压性能。
3. 电子天平:用于测量药液的重量,检测药液的配比是否准确。
4. pH计:用于测定药液的酸碱度。
5. 紫外分光光度计:用于检测药液中的杂质和活性成分的含量。
6. 无菌工作台:用于进行无菌检验和操作。
三、操作步骤:1. 取样:按照规定的抽样方案,从批次中随机取样。
注意避免污染和交叉感染。
2. 外观检查:对样品的色泽、透明度、是否有浑浊、沉淀等进行检查。
3. 标签检查:检查样品上的标签是否完好、清晰,包括产品名称、批号、有效日期等。
4. 物理性质检验:包括药液的密度、温度、粘度、等特性的测定。
5. 包装和标志检验:检查样品的外包装是否完好、符合规定,标志是否准确。
6. 含量测定:根据相关标准,使用紫外分光光度计等仪器测定药液中活性成分的含量。
7. 微生物检验:使用无菌技术,进行微生物检验,包括菌落总数、大肠杆菌等指标的测定。
8. pH值测定:使用pH计测定药液的酸碱度。
9. 无菌检验:在无菌工作台下,对样品进行无菌检验,确保无菌要求。
10. 容器密封性和耐压性检验:使用压力计对容器密封性和耐压性能进行检测。
11. 结论判定:根据检验结果,判断样品是否符合要求。
12. 记录和报告:将检验结果记录在相关文件中,并及时向上级主管部门报告检验结果。
四、注意事项:1. 检验人员应严格遵守无菌操作规程和个人防护措施,以避免交叉感染和个人伤害。
2. 在检验过程中,应做好样品的标识和保存,以免混淆和损坏。
3. 检验仪器和设备应定期校准和维护,确保其准确性和可靠性。
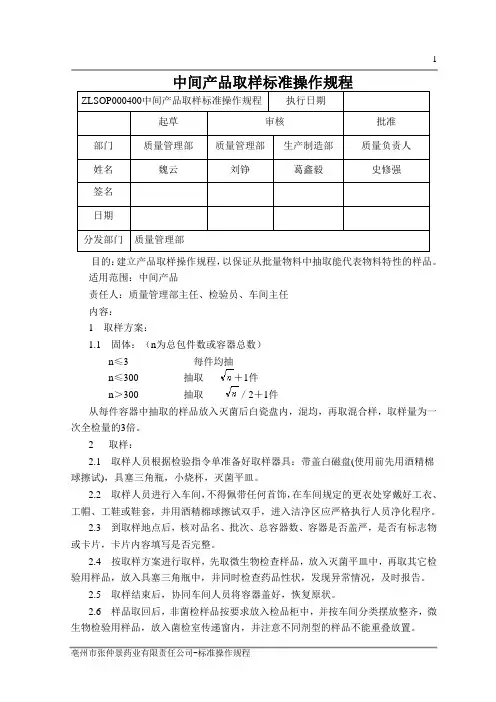
中间产品取样标准操作规程
ZLSOP000400中间产品取样标准操作规程执行日期
起草审核批准部门质量管理部质量管理部生产制造部质量负责人
姓名魏云刘铮葛鑫毅史修强
签名
日期
分发部门质量管理部
目的:建立产品取样操作规程,以保证从批量物料中抽取能代表物料特性的样品。
适用范围:中间产品
责任人:质量管理部主任、检验员、车间主任
内容:
1 取样方案:
1.1 固体:(n为总包件数或容器总数)
n≤3 每件均抽
n≤300 抽取+1件
n>300 抽取/2+1件
从每件容器中抽取的样品放入灭菌后白瓷盘内,混均,再取混合样,取样量为一次全检量的3倍。
2 取样:
2.1 取样人员根据检验指令单准备好取样器具:带盖白磁盘(使用前先用酒精棉球擦试),具塞三角瓶,小烧杯,灭菌平皿。
2.2 取样人员进行入车间,不得佩带任何首饰,在车间规定的更衣处穿戴好工衣、工帽、工鞋或鞋套,并用酒精棉球擦试双手,进入洁净区应严格执行人员净化程序。
2.3 到取样地点后,核对品名、批次、总容器数、容器是否盖严,是否有标志物或卡片,卡片内容填写是否完整。
2.4 按取样方案进行取样,先取微生物检查样品,放入灭菌平皿中,再取其它检验用样品,放入具塞三角瓶中,并同时检查药品性状,发现异常情况,及时报告。
2.5 取样结束后,协同车间人员将容器盖好,恢复原状。
2.6 样品取回后,非菌检样品按要求放入检品柜中,并按车间分类摆放整齐,微生物检验用样品,放入菌检室传递窗内,并注意不同剂型的样品不能重叠放置。
2.7 填写药品取样记录。
3 取样器具每次使用后,应按照各自清洗操作规程清洗。

某某制药有限公司GMP 文件目 的:建立中间产品取样标准操作规程,规范取样行为。
适用范围:中间产品的取样工作。
责 任 人:质量保证室检查员 内 容: 1.操作程序2.取样前的准备工作:2.1质量保证室检查员收到中间站岗位操作人员“请验单”后,做好取样准备。
2.2依据“请验单”的品名、规格、批号、数量(件数)按下列原则计算取样件数及取样量。
2.2.1取样件数:设N 为中间产品总桶数(N):N ≤3件,每件均取样 N =4-300件,按1+N 件取样N >300件,按1)2/(+N 件取样2.2.2取样量:按中间产品取样件数每桶中随机取样,注意取样的代表性和均一性。
取样量为 一次全检量的三倍量,化验剩余,作为留样样品,中间产品保存到该批产品的成品检验合格后一 个月后销毁。
2.3准备取样袋、取样器、广口瓶、手套、辅助工具(均为洁净用具)。
2.3.1取样器: 固体-不锈钢勺、不锈钢探子; 液体-用广口瓶在取样点直接接取。
2.3.2样品盛装容器:固体-具有封口装置的无毒塑料袋(以后称取样袋);液体-广口瓶。
2.3.3需做微生物限度的中间产品取样器、取样袋、辅助工具均应用灭菌或消毒后的器具,在标签上注明“已灭菌”字样以示专用。
取样袋用75%乙醇擦拭消毒,灭菌后的容器、器具,三天内使用。
2.3.4不同中间产品应分别准备取样器和取样手套,不得共用。
2.3.5根据“请验单”在取样袋或广口瓶上贴标签,注明品名、规格、批号、物料编号、数量、取样日期等。
3.取样3.1到中间站核对状态标志,应为黄色“待验”状态标志。
3.2核对“请验单”内容与实物标记是否相符,如品名、规格、批号、来源。
“周转卡”应清楚,完整。
3.3固体──用洁净的不锈钢勺、不锈钢探子,在存放中间产品的不同部位取样,样品放在取样袋内,封口,做好标记。
3.4液体──配液罐内的中间产品在搅拌、循环三分钟后从取样口用广口瓶直接取样,每隔三分钟取一次,共取三次。

液体化工品品质检验操作规程1 目的为了规范液体化工品品质检验业务,保证结果的公正和准确性。
2适用范围适用于液体化工品的品质检验。
3 样品采集3.1 按照GB/T 6680-2003《液体化工产品采样通则》执行。
仅适用于温度不超过100℃,压力为常压或接近常压的液体化工产品。
不适用于在产品标准中有特殊要求的液体产品的采样。
3.2采样的基本要求3.2.1 采样操作人员必须熟悉被采液体化工产品的特性、安全操作的有关知识及处理方法。
3.2.2 采样前应进行预检,并根据检查结果制定采样方案,按此方案采得具有代表性的样品。
由于液体化工产品一般是用容器包装后贮存和运输,应根据容器情况和物的种类来选择采样工具,确定采样方法。
预检内容如下:3.2.2.1 了解被采样物的容器大小、类型、数量、结构和附属设备情况。
3.2.2.2 检查被采样物的容器是否受损、腐蚀、渗漏并核对标志。
3.2.2.3 观察容器内物的颜色,粘度是否正常;表面或底部是否有杂质、分层、沉淀、结块等现象;判断物的类型和均匀性。
3.3 样品的代表性如被采容器内液体已混合均匀,采取混合样品作为代表性样品。
如被采容器内物未混合均匀,可采部位样品按一定比例混合成平均样品作为代表性样品。
3.4 采样设备3.4.1 要求液体产品的取样器应为不锈钢;铜质或铝合金材料制成;取样器的材料不应与液体货物发生化学反应而影响液体产品的品质;取样器应符合相应液体产品的清洁,卫生要求。
取样器的提拉绳应选用符合防静电要求的材料制成。
3.4.2 玻璃采样瓶一般为500mL具内外塞的螺口棕色玻璃瓶。
3.4.3 采样笼把具塞金属瓶或具塞玻璃瓶放人加重金属笼罐中固定而成。
3.4.4 金属制采样瓶、罐3.4.4.1 普通型采样器通常为不锈钢制采样瓶,体积500mL,适用于贮罐、槽车采样。
这是一个均匀直径的管状装置,配有上部和下部隔离翼阀或瓣阀。
向上运动时,可以从罐中任一所选液面收集正确的和相对地未经扰动的试样。
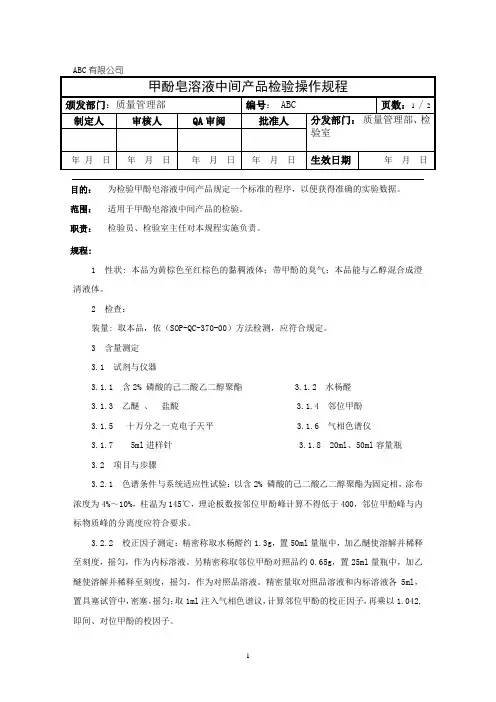
目的:为检验甲酚皂溶液中间产品规定一个标准的程序,以便获得准确的实验数据。
范围:适用于甲酚皂溶液中间产品的检验。
职责:检验员、检验室主任对本规程实施负责。
规程:1 性状: 本品为黄棕色至红棕色的黏稠液体;带甲酚的臭气;本品能与乙醇混合成澄清液体。
2 检查:装量: 取本品,依(SOP-QC-370-00)方法检测,应符合规定。
3 含量测定3.1 试剂与仪器3.1.1 含2% 磷酸的己二酸乙二醇聚酯 3.1.2 水杨醛3.1.3 乙醚、盐酸 3.1.4 邻位甲酚3.1.5 十万分之一克电子天平 3.1.6 气相色谱仪3.1.7 5ml进样针 3.1.8 20ml、50ml容量瓶3.2 项目与步骤3.2.1 色谱条件与系统适应性试验:以含2% 磷酸的己二酸乙二醇聚酯为固定相,涂布浓度为4%~10%,柱温为145℃,理论板数按邻位甲酚峰计算不得低于400,邻位甲酚峰与内标物质峰的分离度应符合要求。
3.2.2 校正因子测定:精密称取水杨醛约1.3g,置50ml量瓶中,加乙醚使溶解并稀释至刻度,摇匀,作为内标溶液。
另精密称取邻位甲酚对照品约0.65g,置25ml量瓶中,加乙醚使溶解并稀释至刻度,摇匀,作为对照品溶液。
精密量取对照品溶液和内标溶液各5ml,置具塞试管中,密塞,摇匀;取1ml注入气相色谱议,计算邻位甲酚的校正因子,再乘以1.042,即间、对位甲酚的校因子。
3.2.3测定法:精密量取本品2ml,置分液漏斗中,加盐酸0.1ml,加水5ml,轻轻振摇,分层,弃去水层。
精密量取乙醚提取液5ml和内标溶液5ml,置具塞试管中,摇匀。
取1ml注入气相色谱议,测定,按下式计算:标示百分含量%=()%10052.052211⨯⨯⨯•+AWfAfA式中:A:为内标物质峰面积;A1:为邻位甲酚峰面积;A2:为间、对位甲酚峰面积;f1:为邻位甲酚校正因子;f2:为间、对位甲酚校正因子;W:为内标物质重量g;0.52为处方中甲酚每1ml中的量g。

GMP质量体系甲酚皂溶液中间产品检验操作规程GMP质量体系是世界范围内广泛应用的医药行业质量管理体系,其中包括药物生产中的中间产品检验操作规程。
甲酚皂溶液是一种常用的消毒剂,广泛应用于医疗、卫生和生命科学等领域。
下面是GMP质量体系甲酚皂溶液中间产品检验操作规程的详细内容。
一、检验原则:1.甲酚皂溶液的中间产品检验要符合国家药典的要求。
2.所有检验人员必须熟悉和掌握检验项目的操作要点和仪器使用方法,确保检验结果准确可靠。
3.检验过程中要严格操作规程,杜绝操作失误和污染。
二、检验项目及要求:1.外观检验:取适量甲酚皂溶液样品,观察其外观是否为淡黄色液体,并无悬浮物和沉淀。
2.PH值检验:使用PH计,将电极插入甲酚皂溶液样品中,记录其PH 值,应在7.0-9.0之间。
3.游离酚含量检验:采用紫外分光光度法检测。
取适量样品,经过适当稀释后,使用紫外分光光度计记录其吸光度,计算游离酚含量,应在0.25%以下。
4. 游离碱含量检验:采用酸碱滴定法检测。
取适量样品,加入适量2%硫酸,用0.1mol/L盐酸滴定至石莓红终点,记录滴定消耗的盐酸体积,计算游离碱含量,应在0.2%以下。
三、检验仪器和设备:1.PH计:具备精确度和稳定性的PH计。
2.紫外分光光度计:具备精确度和稳定性的紫外分光光度计。
3.滴定管、量筒、容量瓶等常用的实验室玻璃仪器。
四、操作步骤:1.取适量甲酚皂溶液样品,放置于检验台上。
2.外观检验:观察甲酚皂溶液样品外观是否符合要求,并记录结果。
3.PH值检验:将PH计电极清洗干净,插入甲酚皂溶液样品中,记录PH值,并与标准要求进行对比。
4.游离酚含量检验:取适量甲酚皂溶液样品,按照紫外分光光度法进行检测,记录吸光度,并计算游离酚含量。
5.游离碱含量检验:取适量甲酚皂溶液样品,按照酸碱滴定法进行检测,记录滴定体积,并计算游离碱含量。
6.检验完毕后,清理仪器和设备。
五、记录与报告:1.检验过程中记录每个检验项目的结果。

原料、中间体与终产物样品检验标准操作规程目的:建立原料与中间体样品检验SOP,确保样品检验操作的规范化和标准化。
范围:公司购入的原料药、中间体及公司自行合成的化合物。
职责:开发部操作人员严格按照本操作规程进行样品检验,部门领导对本规程的有效执行进行监督检查。
内容:1 样品领取由公司项目管理部下达样品检验项目启动单(如属购买的原料、中间体,一并附上其公司的自检报告单),开发部质检科根据项目启动单计算检验所需样品的质量,出具样品检验申请单,申请并领取化合物。
2 样品检测项目的确定根据后续实验的性质和要求及公司开发部的实验条件,开发部质检科与合成部相关实验员商定样品检测项目。
3 样品检测3.1性状3.1.1 比旋度测定*3.1.2 熔点测定*3.2 检查3.2.1 有关物质3.2.2 水分测定*3.2.3 pH值测定*3.2.4 炽灼残渣*3.2.5 重金属检查*3.2.6 其他(砷盐、铁盐、硒等)*3.3 含量测定4 样品检测报告(样品检验报告单中标注样品检验的参考标准,中国药典、美国药典、欧洲药典或企业内控标准)注:标注*项目后附检验细则旋光度测定标准操作规程1 编制依据:《中华人民共和国药典》2005年版(二部)2 定义:偏振光透过1dm并每1ml中含有旋光性物质1g的溶液,在一定波长与温度下测得的旋光度称为比旋度。
3 原理:直线偏振光通过含有某些光学活性的化合物液体或溶液时,能引起旋光现象,使偏振光的平面向左或向右旋转,此种旋转在一定条件下,有一定的度数,其旋转的度数称为旋光度。
4检验操作方法4.1 仪器及用具电热恒温干燥箱电子天平旋光计、旋光管4.2 化学试剂:蔗糖4.3 操作方法4.3.1 旋光计的检定:可用蔗糖作为基准物质进行,取在105℃干燥2小时的蔗糖,用电子天平精密称定,加水溶解并定量稀释制成每1ml中含0.2g的溶液,依法测定,结果应如表:4.3.2 调零点:测定旋光度时,用读数至0.01度,并经检定的旋光计,将测定管用供试品所用的溶剂冲洗数次,缓缓注入适量溶剂,置于旋光计内调整零点或读取3次旋光度,取其平均值作为空白。

GMP质量体系氯霉素滴耳液中间产品检验操作规程中间产品是指在制造过程中所得到的不成品产品,它是制造最终产品的关键步骤之一、为了确保中间产品的质量和合规性,需要制定相应的操作规程进行检验。
以下是GMP质量体系氯霉素滴耳液中间产品检验操作规程,供参考。
1.背景与目的本操作规程的目的是确保氯霉素滴耳液中间产品的质量稳定,并符合相关法规和标准的要求。
2.质量控制标准2.1.外观检查:中间产品应为无色或微黄色的液体,不应有异物或悬浮物。
2.2.pH值检查:中间产品的pH值应在合格范围内,通常为4.5-5.52.3. 氯霉素含量检查:中间产品中的氯霉素含量应在合格范围内,通常为15-25mg/mL。
2.4.细菌限度检查:中间产品的微生物总菌落和大肠菌群应符合合格标准。
2.5.毒性检查:中间产品应通过毒性试验,确保其无毒副作用。
3.检验设备和试剂3.1.pH计:用于测量中间产品的pH值。
3.2.氯霉素含量检测试剂:用于检测中间产品中的氯霉素含量,例如高效液相色谱仪(HPLC)。
3.3.细菌检测培养基和平皿:用于检测中间产品的微生物总菌落和大肠菌群。
3.4.毒性试验设备和试剂:用于进行中间产品的毒性试验,例如小白鼠。
4.检验操作流程4.1.外观检查:将适量中间产品倒入透明玻璃容器中,观察其颜色、透明度和有无异物。
4.2.pH值检查:使用pH计将中间产品的pH值测定并记录。
4.3.氯霉素含量检查:按照氯霉素含量检测方法进行操作,例如利用HPLC进行检测。
4.4.细菌限度检查:将适量中间产品加入细菌检测培养基中,培养一定时间后,通过平皿计数法进行菌落计数。
4.5.毒性检查:将适量中间产品注射到小白鼠体内,观察一段时间内是否出现毒副作用。
5.结果评价和记录5.1.根据质量控制标准,对每个检验项目的结果进行评价,判定是否合格。
5.2.对检验结果进行记录,包括产品批号、检验项目、检验员、检验日期等信息。
6.异常处理和不合格品控制6.1.若中间产品的检验结果不符合标准要求,应立即停止生产,并进行问题调查和分析。
药品检验操作规程《药品检验操作规程》一、检验前准备1. 检验前应清洁检验设备和实验台面,准备所需的检验试剂和标准药品。
2. 确保检验人员身体健康,佩戴好相应的防护用品。
二、检验流程1. 取样根据检验要求,取样并记录样品信息。
2. 外观检查对样品进行外观检查,观察其颜色、形状、气味等特征。
3. 标识检验检验样品标识是否正确,包括批号、生产日期等信息。
4. pH值测定采用合适的试剂进行pH值测定,确保样品符合要求。
5. 含量测定使用适当的分析方法进行样品中有效成分的含量测定。
6. 杂质检查检查样品中是否有杂质,包括微生物、重金属等。
7. 微生物检验进行微生物菌落总数和霉菌、酵母菌的数量检验。
8. 性状检验对样品的物理和化学性状进行检验,包括溶解性、热稳定性等。
9. 稳定性检验对样品进行稳定性试验,检验其在不同条件下的稳定性。
三、检验记录和报告1. 记录检验过程中的所有数据和观察结果。
2. 编制检验报告,并对结果进行评价和分析。
四、质量评定1. 根据检验结果,对样品的质量进行评定。
2. 若样品合格,进行合格放行;若不合格,进行退货或再加工处理。
五、保养和维护1. 定期对检验设备进行保养和维护,确保设备正常运行。
2. 检验人员定期进行技术培训,提高检验水平。
六、紧急处理1. 发现异常情况时,立即停止检验操作,并进行紧急处理。
2. 对异常情况进行记录,并及时报告上级领导。
以上即是药品检验操作规程,希望全体检验人员能够严格按照规程进行操作,确保检验结果准确可靠。
GMP质量体系甲酚皂溶液中间产品检验操作规程一、检验目的为确保生产过程中乙酚皂溶液的质量符合GMP要求,保障产品质量和生产安全,制定本操作规程。
对乙酚皂溶液的中间产品进行检验,确保生产过程中的各项参数符合要求,提供科学依据。
二、检验范围本操作规程适用于乙酚皂溶液制备过程中的中间产品检验,包括成分含量、外观检查、PH值、溶解度、氧化物含量等项目。
三、检验设备与试剂1.PH计2.秤3.试剂瓶4.恒温水浴5.玻璃试管6.紫外分光光度计7.二氧化碳分析仪8.水浴箱9.含氧量测定仪四、检验项目及方法1.成分含量取样:从生产现场勾兑的中间产品中随机取样。
检验方法:将取样品在110°C下烘干至恒重,测取其重量,并与质量分数要求进行比对。
2.外观检查取样:同上。
检验方法:观察取样品是否有颗粒、异物、沉淀等。
3.PH值取样:同上。
检验方法:将取样品溶解于去离子水中,用PH计测定其PH值,与标准值进行比对。
4.溶解度取样:同上。
检验方法:将取样品溶解于去离子水中,观察其溶解程度。
5.氧化物含量取样:同上。
检验方法:取定量取样品进行氧化物含量测定,结果需符合标准。
五、检验结果处理及记录1.对于合格的中间产品,应妥善保存,并填写检验报告。
2.对于不合格的中间产品,应根据具体情况制定整改方案,可返工或销毁,同时填写检验报告。
3.所有检验结果需设定有效期限,过期失效。
4.检验结果需定期进行统计分析,及时发现问题并加以整改。
六、注意事项1.检验人员需经过专业培训,熟悉检验项目及操作方法。
2.检验过程中需严格按照操作规程进行,杜绝人为因素的干扰。
3.检验设备和试剂需定期维护、校准,确保准确可靠。
七、附录本操作规程需定期进行评审,根据生产实际情况进行修订。
涉及到的仪器设备进入维护与校准的记录需保存备查。
药品检验标准操作规程药品检验是保障药品质量安全的重要环节,其操作规程的严谨性和规范性直接关系到药品质量的可靠性和稳定性。
为了确保药品检验工作的准确性和科学性,制定了本操作规程,以规范药品检验标准操作流程,提高药品检验工作的质量和效率。
一、检验前的准备工作。
1. 检验人员应具备相关的药学、化学等专业知识和技能,熟悉药品检验的操作规程和标准。
2. 检验设备和仪器应经过校准和检验,确保其准确性和可靠性。
3. 准备好检验所需的标准药品和试剂,确保其纯度和稳定性。
4. 制定检验计划和流程,明确检验的目的和要求,确保检验工作的针对性和系统性。
二、检验操作流程。
1. 取样。
(1)按照规定的取样方法,从不同批次的药品中取得代表性样品。
(2)遵循正确的取样操作流程,避免外界污染和样品损坏。
2. 外观检验。
(1)对样品进行外观检验,包括颜色、形状、气味等方面的观察。
(2)记录外观检验结果,与标准进行比对,判断样品是否符合规定要求。
3. 物理性质检验。
(1)对样品进行密度、溶解度、熔点等物理性质的检验。
(2)使用准确的仪器和方法进行检验,确保结果的准确性和可靠性。
4. 化学成分检验。
(1)对样品进行主要化学成分的检验,包括含量测定、纯度测定等。
(2)使用准确的试剂和仪器进行检验,确保结果的准确性和可靠性。
5. 微生物检验。
(1)对样品进行微生物污染的检验,包括细菌、霉菌等微生物的检测。
(2)使用无菌操作技术和灭菌方法进行检验,确保结果的准确性和可靠性。
6. 结果判定。
(1)根据检验结果和标准要求,判定样品是否符合规定要求。
(2)对不合格的样品进行处理和记录,确保不合格样品不会流入市场。
三、检验后的处理。
1. 对检验结果进行统计和分析,及时发现问题并采取相应的措施。
2. 对检验过程中发现的问题和不足进行总结和反思,及时改进和完善操作规程。
四、操作规程的执行和监督。
1. 执行操作规程的检验人员应严格按照规程进行操作,确保检验结果的准确性和可靠性。
目的:为检验苯扎溴铵溶液中间产品规定一个标准的程序,以便获得准确的实验数据。
范围:适用于苯扎溴铵溶液中间产品的检验。
职责:检验员,检验室主任对本规程实施负责。
规程:
1 性状:本品为无色或淡黄色的澄清液体, 芳香, 味极苦, 强力振摇则产生多量泡沫;遇低温可能发生沉淀。
2 鉴别:
2.1 试剂与仪器
2.1.1 硫酸 2.1.2 硝酸钠
2.1.3 锌粉 2.1.4 5% 亚硝酸钠溶液
2.1.5 碱性B-萘酚试液 2.1.6 稀硝酸率
2.1.7 乙醇 2.1.8 硝酸银试液
2.1.9 氨试液 2.1.10 硝酸
2.1.11 氢试液 2.1.12氯仿
2.1.13 碘量瓶 2.1.14 电子天平(万分之一克)
2.1.15 移液管 2.1.16 小型三用水箱
2.1.17 烧杯;试管 2.1.18 量瓶
2.1.19 漏斗,漏斗架 2.1.20 滤纸
2.2 项目与步骤
2.2.1 取本品6 ml置水浴上蒸干后, 加硫酸1ml溶解后, 加硝酸钠0.1g, 置水浴上加热5分钟, 放冷, 加水10ml与锌粉0.5g, 置水浴上加热5分钟,取上清液2ml加5% 亚硝酸钠溶液1ml,在冰浴中冷却, 再加碱性B-萘酚试液3ml, 即显橙红色。
2.2.2 取本品溶液(1~100)10 ml加稀硫酸0.5 ml,即生成白色沉淀, 滤过, 沉淀加乙醇即溶
解;滤液显溴化物的鉴别反应。
2.2.2.1 取滤液, 加硝酸银试液, 即生成淡黄色沉淀, 分离 ,沉淀能在氨试液中溶解, 但在硝酸中几乎不溶。
2.2.2.2 取滤液, 滴加氢试液, 溴即离, 加氯仿振摇, 氯仿层变黄色或红棕色。
3. 含量测定
3.1 仪剂与仪器
3.1.1 水 3.1.2 氯仿
3.1.3 溴酚蓝指示液 3.1.4 氢氧化钠试液
3.1.5 四苯硼钠滴定液 (0.02 mol/L) 3.1.6 碘量瓶,量筒
3.1.7 移液管 3.1.8 滴定支架
3.1.9 滴定管
3.2 检验步骤
精密量取本品5ml 置碘量瓶中, 加水50ml 与氢氧化钠试液1ml 摇匀, 加溴酚蓝指示液0.4 ml 与氯仿10 ml, 用四苯硼钠滴定液(0.02 mol/L)滴定,将近终点时必须强力振摇至氯仿层的蓝色消失, 即得。
每1ml 四苯硼钠滴定液(0.02 mol/L)相当于7.969mg 的C 22H 40BrN. 本品为苯扎溴铵水溶液, 含烃铵盐以(C 22H 40BrN)计算,应为4.75%~5.25%。
计算: C%=%10050007969
0⨯⋅⋅⨯⨯F V 样
V 样:样品滴定ml 数
F :校正系数形
C :样品的百分含量(%)
4.规格:500ml ;。