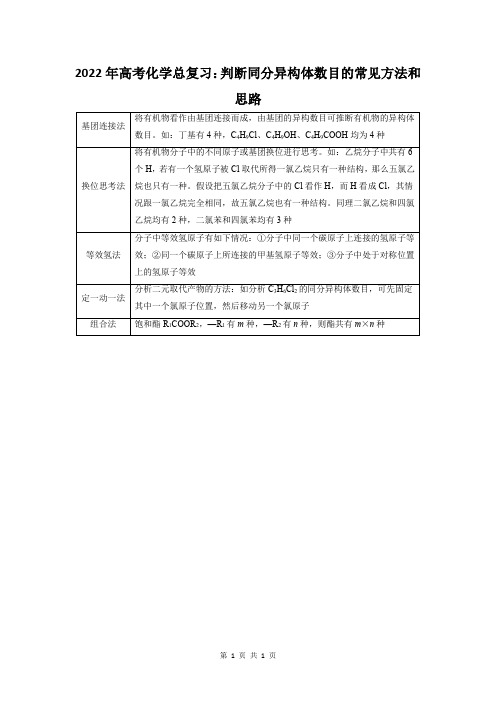
判断同分异构体数目的常见方法和思路
- 格式:pdf
- 大小:215.67 KB
- 文档页数:3

同分异构体数目判断四法同分异构体是指具有相同的分子式,但具有不同结构式的化合物。
同分异构体数目的判断是有机化学中的一个难点,下面介绍四种常见的判断方法。
一、等效氢法要点:①同—C上的H是等效的;②同—C上所连的上的H是等效的;③同一分子中处于轴对称或中心对称位置上的H是等效的。
例1 化合物中,假设两个H被一个和一个取代,那么得到的同分异构体数目为〔〕种。
解析:有两条对称轴即,所以有两种一氯代物即和,而这两种一氯代物都没有对称轴,所以从中再插入一个硝基各有7种,故共有14种。
二、不饱和度法不饱和度又称缺氢指数,即是将有机物分子与碳原子数相等的烷烃相比拟,每减少2个氢原子,那么有机物的不饱和度增加1,用表示。
假设有机物为含氧化合物,因为氧为二价,C=O与C=C“等效〞,所以在进行不饱和度计算时可不考虑氧原子。
至于有机物分子中的卤素原子,可视为氢原子。
例2 化学式为,且遇溶液呈紫色的芳香族化合物的数目是〔〕种。
解析:首先确定的不饱和度,由题中知其为芳香族化合物,而的不饱和度即为4,所以除苯环外,其他都是饱和的,即还有一个和一个,上连接一个和一个,有邻、间、对三种位置,故这类芳香族化合物的数目为3种。
三、优先组合法不同基团的连接组合方法:①定中心,连端基;②插桥梁基,定结构。
例3 某有机物的化学式为,结构中有2个,2个,1个,和1个,写出其可能的结构。
解析:首先定中心,连端基:即,再插入桥梁基,2个可分为两个和1个。
两个的插法有两种,即和;1个的插法有两种,即和。
四、换元法例4 二氯苯的同分异构体有3种,从而推断四氯苯的同分异构体有〔〕种;一氯戊烷有8种同分异构体,那么戊醇属于醇类的同分异构体有〔〕种。
解析:苯只有1种等效氢共6个,从6个中选2个与从6个中选4个完全相同,所以二氯苯的同分异构体有3种,四氯苯的同分异构体也有3种。
同理:把一氯戊烷中的氯换成醇中的,即得戊醇属于醇类的同分异构体有8种。
一.书写同分异构体的一个根本策略1.判类别:据有机物的分子组成判定其可能的类别异构(一般用通式判断)。

烷烃同分异构体数目口诀烷烃是指沿着碳碳键链为C基组成的烃类分子,烷烃同分异构体指在具有相同碳链结构,相同碳链重量的情况下,由于键的分布方式不同,而表现出不同的化学性质,物理性质的同分异构体的总和就是烷烃同分异构体数目。
那么我们如何来计算烷烃同分异构体数目呢?“ 十 - 八” 口诀可以提供我们一个有用的参考,此口诀概括计算方法为:1. 如果烷烃的碳链上有 n 个碳原子,就有 n! 共n× ( n−1 ) × ( n−2 )×...×3×2×1 种构型2. 单路重复:程序从最后一个碳原子开始,将它沿着 clockwise方向折叠,折叠一次等于1个异构体,直到碳链回到原来的顺序,就产生一个环型构型3. 双螺旋重复:若有位靠近碳链起点 -ω和终点α上靠近的碳被折叠,继续从终点α开始,逆时针折叠碳链若干格,直到α与ω重合(落在同一位置),这种折叠产生的异构体等于碳链长度减一。
因此,计算烷烃同分异构体数目的口诀“ 十 - 八” 就用上述的方法便可以计算出。
例如,要计算 C6H12 的烷烃同分异构体数目,n=6,因此有6!= 6×5×4×3×2×1 =720 个烷烃同分异构体。
此外,同分异构体数量也可以使用“Hypothetical Geometric Isomers Formulae” 公式来计算,它将单路重复和双螺旋重复因子分开,当一个有多个构型时,分裂开组成的n组元素之和,即为同分异构体的总数 .当考虑环烷烃的时候,可以假设环状烷烃有两个 end--groups 和一个中心碳,以及其他碳中的基,因此可以转换为 n--alkane 的形式计算,例如 C6H12 -- Cyclohexane,则所得烷烃同分异构体数目为 n--alkane 中的 6!,即 720 个。
综上所述,烷烃同分异构体数目可以使用“ 十 - 八” 口诀或 HypotheticalGeometric Isomers Formulae 公式来计算,本文介绍了烷烃同分异构体数目的定义和计算方法,希望对你有所帮助。


同分异构体书写及数目判断四川省旺苍中学杨全光 628200同分异构体的书写及数目确定是高考的必考点,通常有两种考查形式:一是以选择题的形式考查同分异构体的数目;二是以非选择题的形式考查某些具有特定结构的同分异构体的书写及数目判断。
一、同分异构体的书写先根据化学式写出通式进行物质类别判断后,书写时一定做到有序性和规律性。
1、降碳法(适用于烷烃):书写时要做到全面避免不重复,具体规则为主链由长到短,支链由整到散,位置由心到边,排列由邻到间,碳满四价。
例1、写出分子式为C7H16的所有有机物的结构简式。
【解析】经判断,C7H16为烷烃。
第一步:写出最长碳链(只写出了碳,氢原子根据“碳满四价”补足):(得到1种异构体);第二步:去掉最长碳链中1个碳原子作为支链(取代基),余下碳原子作为主链,依次找出支链在主链中的可能位置(↓表示取代基连接在主链上碳的位置),注意主链结构的对称性和等同性:(主链结构沿虚线对称,2与5、3与4处于对称位置,甲基连接在1或6将会和第一步中结构相同);第三步:去掉最长碳链中的两个碳原子作为支链,出现两种情况:⑴两个碳原子作为2个支链(两个甲基)(主链结构沿3号碳原子对称,采取“定一移二”法〈先将一个甲基固定在2号碳原子后另一个甲基可能连接在2或3或4位置得到3种异构体,然后将固定在2号碳原子的甲基固定在3号碳原子上,则另一个甲基只能连接在3位置得到1种异构体〉将得到4种异构体);⑵作为一个支链(乙基)(得到1种异构体);第四步:去掉最长碳链中的3个碳原子作为支链,也出现两种情况:⑴作为三个支链(三个甲基)(得到1种异构体);⑵作为两个支链(一个甲基和一个乙基):不能产生新的同分异构体。
第五步:最后用氢原子补足碳原子的四个价键。
2、插入法(适用于烯烃、炔烃、酯、醚、酮类等):所谓“插入法”是将官能团拿出,利用降碳法写出剩余部分的碳链异构,再找官能团(相当于取代基)在碳链上的位置(C和H原子间或C和C原子间),将官能团插入,产生位置异构。

2019-2020学年高一化学重难点探究(人教版必修二)重难点13 同分异构体的判断与书写方法探究1.同分异构体的种类、书写思路2.常用的同分异构体的推断方法(1)由烃基的异构体数推断判断只有一种官能团的有机物的同分异构体种数时,根据烃基的异构体数判断较为快捷。
如判断丁醇的同分异构体时,根据组成丁醇可写成C4H9—OH,由于丁基有4种结构,故丁醇有4种同分异构体。
(2)由等效氢原子推断碳链上有几种不同的氢原子,其一元取代物就有几种同分异构体。
一般判断原则:①同一种碳原子上的氢原子是等效的;②同一碳原子所连甲基上的氢原子是等效的;③处于镜面对称位置上的氢原子是等效的。
(3)用替换法推断如一个碳碳双键可以用环替换;碳氧双键可以用碳碳双键替换并将氧原子移到他处;又如碳碳三键相当于两个碳碳双键,也相当于两个环。
不同原子间也可以替换,如二氯苯C6H4Cl2有3种同分异构体,四氯苯C6H2Cl4也有3种同分异构体。
(4)用定一移一法推断对于二元取代物同分异构体的判断,可固定一个取代基的位置,再改变另一个取代基的位置以确定同分异构体的数目。
3.同分异构体的书写口诀主链由长到短;支链由整到散;位置由心到边(一边走,不到端,支链碳数小于挂靠碳离端点位数);排布由对到邻再到间;最后用氢原子补足碳原子的四个价键。
典例剖析例1 (2020·资中县第三中学高一月考)下列烷烃在光照下与氯气反应,能生成三种一氯代烃的是( ) A.CH3CH2CH2CH3B.C.D.答案C解析 A.分子结构中有两种化学环境不同的氢原子,则有两种一氯代物,故A错误;B.分子结构中有一种化学环境不同的氢原子,则有一种一氯代物,故B错误;C.分子结构中有三种化学环境不同的氢原子,则有三种一氯代物,故C正确;D.分子结构中有四种化学环境不同的氢原子,则有四种一氯代物,故D错误;综上所述,答案为C。
【点睛】同一个碳原子上的氢原子,为化学环境相同的氢原子,同一个碳上连接的甲基上的氢原子,也为化学环境相同的氢原子。

考点四:有序思维突破同分异构体的书写及数目判断难点拉分型——讲细练全一、从学法上掌握同分异构体的书写规律和数目判断的方法——夯基固本1.同分异构体的书写规律(1)烷烃:烷烃只存在碳链异构,书写时要注意全面而不重复,具体规则如下:(2)具有官能团的有机物:一般按碳链异构→位置异构→官能团异构的顺序书写。
(3)芳香族化合物:两个取代基在苯环上的位置有邻、间、对3种。
2.同分异构体数目的判断方法(1)记忆法:记住一些常见有机物异构体数目,如①凡只含一个碳原子的分子均无异构体;②乙烷、丙烷、乙烯、丙烯、乙炔、丙炔无异构体;③4个碳原子的烷烃有2种异构体,5个碳原子的烷烃有3种异构体,6个碳原子的烷烃有5种异构体。
(2)基元法:如丁基有4种,则丁醇、戊醛、戊酸都有4种同分异构体。
(3)替代法:如二氯苯(C6H4Cl2)有3种同分异构体,四氯苯也有3种同分异构体(将H和Cl互换);又如CH4的一氯代物只有1种,新戊烷C(CH3)4的一氯代物也只有1种。
(4)等效氢法:等效氢法是判断同分异构体数目的重要方法,其规律有:①同一碳原子上的氢原子等效。
②同一碳原子上的甲基上的氢原子等效。
③位于对称位置上的碳原子上的氢原子等效。
[题组训练]1.(2016·银川模拟)分子式为C3H4Cl2的链状有机物的同分异构体共有(不包括立体异构)()A.6种B.5种C.4种D.3种解析:选B可能的结构有:CH2===CHCHCl2、CCl2===CHCH3、CHCl===CClCH3、CHCl===CHCH2Cl、CH2===CClCH2Cl,B项正确。
2.芳香族化合物A的分子式为C7H6O2,将它与NaHCO3溶液混合加热,有酸性气体产生。
那么包括A在内,属于芳香族化合物的同分异构体的数目是() A.5 B.4C.3 D.2解析:选A芳香族化合物能与NaHCO3溶液发生反应有CO2气体产生,则此物质为,的同分异构体可以是酯,也可以是既含—CHO,又含—OH的化合物,依次组合可得:、、、四种。

同分异构体的快速书写及数目判断同分异构体的书写及数目确定是高考的必考点,通常有两种考查形式:一是以选择题的形式考查同分异构体的数目;二是以非选择题的形式考查某些具有特定结构的同分异构体的书写及数目判断。
一、同分异构体的书写先根据化学式写出通式进行物质类别判断后,书写时一定做到有序性和规律性。
1、降碳法(适用于烷烃):书写时要做到全面避免不重复,具体规则为主链由长到短,支链由整到散,位置由心到边,排列由邻到间,碳满四价。
例1、写出分子式为C7H16的所有有机物的结构简式。
【解析】经判断,C7H16为烷烃。
第一步:写出最长碳链(只写出了碳,氢原子根据“碳满四价”补足):(得到1种异构体);第二步:去掉最长碳链中1个碳原子作为支链(取代基),余下碳原子作为主链,依次找出支链在主链中的可能位置(↓表示取代基连接在主链上碳的位置),注意主链结构的对称性和等同性:(主链结构沿虚线对称,2与5、3与4处于对称位置,甲基连接在1或6将会和第一步中结构相同);第三步:去掉最长碳链中的两个碳原子作为支链,出现两种情况:⑴两个碳原子作为2个支链(两个甲基)(主链结构沿3号碳原子对称,采取“定一移二”法〈先将一个甲基固定在2号碳原子后另一个甲基可能连接在2或3或4位置得到3种异构体,然后将固定在2号碳原子的甲基固定在3号碳原子上,则另一个甲基只能连接在3位置得到1种异构体〉将得到4种异构体);⑵作为一个支链(乙基)(得到1种异构体);第四步:去掉最长碳链中的3个碳原子作为支链,也出现两种情况:⑴作为三个支链(三个甲基)(得到1种异构体);⑵作为两个支链(一个甲基和一个乙基):不能产生新的同分异构体。
第五步:最后用氢原子补足碳原子的四个价键。
2、插入法(适用于烯烃、炔烃、酯、醚、酮类等):所谓“插入法”是将官能团拿出,利用降碳法写出剩余部分的碳链异构,再找官能团(相当于取代基)在碳链上的位置(C和H原子间或C和C原子间),将官能团插入,产生位置异构。

例谈有机化合物同分异构体数目的判断方法嘿,咱今儿就来聊聊有机化合物同分异构体数目的判断方法,这可真是个有趣又重要的事儿呢!你想想看啊,就像一个大家庭里有好多兄弟姐妹,虽然都有血缘关系,但每个人又都有自己的特点。
有机化合物的同分异构体也是这样,它们有着相同的分子式,可结构却不一样。
咱先来说说碳链异构。
就好比搭积木,同样数量的积木,你可以搭出不同形状的结构体吧。
有机化合物里的碳原子也能排列出不同的碳链呢。
比如说丁烷,它就有正丁烷和异丁烷这两种同分异构体。
这就像是同样四根积木,能搭出不一样的样子。
然后是位置异构。
这就像是在一条街上,店铺的位置不同,产生的效果也不同。
比如苯环上的取代基位置不一样,那就是不同的同分异构体啦。
还有官能团异构,这就更有意思了。
就像同样是交通工具,有汽车、自行车、摩托车,虽然都能让你移动,但它们可大不一样呢。
比如醇和醚,它们就是官能团不同的同分异构体呀。
那怎么判断呢?咱得细心点儿,就像侦探找线索一样。
先看看碳链,把可能的碳链都摆出来。
然后再看看官能团的位置,有没有不同的可能性。
举个例子,戊烷有几种同分异构体呢?咱就先把碳链摆出来,有正戊烷、异戊烷和新戊烷三种呢。
是不是很神奇?再比如说,二甲苯有几种同分异构体?这就得好好想想啦,邻二甲苯、间二甲苯和对二甲苯,三种哦。
判断同分异构体数目可不能马虎,这关系到对有机化合物性质的理解呢。
要是弄不清楚,就好像在迷宫里转晕了头,找不到出路呀。
咱在学习的时候,得多做些练习,就像练功一样,练得多了,自然就熟练啦。
遇到难题也别怕,一点点分析,总能找到答案的。
总之啊,有机化合物同分异构体数目的判断方法可是化学里很重要的一部分呢。
掌握了它,就像是拿到了打开有机化学大门的钥匙,能让我们更好地了解和研究有机化合物。
所以呀,可得好好学,好好练,别偷懒哦!这可是关乎我们能不能学好化学的重要环节呢!你说是不是?。

同分异构体数目的判断方法
同分异构体(Isomers)是指具有一定键链的分子的结构形式
相同,但是化合物由不同的原子组成的分子。
它们具有相同的分子式和相同的分子质量,但是在空间上,具有不同的结构和物理性质。
分子结构相同,分子质量相同,但结构形式不同的化合物被称为同分异构体。
要判断对象是否是同分异构体,主要有以下几种方法:
一、根据分子结构,将分子构型进行简化成各种坐标系,如文谱分析、Zimm-Bragg模型、Ball-and-Stick模型等,然后比较
各坐标系的异同。
二、根据构象的不同,改变各元素原子间的键链顺序,形成不同的同分异构体,兼容分析各分子的构型是否相同。
三、根据空间结构不同,比较分子的空间构型,例如构象分析、空间分子结构图、曲面分析等。
四、根据实验分析,比较两种同分异构体的物理性质,如折射率、熔点、沸点等,并对比其它实验指标,以及比较它们的化学特性。
五、利用测序分析技术,根据同分异构体的分子的反应性等化
学特征,考察两个分子的一致性。
根据以上几种方法,我们可以非常准确地判断是否是一个同分异构体,子体不仅可以帮助我们更好理解分子结构,而且还可以提高分子的可利用性和应用价值。

高中化学同分异构体数目秒杀方法高中化学同分异构体数目秒杀方法是指在化学学习中,对于某些具有相同化学式的化合物,可以通过一些快速有效的方法来计算其同分异构体数目。
以下是几种常见的秒杀方法:1. 碳原子数法这种方法适用于分子中相同化学式的不同分子,可以通过计算每个分子中碳原子的数目来确定它们的同分异构体数目。
例如,对于分子 CH4 和 C2H6,它们具有相同的化学式,但它们的分子结构不同,因此它们的同分异构体数目也不同。
CH4 中有四个碳原子,每个碳原子与氢原子结合的方式只有一种,因此共有 4 种同分异构体;而C2H6 中有两个碳原子,每个碳原子与氢原子结合的方式也只有一种,因此共有 6 种同分异构体。
2. 官能团法这种方法适用于分子中具有相同官能团的化合物。
例如,对于分子 HCl 和 H2SO4,它们具有相同的官能团——氢氯酸官能团,但它们的分子结构不同,因此它们的同分异构体数目也不同。
由于氢氯酸官能团中含有一个酸根离子和一个氢离子,因此 HCl 中只有一种氢氯酸分子,而 H2SO4 中有两种氢氯酸分子,因此共有 2 种同分异构体。
3. 分子式相同但结构不同法这种方法适用于分子的分子式相同,但它们的结构不同的情况。
例如,对于分子 H2 和 O2,它们的分子式相同,但它们的结构不同,因此它们的同分异构体数目也不同。
由于 H2 中只有两个氢原子,而O2 中有两个氧原子,因此 H2 中只有一种分子,而 O2 中有两种分子,因此共有 2 种同分异构体。
以上是几种常见的高中化学同分异构体数目秒杀方法,可以帮助学生在考试中快速准确地计算同分异构体数目。
此外,学生还可以学习一些其他有用的同分异构体计算方法,如官能团法、碳原子数法等,以帮助他们更好地应对同分异构体的计算问题。

有机化学基础+判断同分异构体的五种常用方法和有机分子结构的测定海黄和紫檀哪个更有价值怕上当受骗,我们教你如何鉴别小叶紫檀的真伪!点击访问:木缘鸿官网北京十里河古玩市场,美不胜收的各类手串让记者美不胜收。
“黄花梨和紫檀是数一数二的好料,市场认可度又高,所以我们这里专注做这两种木料的手串。
”端木轩的尚女士向记者引见说。
海黄紫檀领风骚手串是源于串珠与手镯的串饰品,今天曾经演化为集装饰、把玩、鉴赏于一体的特征珍藏品。
怕上当受骗,我们教你如何鉴别小叶紫檀的真伪!点击访问:木缘鸿官网“目前珍藏、把玩木质手串的人越来越多,特别是海黄和印度小叶檀最受藏家追捧,有人把黄花梨材质的手串叫做腕中黄金。
”纵观海南黄花梨近十年的价钱行情,不难置信尚女士所言非虚。
一位从事黄花梨买卖多年的店主夏先生通知记者,在他的记忆中,2000年左右黄花梨上等老料的价钱仅为60元/公斤,2002年大量收购时,价格也仅为2万元/吨左右,而往常,普通价钱坚持在7000-8000元/公斤,好点的1公斤料就能过万。
“你看这10年间海南黄花梨价钱涨了百余倍,都说水涨船高,这海黄手串的价钱自然也是一路飙升。
”“这串最低卖8000元,能够说是我们这里海黄、小叶檀里的一级品了,普通这种带鬼脸的海黄就是这个价位。
”檀梨总汇的李女士说着取出手串让记者感受一下,托盘里一串直径2.5mm的海南黄花梨手串熠熠生辉,亦真亦幻的自然纹路令人入迷。
当问到这里最贵的海黄手串的价钱时,李女士和记者打起了“太极”,几经追问才通知记者,“有10万左右的,普通不拿出来”。
同海南黄花梨并排摆放的是印度小叶檀手串,价位从一串三四百元到几千元不等。
李女士引见说,目前市场上印度小叶檀原料售价在1700元/公斤左右,带金星的老料售价更高,固然印度小叶檀手串的整体售价不如海黄手串高,但近年来有的也翻了数十倍,随着老料越来越少,未来印度小叶檀的升值空间很大。
“和海黄手串比起来,印度小叶檀的价钱相对低一些,普通买家能消费得起。

同分异构体数目的判断1. 引言同分异构体是指化学式相同但结构不同的化合物。
在有机化学中,同分异构体的存在给化学合成、分析等领域带来了很大的挑战。
准确判断同分异构体的数目对于研究物质的性质、功能以及应用具有重要意义。
本文将介绍几种常用的方法和技术,帮助判断同分异构体的数目。
2. 化学式计算化学式是指描述化学物质组成的符号表示法。
对于有机化合物而言,化学式由元素符号和相应的原子数量组成。
通过分析化学式,我们可以大致确定同分异构体的数目。
2.1 总原子数的判断一个有机化合物的同分异构体数目取决于其总原子数。
根据数学组合学的原理,一个有机化合物由不同的原子组成,共有多种排列组合方式。
因此,总原子数越大,同分异构体的数目也就越多。
通过计算总原子数,我们可以估算同分异构体的数目的上限。
2.2 原子排列方式的判断除了考虑总原子数,我们还需要考虑同一元素的不同排列方式。
有机化合物中的碳、氢、氧等元素在分子中的位置、连接方式不同,也会导致同分异构体的产生。
因此,对于每个元素,我们需要计算其可能的排列组合方式,从而准确判断同分异构体的数目。
3. 光谱技术分析除了化学式计算,光谱技术是判断同分异构体数目的另一个重要方法。
光谱技术包括红外光谱、质谱、核磁共振等,通过分析不同光谱图谱,我们可以得到关于同分异构体的信息。
3.1 红外光谱红外光谱是通过测量化合物在红外光波段的吸收或发射来确定其分子结构的一种技术。
不同的化学官能团在红外光谱上表现出特异的吸收频率。
通过比对实验红外光谱图谱和数据库中的光谱数据,我们可以确定同分异构体的数目。
3.2 质谱质谱是通过将化合物分解成离子并在质谱仪中进行分析,从而得到化合物的质谱图谱。
不同的同分异构体具有不同的质谱图谱特征,包括离子峰的强度和相对分子质量等。
通过比对实验质谱图谱和数据库中的质谱数据,我们可以确定同分异构体的数目。
3.3 核磁共振核磁共振是通过测量化合物中不同原子核在特定磁场下的共振吸收来确定其分子结构的一种技术。

同分异构体的书写及数目判断技巧总结1.同分异构体的书写规律(1)烷烃:烷烃只存在碳链异构,书写时要注意全面而不重复,具体规则如下:(2)具有官能团的有机物:一般按碳链异构→位置异构→官能团异构的顺序书写。
例:(以C4H10O为例且只写出骨架与官能团)①碳链异构⇒C—C—C—C、②位置异构⇒③官能团异构⇒C—O—C—C—C、、C—C—O—C—C(3)芳香族化合物:两个取代基在苯环上的位置有邻、间、对3种。
(4)限定条件同分异构体的书写解答这类题目时,要注意分析限定条件的含义,弄清楚在限定条件下可以确定什么,一般都是根据官能团的特征反应限定官能团的种类、根据等效氢原子的种类限定对称性(如苯环上的一取代物的种数、核磁共振氢谱中峰的个数等),再针对已知结构中的可变因素书写各种符合要求的同分异构体。
2.同分异构体数目的判断方法(1)记忆法:记住一些常见有机物同分异构体数目,如①凡只含一个碳原子的分子均无异构体;②乙烷、丙烷、乙烯、乙炔无异构体;③4个碳原子的烷烃有2种异构体,5个碳原子的烷烃有3种异构体,6个碳原子的烷烃有5种异构体。
(2)基元法:如丁基有4种,则丁醇、戊醛、戊酸都有4种同分异构体。
(3)替代法:如二氯苯(C6H4Cl2)有3种同分异构体,四氯苯也有3种同分异构体(将H和Cl互换);又如CH4的一氯代物只有1种,新戊烷C(CH3)4的一氯代物也只有1种。
(4)等效氢法:等效氢法是判断同分异构体数目的重要方法,其规律有:①同一碳原子上的氢原子等效。
②同一碳原子上的甲基上的氢原子等效。
③位于对称位置上的碳原子上的氢原子等效。
典例分析1.与F()官能团的种类和数目完全相同的同分异构体有________种(不含立体结构),其中核磁共振氢谱为4组峰,且峰面积之比为1∶2∶3∶4的是________________(写结构简式)。
答案8解析F中含有2个羧基,与F官能团种类和数目完全相同的同分异构体有,共8种。




提升课2同分异构体的书写与判断[核心素养发展目标] 1.学会识别同分异构体,会判断同分异构的数目。
2.掌握限定条件下同分异构体的书写。
一、同分异构体的识别与数目判断1.单官能团有机物同分异构体数目的判断方法(1)基元法:例如丁基有4种,则丁醇、戊醛、戊酸等都有4种同分异构体;—CH3有1种,—C2H5有1种,—C3H7有2种,—C4H9有4种,—C5H11有8种。
(2)替代法:例如二氯苯(C6H4Cl2)有3种同分异构体,四氯苯也有3种同分异构体(将H替代Cl);又如CH4的一氯代物只有1种,新戊烷[C(CH3)4]的一氯代物也只有1种。
(3)等效氢法:等效氢法是判断同分异构体数目的重要方法,其规律有:①同一碳原子上的氢原子等效;②同一碳原子上的甲基氢原子等效;③位于对称位置上的碳原子上的氢原子等效。
当烃分子中有a种等效氢时,其一元取代物就有a种。
2.有机物的官能团异构(1)烯烃——环烷烃,通式:C n H2n(n≥3)。
(2)炔烃——二烯烃,通式:C n H2n-2(n≥4)。
(3)饱和一元醇——饱和一元醚,通式:C n H2n+2O(n≥2)。
(4)醛——酮、烯醇、环醚、环醇,通式:C n H2n O(n≥3)。
(5)羧酸——酯、羟基醛、羟基酮,通式:C n H2n O2(n≥3)。
(6)酚——芳香醇、芳香醚,通式:C n H2n-6O(n≥7)。
(7)硝基烷——氨基酸,通式:C n H2n+1NO2(n≥2)。
1.下列有关同分异构体数目的叙述中,正确的是()A.戊烷有2种同分异构体B.C8H10中只有3种属于芳香烃的同分异构体C.甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有6种D.CH3CH2CH2CH3光照下与氯气反应,只生成1种一氯代物2.青蒿素是抗疟特效药,属于萜类化合物,如图所示有机物也属于萜类化合物,该有机物的一氯取代物有(不含立体异构)()A.5种B.6种C.7种D.8种二、同分异构体的书写1.同分异构体的一般书写步骤碳架异构→位置异构→官能团异构。