冠状动脉分叉病变的分类及介入治疗方法(全文)
- 格式:docx
- 大小:21.79 KB
- 文档页数:13



左主干分叉病变的介入治疗策略(全文)冠状动脉左主干病变通过造影的检出率为5%-7%,一旦左主干出现狭窄或者闭塞,将会引起大面积心肌缺血,乃至恶性心律失常、心源性休克以及猝死等致命并发症。
因此,冠状动脉搭桥手术(CABG)一直是治疗左主干病变的金标准。
随着EXCEL和NOBEL临床研究数据的公布,证明对选择性无保护左主干病变行PCI治疗是安全和有效的。
由于超过80%的左主干病变会累及到左主干末端分叉,目前对于左主干末端分叉病变的最佳介入治疗策略还没有定论,而且左主干分叉病变的PCI治疗一直是临床的难点,所以本文将近年来左主干分叉病变的介入治疗策略做一综述。
一、左主干分病变病例的选择左主干病变治疗方法要依据目前的指南推荐。
目前欧洲的心肌血运重建指南已将SYNTAX评分<22分的左主干病变作为Ⅰb类推荐,将SYNTAX评分为23~32分者作为Ⅱa类推荐,将SYNTAX评分>32分,推荐进行冠脉搭桥手术。
美国的心肌血运重建指南,将SYNTAX评分<22分的左主干病变作为Ⅱa类推荐,将SYNTAX评分为23~32分者作为Ⅱb类推荐。
对左主干病变进行介入治疗时,应当由心脏团队进行决策,由经验丰富的术者完成。
可以通过使用SYNTAX、SYNTAXⅡ、NERS和EuroSCorE评分系统评估患者病变和临床的复杂性。
DEFINITION研究所提出的标准适用于左主干末端分叉病变。
二、术前左主干病变的影像学和功能学评估当左主干合并弥漫病变时,由于缺乏正常的参考血管段,单纯的根据冠脉造影检查评估左主干病变,容易造成误判。
与冠脉造影相比,IVUS 和OCT具有极高的分辨率,能够精确的评估左主干的病变、指导支架的置入以及术后的优化,改善患者的临床预后。
IVUS和OCT检查可以明确左主干斑块分布、组织特性、钙化弧度和狭窄的严重性。
FFR是评估左主干狭窄病变和相应分支病变血流动力学意义的重要诊断工具。
目前左主干介入干预的标准是:(1)造影显示左主干直径狭窄≥70%;(2)通过IVUS 或者OCT检查测得最小管腔面积(MLA)≤6.0mm2;(3)FFR≤0.80。

冠脉分叉病变的介入治疗策略目录➢分叉病变的基本概念➢分叉病变介入治疗的基本方法➢分叉病变的评估及治疗策略➢分叉病变介入治疗的临床问题及技术细节➢分叉病变介入治疗的新型辅助技术一、分叉病变的基本概念➢分叉病变占所有PCI的15%-20%, 30%-45%是真分叉病变;PMV:主干血管近段;MB:主干血管远段;SB:分支血管;POC:汇合多边区;Carina:分叉嵴➢冠脉分叉部血流方向发生改变,导致局部形成涡流或湍流;➢分叉嵴对侧低剪切应力区易形成斑块;➢分叉嵴对侧低剪切应力区湍流场可抑制药物支架再内膜化和损伤新生内膜,高剪切应力区则容易激活血小板。
1, 1, 1 1 , 1, 01, 0 , 10, 1, 11, 0, 00, 1, 00, 0, 1MBDistalMBProximal SB分叉病变的分型Medina 分型分叉病变的分型陈氏分型二、分叉病变介入治疗的基本方法分叉病变介入治疗的基本方法➢单支架技术✓Crossover✓开口精确定位➢双支架技术✓C rush✓C ulotte✓T支架✓V支架➢必要时支架技术单支架技术➢单支架Crossover✓简单Crossover✓支架过渡Crossover➢分支开口精确定位:✓常见用于前降支开口精确定位,也可用于其他分叉病变。
找到真正的开口是关键!✓Szabo技术单支架技术的主要难点在于分支保护!双支架技术➢Crush技术:包括经典Crush、Mini-Crush、DK-Crush 、Step-Crush、Rreversed-Crush等;➢Culotte技术:包括经典Culotte、Mini- Culotte、DK-Culotte等;➢T支架技术:包括经典T支架及改良T支架;➢V支架技术:包括V支架以及Kissing-Stent(SKS )。
Crush技术经典Crush技术Crush技术➢适应症:✓需双支架策略及分支与主支夹角<70°。


冠状动脉分叉病变Lefevre分型介入治疗技巧与策略(coronary bifurcation intervention)关键词介入治疗冠状动脉分叉病变KEY WORD:intervention coronary artery bifurcation lesions冠状动脉分叉病变是冠状动脉介入治疗的一个挑战。
分叉病变日渐增多,目前可以占到介入治疗的15%。
分叉病变治疗结果不令人满意,主要是分支的闭塞或难以通过支架孔隙扩张分支血管。
主要问题是涉及的分支(直径小于2.5mm,尽量避免支架置入)是否要保护。
直径<2.0 mm的小分支血管的闭塞可导致心绞痛或小面积心肌梗死,但临床意义及后果较小;而直径>2.0 mm的分支开口有>50%的狭窄,就需要保护措施,以免分支阻塞后产生严重后果。
最近研究分叉病变的主支和分支均置入支架比仅在主支置入支架的临床事件发生率高[1]。
因此目前主张分叉病变的支架置入仅在主支置入支架,分支用球囊或切割球囊或斑块旋磨治疗。
药物涂层支架可改变分叉病变长期预后。
1分叉病变的特点分叉病变由于主支与分支分叉的角度及斑块的累及部位不同可表现为不同的类型,术者应熟悉分叉病变的各种类型,根据分支的开口或与主支的角度、斑块累及主支与分支的范围、术中斑块可能发生的移行(或称铲雪效应"snow plow effect")做出相应的处理策略,是分叉病变手术成功的关键。
根据主支与分支的角度可分为二种类型:Y型病变:当分支和主支之间的角度小于70度时,此时导丝容易进入分支,但容易出现斑块的移行。
T型病变:当分支和主支之间的角度大于70度时,此时导丝进入分支可能有困难,但斑块移行较少。
根据斑块累及主支和分支的部位分叉病变可分为以下几型(Lefevre分型):1型病变:病变涉及主支近侧和远侧及分支开口。
2型病变:累及分叉位的主支,但未累及分支开口。
3型病变:病变位于主支的分叉近侧。

冠状动脉分叉病变术式演变与进展(全文)冠状动脉叉病变(简称叉病变)约占经皮冠状动脉介入治疗(PCI)术中所有病变的15%~20%。
分叉病变的介入治疗手术成功率低、存在远期心血管事件、靶病变再血管化、再狭窄以及支架内血栓形成等。
在分叉病变术式改良的过程中,出现了T支架系列术式、CRUSH系列术式、Culotte 系列术式等等,本文就分叉病变术式的演变及进展做一阐述。
1.分叉病变的定义与分型欧洲分叉病变俱乐部(EBC)对分叉病变的定义:冠状动脉病变邻近或累及较大分支开口处,该分支血管对于患者有明显的功能价值。
分支血管与缺血部位相关。
其支配大量存活心肌,提供侧支循环等,在PCI治疗过程中不可以丢失。
根据冠状动脉造影中,斑块的具体解剖位置及延续范围,目前对于冠状动脉分叉病变,已有多种不同的分型,如Duke分型、Lefevre 分型、Safian分型、Medina分型、Movahe分型、陈氏分型等从临床角度看分叉病变应分为两类:即病变累及分支开口部的真分叉病变和病变不累及分叉开口部的非真分叉病变,前者在主支支架后分支急性闭塞风险大,故适宜双支架策略和技术,后者则分支急性闭塞风险小,PCI宜采用单支架策略。
冠状动脉分叉病变的再狭窄率仍较高。
主要原因有:(1)支架在分叉病变血管开口处贴壁不良,未能完全覆盖开口。
(2)侧支血管的斑块“铲雪效应”或嵴移位导致其闭塞或明显狭窄。
(3)分叉部位的金属重叠,内皮覆盖缓慢,易出现晚期血栓事件。
NORDIC等临床研究的结果表明:相对于复杂的介入治疗策略,采用必要时支架置入术处理冠脉分叉病变具有操作简单、术后效果好的特点,因此对于边支开口部受累较轻或边支直径较小的分叉病变,目前主张首选必要时支架置入术治疗,但是对于主支和分支血管直径均≥2.5mm的真性分叉病变或预计主支置入支架后分支发生闭塞或严重狭窄者,应选择复杂治疗策略。
2.单支架技术单支架技术操作简单、对于适合的病变,近、远期疗效不劣于甚至优于双支架技术。
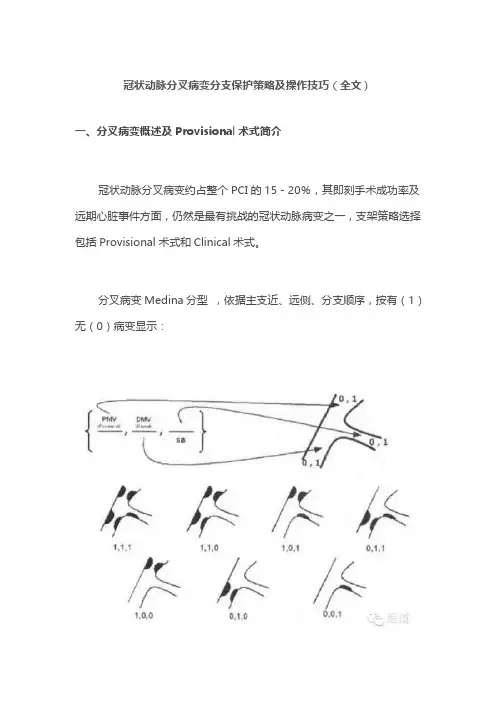
冠状动脉分叉病变分支保护策略及操作技巧(全文)一、分叉病变概述及Provisional术式简介冠状动脉分叉病变约占整个PCI的15-20%,其即刻手术成功率及远期心脏事件方面,仍然是最有挑战的冠状动脉病变之一,支架策略选择包括Provisional术式和Clinical术式。
分叉病变Medina分型,依据主支近、远侧、分支顺序,按有(1)无(0)病变显示:欧洲分叉病变俱乐部(EBC)对于分叉病变处理策略的推荐—对于绝大多数分叉病变推荐的策略是:主支支架置入+近端优化技术,必要时分支支架置入(MV Stenting with POT and Provisional SB Stenting )。
主支支架置入后分支血管存在一定几率发生闭塞的风险。
其危险因素包括:斑块分布、主支支架置入前分支TIMI血流、分叉核直径狭窄程度、分叉角度、主支/分支直径比、主支支架置入前分支狭窄程度。
分支闭塞的机理包括:主支支架置入后,斑块的铲雪效应、分支开口痉挛、分支开口斑块出现夹层、主支斑块出现夹层。
分支闭塞是PCI围术期MI最常见的原因,而围术期MI将增加患者死亡率。
所以,Provisional术式分支血管需要保护。
二、分支保护技术—导丝保护EBC专家共识推荐:分支导丝保护应作为分叉病变的常规操作,除非术者认为分支即使闭塞也不会有任何影响。
操作时应注意(1)导丝头端塑形,做好交换导丝的准备,(2)第二根导丝进入时,尽量减少旋转以避免导丝缠绕影响后续操作。
但分支导丝有时进入困难,影响因素包括:(1)主支近端严重狭窄,(2)分支开口部位狭窄,(3)分叉钝角且TIMI<3。
如果分支导丝进入困难,可使用特殊导丝技术:(1)可考虑使用亲水涂层导丝,但会增加夹层的风险,(2)特殊的导丝头端塑性,包括“导丝反转技术”,(3)可考虑使用单腔或双腔微导管,(4)如果导丝仍无法进入分支,可考虑使用球囊重塑斑块或者使用旋磨技术(最后使用,慎重使用)。

冠状动脉分叉病变分类及介入治疗技术策略关键字:冠状动脉分叉对吻支架对吻球囊扩张冠状动脉分叉处因为血液湍流和高剪切力而容易形成动脉粥样硬化斑块,分叉病变占经皮冠状动脉介入治疗总量的15%~20%。
一个真正的冠状动脉分叉病变是指主支血管(MV,main vessel)和分支血管(SB,side branch)形成倒“Y”型并且狭窄直径大于50%。
分叉病变介入治疗报道具有较低的手术成功率、较高的手术费用、较长的住院时间和较高的临床及造影再狭窄率。
因此,冠状动脉分叉病变介入治疗是介入心脏病学中一个具有挑战性的领域。
然而,最近在支架设计,选择性使用两个支架技术,可以接受的分支结果,以及各种技术的使用(如高压后扩张,对吻球囊扩张和血管内超声)等,使成功治疗并具有极佳长期预后的分叉病变介入治疗的病人数量迅速增加。
1分类分叉病变不仅在解剖形态上(如:斑块的位置、大小,分叉夹角大小,分叉的部位,分支的大小等) 是各种各样的,而且在治疗中解剖形态是有动态变化的(如出现夹层和斑块隆突移位)。
所以,绝对没有两个相同的分叉病变,也没有单一策略可被用于每个分叉病变上。
冠状动脉分叉病变先前已经被依据 MV 和 SB夹角和斑块位置被分类。
根据SB夹角的程度,分叉病变被分为(1) "Y"型:当夹角<70°,SB通过性常常不是很难,但是斑块移位会很显着,而且口部的支架精确定位释放是更困难和(2)"T"型:SB夹角>70°;SB通过性通常是更困难,但是斑块移位常较少,而且口部的支架精确定位释放更直接简单。
有以下几种分类法常常被使用。
1.1 Duke 分类:A型:病变只涉及主支近侧。
B型:只累及分叉后的主支。
C型:病变涉及主支近侧和远侧,分支未涉及。
D型:最常见,占40%,病变累及主支近侧和远侧及分支开口,形成倒“Y”形。
E型:只累及分支。
F型:累及主支近侧和分支开口处。

第一部分:冠状动脉分叉病变介入治疗临床现状据ARTS、SYNTAX等研究统计,冠状动脉分叉病变约占介入治疗的冠脉病变15%~20%。
冠状动脉分叉病变介入治疗策略是每个术者首要面临的问题。
每一个分叉病变都有其独特的分叉角度、血管尺径、斑块分布等特征,因此“没有两个分叉病变是完全一样的”。
冠状动脉分叉病变需要个体化介入处理,表现在治疗策略上就是必要性支架术或双支架术的选择。
一、冠状动脉分叉病变——双支架术式进入药物洗脱支架时代后,既往的一些术式有些被淘汰,有些又焕发新生,同时也涌现一些针对药物洗脱支架的新术式。
T支架术是一项较为“古老”的术式,由于该术式存在边支开口覆盖不完全的缺点,因此只能应用在一些分叉角度较大的病变中。
Culotte术式很好弥补了T技术的缺陷,边支开口覆盖完全,适用范围广泛。
但此术式血管内支架金属负荷较重,且操作较为繁琐,在金属裸支架时代其6个月TLR事件发生率可高达24%,因此此术式应用较少。
应用药物洗脱支架后,Culotte术式其结果产生极大改善,Hoye等研究显示MACE 事件5.3%、TLR15.4%。
不仅如此,Culotte术式在和T支架术、Crush技术比较时也毫不逊色。
Nordic bifurcation Ⅱ研究评价了药物支架时代Culotte技术处理冠脉分叉病变方面的临床效果。
与Crush技术作对比,研究显示术后8月造影显示节段内狭窄方面Culotte技术占优,支架再狭窄方面此优势仍然存在,且有统计学意义。
造影显示Crush技术边支开口再狭窄率高于Culotte技术(9.8%vs. 3.8%,P=0.04)。
SKS双支架术式目前也得到广泛应用,其操作简便,手术成功率高,疗效可靠。
但此术式在主支内两支架对吻处所形成的金属嵴是一个支架血栓形成的隐患,对此还需要进一步长期的研究。
Crush技术是为药物洗脱支架处理分叉病变所发明,该术式通过边支支架突入主支内3~5 mm以达到充分覆盖边支开口目的。

分叉病变的冠脉介入治疗(全文)冠状动脉分叉病变是一种常见的病变类型,具有难度大、耗时长和并发症多的特点。
必要时双支架术式为基础的介入处理策略是目前的主流观点。
当边支血流受损或出现其他需要处理的边支改变时,需转换术式,这是分叉病变介入治疗的难点所在。
1. 分叉病变关键解剖结构和分型血管分叉是动脉粥样硬化形成的重要影响因素。
分叉嵴远端因近端分流而形成低剪切应力区域,通常是斑块首先出现的区域。
分叉嵴近端迎血流面因为高血流剪切应力存在,通常不是动脉粥样硬化首先出现的部位,但当斑块发展至此区域时,高剪切应力则是促进后期斑块破裂的主要因素。
角度是分叉病变介入治疗中首先应当关注的解剖结构。
角度是指血管分叉部多边汇合区域中近端主干(PM)和主支(MB)或分支(SB)开口之间的角度。
分叉血管角度是实施双支架术式难度和术式选择的决定性因素之一。
角度过大者,可能给器械通过带来一定困难。
嵴是导致分叉病变介入治疗变得具有挑战性的核心解剖结构。
嵴一个明显特点是容易被推移,这也是分叉病变处理过程中出现主支远端或分支开口狭窄的主要原因。
当边支开口需要处理时,嵴的重建是影响预后的重要因素之一。
目前有许多学者对分叉病变提出不同分型方法,Medina分型虽然存在不能体现分叉血管角度、直径和指导术式等不足,但简单易记,而且容易区分真假分叉病变,仍然是目前实用性最强的分型方法。
Medina以3个的数字代表PM、MB和SB,其中“1”代表存在病变(狭窄≥50%),“0”代表不存在病变(狭窄<50%)。
当MB和SB开口均存在病变时定义为真性分叉病变(即1,1,1或0,1,1分型)。
在MB和SB的区分中,除了考虑血管直径外,还要考虑远端血管床数量和支配区域的对心功能影响。
2. 必要时分支支架(PS)策略虽然争论不断,但PS策略仍是目前多数学者接受的处理分叉病变的主要方法。
PS策略必须配合分支保护技术,球囊拘禁(JBT)技术是理想方法。
球囊浅埋可以一定程度上阻止嵴推移,而球囊深埋则可更容易地评估MB处理后SB血流,再决定是否扩张SB开口,同时不会增加撤出保护球囊前rewire的困难,是笔者最常使用的SB保护技术。
冠状动脉分叉病变介入治疗策略与方法的选择在药物洗脱支架时代,究竟是采用简单的单支架还是采用复杂的双支架策略治疗分叉病变极具争议。
现有的研究结果显示,单支架术处理分叉病变有略优的临床疗效,且前者有手术操作简单、曝光时间短、并发症发生率低、材料和费用低的优势,故现行指南或共识倾向于简单策略。
然而,对一些分叉病变如严重真分叉病变、主要血管分叉病变等,为规避术中重要血管的闭塞丢失、提高PCI术的安全性,双支架术仍然是不可或缺的选项。
那么,何时选择单支架术?何时需要双支架术?这是医生常需面对的艰难抉择。
一、决定单或双支架术的重要因素:哪些边支血管不容丢失?如果边支丢失与否都不在术者的考虑范围内,那么就不存在分叉病变了。
只有术者不想丢失的边支,才有分叉病变。
那么,什么样的边支是术者不想丢失的呢?1.供血范围较大的边支:供血范围大小主要取决于血管的直径和长度。
因长度较难测量且血管直径越大长度越长,故主要考虑边支血管直径。
此外,向重要部位供血的边支(如房室结、窦房结等)均是不容丢失的。
一般认为,边支血管直径≥2.0 mm需要保护、≥2.25mm应考虑支架植入。
2.狭窄程度较重的边支:包括狭窄的位置、程度和长度。
开口狭窄程度与边支闭塞风险相关。
狭窄越重,越易闭塞,单支架风险越大;边支病变越长,边支闭塞风险越高,越需支架覆盖。
一般认为,边支直径≥2.25 mm、开口狭窄≥50%、且病变长度≥10 mm需考虑支架植入。
3.斑块负荷较重的分叉:分叉部斑块负荷较大,尤其是斑块分布于边支同侧或逼近边支开口者,术中发生斑块推移导致边支闭塞的机会高。
4.分叉夹角极端的边支:分叉远角大('T'型病变)不容易发生嵴移位及斑块推移;而分叉远角小('Y'型病变)则容易发生嵴移位及斑块推移。
因此,'T'型病变更适合单支架术,'Y'型病变更需要双支架术。
然而,主支支架植入后,'T'或超大远角'T'型病变(边支倒钩状发出)一旦发生边支闭塞则拯救十分困难,故应综合其它因素可考虑是否先在边支植入支架,以防止边支丢失。
冠状动脉分叉病变的介入治疗进展何贵新【摘要】@@ 经皮冠状动脉介入术(percutaneous coronary intervention,PCI)分叉病变较为常见,约占30%[1].其处理是冠脉介入治疗的难题之一,因为分叉病变的介入治疗会导致斑块移位、分支血管开口弹性回缩等,甚至分支血管闭塞,从而增加并发症的发生和影响介入治疗的效果.因此,冠脉分叉病变是最复杂的冠脉病变之一.单纯的球囊扩张成形术治疗分叉病变成功率较低,且再狭窄率很高.金属裸支架(baremetal stent,BMS)的应用虽提高了分叉病变介入治疗的临床疗效和成功率,但再狭窄率较高.药物洗脱支架的临床应用显著改善了分叉病变的临床预后.本文就冠脉分叉病变的介入治疗现状综述如下.【期刊名称】《微创医学》【年(卷),期】2011(006)004【总页数】4页(P348-351)【关键词】冠状动脉;分叉病变;支架;介入治疗【作者】何贵新【作者单位】广西中医学院第一附属医院心内科,南宁市,530022【正文语种】中文【中图分类】R541.4;R654.33经皮冠状动脉介入术(percutaneous coronary intervention,PCI)分叉病变较为常见,约占30%[1]。
其处理是冠脉介入治疗的难题之一,因为分叉病变的介入治疗会导致斑块移位、分支血管开口弹性回缩等,甚至分支血管闭塞,从而增加并发症的发生和影响介入治疗的效果。
因此,冠脉分叉病变是最复杂的冠脉病变之一。
单纯的球囊扩张成形术治疗分叉病变成功率较低,且再狭窄率很高。
金属裸支架(baremetal stent,BMS)的应用虽提高了分叉病变介入治疗的临床疗效和成功率,但再狭窄率较高。
药物洗脱支架的临床应用显著改善了分叉病变的临床预后。
本文就冠脉分叉病变的介入治疗现状综述如下。
1 分叉病变定义及分型冠脉分叉病变是指冠脉主支、分支部位分别或同时存在严重狭窄的病变,主要包括左主干分叉病变、前降支-对角支、回旋支-钝缘支和右冠状动脉后三叉病变,约占所有冠状动脉介入治疗的30%,其中20%为主支血管存在病变,分支血管病变轻微。
冠状动脉分叉病变的分类及介入治疗方法(全文)在经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)领域中, 冠状动脉分叉病变是目前具有挑战性的病变类型之一。
冠状动脉分叉部位血液形成湍流且局部剪切力高,易形成动脉粥样硬化斑块[1],冠脉分叉病变占经皮冠状动脉介人治疗总量的15%-20%[2]。
冠脉分叉病变解剖结构千变万化,且治疗过程中也会随时改变,目前尚无适用于所有分叉病变的手术方法。
尽管近年来进展非常大,其治疗策略仍存在争论。
通常分叉病变的手术治疗方式分为六类:(1)单支架技术(one-stent technique,OST);(2)支架球囊技术(stent with balloon technique,SBT);(3)支架对吻技术(kissing stent technique,KST);(4)T支架技术(T stenting technique.TST);(5)支架挤压技术(crush stenting technique,CRT);(6)Cullotte支架技术(Cullotte stenting technique,CUT)。
与简单冠状动脉病变的PCI治疗相比, 分叉病变介入治疗手术远期心血管事件发生率、术后再狭窄率及手术费用较高, 而临床预后较差、手术成功率较低[2]。
因此,冠脉分叉病变最合适的策略、最优化的技术策略不只是要达到最佳的即刻临床效果,更重要的是要获得最佳的长期预后效果:较低的再狭窄、主要不良心血管事件(major adverse cardiovascular events,MACE)的发生率等。
1.分叉病变的定义冠脉分叉病变是指冠脉主支、分支部位分别或同时存在的严重狭窄的病变,主要包括前降支一对角支病变,其次为回旋支一钝缘支病变、右冠状动脉远段病变和左主干末端分叉病变。
冠状动脉真性分叉病变(bifurcation coronary lesions,BCI)是指分叉部位2支血管均有>50%的狭窄病变,且病变累及分支(side branch,SB)血管开口。
欧洲分叉病变俱乐部将分叉病变定义为: 病变邻近或累及较大分支口部, 该分支血管对于患者有明显功能价值(与症状有关、存在大量存活心肌、提供侧支循环以及对左心功能意义重大等),在介入治疗过程中不可丢失[3]。
治疗分叉病变最具有挑战性的是,在处理主支血管病变时,由于“铲雪”效应引起斑块移行、支架嵴移位等原因易导致邻近分支血管受累。
2.分叉病变的常见分型2.1 Duke分型:A型:病变只累及主支近侧。
B型:病变只累及分叉后的主支。
C型:病变累及主支近侧和远侧,分支未受累及。
D型:最常见,占40%,病变累及主支近侧和远侧及分支开口,形成倒“Y”型。
E型:病变只累及分支。
F型:病变累及主支近侧和分支开口处。
2.2 Safian分型主要根据是否存在主支狭窄及其狭窄部位而进行分型。
Ⅰ型:分叉近端和远端主支狭窄。
A:累及边支(真性分叉病变),B:边支正常。
Ⅱ型:分叉近端主支狭窄。
A:累及边支(真性分叉病变),B:边支正常。
Ⅲ型:分叉远端主支狭窄。
A:累及边支(真性分叉病变),B:边支正常。
Ⅳ型:主支正常,边支开口狭窄。
2.3 Lefevre[4]分型1型:病变累及主支近侧和远侧及分支开口。
2型:病变累及分叉部位的主支,但未累及分支开口。
3型:病变位于主支的分叉近侧。
4型:病变累及分叉的各分支开口,而不累及主支分叉的近侧。
4a型:病变累及主支的分叉远侧。
4b型:病变累及分支开口处。
2.4 Medina分型依据主支近、远侧及分支顺序,有病变记录为“1”,“无”病变记录为“0”。
狭窄程度≥50%病变显示为“1,0,1”,则表示主支近侧和分支有病变、主支远侧无病变。
Medina分型简单易记,但与Duke 分型、Lefevre分型、Safian分型类似,只考虑了病变位置和是否累及分支,而对其他分叉病变的信息未给予记录。
目前,国际上多数介入专家推荐此分型,因其简单明了,又可作为治疗参考,被多数人采用[5]。
2.5 Movahed[6]分型这是一种新的、实用的和具有预后价值的分叉病变分类法,考虑了斑块的位置、分布、血管直径、血管分叉角度、病变特征等因素,相对全面。
该分型由前缀、后缀1-4,共5部分组成,前缀B代表分叉病变,后缀1~2描述斑块的分布和血管直径;后缀2描述斑块是否累及分支血管;后缀3描述血管分叉角度;后缀4描述病变的钙化情况或左主干分叉病变。
所有真正的分叉病变被简单地归纳为一个容易记忆的B2类别(B =分叉,2 =同时涉及主支和边支开口)。
V代表角度<70°,T代表>70°。
以 B、C(N、S、L)、1M(1S、2)、V(T)、CA(LM,TR,TO,LL20)表示。
但任何分型都不能全面和真实的反映临床实际情况,手术时具体问题应具体分析2.6 陈氏分型阜外医院陈纪林教授按照分支开口是否有严重狭窄将分叉病变分为3种类型,分支开口有严重狭窄(≥50%)即为I型,反之为Ⅱ型,单纯分支开口严重狭窄为Ⅲ型。
在I和Ⅱ型中根据主支斑块负荷与分支开口的关系分为5个亚型,即中心型(a),指主支斑块骑跨在分支开口的类型,主支斑块负荷若主要集中在分支开口的上方、下方、左侧(对侧)和右侧(同侧)分别为b、c、d、e亚型[7-8]。
主支病变和分支开口的关系及规律性同Ⅰ型。
如分支开口有严重狭窄,而主支无狭窄或仅轻微病变,则为Ⅲ型。
新的分型法简化了分叉病变的分型,该分型法的优点是规律性强,容易记忆,同时对分叉病变的治疗有明确的指导作用,目前该分型已被部分国内外专家所引用并应用于临床[9]。
2.7 DINO分型该分型既提供了分支与主支的角度,又提供了病变分布范围和位置[10]。
DINO分型中冠状动脉分叉的定义由3部分构成:主支近端(proximal main branch,PMB)、主支远端(distal main branch,DMB)及分支(side branch,SB)。
这3个分支构成了3个叉:A.主支近端和主支远端构成了主支叉;B.主支近端和分支构成了近端叉;C.主支远端和分支构成了远端叉。
该分型根据分叉角度将分叉分为3 种:Y 型成角、T 型成角和反向成角[11]。
Y型成角分叉角度<70°;T型成角分叉角度70°-90°;反向成角分叉角度>90°[12]。
根据DINO分型描述分支病变时首先应用名词(三开口,双开口,单开口)或助记符(P代表主支近端,D代表主支远端,S代表分支)描述位置,继而分支成角(Y代表Y型,T代表T型,R代表反向成型)。
例如,一个三开口-T(PDS-T)病变,代表一个累及分叉三开口、分叉T型成角的分叉病变。
3.支架植入术策略及术式选择处理分叉病变的理想结果应该是保证主支满意开通,同时使侧支的残余狭窄<50%,达到TIMI血流3级,冠脉分叉病变具体策略有二:(1)单支架技术策略,有分支闭塞风险;(2)双支架技术策略,无分支闭塞风险,但是技术难度较大,事先确定策略最重要。
需要对分叉部位的病变特点进行仔细的研究,弄清是否真分叉病变和分支的大小,开口狭窄程度,与主支的角度,并判断急性闭塞的风险。
对于真分叉病变,分支血管内径>2.5mm,开口狭窄程度重(≥90%),与主支远端角度小的,一般应选择双支架技术。
国际上目前比较公认分叉病变理想的处理原则是,保证主支及分支的理想开放,或在保证主支理想开放的前提下,分支血管的残余狭窄< 50%,血流TIMI3级或冠状动脉血流储备分数(Fractional Flow Reserve,FFR)≥ 0.75,即分叉病变的支架置入,尽可能的在主支置入一个支架,除非当分支的解剖比主干解剖更重要,分支供血范围大于主支时,可在分支置入支架。
单支架技术处理分叉病变,是目前主流。
需要指出的是,临床中确实有部分分叉病变,因分支血管的管径较粗(≥2.5mm)、供血范围较大,单支架置入后可能会造成分支开口严重狭窄和(或)闭塞,这时应考虑采用双支架治疗策略。
此外,高压后扩张、球囊对吻技术及血管内超声应用也使得双支架植入术效果更理想。
冠状动脉分叉病变介入治疗策略选择时,应当兼顾主支血管的角度、病变的位置和程度以及分支血管的直径及供血范围等。
分叉病变治疗策略应遵循个体化原则,审慎选择。
3.1 单支架技术临床研究表明,分叉病变的处理应倾向于简单策略,在主支内植入支架,分支如果血流好则尽量避免植入支架[13-14]。
只在主支(Main Vessel, MV)植入支架,是临床上最简单和最常用的技术。
一般适合于分支急性闭塞风险很小者。
其操作要点:(1)分别送人主支和分支双导丝;(2)必要时分别预扩主支和分支狭窄病变;(3)分支导丝保留,植入主支支架;(4)必要时(分支残余狭窄严重时)将主支导丝经支架网眼送人分支,分支导丝“交换”送入主支远端;(5)送入大小与血管和支架匹配的球囊分别扩张分支和主支,并最后完成较低压(8~10atm)对吻扩张;(6)造影下主支支架充分扩张,两端无夹层,分支血管扩张满意也无严重夹层,血流正常者即结束;(7)若造影下分支病变未获满意扩张,残余狭窄严重(≥90%)或严重狭窄影响血流而濒临闭塞时,应考虑即时分支(Side Branch,SB)支架植入(即时双支架技术)[15]。
3.2 双支架技术对于真性分叉病变且分叉血管直径较粗的,特别是当分支开口严重狭窄且开口直径大于2.5 mm,供血范围广泛时,直接采用双药物洗脱支架植入是大部分专家的首选治疗方式[16]。
双支架植入的主要问题是技术复杂且急性、亚急性和晚期支架内血栓的风险增大[17],因此对术者的技术和经验要求很高。
分叉双支架术式传统上分为4类:A.先在分支植入支架,然后在主支植入支架,包括“T”、挤压(crush)和分步挤压(step crush)支架技术等;B.先在主支植入支架,然后通过主支支架网眼向分支植入支架,包括即时T(provisional T)、反向挤压(inverse crush)、和内挤压或即时挤压(internal or provisional crush)支架技术等;;C.先在主支植入支架,然后通过网眼向分支植入支架,但第2 个支架在主支近端与第1 个支架重叠包括(culotte or trousers)支架技术;D.在主支和分支同时植入支架,指“V”支架技术。
目前常用的术式包括V支架术(经典的、改良的)、对吻支架术、Crush支架术(包括标准Crush,mini-Crush,Reverse-Crush,Inverted Crush,Step Crush),T支架术(包括经典和改良T支架术、TAP术式等)、Cullote术式(包括经典的、改良的)等[18]。