内部质量审核实施计划
- 格式:doc
- 大小:43.00 KB
- 文档页数:1

iso13485质量管理体系内部审核方案ISO 13485质量管理体系内部审核方案概述ISO 13485是为医疗器械行业制定的质量管理体系标准,要求医疗器械制造商建立和维护一个有效的质量管理体系以确保产品质量和安全性。
内部审核是评估质量管理体系有效性的重要步骤,通过对体系进行周期性审查,可以识别和纠正潜在的问题,持续改进体系的运行。
目标本内部审核方案的目标是确保公司的质量管理体系符合ISO 13485标准的要求,并提供持续改进的机会。
通过内部审核,可以识别并纠正体系中的问题,促进公司质量文化的建立,并增强员工对质量管理体系的意识和参与度。
审核程序1. 选拔审核员内部审核应由经过合适培训并具备相关经验的审核员来执行。
审核员的选拔应根据其专业知识、技能和适用经验进行评估。
最好是建立一个内部审核团队,确保审核的连续性和一致性。
2. 制定审核计划根据ISO 13485标准的要求,制定年度内部审核计划。
审核计划应涵盖所有相关的管理和操作程序,并对审核的频率进行评估。
根据审核计划,确定每次内部审核的审核范围、目标和时间表。
3. 实施内部审核内部审核应按照预定的计划进行。
审核员应准备相关文件和审核记录表,并与审核对象进行会议。
在审核过程中,审核员应进行文件和记录的检查,并与员工进行访谈以了解他们对质量管理体系的理解和遵守情况。
审核员还应观察工作场所和实际操作,并记录发现的任何不符合或改进机会。
4. 编写审核报告审核员应根据审核结果编写审核报告。
报告应包括审核的范围、日期、审核员名单、发现的不符合项和改进机会,以及建议的纠正措施。
报告应清晰明了,并根据不同部门或功能进行分析和总结。
5. 采取纠正措施审核报告应提交给相关部门负责人,并要求他们采取纠正措施以解决发现的不符合项和改进机会。
纠正措施应具体、可执行,并在规定的时间内得到落实。
审核员应跟踪和审查纠正措施的执行情况,并记录并报告进展情况。
6. 审核跟踪在下一次内部审核中,审核员应跟踪上一次审核报告中提出的纠正措施的执行情况。


内部审核的策划和实施步骤概述内部审核在企业管理中起着至关重要的作用,它可以帮助企业发现问题、改进流程,并确保企业在法律、道德和质量等方面符合要求。
本文将介绍内部审核的策划和实施步骤,帮助企业进行有效的内部审核。
策划步骤1.确定内部审核的目的和范围:在策划内部审核之前,需要明确内部审核的目的和范围。
目的可能包括发现问题、改进流程、确保合规等等。
范围可能包括某个部门、某个项目或者整个企业。
2.确定内部审核的周期:根据企业的情况和需要,确定内部审核的周期。
内部审核的周期可以是每月、每季度或每年一次。
周期的确定应该考虑到企业的资源和需求。
3.确定内部审核的团队:选取适当的团队成员参与内部审核。
内部审核团队应该由具有相关经验和知识的人员组成,以确保审核的准确性和有效性。
4.制定内部审核计划:根据目的、范围和周期,制定详细的内部审核计划。
计划应包括审核的时间表、流程和所需资源。
实施步骤1.筹备工作:在内部审核之前,需要做一些筹备工作。
首先,向相关部门通知内部审核的时间和范围。
其次,收集和整理有关文件和记录,以供审核使用。
最后,准备内部审核所需的表格、模板和工具。
2.进行审核:在内部审核过程中,按照计划进行审核工作。
具体步骤如下:–开始会议:在内部审核开始前,召集内部审核团队成员和需要审核的部门的代表开会,介绍内部审核的目的和流程。
–访谈:与相关人员进行面谈,了解他们对相关流程和政策的了解和遵守情况。
这可以通过提问、观察和检查记录等方式进行。
–检查记录和文件:检查相关记录和文件,确保其符合规定要求,并遵守内部政策和相关法律法规。
–检查实际操作:观察实际操作,确保其符合流程和要求,并纠正任何不符合的行为。
–提出建议和改进建议:根据审核结果,提出改进建议,并与相关部门一起讨论并制定改进计划。
3.撰写内部审核报告:在内部审核完成后,整理审核过程中收集的信息和结果,撰写内部审核报告。
报告应该包括审核的目的和范围、发现的问题和建议的改进措施。

IATF16949内部审核方案第1步:准备内部审核计划在开始内部审核前,需要制定一个详细的计划。
该计划应包括以下内容:-内部审核的范围和周期,以确定需要审核的区域和时间段。
-内部审核的团队成员,包括审核员和审核领导者。
-内部审核的资源需求,如审核员培训、文件和记录等。
-内部审核的流程和时间表,包括准备阶段、实地审核和报告编写等步骤。
第2步:准备审核程序和文件在内部审核开始前,需要准备相关的程序和文件,以便审核团队使用。
这些文件包括:-组织的质量相关文件和记录,如工作指导书、工艺流程图和质量检验报告等。
-内部审核的文件和表格,如审核计划、审核报告和问题记录表等。
第3步:实地审核在实施内部审核时,应按照方案中规定的范围和时间表进行。
以下是内部审核的一般步骤和要点:-开始会议:由审核领导者主持,介绍审核目的、过程和时间表。
-拉开帷幕:审核团队用于形容开放性的问题或发现,以引导受审人员讨论和解决问题。
-实地检查:审核团队需参观实地,检查质量管理体系的实施情况,并与工作人员进行交流。
-记录问题:审核团队需记录发现的问题、缺陷和矛盾,以便后续报告和改进。
第4步:问题报告和改进在内部审核结束后,审核团队应编写一份内部审核报告,汇总审核结果和问题建议。
以下是内部审核报告的主要内容:-审核目标和范围的总结。
-审核过程中发现的问题和缺陷。
-对组织质量管理体系的评估和改进建议。
-内部审核团队的反馈和建议。
第5步:内部审核跟踪内部审核结束后,组织应跟踪并落实内部审核报告中的问题和建议。
以下是内部审核跟踪的一些步骤:-制定行动计划:组织应根据内部审核报告中的问题和建议,制定相应的行动计划。
-跟踪行动计划的实施:组织应确保行动计划的实施,并根据需要进行内部审核的跟踪与检查。
-审核成果的验证:组织应通过再次进行内部审核或使用其他验证方法,确保问题解决和改进措施的有效性。

化妆品年度全套内部审核检查计划、内审记录表及内审报告
年度内部审核检查计划
1、内部检查目的:
为了使公司化妆品生产质量体系体系能满足国家法律法规、规章制度、化妆品生产许可工作规范要求以及相关国家标准要求,审查公司体系及体系的运行情况,及时发现问题并加以纠正及预防,使公司体系持续有效、不断改进、不断完善。
2、内部检查组长任命:
为使审核工作计划得以按时按标实施,任命xxx 为内部检查审核组长,负责内部检查工作的计划、实施及指导等工作。
3、审核组成员:
4、内部检查依据:
《化妆品卫生监条例》、《化妆品卫生监督条例实施细则》、《化妆品生产许可工作规范》、《广东省化妆品安全条例》、《化妆品安全技术规范》、《质量手册》等。
5、内部检查计划表:
6、首次会议:
7、内审检查表(人事行政部):
7、内审检查表(品管部):
7、内审检查表(设备部):
7、内审检查表(供销部):
7、内审检查表(生产技术部):
8、不符合项报告:
9、末次会议:
10、化妆品生产质量体系内部检查报告:
内部检查报告。
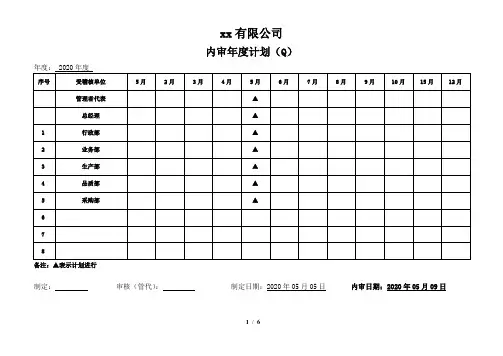
xx有限公司
内审年度计划(Q)
备注:▲表示计划进行
制定:审核(管代):制定日期:2020年05月05日内审日期:2020年05月09日
1/ 6
内审实施计划(Q)
首、末次会议记录表(Q)
不符合报告(Q)
依据:GB/T19001-2016/ISO9001:2015版标准
受审核部门品质部内审编号1/1
审核员: xxx 审核日期2020年05月09日不合格描述:
品质部检查未见4月的质量目标完成情况统计,不符合ISO9001:2015标准9.1.3条款要求
●不符合标准/文件: 9.1.3
●不符合类型:体系性不合格实施性不合格效果性不合格
●不符合程度:轻微严重不合格
审核员:xxx 部门负责人:xxx
不合格原因分析:
品质部负责人责任心不足,以及对相关标准的理解和执行的不到位,造成漏统计4月质量目标完成情况。
分析人:xxx 建议采取的纠正措施:
1. 立即进行GB/T19001-2016/ISO9001:2015 9.1.3条款培训,加强对相关标准的理解。
2. 立即对4月目标完成情况进行统计。
批准:xxx
纠正措施已完成:2020年05月10日开始已经按照要求进行改善。
部门负责人:xxx
跟踪验证:已经整改完成。
审核员:xxx
体系审核报告(Q)。

医疗器械内部审核工作计划
以下是一份医疗器械内部审核工作计划的示例:
1. 审核目标确定:
确定本次审核的目标,例如审核医疗器械质量管理体系是否符合相关法规和标准要求。
2. 审核范围确定:
确定需要审核的医疗器械质量管理体系的相关文件和记录,包括质量手册、程序文件、作业指导书等。
3. 审核计划制定:
制定详细的审核计划,包括审核时间、地点、参与人员、审核方式等。
4. 审核准备:
针对审核目标和范围,收集必要的信息和文件。
对参与审核的人员进行培训,提供相关背景和知识。
准备审核所需的工具和设备,如电脑、审核表、文件夹等。
5. 实施审核:
按照审核计划进行审核。
使用审核表记录审核结果和问题。
进行现场观察和访谈,了解实际操作情况。
6. 问题整理和分析:
将审核过程中发现的问题整理成问题清单。
对问题进行分类和分析,找出根本原因。
7. 编写审核报告:
根据审核结果和问题分析,撰写审核报告,包括问题汇总、原因分析和改进措施建议。
8. 提交审核报告:
将审核报告提交给相关部门和管理层,给予必要的解释和建议。
9. 跟踪改进措施:
跟踪和监督所提出的改进措施的执行情况。
定期评估改进措施的有效性和可行性,并进行必要的调整和改进。
10. 审核结果评估:
对整个审核过程进行评估,包括审核的有效性、及时性和可行性。
提出改进建议,用于提升的审核工作质量。
以上是一份医疗器械内部审核工作计划的示例,具体的工作计划可以根据实际情况进行调整和完善。


内审实施计划一、背景随着企业经营环境的不断变化和复杂化,内部控制和风险管理越来越受到重视。
内部审计作为一种重要的管理工具,在确保企业内部控制有效、风险可控方面发挥着重要作用。
为此,本文将就企业内部审计实施计划进行深入探讨。
二、内审目标内部审计的目标是评估和改进组织的内部控制和风险管理,以提供保障和增强组织价值的建议。
具体包括:1.评估和验证内部控制制度的有效性;2.确认业务执行的合规性,并发现潜在的违规情况;3.识别和评估潜在的风险,提出有效的应对方案;4.提供独立和客观的审计意见,帮助管理层做出数据驱动的决策。
三、内审实施计划1.确定审计范围:首先要明确审核的对象范围,包括审计的业务、流程、部门和地区等。
2.编制审计计划:根据审计范围和目标,制定详细的审计计划,明确审计的时间节点、方法和程序。
3.实施调查和审核:执行审计计划,收集和分析审计证据,评估内部控制和执行情况。
4.撰写审计报告:根据审计调查结果,撰写审计报告,列明问题和改进建议,并提交给管理层。
5.跟踪监督:对审计报告中的问题和建议进行跟踪,确保管理层采取有效措施改进。
四、内审实施方法1.风险驱动:内审工作应当根据风险评估结果确定审计重点,确保资源的有效利用。
2.数据分析:运用数据分析工具和技术,加强审计效率和准确性,发现潜在问题。
3.合作沟通:与被审计部门紧密沟通和合作,增进审计效果,确保合作意识。
4.审计技能:内部审计人员要具备良好的审计技能和专业知识,提升审计质量。
五、内审效果评估内部审计的效果评估主要包括对审计工作本身、审计报告的实施情况和审计影响的评估。
通过对内部审计工作的绩效评估,可以及时纠偏,提升审计质量,提高其对企业的价值贡献。
六、结语内部审计是企业内控和风险管理的重要组成部分,其实施计划的详尽和科学性对于企业的长远发展至关重要。
只有坚持不懈地进行内部审计,持续改进审计方法和手段,才能更好地为企业的健康发展提供保障。
以上就是内审实施计划的相关内容。

区分:■定期□临时发行时间: 2016年 4月 27日审核目的:(1)审查公司质量管理体系运行是否符合策划的安排。
(2)审查公司质量管理体系运行是否得到有效实施和保持。
审核依据:(1)TS/16949:2009《质量管理体系-要求》标准;(2)公司发布的B/0 版《质量手册》、现行《程序文件》、作业指引以及相关规定和准则;(3)顾客的特殊要求。
审核范围:公司各级领导、质量管理体系标准要求实施职责权限有关的各部门、作业岗位和作业人员。
审核组长刘黎审核组员A组:胡纯林(副组长) 朱光明袁银强B组:邓中立(副组长) 罗天骄胡涛C组:杨坤(副组长) 方国栋张智慧审核时间2016年4月27日,28日,29日共计3天现场审核期间受审核部门/人员应注意事项:(1)首、末次会议时管理者代表及审核的部门主管和审核成员全部要准时参加。
(2)审核活动按审核计划安排,被审核有关人员应在本岗位。
(3)审核人员请准时到被审核单位,如有特殊情况请向审核组长请假,指定适宜的代理人员。
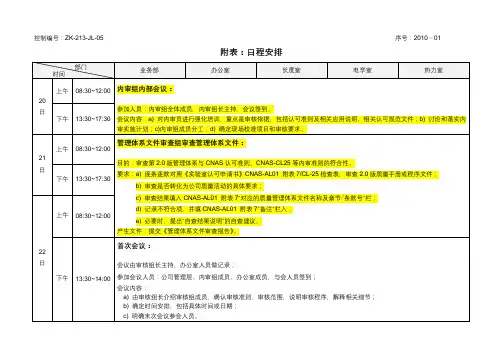
日期时间审核内容、过程、范围、功能审核员4月27日9:00-9:30 首次会议相关全体9:40-10:30管理评审/目标与经营计划4.1, 4.2,5.1~5.5,5.6 ,6.1,7.1,8.1, 8.5.1A9:30-16:30营销与订单/产品防护与交付/顾客反馈7.2, 7.5.1, 8.2.1C10:30-16:30过程设计与开发7.1, 7.2, 7.3, 7.5, 6.3, 6.4, 8.1, 8.2, 8.4, 8.5A9 : 30-16:30生产过程/职责与权限/基础设施和资源提供7.5, 8.2.3, 8.2.4, 8.3, 8.4, 6.1,6.3, 6.4B总经理管理者代表发行部门韩勇刘黎ISO推行内部审核实施计划4月28日9:00-12:00采购过程7.4, 8.4 C 9:00-12:00产品防护与交付7.4.3, 7.5.3, 7.5.4, 7.5.5 B 13:30-16:30人力资源管理6.2 C实际生产生产过程/过程产品的监视和测量(shift 2)7.5, 8.2.3, 8.2.4, 8.3, 8.4, 6.3, 6.4B 9:00-12:00监视和测量装置管理/不合格品控制/设备工装管理8.2, 8.3,7.5.1.5A 13:30-16:30数据分析/纠正预防措施/文件记录控制8.3, 8.4, 8.5 ,4.2.3A4月29日8:30-9:30内部审核8.2.2C 10:30-11:30 审核报告准备/其它审核组13:30-14:30 末次会议相关全体14:30 结束/ 14:30-17:00 不符合项改善报告发放至责任部门审核组附件:审核过程与各职能部门对应参考表(如下图表)序号过程主要涉及部门审核组1 管理评审/目标与经营计划管理者代表/总经理 A2 营销与订单营业部 C3 过程设计与开发工程部 A4 生产过程生产部 B5 产品防护与交付PMC部 C6 顾客反馈营业部 C7 文件记录控制体系推行 A8 人力资源管理人力资源部 B9 基础设施和资源提供生产部 B10 设备工装管理生产部 A11 监视和测量装置管理品质部 A12 采购过程控制采购部 C13 过程产品的监视和测量品质部 B14 不合格品控制生产部 A15 数据分析品质部 A16 标识和可追溯性生产部 A17 目标与经营计划营业部 C18 职责与权限人力资源部 B19 内部审核体系推行 C20 管理评审体系推行 C21 纠正预防措施品质部 A。
化妆品年度全套内部审核检查计划、内审记录表及内审报告
年度内部审核检查计划
1、内部检查目的:
为了使公司化妆品生产质量体系体系能满足国家法律法规、规章制度、化妆品生产许可工作规范要求以及相关国家标准要求,审查公司体系及体系的运行情况,及时发现问题并加以纠正及预防,使公司体系持续有效、不断改进、不断完善。
2、内部检查组长任命:
为使审核工作计划得以按时按标实施,任命xxx 为内部检查审核组长,负责内部检查工作的计划、实施及指导等工作。
3、审核组成员:
4、内部检查依据:
《化妆品卫生监条例》、《化妆品卫生监督条例实施细则》、《化妆品生产许可工作规范》、《广东省化妆品安全条例》、《化妆品安全技术规范》、《质量手册》等。
5、内部检查计划表:
6、首次会议:
7、内审检查表(人事行政部):
7、内审检查表(品管部):。
xxxx年度内部审核计划
一、审核目的:
1.为检查公司质量管理体系是否正常有效并得以保持,并对其符合性、有效性、适宜性进行评价;
通过对公司质量管理体系的内部审核,保证公司质量管理体系的正常持续运作。
二、审核依据:1.xxxx:xxxx标准;
2、公司质量管理xx文件;
3、顾客的要求;
4、相关法律、法规及其他要求。
三、审核范围:
四、审核方式:
五、审核组成员:
六、审核安排:
1.每年对公司整合体系所涉及的管理层、各部门进行一次集中内部审核。
2.每年进行一次管理评审。
七、内部审核的具体审核日期由审核组长提前一周制定内部审核实施计划,并将计划下发至各部门。
编制:审核:批准:日期:。
16949质量管理体系年度审核计划一、审核目的为了确保公司的质量管理体系持续有效运行,符合 IATF 16949 标准的要求,提高产品和服务质量,增强客户满意度,特制定本年度的审核计划。
通过审核,发现质量管理体系中存在的问题和不足之处,采取纠正和预防措施,不断完善和优化质量管理体系,为公司的持续发展提供有力保障。
二、审核范围本次审核范围涵盖公司的所有部门和过程,包括但不限于设计开发、采购、生产制造、销售与服务等。
三、审核依据1、 IATF 16949 质量管理体系标准2、公司的质量管理体系文件,包括质量手册、程序文件、作业指导书等3、适用的法律法规和客户要求四、审核组组成审核组长:_____审核组员:_____、_____、_____五、审核时间安排1、第一次内部审核审核时间:具体时间 1审核部门:采购部、生产部审核天数:2 天2、第二次内部审核审核时间:具体时间 2审核部门:销售部、售后服务部审核天数:2 天3、管理评审评审时间:具体时间 3参与人员:公司高层管理人员、各部门负责人4、第三方审核(如有)审核时间:根据第三方机构安排确定六、审核内容1、采购过程供应商的选择、评价和管理采购合同的签订和执行采购产品的验证和检验2、生产过程生产计划的制定和执行生产设备的维护和保养生产过程中的检验和测试不合格品的控制3、设计开发过程设计开发策划设计输入和输出的评审设计验证和确认设计更改的控制4、销售与服务过程客户需求的识别和确认合同评审客户满意度调查和反馈处理售后服务的提供和改进5、质量管理体系文件质量手册、程序文件和作业指导书的完整性和有效性文件的控制和管理6、内部审核和管理评审内部审核的策划、实施和记录管理评审的输入、输出和决议的执行7、人力资源管理人员的培训和考核员工的资质和能力8、测量、分析和改进数据的收集、分析和应用持续改进项目的实施和效果评估七、审核方法1、查阅文件和记录2、现场观察和检查3、与相关人员进行面谈和询问八、审核结果的处理1、审核组在审核结束后,应及时整理审核发现,编制审核报告。
关于质量、环境及职业健康安全三体系内部审核计划质量、环境以及职业健康安全(QES)是企业可持续发展的三个重要领域,为确保这些筑域的全面实施和有效管理,企业需定期进行内部审核.,本文将介绍•个三体系内部审核计划的详细内容.1.概述该内部审核计划的主要H的是评估企业质奴、环境及职业健康安全三体系的运行状况,发现存在的问题及潜在风险,并提出相应的改进措施,以确保体系的有效性和可持续性.2.范围该内部审核计划主要针对企业的质量管理体系、环境管理体系以及职业健康安全体系,其中包括以下方面:(1)旗量管理体系:包括腹量方针、质献目标、质量;手册、程序文件、I作指导书、记录表等.(2)环境管理体系:包括环境方针、环境目标、环境手册、程序文件、工作指导书、记录表等.(3)职业健康安全体系:包括职业健康安全方针、职业健康安全H标、职业健康安全手册'程序文件、工作指导书、记录表等.3.审核程序内部审核计划采用以下程序:(1)审核准备:包括制定审核方案、确定审核人员、审核范围、时间和地点等。
(2)市核执行:包括学习、r解、收集、审核并确认企业三体系运行情况。
(3)问咫识别:对审核过程中存在的问虺进行记录和报道,确定问题的严重性和紧急性.(4)发现亮点:审核人员可以在执行过程中记录并捕捉到有益的实践、科技等,进一步为企业的持续改进和发展提供指导。
(5)整改跟进:确定问题的整改员任人和整改措施、整改期限、目标等,并进行跟进和追踪.(6)审核报告:在审核过程结束后,审核人员需要写一份审核报告,详细表述问题、亮点及整改措施等。
4.审核周期体系内部审核计划需要定期进行,推荐一年一次,确保企业三体系的持续改进和优化。
5.评价指标审核人m应使用相应的评价指标,以确保企业三体系的有效性和可持续性.具体的评价指标包括:(1)质量管理体系:包括质量目标的达成情况、客户滴意度、生产率、缺陷率等.(2)环境管理体系:包括环境指标的达成情况、实施的环保措施、环保投入等。