维生素药物的理化性质及鉴别
- 格式:doc
- 大小:82.00 KB
- 文档页数:5

一、前言药物化学作为一门涉及化学、药学、生物学等多个学科领域的交叉学科,对于药物的研究、开发、生产和应用具有重要意义。
为了更好地了解药物化学的基本理论、实验技术和研究方法,我们进行了药物化学课题实训。
本次实训以“维生素类药物的理化性质”为主题,旨在掌握维生素类药物的理化性质、化学鉴别原理及基本操作。
二、实训目的1. 熟悉几种常用维生素类药物的理化性质及化学鉴别原理。
2. 学会应用典型药物的理化性质进行化学鉴别,熟悉其基本操作。
3. 培养团队协作精神和实验技能。
三、实训内容1. 实验材料(1)仪器:试管、药匙、滴管、烧杯、量筒、水浴锅等。
(2)药品:维生素B1、维生素B2。
2. 实验步骤(1)维生素B1的理化性质实验1)观察维生素B1的外观、溶解性等基本性质。
2)将维生素B1溶液滴入正丁醇中,观察是否呈现蓝色荧光。
3)向溶液中加入稀酸,观察荧光是否消失。
4)向溶液中加入稀碱,观察荧光是否重新显现。
5)将维生素B1溶液与氯化汞、碘、碘化汞钾试液反应,观察是否产生沉淀。
(2)维生素B2的理化性质实验1)观察维生素B2的外观、溶解性等基本性质。
2)将维生素B2溶液滴入水中,观察是否呈现黄绿色荧光。
3)向溶液中加入酸或碱,观察荧光是否消失。
4)将维生素B2溶液与连二亚硫酸钠反应,观察是否生成无荧光化合物。
(3)维生素B6的理化性质实验1)观察维生素B6的外观、溶解性等基本性质。
2)将维生素B6溶液与氯亚氨基-2,6-二氯醌试液反应,观察是否生成蓝色化合物。
3)将维生素B6溶液与硼酸反应,观察是否与氯亚氨基-2,6-二氯醌试液发生反应。
(4)维生素C的理化性质实验1)观察维生素C的外观、溶解性等基本性质。
2)将维生素C溶液与硝酸银试液反应,观察是否产生黑色沉淀。
3)将维生素C溶液与2,6-二氯靛酚钠试液反应,观察是否褪色。
四、实训结果与分析1. 维生素B1的理化性质实验结果表明,维生素B1在正丁醇中呈现蓝色荧光,加入稀酸后荧光消失,加入稀碱后荧光重新显现,与氯化汞、碘、碘化汞钾试液反应产生沉淀。

药物鉴别试验药物鉴别试验⼀、葡萄糖注射液(⼀)化学结构结构简式:CH2OH—CHOH—CHOH—CHOH—CHOH—CHO系统命名:(2R,3S,4R,5R)-2,3,4,5,6-五羟基⼰醛(⼆)理化性质1.⽆⾊结晶或⽩⾊结晶性或颗粒性粉末,⽆臭,味甜。
易溶于⽔,微溶于⼄醇。
熔点83℃,⽆结晶⽔熔点146℃。
(甜度:a-D-葡萄糖的⽐甜度为0.7,以蔗糖为基准物,凭味觉感官判断)2.旋光性:葡萄糖分⼦结构中有5个不对称碳原⼦,具有旋光性3.黏度:葡萄糖的黏度随着温度的升⾼⽽增⼤。
4.分⼦中的醛基,有还原性,易被氧化成葡萄糖酸5.醛基还能被还原为⼰六醇6.分⼦中有多个羟基,能与酸发⽣酯化反应7.葡萄糖在⽣物体内发⽣氧化反应,放出热量。
(三)鉴别⽅法1.⽐旋度:葡萄糖具有旋光性,为右旋体。
⽐旋度是旋光性物质的特征常数,具有鉴别意义。
D-葡萄糖在20摄⽒度光时的⽐旋光度数值为+52.2.2.化学⽅法(1)醛基鉴别(还原性)1)葡萄糖溶液与银氨溶液反应有银镜反应CH2OH(CHOH)4CHO+2[Ag(NH3)2OH](⽔浴加热)→CH2OH(CHOH)4COONH4+2Ag↓+3NH3↑+H2O2)在碱性溶液中可将铜离⼦还原成红⾊的氧化亚铜沉淀。
A.葡萄糖溶液与新制氢氧化铜悬浊液反应原理:氢氧化钠与硫酸铜反应⽣成氢氧化铜蓝⾊沉淀新制的氢氧化铜具有氧化性,与葡萄糖反应⽣成砖红⾊的氧化亚铜沉淀。
CH2OH(CHOH)4CHO+2Cu(OH)2---加热→CH2OH(CHOH)4COOH+Cu2O↓+2H2O B.与斐林试剂反应葡萄糖为可溶性还原糖,在加热的条件下,溶液的颜⾊变化过程为:浅蓝⾊—棕⾊—砖红⾊,能够⽣成砖红⾊的氧化亚铜沉淀。
C.将葡萄糖的鉴别⽅法修改为:取本品0.2g,加⽔5ml溶解后,加3ml碱性酒⽯酸铜试液,加热,即⽣成氧化亚铜的红⾊沉淀3)与溴⽔反应(与果糖区别)葡萄糖在酸性条件下能被溴⽔氧化⽽使溴⽔褪⾊。




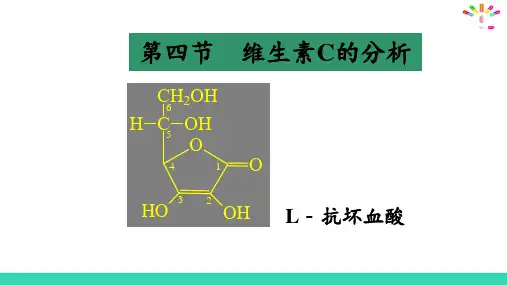
维生素 C维生素 C 又称抗坏血酸,是一种含有 6 个碳原子的酸性多羟基化合物,维生素C 虽然不含有羧基,仍具有有机酸的性质。
天然存在维生素 C 有L 与D 两种异构体,后者无生物活性。
一、理化性质与体内分布维生素 C 有 3 型,氧化时形成仍具有生物活性的脱氢型维生素C。
脱氢型维生素C 进一步氧化或水解,为二酮古洛糖酸,丧失了维生素 C 的活性。
维生素C 呈无色无臭的片状结晶体,易溶于水。
在酸性环境中稳定,遇空气中氧、热、光、碱性物质,特别是有氧化酶及痕量铜、铁等金属离子存在时,可促进其氧化破坏。
氧化酶一般在蔬菜中含量较多,特别是黄瓜和白菜类,但在柑橘类含量较少。
蔬菜在储存过程中维生素 C 都有不同程度损失。
但在某些植物中,特别是枣、刺梨等水果中含有生物类黄酮,能保护食物中维生素 C 的稳定性。
正常摄入量情况下,体内可贮存维生素C1.2~2.0g,最大贮量为3g。
浓度最高的组织是垂体、肾上腺、眼晶状体、血小板和白细胞,但是贮存量最多的是骨骼肌(3~4mg/100g 湿组织)、脑(13~15 mg/100g 湿组织)和肝脏(10~16rag/100g 湿组织)。
在血浆中,维生素C 主要以还原型形式存在,还原型与脱氢型比约为15:1,故测定还原型维生素 C 即可了解血中维生素 C 的水平。
二、生理功能与缺乏(一)生理功能维生素 C 是一种较强的还原剂,可使细胞色素C、细胞色素氧化酶及分子氧还原,与一些金属离子螯合。
虽然它不是辅酶,但可以增加某些金属酶的活性,如脯氨酸羟化酶(Fe2+)、尿黑酸氧化酶(Fe2+)、三甲赖氨酸羟化酶(Fe2+)、对.羟苯丙酮酸羟化酶(Cu+)、多巴胺-β-羟化酶(Cu+)等。
这些金属离子位于酶的活性中心,维生素 C 可维持其还原状态,从而借以发挥生理功能。
1.参与羟化反应羟化反应是体内许多重要物质合成或分解的必要步骤,如胶原和神经递质的合成,各种有机药物或毒物的转化等,都需要通过羟化作用才能完成。

药物分析练习题B 答案一、名词解释1.精密称定:指称取重量应准确至所取重量的千分之一。
2.标准品系指用于生物检定,抗生素或生化药品中含量或效价测定的标准物质,按效价单位(或ug)计,以国际标准品进行标定。
3.一般鉴别试验:一般鉴别试验是依据某一类药物的化学结构或理化性质的特征,通过化学反应来鉴别药物的真伪。
4.定量限:指样品中被测物能被定量测定的最低量,其测定结果应具有一定的准确度和精密度。
5.特殊杂质:指在特定药物的生产和贮藏过程中引入的杂质。
二、填空题1.药典中规定的杂质检查项目,是指该药品在生产和贮藏中可能含有并需要控制的杂质。
2.古蔡氏检砷法的原理为金属锌与酸作用产生H2 ,与药物中微量砷盐反应生成具挥发性的AsH3 ,遇溴化汞试纸,产生黄色至棕色的砷斑,与一定量标准砷溶液产生的砷斑比较,判断药物中砷盐的含量。
3.巴比妥类药物的母核为1,3-二酰亚胺结构,为环状的丙二酰脲结构。
巴比妥类药物常为白色结晶或结晶性粉末,环状结构与碱共热时,可发生水解开环。
巴比妥类药物本身不溶于水,易溶于乙醇等有机溶剂,其钠盐易溶于水而不溶于有机溶剂。
4.对乙酰氨基酚含有酚羟基,与三氯化铁发生呈色反应,可与利多卡因和醋氨苯砜区别。
5.铈量法测定氯丙嗪含量时,当氯丙嗪失去1 个电子显红色,失去2 个电子红色消褪。
6.绿奎宁反应为喹啉类衍生物的特征反应,在酸性水溶液中,滴加微过量的溴水或氯水,再加入过量的氨水,应显绿色。
7.甾体激素类药物分子结构中存在�6�2 1,3 -4-酮基和苯环共轭系统,在紫外光区有特征吸收。
8.链霉素的结构是由一分子链霉胍和一分子链霉双糖胺结合而成的碱性苷。
9.四环素类抗生素在酸性溶液中会发生差向异构化,当pH 小于2 或pH 大于6 时差向异构化速度减小。
10.中国药典的主要内容由凡例、正文、附录和索引四部分组成。
三、选择题1.杂质限量是指药物中所含杂质的最大允许量2.药物的中金属检查中(第一法),溶液的酸碱度通常是弱酸性3.药物氯化物检查中所用的酸是稀硝酸4.药物杂质限量检查的结果是1.0ppm,表示药物所含杂质的重量是药物本身重量的百万分之一5.药物中氯化物检查的意义可以考核生产工艺是否正常和反映药物的纯度水平6.砷盐检查中,为了除去供试品中可能含有的微量硫化物的影响,在导气管中需填装蘸有下列溶液的药棉醋酸铅7.微孔滤膜法是用来检查重金属8.古蔡法检查砷盐中Zn和HCl的作用是D.生成新生台H2↑9.干燥失重主要是检查药物中A.水分及其他挥发性成分10.检查维生素C中重金属:取样2.0g,规定含重金属不得过百万分之十,应吸取标准铅溶液(每1ml=0.01mg的Pb)多少ml C. 2.0ml11.两步滴定法测定阿司匹林的含量时,每1ml氢氧化钠溶液(0.1mol/L)相当于阿司匹林(分子量=180.16)的量是E.18.02mg12.阿司匹林片剂的含量测定采用两步滴定法是因为A.片剂中有酸性稳定剂和分解产物13.阿司匹林的酸碱滴定中,要求采用中性乙醇做溶剂,所谓“中性”是指A.对所用指示剂显中性14.盐酸丁卡因与硝酸作用形成B.N-亚硝基化合物15.药物分子中具有下列哪一基团才能在酸性溶液中直接用亚硝酸钠液滴定C.芳伯氨基16.不能直接与三氯化铁试液反应的药物是D阿司匹林17.苯巴比妥在吡啶溶液中与铜离子作用,生成的络合物颜色为 B.紫色18.哪个药物与吡啶—硫酸酮作用,生成绿色配位化合物E.硫喷妥钠19.银量法测定苯巴比妥的含量,现版中国药典采用什么方法指示终点 E电位滴定法20.能使碘试液褪色的药物是B司可巴比妥四、简答题1.简述维生素C 的主要化学性质。
维生素药物的理化性质及鉴别
维生素:生物的生长和代谢所必需的微量有机物。
分为脂溶性维生素和水溶性维生素两类。
前者包括维生素A、维生素D、维生素E、维生素K等,后者有B族维生素和维生素C。
维生素A
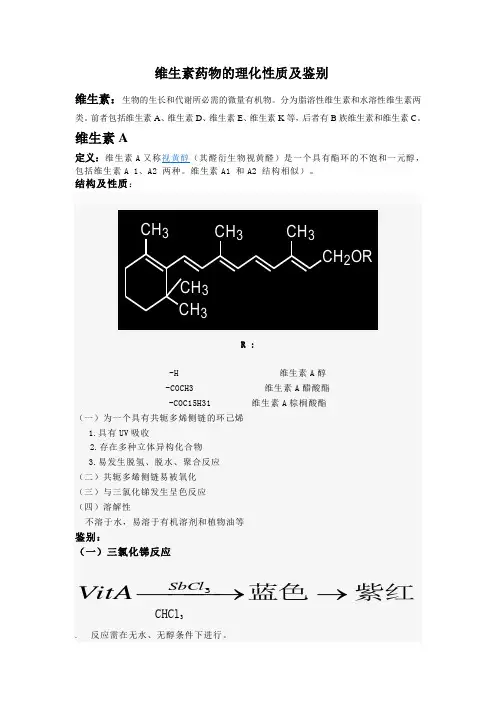
定义:维生素A又称视黄醇(其醛衍生物视黄醛)是一个具有酯环的不饱和一元醇,包括维生素A 1、A2 两种。
维生素A1 和A2 结构相似)。
结构及性质:
VitA
(2)与2,6 - 二氯靛酚反应
(3)与碱性酒石酸铜反应
(4)与KMnO4反应
(银镜)
黑↓−−→−Ag AgNO VitC 3
酚亚胺
二氯靛酚,−−→−-VitC
62红
碱性酒石酸铜↓−−→−O Cu VitC
2+
−−→−24
Mn
KMnO
VitC
2、糖类的反应
3、紫外分光光度法。

《生物产品分析与检验技术》课程单元教学设计卡二、教学内容相关知识第一节维生素概述1.定义:维生素是维持人体正常生理机能所必需的生物活性物质。
2.维生素对人体的意义根据日常生活以举例为主3.维生素类物质的分类(按其溶解性质分)脂溶性维生素:主要有A、D、E、K等水溶性维生素:主要有B族(B1、B2、B12等)、维生素C、烟酸、叶酸、泛酸、抗坏血酸等。
4.维生素测定方法化学分析法、比色法、分光光度法(紫外和荧光)、层析法、色谱法(气相色谱和高效液相色谱)和微生物法等。
第二节维生素B2的特征及分析测定1.维生素B2的化学结构维生素B又称核黄素,分子式为C17H20N4O6,维生素B2的结构是由D-核醇和7,28-二甲基异咯嗪组成,以D-核醇的C1上醇基与异咯嗪上N相连。
2.维生素B2的性质微溶于水,在中性或酸性溶液中加热是稳定的,为体内黄酶类辅基维生素B2的组成部分(黄酶在生物氧化还原中发挥递氢作用)。
当缺乏时,会影响机体的生物氧化,使代谢发生障碍,导致口腔、唇、皮肤、生殖器的炎症和机能障碍,如口角炎、唇炎、舌炎、口腔溃疡、眼结膜炎和阴囊炎等,故本品可用于上述疾病的防治。
体内维生素B2的储存是很有限的,因此每天都要由饮食提供。
B2在食品中以游离形式或磷酸酯等结合形式存在。
膳食中主要来源于各种动物性食品,其中以肝、肾、心、蛋、奶含量最多,其次是植物性食品的豆类和新鲜叶菜类。
主要性质有:2.1紫外吸收:维生素B2的最大吸收波长在267nm、375nm与444nm处。
2.2不稳定性:维生素B2对光线极不稳定,易分解为感光黄素(光化黄)。
2.3旋光性:维生素B2在碱液中呈左旋性。
2.4酸碱两性:维生素B2为两性化合物,可溶于酸和碱。
其水溶液为非解离型,呈黄绿色荧光。
荧光在pH 6~7时最强,在酸或碱中解离,荧光即消失。
3.测定方法维生素B的分析方法主要有荧光法、微生物法、紫外分光光度法、高效液2相色谱法。
(1)荧光反应(荧光法)核黄素在440-500nm波长照射下发生黄绿色荧光,在稀溶液中,荧光强度与核黄素浓度成正比。
葡萄糖结构:葡萄糖含五个羟基,一个醛基理化性质:1.旋光性D-葡萄糖在20摄氏度光时的比旋光度数值为+52.2.2.溶解度在20摄氏度时单一的葡萄糖溶液最高浓度为50%。
3.甜度: a-D-葡萄糖的比甜度为0.7.4.黏度: 葡萄糖的黏度随着温度的升高而增大。
5.还原性: 分子中的醛基,有还原性6 .醛基还能被还原为己六醇7. 分子中有多个羟基,能与酸发生酯化反应鉴别1. (1)分子中的醛基,有还原性,能与银氨溶液反应:CH2OH(CHOH)4CHO+2Ag(NH3)2OH→ CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O ,被氧化成葡萄糖酸注意事项:(1)试管内壁必须洁净(2)银氨溶液随用随配不可久置(3)水浴加热,不可用酒精灯直接加热(4)乙醛用量不宜太多,一般加3滴(5)银镜可用稀HNO3浸泡洗涤除去加热还原生成的银附着在试管壁上,形成银镜,所以,这个反应也叫银镜反应。
2. 葡萄糖溶液与新制氢氧化铜悬浊液反应生成砖红色沉淀(浓度高时生成黄色沉淀)CH2OH(CHOH)4CHO+2Cu(OH)2---加热→CH2OH(CHOH)4COOH+Cu2O↓+2H2O注意事项:(1)新制2Cu(OH)2悬浊液要随用随配、不可久置(2)配制新制Cu(OH)2悬浊液时,所用NaOH溶液必须过量(3)反应液必须直接加热至沸腾(4)葡萄糖分子中虽然含有醛基,但是d-葡萄糖中不含有醛基。
阿司匹林肠溶片结构理化性质:1: 阿司匹林为白色结晶或结晶性粉末,无味或微带醋酸臭,微溶于水,易溶于乙醇、氯仿,微溶于乙醚。
2: 酸性阿司匹林结构中含有羧基3: 水解性结构中含有酯基,因而它又可以在无机酸或碱的催化并微热(水浴)条件下,水解生成水杨酸和乙酸鉴别1:三氯化铁反应水杨酸及其盐在中性或弱酸条件下,与三氯化铁试液反应, 分子中的酯键受热水解,显紫堇色。
这是部分本品水解成水杨酸,三价铁离子与水杨酸的酚羟基结合所致。
维生素B1、磺胺嘧啶、苯巴比妥的鉴别实验报告林冠(浙江大学药学院药学2班 杭州 3031901051)一、 实验目的1、学习并掌握鉴别维生素B1、磺胺嘧啶、苯巴比妥的方法;2、掌握并理解药物鉴别是实验对专属性、灵敏性的要求。
二、 实验设计思路我本次自主实验的课题是通过查阅相关书籍文献,获得三个药物的结构与理化性质等有关内容,设计出区别、鉴定各个药物的不同方案,并根据实验室条件选做其中一个方案。
实验首先需对三种药物进行一般鉴别,区分出三种药物后,再选用专属性较强的反应对三种药物进行专属鉴别,以确证其结构。
通过查阅2000版药典及其它一些资料,获得了三个药物结构及理化性质等有关资料。
苯巴比妥结构如下:分子式:C12H12N2O3;分子量:232.24;理化性质:本品为酸性化合物,在水中极微溶解,能溶于氢氧化钠水溶液;苯环能与硫酸-亚硝酸反应生成橙黄色产物。
磺胺嘧啶结构如下:分子式:C 10H 10N 4O 2S ;分子量:250.28;理化性质:本品为白色或类白色的结晶或粉末;无臭,无味;遇光色渐变暗。
为两性化合物,在水中几乎不溶;在氢氧化钠试液或氨试液中易溶,在稀盐酸中溶解。
维生素B1结构如下:分子式:C 12H 17ClN 4OS.HCl;分子量:337.27;理化性质:本品为白色结晶性粉末;有微弱的特臭,味苦。
有两个碱性基团,具碱性有紫外吸收,为噻唑{翁}盐酸盐 ,在水中易溶。
硫色素反应为其专属反应。
通过对有关资料的搜集,我发现磺胺嘧啶与维生素B1在一定条件下都能与硝酸银反应,且现象有所不同:1、维生素B1与硝酸银反应是由于本品为氯化物,能显氯化物反应:将本品溶于水中,硝酸使成酸性后,加硝酸银试液,即生成白色凝乳状沉淀;分离,沉淀加氨试液即溶解,再加硝酸,沉淀复生成。
2、由于磺胺嘧啶的磺酰氨具酸性,在加入氨试液能与硝酸银反应生成磺胺嘧啶银沉淀,且磺胺嘧啶银溶于硝酸,即加入硝酸溶解,生成磺胺嘧啶银的反应式如下:NH 3.H 2OH 2O++SO 2NN NNH 2SO 2NN N NH 4NH 2NH 2SO 2NN N NH 2SO 2NNN NH 2SO 2NZn N N3、而苯巴比妥理论上不会与硝酸银反应。
维生素药物的理化性质及鉴别
维生素:生物的生长和代谢所必需的微量有机物。
分为脂溶性维生素和水溶性维生素两类。
前者包括维生素A、维生素D、维生素E、维生素K等,后者有B族维生素和维生素C。
维生素A
定义:维生素A又称视黄醇(其醛衍生物视黄醛)是一个具有酯环的不饱和一元醇,包括维生素A 1、A2 两种。
维生素A1 和A2 结构相似)。
结构及性质:
VitA
(2)与2,6 - 二氯靛酚反应
(3)与碱性酒石酸铜反应
(4)与KMnO4反应
(银镜)
黑↓−−→−Ag AgNO VitC 3
酚亚胺
二氯靛酚,−−→−-VitC
62红
碱性酒石酸铜↓−−→−O Cu VitC
2+
−−→−24
Mn
KMnO
VitC
2、糖类的反应
3、紫外分光光度法。