选修三+第三节+晶体结构与性质(共52张PPT)
- 格式:ppt
- 大小:992.00 KB
- 文档页数:40

晶体结构与性质学什么?1.了解分子晶体和原子晶体的概念和特征,能以典型的物质为例描述分子晶体的结构与性质的关系。
2.知道金属键的含义,能列举金属晶体的四种基本堆积模型。
3.能说明离子的形成,了解晶格能的应用。
4.知道分子晶体、原子晶体、离子晶体的结构粒子,粒子间作用力的区别。
高考在本节中的考点是:①晶体常识;②分子晶体与原子晶体;③金属晶体;④离子晶体。
注意:1.晶体与非晶体的区别,晶体中粒子的空间堆积方式,晶胞的结构特点及其应用。
2.晶胞中粒子个数及边长等的计算。
3.晶体类型与性质之间的关系。
4.晶体类型与粒子间作用力的关系。
5.四类晶体的特征及代表物质。
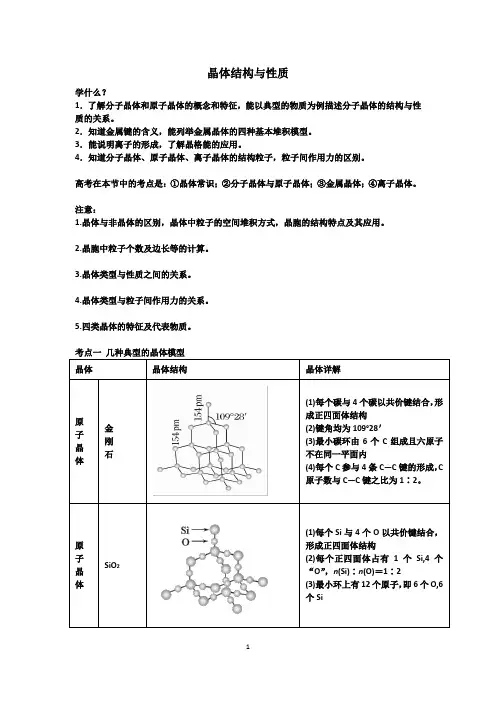
考点一几种典型的晶体模型(1)成正四面体结构(2)(3)不在同一平面内(4)原子数与(1)形成正四面体结构(2)“(3)个(1)8面心又各占据(2)分子有(1)Cl且紧邻的(2)(1)8的(2)个Cs简单立方典型代表数为体心立方典型代表配位数为六方最密典型代表74%面心立方典型代表74%(1)石墨晶体是特殊的晶体,是层状结构,同层内碳原子以共价键形成正六边形平面网状结构,层与层之间以分子间作用力结合。
所以石墨晶体熔、沸点很高,但硬度不大,有滑腻感,能导电。
(2)金刚石和石墨是同素异形体,碳的同素异形体还有碳原子簇,如C60、C100、C200等,这些碳原子簇是分子晶体。
例1 如图表示一些晶体中的某些结构,它们分别是NaCl、CsCl、干冰、金刚石、石墨晶体结构中的某一种的某一部分。
(1)其中代表金刚石的是(填编号字母,下同)________,其中每个碳原子与________个碳原子最接近且距离相等。
金刚石属于________晶体。
(2)其中代表石墨的是________,其中每个正六边形占有碳原子数平均为________个。
(3)其中代表NaCl晶体的是________,每个Na+周围与它最接近且距离相等的Na+有________个。
(4)代表CsCl晶体的是________,它属于________晶体,每个Cs+与________个Cl-紧邻。