工业纯碱中碳酸钠含量的测定
- 格式:doc
- 大小:56.50 KB
- 文档页数:4

纯碱质量执行标准
纯碱,也称为碳酸钠,其质量执行标准会因用途、级别、质量指标等因素有所不同。
在中国,纯碱的执行标准主要由国家标准进行规定。
对于工业纯碱,执行的标准是GB/T 2102-2004《工业碳酸钠及其试验方法》。
这个标准根据优等品和一等品的等级划分,规定了不同等级纯碱的质量指标,包括氯化物、硫酸盐、铁含量、水不溶物等。
对于食用纯碱,执行的标准是GB 1886-2008《食品安全国家标准食品添加剂碳酸钠》。
这个标准规定了食用纯碱的质量和安全要求,以保障人们的食品安全。
另外,国家标准中对纯碱等级还分为优级、一级、合格三种。
其中优级品要求纯碱碳酸钠含量≥92%(干基)、铁≤0.0035%、纯碱盐份≤0.7%、纯碱水不溶物≤0.03%、硫酸盐含量≤0.03%,同时对外观也有一定要求,如轻质纯碱为白色粉末,重质纯碱为白色细小颗粒。
请注意,这些标准可能会随着技术进步和市场需求的变化进行更新和修订。
因此,在实际应用中,应参考最新的标准以确保纯碱的质量和安全。
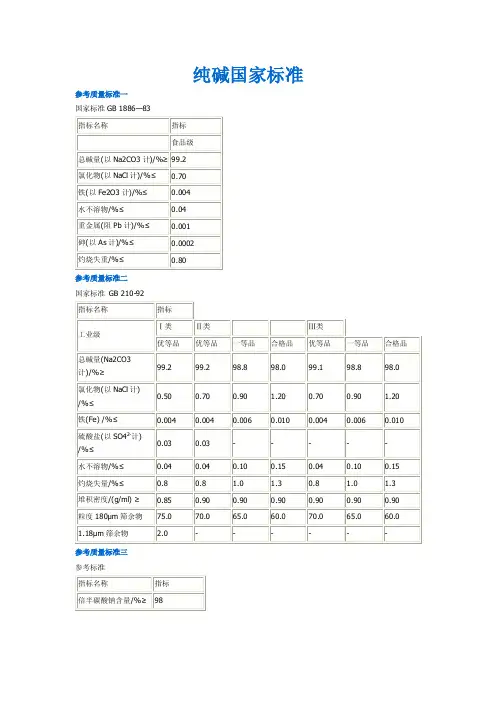
纯碱国家标准参考质量标准一国家标准GB 1886—83参考质量标准二国家标准GB 210-92参考质量标准三参考标准中华人民共和国国家标准中华人民共和国国家标准GB 1886-92食品添加剂碳酸钠代替GB 1886-83Food additive Sodium carbonate GB 8920-88━━━━━━━━━━━━━━━━━━━━━━━━━━━━━━━━━━━━━━━1 主题内容与适用范围本标准规定了食品添加剂碳酸钠的技术要求、试验方法、检验规则以及标志、包装、运输和贮存。
本标准适用于以工业盐为原料,由氨碱法和联碱法制得的食品添加剂碳酸钠。
分子式:Na2CO3相对分子质量:105.99(按1989年国际相对原子质量)2 引用标准GB 601 化学试剂滴定分析(容量分析)用标准溶液的制备GB 602 化学试剂杂质测定用标准溶液的制备GB 603 化学试剂试验方法中所用制剂及制品的制备GB 3049 化工产品中铁含量测定的通用方法邻菲(口罗)啉分光光度法GB 3050 无机化工产品中氯化物含量测定的通用方法电位滴定法GB 3051 无机化工产品中氯化物含量测定的通用方法汞量法GB 4456 包装用聚乙烯吹塑薄膜GB 4857.3 运输包装件基本试验堆码试验方法GB 4857.5 运输包装件基本试验垂直冲击跌落试验方法GB 6678 化工产品采样总则GB 6682 实验室用水规格GB 8450 食品添加剂中砷的测定方法砷斑法GB 8946 塑料编织袋GB 8947 复合塑料编织袋3 技术要求3.1 外观:白色粉状结晶。
3.2 食品添加剂碳酸钠应符合下表要求。
━━━━━━━━━━━━━━━━━━━┳━━━━━━━━━━━━━━━━━━项目┃指标━━━━━━━━━━━━━━━━━━━╋━━━━━━━━━━━━━━━━━━总碱量(以Na2CO3计),%≥ ┃99.2━━━━━━━━━━━━━━━━━━━╋━━━━━━━━━━━━━━━━━━氯化物(以NaCl计)含量,%≤ ┃0.70━━━━━━━━━━━━━━━━━━━╋━━━━━━━━━━━━━━━━━━铁(以Fe计)含量,%≤ ┃0.0040━━━━━━━━━━━━━━━━━━━╋━━━━━━━━━━━━━━━━━━重金属(以Pb计)含量,%≤ ┃0.001━━━━━━━━━━━━━━━━━━━╋━━━━━━━━━━━━━━━━━━砷(以As计)含量,%≤ ┃0.0002━━━━━━━━━━━━━━━━━━━╋━━━━━━━━━━━━━━━━━━烧失量*1),%≤ ┃0.80━━━━━━━━━━━━━━━━━━━╋━━━━━━━━━━━━━━━━━━水不溶物含量,%≤ ┃0.040━━━━━━━━━━━━━━━━━━━┻━━━━━━━━━━━━━━━━━━注:1)为包装时检验结果。

工业纯碱总碱度的测定实验报告实验目的,通过本实验,掌握工业纯碱总碱度的测定方法,了解工业纯碱的质量指标。
实验原理,工业纯碱是碳酸钠的一种,其主要成分为Na2CO3。
在水溶液中,碳酸钠会与酸反应生成盐和水,反应的化学方程式为Na2CO3 + 2HCl → 2NaCl + H2O + CO2↑。
根据反应方程式,可以利用酸碱中和滴定的方法来测定工业纯碱的总碱度。
实验仪器,滴定管、容量瓶、分析天平、PH计、酸度计、试剂瓶等。
实验步骤:1.称取一定质量的工业纯碱样品,溶解于一定体积的去离子水中,得到一定浓度的碱液。
2.取一定体积的碱液,加入几滴酚酞指示剂,使其呈现粉红色。
3.用标定好的盐酸溶液滴定碱液,直至粉红色消失,记录所耗盐酸的体积V1。
4.再加入几滴甲基橙指示剂,使其呈现橙色。
5.继续滴定碱液,直至橙色变为黄色,记录所耗盐酸的体积V2。
实验数据处理:1.根据滴定结果,计算碱液的总碱度。
总碱度=(V1-V2)×标定盐酸的浓度。
2.根据总碱度的测定值,判断工业纯碱的质量是否符合标准。
实验注意事项:1.实验操作中,应注意控制滴定速度,避免出现误差。
2.实验中使用的试剂瓶、容量瓶等玻璃器皿应清洗干净,避免杂质对实验结果的影响。
3.实验结束后,应将实验器材清洗干净,保持实验台面整洁。
结论,通过本次实验,成功测定了工业纯碱的总碱度,并根据测定结果判断了工业纯碱的质量。
实验结果表明,本次工业纯碱样品的总碱度符合标准要求,达到了工业生产的要求。
参考文献:1.《化学实验技术与方法》,XXX,XXX出版社,200X年。
2.《工业纯碱质量标准》,XXX标准出版社,200X年。
本实验报告由XXX编写,仅供参考。
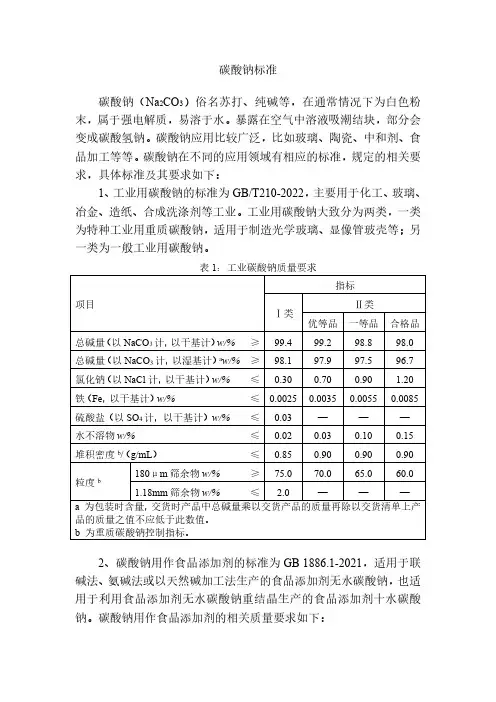
碳酸钠标准碳酸钠(Na2CO3)俗名苏打、纯碱等,在通常情况下为白色粉末,属于强电解质,易溶于水。
暴露在空气中溶液吸潮结块,部分会变成碳酸氢钠。
碳酸钠应用比较广泛,比如玻璃、陶瓷、中和剂、食品加工等等。
碳酸钠在不同的应用领域有相应的标准,规定的相关要求,具体标准及其要求如下:1、工业用碳酸钠的标准为GB/T210-2022,主要用于化工、玻璃、冶金、造纸、合成洗涤剂等工业。
工业用碳酸钠大致分为两类,一类为特种工业用重质碳酸钠,适用于制造光学玻璃、显像管玻壳等;另一类为一般工业用碳酸钠。
表1:工业碳酸钠质量要求项目指标Ⅰ类Ⅱ类优等品一等品合格品总碱量(以NaCO3计,以干基计)w/%≥99.499.298.898.0总碱量(以NaCO3计,以湿基计)a w/%≥98.197.997.596.7氯化钠(以NaCl计,以干基计)w/%≤0.300.700.90 1.20铁(Fe,以干基计)w/%≤0.00250.00350.00550.0085硫酸盐(以SO4计,以干基计)w/%≤0.03———水不溶物w/%≤0.020.030.100.15堆积密度b/(g/mL)≤0.850.900.900.90粒度b 180μm筛余物w/%≥75.070.065.060.0 1.18mm筛余物w/%≤ 2.0———a为包装时含量,交货时产品中总碱量乘以交货产品的质量再除以交货清单上产品的质量之值不应低于此数值。
b为重质碳酸钠控制指标。
2、碳酸钠用作食品添加剂的标准为GB1886.1-2021,适用于联碱法、氨碱法或以天然碱加工法生产的食品添加剂无水碳酸钠,也适用于利用食品添加剂无水碳酸钠重结晶生产的食品添加剂十水碳酸钠。
碳酸钠用作食品添加剂的相关质量要求如下:表2食品添加剂碳酸钠的感官要求项目要求色泽无色或白色状态晶粒、粒状或粉状表3食品添加剂碳酸钠的理化指标项目指标总碱量(以NaCO3计,以干基计)w/%≥99.2总碱量(以NaCO3计,以湿基计)w/%无水碳酸钠≥97.9十水碳酸钠≥36.2水不溶物(以干基计)w/%≤0.03氯化物(以NaCl计)(以干基计)w/%≤0.70铁(Fe)(以干基计)/(mg/kg)≤35.0铅(Pb)(以干基计)/(mg/kg)≤ 2.0铁(As)(以干基计)/(mg/kg)≤ 2.03、碳酸钠用作化学试剂的标准为GB/T639-2008,作为化学试剂的碳酸钠分为优级纯、分析纯和化学纯试剂。

3.工业纯碱总碱度的测定。
工业纯碱是一种重要的化工原料,其总碱度是衡量产品质量的重要指标。
总碱度是指纯碱中碳酸钠的含量,它对于纯碱的生产和使用具有重要意义。
本文将介绍工业纯碱总碱度的测定方法,包括实验原理、实验步骤和数据处理等方面。
一、实验原理总碱度是指纯碱中碳酸钠的含量,它可以通过滴定法进行测定。
在滴定法中,将纯碱溶解于水,然后加入酚酞指示剂,再滴加盐酸标准溶液,直到溶液颜色变化,从而确定纯碱中碳酸钠的含量。
由于在滴定过程中要使用标准溶液,因此需要对其进行标定。
二、实验步骤1.准备试剂和仪器试剂:纯碱、蒸馏水、酚酞指示剂、标准溶液(盐酸)仪器:滴定管、容量瓶、三角瓶、电子天平、称量纸、烧杯2.称量样品用电子天平称取约5g纯碱样品,记录其质量m1。
3.溶解样品将称好的纯碱样品溶解于蒸馏水中,得到溶液。
4.加入指示剂向溶液中加入适量酚酞指示剂。
5.滴定操作用标准溶液滴定溶液,直到溶液颜色发生变化。
记录滴定管的初始体积V1和终点时的体积V2。
6.数据记录记录实验过程中的各项数据,包括称量样品的质量m1、滴定管的初始体积V1、终点时的体积V2等。
三、数据处理1.计算纯碱中碳酸钠的含量按下式计算:Na2CO3=(V1-V2) × c × 0.053 × 100/m1式中:V1为滴定管的初始体积(mL);V2为终点时的体积(mL);c 为标准溶液的浓度(mol/L);m1为称量的样品质量(g);0.053为碳酸钠的摩尔质量(g/mol)。
2.计算总碱度根据纯碱中碳酸钠的含量,按下式计算总碱度:Total alkalinity=Na2CO3 × 100/Na2CO3 × 100%式中:Na2CO3为计算得到的碳酸钠含量(%)。
四、结果分析通过上述实验步骤和数据处理,我们可以得到工业纯碱的总碱度。
总碱度反映了纯碱中碳酸钠的含量,含量越高,说明纯碱的质量越好。
在生产过程中,总碱度控制的不准确会影响产品质量和生产效益。

纯碱中碳酸钠和碳酸氢钠含量测定计算公式碳酸钠和碳酸氢钠是纯碱中的两个主要组分。
测定这两种化合物的含量可以采用酸碱滴定的方法。
下面我将为您详细介绍这个计算公式。
首先,我们需要了解一些基本概念和步骤。
酸碱滴定是一种通过反应的等量点来测定溶液中其中一种化学物质的含量的方法。
在纯碱的测定中,我们使用酸溶液来滴定纯碱的溶液,常用的酸溶液有盐酸和硫酸。
下面是计算纯碱中碳酸钠和碳酸氢钠含量的步骤:1.准备酸溶液准备相应浓度的盐酸或硫酸标准溶液。
这个溶液用来滴定纯碱的溶液,并且需要使用酚酞作为指示剂来标志滴定终点。
2.确定滴定号数用酚酞溶液滴在酸溶液上,记录下溶液变颜色的体积。
这个滴定号数将用于计算试样中碳酸钠和碳酸氢钠的含量。
3.准备样品取一定量的纯碱样品(例如0.1g),溶解在适量的水中。
添加几滴酚酞指示剂到样品中。
4.滴定将酸溶液慢慢滴入样品中,观察溶液的颜色变化。
初始时溶液是红色的,当酸中和完全后溶液变为无色或淡粉红色。
5.记录滴定体积记录滴定时酸溶液的滴定体积(ml)。
这个体积将用于计算样品中碳酸钠和碳酸氢钠的含量。
接下来,我们来计算纯碱中碳酸钠和碳酸氢钠的含量。
碳酸钠(Na2CO3)的含量计算公式:Na2CO3(g/L)=(酸溶液滴定体积-滴定号数)×0.106碳酸氢钠(NaHCO3)的含量计算公式:NaHCO3(g/L)=(酸溶液滴定体积-滴定号数)×0.084其中,酸溶液滴定体积是指滴定过程中酸溶液的体积(ml),滴定号数是指滴定中标志酸溶液变色的体积(ml)。
通过以上的计算公式,我们可以得出纯碱样品中碳酸钠和碳酸氢钠的含量。
这个方法在实验室中被广泛使用,能够准确测定纯碱样品中这两种化合物的含量。
需要注意的是,这个计算公式是基于滴定方法的前提下得出的。
在实际操作中,还需要注意保证反应的完全性,以及正确使用酸碱滴定的方法和技巧。
这样才能得出准确可靠的结果。

纯碱中碳酸钠和碳酸氢钠含量测定注意事项1.样品的选择和制备样品应当代表性,避免混杂其他杂质。
通常可以选择样品中心位置的碳酸钠和碳酸氢钠相对含量较高的部分作为测定样品。
样品的制备要求样品粒度均匀,一般将样品研磨成符合要求的粒度。
2.试剂的选择与质量试剂应选择纯度高、稳定性好的试剂。
例如,用于测定碳酸钠含量的酸可选择精密滴定所需的浓度为0.05mol/L的盐酸,而用于测定碳酸氢钠含量的酸可选择精密滴定所需的浓度为0.1mol/L的硫酸。
3.仪器设备的校准与准备使用滴定管进行试剂滴定时,应先将滴定管进行清洗和校准。
在大气中进行滴定时,可能会发生滴定管内的气泡困扰,因此,可以在滴定之前先在滴定管中注入一定量的溶液,用以防止滴定过程中气泡的困扰。
4.滴定的操作要点滴定时应注意溶液滴定的速度和搅拌的均匀度。
通常的滴定速度为每滴1~2秒,滴定过程中需要充分搅拌样品和试剂,以确保反应完全进行。
5.滴定终点的判定碳酸钠和碳酸氢钠的滴定终点通常使用酸碱指示剂来判断。
碳酸钠滴定时常选择甲基橙作为指示剂,滴定终点为由粉红色变为橙黄色;碳酸氢钠滴定时常选择溴甲酚绿作为指示剂,滴定终点为由黄绿色变为湛蓝色。
6.数据处理与结果分析在滴定实验中,应进行多次重复测定,计算平均值,并计算其相对标准偏差,以确保数据的可靠性。
根据滴定实验的结果,可以计算出碳酸钠和碳酸氢钠的含量。
总结起来,纯碱中碳酸钠和碳酸氢钠含量测定需要注意样品的选择和制备、试剂的选择与质量、仪器设备的校准与准备、滴定的操作要点、滴定终点的判定以及数据处理与结果分析等几个方面。
只有在严格控制这些注意事项的前提下,才能得到准确可靠的测定结果。

工业纯碱总碱度的测定实验报告一、实验目的。
本实验旨在通过实验方法测定工业纯碱的总碱度,掌握测定工业纯碱总碱度的实验技术,提高化学实验操作能力。
二、实验原理。
工业纯碱是一种重要的化工原料,在工业生产中应用广泛。
其总碱度是指单位质量工业纯碱中所含的氢氧化钠和碳酸钠的总量。
本实验将利用酸碱中和反应,通过酸碱滴定的方法,以盐酸为滴定液,甲基橙为指示剂,测定工业纯碱中氢氧化钠和碳酸钠的总量。
三、实验仪器与药品。
1. 50ml滴定瓶。
2. 10ml量筒。
3. 分析天平。
4. 烧杯。
5. 玻璃棒。
6. 精密pH试纸。
7. 盐酸。
8. 甲基橙指示剂。
9. 工业纯碱样品。
四、实验步骤。
1. 取一定质量的工业纯碱样品,溶解于适量蒸馏水中,转移至50ml滴定瓶中,加入几滴甲基橙指示剂。
2. 用盐酸标准溶液滴定至溶液由红色变为黄色,记录滴定消耗的盐酸体积V1。
3. 另取一定质量的工业纯碱样品,溶解于适量蒸馏水中,转移至50ml滴定瓶中,加入几滴甲基橙指示剂。
4. 用盐酸标准溶液滴定至溶液由红色变为黄色,记录滴定消耗的盐酸体积V2。
5. 计算工业纯碱的总碱度,按照下式计算,总碱度(%)=(V1-V2)×N×M/ m。
其中,V1为第一次滴定消耗的盐酸体积(ml),V2为第二次滴定消耗的盐酸体积(ml),N为盐酸的摩尔浓度(mol/L),M为盐酸的摩尔质量(g/mol),m为取样质量(g)。
五、实验数据与结果。
利用上述实验步骤测得实验数据如下:样品质量m = 0.5g。
第一次滴定消耗的盐酸体积V1 = 12.5ml。
第二次滴定消耗的盐酸体积V2 = 24.3ml。
盐酸的摩尔浓度N = 0.1mol/L。
盐酸的摩尔质量M = 36.46g/mol。
根据实验数据,计算得出工业纯碱的总碱度为,总碱度(%)=(12.5-24.3)×0.1×36.46/ 0.5 = 21.8%。
六、实验总结。
通过本次实验,我们成功测定了工业纯碱的总碱度,并掌握了测定工业纯碱总碱度的实验技术。

工业用氢氧化钠国标(实用版)目录1.氢氧化钠的概述2.工业用氢氧化钠国家标准的意义3.工业用氢氧化钠的主要产品4.工业用氢氧化钠中氢氧化钠和碳酸钠含量的测定方法5.工业用氢氧化钠的价格正文氢氧化钠,化学式为 NaOH,是一种强碱性化合物,常被用于工业生产中。
在我国,工业用氢氧化钠的生产和应用有着严格的国家标准,以确保其质量和安全。
一、氢氧化钠的概述氢氧化钠,也被称为烧碱、火碱或苛性钠,是一种常见的强碱性化学物质。
它在工业生产中有着广泛的应用,如用于制造肥皂、纸浆、纺织品等。
同时,氢氧化钠也是许多化学反应的常用试剂,如酸碱中和反应等。
二、工业用氢氧化钠国家标准的意义工业用氢氧化钠国家标准的制定,是为了保证产品质量,确保产品在使用过程中的安全。
标准中规定了工业用氢氧化钠的要求、采样、试验方法、检验规则及标志、包装、运输和储存、安全等内容,是工业用氢氧化钠生产和应用的指南。
三、工业用氢氧化钠的主要产品重庆远诚化工有限公司是一家专业生产工业用氢氧化钠的企业,其主要产品包括片碱、纯碱、氯化钙、聚合氯化铝、氯化铵、次氯酸钠、聚丙烯酰胺、石灰、活性炭、硫酸铵、硫酸钠等。
这些产品广泛应用于化工、冶金、建筑、纺织、造纸等行业。
四、工业用氢氧化钠中氢氧化钠和碳酸钠含量的测定方法工业用氢氧化钠中氢氧化钠和碳酸钠含量的测定,通常采用滴定法。
本标准等效采用 ISO 3196-1975《工业用氢氧化钠—碳酸盐含量测定—滴定法》。
本标准规定了工业用氢氧化钠中碳酸盐含量的测定方法,包括仪器和试剂的准备、采样、试验步骤等。
五、工业用氢氧化钠的价格工业用氢氧化钠的价格因生产厂家、地区、产品规格等因素而异。
一般来说,工业用氢氧化钠的价格在几千元到一万多元一吨之间。
具体价格需要咨询相关厂家或查阅行业报价。
综上所述,工业用氢氧化钠国家标准对于保证产品质量和安全有着重要的意义。

工业碳酸钠总碱度的测定实验报告工业碳酸钠总碱度的测定实验报告示例如下:实验目的:本实验的目的是通过测量工业碳酸钠溶液的总碱度来评估其性能。
实验原理:二氧化碳(CO2)可以与碳酸钠反应生成碳酸氢钠(Na2CO3·H2O),而碳酸氢钠可以通过滴定法来测量其浓度。
同时,滴定过程中,滴入的氢氧化钠(NaOH)也会与CO2反应生成碳酸钠和氢氧化钠滴定液(Na2CO3和OH-)。
因此,可以通过测量滴定液的浓度来评估工业碳酸钠溶液的总碱度。
实验步骤:1. 准备试剂:取100mL蒸馏水,加入1mL氢氧化钠,用电子天平准确称量,排除干扰。
然后,将氢氧化钠滴定液(1.5mL/min)加入氢氧化钠溶液中,用电子天平准确称量,排除干扰。
2. 配制标准溶液:取17.95g碳酸钠,溶解在1000mL蒸馏水中,用电子天平准确称量,排除干扰。
然后将标准溶液制备成1.5mL/min的滴定液,加入氢氧化钠溶液中,用电子天平准确称量,排除干扰。
3. 进行实验:将工业碳酸钠溶液、标准溶液和滴定液分别倒入相应的烧杯中,摇晃均匀,然后烧杯立即放入冰水中浸泡3-5分钟,以分离反应物。
4. 进行滴定:将冰水中浸泡后的烧杯分别加入0.1mL标准溶液、0.5mL滴定液和1.0mL滴定液,用电子天平准确称量,然后开始滴定。
根据滴定液的浓度变化,记录滴定液体积和滴定时间。
5. 重复实验:重复以上步骤进行多次实验,取平均值,即可得到工业碳酸钠溶液的总碱度。
注意事项:在进行实验前,必须将样品处理干净,以确保实验结果的准确性。
在实验过程中,必须严格控制滴定液的浓度和滴定速度,以避免反应过度或反应不足。
在进行实验后,必须将烧杯立即倒入冰水中冷却,以确保结果的准确性。
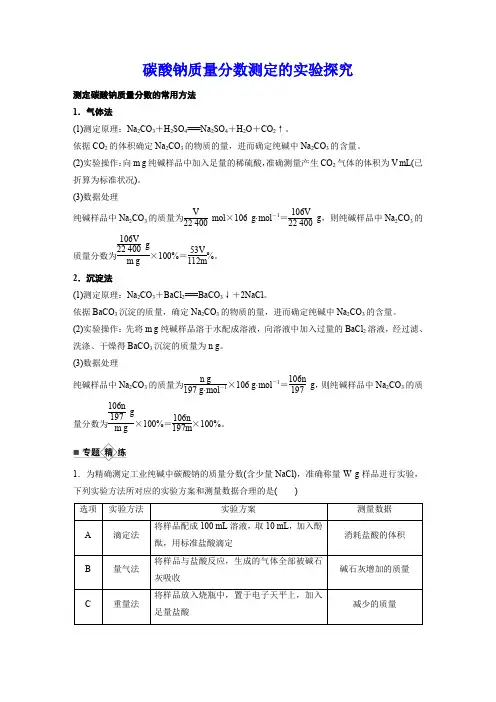
碳酸钠质量分数测定的实验探究测定碳酸钠质量分数的常用方法1.气体法(1)测定原理:Na 2CO 3+H 2SO 4===Na 2SO 4+H 2O +CO 2↑。
依据CO 2的体积确定Na 2CO 3的物质的量,进而确定纯碱中Na 2CO 3的含量。
(2)实验操作:向m g 纯碱样品中加入足量的稀硫酸,准确测量产生CO 2气体的体积为V mL(已折算为标准状况)。
(3)数据处理纯碱样品中Na 2CO 3的质量为V 22 400 mol ×106 g·mol -1=106V 22 400g ,则纯碱样品中Na 2CO 3的质量分数为106V 22 400 g m g ×100%=53V 112m%。
2.沉淀法(1)测定原理:Na 2CO 3+BaCl 2===BaCO 3↓+2NaCl 。
依据BaCO 3沉淀的质量,确定Na 2CO 3的物质的量,进而确定纯碱中Na 2CO 3的含量。
(2)实验操作:先将m g 纯碱样品溶于水配成溶液,向溶液中加入过量的BaCl 2溶液,经过滤、洗涤、干燥得BaCO 3沉淀的质量为n g 。
(3)数据处理纯碱样品中Na 2CO 3的质量为n g 197 g·mol-1×106 g·mol -1=106n 197 g ,则纯碱样品中Na 2CO 3的质量分数为106n 197 g m g ×100%=106n 197m×100%。
1.为精确测定工业纯碱中碳酸钠的质量分数(含少量NaCl),准确称量W g 样品进行实验,下列实验方法所对应的实验方案和测量数据合理的是( )答案 A解析用酚酞做指示剂时,Na2CO3与盐酸发生反应Na2CO3+2HCl===2NaCl+CO2↑+H2O,依据消耗盐酸的量可以计算出样品中Na2CO3的量,进而确定样品中Na2CO3的质量分数,A 项正确;测量碱石灰增重的方法是重量法而不是量气法,B项错误;样品中加入足量盐酸,因盐酸的质量未知,无法通过重量法测量Na2CO3的质量,C项错误;因部分CO2能溶解到水里,与水反应生成H2CO3,故排出水的体积并不是CO2的体积,D项错误。
测量碳酸钠的纯度实验原理碳酸钠(Na2CO3)广泛用于工业生产、制药、制革、制糖、玻璃等领域。
在许多应用中,碳酸钠的纯度是非常重要的,因为纯度低会影响其性能和应用效果。
因此,需要进行测量碳酸钠的纯度的实验。
测量碳酸钠纯度的实验主要依靠化学反应和比色法。
下面将详细说明实验的原理。
首先,实验人员需要为实验准备一组标准溶液。
该标准溶液的浓度应与纯碱溶液的浓度相似。
然后,采用容量瓶将纯碱溶液稀释到适当的浓度。
在实验中,可以使用酸碱滴定法来确定碳酸钠的纯度。
实验人员将标准溶液加入滴定瓶,并加入一滴酚酞指示剂。
然后,利用滴定管逐滴加入待测溶液,直到溶液开始由红色变为无色。
此时记录滴定管中加入的滴数,并据此计算出碳酸钠的纯度。
实验原理是碳酸钠和酸之间的中和反应。
酸和碱之间的反应是一种化学反应,通过加入酚酞指示剂可以获得准确的滴定终点。
碳酸钠中的Na2CO3能与酸发生中和反应,反应产物为盐和水。
在滴定终点附近,碳酸钠的纯度可以根据所添加的酸的摩尔量和滴定终点所需的酸的摩尔量来计算。
根据摩尔比例,可以确定碳酸钠的浓度和纯度。
另一种常用的方法是使用比色法。
比色法是一种通过溶液的颜色来确定其物质浓度的方法。
对于碳酸钠,可以使用酸碱指示剂来进行比色测量。
实验中使用的一种常见的指示剂是甲基橙。
甲基橙呈酸性时呈红色,呈碱性时呈黄色。
实验人员可以根据溶液的颜色变化,来确定溶液中碳酸钠的纯度。
实验中还可以用硫酸二甲酯法来测定碳酸钠的纯度。
该方法基于硫酸二甲酯与碳酸钠的反应,生成甲酸二甲酯。
通过测量甲酸二甲酯的体积,从而确定碳酸钠的浓度和纯度。
实验人员将硫酸二甲酯滴加到待测溶液中,一直滴加到溶液中全部生成甲酸二甲酯为止。
此时测量用掉的硫酸二甲酯体积,即可计算出碳酸钠的纯度。
总结起来,测量碳酸钠的纯度可以使用酸碱滴定法、比色法和硫酸二甲酯法。
这些方法的原理是基于化学反应、指示剂的颜色变化以及生成的反应产物的计量。
选择适当的方法进行实验,可以获得准确且可靠的结果,以确保碳酸钠的纯度满足应用的需求。
碳酸钠含量检测方法
1. 酸碱滴定法:这是一种常用的碳酸钠含量检测方法。
其原理是利用碳酸钠与酸反应生成二氧化碳的性质,通过滴定酸的用量来计算碳酸钠的含量。
具体操作是将待测样品溶解在水中,加入已知浓度的酸溶液,用酚酞作为指示剂,当溶液由红色变为无色时,即为滴定终点。
根据酸的用量和浓度,可以计算出碳酸钠的含量。
2. 重量法:该方法基于碳酸钠与氯化钙反应生成碳酸钙沉淀的原理。
将待测样品溶解在水中,加入过量的氯化钙溶液,使碳酸钠完全反应生成碳酸钙沉淀。
过滤沉淀,并将其干燥、称重。
根据沉淀的质量和化学计量关系,可以计算出碳酸钠的含量。
3. 电位滴定法:电位滴定法是一种基于电位变化来确定滴定终点的方法。
在碳酸钠含量检测中,通常使用盐酸作为滴定剂,用玻璃电极作为指示电极,检测溶液的电位变化。
当滴定剂与碳酸钠反应达到等当点时,电位会发生突跃,通过记录滴定过程中的电位变化,可以确定等当点,从而计算出碳酸钠的含量。
4. 原子吸收光谱法:原子吸收光谱法是一种基于原子吸收光谱原理的分析方法。
将待测样品溶解在水中,通过原子吸收光谱仪测定碳酸钠的特征吸收峰的强度,根据标准曲线或内标法,可以计算出碳酸钠的含量。
需要注意的是,不同的检测方法适用于不同的样品类型和检测要求。
在选择检测方法时,需要考虑样品的性质、检测精度、实验条件等因素。
同时,为了获得准确可靠的检测结果,需要严格按照操作规程进行实验操作,并进行适当的质量控制和验证。
检验碳酸钠的方法
首先,最常用的方法之一是酸碱滴定法。
首先将碳酸钠溶解于水中,然后用酚
酞指示剂滴定至终点。
通过滴定所需的酸的体积,可以计算出碳酸钠的含量。
这种方法简单易行,准确性较高,被广泛应用于实验室和生产现场。
其次,还可以利用重金属离子沉淀法来检验碳酸钠。
将碳酸钠溶液与过量的重
金属离子溶液反应,生成沉淀,然后通过过滤、干燥、称重等步骤,计算出碳酸钠的含量。
这种方法对于含量较高的碳酸钠样品效果较好,但操作过程较为繁琐。
此外,还可以利用酸度法来检验碳酸钠的含量。
将碳酸钠样品溶解于水中,然
后用酸溶液滴定至中和终点,通过滴定所需的酸的体积,计算出碳酸钠的含量。
这种方法操作简便,但对于含量较低的碳酸钠样品可能会出现准确度不高的情况。
最后,还可以利用熔融法来检验碳酸钠的含量。
将碳酸钠样品与熔融剂混合,
然后在高温条件下熔融,通过冷却后的产物的重量变化,计算出碳酸钠的含量。
这种方法适用于含量较高的碳酸钠样品,但操作过程较为复杂,需要高温条件下进行,操作要求较高。
综上所述,检验碳酸钠的方法有多种,可以根据具体情况选择合适的方法。
在
实际操作中,需要根据样品的性质、含量和实验条件等因素综合考虑,选择最合适的检验方法,以保证检验结果的准确性和可靠性。
实验二工业纯碱中总碱度的测定实验目的1.掌握配制和标定HCl标准溶液的方法。
2.学习容量瓶、移液管的使用方法,进一步熟练酸式滴定管的操作方法。
3.掌握工业纯碱中总碱度测定的原理和方法。
主要试剂和仪器仪器:酸滴定管;锥形瓶;容量瓶;移液管;烧杯;洗瓶。
试剂:无水碳酸钠(基准物质,180 0C干燥2~3小时,然后放入干燥器内冷却后备用);浓HCl(相对密度1.19,分析纯);0.2%甲基橙水溶液;工业纯碱试样。
实验原理碳酸钠是重要的化工原料之一,作为制造其他化学品的原料、清洗剂、洗涤剂,广泛应用于轻工日化、建材、化学工业、食品工业、冶金、纺织、石油、国防、医药等领域。
工业碳酸钠,俗称纯碱、苏打或苏打粉,其主要成分为Na2CO3,其中可能还含有少量NaCl、Na2SO4、NaOH或NaHCO3等成分。
工业纯碱总碱度的测定,通常是指用酸碱滴定法滴定主要成分Na2CO3和其他碱性杂质如NaOH 或NaHCO3等的含量,常用于检定纯碱的质量。
可能发生的反应包括:Na2CO3+2HCl = 2NaCl+ H2O+CO2↑NaOH + HCl = NaCl+ H2ONaHCO3+HCl = NaCl+ H2O+CO2↑反应产物为NaCl和H2CO3,化学计量点时pH为3.8左右。
可选用甲基橙为指示剂,用HCl标准溶液滴定至溶液由黄色变为橙色时,即为终点。
工业纯碱长期暴露在空气中能吸收空气中的水分及二氧化碳,生成碳酸氢钠,并结成硬块。
因此要将试样在2700C-3000C烘干2小时,除去试样中的水分,并使NaHCO3全部转化为Na2CO3。
工业纯碱均匀性差,测定的允许误差可稍大。
浓盐酸易挥发出HCl气体,不能直接配制准确浓度的HCl标准溶液。
配制盐酸标准溶液时需用间接配制法,先配制近似浓度的溶液,然后用基准物质标定其准确浓度。
也可用另一已知准确浓度的标准溶液滴定盐酸溶液,再根据它们的体积比求得盐酸溶液的浓度。
标定HCl溶液常用的基准物有无水碳酸钠和硼砂等。