常见气体的制取、净化与干燥复习专题
- 格式:doc
- 大小:407.23 KB
- 文档页数:4
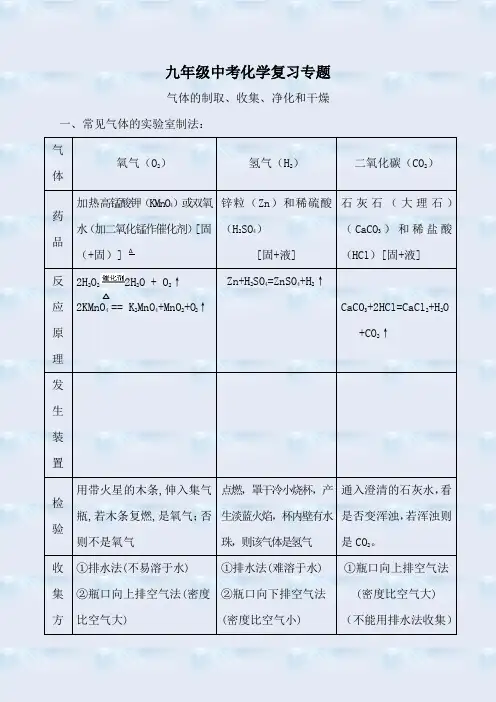
九年级中考化学复习专题气体的制取、收集、净化和干燥一、常见气体的实验室制法:气体氧气(O2)氢气(H2)二氧化碳(CO2)药品加热高锰酸钾(KMnO4)或双氧水(加二氧化锰作催化剂)[固(+固)] Δ锌粒(Zn)和稀硫酸(H2SO4)[固+液]石灰石(大理石)(CaCO3)和稀盐酸(HCl)[固+液]反应原理2H2O22H2O + O2↑2KMnO4 == K2MnO4+MnO2+O2↑Zn+H2SO4=ZnSO4+H2↑CaCO3+2HCl=CaCl2+H2O+CO2↑发生装置检验用带火星的木条,伸入集气瓶,若木条复燃,是氧气;否则不是氧气点燃,罩干冷小烧杯,产生淡蓝火焰,杯内壁有水珠,则该气体是氢气通入澄清的石灰水,看是否变浑浊,若浑浊则是CO2。
收集方①排水法(不易溶于水)②瓶口向上排空气法(密度比空气大)①排水法(难溶于水)②瓶口向下排空气法(密度比空气小)①瓶口向上排空气法(密度比空气大)(不能用排水法收集)法验满验纯验满:用带火星的木条,平放在集气瓶口,若木条复燃,氧气已满,否则没满验纯:<1>用拇指堵住集满氢气的试管口;<2>靠近火焰,移开拇指点火;若“噗”的一声,氢气已纯;若有尖锐的爆鸣声,则氢气不纯验满:用燃着的木条,平放在集气瓶口,若火焰熄灭,则已满;否则没满放置正放倒放正放注意事项①检查装置的气密性②试管口要略向下倾斜(防止凝结在试管口的小水珠倒流入试管底部使试管破裂)③加热时应先使试管均匀受热,再集中在药品部位加热。
④排水法收集完氧气后,先撤导管后撤酒精灯(防止水槽中的水倒流,使试管破裂)⑤用高锰酸钾制取氧气时,①检查装置的气密性②长颈漏斗的管口要插入液面下;③点燃氢气前,一定要检验氢气的纯度(空气中,氢气的体积达到总体积的4%—74.2%点燃会爆炸。
)①检查装置的气密性②长颈漏斗的管口要插入液面下;③不能用排水法收集试口要塞一团棉花。
防此高锰酸钾进入导管。
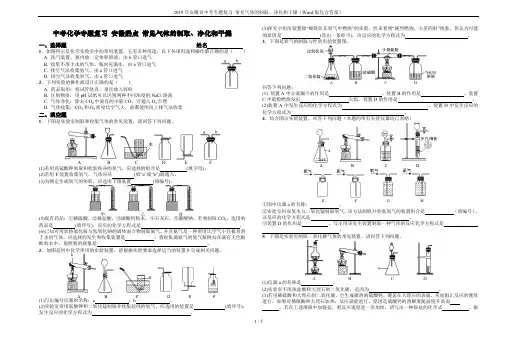
中考化学专题复习 安徽热点 常见气体的制取、净化和干燥一、选择题 姓名1.如图所示是化学实验室中的常用装置,它有多种用途,以下各项用途和操作都正确的是( ) A. 洗气装置,瓶内放一定体积溶液,由b 管口进气 B. 收集不溶于水的气体,瓶内充满水,由a 管口进气 C. 排空气法收集氢气,由a 管口进气 D. 排空气法收集氧气,由a 管口进气2.下列实验的操作或设计正确的是() A. 药品取用:将试管竖直,垂直放入锌粒B. 区别物质:用pH 试纸可以区别两种不同浓度的NaCl 溶液C. 气体净化:除去CO 2中混有的少量CO ,可通入O 2点燃D. 气体收集:CO 2和O 2密度比空气大,故都能用向上排气法收集二、填空题1.下图是实验室制取和收集气体的常见装置,请回答下列问题。
A B C D E F(1)若用高锰酸钾制取和收集纯净的氧气,应选择的组合是 (填字母)。
(2)若用F 装置收集氧气,气体应从 (填“a”或“b”)端通入。
(3)为测定生成氧气的体积,应选用下图装置(填编号)。
(5)现有药品:①稀硫酸,②稀盐酸,③碳酸钙粉末,④石灰石,⑤碳酸钠。
若要制取CO 2,选用的药品是 (填序号),反应的化学方程式是 。
(6)已知可用加热氯化铵与氢氧化钠的固体混合物制取氨气,并且氨气是一种密度比空气小且极易溶于水的气体,应选择的发生和收集装置是 ;将收集满氨气的集气瓶倒扣在滴有无色酚酞的水中,观察到的现象是 。
2.如图是初中化学常用的实验装置,请根据实验要求选择适当的装置并完成相关问题。
(1)写出编号仪器的名称:a;b 。
(2)实验室常用氯酸钾和二氧化锰制取并收集较纯的氧气,应选用的装置是 (填序号),发生反应的化学方程式为 。
(3)探究小组用装置做“细铁丝在氧气中燃烧”的实验,但未看到“剧烈燃烧,火星四射”现象,你认为可能的原因是 (答出一条即可),该反应的化学方程式为 。
3.下图是氧气的制取与性质实验装置图。



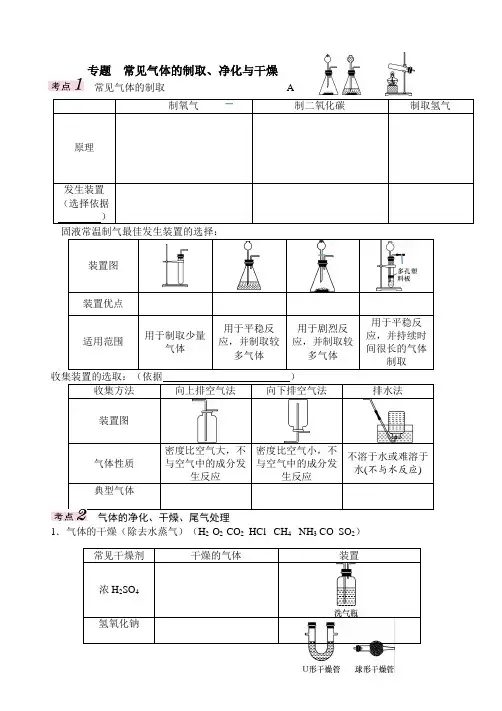
专题 常见气体的制取、净化与干燥常见气体的制取 A 固液常温制气最佳发生装置的选择:装置图装置优点适用范围用于制取少量气体用于平稳反应,并制取较多气体用于剧烈反应,并制取较多气体用于平稳反应,并持续时间很长的气体制取 收集装置的选取:(依据 )收集方法 向上排空气法 向下排空气法排水法装置图气体性质密度比空气大,不与空气中的成分发生反应 密度比空气小,不与空气中的成分发生反应不溶于水或难溶于水(不与水反应)典型气体气体的净化、干燥、尾气处理1.气体的干燥(除去水蒸气)(H 2 O 2 CO 2 HCl CH 4 NH 3 CO SO 2)制氧气 制二氧化碳制取氢气原理发生装置 (选择依据 )常见干燥剂 干燥的气体装置浓H 2SO 4氢氧化钠注意:(1)洗气瓶用液体试剂除杂或干燥气体,气体通过的方向是长管进,短管出。
(2)U 形干燥管和球形干燥管用固体除杂或干燥气体。
2.气体的净化(除去杂质) 3.多功能瓶的使用 装置图目的 洗气或干燥气体 收集气体收集气体收集气体测定气体的体积操作4. 尾气处理5. 【练习】以下是小阳同学制取气体的实验过程,请根据题意回答以下问题.(1)如果他用锌粒和浓盐酸来制取氢气,可以选择______(填序号)做发生装置,装置②的主要仪器有分液漏斗、带导管的双孔胶塞和______(填仪器名称).(2)将一定质量的浓盐酸盛于烧杯中,敞口放置在实验室安全之处.①浓盐酸的质量和放置天数关系的曲线(见图)正确的是______(填写“甲”或“乙”).②随着放置天数的增加,浓盐酸的质量发生变化的主要原因是 .(3)上述制得的氢气含有少量的水蒸气和HCl 气体,若要检验是否有HCl 气体,所用试剂是 。
若要得到干燥、纯净的氢气,需要通过③和④装置,则装置按导管字母连接的顺序是:发生装置→______→______→______→______→收集装置(填字母)。
氧化钙除去气体 气体净化试剂 CO 2 NaOH 溶液、灼热的炭H 2O 浓H 2SO 4 HCl Na 2CO 3溶液、NaHCO 3溶液、AgNO 3溶液 CO 灼热的氧化铜 O 2 灼热的铜丝网(4)实验室用①制取氧气,反应的化学方程式为。
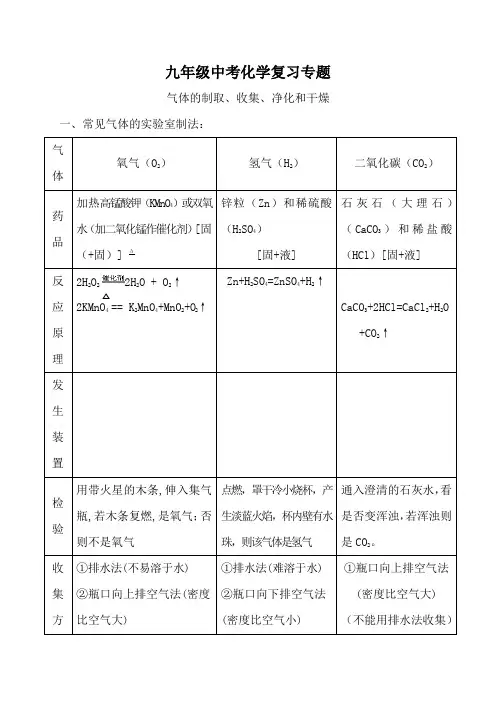
九年级中考化学复习专题气体的制取、收集、净化和干燥一、常见气体的实验室制法:气体氧气(O2)氢气(H2)二氧化碳(CO2)药品加热高锰酸钾(KMnO4)或双氧水(加二氧化锰作催化剂)[固(+固)] Δ锌粒(Zn)和稀硫酸(H2SO4)[固+液]石灰石(大理石)(CaCO3)和稀盐酸(HCl)[固+液]反应原理2H2O22H2O + O2↑2KMnO4 == K2MnO4+MnO2+O2↑Zn+H2SO4=ZnSO4+H2↑CaCO3+2HCl=CaCl2+H2O+CO2↑发生装置检验用带火星的木条,伸入集气瓶,若木条复燃,是氧气;否则不是氧气点燃,罩干冷小烧杯,产生淡蓝火焰,杯内壁有水珠,则该气体是氢气通入澄清的石灰水,看是否变浑浊,若浑浊则是CO2。
收集方①排水法(不易溶于水)②瓶口向上排空气法(密度比空气大)①排水法(难溶于水)②瓶口向下排空气法(密度比空气小)①瓶口向上排空气法(密度比空气大)(不能用排水法收集)法验满验纯验满:用带火星的木条,平放在集气瓶口,若木条复燃,氧气已满,否则没满验纯:<1>用拇指堵住集满氢气的试管口;<2>靠近火焰,移开拇指点火;若“噗”的一声,氢气已纯;若有尖锐的爆鸣声,则氢气不纯验满:用燃着的木条,平放在集气瓶口,若火焰熄灭,则已满;否则没满放置正放倒放正放注意事项①检查装置的气密性②试管口要略向下倾斜(防止凝结在试管口的小水珠倒流入试管底部使试管破裂)③加热时应先使试管均匀受热,再集中在药品部位加热。
④排水法收集完氧气后,先撤导管后撤酒精灯(防止水槽中的水倒流,使试管破裂)⑤用高锰酸钾制取氧气时,①检查装置的气密性②长颈漏斗的管口要插入液面下;③点燃氢气前,一定要检验氢气的纯度(空气中,氢气的体积达到总体积的4%—74.2%点燃会爆炸。
)①检查装置的气密性②长颈漏斗的管口要插入液面下;③不能用排水法收集试口要塞一团棉花。
防此高锰酸钾进入导管。


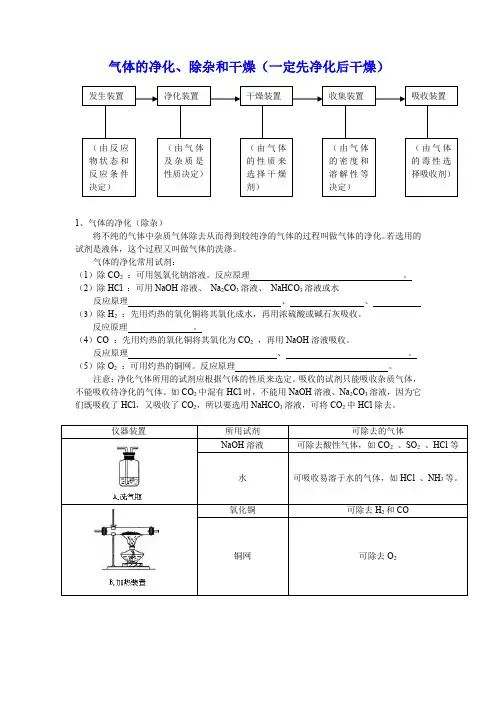
气体的净化、除杂和干燥(一定先净化后干燥)1、气体的净化(除杂)将不纯的气体中杂质气体除去从而得到较纯净的气体的过程叫做气体的净化。
若选用的试剂是液体,这个过程又叫做气体的洗涤。
气体的净化常用试剂:(1)除CO2:可用氢氧化钠溶液。
反应原理。
(2)除HCl :可用NaOH溶液、Na2CO3溶液、NaHCO3溶液或水反应原理、、(3)除H2:先用灼热的氧化铜将其氧化成水,再用浓硫酸或碱石灰吸收。
反应原理。
(4)CO :先用灼热的氧化铜将其氧化为CO2,再用NaOH溶液吸收。
反应原理、。
(5)除O2:可用灼热的铜网。
反应原理。
注意:净化气体所用的试剂应根据气体的性质来选定。
吸收的试剂只能吸收杂质气体,不能吸收待净化的气体。
如CO2中混有HCl时,不能用NaOH溶液、Na2CO3溶液,因为它们既吸收了HCl,又吸收了CO2,所以要选用NaHCO3溶液,可将CO2中HCl除去。
三、气体的检验及性质实验A B C D注意:要证明某混合气体中某气体的存在,必须先除去混合气体中会造成所证气体实验现象不可靠的气体。
初中化学中常验证的气体有水蒸气、CO2、HCl气体、CO、H2等,它们通过试剂所表现的现象分别为:①水蒸气———无水CuSO4———变蓝(一般放在最先验证); ②CO2———澄清的石灰水———白色浑浊; ③HCl———AgNO3溶液———白色沉淀;④H2———灼热氧化铜、无水CuSO4———黑色粉末变红,白色粉末变蓝; ⑤CO———灼热氧化铜、澄清石灰水———黑色粉末变红、石灰水变浑浊。
四、其它1、尾气体的处理方法(当收集的是有毒气体,会污染环境,还需要考虑尾气的处理。
) (1)燃烧法 如:CO (2)液体吸收 如:SO 2 (3)收集法2、水的处理(1)作为杂质而除去:要先除去其他杂质,后干燥。
(2)作为产物的检验:先检验水,再检验其他产物。
(3)水的定测量:前后都要排除外来水的干扰。
备注:证明时,一定要先证明水再证明其它物质,证明水一定要用无水硫酸铜;除去水时,先除去杂质,再除去水 。

常见气体的制取、净化与干燥专题教案
专题复习气体的制取、净化与干燥
教学目标
知识目标:1.掌握O2、CO2、H2的实验室制法。
2.掌握常见的气体净化方法。
3.掌握常见气体的检验
能力目标:
1.会确定制取气体的反应原理,即在什么实验条件下(如常温、加热、加催化剂等),选择什么药品,通过什么反应来制取这种气体
2.会确定制取气体时应采用的实验装置
3.会确定如何验证制得的气体就是所要制取的气体
教学重点:
1.O2、CO2、H2的实验室制法。
2.掌握常见的气体净化方法。
教学难点:气体的净化
教学方法:归纳法练习法
教学过程
一、考点知识梳理
点一 : O2、CO2、H2实验室制取方法对比
气体氧气(O2) 氢气(H2) 二氧化碳(CO2)
药品 :双氧水和二氧化锰氯酸钾和二氧化锰高锰酸钾锌与稀硫酸大理石或石灰石与稀盐酸
固液常温型: 固固加热固液常温型(启普发固液常温型: 实型: 生器的简易装置):
收集排水法(不易溶于水)或向上排水法(不溶于水)向上排空气法
能溶于水方法向上排空气法(密度比空气大) 或向下排空气法(密度比空气小)
检验:将带火星的木条伸入集气瓶点燃;罩干而冷的小通过澄清石灰水,石灰水变浑浊
验满:用带火星的木条靠近集气瓶,木条复燃;用燃着的木条靠近集气瓶口,木条熄灭则说明已满。
考点二:气体的净化与干燥
1.气体的净化
选择气体吸收剂的原则是所选吸收剂只吸收气体中的杂质,而与被提纯的物质不反应,也不产生新的杂质。
多种气体杂质共存时,要注意试剂的选择和除杂质的顺序,一般水蒸气最后除去。
选择“洗气瓶”等吸收装置,不仅要注意药品的名称,还要注意“长进短出”的原则,干燥管要“大进小出”。
常见的气体杂质的吸收剂见下表:
吸收剂吸收的气体杂质
2.气体的干燥
选用干躁剂应根据气体的性质和干燥剂的性质确定,其原则是干燥剂只能吸收气体中的水分,而不能与气体发生反应。
常见的气体的干燥剂的选择
二、典型例题分析(见演示文稿)
三、专题训练 ----历年典型中考习题(见演示文稿)
方法:教师引导,学生合作完成。
布置作业: .
感谢您的阅读,祝您生活愉快。