专题四 常见气体的制取与净化
- 格式:ppt
- 大小:818.50 KB
- 文档页数:27


千里之行,始于足下。
常见的气体制取与净化
常见的气体制取与净化方法有:
1. 空气分离法:通过空气分离装置将空气中的氮气、氧气等组分分离出来,得到高纯度的氮气、氧气等气体。
2. 化学合成法:根据不同气体的物理性质和化学性质,通过化学反应生成目标气体。
例如,氢气可以通过水电解反应或碳一烯饱和蒸馏法制取。
3. 燃烧法:某些气体可以通过燃烧反应制取,如氢气可以通过金属与酸的反应或铝水与水的反应制取。
4. 吸附法:利用吸附剂(如活性炭)将气体分子吸附在表面上,从而实现气体的净化。
例如,对空气中的有害气体进行净化。
5. 洗涤法:将气体与液体接触,通过溶解、循环冲洗等方法,去除气体中的杂质。
例如,对氯气进行液体洗涤以去除其中的杂质。
6. 膜分离法:利用特殊材料的膜进行分离,根据气体分子的大小、形状和亲疏水性等特性来实现气体的分离和纯化。
例如,利用膜分离技术可以将二氧
化碳从天然气中分离出来。
7. 冷凝法:通过降低气体温度使其冷凝,从而分离出目标气体。
例如,液化空气工艺中通过降低空气温度来分离出液态氧气和液态氮气。
这些方法在工业生产和实验室研究中被广泛应用,以满足不同领域的气体
制取和净化需求。
第1页/共1页。
专题复习气体的制备和净化
教学目标
知识目标:1.掌握O2、CO2、H2的实验室制法。
2.掌握常见的气体净化方法。
3.掌握常见气体的检验
能力目标: 1会确定制取气体的反应原理,即在什么实验条件下(如常温、加热、加催化剂等),选择什么药品,通过什么反应来制取这种气体
2.会确定制取气体时应采用的实验装置
3.会确定如何验证制得的气体就是所要制取的气体
教学重点:1、O
2、CO
2
、H
2
的实验室制法。
2.掌握常见的气体净化方法。
教学难点:气体的净化
教学方法:归纳法练习法
教学过程
一、考点知识梳理
考点一: O
2、CO
2
、H
2
实验室制取方法对比
考点二:气体的净化与干燥
1.气体的净化
选择气体吸收剂的原则是所选吸收剂只吸收气体中的杂质,而与被提纯的物质不反应,也不产生新的杂质。
多种气体杂质共存时,要注意试剂的选择和除杂质的顺序,一般水蒸气最后除去。
选择“洗气瓶”等吸收装置,不仅要注意药品的名称,还要注意“长进短出”的原则,干燥管要“大进小出”。
常见的气体杂质的吸收剂见下表:
2.气体的干燥
选用干躁剂应根据气体的性质和干燥剂的性质确定,其原则是干燥剂只能吸收气体中的水分,而不能与气体发生反应。
常见的气体的干燥剂的选择见演示文稿
二、典型例题分析(见演示文稿)
三、专题训练 ----历年典型中考习题(见演示文稿)
方法:教师引导,学生合作完成。
布置作业: .。




常见气体的制取、净化和收集【重点难点提示】1.重点是:初中化学要求的三种常见气体:O2、H2、CO2的制取原理、发生装置、净化和干燥装置及气体收集装置和尾气处理装置,常见气体制备的操作步骤。
2.难点是:气体制取装置的选择及制备原理,气体制备的操作步骤,气体净化和干燥装置的选择。
3.考点是:O2、H2、CO2三种气体制取原理的化学方程式的书写、药品的选择、制取装置的选择及实验操作步骤的确定或排序、气体净化、干燥及收集装置的确定或选择,通过对三种气体制备时反应物的状态、反应条件的分析解决其他类似情况下气体的制取(如CH4、NH3、H2S等),根据气体发生装置的工作原理进行变形或转换。
常见气体的制取、净化和收集是化学实验的主要也是重要组成部分,是学生学好化学实验关键内容。
因此,它是历年中考化学实验部分主要考察内容,题型多样,份量大,有时还往往与其他气体或物质的性质综合在一起出现在综合实验题中。
【经典范例引路】例1 实验室里用加热高锰酸钾法制氧气的步骤包括:①点燃酒精灯给试管加热;②将高锰酸钾加入大试管中,用带导管的塞子塞紧并固定在铁架台上;③检查装置的气密性;④用排水法收集氧气;⑤熄灭酒精灯;⑥将导管移出水槽。
正确操作的顺序是()A.①②③④⑤⑥ B.②①③④⑤⑥C.③②①④⑥⑤ D.③②①④⑤⑥【解题技巧点拨】本题是对实验室制取氧气操作步骤的考察。
常见气体制备的操作步骤为:O2按“检、药、固、热、集、移、熄”的操作顺序进行。
检:检查装置气密性;药:将药品装入大试管;固:用铁夹将大试管固定在铁架台下;热:给试管加热;集:收集气体;移:把导气管移出水面;熄:熄灭酒精灯;H2:按“检、药、固、注、验、集、停”的顺序进行。
注:向大试管中注入稀酸溶液;验:检验氢气的纯度;停:关闭活塞或用弹簧夹紧紧夹住橡皮塞,使反应停止;CO2:按“检、药、注、集、验”的顺序进行。
验:检验是否集满CO2。
方法:将燃着的木条平置于集气瓶口,若火焰熄灭,表明已集满CO2气体,否则未满。

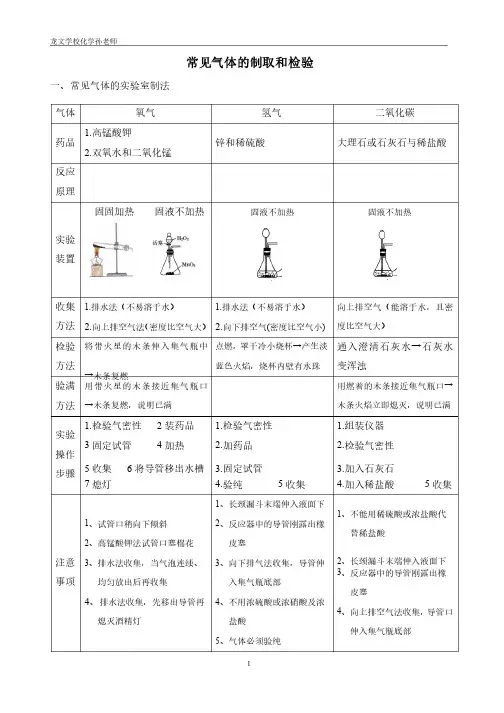
常见气体的制取和检验一、常见气体的实验室制法一、常见气体的实验室制法 气体气体氧气氧气氢气氢气二氧化碳二氧化碳药品药品 1.高锰酸钾高锰酸钾2.双氧水和二氧化锰双氧水和二氧化锰锌和稀硫酸锌和稀硫酸大理石或石灰石与稀盐酸大理石或石灰石与稀盐酸反应原理原理实验装置装置固固加热固固加热 固液不加热固液不加热固液不加热 固液不加热收集方法方法 1.排水法(不易溶于水)排水法(不易溶于水)2.向上排空气法(密度比空气大)1.排水法(不易溶于水)排水法(不易溶于水)2.向下排空气(密度比空气小) 向上排空气(能溶于水,且密度比空气大) 检验方法方法 将带火星的木条伸入集气瓶中→木条复燃木条复燃点燃,罩干冷小烧杯→产生淡蓝色火焰,烧杯内壁有水珠蓝色火焰,烧杯内壁有水珠通入澄清石灰水→石灰水变浑浊变浑浊验满方法方法 用带火星的木条接近集气瓶口→木条复燃,说明已满用燃着的木条接近集气瓶口→木条火焰立即熄灭,说明已满实验操作步骤步骤1.检验气密性检验气密性 2装药品装药品 3固定试管固定试管 4加热加热5收集收集 6将导管移出水槽将导管移出水槽 7熄灯熄灯1.检验气密性检验气密性2.加药品加药品3.固定试管固定试管4.验纯验纯 5收集收集1.组装仪器组装仪器2.检验气密性检验气密性3.加入石灰石加入石灰石4.加入稀盐酸加入稀盐酸 5收集收集注意事项事项 1、试管口稍向下倾斜、试管口稍向下倾斜 2、高锰酸钾法试管口塞棉花、高锰酸钾法试管口塞棉花3、排水法收集,当气泡连续、、排水法收集,当气泡连续、 均匀放出后再收集均匀放出后再收集4、排水法收集,先移出导管再 熄灭酒精灯1、长颈漏斗末端伸入液面下、长颈漏斗末端伸入液面下2、反应器中的导管刚露出橡、反应器中的导管刚露出橡 皮塞皮塞3、向下排气法收集,导管伸、向下排气法收集,导管伸 入集气瓶底部入集气瓶底部4、不用浓硫酸或浓硝酸及浓、不用浓硫酸或浓硝酸及浓 盐酸盐酸5、气体必须验纯、气体必须验纯1、不能用稀硫酸或浓盐酸代、不能用稀硫酸或浓盐酸代 替稀盐酸替稀盐酸2、长颈漏斗末端伸入液面下、长颈漏斗末端伸入液面下3、反应器中的导管刚露出橡、反应器中的导管刚露出橡 皮塞皮塞4、向上排空气法收集,导管口导管口 伸入集气瓶底部伸入集气瓶底部二、常见气体的检验二、常见气体的检验 气体气体 检验方法检验方法现象现象 氧气氧气 二氧化碳二氧化碳 氢气氢气 一氧化碳一氧化碳 甲烷甲烷 氨气氨气 水蒸气水蒸气 氮气氮气 氯化氢氯化氢三、常见气体的净化和干燥三、常见气体的净化和干燥 1、气体的净化、气体的净化(1)净化原则:所选试剂只吸收气体中的杂质,不与被提纯的物质反应,也不产生新的杂质。

常见气体的制取与净化1.常温下,氨气为无色有刺激性恶臭气味的气体,密度比空气小,易溶于水。
氨气溶于 水显弱碱性,实验室可用氯化铵固体和氢氧化钙固体混合加热制取。
则下列说法正确的是A.可用向下排空气法收集到氨气B.氨水能使紫色石蕊试液变红色2.( 2013山东青岛滨州)下列有关制取干燥的氧气或二氧化碳的实验设计中错误的是3•下图为初中化学常见气体的发生与收集装置。
有关这些装置的说法不正确的是()装置川、W 可用于收集密度与空气密度差距较大,且不与空气中各成分反应的气体 装置V 可以用于收集 H 2、Q ,也可以用于实验室收集 CQ 4. 根据表中五种气体在标准状况下的密度和溶解性,回答下列问题:空 NHC HCQ气3l2密度 1 0. 0 1.1/g?L - 1.293771 .717629.43 溶解性— 极难 极 难—易溶溶易溶溶(1) 既能用排水法,又能用向上排空气法收集的气体是. (2) 用如图所示盛满水的集气瓶收集 CH ,气体应从端进入.C.多余的氨气可排放到大气中D. 实验室制氨气的发生装置与双氧水制氧气相同1击A. B. 装置I 可作为固体加热制取气体的发生装置装置n 中长颈漏斗可以用分液漏斗、医用注射器代替I VC. D.5. ( 2013福建福州)下列是初中化学部分重要的实验或实验装置。
请按要求填空:(1) 写出装置A 中发生反应的化学方程式。
(2) 装置B 中浓硫酸的作用是。
(3) 装置D 中玻璃管内的实验现象为。
(4)该套装置中有一个明显的不足之处,应在装置E 后放置燃着的酒精灯处理尾气。
这样做,的原因是。
7.请结合下列常用实验装置,回答下列有关问题.(1 )实验室用过氧化氢溶液和二氧化锰制取氧气可选用的发生装置是 _____________(填序号)•该反应的化学方程式为 ________________ .A.水的电解实验B.测定空气里氧气含量C.探究二氧化碳性质D.气体制备装置实验玻璃管②(2) B 实验如果实验数据小于21%可能原因是(写出一点);(3) C 实验说明二氧化碳具有的性质是; (4) 写出用D 装置制取一种气体的化学方程式。

专题讲座(四)常见气体的实验室制备、净化和收集(精练)完卷时间:50分钟可能用到的相对原子质量:C12 O16 Cl35.5 Sn119 Ce140一、选择题(每小题只有一个正确选项,共12*5分)1.(2021·天津高三一模)下列实验装置能达到实验目的的是A.A B.B C.C D.D2.(2020·天津高三二模)如图是实验室制取气体的装置,其中发生装置相同,干燥和集气装置有两套,分别用图1和图2表示.下列选项中正确的是A.A B.B C.C D.D3.(2021·宁夏银川市·银川一中高三月考)下列制取或收集气体装置中棉花作用不正确的是作用A.A B.B C.C D.D4.(2020·山西晋中市·高三一模)某实验小组拟利用如图装置制取干燥的氮气。
下列说法错误的是A.装置I中发生的反应为NaNO2+NH4Cl加热NaCl+N2↑+2H2OB.加热片刻后需要将酒精灯移开,说明该反应是放热反应C.装置II的作用是冷凝水蒸气D.在装置III末端收集纯净干燥的N2只能用向下排空气法5.(2021·青海西宁市·高三期末)某研究性学习小组讨论甲、乙、丙、丁四种仪器装置的有关用法,其中不合理的是A.甲装置:可用来证明碳的非金属性比硅强B.乙装置:橡皮管的作用是能使水顺利流下C.丙装置:用图示的方法不能检查此装置的气密性D.丁装置:先从①口进气集满二氧化碳,再从②口进气,可收集氢气6.(2021·嫩江市高级中学高三月考)下列物质的实验室制取、检验及分离方法不合理的是(夹持装置已略去,气密性已检验)。
A.制取并检验氨气B.制取并检验SO2气体C.制取并提纯乙酸乙酯D.制取并检验乙炔7.(2020·广东深圳市·明德学校高三月考)用下列实验装置进行相应实验,能达到实验目的的是A.用图甲所示装置验证反应生成二氧化硫B.用图乙装置吸收氨气并防止倒吸C.用图丙装置除去氯气中的氯化氢D.用装置丁收集NO8.(2020·新安县第一高级中学高三开学考试)利用如图装置可以进行实验并能达到实验目的的是A.A B.B C.C D.D9.(2020·江西南昌市·)用所给试剂与图示装置能够制取相应气体的是(夹持仪器略)A .AB .BC .CD .D10.(2020·汪清县汪清第六中学高三月考)以CO 2和Na 2O 2为原料,制取纯净干燥的O 2,实验装置如下:下列说法不正确...的是 A .装置②中试剂可以是NaOH 溶液 B .装置③的作用是干燥O 2 C .收集氧气应选择装置aD .装置②、③之间应增加盛澄清石灰水的洗气瓶11.(2021·江苏南京市·高三二模)实验室用块状碳酸钙与稀盐酸反应制取少量CO 2时,图中装置不能达到相应实验目的的是A .生成CO 2B .净化CO 2C .干燥CO 2D .收集CO 212.(2021·天津高三二模)用下列装置完成相关实验,合理的是A .图①:验证23H CO 的酸性强于23H SiOB .图②:除去2CO 气体中的HCl 杂质NHC.图③:制取并收集乙酸乙酯D.图④:收集3二、主观题(共3小题,共40分)14.(14分)某化学兴趣小组的同学利用下图所示实验装置进行实验(图中a、b、c表示止水夹)。