酸碱中和滴定误差分析
- 格式:ppt
- 大小:1.15 MB
- 文档页数:24



酸碱中和滴定实验误差分析以一元酸和一元碱的中的滴定为例因C标、V定分别代表标准液浓度、所取待测液体积,均为定值,代入上式计算。
但是实际中C标、V定都可能引起误差,一般可把各因素引起的误差转嫁到V读上,若V读偏大,则测定结果偏大;若V读偏小,则测定结果偏小,故通过分析V读的变化情况,可分析滴定的误差。
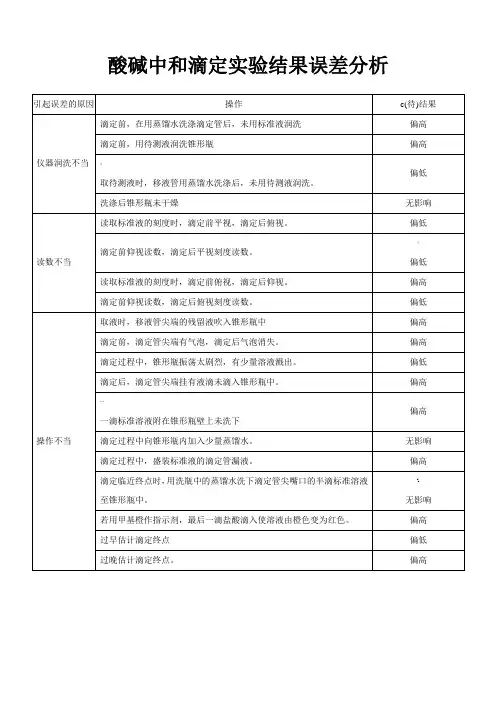
引起误差可能因素有以下几种:(1)视(读数)注意:①滴定管中液体读数时精确到0.01mL ②一般需滴定2-3次,取其平均值(2)洗(仪器洗涤)正确洗法:二管二洗——酸式滴定管和碱式滴定管先用蒸馏水清洗多次,再用待装液润洗几次。
一瓶一洗——锥形瓶只能用蒸馏水洗。
注意:一般滴定管装标准液,锥形瓶里装待测液。
错误洗法导致结果:①滴定管仅用水洗,使标准液变稀,故消耗标准液体积一定变大,V读变大,结果偏大。
②移液管仅用水洗,则待测液变稀,所取待测液溶质物质的量变少,V读变小,结果偏小。
③锥形瓶用待测液洗过,则瓶内待测液的溶质量偏多,V读偏大,结果偏大。
④第一次滴定完后,锥形瓶内液体倒去后,尚未清洗,接着第二次滴定,滴定结果如何,取决于上次滴定情况如何。
(3)漏(液体溅漏)①滴定过程中锥形瓶内液体溅出,则结果偏小。
②终点已到,滴定管下端尖嘴中有液滴,则V读偏大,测定结果偏大。
(4)泡(滴定管尖嘴气泡)正确操作应在滴定前把尖嘴管中的气泡赶尽,最后也不能出现气泡。
如滴定开始有气泡,后气泡消失,则结果偏大。
若先无气泡,后有气泡,则结果偏小。
(5)色(指示剂变色控制与选择)滴定时,眼睛应紧盯着锥形瓶内溶液的颜色变化。
指示剂变色后应半分钟内不复原。
如变色后立即复原,则结果偏小。
另外,同一种滴定,选择的指示剂不同,测定结果不同。
(6)杂(标准物含杂质)用于配制标准液的固体应该是纯净物。
但其中有可能混有杂质,称量时又按需标准物固体质量来称取的,帮一般均会产生误差,在此杂质又分两种情况:①杂质与待测液不反应如NaOH中含NaCl,所配的NaOH溶液浓度变小,滴定盐酸时,NaCl不参与反应,所需标准液的体积偏大,故测定结果偏大。
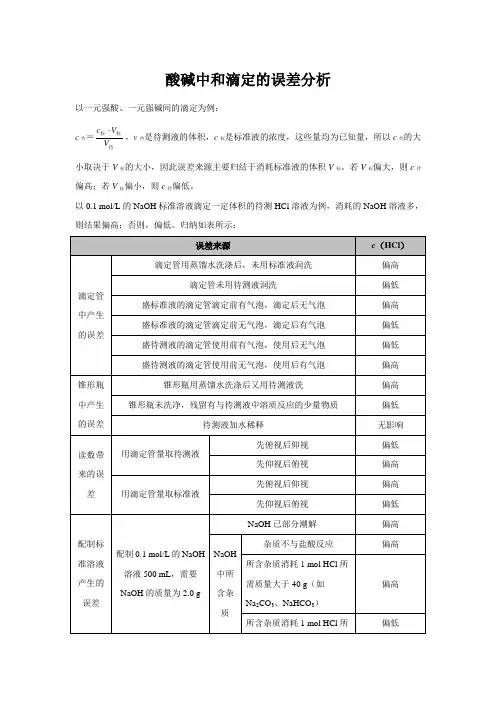
酸碱中和滴定的误差分析以一元强酸、一元强碱间的滴定为例:c待=c VV标标待,v待是待测液的体积,c标是标准液的浓度,这些量均为已知量,所以c待的大小取决于V标的大小,因此误差来源主要归结于消耗标准液的体积V标。
若V标偏大,则c待偏高;若V标偏小,则c待偏低。
以0.1 mol/L的NaOH标准溶液滴定一定体积的待测HCl溶液为例,消耗的NaOH溶液多,则结果偏高;否则,偏低。
归纳如表所示:需质量小于40 g(如Na2O)误区警示(1)对于仰视、俯视液面所造成的读数误差,很容易记反,画图能有效地解决这一问题。
如图3-2-9所示是对量筒和滴定管进行仰视、俯视液面的模拟图。
其共同点在于:俯视时液面位于读取刻度的下方,仰视时液面位于读取刻度的上方(记住“俯下仰上”)。
对于滴定管,仰视所读的值比平视的大,俯视所读的值比平视的小,而量筒正好相反。
图3-2-9(2)在酸碱中和滴定误差分析中,要看清楚标准液与待测液的位置。
当操作相同时,标准液在滴定管中与标准液在锥形瓶中产生的误差情况相反。
典例详析例6-18(2019广东深圳测试)某学生欲用已知物质的量浓度的盐酸来滴定未知物质的量浓度的NaOH溶液,选择甲基橙作指示剂。
请回答下列问题:(1)用标准盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视________。
直到因加入一滴盐酸后,溶液由黄色变为橙色,且________为止。
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是________(填字母)。
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥C.酸式滴定管在滴定前有气泡,滴定后气泡消失D.读取盐酸体积,开始时仰视液面,滴定结束后俯视液面(3)若滴定开始和结束时,酸式滴定管中的液面如图3-2-10所示,则起始读数为________mL,终点读数为________mL;所用盐酸的体积为________mL。

1.装标准液的滴定管没用标准液润洗,其中内壁有水分,导致标准液浓度降低,标准液的体积用量增多,所以待测液浓度就偏高了
2.未用待测液洗涤移液管或所用的滴定管,其内壁有水,所取一定体积的溶液含有的溶质变小,滴定所需的标准液体积就会减小,所以待测液浓度就偏低了。
3.锥形瓶用待测液洗过之后,或多或少留下一些待测液,那么待测液的物质的量变多,要加的标准液要多加,所以偏高
4.滴定的时候计算的是消耗的酸或者碱的物质的量,如果里面残留了水,物质的量浓度是会降低,但是物质的量还是不变的。
因此对结果没有影响
5.读数时会把气泡的体积当做标准液的体积,导致消耗的标准液大于实际值
6.前无气泡而滴定后有气泡,那么气泡体积会使液面上升,所以我们代入计算的标准液体积就减小了,所以C待偏低。
7.滴定前仰视滴定管读数,滴定后平视,导致V标偏小,C待偏低
8.滴定前平视,滴定后仰视,导致V标偏大,C待偏高
9.滴定前仰视,滴定后俯视,导致V标偏小,C待偏低
10.滴定前俯视,滴定后仰视,导致V标偏小,C待偏低
11.滴定待测液的浓度时,消耗标准溶液偏多,结果偏高。
12.标准液滴在锥形瓶外一滴,导致V标偏大,C待偏高
13.溅出待测液,就是待测液的物质的量少了。
消耗的V标偏小,结果偏低。

酸碱中和滴定的误差分析1、来自滴定管产生的误差:①、滴定管水洗后,未用标准液润洗析:因标准液被附在滴定管内壁的水珠稀释了,故消耗的标准液体积多了,所以结果偏高。
②、滴定管水洗后,未用待测液润洗析:因待测液被附在滴定管内壁的水珠稀释了,故消耗的标准液体积少了,所以结果偏低。
③、盛标准液的滴定管滴定前有气泡,滴定后气泡消失析:读出来的标准液体积为实际消耗的标准液体积+ 气泡体积, 故消耗的标准液体积读多了,所以结果偏高。
④、盛待测液的滴定管滴定前有气泡析:读出来的待测液体积为实际量取的待测液体积+ 气泡体积, 即待测液量少了,故消耗的标准液也少,所以结果偏低。
2、来自锥形瓶产生的误差:①、锥形瓶用蒸馏水水洗后又用待测液润洗析:因瓶内壁附着待测液,故锥形瓶内的待测液多了,消耗的标准液也多,所以结果偏高。
②、锥形瓶未洗净,残留有与待测液反应的少量物质,故消耗的标准液少了,所以结果偏低。
③、锥形瓶水洗后未干燥就加入待测液或滴定过程中向锥形瓶内加水析:实际参与中和反应的待测液的总量没变,实际消耗的标准酸液也就不变,故结果不变。
3、来自读数带来的误差:①、用滴定管量取待测液时A、先俯视后仰视(先俯视后平视或先平视后仰视)析:量取待测液的实际体积偏小,消耗的标准液也少,所以结果偏低。
B、先仰视后俯视(先仰视后平视或先平视后俯视)析:量取待测液的实际体积偏多,消耗的标准液也多,所以结果偏高。
②、用滴定管量取标准液时A、先俯视后平视析:读出来的标准液体积为V终-V始,而俯视时V始读小了,读出来的标准液体积偏大了,所以结果偏高。
B、先仰视后平视析:读出来的标准液体积为V终-V始,而俯视时V始读大了,读出来的标准液体积偏小了,所以结果偏低。
C、同理若先俯视后仰视或先平视后仰视,结果偏高;先仰视后俯视或先平视后俯视,结果偏低。
4、来自操作不当带来的误差:①滴定终点时,盛标准液的滴定管尖嘴外挂有一滴标准液的液珠未滴落析:读出来的标准液体积为实际消耗的标准液体积+ 尖嘴外挂的这滴标准液的液珠的体积,读出来的标准液体积偏大了,故结果偏高。

第 1 页 共 5 页酸碱中和滴定实验误差分析1.用已知物质的量浓度的酸(或碱)来测定未知物质的量浓度的碱(或酸)的方法叫做酸碱中和滴定。
2.酸碱中和反应的实质:H ++OH -=H 2O公式:a. n (H +)=n (OH -) b. C (H +)V (H +)=C (OH -)V (OH -)3.中和滴定过程中,容易产生误差的6个方面是:①洗涤仪器(滴定管、移液管、锥形瓶);②气泡;③体积读数(仰视、俯视):俯视刻度线,实际加水量未到刻度线,使溶液的物质的量浓度增大;仰视刻度线,实际加水量超过刻度线,使溶液的物质的量浓度减小;④指示剂选择不当;⑤杂质的影响;⑥操作(如用力过猛引起待测液外溅等)。
具体分析如下:(1)滴定前,在用蒸馏水洗涤滴定管后,未用标准液润洗。
(偏高)(2)滴定前,滴定管尖端有气泡,滴定后气泡消失。
(偏高)(3)滴定前,用待测液润洗锥形瓶。
(偏高)(4)取待测液时,移液管用蒸馏水洗涤后,未用待测液润洗。
(偏低)(5)取液时,移液管尖端的残留液吹入锥形瓶中。
(偏高)(6)读取标准液的刻度时,滴定前平视,滴定后俯视。
(偏低)(7)若用甲基橙作指示剂,最后一滴盐酸滴入使溶液由橙色变为红色。
(偏高)(8)滴定过程中,锥形瓶振荡太剧烈,有少量溶液溅出。
(偏低)(9)滴定后,滴定管尖端挂有液滴未滴入锥形瓶中。
(偏高)(10)滴定前仰视读数,滴定后平视刻度读数。
(偏低)(11)滴定过程中向锥形瓶内加入少量蒸馏水。
(无影响)(12)滴定过程中,滴定管漏液。
(偏高)(13)滴定临近终点时,用洗瓶中的蒸馏水洗下滴定管尖嘴口的半滴标准溶液至锥形瓶中。
(操作正确,无影响)(14)过早估计滴定终点。
(偏低)(15)过晚估计滴定终点。
(偏高)(16)一滴标准溶液附在锥形瓶壁上未洗下。
(偏高)(以上所指偏高偏低抑或无影响是指待测酸碱浓度)分析技巧:1.分析不当操作对公式中四个变量其中一个或多个的大小影响,2.根据公式,分析对V 标准液的影响,V 标准液比理论偏大,则待测液浓度测量值比实际值偏大,反之亦然。

1.盛标准液的滴定管用蒸馏水洗涤后未用标准液润洗。
分析:这时标准液的实际浓度变小了,所以会使其用量有所增加,导致待测液(物质的量浓度)的测定值偏大。
2.锥形瓶用蒸馏水洗涤后再用待测液润洗。
分析:这时待测液的实际总量变多了,使标准液的用量增加,导致待测液的测定值偏大。
3.盛待测液的滴定管或移液管用蒸馏水洗涤后未用待测液润洗。
分析:这时实际所取待测液的总物质的量变少了,所以会使标准液的用量减少,导致待测液的测定值偏少。
4.酸碱中和滴定。
为什么滴定前滴定管尖嘴有气泡。
结果会偏高
因为溶液会填掉气泡的体积,读数就比实际消耗的体积大。
按照读数计算的结果当然是偏高的
滴定前滴定管尖嘴有气泡滴定后尖嘴气泡消失会致使把气体也计算在体积内会使实验结果偏高
5.滴定结束滴定管尖端挂一滴液体还没滴下,为什么碱液的浓度偏大
因为我们读取酸的液体时包括滴定管尖端挂一滴液体还没滴下的这一滴,所以使得V(酸标)偏大, 所以C(碱待)偏大。
6. 酸碱中和滴定中震荡锥形瓶是部分液体溅出导致结果偏低
因为震荡时液体溅出,使得锥形瓶中的反应物减少,那么滴定所需的量就比实际的少,通过计算后结果就会偏低。
高二化学550 酸碱中和滴定误差分析例:用已知浓度的盐酸溶液滴定未知浓度的氢氧化钠溶液已知浓度溶液:标准液未知浓度溶液:待测液反应原理:计算依据:计算公式:1、仪器清洗不当引起的误差(1)盛标准液的滴定管未用标准液润洗,标准液稀释,导致V(标)增大,C(待)增大;(2)盛待测液的滴定管未用待测液润洗,待测液稀释,导致V(标)减小,C(待)减小;(3)锥形瓶用待测液润洗,使待测液溶质增多,导致V(标)增大,C(待)增大;(4)锥形瓶内有水使待测液溶质不变,导致V(标)不变,C(待)不变;2、读数不当引起的误差(1)量待测液时,先仰视,后俯视,导致V(标)增大,C(待)增大;(2)量待测液时,先俯视,后仰视,导致V(标)减小,C(待)减小;(3)标准液读数时,先仰视,后俯视导致V(标)减小,C(待)减小;(4)标准液读数时,先俯视,后仰视,导致V(标)增大,C(待)增大。
3、操作不当引起的误差(1)量待测液时,气泡未排尽,导致V(标)减小,C(待)减小;(2)量标准液时,气泡未排尽,导致V(标)增大,C(待)增大;(3)滴定过程中,待测液被振荡出锥形瓶,导致V(标)减小,C(待)减小;(4)到反应终点时,溶液变色末保持半分钟,即停止滴定,导致V(标)减小,C(待)减小;指示剂的选择选择指示剂时,一般要求变色明显(所以一般不选用石蕊),指示剂的变色范围与恰好中和时的pH要吻合。
①在酸碱中和滴定的实验中,不用石蕊作指示剂,主要原因是:石蕊的“红色→紫色”、“紫色→蓝色”的颜色变化不够明显,不利于及时、准确地作出酸碱是否恰好完全中和的判断。
②强酸强碱相互滴定,生成的盐不水解,溶液显中性,可选择酚酞或甲基橙作指示剂。
酚酞:酸滴定碱——颜色由红刚好褪色;碱滴定酸——颜色由无色到浅红色。
甲基橙:酸滴定碱——颜色由黄色到橙色;碱滴定酸——颜色由红色到橙色。
③强酸弱碱相互滴定时,由于生成强酸弱碱盐使溶液显酸性,所以应选择甲基橙作指示剂。