氨基酸性质及分类
- 格式:doc
- 大小:605.50 KB
- 文档页数:2




氨基酸的分类及功能氨基酸是构成蛋白质的基本单元,大约有20种天然氨基酸。
它们可以按照聚合方式和侧链性质进行分类。
按照聚合方式,氨基酸可以分为两类:必需氨基酸和非必需氨基酸。
必需氨基酸是人体无法合成的,必须通过饮食摄入。
共有9种必需氨基酸,包括异亮氨酸、亮氨酸、苏氨酸、色氨酸、甲硫氨酸、苏氨酸、精氨酸、缬氨酸和苯丙氨酸。
非必需氨基酸是人体可以合成的,一般来自我们的饮食,共有11种非必需氨基酸,包括丙氨酸、谷氨酸、甘氨酸、丝氨酸、组氨酸、缬氨酸、半胱氨酸、脯氨酸、酪氨酸、天冬氨酸和赖氨酸。
按照氨基酸的侧链性质,可以将氨基酸分为非极性氨基酸、极性氨基酸和带电氨基酸。
非极性氨基酸的侧链是由碳和氢组成的,不带电荷。
这类氨基酸包括甘氨酸、丙氨酸、丙基甘氨酸、异亮氨酸、亮氨酸、缬氨酸、亮缬氨酸、苏氨酸和苏缬氨酸。
极性氨基酸的侧链含有带有氧(-OH)或氨基(-NH2)的极性基团。
这类氨基酸包括苏氨酸、丝氨酸、酪氨酸、脯氨酸和色氨酸。
带电氨基酸的侧链含有带正电荷或负电荷的基团。
这类氨基酸包括天冬氨酸、谷氨酸、精氨酸、组氨酸和半胱氨酸。
每一种氨基酸都有其独特的功能和作用。
以下是一些常见氨基酸的功能:1.色氨酸:色氨酸是血清素的前体,它在神经系统中起着调节情绪、睡眠和食欲的作用。
2.蛋氨酸和胱氨酸:蛋氨酸和胱氨酸是硫氨酸的前体,它们参与胶原蛋白的结构和稳定,维持皮肤、骨骼和关节的健康。
3.谷氨酸和天冬氨酸:谷氨酸和天冬氨酸是神经递质的前体,它们在神经系统中传递兴奋信号,参与学习、注意力和记忆的过程。
4.丙氨酸和丝氨酸:丙氨酸和丝氨酸是脱氧核糖核酸(DNA)和核糖核酸(RNA)的构建单元,它们对于细胞增长和分裂至关重要。
5.缬氨酸和苏氨酸:缬氨酸和苏氨酸是肌肉合成和修复所需的重要氨基酸,对于运动员和健身者来说尤为重要。
6.赖氨酸和精氨酸:赖氨酸和精氨酸参与氨基酸代谢和尿素循环,帮助排除体内代谢废物和毒素。
总结起来,不同氨基酸在人体中具有各自独特的功能和作用,包括参与蛋白质合成、神经递质的合成、细胞生长和分裂、肌肉修复和合成等。

20种蛋白质氨基酸在结构上的差别取决于侧链基团R的不同。
通常根据R基团的化学结构或性质将20种氨基酸进行分类。
根据侧链基团的极性1、非极性氨基酸(疏水氨基酸)8种丙氨酸(Ala)缬氨酸(Val)亮氨酸(Leu)异亮氨酸(Ile)脯氨酸(Pro)苯丙氨酸(Phe)色氨酸(Trp)蛋氨酸(Met)2、极性氨基酸(亲水氨基酸):1)极性不带电荷:7种甘氨酸(Gly)丝氨酸(Ser)苏氨酸(Thr)半胱氨酸(Cys)酪氨酸(Tyr)天冬酰胺(Asn)谷氨酰胺(Gln)2)极性带正电荷的氨基酸(碱性氨基酸)3种赖氨酸(Lys)精氨酸(Arg)组氨酸(His)3)极性带负电荷的氨基酸(酸性氨基酸)2种天冬氨酸(Asp)谷氨酸(Glu)氨基酸根据化学结构1、脂肪族氨基酸:丙、缬、亮、异亮、蛋、天冬、谷、赖、精、甘、丝、苏、半胱、天冬酰胺、谷氨酰胺2、芳香族氨基酸:苯丙氨酸、酪氨酸3、杂环族氨基酸:组氨酸、色氨酸4、杂环亚氨基酸:脯氨酸从营养学的角度1、必需氨基酸(essential amino acid):指人体(或其它脊椎动物)不能合成或合成速度远不适应机体的需要,必需由食物蛋白供给,这些氨基酸称为必需氨基酸。
成人必需氨基酸的需要量约为蛋白质需要量的20%~37%。
共有8种其作用分别是:赖氨酸:促进大脑发育,是肝及胆的组成成分,能促进脂肪代谢,调节松果腺、乳腺、黄体及卵巢,防止细胞退化;色氨酸:促进胃液及胰液的产生;苯丙氨酸:参与消除肾及膀胱功能的损耗;蛋氨酸(甲硫氨酸):参与组成血红蛋白、组织与血清,有促进脾脏、胰脏及淋巴的功能;苏氨酸:有转变某些氨基酸达到平衡的功能;异亮氨酸:参与胸腺、脾脏及脑下腺的调节以及代谢;脑下腺属总司令部作用于甲状腺、性腺;亮氨酸:作用平衡异亮氨酸;缬氨酸:作用于黄体、乳腺及卵巢。
2、半必需氨基酸和条件必需氨基酸:精氨酸:精氨酸与脱氧胆酸制成的复合制剂(明诺芬)是主治梅毒、病毒性黄疸等病的有效药物。

氨基酸的性质名词解释氨基酸是构成蛋白质的基本组成部分,其中包含了许多重要的性质名词需要进行解释。
本文将详细介绍氨基酸的性质及其相关名词解释,以帮助读者更好地理解这一重要生物分子。
1. 构成氨基酸的元素氨基酸由4种元素组成:碳(C)、氢(H)、氧(O)和氮(N)。
这些元素的排列和数量的不同会导致氨基酸的种类差异。
2. 构成氨基酸的结构氨基酸的结构分为三部分:氨基基团(NH2)、羧基(COOH)和侧链(R基团)。
氨基基团和羧基通过共价键连接在同一个碳原子上,而侧链则与此碳原子连接在一起。
不同氨基酸的侧链具有不同的性质和功能。
3. 构成氨基酸的胺基酸氨基酸中的氨基基团是由一个氮原子和三个氢原子组成的胺基酸。
胺基酸是组成蛋白质的重要成分,也是合成其他重要生物分子的基础。
4. 构成氨基酸的羧基氨基酸中的羧基是一个碳原子与一个氧原子和一个羟基(OH)相连接的羧酸。
羧基通过脱去一个氧和一个氢原子,形成羧酸根离子,从而使氨基酸以阴离子的形式存在。
5. 构成氨基酸的侧链氨基酸的侧链是与氨基基团和羧基连接在一起的部分。
不同氨基酸的侧链具有不同的大小、形状和化学性质,因此决定了氨基酸的性质和功能。
例如,赖氨酸的侧链富含氨基基团,而苏氨酸的侧链则含有羟基。
6. 构成氨基酸的官能团氨基酸的官能团是指氨基基团和羧基的化学活性部分。
氨基基团具有碱性,而羧基则具有酸性。
它们的共存使得氨基酸在生物体内可以发挥重要的生理功能。
7. 构成氨基酸的立体异构体氨基酸可以存在多种立体异构体,具体取决于氨基基团和羧基的空间排布。
其中最常见的是L型和D型氨基酸。
在自然界中,绝大多数氨基酸都是以L型存在,而D型氨基酸主要存在于细菌和某些植物中。
8. 构成氨基酸的化学性质氨基酸的化学性质主要体现在其官能团的反应性上。
例如,它们可以通过与其他分子发生酯化、酰化、酰胺化等反应形成新的化合物。
此外,氨基酸还可以参与氧化还原、加成和消除等反应。
9. 构成氨基酸的生理功能氨基酸不仅是蛋白质的构成单元,还具有许多重要的生理功能。

氨基酸的分类特点和理化性质氨基酸是构成蛋白质的基本单位,具有多种功能和作用。
根据它们的理化性质和分类特点,氨基酸可以分为非极性氨基酸、极性氨基酸和特殊氨基酸。
1.非极性氨基酸:非极性氨基酸的中心原子由一个氨基基团(NH2)、一个羧基(COOH)、一个氢原子(H)和一个碳原子(C)组成。
这类氨基酸的侧链由多种有机基团组成,不带任何阳离子或阴离子功能性团。
它们通常不溶于水,但溶于有机溶剂。
在生物体内,非极性氨基酸主要负责蛋白质的折叠和稳定。
在非极性氨基酸中,最简单的是甘氨酸、丙氨酸和异亮氨酸等。
这些氨基酸的侧链中带有碳和氢原子,由于不带电荷,属于非极性,因此有亲水性较强。
2.极性氨基酸:这类氨基酸的侧链通常包含含氧或氮等具有强电负性的原子,可以形成氢键、离子键等。
大多数极性氨基酸具有亲水性,能与水进行相互作用,因此溶解度较高。
极性氨基酸可以进一步分为酸性和碱性氨基酸。
-酸性氨基酸:这类氨基酸的侧链含有羟基和羧基,具有负电荷。
代表性的酸性氨基酸有天冬氨酸和谷氨酸等。
这些氨基酸在水溶液中具有酸性,能够释放出负电荷的氢离子,与基性氨基酸发生中和反应。
-碱性氨基酸:这类氨基酸的侧链含有氨基和胺基等功能性团,在水溶液中带正电荷。
代表性的碱性氨基酸有赖氨酸和精氨酸等。
这些氨基酸能够接受负电荷的氢离子,与酸性氨基酸发生中和反应。
3.特殊氨基酸:这是一类在生物体中含量较少,具有特殊功能和结构的氨基酸。
代表性的特殊氨基酸有脯氨酸、半胱氨酸、甲硫氨酸等。
这些氨基酸的结构中具有额外的官能团,能够参与特殊的生化反应和代谢途径。
总的来说,氨基酸的分类特点主要根据其理化性质和功能特点来区分。
非极性氨基酸主要由碳和氢原子组成,溶解度较低,主要负责蛋白质的结构稳定;极性氨基酸具有亲水性,溶解度较高,包括酸性和碱性两种,具有酸碱中和的作用;特殊氨基酸则具有特殊的结构和功能,用于特定的生化反应和代谢途径。
这些特征使得氨基酸能够在生物体内进行多种功能的发挥,并形成复杂的蛋白质结构。
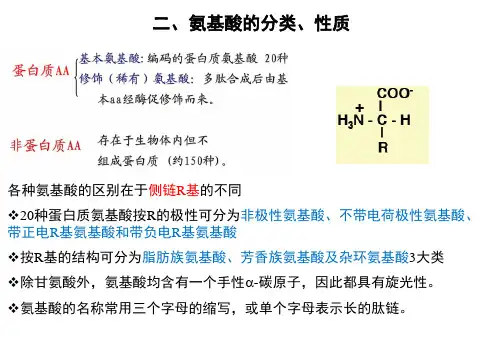

氨基酸分子结构通式氨基酸分子结构通式为RCHNH2COOH。
氨基酸是构成动物营养所需蛋白质的基本物质。
是含有碱性氨基和酸性羧基的有机化合物。
氨基连在α-碳上的为α-氨基酸。
组成蛋白质的氨基酸大部分为α-氨基酸。
氨基酸,是羧酸碳原子上的氢原子被氨基取代后的化合物,氨基酸分子中含有氨基和羧基两种官能团。
与羟基酸类似,氨基酸可按照氨基连在碳链上的不同位置而分为α-,β-,γ-...w-氨基酸,但经蛋白质水解后得到的氨基酸都是α-氨基酸,而且仅有二十几种,他们是构成蛋白质的基本单位。
氨基酸分子结构通式为RCHNH2COOH。
氨基酸在人体内通过代谢可以发挥下列一些作用:①合成组织蛋白质;②变成酸、激素、抗体、肌酸等含氨物质;③转变为碳水化合物和脂肪;④氧化成二氧化碳和水及尿素,产生能量。
蛋白质的基本单位是氨基酸。
如果人体缺乏任何一种必需氨基酸,就可导致生理功能异常,影响机体代谢的正常进行,最后导致疾病。
即使缺乏某些非必需氨基酸,会产生机体代谢障碍。
氨基酸的结构:氨基酸是羧酸分子烃基上的氢原子被氨基取代的化合物。
组成蛋白质的氢基酸几乎都是α一氨基酸,其结构简式为如甘氨酸(氨基乙酸):丙氨酸(α一氨基丙酸):谷氨酸(2一氨基一1,5一戊二酸):氨基酸的性质:物理性质天然的氨基酸均为无色晶体,熔点较高,在200~ 300℃熔化时分解。
它们能溶于强酸或强碱溶液,除少数外一般都能溶于水,而难溶于乙醇、乙醚。
(2)化学性质a.氨基酸的两性氨基酸分子中一COOH是酸性基团,一NH2是碱性基因。
因此,氨基酸是两性化合物,它既可以与酸反应,也可以与碱反应,且都生成盐。
b.成肽反应两个氨基酸分子(可以相同,也可以不同),在酸或碱的存在下加热,通过一分子的氨基与另一分子的羧基问脱去一分子水,缩合形成含有肽踺的化合物,称为成肽反应。
由两个氨基酸分子脱水后形成的含有肽键的化合物称为二肽。
二肽还可以继续与其他氨基酸分子脱水生成三肽、四肽、五肽以至生成长链的多肽。

氨基酸分类引言氨基酸是组成蛋白质的基本单位,具有重要的生化功能。
根据其化学结构和生理性质的不同,氨基酸可以被分为不同的类别。
本文将对氨基酸的分类进行介绍和讨论。
一、根据结构分类1. 构成氨基酸分类的氨基酸和非氨基酸氨基酸可分为两类:构成氨基酸和非构成氨基酸。
构成氨基酸是指由氨基和羧基以及与它们共价结合的 R 基团组成的化合物。
非构成氨基酸则是不具备上述结构的化合物,但其具有与氨基酸类似的生化性质。
2. 构成氨基酸的分类构成氨基酸可以进一步分为三类:脂肪族氨基酸、芳香族氨基酸和含硫氨基酸。
•脂肪族氨基酸:这类氨基酸具有不饱和脂肪酸的特点,例如甘氨酸、丙氨酸等。
•芳香族氨基酸:这类氨基酸包含苯环结构,并且具有特别的性质。
典型的芳香族氨基酸有苯丙氨酸、酪氨酸等。
•含硫氨基酸:这类氨基酸含有硫原子,对于蛋白质的空间结构具有重要的贡献。
典型的含硫氨基酸有蛋氨酸、半胱氨酸等。
二、根据功能分类1. 必需氨基酸和非必需氨基酸根据人体是否能够自身合成来分类,氨基酸可以分为必需氨基酸和非必需氨基酸。
•必需氨基酸:人体无法自身合成,必须通过食物摄入。
例如赖氨酸、异亮氨酸等。
•非必需氨基酸:人体可以自身合成,因此不需要通过食物摄入。
例如丙氨酸、谷氨酸等。
2. 生物活性氨基酸生物活性氨基酸是指具有特定生化功能的氨基酸,它们在人体内参与多种重要的生化反应和代谢过程。
•谷氨酸和天冬酰氨酸:是神经递质的前体,在神经递质合成中起重要作用。
•色氨酸:是色素合成的前体,同时也是神经递质血清素的前体。
•脯氨酸:参与蛋白质的合成过程,并能够稳定细胞膜的结构。
•酪氨酸:参与黑色素的合成,对皮肤、毛发的色素形成有重要影响。
三、根据氨基酸的代谢途径分类1. 转氨基酸和非转氨基酸根据氨基酸是否可以转化为其他氨基酸,可以将氨基酸分为转氨基酸和非转氨基酸。
•转氨基酸:可以在生物体内发生氨基转移反应,出现不同氨基酸之间的转化。
例如谷氨酸和丙氨酸之间的转氨酶反应。

编辑词条氨基酸百科名片氨基酸(amino acid):含有氨基和羧基的一类有机化合物的通称。
生物功能大分子蛋白质的基本组成单位,是构成动物营养所需蛋白质的基本物质。
是含有一个碱性氨基和一个酸性羧基的有机化合物。
氨基连在α-碳上的为α-氨基酸。
天然氨基酸均为α-氨基酸。
目录[隐藏]氨基酸的结构通式氨基酸的分类氨基酸的检测氨基酸的功能氨基酸合成氨基酸所对应的密码子表氨基酸胶囊氨基酸的结构通式氨基酸的分类氨基酸的检测氨基酸的功能氨基酸合成氨基酸所对应的密码子表氨基酸胶囊amino acid (abbr.aa)[编辑本段]氨基酸的结构通式α-氨基酸的结构通式:(R是可变基团)构成蛋白质的氨基酸都是一类含有羧基并在与羧基相连的碳原子下连有氨基的有机化合物,目前自然界中尚未发现蛋白质中有氨基和羧基不连在同一个碳原子上的氨基酸。
[编辑本段]氨基酸的分类天然的氨基酸现已经发现的有300多种,其中人体所需的氨基酸约有22种,分非必需氨基酸和必需氨基酸(人体无法自身合成)。
另有酸性、碱性、中性、杂环分类,是根据其化学性质分类的。
1、必需氨基酸(essential amino acid):指人体(或其它脊椎动物)不能合成或合成速度远不适应机体的需要,必需由食物蛋白供给,这些氨基酸称为必需氨基酸。
共有10种其作用分别是:①赖氨酸(Lysine ):促进大脑发育,是肝及胆的组成成分,能促进脂肪代谢,调节松果腺、乳腺、黄体及卵巢,防止细胞退化;②色氨酸(Tryptophan):促进胃液及胰液的产生;③苯丙氨酸(Phenylalanine):参与消除肾及膀胱功能的损耗;④蛋氨酸(又叫甲硫氨酸)(Methionine);参与组成血红蛋白、组织与血清,有促进脾脏、胰脏及淋巴的功能;⑤苏氨酸(Threonine):有转变某些氨基酸达到平衡的功能;⑥异亮氨酸(Isoleucine ):参与胸腺、脾脏及脑下腺的调节以及代谢;脑下腺属总司令部作用于甲状腺、性腺;⑦亮氨酸(Leucine ):作用平衡异亮氨酸;⑧缬氨酸(Valine):作用于黄体、乳腺及卵巢。
各种物质详细介绍1、精氨酸营养成:精氨酸是一种α氨基酸,亦是20种普遍的自然氨基酸之一。
天然精氨酸为L-型,从水中结晶的产物含两分子结晶水,在乙醇中结晶的是无水物。
由于胍基的存在,精氨酸呈碱性,易与酸反应形成盐。
精氨酸是由瓜氨酸透过胞质酵素精氨基琥珀酸合成酶(ASS)及精氨基琥珀酸裂解酶(ASL)合成。
这个过程所要求较大的能量,这是因为要将每一个分子合成精氨基需要将三磷酸腺苷(A TP)水解成一磷酸腺苷(AMP),即两个三磷酸腺苷当量。
作用:1、细胞分裂2、伤口复原3、排出氨4、免疫功能5、分泌激素副作用:精氨酸是一种可以在体内自然产生的必需氨基酸。
通过营养补充剂摄入有可能带来一定副作用,如导致呼吸急促,瘙痒,湿疹,恶心和胃痛,血液化学品改变等过敏反应等。
此外,存在肝脏和肾脏疾病的人也容易出现不良反应。
但大多数人对精氨酸保健品反应良好,只有少数人在持续使用几个月后会出现明显副作用。
过敏反应是最常见的精氨酸副作用。
尽管任何形式的营养品都有可能出现这类问题,但注射液形式最常见。
如果发现过敏症状,应立即停止使用这种保健品。
左旋精氨酸作为一种常见的氨基酸保健品形式还可能引起其他一些副作用,如恶心,腹部痉挛,胃痛和大便增加等。
哮喘患者如果吸入还有可能引起更严重副作用。
有些人甚至还会痛风发作。
一些人可能在注射左旋精氨酸时会出现面部潮红,头痛和腰痛等严重症状。
有些人甚至还会出现不宁腿和静脉刺激,甚至造成注射点周围组织死亡。
肝脏或肾脏有疾病的人可能出现的精氨酸副作用更严重。
因此,应该在医生监督下谨慎使用这类产品。
存在糖尿病或血糖问题的患者同样容易在服用精氨酸后出现不良反应,因为这种营养品会导致一些人的血糖水平提高。
如果正在服用控制血糖药物,就会带来危险。
如果发现精氨酸的副作用很严重或不断恶化,最好是马上看医生。
总之,任何人都应该遵照使用说明补充这种营养品,尽量避免不必要的副作用。
2、瓜氨酸营养成分:是一种α氨基酸,名字是由首先抽取出瓜氨酸的西瓜而来。
第一章氨基酸(amino acid)的结构与性质第一节氨基酸的结构与分类一、氨基酸的结构组成蛋白质的基本单位是氨基酸。
如将天然的蛋白质完全水解,最后都可得到约二十种不同的氨基酸。
从氨基酸的结构通式可以看出:构成蛋白质的氨基酸均为L—α—氨基酸。
除R 为H(甘氨酸)外,其余氨基酸均具有旋光性。
*在空间各原子有两种排列方式:L—构型与D—构型,它们的关系就像左右手的关系,互为镜像关系,下图以丙氨酸为例:二、氨基酸的分类:1.按氨基酸分子中羧基与氨基的数目分:酸性氨基酸:一氨基二羧基氨基酸,有天冬氨酸、谷氨酸;碱性氨基酸:二氨基一羧基氨基酸,有赖氨酸、精氨酸、组氨酸;中性氨基酸:一氨基一羧基氨基酸,有甘氨酸、丙氨酸、缬氨酸、亮氨酸、异亮氨酸、甲硫氨酸、半胱氨酸、苯丙氨酸、色氨酸、酪氨酸、脯氨酸、天冬酰胺、谷氨酰胺、丝氨酸、苏氨酸。
2.按侧基R 基的结构特点分:脂肪族氨基酸芳香族氨基酸:苯丙氨酸、色氨酸、酪氨酸杂环氨基酸:脯氨酸、组氨酸3.按侧基R 基与水的关系分:非极性氨基酸:有甘氨酸、丙氨酸、缬氨酸、亮氨酸、异亮氨酸、甲硫氨酸、半胱氨酸、苯丙氨酸、色氨酸、酪氨酸、脯氨酸;极性不带电氨基酸:天冬酰胺、谷氨酰胺、丝氨酸、苏氨酸;极性带电氨基酸:天冬氨酸、谷氨酸、赖氨酸、精氨酸、组氨酸。
4. 按氨基酸是否能在人体内合成分:必需氨基酸:指人体内不能合成的氨基酸,必须从食物中摄取,有八种:赖氨酸、色氨酸、甲硫氨酸、笨丙氨酸、缬氨酸、亮氨酸、异亮氨酸、苏氨酸。
非必需氨基酸:指人体内可以合成的氨基酸。
有十种。
半必需氨基酸:指人体内可以合成但合成量不能满足人体需要(特别是婴幼儿时期)的氨基酸,有两种:组氨酸、精氨酸。
三、稀有氨基酸:参加天然蛋白质分子组成的氨基酸,除了上述20 种有遗传密码的基本氨基酸之外,在少数蛋白质分子中还有一些不常见的氨基酸,称为稀有氨基酸。
它们都是在蛋白质分子合成之后,由相应的常见氨基酸分子经酶促化学修饰而成的衍生物。
氨基酸的亚基名词解释氨基酸是构成蛋白质的基本单元,它们在细胞和生物体中发挥着重要的功能。
而了解氨基酸的亚基名词解释将有助于我们更好地理解其作用和重要性。
一、氨基酸的基本结构和分类氨基酸是一种由氨基(NH2)和羧基(COOH)组成的有机分子,它们通常由一个中心碳原子连接着一个氢原子、一个氨基基团、一个羧基基团和一个侧链基团。
氨基和羧基分别赋予了氨基酸氨基酸化学性质中最重要的两个特性:氨基酸能够在酸中释放出质子,羧基能够在碱中接受质子。
根据氨基酸的侧链基团,它们可以被分为20种不同的类型。
二、极性和非极性氨基酸氨基酸的侧链基团决定了其极性或非极性。
极性氨基酸具有带电的侧链基团,如羟基(-OH)、胺基(-NH2)和羧基(-COOH)。
这些带电的功能团使得极性氨基酸在水中具有较高的溶解性,并且可以与其他带电物质相互作用。
相反,非极性氨基酸的侧链基团主要是烃基,如甲基(-CH3)和苯基(-C6H5)。
它们在无极性溶剂中溶解度较高,但在水中溶解度较低。
三、天然和非天然氨基酸天然氨基酸是指在自然界中普遍存在的氨基酸,它们是生命体内蛋白质的构建基石。
天然氨基酸由细胞内的酶合成,并参与各种生物过程。
与此相反,非天然氨基酸是通过人工合成或工程改造而产生的,它们具有特殊的性质和功能。
非天然氨基酸的引入扩展了氨基酸的化学空间,可以通过改变侧链基团来调控蛋白质的稳定性、活性和特异性。
四、必需和非必需氨基酸必需氨基酸是机体无法自主合成的氨基酸,它们必须通过日常饮食中的摄入来满足我们的需求。
共有9种氨基酸被认为是人类体内的必需氨基酸。
非必需氨基酸则是机体可以自主合成的氨基酸,因此不需要从食物中获取。
虽然非必需氨基酸不被视为必需的人类营养素,但它们仍然对正常的生物过程和蛋白质合成起着至关重要的作用。
五、重要氨基酸及其功能每种氨基酸都具有特定的功能和在生物体中的重要作用。
例如,赖氨酸是一种重要的氨基酸,它参与胆碱和肌氨酸的合成。
20种氨基酸的疏水参数见下面:Arg(R)-4.5
Lys(K)-3.9
Asn(N)-3.5
Asp(D)-3.5
Gln(Q)-3.5
Glu(E)-3.5
His(H)-3.2
Pro(P)-1.6
Tyr(Y)-1.3
Trp(W)-0.9
Ser(S)-0.8
Thr(T)-0.7
Gly(G)-0.4
Ala(A)1.8
Met(M)1.9
Cys(C)2.5
Phe(F)2.8
Leu(L)3.8
Val(V)4.2
Ile(I)4.5
疏水性与氨基酸的侧链有关,AA可分为脂肪族,芳香族,极性带电荷和极性不带电荷四种。
前两种非极性,疏水性强;后两种极性还可能形成氢键,亲水;
20种氨基酸的分类
1、非极性氨基酸
包括:甘氨酸、丙氨酸、缬氨酸、亮氨酸、异亮氨酸、苯丙氨酸、脯氨酸2、极性氨基酸
极性中性氨基酸:色氨酸、酪氨酸、丝氨酸、半胱氨酸、蛋氨酸、天冬酰胺、谷氨酰胺、苏氨酸
酸性氨基酸:天冬氨酸、谷氨酸
碱性氨基酸:赖氨酸、精氨酸、组氨酸
其中:属于芳香族氨基酸的是:色氨酸、酪氨酸、苯丙氨酸属于亚氨基酸的是:脯氨酸
含硫氨基酸包括:半胱氨酸、蛋氨酸
注意:在识记时可以只记第一个字,如碱性氨基酸包括:赖精组。