氨基酸的分类特点及理化性质
- 格式:ppt
- 大小:2.07 MB
- 文档页数:91

第一章氨基酸(amino acid)的结构与性质•蛋白质(protein)是一类重要的生物大分子,是生命的物质基础。
分子中主要的元素组成是:C、H、O、N、S等。
其中N元素的含量相对稳定,约为16%,故每克氮相当于6.25克蛋白质。
•蛋白质的基本组成单位---氨基酸第一节氨基酸的结构与分类一、氨基酸的结构组成蛋白质的基本单位是氨基酸。
如将天然的蛋白质完全水解,最后都可得到约二十种不同的氨基酸。
从氨基酸的结构通式可以看出:◆构成蛋白质的氨基酸均为L—α—氨基酸。
◆除R为H(甘氨酸)外,其余氨基酸均具有旋光性。
L-α-氨基酸的结构通式COOH│H2N —C —H│R*在空间各原子有两种排列方式:L——构型与D——构型,它们的关系就像左右手的关系,互为镜像关系,下图以丙氨酸为例:二、氨基酸的分类:1.按氨基酸分子中羧基与氨基的数目分:酸性氨基酸:一氨基二羧基氨基酸,有天冬氨酸、谷氨酸;碱性氨基酸:二氨基一羧基氨基酸,有赖氨酸、精氨酸、组氨酸;中性氨基酸:一氨基一羧基氨基酸,有甘氨酸、丙氨酸、缬氨酸、亮氨酸、异亮氨酸、甲硫氨酸、半胱氨酸、苯丙氨酸、色氨酸、酪氨酸、脯氨酸、天冬酰胺、谷氨酰胺、丝氨酸、苏氨酸。
2.按侧基R基的结构特点分:脂肪族氨基酸芳香族氨基酸:苯丙氨酸、色氨酸、酪氨酸 杂环氨基酸:脯氨酸、组氨酸3.按侧基R基与水的关系分:非极性氨基酸:有甘氨酸、丙氨酸、缬氨酸、亮氨酸、异亮氨酸、甲硫氨酸、半胱氨酸、苯丙氨酸、色氨酸、酪氨酸、脯氨酸;极性不带电氨基酸:天冬酰胺、谷氨酰胺、丝氨酸、苏氨酸;极性带电氨基酸:天冬氨酸、谷氨酸、赖氨酸、精氨酸、组氨酸。
4. 按氨基酸是否能在人体内合成分: 必需氨基酸:指人体内不能合成的氨基酸,必须从食物中摄取,有八种:赖氨酸、色氨酸、甲硫氨酸、苯丙氨酸、缬氨酸、亮氨酸、异亮氨酸、苏氨酸。
非必需氨基酸:指人体内可以合成的氨基酸。
有十种。
半必需氨基酸:指人体内可以合成但合成量不能满足人体需要(特别是婴幼儿时期)的氨基酸,有两种:组氨酸、精氨酸。




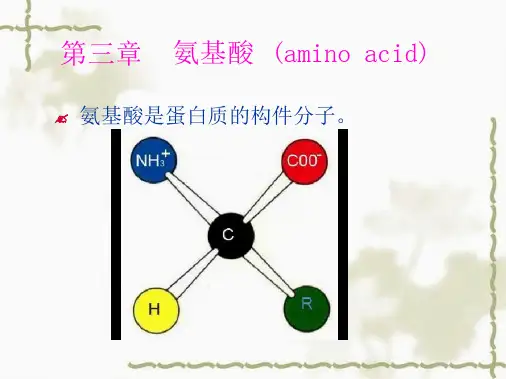

氨基酸的分类特点和理化性质氨基酸是构成蛋白质的基本单位,具有多种功能和作用。
根据它们的理化性质和分类特点,氨基酸可以分为非极性氨基酸、极性氨基酸和特殊氨基酸。
1.非极性氨基酸:非极性氨基酸的中心原子由一个氨基基团(NH2)、一个羧基(COOH)、一个氢原子(H)和一个碳原子(C)组成。
这类氨基酸的侧链由多种有机基团组成,不带任何阳离子或阴离子功能性团。
它们通常不溶于水,但溶于有机溶剂。
在生物体内,非极性氨基酸主要负责蛋白质的折叠和稳定。
在非极性氨基酸中,最简单的是甘氨酸、丙氨酸和异亮氨酸等。
这些氨基酸的侧链中带有碳和氢原子,由于不带电荷,属于非极性,因此有亲水性较强。
2.极性氨基酸:这类氨基酸的侧链通常包含含氧或氮等具有强电负性的原子,可以形成氢键、离子键等。
大多数极性氨基酸具有亲水性,能与水进行相互作用,因此溶解度较高。
极性氨基酸可以进一步分为酸性和碱性氨基酸。
-酸性氨基酸:这类氨基酸的侧链含有羟基和羧基,具有负电荷。
代表性的酸性氨基酸有天冬氨酸和谷氨酸等。
这些氨基酸在水溶液中具有酸性,能够释放出负电荷的氢离子,与基性氨基酸发生中和反应。
-碱性氨基酸:这类氨基酸的侧链含有氨基和胺基等功能性团,在水溶液中带正电荷。
代表性的碱性氨基酸有赖氨酸和精氨酸等。
这些氨基酸能够接受负电荷的氢离子,与酸性氨基酸发生中和反应。
3.特殊氨基酸:这是一类在生物体中含量较少,具有特殊功能和结构的氨基酸。
代表性的特殊氨基酸有脯氨酸、半胱氨酸、甲硫氨酸等。
这些氨基酸的结构中具有额外的官能团,能够参与特殊的生化反应和代谢途径。
总的来说,氨基酸的分类特点主要根据其理化性质和功能特点来区分。
非极性氨基酸主要由碳和氢原子组成,溶解度较低,主要负责蛋白质的结构稳定;极性氨基酸具有亲水性,溶解度较高,包括酸性和碱性两种,具有酸碱中和的作用;特殊氨基酸则具有特殊的结构和功能,用于特定的生化反应和代谢途径。
这些特征使得氨基酸能够在生物体内进行多种功能的发挥,并形成复杂的蛋白质结构。

蛋白质氨基酸共有的理化性质氨基酸是有机化学中的一类结构相对简单的有机化合物,是生物体具有高度组成和功能的重要的组成单位。
氨基酸的分子中包含一个氨基(乙胺基)和一个酸基(羧基),至少包含C、H、O、N 四种化学元素,以脱水缩合方式联接,以-CO-NH-结构连接在一起,因此氨基酸又被称为“二元碱型”。
根据氨基酸的最终加成体,氨基酸可以分为四类:α-酰胺型氨基酸、γ-胺基酸、内酰胺型氨基酸和醛胺型氨基酸。
氨基酸含有一个醇类基团(-HCH2R),是一种典型的碱性氨基,具有较强的核碱反应性质;一个酸类基团(-COOH),具有较强的酸性,可以参与酸基反应;一个酰胺基团(-CO-NH2),可以参与水解、脱水缩合、氨基缩合等反应;一个连接二氧基(-C=O),可形成共价键,是大分子在线缆和蛋白质等生物大分子结构的重要构成部分。
氨基酸的分子结构和分子量,严格来说,其理化性质差别较大:在常温常压下,氨基酸的熔点差异也较大,如γ-氨基丙酸的熔点为172℃,苯丙氨酸的为267℃,而丙二酸的熔点却只有85℃;折射率差异也较大,如右旋糖胺酸的折射率只有1.541,苯兰氨酸的折射率却高达1.641;氨基酸盐的溶解度差别较大,如γ-氨基丙酸钠的溶解度,在0℃下为214g/100ml,而甲基羟基脯氨酸钠在0℃下的溶解度仅为0.15g/100ml;氨基酸的碱度,离子均衡常数和酸度,也有一定差异;氨基酸的质荷比也有较大差异,如精氨酸的质荷比为-0.77,而去氧多巴的质荷比为-1.1等。
通过氨基酸的对比可以发现,同类氨基酸的理化性质具有一定的相似性,它们的分子量和分子式有一定的相似性,比较类似的氨基酸的折射率、熔点等特征也很接近,具有一定的重要性和系统性,可以说是一种有效性的划分。
在生物体中,氨基酸是蛋白质构成的基础,因此不同的氨基酸对它具有重要的作用,通过彼此之间的复合、折叠、加工等,可以组成不同的分子和不同的空间结构,使得蛋白质的形态更加的复杂和丰富,从而发挥出不同的生物学功能,一般来讲,氨基酸的变化越多,蛋白质的功能越丰富、越精确。
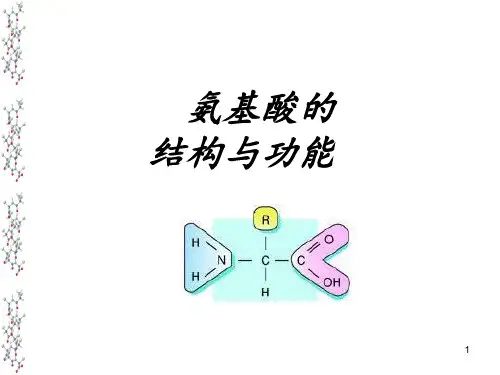

第一章氨基酸(amino acid)的结构与性质第一节氨基酸的结构与分类一、氨基酸的结构组成蛋白质的基本单位是氨基酸。
如将天然的蛋白质完全水解,最后都可得到约二十种不同的氨基酸。
从氨基酸的结构通式可以看出:构成蛋白质的氨基酸均为L—α—氨基酸。
除R 为H(甘氨酸)外,其余氨基酸均具有旋光性。
*在空间各原子有两种排列方式:L—构型与D—构型,它们的关系就像左右手的关系,互为镜像关系,下图以丙氨酸为例:二、氨基酸的分类:1.按氨基酸分子中羧基与氨基的数目分:酸性氨基酸:一氨基二羧基氨基酸,有天冬氨酸、谷氨酸;碱性氨基酸:二氨基一羧基氨基酸,有赖氨酸、精氨酸、组氨酸;中性氨基酸:一氨基一羧基氨基酸,有甘氨酸、丙氨酸、缬氨酸、亮氨酸、异亮氨酸、甲硫氨酸、半胱氨酸、苯丙氨酸、色氨酸、酪氨酸、脯氨酸、天冬酰胺、谷氨酰胺、丝氨酸、苏氨酸。
2.按侧基R 基的结构特点分:脂肪族氨基酸芳香族氨基酸:苯丙氨酸、色氨酸、酪氨酸杂环氨基酸:脯氨酸、组氨酸3.按侧基R 基与水的关系分:非极性氨基酸:有甘氨酸、丙氨酸、缬氨酸、亮氨酸、异亮氨酸、甲硫氨酸、半胱氨酸、苯丙氨酸、色氨酸、酪氨酸、脯氨酸;极性不带电氨基酸:天冬酰胺、谷氨酰胺、丝氨酸、苏氨酸;极性带电氨基酸:天冬氨酸、谷氨酸、赖氨酸、精氨酸、组氨酸。
4. 按氨基酸是否能在人体内合成分:必需氨基酸:指人体内不能合成的氨基酸,必须从食物中摄取,有八种:赖氨酸、色氨酸、甲硫氨酸、笨丙氨酸、缬氨酸、亮氨酸、异亮氨酸、苏氨酸。
非必需氨基酸:指人体内可以合成的氨基酸。
有十种。
半必需氨基酸:指人体内可以合成但合成量不能满足人体需要(特别是婴幼儿时期)的氨基酸,有两种:组氨酸、精氨酸。
三、稀有氨基酸:参加天然蛋白质分子组成的氨基酸,除了上述20 种有遗传密码的基本氨基酸之外,在少数蛋白质分子中还有一些不常见的氨基酸,称为稀有氨基酸。
它们都是在蛋白质分子合成之后,由相应的常见氨基酸分子经酶促化学修饰而成的衍生物。
↓氨基酸侧链的结构、理化性质特点和分类。
(1)结构:氨基酸是指含有氨基的羧酸。
生物体内的各种蛋白质是由20种基本氨基酸构成的。
除甘氨酸外均为L-α-氨基酸其中(脯氨酸是一种L-α-亚氨基酸)。
除甘氨酸外,其它蛋白质氨基酸的α-碳原子均为不对称碳原子(即与α-碳原子键合的四个取代基各不相同),因此氨基酸可以有立体异构体,即可以有不同的构型(D-型与L-型两种构型)。
(2)理化性质特点:a、两性解离及等电点(PI):pH<pI,阳离子;pH=pI,氨基酸的兼性离子呈电中性;pH>pI,阴离子b、紫外吸收,色氨酸、酪氨酸的最大吸收峰在 280 nm 附近。
(3)分类:非极性脂肪族氨基酸;极性中性氨基酸;芳香族氨基酸;酸性氨基酸;碱性氨基酸。
↓蛋白质一级结构、空间分子结构概念和特点;蛋白质的理化性质(1)一级结构:蛋白质多肽链中氨基酸的排列顺序,是蛋白质空间构象和特异生物学功能的基础。
主要的化学键为肽键、二硫键。
二级结构:蛋白质分子中某一段肽链的局部空间结构,即该段肽链主链骨架原子的相对空间位置,并不涉及氨基酸残基侧链的构象。
主要的化学键为氢键。
有α-螺、β-折、β-转角、无规则卷曲。
三级结构:整条肽链中全部氨基酸残基的相对空间位置。
即肽链中所有原子在三维空间的排布位置。
主要的化学键为疏水键、离子键、氢键和 Van der Waals力等。
大分子蛋白质的三级结构常可分割成一个或数个球状或纤维状的区域,折叠得较为紧密,具有一定功能作用的局部区域即结构域,结构域是蛋白质的活性部位。
四级结构:含有二条或多条多肽链的蛋白质分子中,每一条具有完整三级结构的多肽链。
蛋白质分子中各亚基的空间排布及亚基接触部位的布局和相互作用。
(2)蛋白质的理化性质:a、两性电离当蛋白质溶液处于某一pH时,蛋白质解离成正、负离子的趋势相等,即成为兼性离子,净电荷为零,此时溶液的pH称为蛋白质的等电点(PI)。
b、胶体性质分子量自1万至100万,直径可达1~100nm,为胶粒范围之内。
定义:氨基酸(amino acid):是含有一个碱性氨基和一个酸性羧基的有机化合物,氨基一般连在α-碳上。
氨基酸的结构通式是生物功能大分子蛋白质的基本组成单位。
分类:必需氨基酸(essential amino acid):指人(或其它脊椎动物)(赖氨酸,苏氨酸等)自己不能合成,需要从食物中获得的氨基酸。
非必需氨基酸(nonessential amino acid):指人(或其它脊椎动物)自己能由简单的前体合成,不需要从食物中获得的氨基酸。
另有酸性、碱性、中性、杂环分类,是根据其化学性质分类的。
检测:茚三酮反应(ninhydrin reaction):在加热条件下,氨基酸或肽与茚三酮反应生成紫色(与脯氨酸反应生成黄色)化合物的反应。
蛋白质:肽键(peptide bond):一个氨基酸的羧基与另一个的氨基的氨基缩合,除去一分子水形成的酰氨键。
肽(peptide):两个或两个以上氨基通过肽键共价连接形成的聚合物。
是氨基酸通过肽键相连的化合物,蛋白质不完全水解的产物也是肽。
肽按其组成的氨基酸数目为2个、3个和4个等不同而分别称为二肽、三肽和四肽等,一般含10个以下氨基酸组成的称寡肽(oligopeptide),由10个以上氨基酸组成的称多肽(polypeptide),它们都简称为肽。
肽链中的氨基酸已不是游离的氨基酸分子,因为其氨基和羧基在生成肽键中都被结合掉了,因此多肽和蛋白质分子中的氨基酸均称为氨基酸残基(amino acid residue)。
多肽有开链肽和环状肽。
在人体内主要是开链肽。
开链肽具有一个游离的氨基末端和一个游离的羧基末端,分别保留有游离的α-氨基和α-羧基,故又称为多肽链的N端(氨基端)和C端(羧基端),书写时一般将N端写在分子的左边,并用(H)表示,并以此开始对多肽分子中的氨基酸残基依次编号,而将肽链的C端写在分子的右边,并用(OH)来表示。
目前已有约20万种多肽和蛋白质分子中的肽段的氨基酸组成和排列顺序被测定了出来,其中不少是与医学关系密切的多肽,分别具有重要的生理功能或药理作用。