共轭分子与HMO法
- 格式:ppt
- 大小:4.92 MB
- 文档页数:40
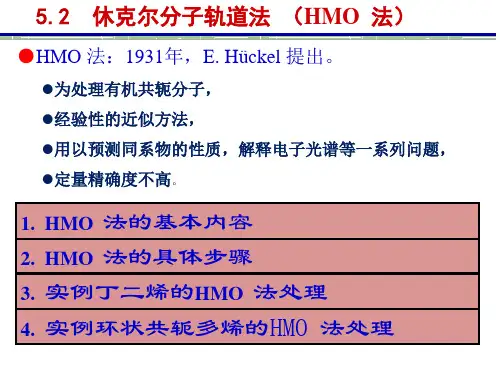

HMO理论的一些粗浅理解休克尔分子轨道法(Hückel molecular orbital method)是用简化的近似分子轨道模型处理共轭分子中的π 电子的方法,1931年由E.休克尔(E. Hückel)提出,简称HMO。
这是一种最简单的分子轨道理论,在有机化学中应用得相当广泛,用以解决共轭分子的结构,探讨分子的性质和反应性能的半经验方法。
HMO法的基本内容:1、承认分子轨道理论的全部内容(1)将分子中每一个电子的运动,看作是在各原子核和其余电子的平均势场中运动(即单电子近似),其单电子的空间波函数为分子轨道;(2)分子轨道采用原子轨道的线性组合,用变分法得到分子轨道和能级;(3)分子轨道内电子排布符合能量最低原理、保里原理和洪特规则;组成分子轨道的原子轨道必须符合能量相近、最大重叠和对称性匹配这三个条件。
2、用HMO法处理共轭分子结构的假设(1)由于π电子在核和σ键所形成的整个分子骨架中运动,可将σ键和π键分开处理。
(2)共轭分子有相对不变的σ骨架,而π电子的状态决定分子的性质。
(3)各个碳原子上p轨道的库仑积分都相同,都等于α,相邻原子轨道间的交换积分都相等,用β表示,而非相邻原子轨道间的交换积分都等于零;不同原子轨道间的重叠积分为零;3、共轭烯烃久期行列式的规律全部由C组成的共轭烯烃,从分子骨架直接写久期行列式(1)画出σ骨架,将参与共轭的原子编号;(2)n个原子参加的共轭体系对应着n阶久期行列式;(3)n阶久期行列式主对角元Aij为x,x=(α-E)/β;(4)若ij两原子以π键键连,则Aij及Aji为1,其它元素均为0;(5)久期行列式沿主对角线对称;(6)对同一分子,若编号不一,其写出的久期行列式虽然不同,但求解的结果相同。
休克尔分子轨道的应用:休克尔分子轨道法是量子化学近似计算方法之一,它以简便迅速著称,适宜于计算平面共轭分子中的π电子结构。
在分析有机共轭分子的稳定性、化学反应活性和电子光谱,及研究有机化合物结构与性能的关系等方面有着广泛应用。

乙烯休克尔行列式
休克尔分子轨道法(Hückel molecular orbital method)是用简化的近似分子轨道模型处理共轭分子中的π电子的方法,1931年由E.休克尔(E. Hückel)提出,简称HMO。
这是一种最简单的分子轨道理论,在有机化学中应用得相当广泛,用以解决共轭分子的结构,探讨分子的性质和反应性能的半经验方法。
原理
在有机化合物中,包含着一大类共轭和芳香烃分子,它们的特点是参与共轭的原子都在一个分子平面上,每个原子都有一个垂直于分子平面的p原子轨道,在这个轨道上的电子称为π电子。


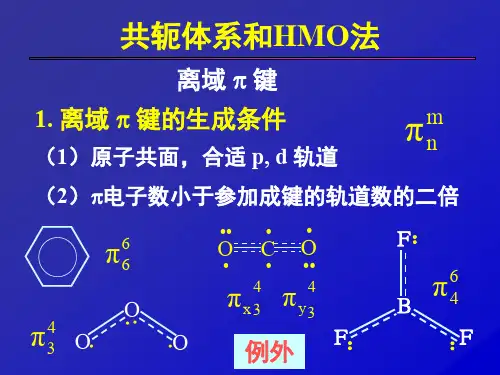




实验三 结构化学的HMO 处理一、实验目的1.巩固和加深理解本课程中所学的有关知识。
2.掌握HMO 法处理共轭分子的方法。
3.学会用HMO 法处理共轭分子所得的结果讨论分子的性质。
二、实验原理若共轭分子中每个π电子k 的运动状态用k ψ来描述,其Schrödinger 方程为:KK E H ψψ=пk ˆ 对含有n 个C 原子的共轭分子,由每个C 原子提供一个p 轨道i Φ线性组合可得分子轨道ψ如下:n n c c c c Φ++Φ+Φ+Φ=ψ 332211再根据线性变分法可得久期方程04321221122222221211112121111=⎥⎥⎥⎥⎦⎤⎢⎢⎢⎢⎣⎡⎥⎥⎥⎥⎦⎤⎢⎢⎢⎢⎣⎡---------c c c c ES H ES H ES H ES H ES H ESH ES H ES H ES H nn nn n n n n n n n n并引入下列假设α====nn H H H 2211⎩⎨⎧=不相邻和,=相邻和j i j i H ij 0,β ⎩⎨⎧≠===ji j i S ij ,0,1 化简可求出n 个K E ,将每个K E 值代回久期方程,得ki c 和k ψ。
进一步计算电荷密度i ρ, ∑=kkik i c n 2ρ 键极ij p , ∑=kkjki k ij c c n p 自由价i F ,∑-=iiji p F F max作分子图,根据结果讨论分子的性质。
HMO 法是个经验性的近似方法,定量结果的精确度不高,但在预测同系物的性质、分子的稳定性和化学反应性能、解释电子光谱等一系列问题上,显示出高度的概括力,因此被广泛应用。
三、实验所需仪器计算机四、实验步骤1. 自选一些直链共轭烯与一些单环共轭多烯。
2. 首先分析分子中п键的形成情况,画出分子骨架并编号,再写出久期方程式,久期行列式,本征方程,本征多项式,求得п分子轨道波函数,画出分子轨道及能级图,计算电荷密度、键极、自由价,作分子图。
休克尔分子轨道法1 目的要求(1) 运用HMO 程序计算若干平面共轭分子的电子结构。
(2) 通过HMO 程序的具体运算,加强对这一基本原理的理解,培养学生运用分子轨道概念解决实际问题的能力。
(3) 熟悉微型计算机和磁盘操作系统。
2 基本原理(1) HMO 方法的基本原理:休克尔分子轨道法是量子化学近似计算方法之一,它以简便迅速著称,适宜于计算平面共轭分子中的π电子结构。
在分析有机共轭分子的稳定性、化学反应活性和电子光谱,及研究有机化合物结构与性能的关系等方面有着广泛应用。
该方法主要运用了下列基本假定:①σ-π分离近似。
对于共轭分子,构成分子骨架的σ电子与构成共轭体系的π电子由于对称性的不同,可以近似地看成互相独立的。
②独立π电子近似。
分子中的电子由于存在相互作用,运动不是独立的,但若将其它电子对某电子的作用加以平均,近似地看成是在核和其它电子形成的固定力场上运动,则该电子的运动就与其它电子的位置无关,是独立的。
③LCAO-MO 近似。
对于π体系,可将每个π分子轨道Ψk 看成是由各原子提供的垂直于共轭体系平面的p 原子轨道i ϕ线性组合构成的,即∑=ii ki k C ϕψ (1)在上述假定下,可列出π体系单电子Schrodinger 方程kk E H ψψκπ=ˆ (2)将(1)式代入(2)式,利用变分原理,可得久期方程式: ()()()0112121211111=-++-+-n n n C ES H C ES H C ES H ()()()0222222212121=-++-+-n n n C ES H C ES H C ES H………………………………………………………………()()()0222111=-++-+-nnn nn n n n n C ES H C ES H C ES H此方程组有非零解的充分条件1121211111n n ES H ES H ES H --- 02222222211112=------nnnn n n n n n n n ES H ES H ES H ES H ES H ES H此行列式亦称为久期行列式。
结构化学的HMO处理实验报告摘要:本实验旨在通过Hückel分子轨道法(HMO)处理有机分子的电子结构,探究不同体系的分子轨道结构和反应性质。
通过从头计算方法,我们研究了苯、萘和壬二烯三种有机分子的HMO处理结果,并对其结果进行了讨论。
实验结果表明,HMO方法能够揭示分子的π电子结构和化学反应行为,并为有机合成的设计和机制研究提供了理论基础。
1.引言结构化学是研究分子构造及其性质的学科,为化学反应的机理研究和有机化合物的设计合成提供了理论基础。
HMO方法是结构化学中重要的计算手段之一,通过简化分子的电子结构,可以分析分子的π电子和化学反应性质。
本实验通过应用HMO方法,计算了苯、萘和壬二烯三种不同体系的分子轨道结构和反应性质,以揭示分子的内禀特性。
2.实验方法2.1 Hückel分子轨道法Hückel近似是简化分子电子结构计算的重要方法,主要适用于共轭体系。
在Hückel近似中,只考虑分子的π电子,忽略σ电子的贡献。
通过构建分子的π轨道哈密顿算符,可以求解分子轨道的能级和电子分布。
2.2从头计算方法为了获得准确的结果,本实验采用从头计算方法,通过量子化学软件实现计算。
基于密度泛函理论和Hartree-Fock方法,从头计算能够精确地描述分子的电子结构和性质。
3.实验结果与讨论通过从头计算方法,我们得到了苯、萘和壬二烯的分子轨道结构。
苯为平面结构,具有6个π电子,分布于分子平面上的分子轨道中。
萘为平面结构,具有10个π电子,分布于分子平面上及其侧链的分子轨道中。
壬二烯为非平面结构,由9个共轭碳原子组成,具有18个π电子,分布在整个分子结构中。
根据分子轨道能级的序列和电子分布,我们可以推测分子的反应性质。
苯具有特殊的稳定性,由于分子平面上的π电子均属于全满轨道,使得苯环对电子不容易进行加成和脱除反应。
萘由于侧链上的π电子轨道参与,具有比苯更高的反应活性,可以进行较多的化学反应。
hmo化学式HMO化学式简介HMO,即Hückel分子轨道理论(Hückel Molecular Orbital Theory),是一种用于描述共轭体系电子结构的量子化学理论。
HMO化学式是在Hückel分子轨道理论基础上推导出来的一种表示共轭体系电子结构的简化表示方法。
一、HMO化学式的基本概念HMO化学式由一组字母和数字组成,用于描述分子中的π电子分布和轨道能级。
其中,字母表示原子,数字表示分子中该原子上的轨道数。
例如,苯分子的HMO化学式为C6H6,表示苯环中有6个碳原子和6个氢原子。
二、HMO化学式的应用HMO化学式可以用于描述共轭体系电子结构和反应机理。
通过观察HMO化学式中的原子和轨道数,可以了解分子中π电子的分布情况,从而预测分子的性质和反应活性。
三、HMO化学式的解读在HMO化学式中,字母表示分子中的原子,数字表示该原子上的轨道数。
例如,苯分子的HMO化学式C6H6中,C表示碳原子,6表示碳原子上有6个π轨道。
苯分子中的C6H6表示苯环中有6个碳原子和6个氢原子。
四、HMO化学式的特点HMO化学式的特点是简洁明了,能够快速描述分子的共轭体系和π电子分布情况。
通过观察HMO化学式中的字母和数字,可以直观地了解分子的结构和电子性质。
五、HMO化学式的局限性HMO化学式虽然可以用于描述共轭体系电子结构,但是它是基于一些简化假设的理论,只适用于具有平面结构、分子轨道重叠较好的共轭体系。
对于非共轭体系和立体化学结构较复杂的分子,HMO 化学式的应用受到限制。
六、HMO化学式的发展HMO化学式是Hückel分子轨道理论的一种应用,它为研究共轭体系的电子结构和反应机理提供了重要的理论基础。
随着量子化学理论的不断发展,现代化学家们已经提出了更加精确的描述共轭体系的理论方法,如密度泛函理论(Density Functional Theory,DFT)和从头算方法(Ab Initio Method)等。