TiO2光解水及CO2催化转化 ppt课件
- 格式:pptx
- 大小:2.95 MB
- 文档页数:40


文章编号:100021506(2003)0620101205纳米TiO 2光催化降解技术在污水处理方面的研究进展江 红,戴春爱(北京交通大学理学院,北京100044)摘 要:光催化技术是一种新兴的高效节能现代污水处理技术,目前还处于实验研究阶段.本文综述了TiO 2光催化降解水中有机物技术的近况,讨论了催化剂颗粒度、p H 值、表面改性、载体、外加氧化剂对其光催化活性的影响,还概述了有机物结构及其它因素与降解效果的关系.关键词:催化化学;二氧化钛;光催化降解;有机物;影响因素中图分类号:O69 文献标识码:AStudy of Photocatolytic Degradationfrom Pollutant W ater by Using N amometer TiO 2J IA N G Hong ,DA I Chun-ai(School of Sciences ,Beijing Jiao Tong University ,Beijing 100044,China )Abstract :Photocatolytic process is one of the technologies with high efficiency and economizingenergy for the removal of pollutant from water.In this paper ,the influence factors such as parti 2cle size ,p H value ,surface modification of TiO 2,canrier ,exterior oxidants ,composition of or 2ganic pollutants and others etc.ane summarized.K ey w ords :catalysis chemistry ;TiO 2;photocatolytic degradation ;organic pollutants ;influence fac 2tors化工废水都含许多对人体有害的物质,特别是有机化合物如有机磷农药、芳香族胺基化合物、氯系溶剂(二氯乙烯、三氯乙烯等)、苯系溶剂以及醛酮等.这些污染水体的有机物质对人体的毒害很大,因此各国政府相继出台了有机污染物的控制排放指标,对有害物质的处理提出了更高的要求.传统的水处理法如吸附法、混凝法、活性污泥法等在实际处理这些有机污染物时均存在着一定的困难,效果尚不理想,因此急需寻找一种经济、有效的方法以降解这些污染物.自1976年J.H.Cary 等人[1]报道了在紫外光照射下,纳米TiO 2可使难降解的有机化合物多氯联苯脱氯,至今,已发现有3000多种难降解的有机化合物可以在紫外线的照射下通过TiO 2迅速降解[2],特别是当水中有机污染物浓度很高或用其它方法很难降解时,这种技术有着更明显的优势.1976年,J.H.Cary 等人对多氯联苯的光催化研究发现,在TiO 2的浊液中浓度为50ug/L 的多氯联苯经0.5h 的紫外线照射,反应物即可全部脱氯[1].此后,光催化降解技术尤其是纳米TiO 2光催化氧化法作为一种水处理技术,引起了各国众多研究者的广泛重视.王怡中、王九思等人[3,4]研究了染料废水中甲基橙、活性艳红X -3B 以纳米TiO 2为催化剂进行光降解脱色,甲基橙反应10min ,脱色率达97.4%;活性艳红X -3B 在充氧条件下光照1h 降解率可达98%.樊彩梅人等研究了纳米TiO 2对水中腐植酸(HA )的降收稿日期:2003204211作者简介:江红(1959—),女,江苏江都人,副教授.em ail :hongjiang1408@ 第27卷第6期2003年12月 北 方 交 通 大 学 学 报JOURNAL OF NORTHERN J IAO TON G UN IV ERSIT Y Vol.27No.6Dec.2003解情况[5].付宏祥等人[6]在研究光催化还原水中重金属离子时发现,在废水p H 为2.5的体系中光照1h后,Cr (Ⅵ)的还原率达85%.R.W.Mattews 等人[7]对水中34种有机污染物进行处理研究表明,光催化降解技术具有常温常压下就可以进行,能彻底破坏有机物、无二次污染、费用较低等优点.美国、日本、加拿大等国已尝试将TiO 2光催化技术应用于水处理,目前国内大多还只限于实验室研究阶段,尚未有把该技术投入实际应用的报道.1 纳米TiO 2光催化降解技术1.1 纳米TiO 2光催化降解机理纳米TiO 2是一种N 型半导体型材料,其化学稳定性高、耐光腐蚀,具有较大的禁带宽度(E q =312eV )、氧化还原电位高、光催化反应驱动力大、光催化活性高等优点.可使一些吸热的化学反应在被光辐射的TiO 2表面得到实现和加速,加之TiO 2无毒、成本低,故TiO 2的光催化研究最为活跃.它的光催化反应机理[8]被认为(如图1所示):当半导体吸收的光能高于其禁带宽度的能量时(波长小于或等于387.5nm ),价带(VB )中的电子就会被激发到导带(CB )上,形成带负电的高活性电子e -,同时在价带上产生带正电的空穴h +(h +氧化电位以标准氢电位计为3.0V ,与氯气的1.36V 和臭氧的2.07V 相比,其氧化性要强得多).在电场的作用下,电子与空穴发生分离,迁移到粒子表面的不同位置,空穴与水、电子与溶解氧反应,分别产生羟基自由基(・OH )和氧自由基(・O -2)等.由于・OH 和・O -2等都具有强氧化性,把大多数吸附在TiO 2表面的有机污染物(简称为R )降解为CO 2、H 2O ,把无机污染物(简称为B +)氧化或还原为无害物.图1 纳米TiO 2光催化降解污染物的反应示意图1.2 光催化技术(1)悬浮相光催化法 目前,国内外悬浮相光催化进行化学合成、污水处理取得较大进展,尤其TiO 2研究最多,进展最快.TiO 2光催化氧化处理水中有机物的反应器有两种形式,即悬浮态和固定床反应器.与固定床光催化反应器相比,悬浮态型光催化反应器在反应速率、反应器设计以及光解操作方面占有许多优势.吴海宝等人[9]采用开放式悬浮相光催化反应器,以太阳光激发染料污水悬浮中的TiO 2产生・OH 自由基将染料氧化脱色.实验结果表明:经过2h 太阳光照射后,阳离子蓝X -GRRL 的染料脱色率在80%~93%之间.李晓红等人[10]采用TiO 2/SnO 2为复合光催化剂,对敌敌畏进行光催化降解研究,结果表明,包覆型的TiO 2/SnO 2光催化活性得到明显提高.但利用悬浮相光催化法进行光催化氧化,存在着催化剂易失活、易凝聚、难分离、利用率低等弊端,这使得该项技术的实际应用受到限制,采用催化剂固定技术则是解决这一问题的有效途径.(2)固定相光催化法 近几年来,人们已将研究的重点转向制备高效的催化薄膜取代催化剂粉末,来解决固体难分离问题.固定相光催化法研究现状见文献[11~15],其中溶胶—凝胶法是目前常用方法.研究表明,膜的比表面积越大,孔隙、孔体积越小,孔径分布越均匀,其催化活性越高.为了提高催化活性,张彭义、蒋展鹏等人考察了溶胶溶液组成、涂覆基材、涂覆方式、涂覆次数及焙烧温度等对制备条件的影响.结果表明,用组成及配比为钛酸异丙酯∶正丙醇∶乙酰丙酮∶水(体积比)为4.5∶35∶1.5∶3.0的溶胶浸涂钛板,并在400℃空气气氛下焙烧30min ,重复浸涂4~6次得到的TiO 2固定膜具有较高的活性,对活性艳红X -3B 的光催化降解性能与0.1g/L 悬浮式TiO 2的性能相当[16].近年来,201北 方 交 通 大 学 学 报 第27卷制备高效的催化膜以取代TiO 2粉末成为人们研究的重点.催化剂载体大致有玻璃、玻璃纤维、空心玻璃球、海沙、金属基等;采用的工艺有:溶胶—凝胶法、浸泡—干燥法、浸涂法、浸渍—烧结法、涂载法等.1.3 可降解有机物类型叶庆国等人[17]研究了以TiO 2半导体为催化剂,有机物分子结构如芳烃取代度、环效应和卤代度对光催化氧化降解的影响.结果表明,对芳烃类衍生物,单取代基较双取代基降解容易,能形成贯穿共轭体系的难降解.环效应、卤代度对光催化降解有较大影响,芳烃、环烷烃、烷烃逐次减弱,卤代度越高,降解越困难,全卤代时基本不降解.2 催化活性影响因素纳米TiO 2被激发产生的空穴/电子对虽然具有很强的氧化还原能力,但在实际应用中也存在一些缺陷.如TiO 2的带隙能较宽,光吸收仅限于紫外光区,限制了其对太阳能的利用;再如空穴易于与电子复合,降低光催化效率;又纳米TiO 2颗粒细小,在废水处理中易于流失,回收困难,不利于催化剂的重复使用,迫使成本升高.因此,需要对TiO 2催化剂进行修饰,以提高其光催化活性及可应用性.目前研究的思路有:2.1 催化剂颗粒度、光照面积对光催化效率的影响市售的TiO 2主要有锐钛矿相和金红石相两种稳定晶型,前者对氧气吸附力较强,活性较高,后者的光催化活性较低.当催化剂的粒径减小,会使TiO 2的吸收带边界蓝移,光催化活性显著提高.对苯酚的光催化降解反应的实验研究证明[18]:粒径小的TiO 2有更高的催化活性,当粒径<15nm 时,显示出量子尺寸效应,即与市售的TiO 2相比,两种晶相的纳米TiO 2均有很高的光催化活性,但锐钛矿相氧化钛对苯酚的深度降解有更高的选择性.还有研究表示[19],采用金属醇盐水解法制备TiO 2纳米粒子,TiO 2粒子长大,晶型由锐钛矿型向金红石型转变,对活性改变也有一定影响.对固定床来讲,将纳米TiO 2颗粒负载在合成纤维、玻璃布、金属网上,使其拥有巨大的比表面积,增加大量反应点;研究显示[20],光催化效率还与催化膜的光照面积成正比.2.2 水溶液pH 值的影响研究表明,p H 值对光催化降解反应的影响有:(1)TiO 2颗粒的分散度 TiO 2颗粒分散得越好,受紫外线照射的面积越大,产生的电子/空穴越多,同时空穴迁移到TiO 2表面的越多,光催化活性就越高.溶液的p H 值能改变颗粒表面的电荷,从而改变颗粒在溶液中的分散情况[21].TiO 2的等电点p H 值为3.0,当溶液p H 值接近TiO 2等电点时,由于范德华引力的作用,颗粒之间容易团聚形成大颗粒.因此,当悬浮液p H 值远离等电点p H 值时,由于颗粒相互间的排斥力,其在溶液中分散很好.此时,有机污染物被纳米TiO 2光催化降解的效率更高.(2)不同有机物的降解反应有不同的最佳p H 值 某些有机物光催化降解时p H 值的影响符合上述等电点理论,如赵梦月等人[22]在有机磷农药光解的研究中发现,p H 值对甲拌磷光解的影响完全符合这一理论,但对硫磷、久效磷、磷胺等来说,p H 值对其光催化效率的影响与等电点理论有偏差.甚至某些有机物的光解的最佳p H 值,恰与等电点理论冲突,如溴氰菊酯[23]光解时,p H 值在3.5左右有最高降解率;而在光催化氧化二氯乙酸时,p H =3时光解效率达到最高.因此,对不同物质而言,其光解时的最佳p H 值不同.在实际水处理工作中,对最佳p H 值的探讨很重要.2.3 外加氧化剂的影响通常的方法是通入O 2或H 2O 2,外加氧化剂不被认为是氧化剂直接参与了降解反应,而是提高光催化效率的重要途径之一,它起到了提高电子/空穴对分离效率的作用.O 2在其中作为光致电子捕获剂、同时作为・OH 的另一个来源以及羟基化产物进一步氧化反应的氧化剂,不会带来二次污染,因此使用更为广泛.H 2O 2比O 2更好,因为它利用电子也可产生・OH ,O 2+e —→O -2,H 2O 2+e —→・OH +OH -.许宜铭等人[24]对苯酚及氯代苯酚的光解研究表明,在溶液中加入少量H 2O 2和O 2均能不同程度地增加光解效率.张颖等人[25]考察加入量对活性艳红X -3B 的光催化氧化反应时发现,H 2O 2的加入可以加快脱色速度,在不加H 2O 2、其它条件均相同的情况下,脱色率仅为50%左右.但H 2O 2的加入对COD Cr 去除率没有很大影响.陈梅兰等人[22]介绍,在光催化氧化溴氰菊酯的过程中,在每升水中加入H 2O 2后301第6期 江 红等:纳米TiO 2光催化降解技术在污水处理方面的研究进展401北 方 交 通 大 学 学 报 第27卷量达5ml以上的,光解率增加不显著.他们认为可能的原因是H2O2也对・OH起消除作用:H2O2+・OH—→H2O+HO2・, HO2・+・OH—→H2O+O22.4 表面改性的影响可以通过添加有机化合物和无机化合物对TiO2进行表面改性.通过表面改性能达到阻止TiO2凝聚、改善分散性以及使电子—空穴有效分离的目的.如用SnO2对TiO2表面改性,由于TiO2的导带高于SnO2的导带,因此可利用SnO2作为电子的沉降载体,把从TiO2价带跃迁到导带的电子迁移到SnO2导带上.同时由于SnO2的价带低于TiO2,其空穴可以转移到TiO2价带上,从而达到较好的电子—空穴分离效果,以相应提高光解效率.同样,ZnO与TiO2也具有光催化协同作用.2.5 载体的影响针对悬浮相催化剂尤其是超细颗粒催化剂粉末与反应液的分离困难,即催化剂的回收很不容易的问题,人们寄希望于找到能提高光催化活性的载体.研究表明在不同基质上TiO2的光催化活性也有区别.崔高峰等人对TiO2负载在不同基材上时的脱色活性进行了比较,结论是:金属基质的负载型光催化膜光催化活性要优于非金属及半导体基质的光催化膜活性[20].另有研究表明[4,26],硅胶作载体的光解效率比玻璃纤维、渥太华沙、三氧化二铝等高,而掺杂SnO2的导电玻璃用作载体时,其光解效率要比硅胶高.在此类载体中,沸石是一种高效、高选择性的光催化剂载体,因为沸石能提供独一无二的纳米微孔反应场(非同一般的内表面布局和粒子交换性能).在这样的反应空间里,存在一般光催化系统难以实现的特殊的光催化性能,如利用沸石作载体制备的TiO2就显示出独特的局部结构以及氧化有机物的选择性[27].2.6 其它因素的影响有机污水中常掺杂一些金属(Ag,Pt,Nb等)和一些离子(如ClO-2,ClO-3,IO-4,S2O2-8,BrO-3,Cl-, Fe3+,SO2-4,PO3-4等),它们对光解效率均有一定的影响.如Ag,Pt可降低TiO2的带隙能、ClO-2,ClO-3等可净化导带电子,最终均可降低电子—空穴的复合几率,而Cl-、SO2-4则会显著降低光子效率,从而导致光催化活性的下降.人们利用这一现象来研究用担载金属的方法,或者用掺入Fe3+等来提高TiO2的光催化活性.在目前的研究中,常见的担载金属有Pt、Pd、W、Ag、Au等,其中Pt、W最常用.在半导体表面担载的金属应控制在一个最适量的范围内.Herman J M等人发现,在光催化剂上,当金属担载量低时,随金属量增加,金属呈正效应,这不仅由于金属的催化性质,还由于电子在金属上的富集减少了半导体表面电子的浓度,从而减少了电子与空穴在半导体表面的复合[28].然而,超出金属量的最佳范围,担载量越多越有害,这是由于过多的带有电子的金属微粒在半导体颗粒上存在时,使光诱导产生的电子与空穴的再复合.金华峰等人[29]为了提高TiO2的光催化活性及其对可见光的吸收率,在TiO2/SiO2中掺杂Fe3+,Fe3+掺杂导致晶粒增大,大大提高对NO-的光解速率.李芳柏等人[30]认为,Au3+掺杂与Fe3+掺杂不同,Au3+能被还原成单质态的金,Au3+掺杂不仅使吸收光谱发生红移,而且能提高对紫外—可见光吸收能力,且掺杂浓度越大,吸光度增加越大.提高催化剂的光吸收能力是改善TiO2的一个主要目标.3 光源的优化与太阳能的利用波长在200~400nm的紫外线所具有的能量是许多物质吸收后产生光化学反应所需要的能量,所以紫外线的光化学作用比可见光的光化学作用要强得多,其光化学作用非常显著.目前已有一些紫外线光源如氙灯、低压汞灯、中压汞灯、高压汞灯、金属卤化物灯、荧光灯等面市.而光谱范围分布在250~410nm 的中压汞灯,其降解反应速率常数是其它光源的1.4倍以上[31].太阳能是清洁而经济的能源,太阳光谱能量中200~400nm的紫外线占太阳全部能量的3%~5%,利用这一部分太阳能作为TiO2光催化反应的光源,无论是从理论上还是实践上都是可行的.但太阳能中可被利用的辐射光范围有限,这是限制太阳能应用的关键因素,这一点只有通过改进光催化剂的吸光情况加以改善,相关的方法主要包括:对TiO2的表面进行改性;利用敏化材料将TiO2敏化从而加大激发光源的可利用波长范围;开发均相催化.4 结语纳米TiO 2光催化降解技术的优点有:(1)水中所含多种有机污染物均可被完全降解为CO 2、H 2O 等,无机污染物被氧化或还原为无害物;(2)反应条件温和、能耗低、在紫外光照射或暴露在太阳光下即可发生反应;(3)合适的光催化剂具有廉价、无毒、稳定及可以重复使用等优点;(4)所需设备结构简单、操作条件容易控制,无二次污染;(5)未来趋势可以利用取之不尽、用之不竭的太阳能作为激活光催化剂的光源,应用范围广.参考文献:[1]Hoigne J ,Bader H.The Role of Hydroxyl Radical Reactions in Ozonnation Processes in Aqueous S olutions[J ].Water Res.,1976,10(2):377.[2]钟王景,邢卫红,徐南平,等.废水中有机污染物高级氧化过程的降解[J ].化工进展,1998,(4):51~53.[3]王怡中,符雁,汤鸿霄.甲基橙溶液多相光催化降解研究[J ].环境科学,1998,19(1):1-4.[4]王九思,赵红花.负载型纳米TiO 2光催化降解活性艳红X -3B 染料[J ].应用化学,2002,19(8):792-794.[5]樊彩梅,孙彦平.纳米TiO 2对水中腐植酸的吸附及光催化降解[J ].应用化学,2001,18(11):912-914.[6]付宏祥,吕功煊,张宏,等.Cr (Ⅵ)离子在TiO 2表面的吸附与光催化还原消除[J ].环境科学,1998,19(3):80-83.[7]Mattews R W.Photo Oxidation of Organic Material in Aqueous Suspensions of TitaniumDioxide [J ].Water Res.,1990,24(5):653.[8]范少华,崔玉民.光催化技术在污水处理方面的应用[J ].化工进展,2002,21(5):345-348.[9]吴海宝,董晓来.太阳能—TiO 2非均相光催化氧化染料污水脱色研究[J ].中国环境科学,1997,17(1):93-96.[10]李晓红,颜秀茹,张月萍,等.TiO 2/SnO 2复合光催化剂的制备及光催化降解敌敌畏[J ].应用化学,2001,18(1):32-35.[11]苏文悦,付贤智,魏可镁.溴代甲烷在SO 2-4/TiO 2上的光催化降解[J ].环境科学,2001,22(2):91-94.[12]席北斗,刘纯新,孔欣.负载型催化剂光催化氧化五氯苯酚钠的效果[J ].环境科学,2001,22(1):41-44.[13]崔玉民,单德杰,朱亦仁.TiO 2薄膜光催化氧化I -的研究[J ].无机化学学报,2001,17(3):401-406.[14]颜秀茹,李晓红,宋宽秀,等.TiO 2/S iO 2的制备及其对DDVP 光催化性能的研究[J ].水处理技术,2000,26(1):42-47.[15]孙尚梅,康振晋,魏志仿.TiO 2膜太阳光催化氧化法处理毛纺染整废水[J ].化工环保,2000,20(1):11-14.[16]张彭义,余刚,蒋展鹏.固定二氧化钛膜的制备及其光催化性能[J ].中国环境科学,2000,20(5):436-440.[17]叶庆国,李明.有机结构对光催化氧化降解影响的初步研究[J ].环境工程,2000,18(4):55-56.[18]张青红,高濂,郭景坤.二氧化钛纳米晶的光催化活性研究[J ].无机材料学报,2000,15(3):556-560.[19]尚静,徐自力,杜尧国,等.TiO 2纳米粒子的结构\表面特性及其光催化活性研究[J ].无机材料学报,2001,16(6):211-216.[20]崔高峰,王伯勇,王青,等.TiO 2在不同基质上光催化活性的比较[J ].工业水处理,2001,21(7):26-27.[21]钟目规.陶瓷微滤膜过滤微米、亚微米级颗粒体系的基础研究和应用开发[D ].南京:南京化工大学,1998.[22]赵梦月,罗菊芬.有机磷农药光催化分解的可行性研究[J ].化工环保,1993,13(2):74-79.[23]陈梅兰,陈金媛,蒋传庆,等.TiO 2光催化降解低浓度溴氰菊酯[J ].环境污染与防治,2000,22(1):13-14.[24]许宜铭,陈文星.苯酚及氯代苯酚化合物TiO 2催化光致降解[J ].环境化学,1990,9(6):13-18.[25]张颖,王桂茹,李朝晖,等.光催化氧化法处理活性染料水溶液[J ].精细化工,2000,17(2):79-81.[26]邱健斌,曹亚安,马颖,等.担载材料对TiO 2薄膜光催化活性的影响[J ].物理化学学报,2000,16(1):1-4.[27]Masakazu Anpo ,Virpi Saloren.E ffectiveness Factorss for Photocatalytic Reactions Occurring in Planar Membranes [J ].J Phys Chem :B ,1997,101(8):2632-2636.[28]崔玉民,朱亦仁,王克中.用复相光催化剂WO 3/CdS/W 深度处理印染废水的研究[J ].工业水处理,2001,21(2):9.[29]金华峰,李文戈,向纪明,等.Fe 3+/TiO 2/SiO 2复合纳米微粒的合成几光催化降解NO 2-[J ].应用化学,2001,18(8):636-639.[30]李芳柏,李湘中.金离子掺杂对二氧化钛催化性能的影响[J ].化学学报,2001,59(7):1072-1077.[31]史载锋.光催化陶瓷膜反应器的实验研究与数学模拟[D ].南京:南京化工大学,1999.501第6期 江 红等:纳米TiO 2光催化降解技术在污水处理方面的研究进展。


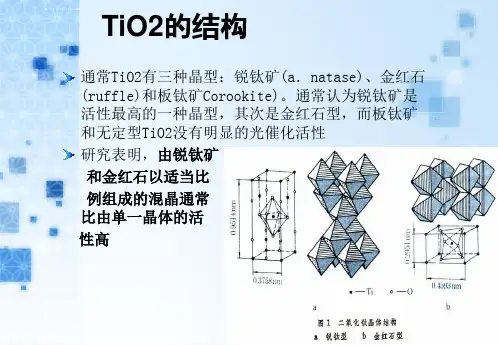


第一节二氧化钛光催化研究现状及机理在社会和经济快速发展的同时,人类赖以生存的环境也遭到不同程度的污染和破坏,最主要包括水体污染和空气污染.不容置疑,水体和空气的净化与保护已成为人类社会实现可持续发展亟待解决的重要问题。
因此,我们亟需一种简便有效的方法来治理水体污染和大气污染。
以产生氢氧自由基(·OH)为主要特点的高级氧化技术(Advanced Oxidation Technology, 亦即深度氧化技术)在环境治理中优势逐渐得以体现并迅速发展。
高级氧化技术反应过程中产生大量·OH,反应速度快,适用范围广,较高的氧化电位使得·OH几乎能将所有的有机物氧化直至完全矿化,反应条件温和,可诱发链反应。
半导体光催化氧化还原技术就为高级氧化技术开辟了一条极富潜力的途径.其主要的特点是,利用半导体物质作为光催化剂以实现光能到化学能的转化,一般不需外加氧化剂.反应过程中电子的传输与得失主要通过(光照条件下)半导体与H2O或O2或OH-和有机物三者间的相互作用完成。
这个过程不需要其他化学助剂,反应条件温和,而且能将有机污染物完全氧化成水和二氧化碳,不会产生二次污染。
美国环保局公布了九大类114种有机物被证实可以通过半导体光催化氧化方法处理,该方法尤其适合于难以或无法生物降解的有毒有机物质。
用作光催化剂的半导体大多数为金属氧化物或硫化物,如TiO2,CdS,ZrO,V2O3,WO3,ZnO,SeO2,GaP,SnO2,SiC,Fe2O3等等。
其中只有TiO2由于化学性质稳定、抗光腐蚀、便宜、无毒并具有较高活性而得到了广泛的研究与应用。
因此本研究采用TiO2形貌及其光催化等方面的进行研究。
1.1.1二氧化钛的研究现状日本学者Fujishima和Honda[1]于1972年在《Nature》杂志上发表了一篇论文,报道了在光辐射下TiO2可以将水分解产生氢气,引起了人们对光催化技术浓厚的兴趣。



