硫铁矿制酸工艺
- 格式:docx
- 大小:139.32 KB
- 文档页数:50

3+2两转两吸
你提的问题够专业了,应当说采用接触法生产硫酸工艺中“3+2”两转两吸生产工艺,生产硫酸最典型的两转两吸流程,常用一、二次转化段数和含二氧化硫气体通过换热器的次序来表示。
“3+2”是指第一次转化用三段催化剂放出的热量,第二次转化用二段催化剂放出的热量;第一次转化前二氧化硫气体依次通过第3换热、第1换热器、;第二次转化前含二氧化硫气体依次通过第5换热器、第4换热器、第2换热器。
硫铁矿制酸的典型两转两吸流程主要有3+2五段转化生产工艺流程和和3+1四段转化生产工艺流程。
回答你的问题是要加分数的,这不是一般的人可以回答上来的问题。


武汉工程大学邮电与信息工程学院毕业设计(论文)说明书论文题目:年产13万吨硫酸转化工艺设计学号:学生姓名:专业班级:指导教师:总评成绩:2015年5月31日目录摘要 (III)Abstract (IV)第一章文献综述 (1)1.1硫酸介绍 (1)1.2硫酸的生产方法 (6)1.3硫铁矿制酸工艺 (7)1.4方案的选择 (9)1.5本次设计的目的及意义 (9)第二章转化工序物料衡算与热量衡算 (10)2.1 产品规模和规格 (10)2.2确定各断进口温度及转化率 (10)2.3转化工序物料衡算 (15)2.4转化器各段的热量衡算 (23)第三章设备选型 (33)3.1换热器计算 (33)3.2转化器计算 (42)3.3其他设备的选择 (43)3.4设备选型一览表 (44)第四章环境保护与治理建议 (46)4.1 三废主要来源 (46)4.2 三废处理方案 (46)设计小结 (48)致谢 (49)参考文献 (50)附录 (51)摘要硫酸作为一种基本的无机化工产品,在国民经济的很多部门如化工、轻工、冶金、化肥等领域都有着广泛的用途。
其主要生产过程包括以下工序:硫铁矿的焙烧、炉气的净化、SO2的转化、SO3的吸收和尾气的处理。
本设计是年产13万吨H2SO4转化系统的工艺设计,主要负责硫酸工艺中SO2到SO3的转换过程,转换工艺流程是通过一转一吸收完成的,涉及4台换热器,主要以高温生成气来预热低温反应气,达到热量的有效利用,最大限度的降低能量损失,做到工业生产的低碳化和环保化,以经济、节能、高效、可持续发展为目标来进行设计。
本设计的计算部分主要分两块:物料衡算和热量衡算。
本次工艺设计的进气体积百分数分别为:SO2=9.0%,N2=80.8%。
第一、第二、第三、第四转化工段的进口、出口温度依次设计为380℃→560℃,480℃→510℃,455℃→470℃,390℃→400℃。
通过物料衡算与热量衡算,对出口温度进行核算,核算的四个转化工段的出口温度依次为:562.07℃、502.37℃、492.79℃、399.01.℃,与设计温度吻合,说明本设计是合理可行的。

三种主要制酸(硫酸)方式比较硫酸的来源主要有三种方式,第一种是硫磺制酸,中国用于制酸的硫磺主要来自石油、天然气加工。
2007年国内硫磺制酸2655万吨,占全部硫酸产量的46.6%。
第二种是贵金属冶炼,2007年中国冶炼烟气制酸1315万吨,占全部硫酸产量的23.1%。
第三种是硫铁矿生产硫酸,2007年硫铁矿制酸1678万吨,占全部硫酸产量的29.4%。
1.硫磺制酸硫磺制酸污染小,资源利用率高。
从近几年来看,中国硫磺制酸原料90%以上进口。
2004年进口硫磺676.6万吨,当年硫磺制酸1621.8万吨,占全部硫酸产量的40.6%;2005年进口硫磺830.6万吨,硫磺制酸1974万吨,占全部硫酸产量的42.7%;2006年进口硫磺881万吨,硫磺制酸2233万吨,占全部硫酸产量的44.3%;2007年进口硫磺965万吨,硫磺制酸2655万吨,占全部硫酸产量的46.6%。
从2005~2007年,硫磺进口分别增长154万吨、50.4万吨、84万吨。
据业内人士介绍,硫磺制酸比较简单,硫磺燃烧变成二氧化硫,再用水吸收。
硫磺浓度比较高,对杂质的清除相对简化,热利用率高,可用废热来发电。
每生产1吨硫酸产蒸汽约1.1~1.3吨以上。
硫磺制酸投资省、上马快,仅是硫铁矿制酸投资额的40%,操作简单,工人劳动强度低,无废渣、废水等污染。
2.硫铁矿制酸化合态硫中可作为硫矿石的矿物主要有:黄铁矿、白铁矿、磁黄铁矿等,黄铁矿分布最为广泛,是中国最重要的硫矿石。
黄铁矿又称硫铁矿,分子式为FeS2,理论硫含量为53.45%,理论铁含量为46.55%。
硫铁矿是中国主要硫资源,占硫资源总量的80%。
其中,硫铁矿占53%,伴生硫铁矿占27%。
国内硫铁矿资源贫矿多富矿少,矿石平均含硫品位只有18%,矿石含硫品位大于35%的富矿仅占总储量的5%,主要集中在中南和华东地区,以广东省最多,约占全国富矿总储量的85%。
中国高品位硫铁矿较少且分布不均,不得不依赖于低品位硫铁矿的开发及精炼。


第1篇一、引言硫酸是一种重要的无机化工原料,广泛应用于化肥、农药、医药、冶金、石油、电子、轻工等领域。
随着我国经济的快速发展,硫酸的需求量逐年增加,因此,研究和开发先进的硫酸生产工艺具有重要意义。
本文将详细介绍硫酸生产工艺,包括原料选择、生产工艺流程、设备配置以及环境保护等方面。
二、原料选择1. 黄铁矿:黄铁矿是生产硫酸的主要原料,其主要成分是二硫化铁(FeS2)。
黄铁矿具有资源丰富、价格较低等优点,在我国硫酸生产中占有重要地位。
2. 煤炭:煤炭是生产硫酸的另一种重要原料,主要用于生产沸腾炉沸腾炉渣。
煤炭具有资源丰富、价格较低等优点,在我国硫酸生产中也占有一定比例。
3. 石灰石:石灰石是生产硫酸的辅助原料,主要用于脱硫。
石灰石在硫酸生产过程中起到中和作用,降低烟气中的二氧化硫排放。
4. 水:水是硫酸生产过程中必不可少的原料,用于生产硫酸和洗涤烟气。
三、生产工艺流程1. 烧结(或沸腾炉)制酸法(1)原料准备:将黄铁矿破碎、磨细,制成粒径小于5mm的粉状原料。
(2)沸腾炉燃烧:将粉状原料与煤炭按一定比例混合,送入沸腾炉进行燃烧。
沸腾炉燃烧过程中,黄铁矿被氧化成二氧化硫气体。
(3)脱硫:将燃烧后的烟气通过脱硫塔,使烟气中的二氧化硫与石灰石粉反应,生成亚硫酸钙。
(4)氧化:将脱硫后的烟气送入接触室,与空气中的氧气反应,使二氧化硫氧化成三氧化硫。
(5)吸收:将氧化后的三氧化硫气体送入吸收塔,与水反应生成硫酸。
2. 烧结炉制酸法(1)原料准备:将黄铁矿破碎、磨细,制成粒径小于5mm的粉状原料。
(2)烧结:将粉状原料与煤炭按一定比例混合,送入烧结炉进行烧结。
烧结过程中,黄铁矿被氧化成二氧化硫气体。
(3)脱硫:将烧结炉排放的烟气通过脱硫塔,使烟气中的二氧化硫与石灰石粉反应,生成亚硫酸钙。
(4)氧化:将脱硫后的烟气送入接触室,与空气中的氧气反应,使二氧化硫氧化成三氧化硫。
(5)吸收:将氧化后的三氧化硫气体送入吸收塔,与水反应生成硫酸。


制作硫酸的工艺流程硫酸是一种重要的化工原料,广泛应用于冶金、化肥、染料、药品等行业。
下面是制作硫酸的一种常用工艺流程,包括原料准备、反应、分离与净化等步骤。
一、原料准备硫酸的主要原料是硫磺、浓硫酸、水和空气。
硫磺是硫酸生产的主要原料,一般采用粉状硫磺。
浓硫酸可以用于催化反应、富硫气体的干燥,同时也是制备稀硫酸的原料。
水是稀硫酸的重要组成部分。
空气可以用于稀释硫酸蒸汽。
二、反应部分1.硫磺的燃烧和变换将硫磺放入能够控制温度和通风的反应装置中,加热至燃点(约为266℃)。
硫磺开始熔化,进而燃烧。
石硫会燃烧成二氧化硫气体(SO2)。
SO2与氧气发生反应生成SO3,反应方程式如下:2SO2+O2⟶2SO32.SO3的冷却与吸收SO3与空气混合,并进入冷却器进行冷却。
然后SO3与浓硫酸反应,形成烟雾状硫酸。
SO3+H2SO4⟶H2S2O73.烟雾状硫酸的稀释将烟雾状硫酸缓慢地注入脱水塔,同时用冷水进行稀释。
稀硫酸生成时放热,因此需要控制温度。
稀硫酸的浓度一般为30%至40%左右。
4.稀硫酸的浓缩与净化稀硫酸进一步通过浓缩,浓度可以达到98%以上。
硫酸浓缩过程需要采用浓缩塔,并进行真空操作以降低温度,减少溢流和露点的问题。
浓硫酸中的杂质,例如重金属盐等,可以通过净化操作去除。
三、分离与净化浓硫酸中可能含有其他有害物质,如氯化铁、氯化镉等,需要分离和净化以得到优质的硫酸产品。
1.污水处理处理硫酸工业污水,主要工艺有沉淀、过滤和氧化等。
根据具体情况,可以采用不同的方法进行处理。
2.产品过滤将浓硫酸通过过滤设备,去除其中的杂质和固体颗粒。
根据需要,可以进行多级过滤以确保产品质量。
3.脱水处理浓硫酸中可能含有大量的水分,需要进行脱水处理。
采用真空脱水工艺,结合脱湿塔和蒸发器等设备,将浓硫酸的水分含量降到最低。
4.清洗与包装清洗硫酸产品容器,确保其干净无尘。
然后将硫酸产品进行包装与储存。
常见的储存方式有钢桶、塑料桶和简单水袋等。

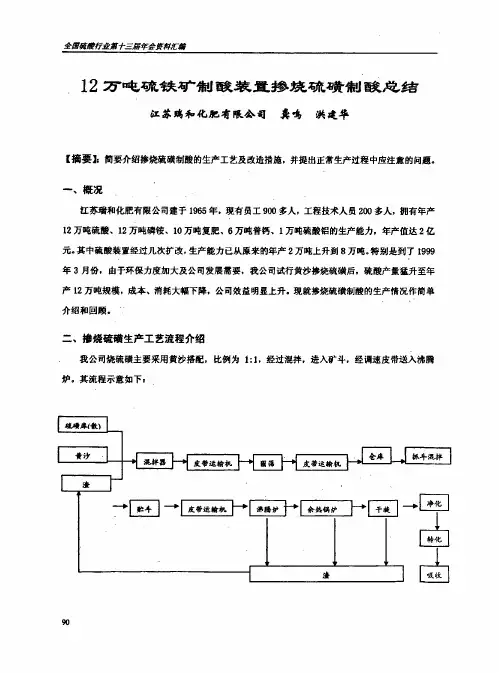
二、工艺流程说明本生产装置为50kt/ a 硫铁矿制酸,封闭酸洗净化,(3+2)二次转化二次吸收。
硫铁矿经原料工段、焙烧工段、净化工段、转化工段、干吸工段等工序,其工艺流程详尽介绍如下:(一)原料岗位在原料厂房内,经料斗至1#皮带入破碎机后经2#皮带至筛分,筛分后经3#皮带至大倾角皮带再至供料皮带进入沸腾炉料斗,料再由沸腾大炉料斗喂入沸腾炉。
(二)焙烧岗位硫铁矿在沸腾炉内与空气鼓风机鼓入的空气在进行沸腾焙烧,焙烧出的高温炉气含SO2 在12-13% ,由炉顶侧向引出,沸腾层温度控制在800-850C,经炉气冷却器冷却,沉降部分粉尘后再进入旋风除尘器进行除尘,同时S02炉气降温至350C左右再进入电除尘器进行除尘。
(三)电除尘器来自焙烧工段的炉气,炉气温度约在350C左右,含尘量约在30g/NM3,进入电除尘器,炉气中的微小尘粒受电场力的作用,经电离、荷电分别向阴极,阳极移动,并沉积于放电极线上和集尘极板上,通过振打,掉落至集灰斗,由溢流螺旋排灰机排出,炉气净化到含尘0.2g/NM3。
进入净化工段。
(四)净化工段净化采用内喷文氏管——泡沫塔——间冷器——电除雾器封闭稀酸洗净化流程。
来自电除尘器的炉气,炉气温度约在300C左右,含尘量约在0.2g/NM3,首先进入内喷文氏管,炉气在喉管内以50米/秒气速冲击送入稀酸,使稀酸雾化,气体与液体充分接触,炉气温度降到65'C左右,炉气中大部分灰尘、砷、氟等杂质被除去。
经增湿后的炉气进入泡沫塔进一步洗涤、冷却,炉气温度降至50 C左右,进入间冷器。
炉气在间冷器内与水间接冷却,换热使炉气温度降至35 C以下,炉气中的热量绝大部分在此设备移出系统。
进入电除雾器进一步除去残余的灰尘和酸雾,使炉气中酸雾<0.03g/NM3 ,砷<1.0mg/NM3,氟<3.0mg/NM3,净化后的炉气进入干燥塔。
由内喷文氏管流出的洗涤稀酸,温度60-65 C进入斜管沉降器,进行固液分离,清液回循环槽,斜管沉降器底部定期排出的酸泥及少量稀酸流至中和槽用石灰中和处理。

浅谈高砷硫精砂制酸工艺一、现实状况我公司硫酸厂采用硫精砂为原料制取硫酸,目前,所用硫精砂主要为朱日和铜矿尾矿浮选硫精砂、还使用过达茂旗、齐华等硫精砂。
从使用综合效益来看,朱日和硫精砂综合效益最大,公司要求大量使用朱日和原料,少量搭配其他地方硫精砂,确保硫酸厂正常生产所需硫精砂用量。
朱日和铜业公司的硫精砂属于高硫磁性铁原料,容易自燃,铁含量较高,使用以来,受矿体变化、选矿工艺调整等因素影响,其品质不够稳定,杂质含量忽高忽低,对生产产生不利影响。
尤其严重的,朱日和硫精砂含砷较高,最高时达到0.5%以上,远远超出工艺要求标准。
对净化、转化、干吸等工段工艺指标影响很大品质波动较大,含有不明杂质,在焙烧、净化工段,工艺操作困难,电除雾器内出现不明泥状物,严重影响净化操作,损害净化设备,电除雾器故障率过高,积泥影响除雾效果,严重时,出现电流、电压不稳,甚至不能正常送电,严重影响除雾效率,并进一步影响转化、吸收等工段操作,同时,严重影响各工段设备的安全运转,降低设备使用寿命,开车率下降,产量下降,造成很大损失。
通过生产调整、试验,已经基本确定:朱日和硫精砂所含不明杂质,是影响净化及转化工段故障率高地根本原因。
通过质量检验单位的工作,基本确定,原料中所含杂质为砷元素,在净化工段电除雾阴极线上积存的带色泥状物,含砷量超过70%,说明硫精砂含有的砷,通过焙烧、和酸洗净化等工艺,没有被有效除去,进入电除雾,在阴极线上富集,严重影响电除雾工作效率,造成停车频繁。
通过工艺试验,烧制红渣时(富氧充分燃烧),砷元素在净化电除雾富集现象能够明显改善。
但是,硫精砂制酸烧制黑渣工艺,能显著提高经济效益,在我公司各种产品销售中,红渣与黑渣的销售价格相差较大,黑渣相比红渣,能提高销售收入20%以上。
但是,现实情况是,在烧制黑渣工艺条件下,硫精砂欠氧焙烧,炉气中砷元素,在净化不能被有效除去。
通过反复试验,调整工艺条件,均不能找到好的办法,能有效的除去进入电除雾炉气中的砷元素,因电除雾故障频发对生产延续性的影响不能有效缓解。
硫磺制酸转化⼯段⼯艺的设计说明200kt/a硫磺制酸转化⼯段⼯艺设计⽬录第⼀章绪论 (1)1.1.硫酸的性质与⽤途 (1)1.2.硫酸的⼯业发展史 (2)1.3.硫酸的⼯业概况及其发展趋势 (3)1.3.1.国外硫酸⼯业概况及其发展趋势 (3)1.3.2.中国硫酸⼯业概况及其发展趋势 (4)第⼆章⼚址的选择 (7)第三章原料的选择 (9)3.1.原料的选择 (9)3.2.硫磺制酸的优点 (9)3.3.硫磺的来源 (10)第四章转化⼯段⼯艺设计 (12)4.1.基本原理 (12)4.1.1.⼆氧化硫氧化热⼒学 (12)4.1.2.⼆氧化硫氧化动⼒学 (12)4.2.⼯艺流程 (14)4.2.1.⼯艺流程的确定 (14)4.2.1.1.⼆转⼆吸与⼀转⼀吸 (14)4.2.1.2."3+1"与"3+2"转化⼯艺的主要区别 (15)4.2.1.3.⼯艺流程的确定 (17)4.2.2.⼯艺条件 (18)4.2.2.1.转化器⼀段⼊⼝条件中⼆氧化硫含量 (18)4.3.⼯艺设备 (20)4.3.1.转化⼯段的主要⼯艺设备 (20)4.3.2.⾃动控制⽅案 (22)4.4⼯艺计算 (23)4.4.1.物料衡算 (24)4.4.2.能量衡算 (26)第五章环境保护与安全⽣产 (33)5.1.环境保护 (33)5.2.安全⽣产 (33)第六章总结 (34)致 (36)参考⽂献 (38)第⼀章绪论1.1 硫酸的性质和⽤途[1,2]硫酸(H 2SO 4)相对分⼦质量98.078,是指SO 3与H 2O 的摩尔⽐等于1的化和物,或指100% H 2SO 4。
外观为⽆⾊透明油状液体,密度(20℃)为1.8305g/cm 3。
⼯业上使⽤的硫酸是硫酸的⽔溶液,即SO 3与H 2O 摩尔⽐≤1的物质。
发烟硫酸是SO 3的硫酸溶液,SO 3与H 2O 的摩尔⽐≥1的物质,亦为⽆⾊油状液体,因其暴露于空⽓中,逸出的SO 3与空⽓中的⽔分结合形成⽩⾊酸雾,固称之为发烟硫酸。
第三章 硫酸生产工艺本章学习要求了解硫酸的性质和用途、制酸用原料、硫铁矿焙烧与流化床反应器以及二氧化硫净化、二氧化硫催化氧化的工艺条件和工艺流程;理解掌握三氧化硫的吸收及尾气处理工艺。
第一节 概 述一、硫酸的性质、产品规格及用途硫酸是基本化学工业中重要产品之一。
在国民经济中占有重要地位,广泛用于石油炼制、冶金、农业生产肥料、炼焦化学工业、电镀业、制革业、橡胶、造纸、油漆、炸药和铅蓄电池制造业、染料、制药等工业部门及某些现代尖端科学领域里。
查一查 硫酸的组成、性质和规格。
二、硫酸的生产原料1.硫铁矿硫铁矿是当前硫酸生产最主要的原料,其主要成分是FeS2,纯粹的FeS2含硫53.45%,含铁46.55%。
根据不同的产矿区,硫铁矿还可能含有铜、锌、铅、锑等有色金属。
一般富矿含硫30%~48%,贫矿含硫在25%以下。
硫铁矿按其来源不同又可分为普通硫铁矿、浮选硫铁矿和含煤硫铁矿。
2.硫黄目前,硫黄是国外制酸的主要原料。
它一般含杂质少,只需在焙烧前除杂净化,制成的炉气无需复杂的精制过程,与以硫铁矿为原料的制酸流程相比较,可节省投资费用。
三、硫酸的生产方法硫酸的工业生产基本上有两种方法,即硝化法和接触法。
硝化法又可分为铅室法和塔式法。
早期的硝化法生产主要反应设备是铅室,因其设备庞大,生产强度低已被淘汰。
后来的生产设备进一步发展为填料塔,所以又有塔式法之称。
无论是铅室法还是塔式法,虽然在历史上起过重要作用,但最终因存在较多不足,诸如成品酸浓度低、杂质多等因素已被接触法所取代。
接触法的基本原理是在催化剂作用下,以空气中的氧氧化二氧化硫,其生产过程分为三步:25 第二节二氧化硫炉气的制备(1)从含硫原料制取二氧化硫气体:S+O2SO24FeS2+11O22Fe2O3+8SO2(2)将二氧化硫氧化为三氧化硫:2SO2+O22SO3 (V2O5为催化剂)(3)三氧化硫与水结合生成硫酸:SO3+H2OH2SO4该法操作简单、稳定、热能利用高、可制得任意浓度的硫酸,因此在硫酸工业中占有重要地位。
硫铁矿制酸工艺 错误!未找到索引项 第一节装置概况 ............................ 2
第二节硫酸及硫氧化物的性质 ................ 3
第三节 工艺流程及其控制特点 .......... 16
第二章 硫铁矿制酸主要工艺原理 ............................................. 25 第一节 沸腾焙烧工艺原理 ............... 25
第二节 炉气净化工艺原理 ............... 33
第三节 三氧化硫吸收工艺原理 ........... 42
第四节 二氧化硫转化的工艺原理 ........ 48
第五节 循环水工艺原理 ................ .52
第一章概述 第一节装置概况 江西铜业集团化工有限公司老系统硫酸装置设计生产能力为 10万 吨/年,以德兴铜矿副产硫精矿为原料,采用氧化焙烧,干法除尘,稀 酸酸洗净化和两转两吸接触法制酸工艺。 本装置还具有高回收率和低 三废”排放等优点。总硫回收率期望值 可达97%(保证值为96.0%以上),工艺流程采用了二转二吸制酸工艺, “ 3+1四段转化,提高硫的利用率,使尾气中 S02及硫酸雾的排放指标 低于《大气污染物综合排放标准》,净化工段20%稀酸外运到大山厂和 泗州厂做为选矿药剂使用,不外排;硫酸钡烧渣是优质铁精矿,直接销 售给钢铁厂,达到综合利用的目的。鼓风机噪音采用消声、隔声及不设 固定岗位等有效措施。
第一早 概述 .......................................................... 2. 本装置技术新、可靠性高,采用以下具有成功业绩的最新技术:DCS 控制系统;阳极保护管壳式酸冷器;二吸塔用高效除雾器控制尾气排放 带出酸沫等。 现在建设的江西铜业(德兴)60万吨/年硫铁矿循环经济项目一期工 程规模为30万吨/年,项目建成后,年产98%工业硫酸25万吨,105% 发烟硫酸15万吨,优质铁精粉182万吨,余热发电量7800万度。计划 于2012年6月竣工投产。
第二节硫酸及硫氧化物的性质
1硫酸的物理性质 硫酸的分子量为98.078,分子式为H2SO4。从化学意义上讲,是三 氧化硫与水的等摩尔化合物,即 SO3H2O。 在工艺技术上,硫酸是指 SO3与H2O以任何比例结合的物质,当 SO3与 出0的摩尔比W1时,称为硫酸,它们的摩尔比〉1时,称为发烟 硫酸。 硫酸的浓度有各种不同的表示方法,在工业上通常用质量百分比浓
度表示。 硫酸的主要物理性质为: 20 C时密度 g/cm3 1.8305 熔点 C 10.37+0.05
沸点 C 100% 275+5 98.479%(最高) 326+5 气化潜热(326.1C时),KJ/mol 50.124
熔解热(100%), KJ/mol 10.726 比热容(25 C), J/(g k) 98.5% 1.412 99.22% 1.405 1.1外观特性 浓硫酸是无色透明液体,能与水或乙醇混合,暴露在空气中迅速吸 收空气中的水份。 发烟硫酸是无色或微有颜色的粘稠状液体, 敞口则挥发窒息性三氧 化硫烟雾。 1・2化学组成 分子量:98.08 O 分子式:H2SO4 II 分子结构: HO — S — OH
II O
1・3密度 100%H2SO4在20C时的密度为1.8305g/cnf,同一温度下,硫酸溶 液的密度首先随它的浓度增加而增加,当浓度达到 98.3%时其密度达到 最大值。当酸浓由98.3%到100%,随酸浓增大而下降,当为100%浓度 时,出现密度的最小值(附表于后)。 发烟硫酸的密度随其中游离的 SO3含量的增加而增加,达到 62% 时密度为最大,以后随 SO3含量增加密度减小,直到100%液体SO3。 (附表于后) 随着温度的升高,硫酸密度减小、体积增大,硫酸密度于是成为函 数变量,其密度与浓度的关系见附表。
表1-1:硫酸溶液的密度(20C时) H2SO4含量 密度 克/厘米
3 SO3 含量
%总重量 %重量 克/升 10 106.6 1.0661 & 16
20 227.9 1.1394 16.33 30 365.5 1.2185 24.49
100.39% 1.394 40 521.1 1.3028 32.65 50 697.6 1.3951 40.80 60 898.9 1.4982 48.95
70 1127 1.6105 57.14 80 1382 1.7272 65.31 90 1633 1.8144 73.47 95 1742 1.8337 77.55 96 1762 1.8355 78.37 97 1781 1.8364 79.18
98 1799 1.8365 80.00 99 1816 1.8432 80.81
100 1830 1.8305 81.63
104.5 1981 1.902 85.31 表1-2硫酸密度与温度的关系 \ 密度sg
/cm \
温度'C
1 10 20 30 40 50 60 70 80 90 93 95 96 97 98 99 100
0 1.00 1.07 1.15 1.23 1.31 1.41 1.51 1.62 1.74 1.83 1.84 1.85 1.85 1.85 1.85 1.85 1.85 10 1700 1307 1104 1262 1731 1140 1550 1931 1823 1682 1903 1444 1684 1684 1684 1584 1184 20 1600 1006 1533 1521 1030 1009 1679 1981 1772 1581 1882 1383 1573 1683 1583 1453 1093 30 1500 1661 1913 1851 1229 1538 1828 1060 1021 1440 1781 1382 1582 1682 1682 1482 1052 40 0229 1,7)6 1352 1120 1628 1737 1948 1459 1700 1889 1780 1381 1581 166 11681 1421 1081
50 0869 1705 1752 1461 1728 9537 1147 1258 1669 1338 1779 1380 1570 1.80 1670 1450 1080
60 0營1%4 1151 1专蔼 1仏1^7 1伊 1缪1% 1159
80 1603 1% 1443 15S4 1@6 仔1吩 1777 伤
100 0兮6 1208 1*6 1除 袂 1甲4 1乡5 17?5 1% 1% 1% 756 45 04 85 30 46 48 44 17 03 31 85 61 86 06 09 09 07 图1-1 SO3水溶液在40C时的密度变化趋势图 1.6 1.4 1.2 1.0 0.8 0 20 40 60 80 100 120 40 60 80 100 硫酸浓度% H2SO4。 发烟硫酸浓度% SO3游离 1・4粘度 硫酸的粘度随温度的升高而降低。硫酸溶液与发烟硫酸的粘度随 其浓度增加而升咼,随温度提咼而降低。 表1-3硫酸粘度与温度的关系数据
硫酸 度% 浓
粘度(帕渺)
15C 20 C 30C 40 C 50 C
93 0.03 0.02 0.01 0.01 0.00 17 31 56 21 84
98 0.03 0.02 0.01 0.01 0.00 49 58 71 29 94 104 0・04 0・03 0.02 0.02 0.01 ・5 74 66 88 08 28
1・5结晶温度 硫酸溶液的结晶温度随硫酸含量的不同而在一个较大的范围内 波动。由于硫酸的结晶湿度随其浓度的不同有很大变化, 为储存和运 输方便,避免在冬季冻结或结晶,商品硫酸的浓度都规定为结晶浓度 低的浓度,如化工公司的主产品硫酸为98%酸,其结晶浓度为-0.7 C 左右。
表1-4不同浓度硫酸结晶温度 硫酸浓度% 92.5 93 97 97.5 98 9&5 100 104.5 结晶温度C -22 -29 -6.9 -3.7 -1.1 +1.8 +10.9 +2.5 1・6二氧化硫在硫酸及发烟硫酸中的溶解度 二氧化硫在同一浓度的硫酸中其溶解度随温度的升高而降低。 在 不同浓度的硫酸中随浓度增高而降低, 直到硫酸浓度83.3%最低。此 后,酸浓增加时,则二氧化硫溶解度又逐渐增加。 表1-5二氧化硫在硫酸及发烟硫酸中的溶解度 硫酸浓度
%H 2SO4
SO2溶解度(克/100克H2SO4)
10 20 30 40 50 80 100 75 5.70 2.46 2.04 1.50 1.15 0.56 0.42
85 4.60 1.38 1.29 1.00 0.73 0.37 0.30 90 4.72 3.04 1.96 1.49 1.16 0.62 0.37 95 5.80 3.02 2.23 1.66 1.38 0.75 0.42 100 6.99 3.82 2.72 2.02 1.72 0.99 0.54 100.4 10.87 5・94 4.31 3.26 2.71 2.07 1.24 1.7三氧化硫和水混合热