肉桂酸-4-羟基化酶检测试剂盒(肉桂酸比色法)
- 格式:doc
- 大小:64.50 KB
- 文档页数:3
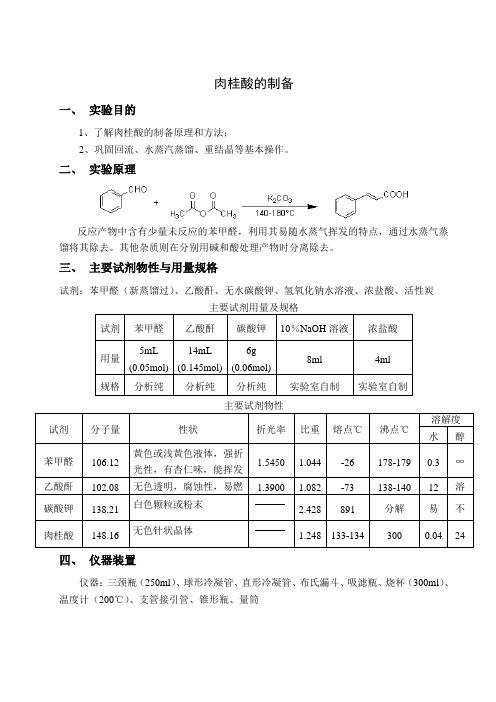
肉桂酸的制备一、实验目的1、了解肉桂酸的制备原理和方法;2、巩固回流、水蒸汽蒸馏、重结晶等基本操作。
二、实验原理反应产物中含有少量未反应的苯甲醛,利用其易随水蒸气挥发的特点,通过水蒸气蒸馏将其除去。
其他杂质则在分别用碱和酸处理产物时分离除去。
三、主要试剂物性与用量规格试剂:苯甲醛(新蒸馏过)、乙酸酐、无水碳酸钾、氢氧化钠水溶液、浓盐酸、活性炭四、仪器装置仪器:三颈瓶(250ml)、球形冷凝管、直形冷凝管、布氏漏斗、吸滤瓶、烧杯(300ml)、温度计(200℃)、支管接引管、锥形瓶、量筒图1 制备肉桂酸的反应装置图图2 水蒸气蒸馏装置图五、实验步骤及现象六、实验结果1、产品性状:浅黄色粉末;2、理论产量:7.4g ;3、实际产量:9.16g ;4、产率:123.8% ;七、实验讨论1、数据分析:A.产率过高,因为没有进行干燥处理,无法准确评估实验产率B.产物呈浅黄色,而非纯白色,说明纯度不高,应进行重结晶2、结果讨论:A.可能是电炉的功率达不到要求,回流时温度一直稳定在130-140℃,而适当的反应温度应在160-170℃,导致在水蒸气蒸馏时蒸出大量苯甲醛与水的互溶物,说明反应不完全,可能还有一些副反应产生B.产物颜色不正,可能的原因是活性炭的用量不够,脱色时间不充分;也可能是因为在水蒸气蒸馏步骤中苯甲醛没有被完全除尽,蒸馏液还是有些浑浊,非完全澄清透明,而苯甲醛为黄色或浅黄色液体。
3、实际操作对实验结果的影响:A.搭装置:回流装置的仪器必须彻底干燥(包括量取苯甲醛和醋酸酐的量筒),否则将会使乙酸酐水解而导致实验失败。
B.加料:碳酸钾不能早取,防止其受潮而使乙酸酐水解;而且必须研细,增大接触面积,使反应彻底充分。
C.回流:加热强度不可过大,否则会把乙酸酐蒸出;升温速度不可过快,缩合反应宜缓慢升温,以防苯甲醛氧化;温度应控制在160~170℃,过低会导致反应不完全,产率偏低。
D.水蒸气蒸馏:进一步巩固安全管与T形管的作用,沸石的加法,是否辅助加热。

分子植物育种(网络版), 2011年, 第9卷, 第1545-1555页 Fenzi Zhiwu Yuzhong (Online), 2011, Vol.9, 1545-1555 http://mpb. 1545研究评述 A Review木质素生物合成相关酶基因调控的研究进展吕淑萍, 倪志勇, 范玲新疆农业科学院核技术生物技术研究所, 乌鲁木齐, 830091 通讯作者: fanling@;作者分子植物育种, 2011年, 第9卷, 第75篇 doi: 10.5376/.2011.09.0075收稿日期:2011年05月03日 接受日期:2011年05月20日 发表日期:2011年06月15日这是一篇采用Creative Commons Attribution License 进行授权的开放取阅论文。
只要对本原作有恰当的引用, 版权所有人允许并同意第三方无条件的使用与传播。
引用格式:吕淑萍等, 2011, 木质素生物合成相关酶基因调控的研究进展, 分子植物育种 V ol.9 No.75 (doi: 10.5376/.2011.09.0075)摘 要 木质素是由3种不同的木质素单体聚合而成的,其含量和单体组成与植物体的许多功能密切相关。
木质素的生物合成首先是通过莽草酸途径在一系列酶的催化作用下转化为芳香族氨基酸,在苯丙氨酸解氨酶PAL 的作用下形成反式肉桂酸,经过羟基化、甲基化等一系列反应形成木质素单体,最后木质素单体聚合形成木质素。
本文根据其反应过程介绍与木质素生物合成中关键酶基因的研究进展。
此外,从木质素特异性启动子以及转录因子的调控等方面介绍了木质素生物合成基因调控的研究趋势。
完整的介绍了木质素生物合成途径及其基因调控的研究进展,并对今后的研究进行了展望。
关键词 木质素; 木质素生物合成; 基因调控Recent Advance in Study of Lignin Biosynthesis Enzymes Gene Regulatory ResearchLv Shuping , Ni Zhiyong , Fan LingInstitute of Nuclear and Biological Technologies, Urumqi, 830091, P.R. China Corresponding author, fanling@; AuthorsAbstract Lignin is a three different monomers lignin aggregate of its content and admixture with plants of the many functionsrelated. The synthesis of lignin begin with shikimic acid, it transform to aromatic amino acid under promotion of a series of enzyme. The aromatic amino acid is formed trans-cinnamic acid by PAL, then, it became lignin monomers after a series of reactions. Finally, lignin monomers aggregate form lignin. The recent advance in study of lignin biosynthesis is involved in this article by course of reaction. In addition, Lignin biosynthesis gene regulatory research would be introduced by xylem-specific promoters, and transcription factors and so on. Finally, The developments of lignin biosyn thesis and genetic regu lation are reviewed and the prospect for further development is also made herein . Keywords Lignin; Lignin biosynthesis; Gene regulation研究背景木质素是地球上数量上仅次于纤维素的有机物,占生物圈有机碳的30%(李金花等, 2007)。


脱落酸合成关键基因全文共四篇示例,供读者参考第一篇示例:脱落酸合成是一种重要的生物合成途径,其在植物内起着关键作用。
脱落酸合成能够产生一种被称为脱落酸的化合物,这种化合物在植物免疫反应、生长发育和环境适应性等方面扮演着重要角色。
脱落酸合成的过程包括多个关键基因的参与,这些基因通过编码不同的酶来共同实现脱落酸的合成。
本文将探讨脱落酸合成的关键基因及其在植物中的重要性。
脱落酸合成的关键基因包括PAL、4CL、CCR、COMT等,在这些基因编码的酶的协同作用下,植物能够顺利合成出脱落酸。
PAL(苯丙氨酸解氨酶)是脱落酸合成途径中的第一个关键酶,它能够将苯丙氨酸转化为肉桂醛,是脱落酸合成的第一步。
4CL(4-羟基肉桂酸琥珀酸还原酶)则是脱落酸合成途径中的第二个关键酶,它能够将肉桂醛转化为肉桂酸,为后续合成脱落酸奠定基础。
CCR(肉桂醇羟基化酶)和COMT(肉桂醇-O-甲基转移酶)则分别在脱落酸合成的后续步骤中发挥作用,帮助植物合成出最终的脱落酸。
脱落酸在植物中具有多重生物功能。
脱落酸被认为是一种植物的重要信号分子,能够参与植物的防御反应。
当植物受到外界胁迫时,脱落酸的合成会被启动,从而促进植物产生防御物质以应对胁迫。
脱落酸还能够调节植物的生长发育。
研究表明,脱落酸可以影响植物的细胞分裂和延长,从而影响植物的生长速度和形态。
脱落酸还被发现在植物的环境适应性中发挥作用。
在干旱、盐碱等恶劣环境下,脱落酸的合成能够促进植物的抗逆性,使其更好地适应恶劣环境的生长。
第二篇示例:脱落酸合成关键基因在植物生长发育过程中起着重要作用,它们控制着植物中脱落酸的合成和积累。
脱落酸是一种植物生长素,能够促进植物的生长和发育,调节植物的生理过程,增强植物的抗逆性。
研究脱落酸合成关键基因对于深入了解植物生长发育机制、提高植物产量和抗逆性具有重要意义。
脱落酸合成关键基因的研究主要集中在拟南芥、水稻、玉米等模式植物上。
拟南芥是一种常用的模式植物,其基因组结构简单、易于转化和遗传分析,被广泛应用于植物生理生态研究中。


烟草重要基因篇:8. 烟草P450基因作者:解敏敏来源:《中国烟草科学》2015年第02期细胞色素P450单加氧酶(cytochrome P450 monooxygenases, CYP450)是一个保守的血红素硫蛋白基因超家族,广泛存在于各种动植物、真菌和细菌中,在信号传递、防御反应以及代谢产物合成等多种代谢途径中起着重要的作用。
P450酶系可能是自然界中最具催化作用的生物催化剂,它所催化的反应类型广泛而复杂。
根据其功能,大体可以分为两类:一类是参与植物次生物质的代谢,如植物激素、信号分子、萜类、防御物质等;另一类是代谢外源信号分子或环境污染物,如农药、环境毒素、有机染料等[1-3]。
1 植物P450基因家族及功能1.1 植物P450基因家族随着植物基因组大规模测序,在越来越多的植物中鉴定到P450。
基于蛋白序列的相似性和亲缘关系,将P450归类为家族和亚家族。
同一家族的成员序列相似性>40%,序列相似性>55%归类为一个亚家族[4]。
随着P450家族成员的增多,部分低于40%的蛋白序列遗传聚类分析中明显聚在一起,它们也被归为同一家族。
植物P450超家族归类为10个氏族和127个家族,是目前为止植物中最大的酶家族[5]。
1969年,Frear[6]首次在棉花(Gossypium hirsutum)中发现P450。
目前在拟南芥(Arabidopsis thaliana)[7]、水稻(Oryza sativa) [7]、苜蓿(Medicago sativa)[3]等多种植物中都鉴定到P450。
其中对拟南芥P450的研究较为广泛深入,拟南芥基因组中含有286个P450基因,其中273个基因被分类,组成45个P450家族和72个亚家族,245个全长基因有基因组注释。
芯片数据分析显示拟南芥P450基因整体上表达量要比看家基因低,但许多基因的表达还具有组织特异性。
如CYP88A3和CYP706A2在叶中的表达高于大部分看家基因,CYP81F4和CYP88A3在根中的表达高于看家基因。
3-羟基-4-甲氧基肉桂酸3-羟基-4-甲氧基肉桂酸(3-hydroxy-4-methoxycinnamic acid)是一种天然有机化合物,属于肉桂酸类化合物。
它的化学式为C10H10O4,分子量为194.18 g/mol。
3-羟基-4-甲氧基肉桂酸常存在于植物中,如肉桂属植物、月桂属植物等。
3-羟基-4-甲氧基肉桂酸具有多种生物活性,对人体健康具有多种益处。
首先,它具有一定的抗氧化活性。
抗氧化活性是指化合物对于自由基的清除能力,能够减少自由基对细胞的损害,从而保护细胞免受氧化应激的伤害。
氧化应激是导致多种疾病的原因之一,如心血管疾病、癌症等。
3-羟基-4-甲氧基肉桂酸的抗氧化活性可以帮助减少这些疾病的风险。
3-羟基-4-甲氧基肉桂酸还具有抗炎作用。
炎症是人体对外界刺激的一种自我保护反应,但过度或慢性炎症可能导致疾病的发生和发展。
研究表明,3-羟基-4-甲氧基肉桂酸能够抑制炎症反应,减轻炎症相关疾病的症状和程度。
这使得3-羟基-4-甲氧基肉桂酸成为潜在的抗炎药物候选物。
3-羟基-4-甲氧基肉桂酸还具有抗菌活性。
研究发现,它对多种细菌和真菌都具有一定的抑制作用。
这种抗菌活性可能使得3-羟基-4-甲氧基肉桂酸成为新型抗生素的潜在来源。
抗生素是治疗细菌感染的重要药物,但由于细菌对抗生素的抗药性越来越严重,需要寻找新的抗生素来解决这一问题。
除了上述生物活性外,3-羟基-4-甲氧基肉桂酸还被发现具有抗肿瘤活性。
肿瘤是一种严重威胁人类健康的疾病,寻找有效的抗肿瘤药物一直是科学家们的目标。
研究发现,3-羟基-4-甲氧基肉桂酸可以抑制肿瘤细胞的生长和扩散,对某些肿瘤具有一定的治疗潜力。
这使得3-羟基-4-甲氧基肉桂酸成为肿瘤治疗研究的热点。
总结起来,3-羟基-4-甲氧基肉桂酸是一种具有多种生物活性的天然有机化合物。
它具有抗氧化、抗炎、抗菌和抗肿瘤活性,对人体健康具有多种益处。
然而,尽管3-羟基-4-甲氧基肉桂酸具有潜在的药用价值,但目前仍需要进一步的研究来探索其药理机制和临床应用前景。
收稿2009-02-04修定 2009-03-05资助国家“863”计划(2006AA10Z110)和国家自然科学基金(30771237)。
*通讯作者(E-mail: chaiyourong1@163.com; Tel: 023-68250744)。
原花青素的生物合成途径、功能基因和代谢工程赵文军, 张迪, 马丽娟, 柴友荣*西南大学农学与生物科技学院, 重庆400716Biosynthetic Pathway, Functional Genes and Metabolic Engineering of ProanthocyanidinsZHAO Wen-Jun, ZHANG Di, MA Li-Juan, CHAI You-Rong *College of Agronomy and Biotechnology, Southwest University, Chongqing 400716, China提要: 原花青素(PA)广泛分布于高等植物中, 与农作物的多种品质性状密切相关。
虽长期受到关注, 但其生物合成途径和主要功能基因的解析则是近年来随着拟南芥等植物突变体研究的深入才取得突破的。
PA经公共苯丙烷-核心类黄酮-原花青素复合途径而合成, 先后涉及12个关键酶(PAL、C4H、4CL、CHS、CHI、F3H、F3’H 、DFR、LDOX/ANS、LAR、ANR、LAC)的催化反应和3种转运蛋白(GST、MATE、ATPase)的胞内转运, 并有6种转录因子(WIP-ZF、MYB、bHLH、WD40、WRKY、MADS)参与调控PA的合成与积累。
这些基因在拷贝数、表达特征、蛋白亚细胞定位、蛋白互作、突变体表型等方面具有显著特点。
PA的代谢工程在牧草品质改良、农产品脱涩、油菜黄籽材料创新、葡萄和葡萄酒品质改良、茶多酚分子育种、作物抗病虫性提高、新型作物拓展等方向具有重要的应用前景, 目前仅在少数方向有所启动, 更待广泛关注和深入研究。
精细石油化工进展第14卷第2期A D V A N C E S I N FI N E P ET R O C H E M I C A LS肉桂酸合成方法研究进展蒋卫华,崔爱军(常卅l大学石油化工学院,常州213264)[摘要]以合成肉桂酸的原料为分类依据,综述了肉桂酸合成方法研究进展,重点介绍了以苯甲醛、苯乙烯、肉桂醛为反应原料的合成方法,包括Per ki n法、苯乙烯一四氯化碳法等,并对各合成工艺的优缺点进行了评述。
【关键词]肉桂酸苯甲醛苯乙烯肉桂醛合成进展肉桂酸是一种微有桂皮味的香料¨J。
在医药行业中肉桂酸可用于局部麻醉剂、抗炎、止痛、抗传染、抗癌、血管扩张剂、抗溃疡剂和低血糖等药物的制备心’3J。
农业上肉桂酸可用作长效杀菌剂、植物生长促进剂和除草剂、果蔬食品保鲜防腐剂等,最新研究还发现肉桂酸对铜绿微囊藻和斜生栅藻具有抑制作用,这为水华的生物治理找到一条安全有效的途径H J。
此外,肉桂酸还可用作测定铀和钒的试剂、分离钍的试剂、镀锌的缓蚀剂、聚氯乙烯的热稳定剂、聚氨基甲酸酯的交联剂、聚己内酰胺的阻燃剂、表面活性剂及负片型感光树脂的合成原料。
肉桂酸及其衍生物的广泛应用使其具有广阔的市场前景”。
7』。
合成肉桂酸的方法有多种,如P er ki n法、K noevenagel法、苯甲醛一丙酮法、苯甲醛一乙烯酮法、苯甲醛一醋酸法、苯乙烯一四氯化碳法、苯乙烯一一氧化碳法、苯乙烯一二氧化碳法、苯基氯甲烷一无水醋酸钠法、卤代苯一丙烯酸法、肉桂醛氧化法等。
以上方法大部分因能耗大、污染重、成本高、产率低等因素而没有实际工业应用价值,或已经被淘汰。
目前工业上生产肉桂酸的方法主要是Per ki n法和苯乙烯一四氯化碳法。
笔者以反应原料为分类依据,对肉桂酸的合成进展进行综述和评价。
1以苯甲醛为原料1.1Pe r ki n法Pe r ki n法是工业和实验室中普遍采用的合成肉桂酸的一种方法,即以苯甲醛和醋酐为原料,在弱碱的作用下醛作为受体,乙酸酐的O/一H被夺去后以负离子的形式作为给予体,进行亲核加成,最后生成肉桂酸。
北京雷根生物技术有限公司 www.leagene.com
肉桂酸-4-羟基化酶(C4H)检测试剂盒(肉桂酸比色法)
简介:
肉桂酸-4-羟基化酶是催化桂皮酸形成咖啡酸、香豆酸的酶。该酶多存在于高等植物、
酵母、菌类可溶性部分物质,属于细胞木质素合成途径中间的关键酶,研究该酶可以探讨
多种生物细胞发育过程中木质素沉积的代谢机理,为减少水果石细胞含量提高其品质提供
依据。
Leagene肉桂酸-4-羟基化酶(C4H)检测试剂盒(肉桂酸比色法)检测原理是以肉桂酸作
为底物,在酶促反应的最适条件下采用每隔一定时间测定产物生成量的方法,于分光光度
计或酶标仪290nm处检测吸光度,以吸光度变化所需酶量进行计算。该试剂盒主要用于植
物组织的裂解液或匀浆液、血清等样品中内源性的肉桂酸-4-羟基化酶活性,尤其适用于检
测水果中肉桂酸-4-羟基化酶活性。该试剂盒仅用于科研领域,不宜用于临床诊断或其他用
途。
组成:
自备材料:
1、 蒸馏水
2、 研钵或匀浆器
3、 离心管或试管
4、 低温离心机
5、 水浴锅或恒温箱
6、 比色杯或酶标板
7、 分光光度计或酶标仪
操作步骤(仅供参考):
1、 准备样品:
编号 名称 TE0407
100T
Storage
试剂(A): C4H Lysis buffer 250ml 4℃ 避光
试剂(B): C4H Assay buffer 5ml 4℃ 避光
试剂(C): NADPH 1支 -20℃
使用说明书 1份
北京雷根生物技术有限公司 www.leagene.com
①植物样品:取植物组织或水果中层果肉,加入C4H Lysis buffer,冰浴情况下充分捣碎
研磨或匀浆,离心,留取上清液,冻存,用于肉桂酸-4-羟基化酶的检测。
②血浆、血清和尿液样品:血浆、血清按照常规方法制备后可以直接用于本试剂盒的测定,
冻存,用于肉桂酸-4-羟基化酶的检测。
③细胞或组织样品:取恰当细胞或组织裂解液,如果有必要需进行适当匀浆,离心,取上
清液,冻存,用于肉桂酸-4-羟基化酶的检测。
④高活性样品:如果样品中含有较高活性的肉桂酸-4-羟基化酶,可以使用蒸馏水或C4H
Lysis buffer稀释进行恰当的稀释。
2、 配制NADPH工作液:取NADPH加入蒸馏水,充分溶解,即为NADPH工作液。该
NADPH工作液保存2周,-20℃保存3个月。
3、 加样:按照下表设置对照管、测定管,溶液应按照顺序依次加入,并注意避免产生气泡。
如果样品中的C4H活性过高,可以减少样品用量或适当稀释后再进行测定。样品的检
测最好能设置2平行管,求平均值。
4、 C4H检测:
①分光光度计检测:立即以分光光度计,比色杯光径1.0cm,以对照管为对照,测定测定
管的吸光度(A测定0)。准确孵育后,立即加入C4H终止液终止反应(备选方案),用C4H碱
性基液调节pH,以分光光度计,比色杯光径1.0cm,以对照管为对照,测定测定管的吸光
度(A测定1)。注意:加入终止液终止反应不是必须步骤,可准确孵育后直接以分光光度计,
比色杯光径1.0cm,以对照管为对照,测定测定管的吸光度(A测定1)。
②酶标仪检测:立即以酶标仪测定,其余同分光光度计检测操作。
计算:
C4H活性单位的定义:在该实验条件下,每1h吸光度变化0.01所需酶量为一个活性
单位。
组织样本C4H(U)={(A测定1-A测定0)×VT}/(W×VS×0.01×t)
式中:A测定1=孵育1h后测定管的吸光度值
A
测定0
=加入C4H Lysis buffer后立即测定的测定管吸光度值
W=组织样本的重量(g)
加入物(ml) 对照管 测定管
蒸馏水 1.657 1.607
待测样品 0.05 0.05
C4H Assay buffer - 0.05
NADPH工作液 0.043 0.043
C4H Lysis buffer 0.25 0.25
北京雷根生物技术有限公司 www.leagene.com
VT=提取酶液的总体积(ml)
VS=测定时所用酶液体积(ml)
液体样本C4H(U)=(A测定1-A测定0)/(0.01×t)
式中:A测定1=孵育1h后测定管的吸光度值
A
测定0
=加入C4H Lysis buffer后立即测定的测定管吸光度值
t=反应时间
注意事项:
1、 待测样品中不能含有酶抑制剂,同时需避免反复冻融。
2、 获得上清液为C4H酶液,应尽快检测,亦可保存。
3、 加入C4H终止液终止反应后,最好采用C4H碱性基液调节pH,以便检测更为准确。
4、 C4H碱性基液具有一定腐蚀性,请小心操作。
5、 如果没有分光光度计,也可以使用普通的酶标仪测定。但本试剂盒不推荐用酶标仪进
行检测,如需酶标仪检测,每次检测指标不宜过多,否则操作时间不一,有可能导
致样本间的差异。
6、 为了您的安全和健康,请穿实验服并戴一次性手套操作。
有效期:
6个月有效。
相关:
编号 名称
CC0007
磷酸缓冲盐溶液(10×PBS,无钙镁)
CM0004
LB培养基
DC0032
Masson三色染色液
DF0135
多聚甲醛溶液(4% PFA)
NR0001
DEPC处理水(0.1%)
PS0013
RIPA裂解液(强)
TC1167
尿素(Urea)检测试剂盒(脲酶波氏比色法)