
常见的金属离子的颜色 Company Document number:WTUT-WT88Y-W8BBGB-BWYTT-19998
过渡金属离子颜色 李蔚妮 成慧明 刘 玥 郑 萃 我们处在五彩缤纷的世界里,绚丽的大自然往往让我们惊叹不已。这一切的颜色的由来,自然是由于各种化合物丰富多彩的颜色的组合。而在有色化学物质家族中,无机金属离子无疑是里面最大的一个旁支。本文讨论几种有趣的使无机金属离子的化合物的颜色转变的方法。 一、物质显色机理 处在低能级的电子吸收某个波段的光向高能级跃迁,如果吸收的光波恰好在可见光区,则物质显出吸收光颜色的互补色。这就是化合物具有千千万万颜色的根本原因。所以要改变物质颜色,从根本上说是要改变某原子或离子的电子排布。 颜色是一种感觉,是人眼对一定波长范围的光的感性辨识。其本质是光,更本质一点说是能量。 各色光对应的电磁波长(单位:nm ): 紫色:400-430,蓝色:430-480,青色:480-500,绿色:500-560,黄色:560-590 橙色:590-620,红色:620-760; 物质之所以能够呈现出颜色是因为它们能够选择性地吸收并发射出某特定波长的电磁波,当这种电磁波的波长处在一定范围中时就会显出相应的颜色。 组成物质的分子(离子、原子)中,电子在一定的轨道范围内运动,而这种运动并不是十分稳定的,因为不同轨道的电子所具有的能量不同,电子随时可能吸收能量从低能轨道进入高能轨道,或是放出能量从高能轨道进入低能轨道,这种电子跃迁中的能量变化以电磁波的形式表现出来,其频率(υ)和两轨道能量差(E 1-E 2=ΔE )的关系: 21= E E h υ? 即:E h υ?= h c E λ?=? 其中,h 是普朗克常量:6.63?10-34 J ?s -1,c 为光速:3.0?108 m ?s -1. 而我们通常所谓的物质的颜色,是指在自然光(太阳光,可看作是连续电磁波)的照射下,电子吸收某波长的光(即吸收光子能量),跃至高能轨道,然后又迅速发射出某波长的光(即光子携带其放出的能量),回到低能轨道,所产生的混合效应: 若物质吸收光能后所发射的光在可见光范围内,此时物质的颜色,就应该是物质吸收的入射光的补色与发射光的混合色。若发射的光不在可见光范围内,则物质的颜色就决定于物质吸收入射光的补色(补色:在自然光中,去掉某一色光而产生的颜色称为反色。例如:黄的补色是蓝,橙的补色是青等。);若此时物质吸收的入射光的补色不在可见光范围内,则显白色。 二、过渡金属离子成色原因 一般来说,未成对的电子相对于成对电子更容易吸收能量发生跃迁,因此我们遇到的大多数有色物质都是含有未成对电子的,如Fe 3+,Cu 2+等。另一方面,由于有相当一部分物质的电子跃迁所产生的电磁波在可见光范围之外,因此往往表现为无色透明或是白色。而我们注意到过渡金属离子具有丰富的颜色,因为它们正好同时符合上述两个条件:
含EDTA的重金属废水解决方案 重金属废水主要来自矿山排水、有色金属冶炼厂除尘排水、有色金属加工厂酸洗水、电镀厂镀件洗涤水、钢铁厂酸洗排水,以及电解、农药、医药、烟草、油漆、颜料等工业生产。废水中的重金属并不是以单一的重金属离子形式存在,而是与一些络合物(如EDTA, DTPA, NTA)结合在一起。EDTA (乙二胺四乙酸)是螯合剂的代表性物质,此外,EDTA对土壤重金属的去除效果明显高于等量的水和阳离子表面活性剂,是目前应用最普遍的重金属污染土壤的修复剂,但这些含EDTA的重金属萃取液将会进入水体.由于 EDTA的强络合性和难生物降解性,在水体中易与碱金属、稀土元素和过渡金属等形成稳定的络合物,成为重金属离子很好的保护伞,増加了处理含 EDTA的重金属废水的难度。重金属去除剂具有在相对低的pH条件下使金属高度分离、形成的金属螯合物易于脱水和稳定等特点。因此,用重金属去除剂去除废水中溶解性重金属离子是一种有效的方法。 传统的工业处理方法是往废水中添加碱(一般是氢氧化钙、石灰石、生石灰等)提高其PH值,使镍离子、铜离子等重金属离子生成难溶性的氢氧化物沉淀,从而降低废水中重金属离子含量而达到国家规定的排放标准。但是此种方法也存在较大的弊端:1、产生较大两的污泥,密度低,含水率高,污泥处置费用较为昂贵;2、还有些金属氢氧化物沉淀是两性的,在弱酸性或者其他条件下,沉淀会溶解,重金属再次进入废水中;3、有些有机重金属废水含有大量的螯合物、络合剂、配合物等大分子有机物,这些络合剂与重金属螯合形成的物质很稳定,抑制金属氢氧化物沉淀的形成。 河北美星环保科技有限公司研发出第三代重金属去除剂产品,其具有以下特点:1、重金属去除剂能够处理EDTA重金属废水中的重金属离子.在没有EDTA 的条件下, Cd2+ ,Cu2+和Pb2+的去除率达到100%,而Zn2+的除率则比较低。 2、随着c(EDTA)的增加,废水中重金属离子的去除率下降;随着重金属去除剂的增加,废水中重金属离子的去除率上升.在相同重金属去除剂用量条件下,对废水中Cd2+,Cu2+和Pb2+的去除率Zn 高。 3、EDTA能够有效地萃取尾矿砂中的重金属,特别是对Cd和Pb具有很高的萃取率.工程实例进一步表明,重金属去除
常见过渡金属离子及化合物颜色: 一.铜副族(IB): 1.1铜化合物:焰色绿;CuF 红;CuCl 白↓;CuBr 黄↓;CuI 棕黄↓;CuCN 白↓;Cu2O 暗红;Cu2S 黑;CuF2 白;CuCl2 棕黄(溶液黄绿);CuBr2 棕;Cu(CN)2 棕黄;CuO 黑;CuS黑↓;CuSO4 无色;CuSO4·5H2O 蓝;Cu(OH)2 淡蓝↓;Cu(OH)2·CuCO3 墨绿;[Cu(H2O)4]2+蓝;[Cu(OH)4]2‐蓝紫;[Cu(NH3)4]2+ 深蓝;[CuCl4]2‐黄;[Cu(en)2]2+ 深蓝紫;炔铜红↓. 1.2 银化合物:AgOH 白(常温分解);Ag2O 黑;新制AgOH 棕黄(混有Ag2O);蛋白银(AgNO3 滴手上) 黑↓;AgF 白;AgCl 白↓;AgBr 淡黄↓;AgI 黄↓(胶体);Ag2S 黑↓;Ag4[Fe(CN)6]白↓;Ag3[Fe(CN)6] 白↓;Ag+,[Ag(NH3)2]+,[Ag(S2O3)2]3‐,[Ag(CN)2]‐无色. 1.3 金化合物:HAuCl4·3H2O 亮黄晶体;KAuCl4·1.5H2O 无色片状晶体;Au2O3 黑; H[Au(NO3)4]·3H2O 黄色晶体;AuBr 灰黄↓;AuI 柠檬黄↓. 二.锌副族(IIB): 2.1 锌化合物:ZnO 白(锌白颜料)↓;ZnI2 无色;ZnS 白↓;ZnCl2 白色晶体(溶解度极大, 水溶液酸性). 2.2 镉化合物:CdO 棕灰↓;CdI2 黄;CdS 黄(镉黄颜料)↓;HgCl2(升汞) 白色;HgNH2Cl 白↓;Hg2Cl2(甘汞) 白↓. 2.3 汞化合物:HgO 红(大晶粒)或黄(小晶粒)↓;HgI2 红或黄(微溶);HgS 黑或红↓; Hg2NI·H2O 红↓;Hg2(NO3)2 无色晶体. 2.4 ZnS 荧光粉:Ag 蓝;Cu 黄绿;Mn 橙. 三. 钪副族(IIIB):略 四.钛副族(IVB): 4.1 钛化合物:Ti3+ 紫红;[TiO(H2O2)2]2+ 橘黄;H2TiO3 白色↓;TiO2 白(钛白颜料)或 桃红(金红石)↓;(NH4)2TiCl6 黄色晶体;[Ti(H2O)6]Cl3 紫色晶体;[Ti(H2O)5Cl]Cl2·H2O 绿色晶体;TiCl4 无色发烟液体. 4.2 锆、铪:MO2,MCl4 白. 五. 钒副族(VB): 5.1 钒化合物:V2+ 紫;V3+ 绿;V4+ 蓝;V5+ 黄;VO 黑;V2O3 黑;VO2 黄;V2O5 黄或 砖红;水合V2O5 棕红;饱和V2O5 溶液(微溶) 淡黄. VO4^3‐黄。 5.2 钒酸根缩聚:随着V 原子个数的增多,由浅黄——〉深红. 5.3 铌、钽:略. 六.铬副族(VIB):
水中金属染色的影响
染色用水中的金属(铁锈等)或金属离子如果含量超标,就会影响染色质量,达不到规定的色相要求。引起色相变化的主要原因有: 1.金属离子-染料结合 金属离子-染料的结合引起色相变化 2.染浴中的金属离子化或金属离子氧化还原反应时染料的还原分解 Fe → Fe3+ + 3e Fe2+ → Fe3+ + e 3.染浴中金属离子与分散剂作用 影响染料的分散稳定性,降低上染率。 易发生金属离子-分散染料结合的染料只占少数。比如蒽醌染料。其中蒽醌类鲜红色染料,由于金属离子-分散染料结合,使色相由红转为红中带蓝。 金属离子-染料结合程度与金属离子的种类有关。Fe2+、Fe3+、Cu2+对染料影响较大。Mg2+、Ca2+对染料的影响虽然较小,但是,当浓度较高时也会对染色产生不良影响。 在染色时,为了防止金属离子的影响,可并用金属螯合剂。对于Fe2+、Fe3+、Cu2+可选用在酸~中性染浴中有效的含EDTA或NTA的金属螯合剂。而对 Mg2+、Ca2+一般可使用聚羧酸类金属螯合剂。 但是,伴随着金属离子化而产生的还原反应,用金属螯合剂是无法解决的,必须另想办法解决。 染浴中如果含有铁粉,Fe离子化成Fe2+ 或Fe3+时产生还原性,离子被金属螯合剂螯合。比如Fe2+与金属螯合剂结合后:Fe2+-EDTA=Fe3+-EDTA+e,因此仅使用金属螯合剂是无法防止还原的。 使用氧化剂能有效防止还原影响,但是剂量得适当。染浴Fe2+含有量为500ppm时,添加1g/L的氯酸钠即可。如果用量过多,氯酸纳的氧化性会对染料产生不良影响,因此不希望使用氯酸纳。金属含量较少时,可使用间硝基苯磺酸纳(Sodium Metanitro benzne Sulfonate)等防止还原。 酸性染浴易引起铁粉或Fe2+等的还原分解。由还原分解引起的不良影响请看下表所示例子。 实际上,由助剂引起的还原分解在日常生产中较为常见。在使用易受影响的染料染色时,建议并用没有还原分解反应的助剂。
螯合剂的种类及其在不同pH值条件下螯合剂的螯合常数 一、螯合剂与螯合物 具有可供配位孤电子对的分子、原子或离子的化合物能够与具有空轨道的金属离子形成配位键,该化合物称为络合物,如能与配位金属离子形成环状结构的化合物称为螯合剂,形成的络合物称为螯合物。螯合剂中至少含有一对孤电子对,而金属离子必须有空的价电子轨道,孤电子对填充入金属离子空轨道,电子对属2个原子共享,形成配位键,中心金属离子空轨道杂化。不同的提供孤电子对的配位体分别与不同金属离子形成正四面体、正六面体、正八面体的螯合物。 1.类型 1.1无机类螯合剂 聚磷酸盐螯合剂: 主要是三聚磷酸钠(STPP)、六偏磷酸钠、焦磷酸钠为主,含磷酸基空间配位基团。 特点:高温下会发生水解而分解,使螯合能力减弱或丧失。而且其螯合能力受pH值影响较大,一般只适合在碱性条件下作螯合剂。 1.2有机类螯合剂 形态分析表明螯合剂提取的重金属主要来源于可交换态或酸溶态、还原态和氧化态。1.21羧酸型 (1)氨基羧酸类:含羧基和胺(氨基)配位基团, 如乙二胺四乙酸(EDTA),氨基三乙酸(又称次氮基三乙酸NTA),二亚乙基三胺五乙酸(DTPA)及其盐等。如:EDTA的4个酸和2个胺(—NRR′)的部分都可作为配体的齿,两个氮原子和四个氧原子可提供形成配位键的电子对。 特点:络合能力强,络合稳定常数大,耐碱性好,但分散力弱且不易被生物降解。(2)羟基羧酸类含羟基、羧基配位基团 这类羧酸主要是柠檬酸(CA)、酒石酸(TA)和葡萄糖酸(GA)。 特点:可生物降解,在酸性条件下羟基与羧基不会离解为氧负离子,因而络合能力很弱,不适宜在酸性介质中应用。 (3)羟氨基羧酸类 这类酸用作螯合剂的典型代表是羟乙基乙二胺三乙酸(HEDTA)和二羟乙基甘氨酸
各个价态的铬的化合物或离子的颜色 Cr[铬]:蓝白色金属 Cr2O3[三氧化二铬]:绿色固体 Cr(OH)3[氢氧化铬]:灰蓝色固体 Cr2(SO4)3[硫酸铬]:桃红色固体 Cr(2+)[二价铬离子]:蓝色离子 Cr(3+)[三价铬离子]:紫色离子 Cr(OH)4 (-)[四氢氧化铬离子]:亮绿色离子 CrO4(2-)[铬酸根离子] :橙黄色离子 CrO2(-)[二氧化铬离子]:绿色离子 Cr2O7(2-)[重铬酸根离子]:橙红色离子 Cr2(SO4)3·6H2O[硫酸铬晶体]:绿色晶体 CrCl3?6H2O[氯化铬晶体]就有三种异构体 [Cr(H2O)6]Cl3[氯化铬晶体]:紫色晶体 [Cr(H2O)5Cl]Cl2?H2O[氯化铬晶体]:浅绿色晶体[Cr(H2O)4Cl2]Cl?2H2O[氯化铬晶体]:暗绿色晶体(NH4)2Cr2O7[重铬酸铵]:橘色固体 K2Cr2O7[重铬酸钾]:橙红色固体 CrO4(2?)[铬酸根离子]:黄色离子 Na2CrO4[铬酸钠]:黄色固体
K2CrO4[铬酸钾]:黄色固体 PbCrO4[铬黄、铬酸铅]:黄色固体 (NH4)2CrO4[铬酸铵]:黄色固体 C5H4N·HCrO3Cl[氯铬酸吡啶盐]:橙黄色晶体 Cr2(OAc)4(H2O)2[乙酸亚铬]:深红色晶体 CrO3[三氧化铬]:暗红色固体 Cr(NO3)3[硝酸铬]:红紫色固体 H2Cr2O7[重铬酸]:橘红色固体 H2CrO4[铬酸]:橙黄色固体 CrO2Cl2[铬酰氯]:暗红色液体 CrCl3[氯化铬]:紫色结晶 NH4[Cr(NCS)4(NH3)2]?H2O[硫氰酸铬铵]:暗红色固体(Fe?Mg)Cr2O4[铬铁矿]:黑色固体 Cr?Al2O3[红宝石];红色固体、褐色固体、紫色固体 Ag2CrO4[铬酸银]:砖红色固体 BaCrO4[铬酸钡]:黄色固体 [Cr(H2O)6](3+)[六水化铬离子]:紫色离子 [Cr(H2O)4(NH3)2](3+)[二氨四水化铬离子]:紫红色离子[Cr(H2O)3(NH3)3](3+)[三氨三水化铬离子]:浅红色离子[Cr(H2O)2(NH3)4](3+)[四氨二水化铬离子]:橙红色离子[Cr(H2O)(NH3)5](3+)[五氨一水化铬离子]:橙黄色离子[Cr(NH3)6](3+)[六氨化铬离子]:黄色离子
三种常见的处理方法的比较 一、石灰中和法 1.1基本原理 石灰中和反应法是在含重金属离子废水中投加消石灰C a( O H ) : , 使它和水中的重金属离子反应生成离子溶度积很小的重金属氢氧化物。通过投药量控制水中P H 值在一定范围内, 使水中重金属氢氧化物的离子浓度积大于其离子溶度积而析出重金属氢氧化物沉淀, 达到去除重金属离子, 净化废水的目的。 将废水收集到废水均化调节池,通过耐腐蚀自吸泵将混合后的废水送至一次中和槽,并且在管路上投加硫酸亚铁溶液作为砷的共沉剂(添加量为Fe/As=10),同时投加石灰乳进行充分搅拌反应,搅拌反应时间为30 min,石灰乳投加量由pH 计自动控制,使一次中和槽出口溶液pH值为7.0;为了使二价铁氧化成三价铁,产生絮凝作用,在一次中和槽后设置氧化槽,进行曝气氧化,经氧化后的废水自流至二次中和槽,再投加石灰乳,石灰乳投加量由pH计自动控制,使二次中和槽出口溶pH值为9~11;在二次中和槽废水出口处投加3号凝聚剂(投加浓度为10 mg/L),处理废水自流至浓密机,进行絮凝、沉淀;上清液自流至澄清池,传统的石灰中和处理重金属废水流程如下: 石灰一段中和及氢氧化钠二段中和时,各种重金属去除率随pH不同而沉淀效果不同,不同的金属的溶度积随PH不同而不同。同一PH所以对重金属的沉淀效果不一样,而废水中的重金属通常不只一种,根据重金属的含量在进水时把配合调到某金属在较低ph溶度积最高时对应的PH。加石灰乳进行中和反应,沉淀废水中的大部分金属。上清液进入下一个调节池,进入调节PH ,进入二次中和反应池,除去剩余的重金属离子。 1.2 石灰中和沉淀的优缺点 采用石灰石作为中和剂有很强的适应性,还具有废水处理工艺流程短、设备简单石灰就地可取,价格低廉,废水处理费用很低,渣含水量较低并易于脱水等优点,但是,石灰中和处理废水后,生成的重金属氢氧化物———矾花,比重小,在强搅拌或输送时又易碎成小颗粒,所以它的沉降速度慢。往往会在沉降分离过程中随水流外溢,又使处理后的废水浊度升高,含重金属离子仍然超标。要求废水不含络合剂如C N 一、N H 。等, 否则水中的重金属离子就会和络合剂发生络合反应, 生成以重金属离子为中心离子以络合剂为配位体的复杂而又稳定的络离子, 使废水处理变得复杂和困难。已沉降的矾花中和渣泥的含水率极高(达99%以上),其过滤脱水性能又很差,加上组成复杂、含重金属品位又低,这给综合回收利用与处置带来了困难,甚至造成二次污染。此外,渣量大,不利于有价金属的回收,也易造成二次污染II。用石灰水处理的重金属废水。由于不同重金属与OH的结合在同一PH下不同,同一金属在不同PH下的溶度积不同。所以,用传统的石灰法处理重金属含量较多的复杂的废水,显然不行,首先某些重金属不能达标排放,其次,处理废水中含钙比较多。在冶炼厂,很难循环使用。 二、硫化沉淀法
EDTA是目前最常用的测定各类金属离子的络合滴定剂,大部分金属离子可以直接滴定其含量,少部分由于动力学原因需要借助返滴定或置换滴定测定。下面我们将对于实验室常见的15种金属离子的EDTA滴定法进行整理。 金属离子如未特殊说明,默认配制成酸性的0.02 mol·L-1的标准溶液,每组测定取25.00 mL。准确加入意味着需要准确知道溶液的浓度和体积。 1.镁、钙 稀释溶液体积至100 mL,加入10 mL氨性缓冲溶液(6.75 g氯化铵、57 mL氨水定容至100 mL),加入铬黑T(钙镁均可)或钙指示剂(仅限钙),滴定至终点溶液颜色由紫红色变为天蓝色。 注意事项:镁存在下测定钙时,用氢氧化钠调节pH使镁沉淀,此时应增加溶液体积,减少氢氧化镁沉淀对钙指示剂的吸附。 2.铝(返滴定或置换滴定) 稀释溶液体积至100 mL,准确加入过量EDTA标准溶液,再加入15 mL醋酸缓冲溶液(60 g醋酸钠、2 mL冰乙酸定容至100 mL),加热煮沸3 min,加入PAN指示剂,用Cu2+标准溶液滴定至终点溶液颜色变为紫红色。加入1~2 g氟化钠后煮沸,再用Cu2+标准溶液滴定至终点溶液颜色变为紫红色。 注意事项:通常采用第二步置换滴定测得的结果。 3.锰(II) 稀释溶液体积至100 mL,用氨水(1+1)调节pH到10,再加入25 mL氨性缓冲溶液(6.75 g氯化铵、57 mL氨水定容至100 mL),加入K-B混合指示剂,滴定至终点溶液颜色由紫红色变为纯蓝色。 注意事项:高价锰可用盐酸羟胺还原后测定。 4.铁(III) 用盐酸(1+1)调节pH到2,水浴加热至60℃,加入Ssal指示剂,滴定至终点溶液颜色由紫红色变为无色或淡黄色。 注意事项:二价铁可用过氧化氢氧化至三价后测定。pH需在1.3 ~ 2之间,太低络合不定量,太高铁离子水解沉淀。 5.钴(II)(返滴定) 准确加入过量EDTA标准溶液,再加入10 mL醋酸缓冲溶液(20 g醋酸钠、2.6 mL冰乙酸定容至100 mL),稀释溶液体积至100 mL,加入PAN或二甲酚橙,用Cu2+标准溶液或Zn2+标准溶液滴定至终点溶液颜色变为紫红色。 注意事项:钴(III)可用过氧化氢还原至钴(II)后测定。可尝试在80℃下直接滴定。 6.镍(返滴定) 稀释溶液体积至100 mL,准确加入过量EDTA标准溶液,再加入2 g六次甲基四胺,加入二甲酚橙,用Zn2+标准溶液滴定至终点溶液颜色变为紫红色。 7.铜 稀释溶液体积至100 mL,加入10 mL氨性缓冲溶液(6.75 g氯化铵、57 mL氨水定容至100 mL),加入PAN指示剂,滴定至终点溶液颜色由紫色变为墨绿色。 8.锌 稀释溶液体积至100 mL,加入2 g六次甲基四胺,加入二甲酚橙或铬黑T,滴定至终点溶液颜色由紫色变为黄色。
化学中常见颜色 有色都有毒,有色都刺激。 1、有色气体:F2(淡黄绿色)、Cl2(黄绿色)、Br2(g)(红棕色)、I2(g)(紫红色)、NO2(红棕色)、O3(淡蓝色),其余均为无色气体。 2、有刺激性气味的气体:HF、HCl、HBr、HI、NH 3、SO2、NO2、F2、Cl2、Br2(g);有臭鸡蛋气味的气体:H2S。 3、极易溶于水能做喷泉实验的气体:NH3、HF、HCl、HBr、HI;能溶于水的气体:CO2、SO2、Cl2、Br2(g)、H2S、NO2。 4、易液化的气体:NH3、Cl2。 5、有毒的气体:F2、HF、Cl2、H2S、SO2、CO、NO2、NO、Br2(g)、HCN。 6、在空气中易形成白雾的气体:NH3、HF、HCl、HBr、HI。 7、常温下不能共存的气体:H2S和SO2、H2S和Cl2、HI和Cl2、NH3和HCl、NO和O2、F2和H2。 8、其水溶液呈酸性的气体:HF、HCl、HBr、HI、H2S、SO2、CO2、NO2、Br2(g)。 可使湿润的红色石蕊试纸变蓝的气体:NH3。 9、有漂白作用的气体:Cl2(有水时)和SO2,但两者同时使用时漂白效果减弱。检验Cl2常用Cl2能使湿润的紫色石蕊试纸先变红后褪色。 10、能使澄清石灰水变浑浊的气体:CO2和SO2,但通入过量气体时沉淀又消失。 11、在空气中可以燃烧的气体:H2、CO、CH4、C2H4、C2H2、H2S。在空气中燃烧火焰呈蓝色(或淡蓝色)的气体:H2S、H2、CO、CH4。 12、具有强氧化性的气体:F2、Cl2、Br2(g)、NO2、O2、O3;具有强或较强还原性的气体:H2S、H2、CO、NH3、HI、HBr、HCl、NO;SO2和N2既具有氧化性又具有还原性。 13、与水可反应的气体:Cl2、F2、NO2、Br2(g)、CO2、SO2、NH3;其中Cl2、NO2、Br2(g)与水的反应属于氧化还原反应(而且都是歧化反应),只有F2与水剧烈反应产生O2。 14、能使湿润的淀粉碘化钾试纸变蓝的气体:Cl2、NO2、Br2(g)、O3。 15、能使溴水和酸性高锰酸钾溶液褪色的气体:H2S、SO2、C2H4、C2H2。 16、可导致酸雨的主要气体:SO2; 导致光化学烟雾的主要气体:NO2等氮氧化物和烃类; 导致臭氧空洞的主要气体:氟氯烃(俗称氟利昂)和NO等氮氧化物; 导致温室效应的主要气体:CO2和CH4等烃;
过渡金属化合物的颜色 ——从晶体场理论到角重叠模型 北京大学化学与分子工程学院2008级 覃翔 00810132 郑雨晴 00810073 王熠 00810067 郭银梁 00810117 曹怀卿 00810027
摘要 本文将从晶体场理论入手,利用角重叠模型深入讨论过渡金属离子及化合物的显色机理,以及影响过渡金属离子及化合物颜色的各种因素。最后加以总结。 关键词 过渡金属 颜色 晶体场理论 配位场理论 角重叠模型d-d跃迁 电荷迁移 目录 1引言 2过渡金属离子及化合物显色机理 2.1颜色的产生 2.2晶体场理论(CFT) 2.3对晶体场理论的补充 2.3.1对d轨道分裂能的进一步解释 2.3.2s,p,d,f轨道的简并性 2.3.3群论 2.3.4配位场理论 2.4角重叠模型(AOM) 2.4.1角重叠模型的基本概念 2.4.2影响重叠积分的因素 2.4.3角重叠模型对σ配体的解释 2.4.4角重叠模型对π配体的解释 2.5电子光谱 2.5.1配位场光谱 2.5.2配位体光谱 2.5.3电荷迁移光谱 3影响过渡金属离子及化合物颜色的因素 4总结 5参考文献 6附录
1.引言 我们在做化学实验的时候,往往会着迷于、惊叹于奇妙的实验现象,而反应过程中奇异的颜色变化是众多实验现象中最能吸引我们的一部分。强烈的求知欲促使我们探究颜色变化的奥秘。比如: 为什么氯化银、溴化银、碘化银颜色依次加深? 白色的氢氧化亚铁被氧化成红褐色的氢氧化铁过程中灰绿色的物质是什么? 为什么氯化钴晶体随着结晶水数目不同,颜色会有明显变化? 为什么铬元素的盐会有如此多种不同的颜色? …… 这仅仅是在实验室中发现的,大自然更加多彩多姿、更加奇妙无比。本文仅仅是从过渡金属颜色这一小的方面来初探颜色的奥秘。 2. 过渡金属离子及化合物显色机理 2.1 颜色的产生 颜色是人对光产生的一种感觉,当一束光的波长在一定范围内时,这束光就可以被人眼看到,人就可以感觉到这束光的颜色。这个范围是400nm‐770nm。我们看到的光除了由光源直接发射的光之外,大多数是由物体反射的光。物体除了反射光以外,也在吸收光,吸收光的波长与反射光波长一致,而且它们所能吸收的光是限定的,即它们只能吸收某一波长或波长范围的光。这一点是由物体自身的结构决定。大量事实表明,对于过渡金属元素来说,其d电子的状态是影响其颜色的决定性因素(对于镧系、锕系的元素,f电子同样影响重大)。下面将详细说明。 还有一点需要提及,当我们在复色光(比如白光)中去掉一种波长的光时,它的补色光将会很明显的被观察到,这被称之为减色效应。 2.2 晶体场理论 过渡金属极易形成配合物(在水溶液中几乎全部以配离子形式存在),它们的配离子也具有颜色。晶体场理论可以很好的解释配合物的颜色。 晶体场理论的基本要点有如下三条: 1.配合物中正负离子之间的相互作用是纯粹的静电作用。中心离子与配体之间通过这种作用力形成化学键,放出能量。 2.d轨道能级的分裂。过渡金属元素有5个d轨道,分别是d xy,d yz,d xz,d x2‐y2,d z2。这五个轨道能量彼此相等(因此也被称为简并轨道)。它们在空间直角坐标系中取向如图: 过渡金属离子最易形成八面体构型配合物和四面体构型配合物。我们构造一个中心位于坐标原点、棱与坐标轴平行的立方体。当形成八面体配合物时,配体从±x,±y,±z六个方向(即
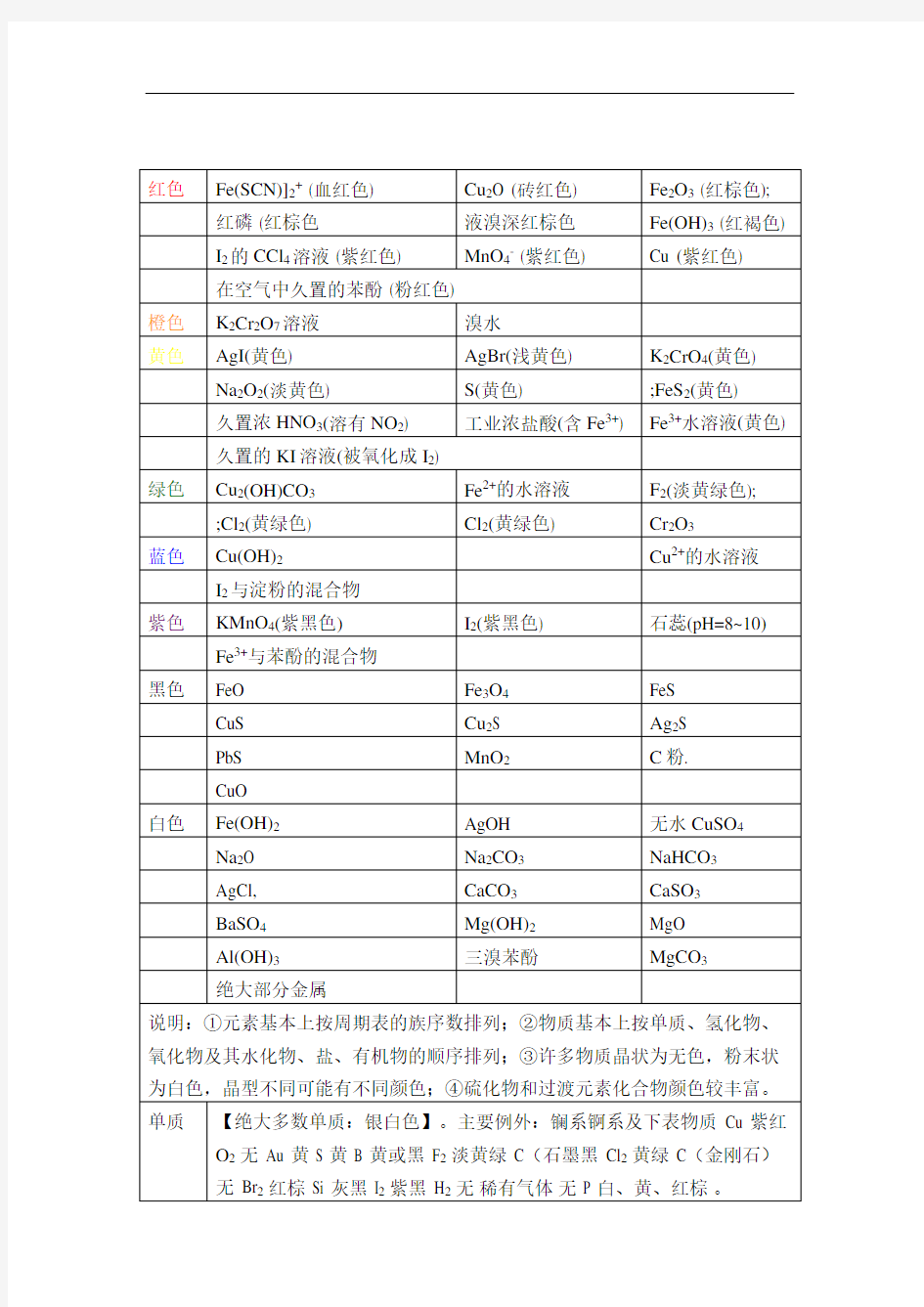
[Fe(SCN)6]3- 血红 [Pt(NH3)4}2+ 顺式绿色反式黄色 Fe3+与苯酚的配合物紫色 Fe3+与CO的配合物血红 二茂铁橙黄色 铝与铝试剂的配合物玫瑰色 1.红色Fe(SCN)]2+(血红色);Cu2O(砖红色);Fe2O3(红棕色);红磷(红棕色);液溴(深红棕色);Fe(OH)3(红褐色);I2的CCl4溶液(紫红色);MnO4-(紫红色);Cu(紫红色);在空气中久置的苯酚(粉红色). 2.橙色:溴水;K2Cr2O7溶液. 3.黄色:AgI(黄色);AgBr(浅黄色);K2CrO4(黄色);Na2O2(淡黄色);S(黄色);FeS2(黄色);久置浓HNO3(溶有NO2);工业浓盐酸(含Fe3+);Fe3+水溶液(黄色);久置的KI溶液(被氧化I2) 4.绿色:Cu2(OH)CO3;Fe2+的水溶液;;Cl2(黄绿色);F2(淡黄绿色);Cr2O3 5.蓝色:Cu(OH)2;;Cu2+的水溶液;I2与淀粉的混合物. 6.紫色:KMnO4(紫黑色);I2(紫黑色);石蕊(pH=8--10);Fe3+与苯酚的混合物. 7.黑色:FeO,Fe3O4,FeS,CuS,Cu2S,Ag2S,PbS,CuO,MnO2,C粉. 8.白色:Fe(OH)2,AgOH,无水 CuSO4,Na2O,Na2CO3,NaHCO3,AgCl,BaSO4,CaCO3,CaSO3,Mg(OH)2, Al(OH)3,三溴苯酚,MgO,MgCO3,绝大部分金属等. 一、单质绝大多数单质:银白色。 Cu 紫红 O2 无 Au 黄 S 黄 B 黄或黑 F2 淡黄绿 C(石墨黑 Cl2 黄绿 C(金刚石)无 Br2 红棕 Si 灰黑 I2 紫黑 H2 无稀有气体无 P 白、黄、红棕。 二、氢化物 LiH等金属氢化物:白 NH3等非金属氢化物:无 三、氧化物大多数非金属氧化物:无主要例外: NO2 棕红 N2O5和P2O5 白 N2O3 暗蓝ClO2 黄
重金属离子有哪些?重金属离子主要是Cr6+、U6+、Te3+、Co3+、Se6+、Pu3+、Hg2+,Mn4+等 备注:重金属,特别是汞、镉、铅、铬等具有显著和生物毒性。它们在水体中不能被微生物降解,而只能发生各种形态相互转化和分散、富集过程(即迁移)。 哪些重金属离子可以使蛋白质变性 下面一段是我从我的化学选修书上摘下来的(自己打上来的): 蛋白质受热到一定温度就会发生不可逆的凝固,凝固后不能在水中溶解,这种变化叫做变性。除了加热以外,在紫外线、X射线、强酸、强碱,铅、铜、汞等重金属的盐类,以及一些有机化合物如甲醛、酒精、苯甲酸等作用下,蛋白质均能发生变性。蛋白质变性后,不仅丧失了原有的可溶性,同时也失去了生理活性。 重金属指比重大于5的金属,(一般指密度大于4.5克每立方厘米的金属)约有45种,如铜、铅、锌、铁、钴、镍、锰、镉、汞、钨、钼、金、银等。尽管锰、铜、锌等重金属是生命活动所需要的微量元素,但是大部分重金属如汞、铅、镉等并非生命活动所必须,而且所有重金属超过一定浓度都对人体有毒。 铁锰同时存在的地下水中,要测锰离子浓度,如何消除铁离子对它的影响? 最近在测定地下水锰离子浓度的时候,铁离子发生很大的干扰,我不知道如何消除,我用的方法是高碘酸钾分光光度法测定锰,不过高碘酸钾好像和铁也反应,导致测试结果偏高!有没有高手能解决这个问题的?小弟先谢谢了!注意:曝气除铁在测定锰,这种方法不能用,因为氢氧化铁会吸附锰离子,导致测试结果偏低。
这是典型的共存离子的干扰和消除。常采用A 控制酸度B 加掩蔽剂C 分离干扰离子 所以建议:可加入氟化钠,使其与铁离子生成无色络合物[FeF6]3- 来消除干扰。 1楼的方法是看到3价铁离子可以和铁单质反应生成亚铁离子,但这种方法不推荐,因为高碘酸存在强氧化性,即使不存在氧化性,亚铁离子本身也存在绿颜色 重金属捕捉剂 一、重金属捕捉剂别名: 重金属离子捕捉剂、重金属离子捕集剂、重金属离子去除剂、重金属离子吸附剂、重金属离子螯合剂等 二、应用范围: 在常温下与较宽的PH范围内能与废水中Hg 、Cd 、Cu 、Pb 、Mn 、Ni 、Zn 、Cr3+等多种重金属离子迅速反应,生成不溶于水的絮状沉淀物,并能生成较大的矾花,从而达到捕集去除重金属离子的目的。 1、常规重金属废水处理,矿山、电镀、电子、线路板等行业排放废水重金属离子捕捉。 2 、核电站反应堆、铀钍的湿法冶金厂、医院、同位素试验堆及生产堆等放射性废水金属离子捕捉。 3、应用在垃圾焚烧发电方面的飞灰重金属治理方面有独特功效。 三、稳定性与灵敏性 1、稳定性: 本品与重金属离子形成稳定的聚合物,在强酸和强碱性环境下均不会析出重金属离子,在-100度至300度的温度范围内重金属螯合物也非常稳定,在自然环境条件下,可保持长达数百年的聚合物稳定性。
浅谈过渡金属配合物的颜色 能源1103班邬娇娇通过对基础化学学科的学习,我了解了一些基本的关于过渡金属配合物的知识。在这里我想浅显地谈一些我对过渡金属配合物丰富的颜色及其形成原因、影响其颜色的因素的认识。 一、过渡金属配合物的颜色:(见附表) 二、过渡金属配合物的形成原因: (1)颜色的形成 颜色是人对光产生的一种感觉,当一束光的波长在一定范围内时,这束光就可以被人眼看到,人就可以感觉到这束光的颜色。这个范围是400nm‐770nm。我们看到的光除了由光源直接发射的光之外,大多数是由物体反射的光。物体除了反射光以外,也在吸收光,吸收光的波长与反射光波长一致,而且它们所能吸收的光是限定的,即它们只能吸收某一波长或波长范围的光。这一点是由物体自身的结构决定。大量事实表明,对于过渡金属元素来说,其 d 电子的状态是影响其颜色的决定性因素(对于镧系、锕系的元素,f 电子同样影响重大)。 还有一点需要提及,当我们在复色光(比如白光)中去掉一种波长的光时,它的补色光将会很明显的被观察到,这被称之为减色效应。物质吸收的颜色于物质呈现的颜色互为补色。 下表位物质吸收颜色于物质呈现颜色的互补关系。
(2)晶体场理论解释过渡金属配合物颜色的形成 含d1~d9的过渡金属配离子,由于d轨道没有充满,d 电子可以吸收某一波长的可见光能量而从能量较低的t2g轨道跃迁至能量较高的e g轨道(称之为d‐d 跃迁),从而使得被吸收的光的补色可见(减色效应),因此过渡金属离子显色。 d‐d 跃迁的能量恰好等于轨道之间的分裂能Δ0 E(e g)-E(t2g)=Δ0=hν=hc/λ c:光速,c=2.9979×1010 cm/s h:Planck常数,h=6.6262×10-34J·s 故光能与波数(ν=1/λ,单位: cm-1)成正比 配离子吸收光的能量一般为10000~30000cm-1,包括了全部可见光区,因而配离子一般都有颜色。 故由上可知,配离子形成的化合物有颜色的两个条件是:d 轨道上的电子没有全充满。配离子吸收光的能量在可见光能量范围之内。 三、影响过渡金属配合物的颜色的因素:
重金属对人体的危害 一、什么叫重金属 重金属指比重大于4或5的金属,约有45种,如铜、铅、锌、铁、钴、镍、锰、镉、汞、钨、钼、金、银等。尽管锰、铜、锌等重金属是生命活动所需要的微量元素,但是大部分重金属如汞、铅、镉等并非生命活动所必须,而且所有重金属超过一定浓度都对人体有毒。 从环境污染方面看,重金属是指汞、镉、铅以及“类金属”-----砷等生物毒性显著的重金属。对人体毒害最大的有5种:铅、汞、砷、镉。这些重金属在水中不能被分解,人饮用后毒性放大,与水中的其他毒素结合生成毒性更大的有机物。 二、废水中重金属的来源 1.铅的来源。 水体中的铅一般来自于冶炼、制造和使用铅制品的工矿企业,尤其是来自有色金属冶炼过程中所排出的含铅废水、废气和废渣。铅常被用作原料应用于蓄电池、电镀、颜料、橡胶、农药、燃料等制造业。铅板制作工艺中排放的酸性废水(pH<3)铅浓度最高,电镀废液产生的废水铅浓度也很高。 2.镉的来源。 镉是一种灰白色的金属,自然界中主要以二价形式存在。镉电镀可以为钢、铁等提供一种抗腐蚀性的保护层,具有吸附性好且镀层均匀光洁等特点,因此工业上90%的福用于电镀颜料、塑料稳定剂、合金及电池等行业,含镉废水的来源还包括金属矿山的采选、冶炼、电解、农药、医药、电镀、纺织印染等行业的生产过程中。 3.汞的来源。 汞俗称水银,是地壳中相当稀少的一种元素。但是当今社会人类活动很大程度上造成了水体汞污染。水体中汞污染主要来自氯碱、塑料、电池、电子等工业排放的废水以及废旧医疗器械的处置。除此之外,节能灯和荧光灯的废弃也会带来汞污染。中国就是全球汞使用量和排放量最大的国家。 4.砷的来源 砷污染的主要来源为:(1)砷化物的开采和冶炼。特别是在我国流传广泛的土法炼砷,常造成砷对环境的持续污染;(2)在某些有色金属的开发和冶炼中,常常有或多或少的砷化物排出,污染周围环境;(3)砷化物的广泛利用,如含砷农药的生产和使用,又如作为玻璃、木材、制革、纺织、化工、陶器、颜料、化肥等工业的原材料,均增加了环境中的砷污染量;(4)煤的燃烧,可致不同程度的砷污染。 5.铜的来源 铜的化合物以一价或二价状态存在。在天然水中,溶解的铜量随pH值的升高而降低。在冶炼、金属加工、机器制造、有机合成及其他工业的废水中都含有铜,
重金属离子有哪些? 重金属离子主要是Cr6+、U6+、Te3+、Co3+、Se6+、Pu3+、Hg2+,Mn4+等备注:重金属,特别是汞、镉、铅、铬等具有显著和生物毒性。它们在水体中不能被微生物降解,而只能发生各种形态相互转化和分散、富集过程(即迁移)。 哪些重金属离子可以使蛋白质变性 下面一段是我从我的化学选修书上摘下来的(自己打上来的): 蛋白质受热到一定温度就会发生不可逆的凝固,凝固后不能在水中溶解,这种变化叫做变性。除了加热以外,在紫外线、X射线、强酸、强碱,铅、铜、汞等重金属的盐类,以及一些有机化合物如甲醛、酒精、苯甲酸等作用下,蛋白质均能发生变性。蛋白质变性后,不仅丧失了原有的可溶性,同时也失去了生理活性。 重金属指比重大于5的金属,(一般指密度大于4.5克每立方厘米的金属)约有45种,如铜、铅、锌、铁、钴、镍、锰、镉、汞、钨、钼、金、银等。尽管锰、铜、锌等重金属是生命活动所需要的微量元素,但是大部分重金属如汞、铅、镉等并非生命活动所必须,而且所有重金属超过一定浓度都对人体有毒。 铁锰同时存在的地下水中,要测锰离子浓度,如何消除铁离子对它的影响? 最近在测定地下水锰离子浓度的时候,铁离子发生很大的干扰,我不知道如何消除,我用的方法是高碘酸钾分光光度法测定锰,不过高碘酸钾好像和铁也反应,导致测试结果偏高!有没有高手能解决这个问题的?小弟先谢谢了!注意:曝气除铁在测定锰,这种方法不能用,因为氢氧化铁会吸附锰离子,导致测试结果偏低。 这是典型的共存离子的干扰和消除。常采用A 控制酸度B 加掩蔽剂C 分离干扰离子 所以建议:可加入氟化钠,使其与铁离子生成无色络合物[FeF6]3- 来消除干扰。 1楼的方法是看到3价铁离子可以和铁单质反应生成亚铁离子,但这种方法不推荐,因为高碘酸存在强氧化性,即使不存在氧化性,亚铁离子本身也存在绿颜色 重金属捕捉剂 一、重金属捕捉剂别名:
中学化学常见粒子颜色汇总 1.红色Fe(SCN)]2+(血红色);Cu2O(砖红色);Fe2O3(红棕色);红磷(红棕色);液溴(深红棕色); Fe(OH)3(红褐色);I2的CCl4溶液(紫红色);MnO4-(紫红色);Cu(紫红色); 在空气中久置的苯酚(粉红色). 2.橙色:溴水;K2Cr2O7溶液. 3.黄色:AgI(黄色);AgBr(浅黄色);K2CrO4(黄色);Na2O2(淡黄色);S(黄色);FeS2(黄色);久置 浓HNO3(溶有NO2);工业浓盐酸(含Fe3+);Fe3+水溶液(黄色);久置的KI溶液(被氧化成I2) 4.绿色:Cu2(OH)2CO3;Fe2+的水溶液;FeSO4.7H2O;Cl2(黄绿色);F2(淡黄绿色);Cr2O3 5.蓝色:Cu(OH)2;CuSO4.5H2O;Cu2+的水溶液;I2与淀粉的混合物. 6.紫色:KMnO4(紫黑色);I2(紫黑色);石蕊(pH=8--10);Fe3+与苯酚的混合物. 7.黑色:FeO,Fe3O4,FeS,CuS,Cu2S,Ag2S,PbS,CuO,MnO2,C粉. 8.白色:Fe(OH)2,AgOH,无水CuSO4,Na2O,Na2CO3,NaHCO3,AgCl,BaSO4,CaCO3, CaSO3,Mg(OH)2,Al(OH)3,三溴苯酚,MgO,MgCO3,绝大部分金属等. 一、单质绝大多数单质:银白色。 Cu 紫红O2无Au 黄S 黄B 黄或黑F2淡黄绿C(石墨黑Cl2黄绿C(金刚石)无Br2红棕Si 灰黑I2紫黑H2无稀有气体无P 白、黄、红棕。 二、氢化物LiH等金属氢化物:白NH3等非金属氢化物:无 三、氧化物大多数非金属氧化物:无 主要例外:NO2棕红N2O5和P2O5白N2O3暗蓝ClO2黄 大多数主族金属的氧化物:白 主要例外:Na2O2浅黄PbO 黄K2O 黄Pb3O4红K2O2橙Rb2O 亮黄Rb2O2棕Cs2O 橙红Cs2O2黄大多数过渡元素氧化物有颜色MnO 绿CuO 黑MnO2黑Ag2O 棕黑FeO 黑ZnO 白Fe3O4黑Hg2O 黑Fe2O3红棕HgO 红或黄Cu2O 红V2O5橙 四、氧化物的水化物大多数:白色或无色其中酸:无色为主碱:白色为主 主要例外:CsOH 亮黄Fe(OH)3红褐HNO2溶液亮蓝Cu(OH)2蓝Hg(OH)2桔红 五、盐大多数白色或无色 主要例外:K2S 棕黄CuFeS2黄KHS 黄ZnS 白Al2S3黄Ag2S 黑MnS 浅红CdS 黄FeS 黑棕SnS 棕FeS2黄Sb2S3黑或橙红CoS 黑HgS 红NiS 黑PbS 黑CuS、Cu2S 黑Bi2S3黑FeCl3·6H2O棕黄Na3P红FeSO4·9H2O蓝绿NaBiO3黄Fe2(SO4)3·9H2O棕黄 MnCl2粉红Fe3C 灰MnSO4淡红FeCO3灰Ag2CO3黄Fe(SCN)3 暗红Ag3PO4黄CuCl2棕黄AgF 黄CuCl2·7H2O 蓝绿AgCl 白CuSO4白AgBr 浅黄CuSO4·5H2O 蓝 AgI 黄Cu2(OH)2CO3暗绿盐溶液中离子特色:NO2-浅黄Cu2+或[Cu(H2O)4]2+蓝 MnO4-紫红[CuCl4]2-黄MnO42-绿[Cu(NH3)4]2+深蓝Cr2O72-橙红Fe2+浅绿CrO42-黄非金属互化物PCl3无XeF2、XeF4、XeF6无PCl5浅黄氯水黄绿CCl4无溴水黄-橙CS2无碘水黄褐SiC 无或黑溴的有机溶液橙红-红棕SiF4无I2的有机溶液紫红 六.其它 甲基橙橙CXHY(烃)、CXHYOZ 无(有些固体白色)石蕊试液紫 大多数卤代烃无(有些固体白色)石蕊试纸蓝或红石蕊遇酸变红石蕊遇碱变蓝 葡萄糖白果糖无蔗糖无酚酞无麦芽糖白酚酞遇碱红淀粉白 蛋白质遇浓HNO3变黄纤维素白I2遇淀粉变蓝TNT 淡黄Fe3+遇酚酞溶液紫 焰色反应Li 紫红Ca 砖红Na 黄Sr 洋红K 浅紫(通过蓝色钴玻璃)Ba 黄绿Rb 紫Cu 绿稀有气体放电颜色He 粉红Ne 鲜红Ar 紫
摘要 本文概述了淋洗法修复重金属污染土壤的机理和淋洗剂的主要种类及应用研究进展。提出高效环保淋洗剂的开发,以及快速淋洗设备的研制及过程集成,是今后重金属铬污染土壤淋洗修复技术的重要研究方向。重金属作为一种持久性污染物已越来越多地被关注和重视. 重金属矿山的开采利用是造成当今世界重金属污染的主要原因,并已经严重威胁和影响人类的生存和发展.本文从我国重金属铬的利用入手,淋洗法是修复重金属铬污染土壤的一种快速、有效的方法。其中淋洗剂是决定淋洗修复技术成败和是否产生二次环境污染的重要因素。 关键词:重金属;铬污染土壤;淋洗法;修复 ABSTRACT This article summarizes the elution method to repair the mechanism of heavy metal contaminated soil and the main types and application research progress of spray lotion. Put forward the development of efficient environmental protection spray lotion, as well as the rapid development and process of leaching device integration, is the heavy metal chromium leaching of soil bioremediation technology of the important research direction. Heavy metals, as a kind of persistent pollutant has increasingly concern and attention. Heavy metal mine exploitation is the main reason for the heavy metal pollution in the world, and has a serious threat and influence human survival and development. In this paper, from the use of our country heavy metal chromium, elution method is one of the repair of heavy metal chromium contaminated soil rapid and effective method. The spray lotion is to determine whether success of injector repair technology and important factor in the production of secondary pollution of the environment. Key words :Heavy metals; Chromium contaminated soil; Elution method; repair