席夫碱及其过渡金属配合物的合成与研究
- 格式:pdf
- 大小:1.87 MB
- 文档页数:71



学 术 论 坛232科技资讯 SCIENCE & TECHNOLOGY INFORMATIONDOI:10.16661/ki.1672-3791.2017.35.232席夫碱及其金属配合物的抗肿瘤活性研究进展①陈月虎* 汤书君 杜艳凤(齐鲁医药学院 山东淄博 255213)摘 要:席夫碱及其金属配合物合成简单,性质稳定,并由于其具有较好的抗肿瘤生物活性,在生物医学、分析化学、功能材料和防腐蚀等领域具有重要应用,且在新药研发方面具有重要意义。
本论文针对席夫碱及其金属配合物的抗肿瘤研究进行归纳整理,进而为席夫碱及其金属配合物在抗肿瘤方面的应用及抗肿瘤药物的研发提供一定的借鉴意义。
关键词:席夫碱 金属配合物 抗肿瘤活性中图分类号:O641.4 文献标识码:A 文章编号:1672-3791(2017)12(b)-0232-02目前恶性肿瘤在许多国家和地区已经成为死亡原因,并且发病增高的趋势仍未发生明显变化。
尽管近几十年来,人类对癌症治疗的投入不断加大,部分肿瘤疗效也得到提高,人类在癌症分子水平研究上逐渐有了显著进步,但是大部分主要恶性肿瘤的治疗效果仍不明显,患者5年生存率仍没有明显提高,人类依然需要面对癌症的威胁。
如今,癌症已然成为了人类的第二大致命疾病,预计到2030年全球将有高达2700万例的癌症患者,而死于恶性肿瘤的人数更是将持续攀升并可能超过1100万[1]。
20世纪60年代人们发现顺铂具有抗细胞增殖作用,1978年顺铂上市并迅速推广,研究发现许多非铂类金属配合物同样也对肿瘤具有抑制作用。
因此,生物化学研究的热点逐渐集中于化合物的不同化学配位方式与生物学活性之间的关系。
许多过渡金属配合物被人类合成出来,同时,大量的新型配体也不断被研发出来,其中席夫碱类配体也以其具有良好的生物活性而成为近年来药物化学研究的热点。
1 席夫碱及其金属配合物1.1 席夫碱的概述席夫碱(Schiff base)是德国化学家Hugo Schiff在1864年首次合成报道,是由含有氨基及活泼羰基的两种化合物通过脱水缩合形成的含有亚氨基或烷亚氨基(-RC=N-)的一类有机物[2]。

席夫碱化学研究的进展作者:陈岩刘红来源:《中国化工贸易·下旬刊》2019年第06期摘要:席夫碱及其配合物具有类似燃料的光物理性质,在农业、国防、医药、工业等行业具有潜在的广阔的应用前景。
因此,本文以席夫碱为研究对象,介绍了席夫碱合成原理及组成,阐述了席夫碱大环化合物及聚合物的合成研究进展,并对其在金属离子鉴别、高分子化学、生物化学方面的研究情况进行了简单的分析,以期为席夫碱在现代科学生产中优势的充分发挥提供一定的参考。
关键词:席夫碱;化学合成;聚合物;大环化合物席夫碱是二十世纪发现的新型物质,其不仅在药学领域具有较为突出的抗病毒、杀菌作用,而且在催化剂领域、分析化学领域具有广泛的应用。
如以席夫碱为配体,通过色谱分析或光度分析可以有效鉴别金属离子。
在席夫碱广泛应用的背景下,为了进一步发挥席夫碱优势,对席夫碱化学研究进展进行适当分析具有非常重要的意义。
1 席夫碱概述席夫碱主要指含有(-RC=N-)亚胺、或者甲亚胺基团的一类有机化合物的统称。
一般通过胺或者氨、活性羧基缩合后,可合成席夫碱。
如在碱性环境中,醛类化合物、伯胺反应可获得席夫碱。
2 席夫碱化学合成研究进展2.1 席夫碱聚合物合成研究进展现阶段针对席夫碱聚合物合成研究主要为表面一维席夫碱聚合物扫描隧道显微技术研究。
表面一维席夫碱聚合物扫描隧道显微技术又可称为STM技术,其主要是基于醛、胺脱水后形成席夫碱反应的可逆特征,进行一维、二维聚合物的制备。
其在催化、纳米电子学、传感等领域具有广阔的应用。
如汪欣等为研究芳香二醛、二胺等不同化学结构在高定向热解石墨表面上席夫碱聚合反应。
利用4-氨基安替比林席夫碱-Pt(II)配合物作为活性单体,与联苯二胺、对苯二胺等发生反应,获得高度有序的一维线性席夫碱聚合物。
并得出上述物质均可与芳香族二胺发生反应[1]。
随后其在辛酸环境中利用不同浓度对苯二甲醛、4,4-二氨基对三联苯发生反应,获得一维聚合物组装状态,发现单体浓度所對应获得的一维席夫碱聚合物结构随时间出现了明显的变化。

陕西师范大学硕士学位论文席夫碱、苯乙酸及其铜、锰配合物的合成及结构表征姓名:***申请学位级别:硕士专业:无机化学指导教师:***20070501N(1)Is‘1心5)Cs(1)-N(1)-s0)S(1)-N(1)-c(8)cri)-c(2)-c(3)op)-c(2)-c(Dc(3)-C(4)-C(5)S(1)-C(5)-C(6)C(5)-C(6)-C(7)106-5402)134.42(13)112.81(1&120.9(3)118.0(3)119.邓)120.晌120.4(3)S(1)-oo)-cu0)Cu0)-N0)-C(8)Cu(1)-N(2)-C(9)c(1)-C(2)-C(7)q务c(3>C(4)S(1)-C(5)-C(4)c(4)-c(5)-c(6)C(2)-C(7)-c46)126.s201)112.69(1n10&3(2)121.o(4)121.9(3)120.5(2)119.5(3)120.蚋图2.6.1配合物1的分子结构图图2.6.6配合物3沿b轴的堆积图图2.6.7配合物3的氢键图2.6.3配合物5[Cu(CnNzI'11‘o)CI·H20】的晶体结构表征Cu(CnN2H160)C!·H20为片状晶体,席夫碱在参与配位的过程中失去一个质予成为负一价,C1-作为阴离子使分子单元处于中性,该配合物的晶胞结构单元图如所示。
从配合物的分子结构图可以看出,铜与去质子的席夫碱【c11H17N30]’和HzO发生配位,Cll与N1,N2,N3,01,02配位处于一个四方锥形中心。
由晶体堆积图可知,每个配合物晶体结构单元由0.H…O,O-H…CI,N-H…a,O.H…N氢键桥联到一块。
由氢键国可知Cll作为电子受体分别与02、N2、N3形成氢键N2-H2A…C11、02一H2C…CII、N3·H3B…C11,02作为电子供体,还与01形成氢键02.H2B…01,键长都在2.699--3.366^范围内,两个O.H…O键的存在,使得两个分子单元连接铜门/。

第26卷第3期Vol.26,No.3滨州学院学报Journal of Binzhou U niversity2010年6月J un.,2010氨基酸席夫碱金属配合物的研究进展收稿日期:2010-01-04 修回日期:2010-03-21基金项目:滨州学院青年人才创新工程科研基金项目(BZXYQNL G200704)作者简介:张 然(1982—),女,山东单县人,助教,硕士,主要从事氨基酸衍生物金属配合物研究,E Οmail :zhangran19820724@.张 然(滨州学院材料化学研究所,山东滨州256603) 摘 要:概述了近年来国内外在氨基酸席夫碱金属配合物领域的研究,探讨了氨基酸席夫碱配合物与DNA 之间作用机理,并对该领域的研究前景作出展望. 关键词:氨基酸席夫碱;金属配合物;DNA 中图分类号:O 621 文献标识码:A 文章编号:1673-2618(2010)03-0074-050 引言氨基酸是重要的生理活性物质,是生物体内合成蛋白质、激素、酶及抗体的原料,在生物体内参与多种生物化学过程.除作为肽及蛋白质的合成原料外,氨基酸其他形式的衍生物如氮取代或碳取代的酸、酯、酰胺、酰肼、盐以及金属配合物等大多也具有生物及生理活性[1-2].氨基酸等小分子生物配体的金属配合物不但具有重要生物功能,而且往往也是金属蛋白、金属酶等生命大分子配合物为维持其结构和功能所必需的活性中心[3].因此研究它们与金属元素的配位行为对金属氨基酸配合物体系的进一步完善和发展,也对金属离子在体内的存在形式和作用机理以及蛋白质的构效关系的认识有着重要的意义.近20多年来氨基酸席夫碱金属配合物的研究引起了许多化学工作者的兴趣,并报道了不少研究成果,主要涉及配合物的合成、结构和性质研究,且包括了大部分过渡金属离子[2-36].1 过渡金属氨基酸席夫碱配合物近年来,由于氨基酸的特殊结构,使其形成的氨基酸席夫碱及金属配合物研究领域显得尤为活跃.氨基酸席夫碱是指利用各种氨基酸与带有羰基的不同醛或酮进行反应得到的含有C =N 结构的产物.它是一类非常重要的被修饰了的氨基酸配体,其特点是含有多个强电负性的配位原子(N 、O ),具有较强的配位能力和多样的配位方式.当氨基酸席夫碱与过渡金属发生反应时,配体易通过亚胺上的氮、羧基上的氧与金属原子形成较稳定的五元、六元螯合环,文献已报道了大量的配合物及晶体结构[2-6].这些金属配合物可以作为研究维生素B6酶反应的优良模型[7],并对生物无机化学和医药方面有着重要的意义,其抗肿瘤药物活性比一般的席夫碱有机化合物效果更为明显,已经有人研究了这类配合物与DNA 的相互作用[28-32].毕思玮等[8]合成了氨基酸系列水杨醛席夫碱与Cu (Ⅱ)配合物,比较了配合物的抗菌活性与稳定性、结构间的关系,结果表明,抗菌活性随配体中氨基酸残基非配位基R 的增大而减小,这说明随稳定性的提高,抗菌活性减小.王忠等[9]合成了4-氯苯甲醛缩甘氨酸席夫碱的Co (Ⅱ)、Cu (Ⅱ)、Zn (Ⅱ)、Ni (Ⅱ)配合物,并测定分析了其组成与结构,抗菌活性实验表明,4种配合物对浅部真菌都有较强的抗菌作用.Casella 等[10]也合成了一系列不对称O 2载体模型化合物:Co (Sal ΟL ΟAA ),Co (Pdx ΟL ΟAA ),(Sal =水杨醛,Pdx =吡哆醛,AA =第3期张 然 氨基酸席夫碱金属配合物的研究进展丙氨酸、缬氨酸、苯丙氨酸、组氨酸).氨基酸及其衍生物的锌配合物抗菌活性的研究报道较多,其他应用报道较少.刘兴荣[11]等合成了5-硝基水杨酸缩甘氨酸schiff碱与Zn(Ⅱ)的配合物,并进行了抑菌活性实验,表明Zn(Ⅱ)配合物对枯草杆菌、杂色霉菌有抑菌活性.毕思玮等[12]合成了亮氨酸水杨醛席夫碱及其锌(Ⅱ)的配合物,进行了表征,并测定了配合物的稳定常数,抗菌活性实验表明,配合物的抗菌活性优于配体抗菌活性.范谦等[13]合成了组氨酸席夫碱Mn(Ⅱ)配合物,表征分析了其结构,并研究了该配合物对环己烯烯丙位氧化的催化性能,考察了温度、时间、溶剂、氧压力等因素对反应的影响.V.ParedesΟGarcía等[14]利用5-溴水杨醛和甘氨酸缩合的产物与Fe(NO3)3在甲醇溶液中形成配合物,甘氨酸中两个羧基氧分别与两个铁离子配位,起到桥联的作用.同时,甘氨酸中氨基氮原子和水杨醛中酚氧原子以及配位水中氧原子与铁离子形成六配位的变形八面体构型.2 稀土氨基酸席夫碱配合物通常是利用稀土盐与氨基酸席夫碱在醇溶液中反应制得,由于在碱性条件下稀土离子易沉淀,所以很难获得晶体.近年来,浙江大学的姚克敏课题组已对稀土氨基酸席夫碱配合物的研究做了大量的工作[15],并发现它们具有较好的催化性能.如配合物[LnCu2(H2T AL Y)(NO3)5](NO3)2・n H2O (H2T AL Y为4甘醇醛缩双赖氨酸席夫碱)可在不加助催化剂时单独催化聚合甲基丙烯酸甲酯(MMA),转化率可高达100%.3 还原型氨基酸席夫碱配合物氨基酸席夫碱及其配合物的生物活性研究,前人已经做了不少的工作[10-18].为了克服这类物质由于C=N双键的刚性而稳定性差的弱点,在保证活性基因的情况下,将席夫碱配体中的C=N双键还原为C-N单键.这使其结构具有更好的柔韧性,对于寻求稳定的模型配合物或高效低毒的杀菌药物等均有重要意义.从文献[18-22]来看,还原型氨基酸席夫碱配合物的研究大多集中于配合物的结构测定等表征,而对所合成的配合物的生物活性及活性影响因素的研究报道较少.胡久荣等[23]以水杨醛通过苯丙氨酸氨基的反应对其进行修饰,选择生命必须微量元素Cu(Ⅱ)作为中心离子,在乙醇和水的混合溶剂中合成了3种配合物,[Cu (Hsp he)(p hen)](ClO4)・3H2O、[Cu(Hsp he)(2, 2′Οbip y)](ClO4)、[Cu(Hsp he)(2,2′Οbipy)] (NO3).(Hsp he=N-(2-羟苄基)-DL-α-苯丙氨酸根,p hen=1,10-邻菲咯啉,2,2′-bipy= 2,2′-联吡啶),并对配合物的晶体结构及其抑菌活性进行了研究.4 氨基酸席夫碱配合物与DNA之间作用研究 DNA是由大量脱氧核糖核酸组成的大分子,其中的戊糖和磷酸基起着结构性的作用,而碱基则起着携带遗传信息的作用.配合物与DNA的结合按化学键来划分主要有共价键和非共价键两种,其中非共价键对了解金属配合物的抗肿瘤活性和其与DNA作用模式之间的关系起着非常重要的作用,主要包括3种方式:静电作用、沟面作用和插入作用[24-28].(1)静电作用.核酸是一种带负电荷的多聚阴离子,通常以钠盐形式存在.金属离子及许多配合物带有正电荷,因此它们可以与核酸在外层通过静电发生作用.(2)沟面作用.配合物结合在DNA的沟面,主要靠碱基疏水起稳定作用.(3)插入作用.配合物以含有平面芳香杂环的配体插入相重叠,通过Π-Π堆积作用相互结合.最近,发现氨基酸席夫碱的三元配合物对DNA有较好的插入或部分插入作用[29-31],因此这类配合物有可能成为新的DNA切割剂或抗癌和抗病菌药物,在医学上有着潜在的应用前景.研究氨基酸席夫碱的配合物与DNA相互作用有重要意义.利用紫外光谱方法检测DNA与配合物之间的相互作用是最常用的分析方法,增色效应和减色效应是与DNA双螺旋结构和空间构型密切相关的特有光谱性质,增色效应是配合物与DNA中碱基基团配位,DNA双螺旋结构改变的结果;而减色效应是化合物与DNA中磷酸基团静电作用,使DNA发生空间轴向收缩的结果[32-33].57滨州学院学报第26卷图1是配合物[YbL (H 2O )](NO 3)2・2H 2O (HL 即香兰素缩赖氨酸席夫碱)在不同DNA 浓度下的电子光谱[34],紫外光谱显示加入DNA 后,该配合物在280nm 、310nm左右的吸收峰强度均增(1)r =0,(2)r =0.30,(3)r =0.60,(4)r =1.19;r =c DNA /c M图1 DNA 对配合物[YbL (H 2O )](NO 3)2・2H 2O紫外光谱的影响强,且280nm 处的吸光度(A )随着DNA 与配合物浓度比(r =c DNA /c M )的增大而不断增强.配合物吸收峰的增强可能是由于磷酸基团上所带负电荷与稀土阳离子发生静电结合,使配合物在DNA 表面分子发生长距离自组装[35].5 展望及结论氨基酸席夫碱配合物的合成、晶体结构和结构特性与物质分子性质或生物活性或材料的定量关系,涉及生物学、配位化学、医学等学科领域中所关注的热点,亟待研究.由于含多功能基席夫碱配体及其配合物在立体化学、结构学、异构现象、磁学、光谱学、动力学和反应机理、配位反应、分析化学、催化、稳定剂、染料和颜料、摄影、电光显示以及农业等领域都有着重要的作用,而目前还未见有在氨基酸席夫碱配体中引入多功能基的研究的报道,因此此领域应该是将来的研究热点[36].总结了近几年过渡金属,稀土金属以及还原性氨基酸配合物的研究进展,重点讨论氨基酸席夫碱配合物与DNA 之间作用机理,并对氨基酸配合物领域的研究前景作出展望.氨基酸作为生物体内重要的生物活性组分,其金属配合物的结构与生物性能之间的关联是广大氨基酸工作者的研究热点.参 考 文 献:[1] Andrew St reitwieser J r ,Clayton H Heat hcock.Int roduction to organic chemist ry[M ].New Y ork :Macmillan Publishing Company ,1992.[2] 郭应臣,邱东方,包晓玉,等.L Ο苏氨酸铜(Ⅱ)超分子配合物的合成、晶体结构及性质[J ].化学通报,2010(1):79-82.[3] 倪嘉缵.稀土生物无机化学[M ].北京:科学出版社,1995.[4] 刘峥,王渊,葛彩叶.电有机合成3,5-二溴水杨醛缩丝氨酸过渡金属配合物的研究[J ].应用化工,2009,38(7):1017-1021.[5] 陈蔷薇,倪伟双,吴夏冰,等.氨基酸-镧配合物的合成及单晶培养研究[J ].广州化工,2009,37(6):126-127.[6] 耿杰,于海佳,张海元,等.稀土氨基酸配合物与核酸的相互作用[J ].化学进展,2009(5):866-871.[7] 祝振富,黎植昌.氨基酸Schiff 碱金属配合物的研究进展[J ].氨基酸和生物资源,1997(1):31-35.[8] 毕思玮,刘树祥.氨基酸水杨醛席夫碱与Cu (Ⅱ)配合物的合成及其抗菌活性和稳定性、结构间的关系[J ].无机化学学报,1996,12(4):423-425.[9] 王忠,吴自慎,严振寰.4-氯苯甲醛甘氨酸席夫碱及其Cu (Ⅱ)、Zn (Ⅱ)、Co (Ⅱ)、Ni (Ⅱ)配合物合成、表征及抗菌活性研究[J ].华中师范大学学报,1995,29(2):197-201.[10] Casella L ,Gullotti M.Synt hesis ,stereochemist ry ,and oxygenation of cobalt (Ⅱ)Οpyridoxal modelcomplexes :A new family of chiral dioxygen carriers[J ].Inorg Chem ,1986,25(9):1293.[11] 刘兴荣,刘培漫,李明霞,等.Co (Ⅱ)、Ni (Ⅱ)、Cu (Ⅱ)和Zn (Ⅱ)的5-硝基水杨酸缩甘氨酸Schiff 碱配合物的合成及表征[J ].山东医科大学学报,1995,33(3):257-259.6777第3期张 然 氨基酸席夫碱金属配合物的研究进展[12] 毕思玮,李桂芝.亮氨酸水杨醛席夫碱及其锌(Ⅱ)的配合物的合成、稳定性和抗菌活性[J].四川师范学院学报,1996,17(3):54-57.[13] 范谦,黎耀辉,程克梅.组氨酸席夫碱锰配合物的合成及环己烯催化氧化[J].四川大学学报,2001,38(2):230-234.[14] ParedesΟGarcía V,VenegasΟYazigi D,Latorre R O,et al.Elect ronic properties of mixed valence i2ron(Ⅱ,Ⅲ)dinuclear complexes wit h carboxylate bridges[J].Olyhedron,2006,25:2026-2032.[15] 姚克敏,李宁,黄巧虹.L n(Ⅲ)-Cu(Ⅱ)与直链醚-氨基酸新型schiff碱异核配合物的合成和催化[J].中国科学(B缉),1998,28(6):517.[16] 毕思伟,高恩庆,田君濂.N-亚水杨基氨基酸3d金属配合物的合成、表征和抑菌活性[J].应用化学,1995,12(6):13-16.[17] L uo Zengwei,Li Baohua,Fang Xiantao,et al.Novel chiral solvating agent s derived from nat ural a2mino acid:enantiodiscrimination for chiral aΟarylalkylamines[J].Tet rahedron Letters,2007,48: 1753-1756.[18] K oh L L,Ranford J D,Robinson W T,et al.Model for t he reduced Schiff base intermediate be2tween amino acids and Pyridoxal:copper(Ⅱ)co mplexes of N-(2-Hydroxybenzyl)amino acids wit h no npolar side chains and t he crystal st ruct ures of[Cu(N-(2-hydroxybenzyl)-d,l-ala2 nine)(p hen)]・H2O and[Cu(N-(2-hydroxybenzyl)-d,l-alanine)(imidazole)][J].Inorg Chem,1996,35:6466-6472.[19] Ranford J D,Vittal J J,Wu D.Topochemical Conversion of a hydrogenΟbonded t hreeΟdimensionalnetwork into a covalently bonded f ramework[J].Angew Chem Int Ed,1998,37:1114-1116.[20] Ranford J D,Vittal J J,Wu D.Thermal conversion of a helical coil into a t hreeΟdimensional chiralf ramework[J].Angew Chem Int Ed,1999,38:3498-3501.[21] Yang C T,Moubaraki B,Vittal J J,et al.Synt heses,st ruct ural properties and catecholase activityof copper(Ⅱ)complexes wit h reduced Schiff base N-(2-hydroxybenzyl)-amino acids[J].J Chem Soc,Dalton Trans,2004:113-121.[22] Yang C T,Moubaraki B,Murray K S,et al.Synt hesis,characterization and properties of ternarycopper(Ⅱ)complexes containing reduced Schiff base N-(2-hydroxybenzyl)-α-amino acids and1,10-p henant hroline[J].J Chem Soc,Dalton Trans,2003(5):880-889.[23] 胡久荣,梁福沛,陈自卢,等.铜(Ⅱ)-N-(2-羟苄基)-DL-α-苯丙氨酸-2,2′-联吡啶(或1,10-邻菲咯啉)三元配合物的合成、晶体结构及抑菌活性[J].无机化学学报,2006,22(11):1989-1995. [24] Pyle A M,Rehmann J P,Meshorer R,et al.MixedΟligand complexes of rut henium(Ⅱ):factorsgoverning binding to DNA[J].J Am Chem Soc,1989,111:3051-3058.[25] Wade W S,Derron P B.Alteration of t he sequence specificity of distamycin on DNA by replace2ment of an NΟmet hylpyrrolecarboxamide wit h pyridine-2-carboxamide[J].J Am Chem Soc, 1987,109:1574.[26] Wilson D,Wang YH,Kusuma S,et al.Binding st rengt h and specificity in DNA interactions:t hedesign of tdot.T specific intercalators[J].J Am Chem Soc,1985,107(17):4989-4995. [27] Ibanez V,Geacintor N E,Gagiano A G,et al.Physical binding of tet raols derived f rom7,8-di2hydroxy-9,10-epoxybenzo[a]pyrene to DNA[J].J Am Chem Soc,1980,102(17):5661-5666.[28] 胡亚敏,王兴明,张欢.金属配合物与DNA相互作用的研究进展[J].化学与生物工程,2007,24(8):1-4.87滨州学院学报第26卷[29] Chikira M,Tomizawa Y,Fukita D,et al.DNAΟfiber EPR st udy of t he orientation of Cu(Ⅱ)com2plexes of1,10-p henant hroline and it s derivatives bound to DNA:mono(p henant hroline)-cop2 per(Ⅱ)and it s ternary complexes wit h amino acids[J].J Inorg Biochem,2002,89(1):163-173.[30] 李红,乐学义,计亮年.邻菲咯啉-铜(Ⅱ)-L-亮氨酸配合物与DNA的结合[J].化学通报,2003,66(12):847-850.[31] 李红,乐学义,吴建中.铜(Ⅱ)邻菲咯啉蛋氨酸配合物与DNA相互作用的研究[J].化学学报,2003,61(2):245-250.[32] 张朝红,臧树良,耿兵,等.紫外和圆二色光谱法研究丁基锡化合物与牛血清白蛋白的相互作用[J].分析科学学报,2005,21(2):179.[33] 张朝红,苏欣,臧树良,等.用紫外光谱和荧光光谱研究三丁基锡化合物与脱氧核糖核酸的相互作用[J].分析科学学报,2006,22:267-270.[34] 陆晓红,林秋月,贺新前,等.稀土-香兰素缩赖氨酸席夫碱配合物的合成、表征及其与DNA作用的研究[J].中国稀土学报,2006,24(4):403-407.[35] 郭东方,何疆,曾正志.肉桂酸-邻菲罗啉-稀土三元配合物对DNA作用的光谱研究[J].中国稀土学报,2004,22(2):55-60.[36] 高恩君,赵淑敏,刘祁涛.混合配体配合物钯(Ⅱ)-联喹啉-苯乙基丙二酸根与DNA作用研究[J].无机化学学报,2004,20(2):191-194.R esearch Advances in Amino Acid Schiff B ase Metal ComplexesZHAN G Ran(I nstit ute of M ateri al Chemist ry,B i nz hou Universit y,B i nz hou256603,Chi na)Abstract:The research on metal complexes of amino acid schiff base in recent years is overviewed. The f unction of interactio n of metal complexes and DNA is also presented,and t he perspective in t his field is p ropected as well.K ey w ords:amino acid Schiff base;metal complexes;DNA(责任编辑:贾晶晶)。
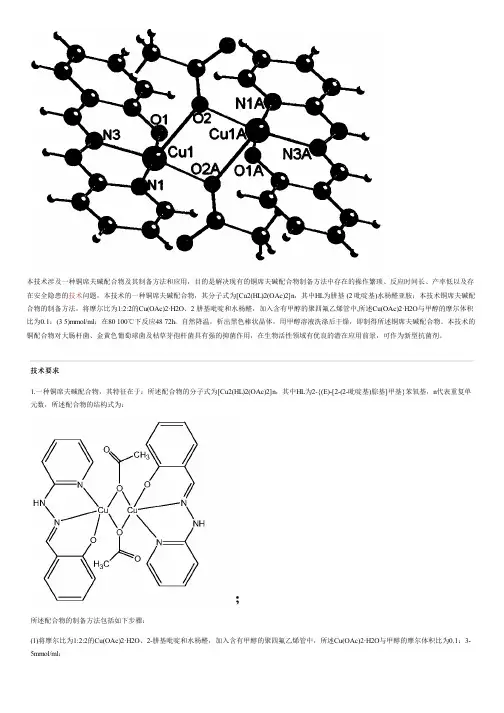
本技术涉及一种铜席夫碱配合物及其制备方法和应用,目的是解决现有的铜席夫碱配合物制备方法中存在的操作繁琐、反应时间长、产率低以及存在安全隐患的技术问题,本技术的一种铜席夫碱配合物,其分子式为[Cu2(HL)2(OAc)2]n,其中HL为肼基(2吡啶基)水杨醛亚胺;本技术铜席夫碱配合物的制备方法,将摩尔比为1:2:2的Cu(OAc)2·H2O、2肼基吡啶和水杨醛,加入含有甲醇的聚四氟乙烯管中,所述Cu(OAc)2·H2O与甲醇的摩尔体积比为0.1:(35)mmol/ml;在80100℃下反应4872h,自然降温,析出黑色棒状晶体,用甲醇溶液洗涤后干燥,即制得所述铜席夫碱配合物。
本技术的铜配合物对大肠杆菌、金黄色葡萄球菌及枯草芽孢杆菌具有强的抑菌作用,在生物活性领域有优良的潜在应用前景,可作为新型抗菌剂。
技术要求1.一种铜席夫碱配合物,其特征在于:所述配合物的分子式为[Cu2(HL)2(OAc)2]n,其中HL为2-{(E)-[2-(2-吡啶基)腙基]甲基}苯氧基,n代表重复单元数,所述配合物的结构式为:所述配合物的制备方法包括如下步骤:(1)将摩尔比为1:2:2的Cu(OAc)2·H2O、2-肼基吡啶和水杨醛,加入含有甲醇的聚四氟乙烯管中,所述Cu(OAc)2·H2O与甲醇的摩尔体积比为0.1:3-5mmol/ml;(2)将所述聚四氟乙烯管置于不锈钢反应釜中密封,在80-100℃下反应48-72h,自然降温,析出黑色棒状晶体,用甲醇溶液洗涤后干燥,即制得所述铜席夫碱配合物。
2.根据权利要求1所述的一种铜席夫碱配合物,其特征在于:所述配合物的晶体属单斜晶系,空间群为C2/c,晶胞参数为:α=90°,β=120.7(6)°,γ=90°。
3.一种含有权利要求1所述的铜席夫碱配合物的抑菌剂。
技术说明书一种铜席夫碱配合物及其制备方法和应用技术领域本技术涉及一种铜席夫碱配合物及其制备方法和应用。


《席夫碱过渡金属配合物催化去除给水中的溶解氧》席夫碱过渡金属配合物催化去除给水中溶解氧的高效应用一、引言随着工业化和城市化的快速发展,给水中的溶解氧(Dissolved Oxygen,DO)问题日益突出。
过高的溶解氧浓度不仅对供水管网及终端用水设备造成腐蚀,还可能对水生生物产生不利影响。
因此,有效去除给水中的溶解氧成为水处理领域的重要课题。
近年来,席夫碱过渡金属配合物因其独特的化学性质和催化性能,在给水处理中显示出良好的应用前景。
本文将探讨席夫碱过渡金属配合物催化去除给水中溶解氧的机理、方法及优势。
二、席夫碱过渡金属配合物的概述席夫碱是一类含有亚胺基(—C=N—)的有机化合物,具有较好的配位能力。
与过渡金属离子形成的配合物具有良好的稳定性、催化活性和选择性。
在给水处理中,通过席夫碱过渡金属配合物催化反应,可有效降低水中溶解氧的浓度。
三、席夫碱过渡金属配合物催化去除溶解氧的机理席夫碱过渡金属配合物通过与水中的溶解氧发生化学反应,生成无害或低毒的化合物,从而达到去除溶解氧的目的。
具体反应过程中,配合物中的金属离子与氧分子发生电子转移,形成金属-氧键,进而将氧分子转化为其他形态。
此过程中,配合物的结构保持稳定,并可循环利用。
四、催化去除溶解氧的方法1. 制备席夫碱过渡金属配合物:选择适当的席夫碱和过渡金属离子,按照一定比例混合,制备出稳定的配合物。
2. 催化反应:将制备好的配合物加入给水中,通过搅拌、加热等方式促进催化反应的进行。
3. 检测与分离:反应完成后,通过检测手段确定水中溶解氧的浓度是否达到要求,并对反应后的溶液进行分离、回收或处理。
五、优势与应用前景(一)优势:1. 高效性:席夫碱过渡金属配合物具有较高的催化活性,可快速降低水中溶解氧的浓度。
2. 选择性:配合物对氧分子具有较好的选择性,可避免其他有益物质的损失。
3. 稳定性:配合物结构稳定,可循环利用,降低处理成本。
4. 环境友好:反应过程中不产生有害物质,符合绿色化学的要求。

氨基酸水杨醛席夫碱铜配合物的合成及其表征周雨515020910133一、实验目的1、了解氨基酸类、席夫碱类化合物及其重要作用2、掌握制备氨基酸水杨醛席夫碱铜配合物的制备方法,熟悉基本实验操作3、掌握表征该铜配合物的各种现代仪器分析手段的基本原理以及操作流程二、实验原理氨基酸是羧酸链上碳原子的氢被氨基取代之后的化合物,含有氨基和羧基两种官能团,可以根据氨基在碳链上取代的位置分为α-,β-,γ-氨基酸。
其中组成蛋白质的大都是α-氨基酸,有20种,除甘氨酸外均是L-α-氨基酸(具有手性)。
常用的非手性氨基酸有甘氨酸、β-丙氨酸,这些氨基酸价格低廉因而广泛应用在生化、医药等领域。
水杨醛是邻羟基苯甲醛,广泛应用于有机合成中,是一种常见的工业原料。
席夫碱主要是指含有亚胺或者甲亚胺官能团的化合物,通常由胺和活性羰基化合物发生缩合反应来制备。
席夫碱中的氧原子和氮原子可以与过渡金属形成六元环稳定配合物,其中席夫碱的钴、镍配合物已经作为催化剂在工业上得到应用。
同时由于其良好的配位性质,席夫碱可以用于鉴定离子和定量分析离子的含量。
本实验通过使用水杨醛与甘氨酸、β-丙氨酸发生缩合反应生成席夫碱类化合物,席夫碱中含有的氮原子和氧原子和加入的金属铜盐形成稳定的六元环配合物。
合成的金属有机配合物可以通过多种手段进行表征,其中常用的包括通过红外光谱方法、紫外光谱方法鉴定该配合物中含有的官能团,通过XRD表征合成配合物形成的晶体结构,通过核磁分析确定化合物相关信息等。
三、实验仪器和试剂仪器:核磁共振仪,红外光谱仪,X射线衍射仪,250mL圆底烧瓶,搅拌子,搅拌器,干燥器,胶头滴管,量筒,锥形瓶,pH试纸等。
试剂:氢氧化钾,β-丙氨酸,醋酸铜,蒸馏水,无水乙醇,无水乙醚,溴化钾,氘代氯仿,水杨醛。
试剂均为化学纯级别。
四、实验流程1、制备流程配体制备流程:将3.4g(60mmol)氢氧化钾和5.35g(60mmol)β-氨基酸溶于10mL水,加入250mL烧瓶,将7.3g水杨醛溶于40mL无水乙醇,待两者固体完全溶解后,将水杨醛缓慢滴入体系,溶液变成黄色。

席夫碱席夫碱主要是指含有亚胺或甲亚胺特性基团(-RC=N-)的一类有机化合物,通常席夫碱是由胺和活性羰基缩合而成。
席夫碱类化合物及其金属配合物主要在药学、催化、分析化学、腐蚀以及光致变色领域的重要应用。
在医学领域,席夫碱具有抑菌、杀菌、抗肿瘤、抗病毒的生物活性[ 1];在催化领域,席夫碱的钴、镍和钯的配合物已经作为催化剂使用[ 2];在分析化学领域,席夫碱作为良好配体,可以用来鉴别、鉴定金属离子和定量分析金属离子的含量[ 3];在腐蚀领域,某些芳香族的席夫碱经常作为铜的缓蚀剂[ 4];在光致变色领域,某些含有特性基团的席夫碱也具有独特的应用[ 5]。
合成方法Schiff碱稀土配合物的合成方法主要有直接合成法和分步合成法,(该把直接合成法和分步合成法介绍一下)分步合成法得到的产品无论是在(产品)产率上,还是在(产品)纯度上都较直接合成法理想。
当反应活性低或选择性不好,用前述两种方法合成的产物不稳定或者产率低时,可选用模板合成法。
所谓模板合成法就是将金属离子作为模板试剂加入到羰基化合物中与胺类化合物反应的一类合成方法。
如(在)合成二羰基化合物和多胺的Schiff碱配体及其配合物时多采用此方法。
当合成的Schiff碱在反应溶剂中溶解度很小,上述三种合成方法均不适用时,一般采用逐滴反应法,即向胺类化合物与金属离子的混合溶液中逐滴活泼碳基化合物溶液的一种方法[ 6]。
这些合成方法适用于不同类型的Schiff碱金属配合物,它们各有优缺点。
大多数氨基酸Schiff碱稀土配合物的制备均可采用分步合成法。
(但分步合成法是制备氨基酸Schiff碱稀土配合物最常用的一种方法)催化领域的应用席夫碱及其配合物在催化领域的应用也很广泛,概括起来说,席夫碱做催化剂主要应用于聚合反应、不对称催化环丙烷化反应以及烯烃催化氧化方面和电催化领域等。
魏丹毅[ 7]等合成了9种稀土元素(La,Pr,Nd,Sm,Gd,Tb,Er,Yb,Y)与水杨醛-缩β-丙氨酸(H2L)的双核配合物,发现此配合物对甲基丙烯酸甲酯(MMA)的聚合反应有催化活性;姚克敏[ 8]等用直链醚-脂肪族氨基酸新型Schiff碱作为综合配体与稀土离子配位,发现它们在甲基丙烯酸甲酯聚合中有较好的催化活性;Yong [ 9]等发现钛席夫碱配合物对乙烯、苯乙烯的聚合反应有很好的催化活性.近年来,不对称催化环丙烷化反应已经成为研究的热焦点,在其催化剂体系中铜的席夫碱配合物是被研究最早最深人的体系之一。
含氟席夫碱配体及其Zn配合物的合成与表征杜可杰;赵媛;林英武【摘要】含salophen配体的锌金属配合物具有优异的荧光性能,成为生物荧光探针研究领域的重要研究对象。
本文合成含氟salophen配体及其相应的Zn( salophen)金属配合物,分别采用1 H NMR、IR、LC-MS、元素分析对其进行了详细的表征。
结果表明, Zn金属与配体及甲醇中氧、氮形成五配位结构。
紫外—可见光谱研究显示, Zn ( salo-phen)金属配合物在295 nm、397 nm处有典型特征吸收峰。
荧光光谱显示,在397 nm波长激发下,配合物在507 nm有最大荧光发射峰。
结果表明该配合物具有潜在的作为生物荧光探针的研究价值。
%In the past few decades,Zn(II) metal complexes has attracted a great deal of interest as biological probes in living cell imaging,because of their photophysical properties such as high luminescence,good photostability.In this work,a zinc complex containing flu-orine substituted group, Zn( salophen ) , was designed and synthesised. The sample was characterized by 1 H NMR, IR, LC-MS and elemental analysis. Results suggested that the zinc metal displays a square-planar arrangement formed by the N/O-donor atoms,while the axial position bind a solvent molecule. In the presence of good donor solvents, Zn ( salophen) metal complex form five-coordinate structure. The absorption spectrum of zinc complex consists of two distinguishable bands at 295 and 397 nm in ethanol solution,while consisting of two bands at 297 and 404 nm in DMSO solution.Zn(salophen) metal complex exhibits emission with maximum emission wavelength at 507 nm.【期刊名称】《南华大学学报(自然科学版)》【年(卷),期】2016(030)003【总页数】5页(P79-83)【关键词】锌金属配合物;荧光;氟取代【作者】杜可杰;赵媛;林英武【作者单位】南华大学化学化工学院,湖南衡阳421001;南华大学化学化工学院,湖南衡阳421001;南华大学化学化工学院,湖南衡阳421001【正文语种】中文【中图分类】O627.23分子荧光成像是生物分子成像中最具代表性的成像方式之一,它具有分辨率高、灵敏度好及无辐射等特点.近几年来,由于随着生物体内化学发光成像技术的发展,分子荧光研究,特别是细胞内选择性生物荧光探针的研究,在近几年引起广大研究者的关注[1-2].但是,目前,大部分生物荧光探针为有机小分子化合物[3].相对于有机小分子荧光化合物而言,过渡金属配合物由于具有发光效率高、荧光寿命长、光稳定性好、stokes位移大等特点,被广泛应用于生物荧光探针研究.相比于荧光蛋白与荧光纳米颗粒,小分子金属荧光探针具有使用方便、选择性强、容易进入细胞等特点.目前,过渡金属荧光探针研究对象主要集中在Re、Ir、Ru、Pt等过渡金属[4-5].并且已有多种理想的金属配合物荧光探针应用于细胞膜、细胞质、线粒体、溶酶体等的定位成像[6],如巢晖课题组相继报道了系列可以用于细胞线粒体内NO的有效荧光成像检测的Ir配合物[7].但是Ir、Pt金属配合物作为细胞内荧光探针,往往存在比较大的细胞毒性,金属锌为d10电子结构元素,具有良好的光电性质,而且Zn金属是多种生物酶的活性中心,具有良好的生物相容性,因此,通过合理设计,引入不同柔性或刚性配体,即可合成出具有优秀光电活性的双光子细胞内荧光探针.当配体中引入氟原子或含氟基团后,配体电子密度及整体极性会发生明显变化,导致其光电性能的大幅改变[8],在生物应用方面,则能提高化合物的脂溶性和渗透性以及在生物膜上的溶解性,促进药物在生物体内的吸收与传递速度,使生理作用发生变化[9].本文合成了一例新型含氟salophen配体,进而合成其Zn金属配合物,图1列出了配体及配合物的合成路线.通过1H NMR、IR、LC-MS及元素分析对其进行了详细表征,并研究了其紫外—可见光谱特性及荧光光谱特性.1.1 主要仪器与试剂4-氟-1,2-苯二胺、邻羟基苯甲醛、Zn(AC)2 均购于阿达玛斯贝塔(上海)化学试剂有限公司),其余常用试剂均为分析纯.EQUINOX55傅立叶红外光谱仪 (岛津IR Prestige-21,日本),核磁共振波谱仪(Bruker AVANCE 400,德国),元素分析仪(Elementar Vario EL,德国 ),LC-MS(安捷伦,美国),安捷伦紫外—可见光谱仪(Agilent 8453,美国),荧光分光光度计(PerkineElmer LS 55 ,美国)1.2 实验步骤1.2.1 Salophen配体的合成配体及配合物合成参考支志明课题组报道方法并进行改进[10].将原料邻羟基苯甲醛(水杨醛过量)0.678 mL(6.5 mmol)与4-氟-1,2-苯二胺0.378 g(3 mmol)溶解于适量甲醇溶剂中,50 ℃回流,磁力搅拌反应4 h,冷却,抽滤,冷甲醇洗涤数次,干燥.红棕色产品用氯仿重结晶,得红棕色针状晶体0.87 g,收集备用.产率:78%.配体用1H NMR、红外光谱(IR)和LC-MS质谱及元素分析进行表征.1H NMR(400 MHz,DMSO-d6):δ=12.79(s,2H),8.96(s,1H),8.92(s,1H),7.67(t,J=8.0,2H),7.53(t,J=7.2,1H),7.40-7.46(m,3H),7.26(t,J=8.4,1H),6.98(d,J=8.4,2H),6.96(d,J=8.4,2H).IR(KBr,υ/cm-1):758.02,908.47,1109.07,1149.57,1192.01,1276.88,1479.40,1562.34,1614.42,3689.83.LC-MS:m/z=335.1[M+H+].元素分析:Calcd(%):C,71.85;H,4.52;N,8.38.Found(%):C,71.35;H,4.86;N,7.99.1.2.2 Zn(salophen)配合物的合成取上一实验合成的salophen配体0.8 g溶解于3 mL氯仿中,再取0.172 gZn(AC)2溶解在10 mL的甲醇中,混合.46 ℃回流5 h,冷却,减压抽滤,冷乙醇洗涤,得亮黄色固体,真空干燥,得0.85 g产品.产率:87%.产物用红外光谱、LC-MS及元素分析进行表征.IR(KBr,υ/cm-1)491.85,754.17,852.54,983.70,1153.43,1325.10,1384.89,1469.76,1529.55,1591.27,1616.35,3074.53.LC-MS:m/z=429[M+H+].元素分析:Calcd(%):C,58.83;H,3.76;N,6.53.Found(%):C,59.26;H,3.97;N,6.84.2.1 含氟salophen配体表征及结果分析合成配体经过氯仿重结晶之后得到针状橙红色微晶,将该微晶收集,用于进一步表征.通过样品的1H NMR表征结果分析,在化学位移为12.79 处出现典型酚羟基质子峰,在化学位移为8.96与8.92处为HC=N基团上质子峰,苯环上其余质子化学位移均在6.96~7.67 范围内出现相应单峰、双重峰或三重峰.且所有质子峰积分面积与质子数完全相符.核磁结果说明,所测试样品为预期目标产物.样品的元素分析结果显示,C、H、N含量均在理论计算允许误差内,表明配体纯度符合实验要求.在波数为 4 000~400 cm-1范围内测定了配体的红外光谱(图2),实验结果显示醛基的C=O伸缩振动吸收峰(1658 cm-1)消失,氨基N-H吸收峰(3 400 cm-1)也消失.而1614 cm-1处出现吸收峰,为-C=N-特征吸收峰,1109 cm-1为C-F吸收峰,3 689 cm-1为典型的Ar-OH伸缩振动吸收峰.从红外谱图可以看出,原料特征峰消失,形成salophen配体特征吸收峰.进一步表明合成样品为所预期的目标产物.所合成样品的LC-MS表征结果显示,样品荷质比(M/Z)为335.1,为样品加H+的位置峰,质谱结果更明确的显示样品即为所设计的目标产物.在配体合成过程中,对其合成温度进行了优化,发现适当降低温度,在50 ℃,产品的产率最高.产物通过氯仿重结晶,可得到较纯的针状晶体,合成溶剂选用甲醇比乙醇产率更高.2.2 Zn(salophen)金属配合物表征及结果分析Zn(salophen)金属配合物合成通过重结晶进行纯化,样品通过LC-MS、元素分析进行初步表征.样品的LC-MS表征结果显示,在荷质比M/Z=429处出现强峰,这是Zn(salophen)金属配合物的分子量加氢的位置峰.配合物中Zn(II)为五配位结构,Zn金属分别与salophen配体中2个N原子、2个O氧原子及1个甲醇氧进行配位,质谱结果显示合成配合物为所预期的目标产物.元素分析结果显示C、H、N含量均在理论计算允许误差内,元素分析结果更证明配合物中Zn(II)金属离子与甲醇中氧原子配位形成五配位结构,也证明了LC-MS结果的正确性,且所测样品纯度较高.用KBr压片,在波数为 4 000~400 cm-1的范围测定了配合物的红外吸收光谱(图3).结果显示,3 074 cm-1处出现一强吸收峰,此为配体与Zn(II)配位烷烃吸收峰,因为氧原子与Zn金属离子形成配位键,导致其原子上的电子云密度降低,使得Ar-O键中的成键电子更偏向于配位原子,从而导致苯环上C-O共价键的键强度降低,其伸缩振动吸收峰低场移动.通常在形成配位键后,配位原子(如N)电子云密度降低,相应红外伸缩振动吸收峰会向低波移动,但样品的红外结果显示,-C=N-伸缩振动吸收峰出现在1 616 cm-1,与配体-C=N-伸缩振动吸收峰(1 614 cm-1)位置类似,我们推测这是由于在Zn(salophen)配合物中,Zn(II)原子与salophen配位后形成五配位结构,配位基团包含两个Ar-O-与一个CH3O-,导致Zn中心电子云密度增强,进而导致配体与Zn配位前后-C=N-伸缩振动吸收峰几乎没有变化.这些结果都表明我们合成的配合物为目标产物.salophen配体有四个配位原子,Zn(II)金属与其配位过程中,结构与溶剂有关,往往与一个溶剂分子配位形成五配位结构[11].在之前报道的几例晶体结构中已经得到证实,本文中,质谱、元素分析等表征结果显示,Zn(II)金属配合物也形成典型的五配位结构.但是由于其溶解性问题,暂时没有得到其晶体结构.2.3 配合物紫外—可见光谱分析样品的紫外—可见光谱在乙醇或DMSO溶剂中测定(图4).结果显示,Zn(salophen)金属配合物270-500 nm处出现两个吸收峰,这是由于配体间电子π-π*跃迁产生的,而这两个吸收峰的出现也与之前报道[12]的类似的含salophen配体的Zn(II)配合物的吸收峰位置相似.在乙醇溶剂中,Zn配合物在295 nm、397 nm有最强吸收峰,而在DMSO溶剂中Zn配合物在297 nm、404 nm有最强吸收峰,这可能是因为在极性溶剂中,溶剂极性越大,配合物与溶剂作用越大,激发态越稳定,能量越低,导致吸收峰波长红移.2.4 配合物荧光光谱分析为探测配合物荧光性能,对合成Zn(salophen)配合物进行了荧光测定(图5).在乙醇溶剂中,用397 nm激发,Zn(salophen)配合物在507 nm出现强烈的荧光发射峰.该发射光谱也与之前Ferran课题组报道的类似Zn(salophen)配合物一致.北京大学张俊龙课题组通过salophen衍生物的Zn配合物的细胞内荧光探针功能进行了深入的研究[13],并且发现,分子间Zn…O作用可以改变配合物聚集状态,进而影响其细胞摄取能力及生物成像功能.本文所合成的Zn(salophen)金属配合物,由于含有氟取代基团,在不改变荧光性能的前提下,增加了其生物相容性,因此,在生物荧光探针方面具有潜在的研究与应用价值.本文合成了一例含氟salophen配体,并进一步合成了Zn(II)金属配合物,通过1H NMR、IR、LC-MS及元素分析分别对配体与Zn(II)金属配合物进行了表征,结果表明,Zn与salophen配体及甲醇分子形成五配位结构,且配合物具有良好的荧光性能,具有作为潜在的细胞内双光子荧光探针的应用价值.【相关文献】[1] Tang Y H,Kong X Q,Xu A,et al.Development of a two-photon fluorescent probe for imaging of endogenous formaldehyde in living tissues[J].Angewandte Chemie International Edition,2016,55(10):3356-3359.[2] Bae S K,Heo C H,Choi D J,et al.A ratiometric two-photon fluorescent probe reveals reduction in mitochondrial H2S production in parkinson’s disease gene knockout astrocytes[J].Journal of the American Chemical Society,2013,135(26):9915-9923.[3] Yao S,Belfield K D.Two-photon fluorescent probes for bioimaging[J].European Journal of Organic Chemistry,2012,2012(17):3199-3217.[4] Li G Y,Lin Q,Sun L L,et al.A mitochondrial targeted two-photon iridium(Ⅲ) phosphorescent probe for selective detection of hypochlorite in live cells and invivo[J].Biomaterials,2015,53:285-295.[5] Kim H M,Cho B R.Small-molecule two-photon probes for bioimagingapplications[J].Chemical Reviews,2015,115(11):5014-5055.[6] Chen Y,Guan R L,Zhang C,et al.Two-photon luminescent metal complexes for bioimaging and cancer phototherapy[J].Coordination Chemistry Reviews,2016,310:16-40.[7] Huang Huaiyi,Yang Liang,Zhang Pingyu,et al.Real-time tracking mitochondrial dynamic remodeling with two-photon phosphorescent iridium (III)complexes[J].Biomaterials,2016,83:321-331.[8] Vent-Schmidt T,Brosi F,Metzger J,et al.Fluorine-rich fluorides:new insights into the chemistry of polyfluoride anions[J].Angewandte Chemie InternationalEdition,2015,54(28):8279-8283.[9] Gillis E P,Eastman K J,Hill M D,et al.Applications of fluorine in medicinalchemistry[J].Journal of Medicinal Chemistry,2015,58(21):8315-8359.[10] Tong G S,Chow P K,To W P,et al.A theoretical investigation into the luminescentproperties of d8-transition-metal complexes with tetradentate schiff baseligands[J].Chemistry,2014,20(21):6433-6443.[11] Germain M E,Vargo T R,Khalifah P G,et al.Fluorescent detection of nitroaromatics and 2,3-nimethyl-2,3-dinitrobutane (DMNB) by a zinccomplex:(salophen)Zn[J].2007,46(11):4422-4429.[12] Sabaté F,Giannicchi I G,Acón L,et al.Anion selectivity of Zn-salophenreceptors:influence of ligand substituents[J].Inorganica Chimica Acta,2015,434:1-6. [13] Tang J,Cai Y B,Jing J,et al.Unravelling the correlation between metal induced aggregation and cellular uptake/subcellular localization of Znsalen:an overlooked rule for design of luminescent metal probes[J].Chemical Science,2015,6(4):2389-2397.。
希夫碱金属配合物的研究及进展摘要:本文综述了希夫碱金属配合物的研究现状和分类,以及其催化性能,抗菌抗癌性,在电极和荧光性方面的应用,并对此配合物今后的研究做了进一步的展望。
关键词:希夫碱;金属配合物;应用研究;展望The Research and Progress ofSchiff-alkali Metal ComplexesAbstract:Research status and classification of Schiff-alkali metal complexes were summarized in this paper, and several aspects of the application such as catalytic properties, antibacterial and anti-cancer, electrode and fluorescence were outlined. Moreover, the further prospects of the complexes are expounded.Key words: Schiff –alkali Mental complexes Application and research Prospect希夫碱化合物是指由伯胺与活泼羰基化合物合成的一类含有亚甲胺基的化合物,其吡啶环上存在着配位能力极强的N原子,以及环外N原子,是一种性能优良的有机配体,而金属离子含有空轨道,可接纳配体提供的电子对,从而形成配合物。
官能化的希夫碱金属配合物结构稳定而丰富[1],在生物、催化、材料及分析化学领域存在广泛应用而引起人们的广泛兴趣。
现将希夫碱金属配合物的研究进展和主要类型综述如下。
1.希夫碱金属配合物的研究现状目前,某些氨基酸希夫碱金属配合物的研究已取得了极大的进展[2],例如可用作活性高,反应条件温和的催化剂,其中由水杨醛和各种氨基酸衍生的希夫碱配合物在合成与催化等方面的应用也越来越广泛。