碘克沙醇杂质经验总结分享
- 格式:pdf
- 大小:110.80 KB
- 文档页数:1
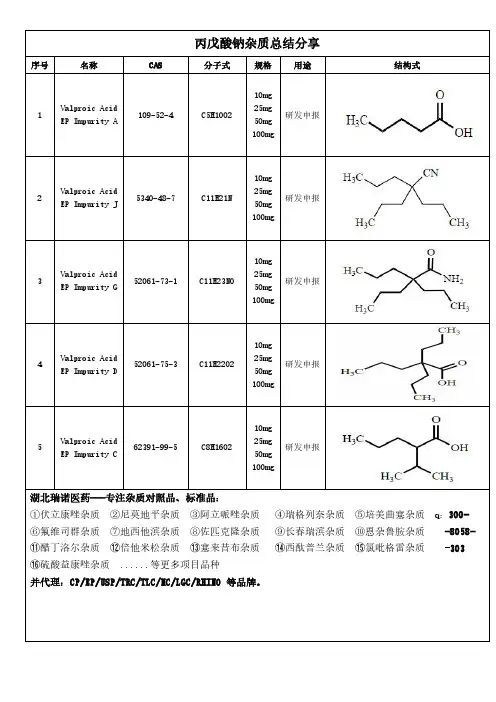
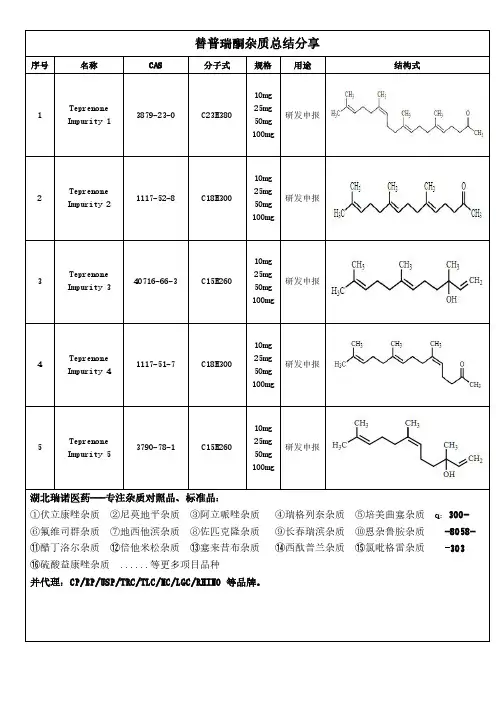
替普瑞酮杂质总结分享
序号
名称
CAS
分子式
规格
用途
结构式
1
Teprenone Impurity 1
3879-23-0C23H38O
10mg 25mg 50mg 100mg
研发申报
2
Teprenone Impurity 2
1117-52-8C18H30O
10mg 25mg 50mg 100mg
研发申报
3
Teprenone Impurity 3
40716-66-3C15H26O
10mg 25mg 50mg 100mg
研发申报
4
Teprenone Impurity 4
1117-51-7C18H30O
10mg 25mg 50mg 100mg
研发申报
5
Teprenone Impurity 5
3790-78-1C15H26O
10mg 25mg 50mg 100mg
研发申报
湖北瑞诺医药---专注杂质对照品、标准品:①伏立康唑杂质②尼莫地平杂质③阿立哌唑杂质④瑞格列奈杂质⑤培美曲塞杂质q:300-
⑥氟维司群杂质⑦地西他滨杂质⑧佐匹克隆杂质⑨长春瑞滨杂质⑩恩杂鲁胺杂质-8058-⑪醋丁洛尔杂质⑫倍他米松杂质
⑬塞来昔布杂质
⑭西酞普兰杂质
⑮氯吡格雷杂质
-303
⑯硫酸益康唑杂质......等更多项目品种
并代理:CP/EP/USP/TRC/TLC/MC/LGC/RHINO 等品牌。
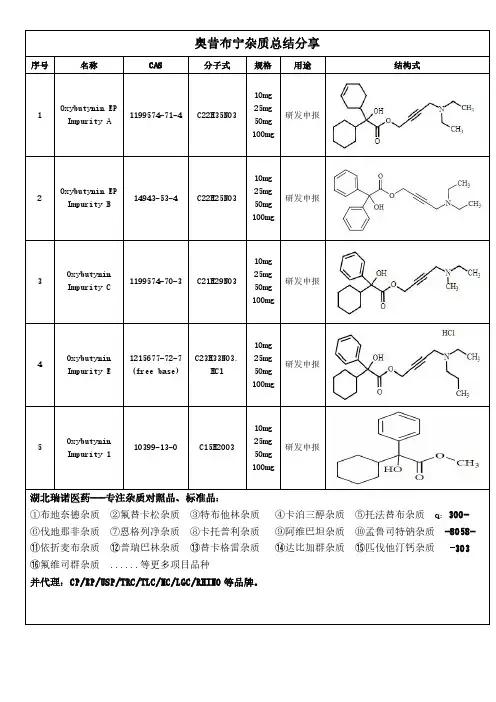
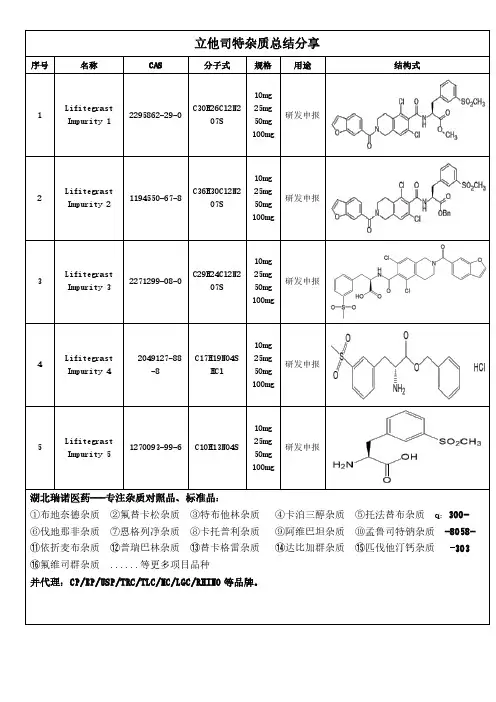
立他司特杂质总结分享
序号
名称
CAS
分子式
规格
用途
结构式
1
Lifitegrast Impurity 1
2295862-29-0
C30H26Cl2N2
O7S
10mg 25mg 50mg 100mg
研发申报
2
Lifitegrast Impurity 2
1194550-67-8
C36H30Cl2N2
O7S
10mg 25mg 50mg 100mg
研发申报
3
Lifitegrast Impurity 3
2271299-08-0
C29H24Cl2N2
O7S
10mg 25mg 50mg 100mg
研发申报
4
Lifitegrast Impurity 42049127-88
-8C17H19NO4S
HCl
10mg 25mg 50mg 100mg
研发申报
5
Lifitegrast Impurity 5
1270093-99-6C10H13NO4S
10mg 25mg 50mg 100mg
研发申报
湖北瑞诺医药---专注杂质对照品、标准品:①布地奈德杂质②氟替卡松杂质③特布他林杂质④卡泊三醇杂质⑤托法替布杂质q:300-
⑥伐地那非杂质⑦恩格列净杂质⑧卡托普利杂质⑨阿维巴坦杂质⑩孟鲁司特钠杂质-8058-⑪依折麦布杂质⑫普瑞巴林杂质
⑬替卡格雷杂质
⑭达比加群杂质
⑮匹伐他汀钙杂质
-303
⑯氟维司群杂质......等更多项目品种
并代理:CP/EP/USP/TRC/TLC/MC/LGC/RHINO 等品牌。

碘帕醇-370和碘克沙醇-320在多排CT检查患者中的有效性和安全性比较Dushyant V. Sahani, MD, Gilles Soulez, MD, Ke-min Chen, MD, Luigi Lepanto, MD, Jian-rong Xu, MD, Rendon C. Nelson, MD, Luigi Grazioli, MD, Angelo Vanzulli, MD, Jay P. Heiken, MD 及参加IMP ACT研究的研究者目的:在对比增强多排计算机断层扫描(CE-MDCT)检查中,前瞻性地比较碘帕醇-370和碘克沙醇-320对患者心率(HR)和对比增强有效性的影响。
方法:IMPACT是一项多中心、双盲研究,包括166例经随机化分配,按4 mL/秒静脉注射等碘剂量(40 gI)的碘帕醇-370或碘克沙醇-320进行肝脏(n = 121)或外周动脉(n = 45)CE-MDCT检查的患者。
CE-MDCT检查采用16排MDCT扫描仪,按照预定成像方案进行。
患者取仰卧位,在注射对比剂前测量心率并持续监测至给药后5分钟。
比较两组患者的HR均值和峰值增加量、以及HR增加量达到预定范围(>5且<10、≥10且<15、≥15且<20、>20 bpm)的受试者比例。
由两位处于盲态的独立阅片人评估肝脏图像,通过预设定感兴趣区在动脉期和门脉期的表现评价对比增强[Hounsfield单位(HU)]。
结果:对HR的影响:84例患者使用碘帕醇-370,82例接受碘克沙醇-320。
两组的平均年龄、性别分布、体重、总碘剂量、剂量/体重、合并用药及β阻滞剂使用情况均可比。
两组的基线HR平均值(碘帕醇-370组:72.3 ±12.5 bpm;碘克沙醇-320组:74.5 ±11.9 bpm)和给药后峰值HR较基线值的平均变化量(碘帕醇-370组:8.0 ±9.3 bpm,而碘克沙醇-320组为8.4 ±14.7 bpm,P = 0.72)均相似。
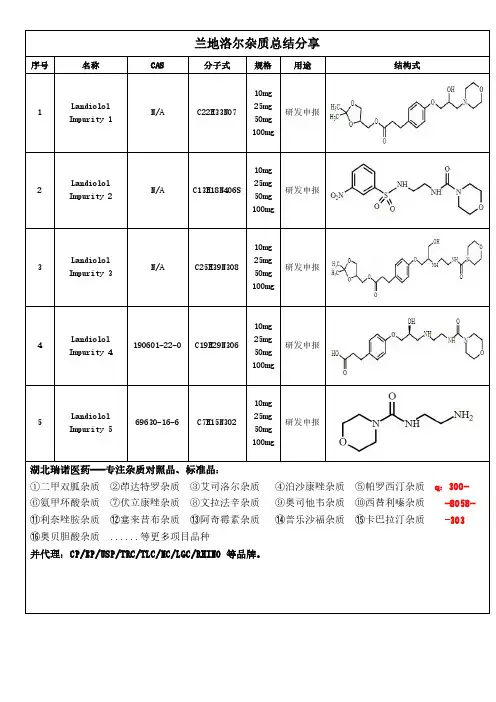
兰地洛尔杂质总结分享
序号
名称
CAS
分子式
规格用途
结构式
1
Landiolol Impurity 1
N/A C22H33NO710mg 25mg 50mg 100mg
研发申报
2
Landiolol Impurity 2
N/A C13H18N4O6S
10mg 25mg 50mg 100mg
研发申报
3
Landiolol Impurity 3
N/A C25H39N3O8
10mg 25mg 50mg 100mg
研发申报
4
Landiolol Impurity 4
190601-22-0C19H29N3O6
10mg 25mg 50mg 100mg
研发申报
5
Landiolol Impurity 5
69630-16-6C7H15N3O2
10mg 25mg 50mg 100mg
研发申报
湖北瑞诺医药---专注杂质对照品、标准品:①二甲双胍杂质②茚达特罗杂质③艾司洛尔杂质④泊沙康唑杂质⑤帕罗西汀杂质q:300-
⑥氨甲环酸杂质⑦伏立康唑杂质⑧文拉法辛杂质⑨奥司他韦杂质⑩西替利嗪杂质-8058-⑪利奈唑胺杂质⑫塞来昔布杂质
⑬阿奇霉素杂质
⑭普乐沙福杂质
⑮卡巴拉汀杂质
-303
⑯奥贝胆酸杂质......等更多项目品种
并代理:CP/EP/USP/TRC/TLC/MC/LGC/RHINO 等品牌。

在检验分析中的小经验与小技巧分享(doc 18页)部门: xxx时间: xxx整理范文,仅供参考,可下载自行编辑1、检验吲哒帕胺片的含量测定时,采用超声波超声可使片剂更易分散,主成分溶解完全,没有浪费,与研磨转移方法比较,对含量均匀度测定没有影响,且简单方便且更合理。
2、乙醇溶解主成分后,不能溶解辅料,需要过滤。
采用离心方法使辅料沉淀,取上清夜。
(注意,有很多离心管不具塞子,可用柔软的塑料薄膜袋扎橡皮筋做塞子。
没有塞子离心,偏差可达5%),与薄膜过滤法比较,对测定结果没有影响。
而且,如果过滤法操作不够快速,乙醇挥发,易影响测定结果。
3、在做中药材的浸出物的检测时,一定要按标准控制好溶剂的浓度(如乙醇等),否则检验结果会差异很大。
4、当液相鉴别中供试品与对照品出峰时间不一致,无法判断是否合格时,可用对照品与供试品各半配成混合溶液后进样,若峰宽未变宽,未出现驼峰,即可判断为合格。
5、做原料残留物检测的时候,如果主药对杂质有干扰,现有方法无法检出,需要自己建方法的话,要优先考虑利用理化性质将杂质分离出来再进行测定。
往往有意想不到的效果。
6、在药材薄层色谱鉴别时应该考虑一下展开剂的温度与配制顺序,有时会影响色谱的结果。
7、做药品有机溶剂残留量检查时,可以不拘泥于规定的色谱柱, 通常的DB-624可以满足要求, 取样量也可以灵活调整, 标准溶液浓度根据限度做相应调整就可以了。
8、薄层色谱鉴别时饱和时间一定要够。
9、在采用HPLC法测物质含量时,如若流动相中用了缓冲盐,一定要注意其pH值,放置过程中可能会产生变化,而某些药物对这种变化很敏感。
10、用HPLC法测物质含量时,温度的控制极其重要,最好用有柱温箱的,如果没有就要装空调保持恒温后再测定,否则会出现基线飘移,结果不准确。
11、有些品种温度的影响非常大,我遇到一个品种.对照品溶液不能放在冰箱中,放在液相室内还开着空调,第二天才能做,否则第二天的对照品到中午也不能用。

第三章 药物的杂质检查杂质(forin 、impurities )是指:1. 有毒副作用的物质2. 本身无毒副作用,但影响药物的稳定性和疗效的物质3. 本身无毒副作用,也不影响药物的稳定性和疗效,但影响药物的科学管理的物质药物中杂质的来源1. 生产过程中引入(1)原料、反应中间体及副产物(2)试剂、溶剂、催化剂类(3)生产中所用金属器皿、装置以及其他不耐酸、碱的金属工具所带来的杂质2. 贮藏过程中产生水解、氧化、分解、异构化、晶形转变、聚合、潮解和发霉等易发生水解反应的结构:酯、内酯、酰胺、卤代烃、苷类等药物中的杂质按来源分为1. 一般杂质(general impurities )如氯化物、硫酸盐、铁盐、重金属、砷盐、酸、碱、水分、易炭化物、炽灼残渣等。
一般杂质的检查方法收载在中国药典的附录中。
2. 特殊杂质(special impurities ):指某一个或某一类药物的生产或贮藏过程中引入的杂质,如阿司匹林中的游离水杨酸、异烟肼中的游离肼、甾体激素中的有关物质。
特殊杂质检查方法收载在中国药典正文各药品的质量标准中。
杂质限量:指药物中允许杂质存在的最大量,通常用百分之几或百万分之几来表示药物的杂质检查法1. 对照法限量检查法 (Limit Test )特点:不需知道杂质的准确含量2. 灵敏度法系指在供试品溶液中加入试剂,在一定反应条件下,不得有正反应出现。
特点:不需对照物质3. 比较法含量测定法:测定杂质的绝对含量,如测定吸光度、pH 值等。
特点:准确测定杂质的量,不需对照品杂质限量的计算供试品量允许杂质存在的最大量杂质限量一般杂质检查规则《药品检验操作标准》规定:1. 遵循平行操作原则(1)仪器的配对性:如纳氏比色管应配对,刻度线高低相差不超过 2mm ,砷盐检查时导气管长度及孔的大小要一致(2)对照品与供试品同步操作2. 正确的比色、比浊方法3. 检查结果不符合规定或在限度边缘时应对供试管和对照管各复查二份氯化物检查法(一)原理 对照法检查方法 药典附录除另有规定外,取各药品项下规定量的供试品,加水溶解使成25ml (溶液如显碱性,可滴加硝酸使成中性),再加稀硝酸10m1;溶液如不澄清,应滤过;置50ml 纳氏比色管中,加水使成约40m1,摇匀,即得供试溶液。

核准日期:2011年12月01日修正日期:2011年12月29日碘克沙醇打针液解释书请细心浏览解释书并在医师指点下应用.【药品名称】通用名:碘克沙醇打针液英文名:Iodixanol Injection汉语拼音:Diankeshachun Zhusheye【成份】本品活性成份为碘克沙醇.化学名称:5,5’-((2-羟基-1,3-丙二基)-双(乙酰基氨基))-双(N,N’-双(2,3-二羟基丙基)-2,4,6-三碘-1,3-苯二甲酰胺).化学构造式:分子式:C35H44I6N6O15分子量:1550.20辅料:氨丁三醇,氯化钠,氯化钙,EDTA钙钠,盐酸调节pH,打针用水【性状】本品为无色或淡黄色的澄明液体.碘克沙醇是一非离子型.双体.六碘.水溶性的X 线造影剂.与全血和其它响应规格的非离子型单体造影剂比拟,所有临床应用浓度的纯碘克沙醇水溶液具有较低的渗入渗出压.经由过程参加电解质,本品和正常的体液等渗.本品的渗入渗出压和粘度值如下:浓度渗入渗出压mOsm/kg H2O粘度(mPa﹒s)37℃20℃37℃320mgI/ml 290*办法:蒸汽压渗入渗出压测定法.本品的pH 值为.【顺应症】X-线比较剂,用于成人的血汗管造影.脑血管造影(通例的与i.a.DSA).外周动脉造影(通例的与i.a.DSA).腹部血管造影(通例的与i.a.DSA).尿路造影,静脉造影以及CT加强检讨;儿童血汗管造影.尿路造影和CT加强检讨.【规格】50ml:16g(I)【用法用量】给药剂量取决于检讨的类型.年纪.体重.心输出量和病人全身情形及所应用的技巧.平日应用的碘浓度和用量与其它当今应用的含碘X 线比较剂类似,但在一些研讨中应用较低碘浓度的碘克沙醇打针液也得到足够的诊断信息.与其它比较剂一样,在给药前后应给病人充足的水分.下列推举的剂量可作为指点,用于动脉内打针的单次剂量,可反复应用.顺应症/检讨用量动脉内应用动脉造影选择性脑动脉造影一次打针5~10 ml自动脉造影一次打针40~60 ml外周动脉造影一次打针30~60 ml 血汗管造影左心室与自动脉根打针一次打针30~60 ml 选择性冠状动脉造影一次打针4~8 ml儿童依据年纪.体重和病理情形(推举最大总剂量为按体重10ml/kg)静脉内应用尿路造影成人40~80 ml儿童<7kg 按体重2~4 ml/kg儿童>7kg 按体重2~3 ml/kg所有剂量均依据年纪.体重及病理情形(最大剂量为50ml)CT加强成人:头部CT 50-150ml成人:体部CT 75-150ml儿童:头.体部CT 按体重2-3ml/kg 可至50ml(少数病例可至150ml)老年人: 与其他成年人剂量雷同.【不良反响】下面列举了应用本品进行放射学检讨而可能产生的不良反响.与含碘比较剂有关的不良反响本质上一般都为轻到中度且为临时性的,非离子型比较剂的不良反响要比离子型比较剂更少.重度反响和致逝世反响平常罕有.罕有的不良反响为轻度的感到平常,如热感或冷感.外周血管造影常会引起热感(发病率>1:10),而远端痛苦悲伤偶然产生(发病率<1:10,但>1:100).腹部不适/痛苦悲伤平常罕有(发病率<1:1000),胃肠道反响如恶心.吐逆也很少见(发病率<1:100,但>1:1000).过敏反响偶然产生,平日表示为轻度的呼吸道和皮肤反响,如呼吸艰苦.皮疹.红斑.荨麻疹.瘙痒和血管性水肿,它们可在打针后立刻消失也可在几天后消失.可能产生低血压或发烧.曾有报导产生轻微甚至毒性皮肤反响.轻微的反响如喉头水肿.支气管痉挛或肺水肿和过敏样休克平常罕有.过敏样反响的产生可能与剂量和用药门路无关,轻微反响的最初症状可能仅是稍微的过敏症状,必须立时停滞中断应用比较剂,须要时应立刻经由过程静脉给药进行响应的治疗.应用β受体阻滞剂的病人其过敏反响的症状可能不典范,轻易误为迷走神经反响.迷走神经反响可引起低血压和心律过缓,很少见.碘中毒或“碘中毒性腮腺炎”是一种罕有的与应用碘比较剂有关的并发症,表示为腮腺的肿胀和触痛,可中断至检讨后10 天.短暂性血清肌酐上升也很罕有,但平日无临床意义.肾功效衰竭平常罕有,不过在高危病人组有致逝世病例的报导.冠脉.脑或肾动脉打针后会引起动脉痉挛并导致局部缺血.神经体系反响平常罕有,它们可为头痛.眩晕.癫痫发生发火或短暂性活动或感到障碍.偶可在随访的CT 扫描时见到比较剂经由过程血脑樊篱为脑皮质摄取,有时可伴短暂性意识隐约或皮层盲.心脏并发症如心律杂乱.心功效减退或心肌缺血都很少见.可能产生高血压.静脉造影后的血栓性静脉炎和静脉内血栓形成很少见.曾有极个体关节痛的病例报导.可能产生轻微的呼吸道症状和征兆(包含呼吸艰苦,支气管痉挛,喉痉挛,非心源性肺水肿)和咳嗽.【禁忌】未经掌握症状的甲亢患者及既往对本品有轻微不良反响史的患者.【留意事项】应用非离子型造影剂的一般留意事项有过敏.哮喘和对含碘制剂有过不良反响的需特别留意.对这些病例可斟酌应用预防用药,如类固醇,H1,H2组胺受体拮抗剂等.应用本品后产生轻微反响的风险较小.但是,含碘比较剂可激发过敏样反响或其它过敏反响的表示.是以应预先辈行急救措施的练习并准备必须的挽救药物和器械以敷衍可能消失的轻微反响.在全部X 线检讨进程中应始终应用内置插管或导管以保持静脉输液通路疏浚.鉴于预实验对由非离子型比较剂引起的过敏反响猜测的精确性极低,以及预实验本身也可能导致轻微过敏反响,是以不建议采取预实验来猜测碘过敏反响.在体外实验中,非离子型比较剂对凝血体系的影响较离子型比较剂轻.在施行血管造影术时,应十分当心在血管内的技巧操纵,不时地用肝素化的心理盐水灌洗导管以削减与操纵技巧相干的血栓形成和栓塞.在用比较剂前后必须包管病人体内有足够的水分.这一点尤其合适患有多发性骨髓瘤.糖尿病.肾功效不全的病人及婴幼儿和老年人.小于 1 岁的婴儿,特别是新生儿易引起电解质杂乱和血液动力学掉调.对有轻微心脏病和肺动脉高压的病人需特别留意.因为他们易成长为血液动力学掉折衷心律杂乱.有急性脑病,脑瘤,或癫痫病史的病人要预防癫痫发生发火并需特别留意.别的,酗酒及药物成瘾者其癫痫发生发火和精神病理学转变的安全大为增长.为预防应用比较剂后的急性肾功效衰竭,对已有肾功效伤害和糖尿病的病人需特别留意,因为他们的安全性较大.异型球蛋白血症(多发性骨髓瘤病和Waldenstrom 巨球蛋白血症)的病人安全性也较大.预防措施包含:−肯定有高危身分的病人.−确保体内有充足的水分.若有须要,可在检讨前由静脉保持输液直到比较剂从肾脏消除.−在比较剂消除之前防止任何加重肾脏累赘的肾毒性药物.口服胆囊比较剂.动脉钳闭术.肾动脉成形术或其它大型手术.−推迟再次造影检讨直到肾功效恢复至检讨前程度.为防止乳酸性酸中毒,在对应用二甲双胍的糖尿病人血管内打针含碘比较剂前,必须测定血清肌酐程度.对于血清肌酐/肾功效正常的患者:在打针比较剂时必须停用二甲双胍并在48 小时内不克不及恢复用药,或直至肾功效/血清肌酐达正常值.对于血清肌酐/肾功效不正常的患者:必须停用二甲双胍并将比较剂检讨推迟至48 小时后.只有在肾功效/血清肌酐程度恒定后才干恢复二甲双胍的用药.对有些肾功效不正常或未知的急救病例,大夫必须评估应用比较剂检讨的利弊,并需采纳预防措施:停用二甲双胍.给病人充足的水分.监测肾功效和细心不雅察乳酸性酸中毒的症状.轻微肝肾功效不全的病人需特别留意,因为这些病人消除比较剂的时光明显延伸.血透的病人可能接收比较剂检讨,在打针比较剂后立刻进行血液透析不是必须的,因为没有证据标明血液透析能呵护肾功效伤害的病人不得比较剂肾病.含碘比较剂可加重重症肌无力的症状.嗜铬细胞瘤病人在介入治疗时应赐与预防高血压危象的α 受体阻滞剂.甲亢病人也需特别留意.多发结节性甲状腺肿的病人在应用碘比较剂后有成长成甲亢的可能.应清晰地熟悉到早产儿在应用比较剂后有短暂性甲减的可能.今朝尚无碘克沙醇打针液外渗的报导.但因为碘克沙醇打针液是等渗的,一旦外渗,它所引起的局部痛苦悲伤和水肿比高渗比较剂引起的症状轻.通例处理办法为举高患肢和局部冷敷.万一产生隔室分解症需手术减压.不雅察时光:应用比较剂后的病人应至少不雅察30 分钟,因为大多半的轻微不良反响都产生在这段时光.然而,经验标明:过敏反响可能产生在几小时甚至几天后.【妊妇及哺乳期妇女用药】人类怀胎时代应用本品的安然性并未确立.动物实验研讨的成果并未直接或间接标明对人类生殖.胚胎或胎儿发育.怀胎进程.围产期及产后的伤害感化.因为在怀胎的任何时刻都应防止射线的照耀,所以无论应用比较剂与否,在对怀胎妇女进行X 线检讨前必须郑重衡量利弊.本品不该用于怀胎妇女,除非利大于弊,并且临床大夫以为必须.比较剂在人类乳汁中的排出量未知,固然估量很少,但在应用本品前应停滞母乳豢养,并中断到至少24小时后.【儿童用药】见【用法与用量】项下内容【老年患者用药】与其他成年人用药剂量雷同.【药物互相感化】应用比较剂可能会导致短暂性肾功效不全,这可使服用二甲双胍的糖尿病人产生乳酸性酸中毒(详见【留意事项】项下内容).两周内用白细胞介素-2 治疗的病人其延迟反响的安全性会增长(伤风样症状和皮肤反响).所有的含碘比较剂都邑影响甲状腺功效的测定,甲状腺碘联合才能降低会中断几周.血清和尿中高浓度的比较剂会影响胆红素.蛋白或无机物(如铁.铜.钙和磷酸盐)的实验室测定成果.在应用比较剂的当天不该做这些检讨.配伍禁忌未发明有配伍禁忌.但是本品不克不及直接和其他药物混用.必须应用单独的打针器.【药物过量】具有正常肾功效的病人不轻易产生药物过量.检讨的中断时光很重要,因为肾脏耐受大剂量比较剂的才能有限(t½约 2 小时).万一过量,必须经由过程输液改正水电解质的不服衡,并中断监测肾功效至少3 天,如须要可进行血透以消除碘克沙醇.没有特别的拮抗剂.【药理毒理】打针时,有机联合碘在血管/组织中接收射线.在对健康自愿者静脉内打针碘克沙醇落后行检讨,大多半的血液动力学.临床化学和血凝参数与打针前的数值比较,未发明显著误差.所不雅察到的少量实验室参数的转变是微小的且无临床意义.碘克沙醇打针液对病人肾功效只产生稍微的影响.对于血清肌酐程度在的糖尿病患者,应用本品后仅3%病人肌酐程度的上升,而无肌酐程度上升的病人.从临近的管状细胞释放的酶(碱性磷酸酶和N-乙酰-β-葡萄糖亚酰胺酶)较打针非离子型单体比较剂要少,与离子单体型比较剂比较也有雷同的趋向.碘克沙醇打针液还有很好的肾脏耐受性.打针碘克沙醇打针液与其它比较剂比较,对血汗管参数,如:LVEDP.LVSP.心率和QT-时光以及股血管血流的影响较少.临床前安然性数据在大鼠与兔子的生殖研讨中没有证据显示由碘克沙醇引起的滋生力伤害或致畸.【药代动力学】碘克沙醇在体内快速散布,平均散布半衰期约为21 分钟.表不雅散布容积与细胞外液量(0.26 l/kg 体重)雷同,这标明碘克沙醇仅散布在细胞外液.没有检测到代谢物.蛋白联合率低于2%.平均渗出半衰期约为 2 小时.碘克沙醇重要由肾小球滤过经肾脏渗出.健康自愿者经静脉打针后,约80%的打针量在 4 小时内以本相从尿中排出,97%在24 小时内排出.只有约 1.2%的打针量在72 小时内从粪便中渗出.最大尿药浓度在打针后约 1 小时内消失.在所推举的剂量规模内未不雅察到有剂量依附性的动力学特点.【应用与操纵指点】如所有的非胃肠道药品,在应用碘克沙醇打针液前应进行目检,以检讨是否有微粒.变色和容器的破坏现象.仅在打针前才将产品抽入打针器.每瓶仅供一人应用,用剩药液弃去.在应用碘克沙醇打针液前可加热至体温(37ºC).【包装】玻璃瓶装.10瓶/盒.【贮藏】遮光,常温贮藏.【有效期】12个月.【履行尺度】YBH04502011【同意文号】国药准字H20113465【临盆企业】北京北陆药业股份有限公司【临盆地址】北京市密云县工业开辟区【邮政编码】101500【德律风号码】(010)62622266【传真号码】(010)82626933【网址】。
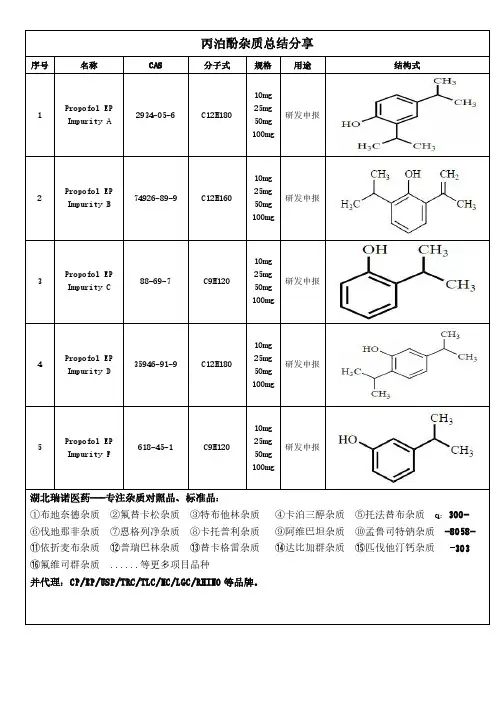
碘克沙醇杂质总结分享
序号名称CAS分子式规格用途结构式
1IodixanolEPImpurityB31127-80-7C16H20I3N3O710mg25mg50mg100mg研发申报
2IodixanolEPImpurityC171897-74-8C33H42I6N6O1410mg25mg50mg100mg研发申报
3IodixanolEPImpurityE255376-57-9C32H38I6N6O1310mg25mg50mg100mg研发申报
4IodixanolEPImpurityAN/AC19H26I3N3O910mg25mg50mg100mg研发申报
湖北瑞诺医药---专注杂质对照品、标准品:
①伏立康唑杂质②尼莫地平杂质③阿立哌唑杂质④瑞格列奈杂质⑤培美曲塞杂质q:300-
⑥氟维司群杂质⑦地西他滨杂质⑧佐匹克隆杂质⑨长春瑞滨杂质⑩恩杂鲁胺杂质-8058-
⑪醋丁洛尔杂质⑫倍他米松杂质⑬塞来昔布杂质⑭西酞普兰杂质⑮氯吡格雷杂质-303
⑯硫酸益康唑杂质......等更多项目品种
并代理:CP/EP/USP/TRC/TLC/MC/LGC/RHINO等品牌。