自体骨髓干细胞肝内移植治疗失代偿期 肝硬化的初步临床观察
- 格式:pdf
- 大小:197.18 KB
- 文档页数:3

72经肝动脉自体骨髓干细胞移植治疗失代偿期肝硬化30例宋向奎刘健曹名波张立达李晓芳贾百灵张炳勇【摘要】目的探讨经肝动脉自体骨髓干细胞(B M SC)移植对失代偿期肝硬化患者的治疗作用。
方法选择肝硬化失代偿期患者30例,其中男2l例。
女9例,年龄24—75岁,平均(52±12)岁。
在无茵条件下抽取骨髓80一90H d,分离纯化骨髓干细胞,制备成骨髓干细胞悬液40I I l l,然后经肝动脉置管并缓慢泵入肝脏。
检测术后4周肝功能、凝血功能的变化,并观察症状、体征和不良反应情况。
结果术后4周与术前比较白蛋白、前白蛋白、活化部分凝血活酶时间(A P7r r),差异均有统计学意义(P<0.05),丙氨酸氨基转移酶、天门冬氨酸氨基转移酶、总胆红素比较差异无统计学意义(P>O.05)。
移植后患者临床症状(食欲、精神、腹胀、乏力)及体征(腹水、下肢水肿)均有明显改善;移植术中和术后来见明显不良反应或并发症发生。
结论自体B M SC移植治疗肝硬化失代偿期患者近期安全有效,不良反应少,生存质量提高。
【关键词l骨髓干细胞;移植;失代偿期肝硬化肝硬化是由多种病因引起的慢性、进行性、弥漫性肝脏病变,随着病情的发展进入肝硬化失代偿期,形成门静脉高压症,导致腹水、消化道出血和肝性脑病等一系列并发症,危及生命。
目前,治疗失代偿期肝硬化,在临床上不论是内科综合治疗,还是外科手术治疗,总体治疗效果不满意,大多预后不良。
原位肝移植是最理想的治疗方法,但是由于器官捐赠者的短缺、移植后免疫排斥反应、围术期风险、高昂的医疗赞以及道德伦理等问题等条件的制约,难以使更多的患者受益。
干细胞作为一类具有自我更新能力和多向分化潜能的细胞,利用其组织再生和损伤修复的功能,可在一定程度上改善终末期肝病患者的肝功能,为该病的治疗提供了新的思路。
l资料与方法1.1一般资料:我们选择了2009年8月至2010年2月在河南省人民医院消化内科住院的失代偿期肝硬化患者30例,肝功能C hi l d—T ur cot t e—Pus h(C T P)B级,临床诊断符合2000年修订的《病毒肝炎防治方案》诊断标准。









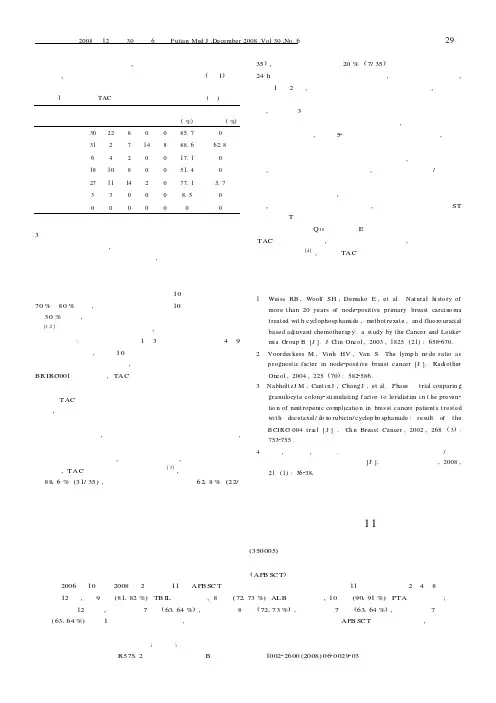
外有脱发、口腔炎、疲乏等,没有患者因不良反应终止化疗或死亡,未发生低血压、支气管哮喘等过敏反应(表1)。
表1 乳腺癌TAC方案术后辅助化疗的毒副反应(例)毒副反应表现例数Ⅰ度Ⅱ度Ⅲ度Ⅳ度发生率(%)Ⅲ、Ⅳ度发生率(%)血红蛋白减低302280085170白细胞减少312714888166218血小板减少6420017110消化道反应181080051140谷丙转氨酶升高271114207711517心脏毒性330008150过敏反应00000003 讨论在乳腺癌病例中,肿瘤大小、淋巴结转移情况及组织病理学性质是乳腺癌预后的重要指标,腋窝淋巴结状态是影响乳腺癌预后众多因素中最重要因素之一。
患者的生存期、局部复发、复发时间、远处转移及治疗失败与腋窝淋巴结转移数目密切相关。
腋窝淋巴结阴性的患者10年无瘤生存率在70%~80%左右,而腋窝淋巴结阳性者10年无瘤生存率则在30%以下,生存率随着阳性淋巴结数目的增多而递减[1,2]。
一般根据腋窝淋巴结镜检,将患者预后由好到差分为以下几组:无淋巴结转移或1~3个淋巴结转移组、4~9个淋巴结转移组,以及10个淋巴结以上有转移组。
腋窝淋巴结阳性患者预后较差,国际乳腺癌研究组设计的BR IRG001试验显示,TAC方案对改善腋窝淋巴结阳性的乳腺癌患者术后辅助化疗的无瘤生存期及总生存期均具有优越性。
TAC方案化疗后的近期毒性主要表现为严重的骨髓抑制,而消化道反应、肝肾功能损害、心脏毒性方面与其他术后辅助化疗方案的毒副作用大致相仿。
大多数化疗药有不同程度的骨髓抑制,骨髓抑制成为化疗的剂量限制性毒性,常因骨髓抑制而被迫中断化疗。
骨髓抑制首先表现为中性粒细胞减少和白细胞减少,继而血小板减少,严重者可出现全血减少,TAC方案骨髓毒性反应明显[3],其中白细胞下降达8816%(31/35),其中Ⅲ~Ⅳ度骨髓抑制达6218%(22/35),其中Ⅳ度发生率为20%(7/35)。
本方案需在化疗后24h用粒细胞集落刺激因子注射治疗,并密切检测血常规,常规1周2次,出现Ⅳ度骨髓抑制后每天查血常规,并在出现Ⅳ度骨髓抑制后给予预防性抗菌素治疗、口腔护理等治疗,若连续3天Ⅳ度骨髓抑制者给予抗真菌药物预防真菌感染。
经门静脉自体骨髓细胞回输治疗失代偿期肝硬化42例疗效分析张景春; 赵向宁; 刘保池【期刊名称】《《河南外科学杂志》》【年(卷),期】2019(025)006【总页数】3页(P13-15)【关键词】失代偿期肝硬化; 自体骨髓细胞; 门静脉; 肝功能【作者】张景春; 赵向宁; 刘保池【作者单位】河南科技大学第二附属医院肝胆外科洛阳471000; 上海市公共卫生临床中心普外科上海201508【正文语种】中文【中图分类】R657.3+1失代偿期肝硬化是临床上各种肝病的终末期病变,在我国发病率高、危害严重,除肝移植外目前临床上缺乏有效的治疗方法。
近年来,随着干细胞治疗技术及再生医学的发展,干细胞治疗已在多个领域内得到应用,为多种疾病的治疗提供了崭新的思路[1-2]。
有关骨髓干细胞治疗肝功能损伤的研究已有较多的报道,多中心研究证实自体骨髓干细胞可以修复患者受损的肝功能,也为终末期肝病的治疗提供了新的思路[3-5]。
本研究采取经门静脉输液港途径回输自体骨髓细胞治疗失代偿期肝硬化患者,以评价该治疗方法的效果及安全性。
1 资料与方法1.1 一般资料选择我科2018-03—2019-01间收治的失代偿期肝硬化患者42例。
男24例,女18例;年龄45~72岁,平均56.2岁。
根据患者病史、症状、体征及腹部超声、CT或MRI、肝纤维化无创检查结果均符合2000年修订的《病毒性肝炎防治方案》有关肝硬化的诊断标准[6]。
其中乙型肝炎肝硬化28例,丙型肝炎肝硬化6例,酒精性肝硬化6例,原发性胆汁性肝硬化2例。
肝功能分级:Child-Pugh分级B/C级。
并发肝性脑病1例,无感染及肝内占位性病变。
1.2 治疗方法患者入院后完善常规检查及术前准备。
硫普罗宁(山东罗欣药业集团公司)0.2 g加入5%葡萄糖注射液250 mL中静脉滴注,1次/d。
门冬氨酸钾镁注射液30 mL、维生素C 3.0 g加入10%葡萄糖注射液250 mL中静脉滴注,1次/d。
自体外周血干细胞治疗肝硬化的护理体会\【摘要】目的:总结自体外周血干细胞治疗肝硬化患者的护理方法。
方法:选择肝硬化失代偿期患者35 例,通过粒细胞刺激因子200ug皮下注射一日两次,连续四天,动员外周血干细胞,第五天应用血细胞分离机进行外周血干细胞分离单采。
在dsa下股动脉穿刺,经肝动脉将单采的细胞悬液移植入肝脏,通过加强采集前后及术前、术后的护理、出院指导,观察疗效。
结果:通过加强采集前后及术前、术后的护理、宣教指导,患者住院期间无不良反应及并发症,通过出院后一个月、三个月、六个月随访取得了良好的疗效。
结论:通过加强自体外周血干细胞治疗肝硬化患者的护理提高了患者的依从性及治疗效果。
【关键词】自体外周血干细胞;肝硬化;护理【中图分类号】r473.6 【文献标识码】a 【文章编号】1004-7484(2012)09-0202-01肝硬化是临床上的常见病、多发病,该病进入失代偿期后逐渐发展,最终可能导致肝功能衰竭而死亡。
虽然开展肝脏移植取得了一定的治疗效果,但是供移植的肝脏来源有限,此外器官移植的费用之高也令患者望而却步。
目前临床上主要仍以保肝对症支持治疗及预防并发症为主,因此失代偿期肝硬化的治疗效果不甚理想。
近年来骨髓干细胞移植治疗已在医学领域取得了令人瞩目的成就,也为终末期肝病的治疗提供了新方法,自体干细胞移植不存在免疫排斥及伦理问题,是一种具有广阔应用前景的有效治疗手段。
自2009年我科开展的自体外周血干细胞治疗对肝硬化取得了良好的治疗效果,现将护理体会报道如下:1 临床资料1.1 病例选择选择了2009年9月~2011年10月我科接受自体外周血干细胞治疗的肝硬化住院患者35例,女性10例,男性25例,其中肝炎后肝硬化30例,酒精性肝硬化4例,血吸虫性肝硬化1 例,年龄24~ 63岁,中位年龄51岁。
肝功能child-pugh a级5例,b级20例,c级10例,患者治疗前均明确诊断肝硬化[1]。
自体骨髓干细胞移植治疗肝衰竭[作者:潘兴南来源:180医院网络点击数:1259 更新时间:2007-7-25 文章录入:csw ]【字体:】乙型肝炎病毒感染是严重影响人类健康的疾病,估计全球约有3.5亿慢性HBV感染者。
在围生期和婴幼儿期感染的人群中,约25%在成年时将发展成肝硬化或肝癌。
慢性乙型肝炎患者中,肝硬化失代偿的年发生率约3%,5年累计发生率约16%,乙肝肝硬化代偿期和失代偿期的5年病死率分别为14%~20%和70%~86%。
全球每年约100万患者死于HBV相关的肝病,包括肝衰竭、肝硬化和肝癌等终末期肝病患者。
我国属HBV感染高发流行区,据流行病学调查统计,我国估计约1.2亿人为慢性HBV 感染,占全世界慢性HBV感染者的1/3,我国每年因慢性乙肝(包括肝硬化、肝癌)直接经济损失约9000亿人民币。
原位肝移植和肝干细胞移植均为终末期肝病有效的治疗手段,但前者因供肝来源有限、终身免疫抑制剂的应用等,使原位肝移植的临床应用受到限制,肝干细胞移植目前虽然尚不能取代原位肝移植,但因其取之于患者自身,不存在免疫排斥反应,且创伤小,治疗费用低,成为当前研究热点。
骨髓干细胞是肝干细胞的重要肝外来源。
骨髓干细胞在特定环境下可分化成骨髓源性肝干细胞(bonemarrow derived liver stem cell,BDLSC)、肝细胞及胆管细胞,从而参与肝功能的修复和重构。
大量研究证明,骨髓中确实存在能分化为肝细胞的干细胞,将其直接移植到肝脏,在肝脏微环境调节下可分化为肝细胞,可用于临床治疗。
近年来,人们已成功地开发了多种方法分离人类骨髓间充质干细胞,并在体外分化成为肝干细胞,且已发现肝细胞生长因子(HGF)是目前最强的肝细胞诱导分化剂。
用高浓度的HGF、FGF4诱导体外培养的大鼠骨髓干细胞,RT-PCR检测到白蛋白及AFP的表达,免疫细胞化学也证实了经诱导的干细胞出现了AFP、白蛋白及CK8/18等肝前体细胞的特征性表达。