氨基酸
- 格式:doc
- 大小:28.00 KB
- 文档页数:2

氨基酸的功效与作用18种氨基酸是构成蛋白质的基本单位,对人体的生长、发育和维持正常生理功能起着重要的作用。
氨基酸被广泛用于医药、保健品、化妆品等多个领域。
下面我们将详细介绍18种常见的氨基酸的功效与作用。
1. 谷氨酸(Glutamine)作用:谷氨酸是一种非必需氨基酸,是脑内最丰富的神经递质。
它可提供大脑的能量,增强脑力,改善记忆力,促进睡眠,减轻焦虑和紧张情绪。
此外,谷氨酸还可加快肌肉疲劳的恢复,促进胃肠道的健康。
2. 赖氨酸(Lysine)作用:赖氨酸是一种必需氨基酸,对增强免疫力、促进生长发育、维持心血管健康具有重要作用。
赖氨酸还可帮助合成胶原蛋白,维护皮肤的弹性,促进伤口愈合。
3. 酪氨酸(Tyrosine)作用:酪氨酸是一种非必需氨基酸,是合成肾上腺素、多巴胺、甲状腺激素等重要物质的前体。
它具有提神、增强记忆、改善心情、减轻抑郁等作用。
此外,酪氨酸还可帮助抗氧化,维护皮肤的健康。
4. 苯丙氨酸(Phenylalanine)作用:苯丙氨酸是一种必需氨基酸,是合成多种神经递质的前体。
它能提高注意力、增强记忆、改善心情和消除疲劳。
苯丙氨酸还可参与黑色素的合成,有助于维护皮肤和毛发的健康。
5. 色氨酸(Tryptophan)作用:色氨酸是一种必需氨基酸,是合成5-羟色胺的前体,可以提高情绪、改善睡眠质量,并具有抗抑郁的作用。
此外,色氨酸还具有调节食欲、促进生长发育和维护皮肤健康的功能。
6. 鸟氨酸(Arginine)作用:鸟氨酸是一种半必需氨基酸,对增强免疫力、促进生长激素的分泌、改善心血管功能等具有重要作用。
鸟氨酸还可促进伤口愈合,改善肝功能。
7. 天冬氨酸(Aspartic Acid)作用:天冬氨酸是一种非必需氨基酸,在脑内具有兴奋作用,可以提高注意力和学习能力。
天冬氨酸还可促进肾脏的解毒功能,调节肝脏代谢。
8. 缬氨酸(Valine)作用:缬氨酸是一种必需氨基酸,是组成肌肉蛋白质的主要成分之一,对维持肌肉组织的健康起着重要作用。

常见的20种氨基酸首先是甘氨酸,这甘氨酸啊就像个低调的小老弟,结构比较简单,在很多地方都默默发挥着作用呢。
丙氨酸,它就像是氨基酸家族里的普通一员,但是可别小瞧它,在构建蛋白质的时候也是个得力小助手。
缬氨酸呢,有点像那种默默干活的小工匠,稳稳地在蛋白质结构里出着自己的一份力。
亮氨酸和异亮氨酸这俩呀,就像是一对双胞胎,虽然有点相似,但是各自有着独特的作用,在蛋白质合成里可都是不可或缺的。
脯氨酸就比较特殊啦,它的结构有点像个小环,就像戴着个小戒指一样,在蛋白质的空间结构稳定方面有一手。
苯丙氨酸,一听这名字就感觉有点高级,它可是有个苯环的,就像氨基酸里带着个特殊的标志。
酪氨酸呢,感觉像是个有点文艺范的氨基酸,它和一些生理过程里的信号传导啥的有着千丝万缕的联系。
色氨酸,这个家伙可不得了,它能参与合成一些重要的神经递质,就像大脑里的小助手。
丝氨酸,就像个滑溜溜的小角色,它在很多酶的活性中心啥的能起到关键作用。
苏氨酸,像是那种规规矩矩的小成员,在蛋白质的构建和功能发挥上有着稳定的贡献。
半胱氨酸可就有趣啦,它有个巯基,就像带着个小尾巴,这个小尾巴还能和别的半胱氨酸牵手,形成二硫键,就像氨基酸之间的小拉手。
蛋氨酸,这可是蛋白质合成开始的时候经常用到的起始氨基酸,就像个带头大哥一样。
天冬酰胺和谷氨酰胺,这俩有点像一对兄弟,它们在氮的转运和储存方面有着重要的工作。
天冬氨酸,它和一些酸性环境下的生理过程有关,就像专门负责处理酸性事务的小能手。
谷氨酸呢,在神经传递等方面也有很重要的戏份,就像个信息传递员。
精氨酸,感觉像是个精力充沛的氨基酸,在很多生理功能里都有着活跃的表现。
组氨酸,它在一些酶的活性调节等方面有特殊的本领,就像个小小的调节器。
赖氨酸,就像个结实的小钉子,在蛋白质和其他生物分子的结合等方面发挥着重要的作用。

人体21种氨基酸人体中的21种氨基酸对于生命的构建和维护至关重要。
这21种氨基酸包括甘氨酸、丙氨酸、缬氨酸、亮氨酸、异亮氨酸、甲硫氨酸(蛋氨酸)、脯氨酸、色氨酸、丝氨酸、酪氨酸、半胱氨酸、苯丙氨酸、天冬酰胺、谷氨酰胺、苏氨酸、天门冬氨酸、谷氨酸、赖氨酸、精氨酸和组氨酸。
其中,甘氨酸是最简单的氨基酸,而其他氨基酸均由甘氨酸通过不同的组合方式形成。
这些氨基酸在人体中发挥着各种生理功能。
例如,甲硫氨酸(蛋氨酸)是蛋白质合成所必需的,而半胱氨酸则参与构成头发、皮肤和指甲的基本结构。
此外,精氨酸对于免疫系统的正常运作至关重要,而组氨酸则在神经系统发育和功能中扮演关键角色。
总的来说,人体中的21种氨基酸在生命的构建和维护中扮演着重要的角色。
它们在人体的各种生理过程中发挥着不可或缺的作用,因此,确保这些氨基酸的摄入对于维持身体健康至关重要。
氨基酸的摄入与膳食平衡为了维持人体健康,我们需要确保摄入足够的21种氨基酸。
一般来说,动物性食物来源的氨基酸较为丰富,如肉类、蛋类、奶制品等。
植物性食物中也含有氨基酸,但种类和含量相对较少。
因此,合理的膳食搭配有助于满足人体对氨基酸的需求。
膳食平衡对于氨基酸的摄入至关重要。
首先,要保证各种氨基酸的比例适当,以满足人体各种生理需求。
其次,要关注氨基酸的摄入量,特别是对于生长发育中的儿童、孕妇、老年人等特殊人群,更要注重氨基酸的摄入。
此外,生活方式和身体状况也会影响氨基酸的需求,如剧烈运动、慢性疾病等,都需要适当增加氨基酸的摄入。
氨基酸与疾病防治科学研究表明,氨基酸在疾病防治中具有一定的作用。
例如,苏氨酸和赖氨酸有助于增强免疫力,预防感染性疾病;色氨酸有助于改善情绪,预防抑郁症;谷氨酰胺对胃肠道功能有很好的保护作用,预防消化系统疾病等。
因此,通过调整膳食结构,增加氨基酸的摄入,有助于预防和控制多种疾病。
氨基酸的研究与应用随着科学技术的不断发展,氨基酸在生物医学、食品工业、制药等领域的研究与应用越来越广泛。

氨基酸的作用
氨基酸是组成蛋白质的基本单元,它在机体中发挥着多种重要作用:
1. 构建蛋白质:氨基酸通过脱水缩合反应,将单体氨基酸连接起来形成多肽链,最终构建各种功能性蛋白质。
不同种类和顺序的氨基酸决定了蛋白质的结构和功能。
2. 维持生命活动:许多酶、激素和抗体等生命活动中的重要分子都是由氨基酸构成的。
它们参与体内的新陈代谢、信号传导、免疫应答等生物过程,维持机体的正常功能。
3. 供能:在缺乏碳水化合物和脂肪供能时,氨基酸可以通过蛋白质的分解产生能量。
氨基酸中的碳原子经过解氨基、脱羧等反应,转化为葡萄糖或酮体,提供能量供给。
4. 合成其他生物分子:氨基酸还可以用于合成其他生物分子,如血红蛋白、神经递质、胶原蛋白等。
例如,赖氨酸、色氨酸等是合成生物活性物质的前体,通过代谢途径进一步转化为重要的信号分子和生理活性物质。
5. 维护酸碱平衡:氨基酸参与体液内酸碱平衡的调节。
当体液过酸或过碱时,一些氨基酸可以作为缓冲剂,接受或释放氢离子,维持体液pH值的稳定。
总的来说,氨基酸的作用与构建蛋白质、维持生命活动、供能、
合成其他生物分子和维护酸碱平衡密切相关。
这些作用对于维持机体的正常生理功能和生存至关重要。

20种常见氨基酸氨基酸是构成蛋白质分子的基本单元,也是细胞生命活动中不可或缺的有机化合物之一。
目前已发现了20种常见氨基酸,它们各自在不同的情况下发挥着重要作用。
1. 丝氨酸(Serine)是蛋白质中含量较高的氨基酸之一,它与钙离子结合,能够帮助肌肉收缩,并参与酶的催化作用。
2. 苏氨酸(Threonine)是人体必须的氨基酸,它是合成蛋白质和核酸的原料之一,同时也是重要的肌肉营养素。
3. 天冬酰胺(Asparagine)是人体自主合成的一种非必需氨基酸,具有调节中枢神经系统功能、促进肝脏解毒、增强人体免疫力等多项作用。
4. 赖氨酸(Lysine)是蛋白质质量评价所必须的氨基酸之一,它还能加速人体生长发育,提高体力和抗病能力。
5. 谷氨酰胺(Glutamine)是人体必须的氨基酸,它对肠道黏膜细胞有营养保护作用,能够促进肠道细胞生长、维持肠道屏障功能。
6. 组氨酸(Histidine)是非常重要的氨基酸之一,也是人体必需的氨基酸,它能够促进生长发育、增强记忆力、改善睡眠质量。
7. 赛氨酸(Cysteine)对人体健康有很多好处,如抗氧化、降脂降压、保肝等。
8. 苯丙氨酸(Phenylalanine)是非常重要的氨基酸之一,它能够促进神经系统的正常发育功能,同时还能抑制食欲、减肥。
9. 精氨酸(Arginine)是人体必需的氨基酸之一,能够降低血液中的胆固醇、促进肌肉生长、增强免疫力。
10. 酪氨酸(Tyrosine)是人体能产生的非必需氨基酸,它参与了体内多种生化反应,对皮肤、头发、甲状腺功能等都有很好的调节作用。
11. 色氨酸(Tryptophan)是人体必须的氨基酸之一,它参与了体内多种生化反应,能够抑制食欲、促进睡眠、提高免疫力。
12. 酪氨酸(Tyrosine)是人体能产生的非必需氨基酸,它参与了体内多种生化反应,对皮肤、头发、甲状腺功能等都有很好的调节作用。
13. 苯丙胺酸(Tyrptophan)参与胡萝卜素合成、促进生长发育等功能。

22种氨基酸的作用一、引言氨基酸是构成蛋白质的基本单位,也是生命活动中不可或缺的重要物质。
人体内有22种不同的氨基酸,每种氨基酸都有其独特的生理作用。
本文将详细介绍这22种氨基酸的作用,包括它们的种类与分布、功能、在生物体内的互动与平衡,以及不同种类氨基酸的生理作用及临床应用。
二、氨基酸的种类与分布人体内的22种氨基酸按照其化学结构可分为中性、酸性、碱性三类。
这些氨基酸广泛分布于人体各部位,参与蛋白质的合成、分解以及多种代谢过程。
例如,赖氨酸主要分布在骨骼肌、皮肤、毛发等部位,而谷氨酸则主要分布在脑部和肝脏。
三、氨基酸的功能1.蛋白质合成:氨基酸是蛋白质合成的基本原料,通过脱水缩合反应形成肽链,进而形成具有特定功能的蛋白质。
2.能量代谢:部分氨基酸如亮氨酸、异亮氨酸等可参与能量代谢过程,为人体提供能量。
3.细胞信号传导:部分氨基酸如谷氨酸、天冬氨酸等可作为神经递质参与细胞信号传导,影响神经系统的功能。
4.免疫调节:部分氨基酸如谷氨酰胺等可参与免疫调节过程,影响机体的免疫应答。
5.抗氧化:部分氨基酸如谷胱甘肽等具有抗氧化作用,可保护细胞免受氧化损伤。
四、氨基酸在生物体内的互动与平衡1.氮平衡:人体内的氮元素主要来源于蛋白质的分解和合成,通过氮平衡可以反映蛋白质的合成与分解情况。
2.氨基酸代谢:人体内的氨基酸代谢是一个复杂的过程,不同种类的氨基酸之间存在相互转化和利用关系。
例如,苯丙氨酸可以转化为酪氨酸,而酪氨酸又可以转化为多巴胺等神经递质。
3.氨基酸平衡:人体内的氨基酸处于动态平衡状态,不同种类的氨基酸之间保持一定的比例关系。
这种平衡对于维持机体的正常生理功能具有重要意义。
4.氨基酸与维生素的关系:部分氨基酸可以参与维生素的合成和分解过程,如色氨酸可以参与维生素B6的合成,而组氨酸可以参与维生素B12的合成。
5.氨基酸与矿物质的关系:部分氨基酸可以与矿物质结合形成螯合物,提高矿物质的吸收和利用效率。

人体21种氨基酸摘要:一、引言二、氨基酸的定义与作用1.蛋白质的基本组成单位2.生命活动的重要组成部分三、人体必需氨基酸1.9 种必需氨基酸2.对健康的重要作用四、非必需氨基酸1.12 种非必需氨基酸2.对人体的作用五、氨基酸的来源1.食物中的氨基酸2.内源性氨基酸六、氨基酸的平衡与健康1.氨基酸的摄入与代谢2.氨基酸不平衡的影响七、氨基酸在医疗和保健中的应用1.氨基酸治疗2.氨基酸保健品八、结论正文:一、引言氨基酸是构成生物体内蛋白质的基本组成单位,对于生命活动至关重要。
人体内有21 种氨基酸,其中9 种是必需氨基酸,12 种是非必需氨基酸。
本文将对这些氨基酸进行详细介绍,并探讨其在人体健康中的作用及来源。
二、氨基酸的定义与作用氨基酸是一种含有氨基(NH2)和羧基(COOH)的有机化合物。
它是蛋白质的基本组成单位,在人体内参与生命活动的各个方面,如生长发育、免疫反应、物质代谢等。
此外,氨基酸还可以通过转氨基作用生成其他非必需氨基酸,对人体健康具有重要作用。
三、人体必需氨基酸人体必需氨基酸是指人体无法自行合成,必须通过食物摄入的氨基酸。
根据研究,人体必需氨基酸共有9 种,分别是赖氨酸、色氨酸、苯丙氨酸、蛋氨酸、苏氨酸、异亮氨酸、亮氨酸、缬氨酸和组氨酸。
这些氨基酸对于健康至关重要,如赖氨酸参与肌肉合成,色氨酸有助于调节情绪等。
四、非必需氨基酸非必需氨基酸是指人体可以自行合成的氨基酸。
人体内有12 种非必需氨基酸,分别是丙氨酸、丝氨酸、天冬氨酸、谷氨酸、半胱氨酸、甲硫氨酸、精氨酸、酪氨酸、脯氨酸、羟脯氨酸和甘氨酸。
尽管人体可以自行合成这些氨基酸,但它们在人体内仍然具有重要作用,如参与肌肉修复、提高免疫力和抗氧化等。
五、氨基酸的来源氨基酸的来源主要有两种:食物中的氨基酸和内源性氨基酸。
食物中的氨基酸主要包括动物性食品、豆类、坚果等。
内源性氨基酸则是人体通过转氨基作用生成的氨基酸。
保持氨基酸摄入与代谢的平衡对于人体健康至关重要。

以下是常见的23种氨基酸:
1. 丙氨酸(Ala)
2. 谷氨酸(Glu)
3. 缬氨酸(Val)
4. 苯丙氨酸(Phe)
5. 青光氨酸(Trp)
6. 天冬氨酸(Asp)
7. 亮氨酸(Leu)
8. 色氨酸(His)
9. 甘氨酸(Gly)
10. 精氨酸(Arg)
11. 組氨酸(His)
12. 异亮氨酸(Ile)
13. 赖氨酸(Lys)
14. 苏氨酸(Ser)
15. 脯氨酸(Pro)
16. 酪氨酸(Tyr)
17. 山梨氨酸(Thr)
18. 脯氨酸(Pro)
19. 酪氨酸(Tyr)
20. 苏氨酸(Cys)
21. 甲硫氨酸(Met)
22. 酪氨酸(Trp)
23. 精氨酸(Lys)
这些氨基酸是构成蛋白质的基本组成部分,它们在生物体内发挥着重要的功能。
不同的氨基酸通过连接形成多肽链,进一步组合成蛋白质。
它们具有不同的化学性质和作用,对生物体的生理功能至关重要。

.第3章氨基酸四大类生物分子中蛋白质是生物功能的主要载体,而氨基酸(amino acid)是蛋白质的构件分子。
自然界中存成千上万在的种蛋白质,在结构和功能上的惊人的多样性归根结底是由20种常见氨基酸的内在性质造成的。
这些性质包括①聚合能力,②特有的酸碱性质,③侧链的结构及其化学功能的多样性,④手性。
本章主要讲述这些性质,它们是讨论蛋白质和酶的结构、功能以及许多其他有关问题的基础。
一、氨基酸—蛋白质的构件分子(一)蛋白质的水解一百多年前就开始了关于蛋白质的化学研究。
在早期的研究中,水解作用提供了关于蛋白质组成和结构的极其价值的资料。
蛋白质可以被酸、碱或蛋白酶催化水解。
在水解过程中,逐渐降解成相对分子质量越来越小的肽段(peptide fragment),直到最后成为氨基酸的混合物。
根据蛋白质的水解程度,可分为完全水解和部分水解两种情况。
完全水解或称彻底水解,得到的水解产物是各种氨基酸的混合物。
部分水解即不完全水解,得到的产物是各种大小不等的肽段和氨基酸。
下面简略地介绍酸、碱和酶3种水解方法及其优缺点:⑴酸水解常用H2SO4或HCl进行水解。
一般6mol/L HCl,4mol/L H2SO4;回流煮沸20h左右可使蛋白质完全水解。
酸水解的优点是不引起消旋作用(racemization),得到的是L-氨基酸。
缺点是色氨酸完全被沸酸所破坏,羟基氨基酸(丝氨酸及苏氨酸)有一小部分被分解,同时天冬氨酸和谷氨酰胺的酰胺基被水解下来。
⑵碱水解一般与5mol/L NaOH共煮10~20h,即可使蛋白质完全水解。
水解过程中多数氨基酸遭到不同程度的破坏,并且产生消旋现象,所得产物是D-和L-氨基酸的混合物,称消旋物(见本章氨基酸的光学活性部分)。
此外,碱水解所需时间较长。
因此酶法主要用于部分水解。
常用的蛋白酶有胰蛋白酶(trypsin)、胰凝乳蛋白酶或称糜蛋白酶(chymotrypsin)以及胃蛋白酶(pepsin)等,它们主要用于蛋白质一级结构分析以获得蛋白质的部分水解产物。

氨基酸水解什么是氨基酸水解氨基酸水解是一种生物化学过程,指的是将蛋白质分子中的肽键水解成氨基酸单元的过程。
蛋白质是由多个氨基酸通过肽键连接而成的,而氨基酸水解则是将这些肽键断裂,释放出单独的氨基酸。
氨基酸水解的方法氨基酸水解可以通过不同的方法实现。
以下是常用的两种方法:酶法水解酶法水解是利用特定的酶来催化氨基酸间的肽键水解。
常用的酶包括胃蛋白酶、胰蛋白酶等。
这些酶在适宜的pH和温度下能够高效地将蛋白质水解成氨基酸。
由于不同蛋白质的结构和肽键的结构不同,所以针对不同的蛋白质可能需要选择不同的酶来进行水解。
此外,需要对酶的作用条件进行优化,以提高水解效率。
酸碱法水解酸碱法水解是利用酸或碱来断裂肽键,将蛋白质水解成氨基酸。
一般而言,使用强碱(如NaOH)或强酸(如HCl)可以较快地将蛋白质水解。
然而,酸碱法水解需要控制酸碱条件,过高或过低的pH值可能导致氨基酸的损失或变性。
因此,在进行酸碱法水解时,需要仔细选择酸碱的种类和浓度,以及适宜的温度和反应时间。
氨基酸水解的应用氨基酸水解在食品工业、医药领域和生物技术等多个领域具有广泛的应用。
食品工业在食品工业中,氨基酸水解可以将蛋白质水解成氨基酸,并应用于增味剂和增香剂的生产中。
水解的氨基酸具有更强的风味和香气,可以提高食品的口感和香气。
同时,氨基酸水解也可以降低蛋白质的过敏性,使蛋白质更易于被人体吸收,提高食品的营养价值。
医药领域在医药领域,氨基酸水解可以应用于药物制剂的开发。
水解的氨基酸可以作为药物的原料或辅料,用于提高药物的溶解性、稳定性和生物利用度。
此外,氨基酸水解还可以用于生产生物制剂,如氨基酸复合营养剂、氨基酸口服液等。
生物技术在生物技术领域,氨基酸水解可以用于分离和纯化蛋白质。
通过水解蛋白质,可以得到单独的氨基酸,进而进行氨基酸序列分析、结构研究和功能研究。
此外,氨基酸水解也可以应用于蛋白质工程,通过改变氨基酸序列和结构,设计出具有特定功能的蛋白质。
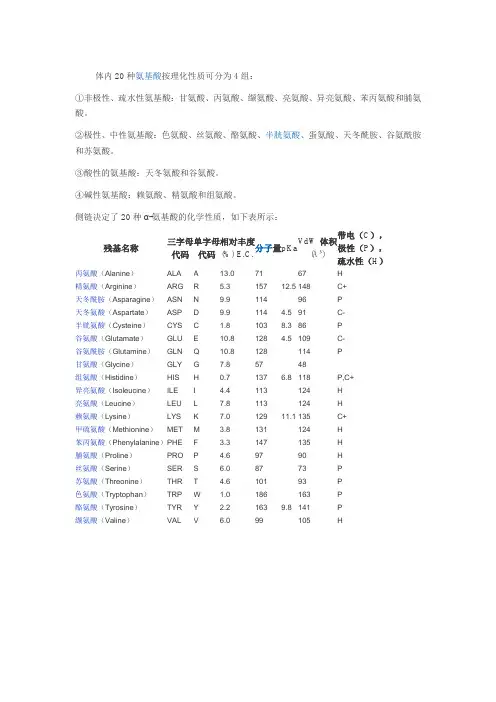
体内20种氨基酸按理化性质可分为4组:①非极性、疏水性氨基酸:甘氨酸、丙氨酸、缬氨酸、亮氨酸、异亮氨酸、苯丙氨酸和脯氨酸。
②极性、中性氨基酸:色氨酸、丝氨酸、酪氨酸、半胱氨酸、蛋氨酸、天冬酰胺、谷氨酰胺和苏氨酸。
③酸性的氨基酸:天冬氨酸和谷氨酸。
④碱性氨基酸:赖氨酸、精氨酸和组氨酸。
侧链决定了20种α-氨基酸的化学性质,如下表所示:残基名称三字母代码单字母代码相对丰度(%) E.C.分子量p KaVdW体积(ų)带电(C),极性(P),疏水性(H)丙氨酸(Alanine)ALA A 13.0 71 67 H精氨酸(Arginine)ARG R 5.3 157 12.5 148 C+ 天冬酰胺(Asparagine)ASN N 9.9 114 96 P天冬氨酸(Aspartate)ASP D 9.9 114 4.5 91 C-半胱氨酸(Cysteine)CYS C 1.8 103 8.3 86 P谷氨酸(Glutamate)GLU E 10.8 128 4.5 109 C-谷氨酰胺(Glutamine)GLN Q 10.8 128 114 P甘氨酸(Glycine)GLY G 7.8 57 48组氨酸(Histidine)HIS H 0.7 137 6.8 118 P,C+ 异亮氨酸(Isoleucine)ILE I 4.4 113 124 H亮氨酸(Leucine)LEU L 7.8 113 124 H赖氨酸(Lysine)LYS K 7.0 129 11.1 135 C+ 甲硫氨酸(Methionine)MET M 3.8 131 124 H苯丙氨酸(Phenylalanine)P HE F 3.3 147 135 H脯氨酸(Proline)PRO P 4.6 97 90 H丝氨酸(Serine)SER S 6.0 87 73 P苏氨酸(Threonine)THR T 4.6 101 93 P色氨酸(Tryptophan)TRP W 1.0 186 163 P酪氨酸(Tyrosine)TYR Y 2.2 163 9.8 141 P缬氨酸(Valine)VAL V 6.0 99 105 H。
人体20种氨基酸人体中有20种氨基酸,它们是构成蛋白质的基础。
每个氨基酸由一个氨基基团、一个羧基和一个侧链组成。
这些氨基酸在人体中发挥着不同的重要功能。
下面将逐个介绍这20种氨基酸及其功能。
1. 丙氨酸(Alanine): 丙氨酸是体内代谢过程中产生的一种氨基酸,它是肌肉组织中最丰富的氨基酸之一,能够提供能量并促进肌肉生长。
2. 缬氨酸(Valine): 缬氨酸是支链氨基酸之一,它在体内参与合成肌肉蛋白质,维持氮平衡,并提供能量。
3. 亮氨酸(Leucine): 亮氨酸是人体无法合成的必需氨基酸之一,它对于肌肉生长和修复非常重要,还参与蛋白质合成和能量代谢。
4. 异亮氨酸(Isoleucine): 异亮氨酸也是一种支链氨基酸,它在肌肉合成和修复中起到重要作用,还参与能量代谢和血糖调节。
5. 苏氨酸(Threonine): 苏氨酸是一种必需氨基酸,它是合成胶原蛋白和其他重要蛋白质的基础,还参与免疫系统的功能。
6. 赖氨酸(Lysine): 赖氨酸是人体无法合成的必需氨基酸之一,它对于细胞生长、骨骼发育和组织修复至关重要,还参与体内激素和抗体的合成。
7. 苯丙氨酸(Phenylalanine): 苯丙氨酸是一种重要的氨基酸,它参与合成多种蛋白质和神经递质,对大脑功能和情绪调节有影响。
8. 色氨酸(Tryptophan): 色氨酸是一种必需氨基酸,它是合成5-羟色胺的前体物质,对于调节情绪、睡眠和免疫功能至关重要。
9. 甲硫氨酸(Methionine): 甲硫氨酸是一种硫氨基酸,它参与合成蛋白质和维持正常的蛋白质结构,还具有抗氧化和解毒作用。
10. 组氨酸(Histidine): 组氨酸是一种重要的氨基酸,它是组胺的前体,对细胞生长和修复、酸碱平衡和神经传导有重要作用。
11. 苏氨酸(Serine): 苏氨酸是一种非必需氨基酸,它参与合成多种蛋白质和磷脂,对细胞分裂和免疫系统功能有影响。
12. 苏胺酸(Asparagine): 苏胺酸是一种氨基酸,它参与合成多种蛋白质和核酸,对神经系统和肝脏功能有影响。
二十种氨基酸二十种氨基酸是生命赖以存在和运行的基础元素。
在生物体中,它们组成蛋白质,是各种物质形成、保护、维护细胞结构和活动的重要物质。
因此,了解二十种氨基酸的结构和功能,对研究蛋白质的分子基础及其生物学功能具有重要意义。
二十种氨基酸可以分为以下五类:1)甲胺酸(Gly);2)丙氨酸(Ala);3)酪氨酸(Val);4)苯丙氨酸(Phe);5)缬氨酸(Leu)。
其中,甲胺酸是最丰富的氨基酸,其结构图如下:甲胺酸是最重要的氨基酸,因为它可以形成多种重要的氨基酸交联,并可以增强蛋白质的稳定性。
甲胺酸还可以与丙氨酸形成氨基酸脱水素,这是蛋白质质量控制的负责物质。
丙氨酸也是蛋白质和脂肪代谢的重要物质,它可以与钾离子和钙离子形成氨基酸盐,这些氨基酸盐可以用来调节细胞和生物体内的pH值。
酪氨酸是遗传材料的重要物质,它可以参与DNA的修复和维护。
它也是一种必需的氨基酸,它可以合成胆固醇,并参与脂肪和脂肪酸的代谢。
苯丙氨酸可以参与激素分泌,这是一种可以调节人体活动和代谢的重要因素。
缬氨酸则可以保护DNA免受环境污染的影响。
此外,还有许多其他的氨基酸,包括丝氨酸(Ser),苏氨酸(Thr),大肽酸(Tyr),赖氨酸(Lys),苯丙氨酸(Trp),甘氨酸(Glu),脯氨酸(Pro),天冬氨酸(Asn),精氨酸(Arg),组氨酸(His),异亮氨酸(Ile),氨基酰基硫类(Cys),氨基乙酰胆碱(Met),氨基乙酰谷氨酰胺(Gly),谷氨酸(Asp),硫硫胺(Thr)和精胺酸(Prd)。
它们都是蛋白质的重要组成部分,在蛋白质的功能中起着重要作用。
了解二十种氨基酸的结构、功能、性质,以及其在蛋白质的形成和发挥功能中的重要性,对于研究蛋白质的分子基础及其生物学功能具有重要意义。
关于氨基酸的研究可以帮助我们了解基因组结构、研究蛋白质结构和功能,以及发现新的药物,改善人类健康。
纽康特氨基酸
纽康特氨基酸是一种重要的生物化学物质,它对人体的健康有着很多
的好处。
氨基酸是构成蛋白质的基本单元,在人体内有很多重要的生
理功能。
纽康特氨基酸是一种高品质的氨基酸,具有许多独特的性质,适合人体吸收利用。
纽康特氨基酸是一种全天然纯净的氨基酸,其品质和吸收性非常高。
纽康特氨基酸主要来源于牛奶和乳清蛋白中,它是一种具有高营养价
值的营养物质,能够提高人体免疫力,促进人体健康。
纽康特氨基酸有很多好处,可以增强人体免疫系统的功能,提高身体
的抗病能力。
此外,纽康特氨基酸还能够提高肝脏功能,减少肝脏损伤。
它还可以促进胃肠道的健康,增强肠道的吸收能力。
纽康特氨基酸还能够增强身体的肌肉力量和耐力,使人体更具有活力。
此外,它还能够促进人体新陈代谢,增强身体的能量。
它还能够降低
胆固醇,预防心血管疾病的发生。
总之,纽康特氨基酸是一种非常重要的营养物质,能够对人体健康产
生很多积极的影响。
如果您想要增强身体的免疫力,增强体质,提高
肌肉力量,预防疾病的发生,那么纽康特氨基酸就是您的首选。
需要注意的是,尽管纽康特氨基酸具有很多好处,但是也不要过量摄入。
过量摄入会对身体造成一定的伤害。
因此,我们应该在医生的指导下适量地食用纽康特氨基酸,以便发挥它的作用,提高身体的健康水平。
人体需要的21氨基酸人体蛋白质的构成基础是氨基酸,氨基酸共有20种常见的类型,这些被称为标准氨基酸,是构成蛋白质的基本单元。
这20种标准氨基酸是:1. 丙氨酸(Alanine, Ala, A)2. 精氨酸(Arginine, Arg, R)3. 天冬氨酸(Aspartic acid, Asp, D)4. 天冬酰胺(Asparagine, Asn, N)5. 半胱氨酸(Cysteine, Cys, C)6. 谷氨酸(Glutamic acid, Glu, E)7. 谷氨酰胺(Glutamine, Gln, Q)8. 甘氨酸(Glycine, Gly, G)9. 组氨酸(Histidine, His, H)10. 异亮氨酸(Isoleucine, Ile, I)11. 亮氨酸(Leucine, Leu, L)12. 赖氨酸(Lysine, Lys, K)13. 甲硫氨酸(Methionine, Met, M)14. 苯丙氨酸(Phenylalanine, Phe, F)15. 脯氨酸(Proline, Pro, P)16. 丝氨酸(Serine, Ser, S)17. 胸腺氨酸(Threonine, Thr, T)18. 色氨酸(Tryptophan, Trp, W)19. 酪氨酸(Tyrosine, Tyr, Y)20. 缬氨酸(Valine, Val, V)除此之外,还有一些氨基酸不是由遗传密码直接编码的,但它们也存在于蛋白质中,例如:21. 硒代半胱氨酸(Selenocysteine,被认为是第21种“标准”氨基酸)22. 吡咯赖氨酸(Pyrrolysine,有时被认为是第22种“标准”氨基酸)硒代半胱氨酸在蛋白质合成中的插入是通过特定的RNA 结构和专门的延伸因子进行的,这使得它成为蛋白质生物合成的罕见组分。
吡咯赖氨酸在某些古细菌和少数细菌中发现。
人体可以自己合成一部分氨基酸,这些被称为非必需氨基酸。
氨基酸是一类同时含有氨基和羧基的有机小分子。
组成多肽和蛋白质的氨基酸除Gly外,都属于L型的α- 氨基酸(Pro为亚氨基酸)。
氨基酸不仅可以作为寡肽、多肽和蛋白质的组成单位或生物活性物质的前体,也可以作为神经递质或糖异生的前体,还能氧化分解产生ATP。
目前已发现蛋白质氨基酸有22种,其中20种最为常见,而硒半胱氨酸和吡咯赖氨酸比较罕见。
非蛋白质氨基酸通常以游离的形式存在,作为代谢的中间物和某些物质的前体,具有特殊的生理功能。
22种标准氨基酸可使用三字母或单字母缩写来表示。
某些标准氨基酸在细胞内会经历一些特殊的修饰成为非标准蛋白质氨基酸。
氨基酸有多种不同的分类方法:根据R基团的化学结构和在pH7时的带电状况,可分为脂肪族氨基酸、不带电荷的极性氨基酸、芳香族氨基酸、带正电荷的极性氨基酸和带负电荷的极性氨基酸;根据R基团对水分子的亲和性,可分为亲水氨基酸和疏水氨基酸;根据对动物的营养价值,可分为必需氨基酸和非必需氨基酸。
氨基酸的性质由其结构决定。
其共性有:缩合反应、手性(Gly除外)、两性解离、具有等电点,以及氨基酸氨基和羧基参与的化学反应,包括与亚硝酸的反应、与甲醛的反应、Sanger 反应、与异硫氰酸苯酯的反应和与茚三酮的反应等。
与亚硝酸的反应可用于Van Slyke定氮,与甲醛的反应可用于甲醛滴定,Sanger反应和与异硫氰酸苯酯的反应可用来测定N-端氨基酸。
只有脯氨酸和羟脯氨酸与茚三酮反应产生黄色物质,其余生成蓝紫色物质,利用此反应可对氨基酸进行定性或定量分析。
多数氨基酸的侧链可能发生特殊的反应,可以此鉴定氨基酸。
不同氨基酸在物理、化学性质上的差异可用来分离氨基酸,其中最常见的方法是电泳和层析。
肽是氨基酸之间以肽键相连的聚合物,它包括寡肽、多肽和蛋白质。
氨基酸是构成肽的基本单位。
线形肽链都含有N端和C端,书写一条肽链的序列总是从N端到C端。
肽键具有部分双键的性质,多为反式,也有顺式。
酰胺平面中Cα-N单键旋转的角度称为Φ,Cα-C单键旋转的角度称为ψ。
L-蛋氨酸价格比dl型的高很多,而两者生理活性相同。
L-组氨酸在水中溶解度远比盐酸盐低。
L-赖氨酸稳定性很差,一般用其盐类。
1、L-丙氨酸:白色结晶性粉末,有特殊甜味,甜度约为蔗糖的70%。
化学性能
稳定,易溶于水,微溶于乙醇。
5%水溶液PH=5.5-7.0。
2、L-精氨酸:白色结晶性粉末,经水重结晶后,于105℃失去结晶水,水溶液
呈强碱性,可从空气中吸收二氧化碳。
溶于水,微溶于乙醇。
成人为非必须氨基酸,但体内生成速度慢,婴幼儿为必须氨基酸,有一定解毒作用。
3、L-精氨酸盐酸盐:白色或近白色几乎无臭结晶性粉末。
干燥状态下稳定。
3%
水溶液pH=5.7。
易溶于水,微溶于热乙醇。
4 、L-天冬氨酸:白色结晶性粉末,无臭。
稍有酸味,难溶于水,易溶于热水,
不溶于乙醇,属非必须氨基酸。
5、L-天冬酰胺:白色结晶性粉末,稍有甜味。
遇碱水解成天冬氨酸。
溶于水,
几乎不溶于乙醇,水溶液呈酸性。
为非必须氨基酸。
6、L-胱氨酸:白色针状,几乎无臭,在热碱水溶液中易分解,极难溶于水和乙
醇。
为非必须氨基酸,对构成皮肤和毛发是必须物质,可促进手术及外伤的治疗,刺激造血功能,促进白血球生成。
7、L-谷氨酰胺:白色结晶性粉末,稍有甜味,结晶状态稳定,遇酸碱热水不稳
定,可水解成L-谷氨酸。
溶于水呈酸性,几乎不溶于乙醇,属非必须氨基酸。
8、甘氨酸(氨基乙酸) :结晶性粉末,有特殊甜味,水溶液呈微酸性。
易溶
于水,极难溶于乙醇。
9、L-组氨酸:稍有苦味,易与金属离子形成络盐。
溶于水,极难溶于乙醇。
因
溶解度极小,常用其盐酸盐。
10、L-组氨酸盐酸盐:稍有酸、苦味,性质稳定。
易溶于水,在水中溶解度远比
L-组氨酸大,不溶于乙醇。
属于必需氨基酸,在体内合成较慢,D-型与L-型生理效果相同。
11、DL-异亮氨酸:稍有苦味,10%溶液的pH=5.5-7.0,溶于水,几乎不溶于乙
醇。
12 、L-异亮氨酸:略苦,无臭,10%溶液的pH=5.5-7.0,溶于水,化学性能稳
定,加工受热时几乎无损失,微溶于热乙醇。
为必需氨基酸,仅L-型有生理功效。
过量食用将与亮氨酸产生拮抗作用,有碍发育。
13、DL-亮氨酸:细白色晶体,无臭,略甜。
10%溶液pH=5.5-7.0.
14、L-亮氨酸:白色结晶性粉末,略苦。
略溶于水,微溶于乙醇,属于必需氨基
酸,为婴儿正常生长及成人维持氮平衡所必需。
15、L-赖氨酸盐酸盐:白色或近白色自由流动的结晶性粉末,几乎无臭,通常较
稳定,高湿下易结块,稍着色。
φ≤60%时稳定,≥60%时生成二水合物。
与维生素C和维生素k3共存则着色。
易溶于水。
为必需氨基酸,缺乏导致生长障碍,D-型无生理效果。
16、DL-蛋氨酸:白色薄片状结晶或结晶性粉末,有特殊气味,味微甜。
10%水
溶液pH=5.6-6.1。
对热及空气稳定,溶于水、稀酸碱,极难溶于乙醇。
为必需氨基酸。
17、L-蛋氨酸:无色或白色有光泽片状结晶或白色结晶性粉末。
微苦,溶于水,
难溶于乙醇。
L-型与D-型生理效果相同,L-型价更贵。
多采用DL-型。
18、DL-苯丙氨酸:白色小片状结晶或结晶性粉末。
无臭,溶于水、稀无机酸,
极难溶于乙醇。
生理效能与L-型相同。
19、L-苯丙氨酸:无色至白色片状晶体或白色结晶性粉末。
略苦,10%水溶液
pH=5.4-6.0。
在热、光照、空气中稳定。
与葡萄糖一起加热着色,碱性下不稳定。
溶于水,难溶于乙醇、稀无机酸、碱性溶液。
为必需氨基酸,生理作用与酪氨酸有关。
可影响甲状腺激素和毛发、皮肤的黑色素。
D-型与L-型生理效果相同。
20、L-脯氨酸:晶体或结晶性粉末,无臭,有较强甜味。
不纯物有吸湿性,其为
亚氨基酸,与其他氨基酸性质不同,极易溶于水,溶于乙醇。
21、DL-丝氨酸:晶体或结晶性粉末,相对密度为1.537,溶于水,不溶于乙醇。
22、L-丝氨酸:白色结晶性粉末,无臭,微甜,溶于水,不溶于乙醇。
为非必须
氨基酸。
23、DL-苏氨酸:晶体或结晶性粉末,无臭,味甜。
化学性能较稳定,溶于水,
甜味爽口,难溶于乙醇等。
DL-型生理作用为L-型的一半,缺乏时易引起食欲不振等。
24、L-苏氨酸:无臭,微甜。
高温遇稀碱分解,遇酸缓慢分解。
易溶于水,不溶
于乙醇。
为必需氨基酸。
生理效果为DL-型的2倍。
25、DL-色氨酸:白色至黄白色结晶或结晶性粉末。
无臭或略臭,略甜,L-型味
苦,D-型甜度与蔗糖相当。
0.2%水溶液pH=5.5-7.0。
耐酸,耐光性差。
溶于水,微溶于乙醇。
26、L-色氨酸:无臭或微臭,稍苦。
长时间光照着色,与水共热产生少量吲哚,
如在氢氧化钠。
硫酸铜存在下加热产生多量吲哚。
色氨酸与酸在暗处加热较稳定,与其他氨基酸、糖醛类共存时极易分解。
略溶于水,溶于热水、热乙醇。
属必需氨基酸。
27、L-酪氨酸:无色或白色丝光状针状结晶或结晶性粉末。
纯品稳定,化学性质
较活泼。
微溶于水,不溶于无水乙醇。
为非必需氨基酸。
28、L-缬氨酸:白色单斜晶系晶体或结晶性粉末,无臭略苦,5%水溶液
pH=5.5-7.0.。
对热、光、空气稳定。
易溶于水,几乎不溶于乙醇,与亮氨酸分离困难。
属必需氨基酸。
L-型生理效果为D-型的2倍。
缺乏可引起神经障碍、停止发育、体重下降、贫血等。
29、L-半胱氨酸:半胱氨酸盐酸盐无水物(C3H7NO2S·HCl)为白色结晶或结晶性
粉末,易溶于水,具有臭味。
因半胱氨酸对酸稳定,故一般都以盐酸盐形式存在,半胱氨酸盐酸盐一水物(C3H7NO2S·HCl·H2O)为白色或无色结晶,具异臭,味酸,水溶液呈酸性反应。
易溶于水,在乙醇中极微溶解。
它对酸稳定,而在中性及碱性溶液中易被空气氧化为半胱氨酸,微量铁及重金属可促进其氧化。
29、牛磺酸:白色结晶或结晶性粉末,无臭,微酸,水溶液pH=4.1-5.6。
溶于水,
不溶于乙醇,。
有利于对婴幼儿大脑发育、神经传导、视觉机能的完善、钙的吸收及脂类物质的消化吸收。
属非必需氨基酸。