3-立体化学基础(09药学)
- 格式:ppt
- 大小:2.29 MB
- 文档页数:82







第十七章 立体化学基础【竞赛要求】有机立体化学基本概念。
构型与构象。
顺反异构(trans -、cis -和Z -、E -构型)。
手性异构。
endo -和exo -。
D,L 构型。
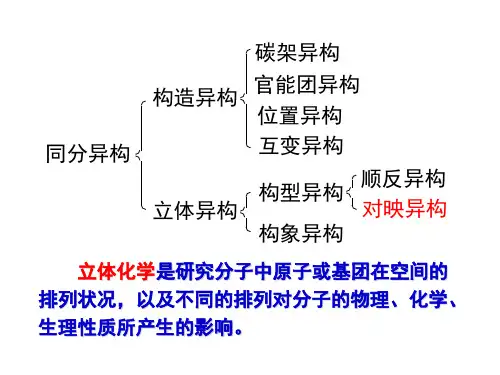
【知识梳理】从三维空间结构研究分子的立体结构,及其立体结构对其物理性质和化学性质的影响的科学叫立体化学。
一、异构体的分类按结构不同,同分异构现象分为两大类。
一类是由于分子中原子或原子团的连接次序不同而产生的异构,称为构造异构。
构造异构包括碳链异构、官能团异构、位置异构及互变异构等。
另一类是由于分子中原子或原子团在空间的排列位置不同而引起的异构,称为立体异构。
立体异构包括顺反异构、对映异构和构象异构。
二、立体异构 (一)顺反异构分子中存在双键或环等限制旋转的因素,使分子中某些原子或基团在空间位置不同,产生顺反异构现象。
双键可以是C=C 、C=N 、N=N 。
双键产生顺反异构体的条件是双键两端每个原子所连二基团或原子不同。
如:顺反异构的构型以前用顺– 和反– 表示。
如:a b ca bcab c a dcab c c dcH H C = CH 3 CH 3 C 顺 – 2 – 丁烯 H CH 3C =CH 3H C 反 – 2 – 丁烯但顺反异构体的两个双键碳原子上没有两个相同的取代基用这种命名法就无能为力。
如:系统命名法规定将双键碳链上连接的取代基按次序规则的顺序比较,高序位基在双键同侧的称Z 型,反之称E 型。
如上化合物按此规定应为E 型。
命名为E – 4 – 甲基 – 3 – 已基 – 2 – 戊烯。
所谓“次序规则”,就是把各种取代基按先后次序排列的规则。
(1)原子序数大的优先,如I >Br >Cl >S >P >F >O >N >C >H ,未共用电子对为最小;(2)同位素质量数大的优先,如D >H ;(3)二个基团中第一个原子相同时,依次比较第二、第三个原子; (4)重键,如:分别可看作:(5)当取代基的结构完全相同,只是构型不同时,则R >S ,Z >E 。


化学中的立体化学化学是自然科学的一个重要分支,它研究了物质的组成、结构、性质和变化规律。
其中,化学中的立体化学是一个关键性的领域。
在化学反应中,往往需要考虑分子的立体结构,才能解释各种现象,如光学活性、对映体、手性等。
本文将深入探讨化学中的立体化学。
一、立体化学的起源与发展立体化学起源于十九世纪末,当时的化学家们意识到一些分子无法用一般无规则的化学键来描述。
这些分子似乎在三维空间中有着特定的构象。
最早提出立体化学学说的化学家是法国科学家范锡尔 Jean-Baptiste van't Hoff 和德国化学家 Jacobus Henricus van't Hoff,他们的工作为后来的有机化学和生物化学研究打下了基础。
随着实验技术和分析方法的发展,人们越来越深入地研究和理解立体化学。
二、分子的立体结构分子的立体结构是指其在三维空间中的空间排列方式。
在一个分子中,原子可以沿不同的轴线方向排列,在这个过程中,原子之间存在着不同的空间关系。
这些关系可以通过分子的构象图来表示。
在立体化学中,分子的立体结构往往是由手性中心决定的。
手性中心是指一个分子中四个不同的官能团围绕着一个碳原子依次排列的情况。
分子的手性中心可以对应两种空间构象,分别称为左旋体和右旋体,也称之为对映体,它们在物理性质上完全一致,但在化学性质、生物活性、药效方面却可以有很大的差异。
三、光学活性和对映体光学活性是指物质能使入射光的平面偏振光发生旋转的现象,只有具有手性的分子才能表现出光学活性。
一个物质如果同时存在左旋体和右旋体,那么它称为光学异构体,或对映体。
两个对映体在物理性质方面都完全一样,但在化学性质和生物活性上可以有很大的不同。
对映体具有重要的生物学意义。
例如,在药学领域,药物的对映体可能会产生完全不同的生物活性,有时候甚至有毒性反应。
所以在药物研究和开发过程中,必须对药物的对映体进行区分和鉴定。
四、手性合成和手性分离技术手性合成是指在化学合成中通过控制反应条件,使产物的结构保持手性的过程。

第16讲《立体化学基础》高中化学奥林匹克竞赛辅导讲座第16讲立体化学基础【竞赛要求】有机立体化学基本概念。
构型与构象。
顺反异构(trans-、cis-和Z-、E-构型)。
手性异构。
endo-和exo-。
D,L构型。
【知识梳理】从三维空间结构研究分子的立体结构,及其立体结构对其物理性质和化学性质的影响的科学叫立体化学。
一、异构体的分类按结构不同,同分异构现象分为两大类。
一类是由于分子中原子或原子团的连接次序不同而产生的异构,称为构造异构。
构造异构包括碳链异构、官能团异构、位置异构及互变异构等。
另一类是由于分子中原子或原子团在空间的排列位置不同而引起的异构,称为立体异构。
立体异构包括顺反异构、对映异构和构象异构。
二、立体异构(一)顺反异构分子中存在双键或环等限制旋转的因素,使分子中某些原子或基团在空间位置不同,产生顺反异构现象。
双键可以是C=C、C=N、N=N。
双键产生顺反异构体的条件是双键两端每个原子所连二基团或原子不同。
a b如:顺反异构的构型以前用顺�C 和反�C 表示。
如:H H CH3 H C = C C = CCH3 H CH3 CH3顺�C 2 �C 丁烯反�C 2 �C 丁烯a b c ca b c cc c a ba dc d但顺反异构体的两个双键碳原子上没有两个相同的取代基用这种命名法就无能为力。
如: H3C CH2CH3C = CH CH(CH3)2系统命名法规定将双键碳链上连接的取代基按次序规则的顺序比较,高序位基在双键同侧的称Z型,反之称E型。
如上化合物按此规定应为E型。
命名为E �C 4 �C 甲基�C 3 �C 已基�C 2 �C 戊烯。
所谓“次序规则”,就是把各种取代基按先后次序排列的规则。
(1)原子序数大的优先,如I>Br>Cl>S>P>F>O>N>C>H,未共用电子对为最小;(2)同位素质量数大的优先,如D>H;(3)二个基团中第一个原子相同时,依次比较第二、第三个原子;(4)重键,如:分别可看作:(5)当取代基的结构完全相同,只是构型不同时,则R>S,Z>E。