酪氨酸酶抑制剂筛选
- 格式:pptx
- 大小:807.61 KB
- 文档页数:35


酪氨酸酶概念:酪氨酸酶(EC 1.14.18.1)是一种含铜的氧化还原酶,它与生物体合成色素直接相关.(长的黑有很大的一部分原因在自己)在人体中,它与色素障碍性疾病及恶性黑色素肿瘤的发生与治疗有关(酪氨酸酶的分布与动物的生理功能息息相关,不同动物的酪氨酸酶在体内分布的部位不同.多数昆虫在正常生理状态下,酪氨酸酶以酶原的形式存在,不同类型的酪氨酸酶存在于昆虫的特定部位,以完成特定的生理功能.美洲蜚蠊存在于血红细胞内,而麻蝇则仅存在于血浆中,并且在表皮中主要以活化形式的酪氨酸酶存在.昆虫酪氨酸酶除参与黑色素的形成外还是唯一参与角质硬化的酶.昆虫高度硬化的角质能阻断微生物和异物的入侵,并为柔软的元脊椎动物身体提供了保护.在节肢动物中,酪氨酸酶还参与其他两种重要的生理过程——防御反应和伤口愈合.哺乳动物酪氨酸酶催化产生的黑色素被分泌进入到表皮和毛发的角质细胞中,使体表着色,从而起保护皮肤和眼睛、抵御紫外线的辐射和防止内部组织过热等作用.哺乳动物酪氨酸酶常见于黑素细胞中,黑素细胞是存在于皮肤,发囊和眼睛中并产生色素的高度特异性的细胞[1“].酪氨酸酶功能减退或缺失时,即会影响黑色素代谢,从而发生疾病如白癫疯和白化病.动物与人的常染色体隐性疾病也与酪氨酸酶的缺失或活性下降有关.)作用机制:酪氨酸酶主要参与两个反应过程:催化L.酪氨酸羟基化转变为L-多巴和氧化L-多巴形成多巴醌,多巴醌经一系列反应后,形成黑色素,与人体雀斑、褐斑等黑色素过度沉积等疾病的发生有关,并与昆虫的蜕皮(蝉蜕可以入药)和(苹果)果蔬的褐化有很大关系(黑色素生物合成过程可大体分为两个阶段,第一阶段是由酪氨酸酶催化酪氨酸被羟化反应形成L_3,4一二羟基丙氨酸(L_多巴)(单酚酶活性),并进步将L_多巴氧化生成多巴醌(二酚酶活性)。
这两步反应都是由酪氨酸酶催化的,酪氨酸酶在这里显示了独特的双重催化功能.第二阶段从多巴醌(DOPAqui—non)为原料从两个不同途径分别生成真黑素和褪黑素的过程.真黑素生成,多巴醌经多聚化反应等一系列反应生成无色多巴色素,极不稳定的无色多巴色素被另一分子多巴醌氧化为多巴色素,多巴色素经异构、脱羧生成5,6一二羟基吲哚(DHI),5,6一二羟基吲哚(DHI)由酪氨酸酶催化氧化为真黑色素的前体吲哚一5,6一醌(IndQu);褪黑素生成,多巴醌(DOPAquinon)与半胱氨酸(Cys)反应生成产生5-Cys一多巴及5-Cys一多巴醌,然后成环、脱羧变成苯肼噻嗪的衍生物,最后形成褪黑素.在第二阶段,只有少数几步反应由酪氨酸酶、异构酶或金属离子催化,大部分反应都是自发的,因此酪氨酸酶是整个黑色素生成反应的限速酶,第一阶段的两步反应是限速步骤.)活性中心:酪氨酸酶的活性中心是由两个含铜离子位点构成.在催化过程中,双核铜离子位点以3种形态存在,分别是氧化态、还原态和脱氧态.研究表明与酪氨酸酶结合的双核铜离子活性中心与在血蓝蛋白中发现的活性中心非常相似、白化病概念:白化病是由黑色素合成相关基因突变导致黑色素沉着减少或缺失引起的一类遗传性疾病的总称。
化学抗肿瘤药物经过半个多世纪的发展,已经进入靶向治疗药物时代。
小分子靶向药物在临床上的应用日益增多,在一些肿瘤类别中已经进入一线用药地位,比如肾癌、慢粒白、多发性骨髓瘤等。
本文对小分子靶向治疗药物做一综述。
小分子靶向治疗药物简介一、受体酪氨酸激酶抑制剂作为抗肿瘤药物靶点的酪氨酸激酶有两类,一类是受体酪氨酸激酶(RTKs),另一类是非受体酪氨酸激酶(nrRTKs)。
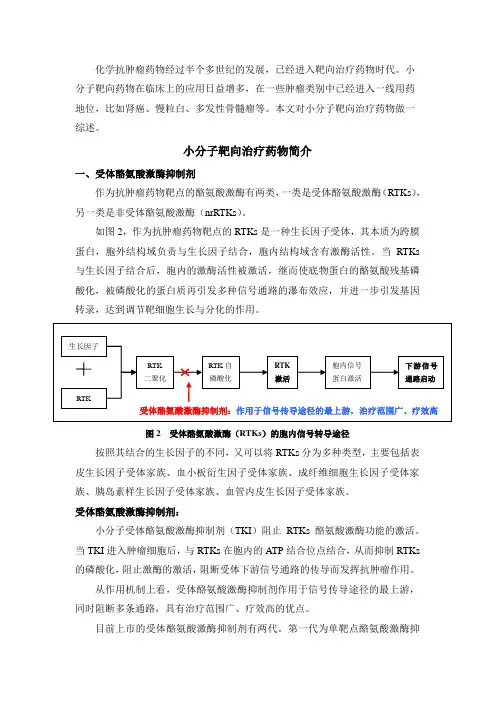
如图2,作为抗肿瘤药物靶点的RTKs是一种生长因子受体,其本质为跨膜蛋白,胞外结构域负责与生长因子结合,胞内结构域含有激酶活性。
当RTKs 与生长因子结合后,胞内的激酶活性被激活,继而使底物蛋白的酪氨酸残基磷酸化,被磷酸化的蛋白质再引发多种信号通路的瀑布效应,并进一步引发基因转录,达到调节靶细胞生长与分化的作用。
图2 受体酪氨酸激酶(RTKs)的胞内信号转导途径按照其结合的生长因子的不同,又可以将RTKs分为多种类型,主要包括表皮生长因子受体家族、血小板衍生因子受体家族、成纤维细胞生长因子受体家族、胰岛素样生长因子受体家族、血管内皮生长因子受体家族。
受体酪氨酸激酶抑制剂:小分子受体酪氨酸激酶抑制剂(TKI)阻止RTKs酪氨酸激酶功能的激活。
当TKI进入肿瘤细胞后,与RTKs在胞内的ATP结合位点结合,从而抑制RTKs 的磷酸化,阻止激酶的激活,阻断受体下游信号通路的传导而发挥抗肿瘤作用。
从作用机制上看,受体酪氨酸激酶抑制剂作用于信号传导途径的最上游,同时阻断多条通路,具有治疗范围广、疗效高的优点。
目前上市的受体酪氨酸激酶抑制剂有两代。
第一代为单靶点酪氨酸激酶抑制剂,如吉非替尼、厄洛替尼。
表已上市的酪氨酸激酶抑制剂注:EGFR:表皮生长因子受体,属HER家族;VEGFR:血管内皮生长因子;PDGFR:血小板衍生因子;HER2:HER家族的一种受体;Abl-Bcr:一种非受体酪氨酸激酶;Raf:酪氨酸激酶的下游信号通路中的一种蛋白;Flt-3:Src:一种非受体酪氨酸激酶;c-kit:Ret:胶质细胞源性神经营养因子的受体吉非替尼为EGFR酪氨酸激酶抑制剂,主要用于非小细胞肺癌,对酪氨酸激酶基因编码区突变型肿瘤的有效率高达80%以上。

小分子抑制剂化学生物学【实用版】目录一、什么是小分子抑制剂二、小分子抑制剂的分类三、小分子抑制剂的应用四、总结正文一、什么是小分子抑制剂小分子抑制剂是一种具有抑制生物体内某些特定分子活性的化合物,通常用于治疗疾病。
它们能够与目标分子结合,从而阻止其发挥作用,进而达到治疗目的。
在生物医学领域,小分子抑制剂的研究和应用正逐渐成为药物研发的热点之一。
二、小分子抑制剂的分类根据作用机制和靶点不同,小分子抑制剂可分为以下几类:1.受体酪氨酸激酶抑制剂:这类抑制剂主要针对受体酪氨酸激酶(RTK),如表皮生长因子受体(EGFR)等。
RTK 在细胞生长、分化和侵袭过程中发挥重要作用,因此这类抑制剂常用于治疗癌症等疾病。
2.非受体酪氨酸激酶抑制剂:这类抑制剂作用于非受体酪氨酸激酶,如 Src 家族激酶、JAK 家族激酶等。
它们在细胞内参与多种信号传导过程,与多种疾病的发生发展密切相关。
3.丝氨酸/色氨酸激酶抑制剂:这类抑制剂主要针对丝氨酸/色氨酸激酶,如蛋白激酶C(PKC)等。
丝氨酸/色氨酸激酶在细胞内调控多种生物学过程,与肿瘤、炎症等疾病有关。
三、小分子抑制剂的应用小分子抑制剂在医学领域具有广泛的应用前景,部分已成功上市并应用于临床治疗。
例如:1.伊马替尼(Imatinib):是一种针对 BCR-ABL 融合基因的酪氨酸激酶抑制剂,用于治疗慢性髓系白血病(CML)等疾病。
2.贝伐珠单抗(Bevacizumab):是一种针对血管内皮生长因子(VEGF)的受体酪氨酸激酶抑制剂,用于治疗多种肿瘤,如结直肠癌、肺癌等。
3.托珠单抗(Tocilizumab):是一种针对白介素 -6(IL-6)受体的单克隆抗体,用于治疗风湿性关节炎等疾病。
总之,小分子抑制剂作为一种新型药物,在生物医学领域具有广泛的研究价值和应用前景。
第1页共1页。

Src蛋白酪氨酸激酶抑制剂在骨质疏松症中的研究进展
刘宝成;屈孝东;常彦海;杨波
【期刊名称】《临床医学进展》
【年(卷),期】2022(12)5
【摘要】骨质破坏发生在衰老和许多疾病中,其中最常见的是骨质疏松。
骨质疏松症(Osteoporosis, OP)是中国中老年患者最常见且发病率高的全身代谢性骨病,其发生是多种因素造成人体骨密度及骨质量下降,骨骼微小结构破坏,骨骼易脆性增高,导致老年人更容易在日常活动中发生骨折。
Src蛋白酪氨酸激酶抑制剂能够抑制Src蛋白酪氨酸激酶活性,对于骨质疏松的靶向治疗具有精准、稳定性强、副作用小,可直接进入病灶、无明显毒副作用等特点。
本文就Src蛋白酪氨酸激酶抑制剂在骨质疏松症中的研究进展做一综述。
【总页数】7页(P3827-3833)
【作者】刘宝成;屈孝东;常彦海;杨波
【作者单位】西安医学院西安;陕西省人民医院西安
【正文语种】中文
【中图分类】R73
【相关文献】
1.Src酪氨酸激酶抑制剂对人胃癌细胞SGC7901上皮-间质转变相关基因的作用及机制
2.Src酪氨酸激酶抑制剂逆转人胃癌顺铂耐药细胞SGC7901/DDP的作用及机制
3.Src 酪氨酸激酶抑制剂Ⅱ对膀胱移行细胞癌T24细胞生长、增殖的影响
4.
体外Src蛋白酪氨酸激酶抑制剂筛选模型的建立5.神经胶质瘤中受体酪氨酸激酶信号传导系统及酪氨酸激酶抑制剂的研究进展
因版权原因,仅展示原文概要,查看原文内容请购买。

色氨酸抑制酪氨酸酶的原理
酪氨酸酶是一种重要的酶,它能够催化酪氨酸的氧化反应,将其转化为多巴胺和其他生物活性物质。
这些物质在人体中起着重要的生理作用,如调节情绪、控制运动等。
然而,当酪氨酸酶活性过高时,会导致多巴胺等物质的过度分泌,从而引发一系列疾病,如帕金森病、精神分裂症等。
因此,抑制酪氨酸酶活性成为了一种重要的治疗策略。
以色氨酸是一种必需氨基酸,它在人体内可以被转化为5-羟色胺,这是一种重要的神经递质,能够调节情绪、睡眠等。
此外,色氨酸还可以被转化为色氨酸酶抑制剂,从而抑制酪氨酸酶的活性。
色氨酸酶抑制剂是一种天然的药物,已被广泛应用于治疗多种疾病,如帕金森病、抑郁症等。
色氨酸酶抑制剂的作用机制是通过竞争性抑制酪氨酸酶的活性。
当色氨酸酶抑制剂与酪氨酸酶结合时,它们会竞争性地占据酪氨酸酶的活性中心,从而阻止酪氨酸的氧化反应。
这样一来,多巴胺等物质的分泌就会减少,从而达到抑制酪氨酸酶活性的目的。
除了色氨酸酶抑制剂外,还有其他一些化合物也可以抑制酪氨酸酶的活性,如苯丙氨酸、酪氨酸等。
这些化合物的作用机制与色氨酸酶抑制剂类似,都是通过竞争性抑制酪氨酸酶的活性。
以色氨酸抑制酪氨酸酶的原理是通过竞争性抑制酪氨酸酶的活性,
从而减少多巴胺等物质的分泌,达到治疗相关疾病的目的。
这种治疗策略已被广泛应用于临床实践中,为相关疾病的治疗提供了一种有效的手段。

蛋白质磷酸化对于许多生物现象的引发是很必要的,包括细胞生长、增殖、泛素(ubiquitin)介导的蛋白降解等过程。
特别是酪氨酸磷酸化,作为细胞信号转导和酶活性调控的一种主要方式,通常通过引发蛋白质之间的相互作用,进而介导生长因子、荷尔蒙和细胞因子等对细胞膜上受体的信号调控。
然而,酪氨酸磷酸化在细胞的所有磷酸化修饰中所占的比例却非常低。
大概10%的细胞蛋白会受到磷酸化共价修饰,但每100次蛋白的磷酸化修饰中仅有1次酪氨酸基团的修饰。
与大部分细胞中的丝氨酸和苏氨酸磷酸化水平相比,酪氨酸磷酸化的水平估计要低2000倍。
正是由于细胞中酪氨酸磷酸化的水平相当低,才能保证细胞在内外信号的刺激下,作出灵敏的反应,所以研究酪氨酸的磷酸化对于细胞信号的调控和许多重要生物现象的研究具有极为重要的意义,而对发生酪氨酸磷酸化的蛋白质的识别及磷酸化位点的鉴定对揭示细胞过程的调控和药物的作用位点起到非常重要的作用。
研究蛋白质磷酸化的相关方法:磷酸化Western Blot对于信号转导科研来说,抗酪氨酸磷酸化抗体的出现是一个意义重大的事件。
在没有抗酪氨酸磷酸化抗体之前,蛋白质和酶的酪氨酸磷酸化只能通过非常危险的并且很费时的放射性实验来检测。
而利用抗酪氨酸磷酸化抗体,则可以通过Western Blot或其它免疫学方法轻松地检测到磷酸化信号。
常规的检测方法包括:用抗酪氨酸磷酸化抗体在Western Blot上检测内源或外源表达的磷酸化蛋白。
如果目标蛋白的含量较低,也可利用免疫沉淀的方法先富集发生磷酸化的酪氨酸蛋白,再检测目标蛋白的水平。
抗酪氨酸磷酸化抗体也常用于检测在不同处理的条件下,细胞内总的酪氨酸磷酸化水平的变化情况,作为许多细胞生物现象的一个重要指标。
我们都知道如果需要检测某一个目标蛋白的某一特定位点的磷酸化状态,可以选用该蛋白特定位点的磷酸化特异性抗体。
但由于我们研究的通常是新的磷酸化位点,或者这些蛋白特定位点的磷酸化抗体效果不够好,我们不得不自己制备磷酸化抗体。

希美替尼结构式-概述说明以及解释1.引言1.1 概述希美替尼(Imatinib)是一种广泛应用于白血病和其他恶性肿瘤治疗的靶向治疗药物。
它是第一代酪氨酸激酶抑制剂,通过抑制异常的酪氨酸激酶活性,阻止了癌细胞的生长和扩散。
希美替尼已被证明在治疗慢性髓性白血病(CML)、急性淋巴性白血病(ALL)和一些消化道肿瘤等疾病中具有显著的疗效。
随着对希美替尼的深入研究,人们对其治疗机制和潜在的临床应用也有了更深入的了解。
本文将着重介绍希美替尼的化学结构、药理作用以及临床应用,以期为读者提供更全面的了解和认识。
1.2 文章结构文章结构部分主要是说明整篇文章的结构安排,帮助读者更好地理解文章的内容组织。
本文的结构分为引言、正文和结论三个部分。
引言部分主要包括概述、文章结构和目的三个方面。
在概述部分,会简要介绍希美替尼这种药物的背景和重要性。
文章结构部分即是本段,将会介绍整篇文章的结构安排。
目的部分则明确了本文撰写的目的和意义。
正文部分包括了希美替尼的化学结构、药理作用以及临床应用三个方面,分别介绍了这种药物的化学成分、作用机制以及临床使用的情况。
结论部分则对全文的内容进行总结,强调希美替尼的重要性和未来发展的展望。
同时,通过结论部分可以让读者更清晰地理解全文的核心意义和价值。
最后,结尾的结束语也是文章的收尾部分,可以对全文进行一个简短的总结或思考。
整个文章结构分明,逻辑清晰,能够很好地引导读者了解希美替尼这一药物的相关知识和重要性。
1.3 目的:本文的主要目的是详细介绍希美替尼这一药物的化学结构、药理作用以及临床应用,以便读者能够更全面地了解这一重要药物。
通过对希美替尼的研究和分析,可以帮助读者更好地认识并理解希美替尼在临床上的作用机制和应用领域,为医学研究和医疗实践提供参考和指导。
希美替尼作为一种重要的药物,对于肿瘤治疗以及其他相关疾病的治疗具有重要的意义,因此深入了解和研究希美替尼,可以为临床医生和研究人员提供更多选择和参考,有助于促进医疗领域的发展和进步。

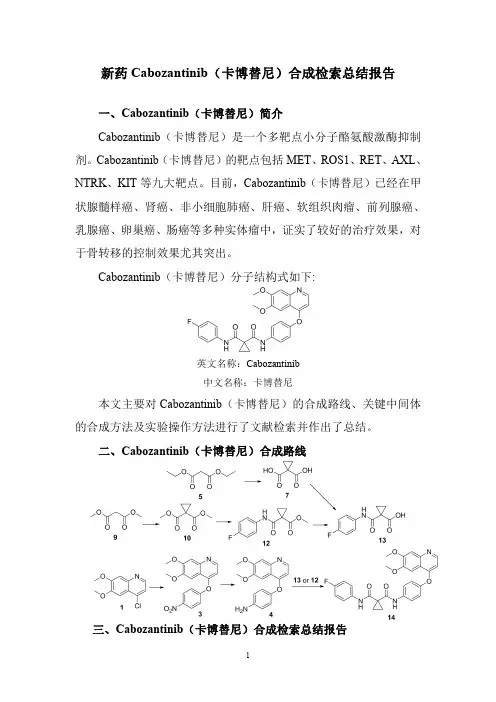
新药Cabozantinib(卡博替尼)合成检索总结报告一、Cabozantinib(卡博替尼)简介Cabozantinib(卡博替尼)是一个多靶点小分子酪氨酸激酶抑制剂。
Cabozantinib(卡博替尼)的靶点包括MET、ROS1、RET、AXL、NTRK、KIT等九大靶点。
目前,Cabozantinib(卡博替尼)已经在甲状腺髓样癌、肾癌、非小细胞肺癌、肝癌、软组织肉瘤、前列腺癌、乳腺癌、卵巢癌、肠癌等多种实体瘤中,证实了较好的治疗效果,对于骨转移的控制效果尤其突出。
Cabozantinib(卡博替尼)分子结构式如下:英文名称:Cabozantinib中文名称:卡博替尼本文主要对Cabozantinib(卡博替尼)的合成路线、关键中间体的合成方法及实验操作方法进行了文献检索并作出了总结。
二、Cabozantinib(卡博替尼)合成路线三、Cabozantinib(卡博替尼)合成检索总结报告(一)Cabozantinib (卡博替尼)中间体3的合成合成方法实验步骤参考文献操作方法一The intermediate 1(45.0g,0.2mol)was dissolved in chlorobenzene (450mL,10v/w),4-nitrophenol 2(70.1g,0.50mol)and N,N-diisopropylethylamine (51.7g,0.4mol)were sequentially added.After stirring at 140o C for 14h,the reaction mixture was cooled to r.t.,The precipitates were collected by filtration and washed with appropriatepetroleum ether to afford compound 3as a yellow solid in 88.2%yield.Bioorganic and Medicinal ChemistryLetters ;vol.29;nb.19;(2019);Art.No:126630.操作方法二To chloroquinoline 1(0.24g,1.1mmol)in diphenyl ether (20mL)was added 4-nitrophenol 2(0.30g,2.2mmol)and the resulting mixture was heated to 170°C.for 24h.The mixture was partitioned between ethyl acetate and 1M NaOH(aq).The organic phase was collected,washed with water and brine,dried (MgSO 4),filtered and concentrated.The residue was purified by flash column chromatography (90%ethyl acetate/hexanes-ethyl acetate)to afford 3(0.25g,69%)as a colorless solid.US2008/4273(2008);(A1)English操作方法三4-Nitrophenol 2(12.5g,89.6mmol)was added into a suspension of 4-chloro-6,7-dimethoxyquinoline 1(10.0g,44.8mmol)in PhCl (80mL).The resulting mixture was stirred at reflux for 16h.The solvent was evaporated under reduced pressure,and the residue was dissolved in CH 2Cl 2(150mL)The solution was washed by 10%NaOH aqueous solution (3×30mL),water (30mL)and dried (MgSO 4),and evaporated to obtain the title compound 3as a yellow solid (9.6g,65.7%)without further purification.Bioorganic and MedicinalChemistry ;vol.27;nb.17;(2019);p.3825–3835.操作方法四4-chloro-6,7-dimethoxyquinoline 1(671mg,3.0mmol)and 4-nitrophenol 2(500mg,3.6mmol)were placed in 7mL of chlorobenzene.Heat slowly to 140°C and continue to react at this temperature for 20h.Then the heating was stopped,cooled to room temperature,the solvent was evaporated under reduced pressure,and the residue was dissolved in dichloromethane.Then washed successively with saturated potassium carbonate solution,washed with water,dried over anhydrous sodium sulfate,and concentrated under reduced pressure,purified by silica gel column chromatography (PE /CN109988110;(2019);(A)Chinese.EA =3:1),to give apale yellow solid (3)620mg,63%yield.操作方法五To a suspension of 4-chloro-6,7-dimethoxyquinoline 1(40g,0.18mol)and 4-nitrophenol 2(26.2g,0.19mol)in toluene (60mL)was added DIPEA (27.8g,0.22mol).The reaction was heated to 115°C for 24hours and then concentrated in vacuo.The residue was washed with EtOH (40mL)to give the title compound 3as a pale yellow solid (28g,47.8%).WO2013/180949;(2013);(A1)English操作方法六A reactor was sequentially charged with 4-chloro-6,7-dimethoxy-quinoline 1(8.0kg),4-nitrophenol 2(7.0kg),4-dimethylaminopyridine (0.9kg),and 2,6-lutidine (40.0kg).The reactor contents were heated to approximately147°C.When the reaction was complete (less than 5percent starting material remaining as determined by in process HPLC analysis,approximately 20hours),the reactor contents were allowed to cool to approximately 25°C.Methanol (26.0kg)was added,followed by potassiumcarbonate (3.0kg)dissolved in water (50.0kg).The reactor contents were stirred for approximately 2hours.Theresulting solid precipitate was filtered,washed with water (67.0kg),and dried at 25°C for approximately 12hours to afford the title compound 3(4.0kg).WO2015/164869;(2015);(A1)English;EP2017/2758057(2017);(B1)English操作方法七523g of p-nitrophenol 2(3.76mol)was dissolved in 600ml (6.45mol)of N,N-dimethylacetamide,(4.3mol)of potassium t-butoxide and 800g (3.58mol)of4-chloro-6,7-dimethoxyquinoline 1and 1.5L (16.1mol)of N,N-Dimethylacetamide solution,and the reaction solution was heated to 100°C to 120°C and reacted for 2hours.The reaction solution was cooled to room temperature,poured into 3.5L ice water,stirred for 1to 2hours and then filtered.The filter cake was washed twice with 2L of water and then dried in vacuo at 35°C,To give 6,7-dimethoxy-4-(4-nitro-phenoxy)quinoline 3as a pale yellowish white powder 918.2g,the molar yield was 78.6%.CN103664778;(2017);(B)Chinese(二)Cabozantinib (卡博替尼)中间体4的合成合成方法实验步骤参考文献To 3(0.25g,0.77mmol)in 1:1MeOH/THF (50mL)was added Zn dust (0.55g,8.4mmol)and ammonium chloride操作方法一(0.085g,1.6mmol)in water(5mL).The resulting mixturewas heated to reflux for2h,then filtered through celite and concentrated.The residue was dissolved in dichloromethane,washed with water,brine,dried(MgSO4),filtered andconcentrated to provide crude4(0.25g,>100%)which wasused without further purification.US2008/4273(2008);(A1)English操作方法二500ml of methanol was added to the autoclave,and100g of intermediate3and25g of Raney nickel were added.Raisethe temperature at30°C for10hours;Press filtration,concentration,crystallization,filtration,and drying gave86gof Intermediate4in a yield of95%.CN108264482;(2018);(A)ChiNese;CN110240563;(2019);(A).操作方法三Conc hydrochloric acid(11mL,0.2v/w)and iron powder(56.7g,1.0mol)were sequentially added into90%ethanol(550mL,10v/w)under stirring for10min.Then thereaction mixture was heated to60o C,the intermediate3(55.0g,0.17mol)was added.After refluxing for1h,activatedcarbon(1.5g)was added and then reflux for30min.Themixture was filtered while hot,the filtrate was cooled toroom temperature,adjusted to pH12with10N NaOH,poured into water and stirred for2h.The precipitates werecollected by filtration and washed with water until the filtratewas nearly neutral to obtain compound4as a pale yellowsolid in90.7%yield.m.p.:196.4-197.2o C.Bioorganic andMedicinalChemistryLetters;vol.29;nb.19;(2019);Art.No:126630.操作方法四A mixture of3(9.6g,29.4mmol),Fe(8.2g,0.15mol)andAcOH(0.5mL)in90%EtOH(100mL)was refluxed withvigorous agitation for4h.The hot solution was filteredthrough celite and the filter cake was washed with hot EtOH(20mL).The combined filtrate was concentrated underreduced pressure to afford a dark brown solid,which wasrecrystallized from EtOH to afford4as yellow solid(7.2g,82.9%).Bioorganic andMedicinalChemistry;vol.27;nb.17;(2019);p.3825-3835操作方法五6,7-dimethoxy-4-(4-nitrophenyloxy)quinoline3(620mg,1.9mmol)was dissolved in ethanol(40mL).After beingdissolved by stirring,tin(II)chloride dihydrate(1.25g,4.9mmol)was added in portions.After the addition wascompleted,slowly increase to70°C for6h.After thereaction was completed,the reaction solution was cooled toroom temperature and diluted with a1N NaOH(10mL)aqueous solution.It was extracted with ethyl acetate(3×15mL),and the organic layer was combined and washedsequentially with1N aqueous NaOH,water and saturatedaqueous sodium chloride.Dried over anhydrous sodiumsulfate,filtered,and concentrated under reduced pressure toyield a yellow solid355mg,60%yield.CN109988110;(2019);(A)Chinese。

布鲁顿酪氨酸激酶(BTK)抑制剂在治疗炎症免疫性疾病中的研究进展任玮杰,岑丽芳,邹 毅*(中国药科大学药学院, 南京 211198)摘 要 布鲁顿酪氨酸激酶(Bruton’s tyrosine kinase, BTK )是一种胞质酪氨酸激酶,参与B 细胞和粒细胞的活化,在B 细胞和Fcγ受体下游发挥作用。
临床前研究表明,抑制BTK 活性可能成为自身免疫性疾病和过敏等炎症免疫相关病症的潜在治疗方法。
本文总结了BTK 在免疫相关疾病中的作用机制,并对目前临床在研的BTK 抑制剂用于免疫相关疾病治疗的研究情况进行了综述,以期为BTK 抑制剂在非肿瘤适应证的研究提供新思路。
关键词 布鲁顿酪氨酸激酶;炎症免疫;自身免疫性疾病;过敏;临床研究中图分类号 R914;R593 文献标志码 A文章编号 1000−5048(2024)01−0063−10doi :10.11665/j.issn.1000−5048.2023121103引用本文 任玮杰,岑丽芳,邹毅. 布鲁顿酪氨酸激酶(BTK)抑制剂在治疗炎症免疫性疾病中的研究进展[J]. 中国药科大学学报,2024,55(1):63 − 72.Cite this article as: REN Weijie, CEN Lifang, ZOU Yi. Research progress of Bruton's tyrosine kinase (BTK) inhibitors in the treatment of inflammatory and immune-mediated diseases[J]. J China Pharm Univ , 2024, 55(1): 63 − 72.Research progress of Bruton's tyrosine kinase (BTK) inhibitors in the treatment of inflammatory and immune-mediated diseasesREN Weijie, CEN Lifang, ZOU Yi *School of Pharmacy, China Pharmaceutical University, Nanjing 211198, ChinaAbstract Bruton’s tyrosine kinase (BTK), a cytoplasmic tyrosine kinase, plays a central role in the activation of B cells and granulocytes, operating downstream of B cell and Fcγ receptors, and is considered an attractive target for treating autoimmune diseases. Preclinical investigations have demonstrated that inhibition of BTK activity holds promise as a potential therapeutic strategy for inflammatory immune responses such as autoimmune diseases and allergies. This review provides an overview of the mechanisms by which BTK contributes to immune-related diseases and summarizes current research on the development of BTK inhibitors for treating these conditions, aiming to offer novel insights into non-oncology applications for BTK inhibitors.Key words BTK; inflammatory immunity; autoimmune diseases; allergy; clinical research炎症免疫反应是机体一种重要的免疫防御机制。
第42卷第1期中国高原医学与生物学杂志Vol. 42No. 1 2021 年C H IN E S E HIGH ALTITU DE M E D IC IN E A N D B IO L O G Y2021四氢嘧啶对酪氨酸酶的抑制作用机制及类型%张芳,张鑫,杨海山,王志博,汪明香,沈国平,王嵘,朱德锐‘(青海大学医学院,基础医学研究中心,青海西宁810001)摘要目的研究四氢嘧啶(Ectoine)对酪氨酸酶的抑制作用机制及类型。
方法用分光光度法测定不同质量分数的Ectoine及与美白剂复配时对酪氨酸酶的抑制率,并采用酶促动力学法探讨Ectoine对路氣酸酶的抑制作用类型。
结果Ectoine对路氣酸酶抑制率随其浓度升高而增加,当浓度大于2. 0%时,抑制率升高趋势平缓,其半抑制浓度(IC5Q)为4. 58 g/L;Ect〇in e分别与 V C乙基醚、烟酰胺复配时,酪氨酸酶的抑制效果明显提高,尤以2. 5% Ectoine最佳,抑制率分别为75.03%、66. 17%;Ectoine的抑制类型为可逆抑制中的非竞争性抑制,抑制常数(K J为0.41 g/L。
结论Ectoine对酪氨酸酶有一定的抑制作用,分别与V C乙基醚、烟酰胺复配对酪氨酸酶的抑制作用具有协同效果,其作用机制及类型为可逆抑制中的非竞争性抑制。
关键词:四氢嘧啶;酪氨酸酶;抑制率;可逆抑制;非竞争性中图分类号:R36 文献标识码:AD0I: 10. 13452/j. cnki. jqmc. 2021.01.006Mechanism and types of inhibitory effects of Ectoine on tyrosinasexZHANG Fang,ZHANG Xin,YANG Haishan,WANG Zhibo,WANG Mingxiang,SHEN Guoping,WANG Rong,ZHU Deaii(Research Center of Basic Medical Sciences,Medical College of Qinghai University,Xining 810001,China) Abstract Objective To investigate the mechanism and types of inhibitory effects of Ectoine on tyrosinase. Methods The inhibition rate of tyrosinase by different concentrations of Etoine and its combination with whitening a- gent was determined by spectrophotometry, and the inhibition type of tyrosinase by Etoine was discussed by enzymatic kinetics method. Results The inhibitory rate of Ectoine on tyrosinase increased with the increase of its concentration. When the concentration of Etoine was higher than 2. 0%,the inhibition rate increased slowly and the semi-in- hibitory concentration(IC50) was 4.58 g/L. When Etoine was mixed with VC ethyl ether and nicotinamide respectively, the inhibitory effect of tyrosinase was significantly improved. The best effect was 2. 5% Etoine with the inhibition rates of 75. 03% and 66. 17% respectively ; the inhibition type of Etoine was noncompetitive inhibition in revers- ihle inhibition, and the inhibition constant ( Km) was 0. 41 g/L. Conclusion Ectoine has a significant effect on the inhibition of tyrosinase, and it has a synergistic effect on tyrosinase in combination with VC ethyl ether and nicotinamide. The mechanism and type of action is the non-competitive inhibition of reversible inhibition.Keywords: Ectoine; tyrosinase; inhibition rate; reversible inhibition; non-competitive※:国家自然科学基金项目(31760034;21%7018),青海省重点研发与转化计划项目(2019SF121),青海省基础应用研究汁划项目(2020Z J767),高原特色盐湖生物资源的集成研发与转化闭队计划项目(2018KYT1);*通信作者,硕士生导师;E-m ail:z h m le m i2005@ 126.c o m张芳(1990〜)女,汉族,江西籍,在读硕士研究生42有学者认为||:,美白剂是通过抑制酪氨酸酶的活 性,阻断黑色素的合成反应链,减少其在皮肤内的生成 继而达到祛斑美白效果,但美白剂对酪氨酸酶的抑制 作用机理及类型不明。