主要基团的红外特征吸收峰
- 格式:docx
- 大小:37.14 KB
- 文档页数:2

红外各基团特征峰对照表在化学和材料科学领域,红外光谱分析是一种非常重要的研究手段。
通过对样品的红外吸收光谱进行分析,可以获取有关分子结构和化学键的信息。
而红外各基团特征峰对照表则是帮助我们解读红外光谱的重要工具。
红外光谱是基于分子对红外光的吸收而产生的。
当红外光照射到分子时,分子中的某些化学键会吸收特定频率的红外光,导致分子的振动和转动状态发生改变。
这些吸收峰的位置和强度与分子中的基团和化学键的类型、数量以及周围环境有关。
常见的官能团在红外光谱中都有其特征的吸收峰位置。
例如,羟基(OH)在 3200 3600 cm⁻¹范围内有强而宽的吸收峰。
醇类中的羟基通常在 3300 3600 cm⁻¹,而羧酸中的羟基由于形成了氢键,吸收峰会更宽,出现在 2500 3300 cm⁻¹。
羰基(C=O)是另一个重要的官能团,其特征峰通常在 1650 1750 cm⁻¹。
醛类中的羰基吸收峰在 1720 1740 cm⁻¹,酮类的羰基吸收峰则在 1710 1730 cm⁻¹。
羧酸及其衍生物中的羰基吸收峰位置会有所不同,例如酯类中的羰基吸收峰在 1730 1750 cm⁻¹。
胺基(NH₂)的吸收峰在 3300 3500 cm⁻¹,分为对称和不对称伸缩振动。
芳香族胺的吸收峰位置相对较低。
碳碳双键(C=C)的吸收峰在1620 1680 cm⁻¹,但强度通常较弱。
而碳碳三键(C≡C)的吸收峰在 2100 2260 cm⁻¹,具有较强的吸收强度。
醚键(COC)的特征吸收峰在 1050 1300 cm⁻¹。
苯环的骨架振动在 1450 1600 cm⁻¹范围内有多个吸收峰。
除了上述常见的官能团,还有许多其他基团也有各自独特的红外特征峰。
例如,硝基(NO₂)、氰基(CN)、卤素(X)等。
在实际应用中,使用红外各基团特征峰对照表时需要注意一些问题。
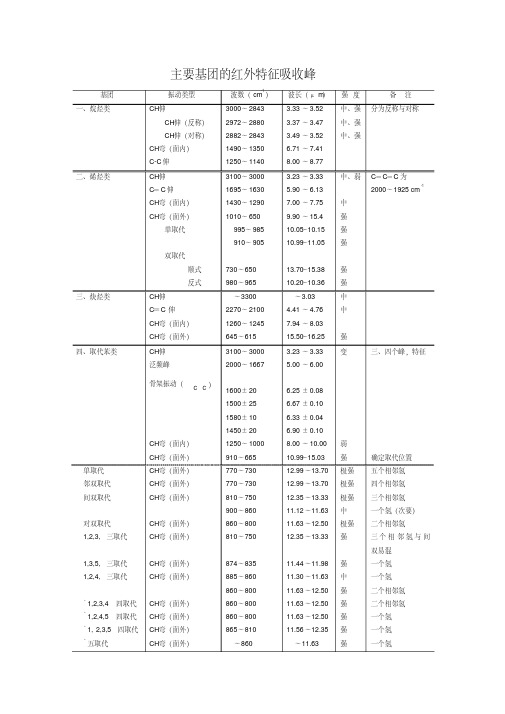
主要基团的红外特征吸收峰基团振动类型波数(cm-1)波长(μm)强度备注一、烷烃类CH伸CH伸(反称)CH伸(对称)CH弯(面内)C-C伸3000~28432972~28802882~28431490~13501250~11403.33~3.523.37~3.473.49~3.526.71~7.418.00~8.77中、强中、强中、强分为反称与对称二、烯烃类CH伸C=C伸CH弯(面内)CH弯(面外)单取代双取代顺式反式3100~30001695~16301430~12901010~650995~985910~905730~650980~9653.23~3.335.90~6.137.00~7.759.90~15.410.05~10.1510.99~11.0513.70~15.3810.20~10.36中、弱中强强强强强C=C=C为2000~1925 cm-1三、炔烃类CH伸C≡C 伸CH弯(面内)CH弯(面外)~33002270~21001260~1245645~615~3.034.41~4.767.94~8.0315.50~16.25中中强四、取代苯类CH伸泛频峰骨架振动(CC)CH弯(面内)CH弯(面外)3100~30002000~16671600±201500±251580±101450±201250~1000910~6653.23~3.335.00~6.006.25±0.086.67±0.106.33±0.046.90±0.108.00~10.0010.99~15.03变弱强三、四个峰,特征确定取代位置单取代邻双取代间双取代对双取代1,2,3,三取代1,3,5,三取代1,2,4,三取代﹡1,2,3,4四取代﹡1,2,4,5四取代﹡1,2,3,5四取代﹡五取代CH弯(面外)CH弯(面外)CH弯(面外)CH弯(面外)CH弯(面外)CH弯(面外)CH弯(面外)CH弯(面外)CH弯(面外)CH弯(面外)CH弯(面外)770~730770~730810~750900~860860~800810~750874~835885~860860~800860~800860~800865~810~86012.99~13.7012.99~13.7012.35~13.3311.12~11.6311.63~12.5012.35~13.3311.44~11.9811.30~11.6311.63~12.5011.63~12.5011.63~12.5011.56~12.35~11.63极强极强极强中极强强强中强强强强强五个相邻氢四个相邻氢三个相邻氢一个氢(次要)二个相邻氢三个相邻氢与间双易混一个氢一个氢二个相邻氢二个相邻氢一个氢一个氢一个氢五、醇类、酚类OH伸OH弯(面内)C—O伸O—H弯(面外)3700~32001410~12601260~1000750~6502.70~3.137.09~7.937.94~10.0013.33~15.38变弱强强液态有此峰OH伸缩频率游离OH分子间氢键分子内氢键OH弯或C—O伸伯醇(饱和)仲醇(饱和)叔醇(饱和)酚类(ФOH)OH伸OH伸OH伸(单桥)OH弯(面内)C—O伸OH弯(面内)C—O伸OH弯(面内)C—O伸OH弯(面内)Ф—O伸3650~35903500~33003570~3450~14001250~1000~14001125~1000~14001210~11001390~13301260~11802.74~2.792.86~3.032.80~2.90~7.148.00~10.00~7.148.89~10.00~7.148.26~9.097.20~7.527.94~8.47强强强强强强强强强中强锐峰钝峰(稀释向低频移动*)钝峰(稀释无影响)六、醚类C—O—C伸1270~1010 7.87~9.90 强或标C—O伸脂链醚脂环醚芳醚(氧与芳环相连)C—O—C伸C—O—C伸(反称)C—O—C伸(对称)=C—O—C伸(反称)=C—O—C伸(对称)CH伸1225~10601100~1030980~9001270~12301050~1000~28258.16~9.439.09~9.7110.20~11.117.87~8.139.52~10.00~3.53强强强强中弱氧与侧链碳相连的芳醚同脂醚O—CH3的特征峰七、醛类(—CHO)CH伸C=O伸CH弯(面外)2850~27101755~1665975~7803.51~3.695.70~6.0010.2~12.80弱很强中一般~2820及~2720cm-1两个带饱和脂肪醛α,β-不饱和醛芳醛C=O伸C=O伸C=O伸~1725~1685~1695~5.80~5.93~5.90强强强八、酮类OC C=O伸C—C伸泛频1700~16301250~10303510~33905.78~6.138.00~9.702.85~2.95极强弱很弱脂酮饱和链状酮α,β-不饱和酮β二酮芳酮类Ar—CO C=O伸C=O伸C=O伸C=O伸C=O伸1725~17051690~16751640~15401700~16301690~16805.80~5.865.92~5.976.10~6.495.88~6.145.92~5.95强强强强强C=O与C=C共轭向低频移动谱带较宽二芳基酮1-酮基-2-羟基(或氨基)芳酮脂环酮四环元酮五元环酮六元、七元环酮C =O 伸C =O 伸C =O 伸C =O 伸C =O 伸1670~1660 1665~1635~1775 1750~1740 1745~1725 5.99~6.02 6.01~6.12~5.63 5.71~5.75 5.73~5.80 强强强强强九、羧酸类(—COOH )OH 伸C =O 伸OH 弯(面内)C —O 伸OH 弯(面外)3400~2500 1740~1650 ~1430 ~1300 950~9002.94~4.00 5.75~6.06 ~6.99 ~7.69 10.53~11.11中强弱中弱在稀溶液中,单体酸为锐峰在~3350cm -1;二聚体为宽峰,以~3000cm -1为中心脂肪酸R —COOH α,β-不饱和酸芳酸C =O 伸C =O 伸C =O 伸1725~1700 1705~1690 1700~16505.80~5.88 5.87~5.91 5.88~6.06强强强氢键十、酸酐链酸酐C =O 伸(反称)C =O 伸(对称)C —O 伸1850~1800 1780~1740 1170~1050 5.41~5.56 5.62~5.75 8.55~9.52 强强强共轭时每个谱带降20 cm-1环酸酐(五元环)C =O 伸(反称)C =O 伸(对称)C —O 伸1870~1820 1800~1750 1300~1200 5.35~5.49 5.56~5.71 7.69~8.33 强强强共轭时每个谱带降20cm-1十一、酯类C OR OC =O 伸(泛频)C =O 伸C —O —C 伸~3450 1770~1720 1280—1100~2.90 5.65~5.81 7.81~9.09弱强强多数酯C =O 伸缩振动正常饱和酯α,β-不饱和酯δ-内酯γ-内酯(饱和)β-内酯C =O 伸C =O 伸C =O 伸C =O 伸C =O 伸1744~1739 ~1720 1750~1735 1780~1760 ~1820 5.73~5.75 ~5.81 5.71~5.76 5.62~5.68 ~5.50 强强强强强十二、胺NH 伸NH 弯(面内)C —N 伸NH 弯(面外)3500~3300 1650~1550 1340~1020 900~650 2.86~3.03 6.06~6.45 7.46~9.80 11.1~15.4 中中强伯胺强,中;仲胺极弱伯胺类仲胺类叔胺类NH 伸(反称、对称)NH 弯(面内)C —N 伸NH 伸NH 弯(面内)C —N 伸C —N 伸(芳香)3500~3400 1650~1590 1340~1020 3500—3300 1650—1550 1350—1020 1360~10202.86~2.94 6.06~6.29 7.46~9.80 2.86—3.03 6.06—6.45 7.41—9.80 7.35~9.80中、中强、中中、弱中极弱中、弱中、弱双峰一个峰十三、酰胺(脂肪与芳香酰胺数据类似)NH伸C=O伸NH弯(面内)C—N伸3500~31001680~16301640~15501420~14002.86~3.225.95~6.136.10~6.457.04~7.14强强强中伯酰胺双峰仲酰胺单峰谱带Ⅰ谱带Ⅱ谱带Ⅲ伯酰胺仲酰胺叔酰胺NH伸(反称)(对称)C=O伸NH弯(剪式)C—N伸NH2面内摇NH2面外摇NH伸C=O伸NH弯+C—N伸C—N伸+NH弯C=O伸~3350~31801680~16501650~16201420~1400~1150750~600~32701680~16301570~15151310~12001670~1630~2.98~3.145.95~6.066.06~6.157.04~7.14~8.701.33~1.67~3.095.95~6.136.37~6.607.63~8.335.99~6.13强强强强中弱中强强中中两峰重合两峰重合十四、氰类化合物脂肪族氰α、β芳香氰α、β不饱和氰C≡N伸C≡N伸C≡N伸2260~22402240~22202235~22154.43~4.464.46~4.514.47~4.52强强强十五、硝基化合物R—NO2 Ar—NO2NO2伸(反称)NO2伸(对称)NO2伸(反称)NO2伸(对称)1590~15301390~13501530~15101350~13306.29~6.547.19~7.416.54~6.627.41~7.52强强强强。

红外各基团特征峰对照表在化学和材料科学领域,红外光谱是一种非常重要的分析工具。
它通过测量物质对红外光的吸收情况,能够提供有关分子结构和化学键的信息。
而理解红外各基团的特征峰,则是解读红外光谱的关键。
红外光谱的波长范围通常在 25 至 25 微米之间,对应的波数范围大约是 4000 至 400 厘米⁻¹。
在这个范围内,不同的基团会产生特定的吸收峰,这些吸收峰的位置、强度和形状都与基团的结构和化学环境有关。
首先,让我们来看看羟基(OH)基团。
在自由状态下,羟基的伸缩振动吸收峰通常出现在 3650 至 3600 厘米⁻¹的范围内。
然而,如果羟基形成了氢键,例如在醇类或羧酸中,这个吸收峰会向低波数方向移动,可能出现在 3500 至 3200 厘米⁻¹之间。
接下来是羰基(C=O)基团。
羰基的伸缩振动吸收峰是红外光谱中一个非常显著的特征峰。
醛类中的羰基吸收峰一般在 1730 至 1710 厘米⁻¹,酮类中的羰基吸收峰则在 1715 至 1680 厘米⁻¹。
羧酸及其衍生物中的羰基吸收峰位置会有所不同,例如羧酸中的羰基吸收峰在 1700 至 1680 厘米⁻¹,酯类中的羰基吸收峰在 1735 至 1720 厘米⁻¹。
氨基(NH₂)基团也是常见的。
伯胺中氨基的对称和不对称伸缩振动吸收峰分别在 3500 至 3300 厘米⁻¹和 3400 至 3200 厘米⁻¹。
仲胺的吸收峰位置相对较低,在 3350 至 3310 厘米⁻¹。
碳碳双键(C=C)的伸缩振动吸收峰通常出现在 1680 至 1620 厘米⁻¹。
但需要注意的是,这个吸收峰强度较弱,并且容易受到共轭效应的影响。
当双键与其他基团共轭时,吸收峰的位置会向低波数方向移动。
碳碳三键(C≡C)的伸缩振动吸收峰则较强,一般在 2260 至 2100厘米⁻¹。

主要基团的红外特征吸收峰团基\7m 1 C 数波 /(\ 长波 度强注备类M烷、一伸C 3 88 2 -3302 53 - 3 3 3 强4 \7称反 /(\ 伸C.47 3 - 3 强4\7 毅X /(\ 伸C 2 5 3 - 3 强4\7 内面 /(\弯 H C 55 3 1- 99 4^1 4 - ^1 7 伸7 - 类M、二伸C33 3 - 3 2 3弱4伸C _L C33 6 1- 5 9 67 O2\7内面 /(\ 弯H C 99 2 1- 33 47-中#) 面/(\ 弯 H C 15.499 9强代取 单强强O 5 6 - O强强类焕二、一伸CO 33 3 -3 - 中7 4 - ^1 4中\7 内面 /(\ 弯H C 0-#)面/(\ 弯H C强伸C3 3 3 - 3 2变征特 *, 个四二、 峰频 泛7 6 6 ^1 - 000 - 5\7 CC/(\ 动振 架骨\7内面 /(\ 弯H C 000 ^1 -弱- ■- - - - \)/ -外一 面一一强代 取 单-- -i •- - - O- O9 9 2强极 邻#) 面/(\ 弯 H C O- OT 9 9 2强极#) 面/(\ 弯 H CT 5 3 2强极 三O 6 8 - O 中©氢个 一#) 面/(\ 弯 H C O88 - O 6.50 2 T 3 6 ^1 强极"一代取 三 3 2 ^1#) 面/(\ 弯 H CT 5 3 2强混易 双 代取 三 3 ^1#) 面/(\ 弯 H C 8 £ ^1 ^1 -强氢个 一 代取 三2 #) 面/(\ 弯 H C3 6 ^1 ^1 - .30 中氢个 一O 88 - O 6 .50 2 T 3 6 ^1 强"一代取 四 3 2 ^1#) 面/(\ 弯 H C O 88 - O 6 .50 2 T 3 6 ^1 强"一代取 四2 #) 面/(\ 弯 H C O 88 - O 6.50 2 T 3 6 ^1 强氢个 一 代取 四3 ^1 #) 面 /(\ 弯 H C5 3 2 T 6强氢个 一 代取 五#)面/(\ 弯H C8 -3 6 ^1 ^1 -强氢个 一五、醇类、酚类OH伸3700〜3200 2.70 〜3.13 变OH弯(面内)1410〜1260 7.09 〜7.93 弱c— O伸1260〜1000 7.94 〜10.00 强C—H弯(面外)750〜650 13.33 〜15.38 强液态有此峰0H伸缩频率游离0H OH伸3650〜3590 2.74 〜2.79 强锐峰分子间氢键OH伸3500〜3300 2.86 〜3.03 强钝峰(稀释向低频移动*)分子内氢键OH伸(单桥)3570〜3450 2.80 〜2.90 强钝峰(稀释无影响)0H弯或C—O伸伯醇(饱和)OH弯(面内)〜1400 〜7.14 强c— O伸1250〜1000 8.00 〜10.00 强仲醇(饱和)OH弯(面内)〜1400 〜7.14 强c— O伸1125〜1000 8.89 〜10.00 强叔醇(饱和)OH弯(面内)〜1400 〜7.14 强c— O伸1210〜1100 8.26 ~ 9.09 强酚类(①0H OH弯(面内)1390〜1330 7.20 〜7.52 中①一O伸1260〜1180 7.94 〜8.47 强六、醚类c— C— C 伸1270〜1010 7.87 ~ 9.90 强或标c—O伸脂链醚c— C— C 伸1225〜1060 8.16 〜9.43 强脂环醚C—C-C伸(反称)1100〜1030 9.09 〜9.71 强C—C-C伸(对称)980〜900 10.20 〜11.11 强芳醚=(—O-C伸 (反称1270〜1230 7.87 〜8.13 强氧与侧链碳相连(氧与芳环相连)=(—O-C伸 (对称1050〜1000 9.52 〜10.00 中的芳醚同脂醚CH伸〜2825 〜3.53 弱O- CH的特征峰七、醛类CH伸2850〜2710 3.51 〜3.69 弱—般~ 2820 及~ (—CHO 2720cm1两个带C= O伸1755〜1665 5.70 ~ 6.00 很强CH弯(面外)975〜780 10.2 〜12.80 中饱和脂肪醛C= O伸〜1725 〜5.80 强a ,卩-不饱和醛C= O伸〜1685 〜5.93 强芳醛C= O伸〜1695 〜5.90 强八、酮类C= O伸1700〜1630 5.78 〜6.13 极强X c— C伸1250〜1030 8.00 〜9.70 弱.C= O泛频3510〜3390 2.85 〜2.95 很弱脂酮饱和链状酮C= O伸1725〜1705 5.80 〜5.86 强a,B-不饱和酮C= O伸1690〜1675 5.92 〜5.97 强C= O与C= C共轭向低频移动B二酮C= O伸1640〜1540 6.10 ~ 6.49 强谱带较宽芳酮类C= O伸1700〜1630 5.88 〜6.14 强Ar—CO C= O伸1690〜1680 5.92 ~ 5.95 强二芳基酮C= O伸1670〜1660 5.99 〜6.02 强1-酮基-2-羟基C= O伸1665〜1635 6.01 〜6.12 强(或氨基)芳酮脂环酮四环元酮C= O伸〜1775 〜5.63 强五元环酮C= O伸1750〜1740 5.71 〜5.75 强六元、七元环酮C= O伸1745〜1725 5.73 〜5.80 强九、羧酸类OH伸3400〜2500 2.94 ~ 4.00 中在稀溶液中,单体(—COOH C= O伸1740〜1650 5.75 ~ 6.06 强酸为锐峰在〜0H弯(面内)〜1430 〜6.99 弱3350cm1;二聚体c— O伸〜1300 〜7.69 中为宽峰,以〜0H弯(面外)950~ 900 10.53 〜11.11 弱3000cm!1为中心脂肪酸R—COOH C= O伸1725〜1700 5.80 〜5.88 强a,B-不饱和酸C= O伸1705〜1690 5.87 〜5.91 强芳酸C= O伸1700〜1650 5.88 ~ 6.06 强氢键十、酸酐链酸酐C= O伸(反称)1850〜1800 5.41 ~ 5.56 强共轭时每个谱带C= O伸(对称)1780〜1740 5.62 〜5.75 强降20 cm-1c— O伸1170〜1050 8.55 〜9.52 强环酸酐C= O伸(反称)1870〜1820 5.35 ~ 5.49 强共轭时每个谱带(五元环)C= O伸(对称)1800〜1750 5.56 〜5.71 强降20cm1c— O伸1300〜1200 7.69 〜8.33 强十一、酯类C= O伸(泛频)〜3450 〜2.90 弱C= O伸1770〜1720 5.65 〜5.81 强多数酯一C—O—R c— C— C 伸1280—1100 7.81 ~ 9.09 强C= O伸缩振动正常饱和酯C= C伸1744〜1739 5.73 〜5.75 强a,B-不饱和酯C= C伸〜1720 〜5.81 强S -内酯C= C伸1750〜1735 5.71 〜5.76 强Y -内酯(饱和)C= C伸1780〜1760 5.62 〜5.68 强B -内酯C= C伸〜1820 〜5.50 强十二、胺NH伸3500〜3300 2.86 〜3.03 中伯胺强,中;仲胺NH弯(面内)1650〜1550 6.06 ~ 6.45 极弱C— N伸1340〜1020 7.46 〜9.80 中NH弯(面外)900〜650 11.1 〜15.4 强伯胺类NH伸(反称、对称)3500〜3400 2.86 〜2.94 中、中双峰NH弯(面内)1650〜1590 6.06 〜6.29 强、中C— N伸1340〜1020 7.46 〜9.80 中、弱仲胺类NH伸3500—3300 2.86 —3.03 中一个峰NH弯(面内)1650—1550 6.06 —6.45 极弱C— N伸1350—1020 7.41 —9.80 中、弱叔胺类C— N伸(芳香)1360〜1020 7.35 〜9.80 中、弱胺芳 酰与 三恤十— 伸H N-5 32 23 - 6 8 2强30 6 7 88 6强I 带谱\7 内面/(\弯H N 55 5 7 6 4 & - O 66强n 带谱 - -- -申W _ C --一 04一14一m一14一_ 4 - 7 7中_ -- 山带 谱_ 一胺 酰 伯 一- » 反/(\ N。

主要基团的红外特征吸收峰基团振动类型波数(cm-1)波长(μm)强度备注一、烷烃类CH伸CH伸(反称)CH伸(对称)CH弯(面内)C-C伸3000~28432972~28802882~28431490~13501250~11403.33~3.523.37~3.473.49~3.526.71~7.418.00~8.77中、强中、强中、强分为反称与对称二、烯烃类CH伸C=C伸CH弯(面内)CH弯(面外)单取代双取代顺式反式3100~30001695~16301430~12901010~650995~985910~905730~650980~9653.23~3.335.90~6.137.00~7.759.90~15.410.05~10.1510.99~11.0513.70~15.3810.20~10.36中、弱中强强强强强C=C=C为2000~1925 cm-1三、炔烃类CH伸C≡C 伸CH弯(面内)CH弯(面外)~33002270~21001260~1245645~615~3.034.41~4.767.94~8.0315.50~16.25中中强四、取代苯类CH伸泛频峰骨架振动(CC=ν)CH弯(面内)CH弯(面外)3100~30002000~16671600±201500±251580±101450±201250~1000910~6653.23~3.335.00~6.006.25±0.086.67±0.106.33±0.046.90±0.108.00~10.0010.99~15.03变弱强三、四个峰,特征确定取代位置单取代邻双取代间双取代对双取代1,2,3,三取代1,3,5,三取代1,2,4,三取代﹡1,2,3,4四取代﹡1,2,4,5四取代﹡1,2,3,5四取代﹡五取代CH弯(面外)CH弯(面外)CH弯(面外)CH弯(面外)CH弯(面外)CH弯(面外)CH弯(面外)CH弯(面外)CH弯(面外)CH弯(面外)CH弯(面外)770~730770~730810~750900~860860~800810~750874~835885~860860~800860~800860~800865~810~86012.99~13.7012.99~13.7012.35~13.3311.12~11.6311.63~12.5012.35~13.3311.44~11.9811.30~11.6311.63~12.5011.63~12.5011.63~12.5011.56~12.35~11.63极强极强极强中极强强强中强强强强强五个相邻氢四个相邻氢三个相邻氢一个氢(次要)二个相邻氢三个相邻氢与间双易混一个氢一个氢二个相邻氢二个相邻氢一个氢一个氢一个氢。

主要基团的红外特征吸收峰
9.90 12.80
2.95 11.11
9.09 15.4
7.14
红外波谱
分子被激发后,分子中各个原子或基团(化学键)都会产生特征的振动,从而在特点的位置会出现吸收。
相同类型的化学键的振动都是非常接近的,总是在某一范围内出现。
常见官能团的红外吸收频率
整个红外谱图可以分为两个区,4000~1350区是由伸缩振动所产生的吸收带,光谱比较简单
但具有强烈的特征性,1350~650处指纹区。
通常,4000~2500处高波数端,有与折合质量小的氢原子相结合的官能团O-H, N-H, C-H, S-H 键的伸缩振动吸收带,在2500-1900波数范围内常常出现力常数大的三件、累积双键如:- C≡C-,- C≡N, -C=C=C-, -C=C=O, -N=C=O等的伸缩振动吸收带。
在1900以下的波数端有-C=C-, -C=O, -C=N-, -C=O等的伸缩振动以及芳环的骨架振动。
1350~650指纹区处,有C-O, C-X的伸缩振动以及C-C的骨架振动,还有力常数较小的弯曲振动产生的吸收峰,因此光谱非常复杂。
该区域各峰的吸收位置受整体分子结构的影响较大,分子结构稍有不同,吸收也会有细微的差别,所以指纹区对于用已知物来鉴别未知物十分重要。
主要基团的红外特征吸收峰团基C数波/(\ 长波 度强注备类M 烷、 一伸C 2 5 3 - 3 3 3强4 \7称 反 /(\伸C.47 3 - 3 强42 53 - 3 强4\7内 面/(\弯H C 55 3 99 4 ^1 ^1 4 - ^1 7 & 伸心T 55 27 - 类M、二伸C3 3 3 - 3 2 3弱433 65 96 中mm 5C 99 ^1 - 00 220\7内面 /(\ 弯H C 99 2 33 4 ^17-强#) 面/(\ 弯H C强代取 单 5 8 9 - 5 9 9强强强类焕二、一伸C 3 3 -3 -中伸C中\7内面 /(\ 弯H C 5 ^1 - 2 0-强#) 面/(\ 弯H C伸C3 3 3 - 3 2变征特 *, 个四二、 峰 频 泛 76 6 ^1 - 00 0 - 5 弱强/(\动振 架 骨亠)\7 内面 /(\弯H C#)面/(\ 弯H C O T 55 27代取 单 #) 面 /(\ 弯H C 70 3 T 强 极 邻#) 面 /(\ 弯H C 70 3 T强 极 #) 面 /(\ 弯H C 3 3 3 T 5 3 2 强 极三#) 面 /(\ 弯H C中© 氢 个 一代取 三 3 2 ^1#) 面/(\ 弯H C55 2 T 3 6 ^1 强极"一代取 三3 ^1 #) 面/(\ 弯H C3 3 3 T 5 3 2 强代取 三2 #) 面/(\ 弯H C 8 £ T ^1 ^1 强混易 双 代取 四3 2 ^1#) 面/(\ 弯H C 3 6 ^1 ^1 - O ^1 中氢个 一 代取 四2 #) 面/(\ 弯H C 55 2 T 3 6 ^1 强氢个 一 代取 四3 ^1 #) 面/(\ 弯H C 55 2 T 3 6 ^1 强"一代取 五#)面/(\ 弯H C55 2 ^1 - 3 6 强"一5 3 2 T6 ^1 ^1强氢个 一 8 -3 6 ^1 ^1 -强氢个 一氢个 一五、醇类、酚类OH伸3700〜3200 2.70 〜3.13 变液态有此峰OH弯(面内)1410〜1260 7.09 〜7.93 弱c— O伸1260〜1000 7.94 〜10.00 强C—H弯(面外)750〜650 13.33 〜15.38 强0H伸缩频率OH伸3650〜3590 2.74 〜2.79 强锐峰游离0H OH伸3500〜3300 2.86 〜3.03 强钝峰(稀释向低频分子间氢键OH伸(单桥)3570〜3450 2.80 〜2.90 强移动*)分子内氢键OH弯(面内)〜1400 〜7.14 强钝峰(稀释无影0H弯或C— O伸c— O伸1250〜1000 8.00 〜10.00 强响)伯醇(饱和)OH弯(面内)〜1400 〜7.14 强仲醇(饱和)c— O伸1125〜1000 8.89 〜10.00 强叔醇(饱和)OH弯(面内)〜1400 〜7.14 强酚类(①0H c— O伸1210〜1100 8.26 ~ 9.09 强OH弯(面内)1390〜1330 7.20 〜7.52 中①一O伸1260〜1180 7.94 〜8.47 强六、醚类c— C— C 伸1270〜1010 7.87 ~ 9.90 强或标c—O伸脂链醚c— C— C 伸1225〜1060 8.16 〜9.43 强氧与侧链碳相连脂环醚C——C伸(反称)1100〜1030 9.09 〜9.71 强的芳醚同脂醚芳醚C——C伸(对称)980〜900 10.20 〜11.11 强O— CH的特征峰(氧与芳环相连)=C—C-C# (反称)1270〜1230 7.87 〜8.13 强=C—C-C# (对称)1050〜1000 9.52 〜10.00 中CH伸〜2825 〜3.53 弱七、醛类CH伸2850〜2710 3.51 〜3.69 弱—般~ 2820 及~(—CHO C= O伸1755〜1665 5.70 ~ 6.00 很强2720cm1两个带CH弯(面外)975〜780 10.2 〜12.80 中饱和脂肪醛C= O伸〜1725 〜5.80 强a ,卩-不饱和醛C= O伸〜1685 〜5.93 强芳醛C= O伸〜1695 〜5.90 强八、酮类C= O伸1700〜1630 5.78 〜6.13 极强c— C伸1250〜1030 8.00 〜9.70 弱泛频3510〜3390 2.85 〜2.95 很弱脂酮C= O伸1725〜1705 5.80 〜5.86 强C= O与C= C共轭饱和链状酮C= O伸1690〜1675 5.92 〜5.97 强向低频移动a-不饱和酮C= O伸1640〜1540 6.10 ~ 6.49 强谱带较宽B二酮C= O伸1700〜1630 5.88 〜6.14 强芳酮类C= O伸1690〜1680 5.92 ~ 5.95 强Ar — CO二芳基酮C= O伸1670〜1660 5.99 〜6.02 强1-酮基-2-羟基C= O伸1665〜1635 6.01 〜6.12 强(或氨基)芳酮C= O伸〜1775 〜5.63 强脂环酮C= O伸1750〜1740 5.71 〜5.75 强四环元酮C= O伸1745〜1725 5.73 〜5.80 强五元环酮六元、七元环酮九、羧酸类OH伸3400〜2500 2.94 〜4.00 中在稀溶液中,单体(—COOH C= O伸1740〜1650 5.75 ~ 6.06 强酸为锐峰在〜0H弯(面内)〜1430 〜6.99 弱3350cm1;二聚体c— O伸〜1300 〜7.69 中为宽峰,以〜0H弯(面外)950 ~ 900 10.53 〜11.11 弱3000cm1为中心脂肪酸C= O伸1725〜1700 5.80 〜5.88 强氢键F—COOH C= O伸1705〜1690 5.87 〜5.91 强a, B-不饱和酸C= O伸1700〜1650 5.88 ~ 6.06 强芳酸十、酸酐链酸酐C= O伸(反称)1850〜1800 5.41 ~ 5.56 强共轭时每个谱带C= O伸(对称)1780〜1740 5.62 〜5.75 强降20 cmc— O伸1170〜1050 8.55 〜9.52 强环酸酐C= O伸(反称)1870〜1820 5.35 ~ 5.49 强共轭时每个谱带(五元环)C= O伸(对称)1800〜1750 5.56 〜5.71 强降20cm1c— O伸1300〜1200 7.69 〜8.33 强十一、酯类C= O伸(泛频)〜3450 〜2.90 弱多数酯C= O伸1770〜1720 5.65 〜5.81 强c— C—C 伸1280—1100 7.81 ~ 9.09 强C= O伸缩振动C= C伸1744〜1739 5.73 〜5.75 强正常饱和酯C= C伸〜1720 〜5.81 强a,B-不饱和酯C= C伸1750〜1735 5.71 〜5.76 强S -内酯C= C伸1780〜1760 5.62 〜5.68 强Y -内酯(饱和)C= C伸〜1820 〜5.50 强B -内酯十二、胺NH伸3500〜3300 2.86 〜3.03 中伯胺强,中;仲胺NH弯(面内)1650〜1550 6.06 ~ 6.45 中极弱C— N伸1340〜1020 7.46 〜9.80 强NH弯(面外)900〜650 11.1 〜15.4类胺 伯对反 /(\ 伸N 330 - 5 3 942 -882中4类胺 仲\7 内面/(\ 弯H N99 5 55 69 2 & - 中峰个 一类 胺 叔O ^1 - O 33 ^188 9 - 弱4伸N0 3 6 8 2 中\7内面/(\弯H N4弱极O ^1 55 3 88 9 ^1 4 弱4O ^1 - 388 9 - 5 3弱4胺酰二、一 十 伸N2 23 - 6 8 2强伸_L C 33 6 ^1 - O 8 6 ^1强内面/(\ 弯H N55 5 T O ^1 4- O ^1强I 带谱中n 带谱山带 谱胺 酰 伯 仮N55 33 -8 9 2 -强 胺 酰 仲4 ^1 3 - 强 胺酰 叔伸_L C55 6 T O 8 6 ^1 0 - 5 9 5 强\7式剪 /(\ 弯H NO 2 6 ^1 - 55 6强中55- 弱.67 ^1 - 3 ^1中伸N 2 3 - 3 - 强伸_L C33 6 ^1 - O 8强60- 中3 3- 3 6中伸_L C33 66强氤芳np 、a强np、a强物 合五 十33 5 T 99 5 55 - 22 强Q N Ar55 3 ^1 - 99 3 ^1 4 - 9 ^1强66 - 强33 355 32 5- ^1 4强。
物质的红外光谱是其分子结构的反映,谱图中的吸收峰与分子中各基团的振动形式相对应。
多原子分子的红外光谱与其结构的矢系,一般是通过实验手段得到。
这就是通过比较大量己知化合物的红外光谱,从中总结岀各种基团的吸收规律。
实验表明,组成分子的各种基团,如0-H、N-H、C-H、C二C、C=OH和C C等,都有自己的特定的红外吸收区域,分子的其它部分对其吸收位置影响较小。
通常把这种能代表及存在、并有较高强度的吸收谱带称为基团频率,其所在的位置一般又称为特征吸收峰。
一、基团频率区和指纹区(一)基团频率区中红外光谱区可分成4000 cm-1 ~1300 cm-1 和1800cm-l (1300 cm-1) ~ 600 cm-1两个区域。
最有分析价值的基团频率在4000 cm-1 ~ 1300 cm-1之间,这一区域称为基团频率区、官能团区或特征区。
区的峰是由伸缩振动产生的吸收带,比较稀疏,容易辨认,常用于鉴定官能团。
在1800 cm-1 (1300 cm-1) ~600 cm-1区域,除单键的伸缩振动外,还有因变形振动产生的谱带。
这种振动与整个分子的结构有矢。
当分子结构稍有不同时,该区的吸收就有细微的差异,并显示出分子特征。
这种情况就像人的指纹一样,因此称为指纹区。
指纹区对于指认结构类似的化合物很有帮助,而且可以作为化合物存在某种基团的旁证。
基团频率区可分为三个区域:(1)4000 ~2500 cm-1 X-H伸缩振动区叹可以是0、H、C或S等原子。
O-H基的伸缩振动出现在3650-3200 cm-1围,它可以作为判断有无醇类、酚类和有机酸类的重要依据。
当醇和酚溶于非极性溶剂(如CCI4),浓度于O.OImol.dm-3时,在3650~3580cm-l处出现游离0・H基的伸缩振动吸收,峰形尖锐,且没有其它吸收峰干扰,易于识别。
当试样浓度增加时,疑基化合物产生缔合现象,0-H基的伸缩振动吸收峰向低波数方向位移,在3400 ~3200 cm-1出现一个宽而强的吸收峰。
主要基团的红外特征吸收峰
红外光谱是一种常用的分析方法,可用于确定分子中不同基团的存
在与否以及它们的结构。
每个基团在红外光谱上都有特征吸收峰,通
过分析这些吸收峰的位置和强度,可以确定分子中不同基团的类型和
数量。
本文将介绍一些常见主要基团的红外特征吸收峰。
1. 羧基(COOH):羧基是有机化合物中常见的一个基团,其红外
吸收峰通常出现在1700-1750 cm-1范围内。
这个吸收峰的强度通常较高,特征明显。
2. 羰基(C=O):羰基是许多有机化合物中都存在的一个重要基团,其红外吸收峰通常出现在1650-1750 cm-1范围内。
酮和醛中的羰基吸
收峰位置大致相同,但醛的吸收峰强度通常较高。
3. 羟基(OH):羟基是醇、酚和羧酸等化合物中的一个常见基团,其红外吸收峰通常出现在3200-3600 cm-1范围内。
醇中的羟基吸收峰
位置比酚和羧酸中的羟基吸收峰位置更低。
4. 氨基(NH2):氨基是氨和氨基酸等化合物中的一个重要基团,
其红外吸收峰通常出现在3300-3500 cm-1范围内。
氨基的吸收峰呈现
为两个峰,其中一个位于3200-3400 cm-1范围内,另一个位于1500-1600 cm-1 范围内。
5. 烷基(C-H):烷基是烷烃(如甲烷、乙烷等)中的基团,其红
外吸收峰通常出现在2850-3000 cm-1范围内。
饱和烃的烷基呈现为一
个宽而强烈的吸收峰,不饱和烃的烷基吸收峰会显示出分裂。
6. 苯环的C-H:苯环的C-H键是芳香化合物中的一个重要基团,其
红外吸收峰通常出现在3020-3100 cm-1范围内。
这个吸收峰是一个强
而尖锐的峰。
以上所列举的是一些常见的主要基团的红外特征吸收峰,它们在红
外光谱分析中起着重要的作用。
当我们测试一个化合物的红外光谱时,可以通过与这些特征吸收峰的对比来确定分子中存在哪些基团,并据
此推测化合物的结构。
需要指出的是,红外光谱的解读需要综合考虑
各个吸收峰的位置、强度和形状,因此在实际分析中还需进一步结合
其他信息进行准确定性的判断。
在红外光谱分析中,准确识别主要基团的红外特征吸收峰对于化学
和生物科学领域的研究具有重要意义。
通过红外光谱分析,科学家们
可以更好地理解化合物的结构、性质和反应机制,从而推动相关研究
的进展。
总结起来,红外光谱分析是一种强大的工具,可用于识别化合物中
的不同基团。
通过分析主要基团的红外特征吸收峰,我们能够更好地
理解化合物的结构以及化学与生物过程中的相关性质和反应机制。
随
着红外光谱技术的不断发展,我们相信会有更多的基团和吸收峰被发
现并应用于实际研究中,为科学研究做出更大的贡献。