农业部公告第2513号――《兽药质量标准》(2017年版)
- 格式:doc
- 大小:24.00 KB
- 文档页数:2

中华人民共和国农业部公告第2525号——新兽药注册
目录
文章属性
•【制定机关】农业部(已撤销)
•【公布日期】2017.05.03
•【文号】中华人民共和国农业部公告第2525号
•【施行日期】2017.05.03
•【效力等级】部门规范性文件
•【时效性】现行有效
•【主题分类】农业科技
正文
中华人民共和国农业部公告
第2525号
根据《兽药管理条例》和《兽药注册办法》规定,经审查,批准普莱柯生物工程股份有限公司等8家单位申报的鸡新城疫、禽流感(H9亚型)、传染性法氏囊病三联灭活疫苗(La Sota株+SZ株+rVP2蛋白)等2种兽药产品为新兽药,核发《新兽药注册证书》,并发布产品试行规程、质量标准、说明书和标签,自发布之日起执行。
特此公告。
附件:1.新兽药注册目录
2.试行规程(略)
3.质量标准(略)
4.说明书和标签
农业部
2017年5月3日
附件1。

药物饲料添加剂品种目录及使用规范The pony was revised in January 2021附件:关于发布《药物饲料添加剂品种目录及使用规范》的公告(征求意见稿)为加强药物饲料添加剂管理,进一步规范药物饲料添加剂使用,根据《兽药管理条例》规定,我部组织修订了《药物饲料添加剂品种目录及使用规范》(附录1、附录2),现就有关事项公告如下:一、本公告收载的品种按照规定取得“兽药添字”产品批准文号或《进口兽药注册证书》的,可作为药物饲料添加剂使用,并按照附录2规定的使用规范执行。
公告收载品种的质量标准变更或废止的,按照我部发布的同品种兽药质量标准或有关废止、禁止性规定执行。
二、除本公告收载品种及我部批准的其他药物饲料添加剂外,饲料生产企业不得在饲料中添加其他兽药。
三、饲料生产企业应按照本公告规定使用药物饲料添加剂,禁止违反“添加量”规定,超量使用药物饲料添加剂;禁止违反“适用动物”规定,在其他动物饲料产品中使用药物饲料添加剂;禁止违反“注意事项”规定,生产不符合本公告要求的饲料产品。
四、饲料生产企业生产含有药物饲料添加剂的饲料的,在同一产品中添加的药物饲料添加剂不得超过3种,且必须在饲料产品标签中标明所含全部药物饲料添加剂成分的通用名、含量、适用动物、休药期及使用注意事项等内容。
五、本公告自发布之日起执行。
原农牧发〔2001〕20号、农业部公告第168号和农业部公告第220号同时废止。
附录1药物饲料添加剂品种目录序号药物饲料添加剂名称1二硝托胺预混剂2土霉素钙预混剂3山花黄芩提取物散4马度米星铵预混剂5甲基盐霉素尼卡巴嗪预混剂6甲基盐霉素预混剂7吉他霉素预混剂8地克珠利预混剂9亚甲基水杨酸杆菌肽预混剂10那西肽预混剂11杆菌肽锌预混剂12阿维拉霉素预混剂13金霉素预混剂14盐酸氨丙啉乙氧酰胺苯甲酯预混剂15盐酸氨丙啉乙氧酰胺苯甲酯磺胺喹恶啉预混剂16盐酸氯苯胍预混剂17盐霉素预混剂18盐霉素钠预混剂19莫能菌素预混剂20恩拉霉素预混剂21海南霉素钠预混剂22黄霉素预混剂23维吉尼亚霉素预混剂24博落回散25喹烯酮预混剂26氯羟吡啶预混剂附录2药物饲料添加剂使用规范一、二硝托胺预混剂(Dinitolmide Premix)【执行标准】2015年版《中国兽药典》【有效成分】二硝托胺【适用动物】鸡【作用与用途】抗球虫药。

2017兽药质量标准2017年兽药质量标准的制定是为了确保兽药的质量与安全。
兽药作为一种用于预防、控制和治疗动物疾病的药物,其质量标准要求严格,以保障动物的健康和人类的食品安全。
2017年兽药质量标准主要包括以下几个方面的内容:第一,有关兽药的生产要求。
兽药的生产必须在符合质量管理系统要求的条件下进行,以确保兽药的质量和安全性。
此外,生产过程中还需要遵守相关法律法规,如药品生产质量管理规范、药品GMP等。
兽药生产企业必须建立合适的生产设备和设施,确保生产过程的可操作性和有效性。
第二,有关兽药原料和药品成分的要求。
兽药的原料必须符合药典规定的质量标准,包括其纯度、含量、痕量杂质等方面的要求。
兽药的成分应符合药品注册的要求,并且需要进行有效的检测和分析。
第三,有关兽药的稳定性要求。
兽药的稳定性是指其在一定条件下的保存期限内,其质量和性能能够保持稳定。
稳定性的评估必须符合相关的规定和标准,并且需要进行相应的实验和检测。
第四,有关兽药的包装要求。
兽药的包装必须符合相关的法规和标准要求,以防止其受到污染和破坏。
包装材料和包装工艺必须符合卫生要求,并且需要对包装进行必要的标识和说明。
第五,有关兽药的质量控制要求。
兽药的质量控制主要包括分析方法的验证、质量控制样品的制备和使用、质量控制记录的保存和归档等方面的要求。
兽药企业必须建立完善的质量控制体系,并且进行有效的质量控制措施。
以上仅是2017年兽药质量标准的一部分内容,具体的标准还有更多详细的要求。
2017年兽药质量标准的制定是为了确保兽药的质量和安全性,提高兽药在动物疾病控制和人类食品安全方面的作用。
兽药企业必须严格遵守相关的标准和规定,确保兽药的质量和安全性。
只有如此,我们才能有效地预防和控制动物疾病,保障兽群的健康和人类的食品安全。

中华人民共和国农业部公告第2253号文章属性•【制定机关】农业部(已撤销)•【公布日期】2015.05.04•【文号】中华人民共和国农业部公告第2253号•【施行日期】2015.05.04•【效力等级】部门规范性文件•【时效性】现行有效•【主题分类】畜牧业正文中华人民共和国农业部公告第2253号根据《兽药管理条例》和《兽药注册办法》规定,经审核,批准西班牙海博莱生物大药厂等2家公司生产的猪伪狂犬病毒gE糖蛋白阻断ELISA抗体检测试剂盒等2种兽药产品在我国注册,核发《进口兽药注册证书》,并发布产品质量标准、说明书和标签,自发布之日起执行。
批准梅里亚有限公司等2家公司生产的禽病毒性关节炎油乳剂灭活疫苗(Olson WVU2937株)等2种兽药产品在我国再注册,核发《进口兽药注册证书》,并发布修订后的产品质量标准、说明书和标签,自发布之日起执行。
此前发布的同品种兽药产品质量标准同时废止。
批准美国礼来公司生产的阿维拉霉素预混剂变更注册,并发布修订后的产品质量标准、说明书和标签。
此前发布的同品种兽药产品质量标准同时废止。
批准都法玛制药等2家公司生产的伊维菌素预混剂等3种兽药产品在我国变更注册。
特此公告。
附件:1.进口兽药注册目录2.质量标准3.说明书和标签农业部2015年5月4日附件1:进口兽药注册目录兽药名称生产厂名称进口兽药注册证书号有效期限备注猪伪狂犬病毒gE糖蛋白阻断ELISA抗体检测试剂盒Blocking ELISA Test Technique for the Detection of Specific Antibodies of the gE Glycoprotein of the Aujeszky’s Disease Virus in Pig Serum 西班牙海博莱生物大药厂LABORATORIOSHIPPA, S.A(2015)外兽药证字24号2015.05-2020.04注册多杀霉素咀嚼片Spinosad Chewable Tablets 美国艾伯维公司AbbVie, Inc.(2015)外兽药证2015.05-注册字25号2020.04 禽病毒性关节炎油乳剂灭活疫苗(Olson WVU2937株)Infectious Arthritis Vaccine, Inactivated (Strain Olson WVU2937) 梅里亚有限公司意大利生产厂Merial ItaliaS.p.A(2015)外兽药证字26号2015.05-2020.04再注册鸡传染性鼻炎灭活疫苗(A型+C型)Coryza Vaccine, Inactivated (Serotype A+ Serotype C) 梅里亚有限公司法国生产厂MerialS.A.S,France(2015)外兽药证字27号2015.05-2020.04再注册阿维拉霉素预混剂(10%)Avilamycin Premix 美国礼来公司英国DISTA生产厂Eli Lily andCompany Limited(2014)外兽药证字04号2014.02-2019.01变更注册:变更兽药质量标准阿维拉霉素预混剂(20%)Avilamycin Premix (2014)外兽药证字05号2014.02-2019.01 伊维菌素预混剂0.6%Ivermectin Premix (IVOMEC?) 都法玛制药Dopharma B.V.(2011)外兽药证字32号2011.08-2016.07变更注册:变更有效期为3年延胡索酸泰妙菌素可溶性粉(45%)Tiamulin Fumarate Soluble Power(45%) 奥地利Sandoz生产厂Sandoz GmbH(2011)外兽药证字11号2011.05-2016.04变更注册:生产厂名称由瑞士诺华公司奥地利Sandoz生产厂变更为奥地利Sandoz生产厂延胡索酸泰妙菌素预混剂(80%)Tiamulin Fumarate Premix(80%) 奥地利Sandoz生产厂Sandoz GmbH(2011)外兽药证字12号2011.05-2016.04附件2(略)附件3:猪伪狂犬病毒gE糖蛋白阻断ELISA抗体检测试剂盒等5种兽药产品说明书和标签一、猪伪狂犬病毒gE糖蛋白阻断ELISA抗体检测试剂盒说明书和标签(一)猪伪狂犬病毒gE糖蛋白阻断ELISA抗体检测试剂盒说明书【兽药名称】通用名猪伪狂犬病毒gE糖蛋白阻断ELISA抗体检测试剂盒商品名无英文名Blocking ELISA Test Technique for the Detection of Specific Antibodies of the gE Glycoprotein of the Aujeszky’s Disease Virus in Pig Serum汉语拼音Zhuweikuangquanbingdu gE Tangdanbai Zuduan ELISA Kangti Jianceshijihe【性状】(1)抗原包被板表面光洁、无裂纹、无异物,96孔/块,5块/盒。

中华人民共和国农业部公告第2550号——新兽药注册目录
正文:
----------------------------------------------------------------------------------------------------------------------------------------------------
中华人民共和国农业部公告
第2550号
根据《兽药管理条例》和《兽药注册办法》规定,经审查,批准中国农业科学院兰州兽医研究所申报的口蹄疫O型、A型、亚洲1型三价灭活疫苗(O/HB/HK/99株+AF/72株+Asia-1/XJ/KLMY/04株,悬浮培养)变更注册,并发布修订后的试行规程、质量标准、说明书和标签,自发布之日起执行。
原我部发布的该产品试行规程、质量标准、说明书和标签同时废止。
特此公告。
附件:1.新兽药注册目录
2.试行规程(略)
3.质量标准(略)
4.说明书和标签
农业部
2017年7月17日
附件1
新兽药注册目录
新兽药名称
研制单位
类别
新兽药注册证书号
备注
监测期
口蹄疫O型、A型、亚洲1型三价灭活疫苗(O/HB/HK/99株+AF/72株+Asia-1/XJ/KLMY/04株,悬浮培养)中国农业科学院
兰州兽医研究所
二类
(2010)新兽药证字04号
变更注册:规格由“(1)50ml/瓶(2)100ml/瓶”变更为“(1)20ml/瓶(2)50ml/瓶(3)100ml/瓶(4)250ml/瓶”,使用剂量由“牛每头3ml”变更为“牛每头2ml”,生产工艺由“转瓶生产”变更为“悬浮生产”/
——结束——。

国家三类新兽药———苦参功劳颗粒高艳艳;周德刚;郝洁;姚路路;杨会鲜;潘贵珍;李召斌;高富红【期刊名称】《兽药市场指南》【年(卷),期】2017(0)7【摘要】2017年05月03日,中华人民共和国农业部发布2526号公告,批准苦参功劳颗粒为国家三类新兽药,新兽药证书号:(2017)新兽药证字24号。
该新兽药由中国兽药药品监察所、洛阳惠中兽药有限公司等4家单位共同开发研制,是“国家十一五科技支撑计划项目子课题”后续成果。
一、研发背景大肠杆菌病是鸡群中普遍存在的传染病,发病率为11%-69%,死亡率为3.8%-72.9%,致死率为40.2%-90.3%,是危害养殖业健康发展的重要疾病。
近年来,随着细菌耐药性的出现和日趋严重,大肠杆菌耐药率高居首位,多地出现了多重、超强耐药菌株。
耐药性的存在使抗生素的疗效减弱,治疗费用增加,增加了治疗的难度与成本,给养殖业带来重大的经济损失。
【总页数】3页(P15-17)【关键词】三类新兽药;颗粒;苦参;中华人民共和国农业部;大肠杆菌病;细菌耐药性;中国兽药;计划项目;【作者】高艳艳;周德刚;郝洁;姚路路;杨会鲜;潘贵珍;李召斌;高富红【作者单位】洛阳惠中兽药有限公司;国家兽用药品工程技术研究中心【正文语种】中文【中图分类】S859.6【相关文献】1.国家三类新兽药治疗大肠杆菌病纯中药制剂苦参苍术口服液 [J], 无2.国家三类新兽药——马针颗粒 [J], 曹慧雅;邓菲;王艳艳3.国家三类新兽药——北芪五加颗粒 [J], 陈五常;赵留涛;魏红艳;韩志霞4.国家三类新兽药苦参功劳颗粒 [J], 高艳艳;周德刚;王勇;李永亮;亓俊杰5.国家三类新兽药苦参止痢颗粒 [J],因版权原因,仅展示原文概要,查看原文内容请购买。

内蒙古自治区农牧业厅关于下达2017年全区兽药质量监督抽检计划的通知正文:----------------------------------------------------------------------------------------------------------------------------------------------------关于下达2017年全区兽药质量监督抽检计划的通知内农牧医发〔2017〕54号各盟市、计划单列市农牧业局:为加强兽药质量监督抽检工作,规范和整顿兽药市场,打击制售假劣兽药的违法行为,提高我区兽药质量。
根据农业部《关于印发2017年兽药质量监督抽检计划的通知》(农医发〔2017〕2号)要求,本着“双随机一公开”原则,我厅制订了2017年全区兽药质量监督抽检计划,现将有关事宜通知如下。
一、抽样原则兽药质量监督抽检要遵循突出重点、科学合理、客观公正及“证据先行保存”的原则。
即重点抽检兽药生产经营问题较多、诚信较差企业的产品以及未赋二维码、未上传信息的产品;合理利用检验资源,减少信誉好、产品质量稳定企业的产品抽检比例,原则上对每个标称生产企业抽检累计不应超过15批次,加大对近年来没有实施抽检企业的产品抽检力度;客观公正体现在除抽检区外产品外,对我区兽药生产企业的产品也要实施抽检;“证据先行保存”主要是在抽样时,要将购进凭证复印或拍照,并核查记录备查。
二、抽样重点及数量兽药质量监督抽检实行“抓住大的,掌握小的”,即:重点从规模较大具有批发业务的兽药经营企业抽样;在小型零售企业少抽或不抽,但要了解、掌握小型零售企业的兽药产品购进来源。
(一)监督抽检。
近年来未被抽检的兽药生产企业产品以及进口兽药产品列入监督抽检范围,抽检不少于300批次,其中,我区兽药生产、经营、使用环节抽检分别为50、150、100批次。
(二)跟踪抽检。
将2017年度重点监控的兽药生产企业(附件1)、销售量大的企业、有被举报记录的企业产品列入跟踪抽检范围,抽检不少于300批次。

附件:关于发布《药物饲料添加剂品种目录及使用规范》的公告(征求意见稿)为加强药物饲料添加剂管理,进一步规范药物饲料添加剂使用,根据《兽药管理条例》规定,我部组织修订了《药物饲料添加剂品种目录及使用规范》 (附录1、附录2),现就有关事项公告如下:一、本公告收载的品种按照规定取得“兽药添字”产品批准文号或者《进口兽药注册证书》的,可作为药物饲料添加剂使用,并按照附录2 规定的使用规范执行。
公告收载品种的质量标准变更或者废止的,按照我部发布的同品种兽药质量标准或者有关废止、禁止性规定执行。
二、除本公告收载品种及我部批准的其他药物饲料添加剂外,饲料生产企业不得在饲料中添加其他兽药。
三、饲料生产企业应按照本公告规定使用药物饲料添加剂,禁止违反“添加量”规定,超量使用药物饲料添加剂;禁止违反“合用动物”规定,在其他动物饲料产品中使用药物饲料添加剂;禁止违反“注意事项”规定,生产不符合本公告要求的饲料产品。
四、饲料生产企业生产含有药物饲料添加剂的饲料的,在同一产品中添加的药物饲料添加剂不得超过3 种,且必须在饲料产品标签中标明所含全部药物饲料添加剂成份的通用名、含量、合用动物、休药期及使用注意事项等内容。
五、本公告自发布之日起执行。
原农牧发〔2001〕20 号、农业部公告第168 号和农业部公告第220 号同时废止。
附录11 二硝托胺预混剂2 土霉素钙预混剂3 山花黄芩提取物散4 马度米星铵预混剂5 甲基盐霉素尼卡巴嗪预混剂6 甲基盐霉素预混剂7 吉他霉素预混剂8 地克珠利预混剂9 亚甲基水杨酸杆菌肽预混剂10 那西肽预混剂11 杆菌肽锌预混剂12 阿维拉霉素预混剂13 金霉素预混剂14 盐酸氨丙啉乙氧酰胺苯甲酯预混剂15 盐酸氨丙啉乙氧酰胺苯甲酯磺胺喹噁啉预混剂16 盐酸氯苯胍预混剂17 盐霉素预混剂18 盐霉素钠预混剂19 莫能菌素预混剂20 恩拉霉素预混剂21 海南霉素钠预混剂22 黄霉素预混剂23 维吉尼亚霉素预混剂24 博落回散25 喹烯酮预混剂26 氯羟吡啶预混剂附录2药物饲料添加剂使用规范一、二硝托胺预混剂(Dinitolmide Premix)【执行标准】2022 年版《中国兽药典》【有效成份】二硝托胺【合用动物】鸡【作用与用途】抗球虫药。


农业部关于2017年第一期兽药质量监督抽检情况的通报文章属性•【制定机关】农业部(已撤销)•【公布日期】2017.04.19•【文号】农医发[2017]12号•【施行日期】2017.04.19•【效力等级】部门规范性文件•【时效性】现行有效•【主题分类】畜牧业正文农业部关于2017年第一期兽药质量监督抽检情况的通报农医发[2017]12号各省、自治区、直辖市畜牧兽医(农牧、农业)厅(局、委、办),新疆生产建设兵团畜牧兽医局:现将2016年第四季度兽药质量监督抽检情况通报如下。
一、基本情况(一)兽用生物制品抽检情况2016年第四季度共完成兽用生物制品监督抽检34批,合格33批,不合格1批(附件1),合格率97.1%。
(二)兽用化学药品、中兽药抽检情况2016年第四季度共完成兽用化学药品、中兽药监督抽检4754批,合格4567批,不合格187批(附件2、附件3),合格率96.1%,比2016年第三季度(96.0%)提高0.1个百分点,比2015年同期(95.9%)提高0.2个百分点。
其中,兽药监测抽检3859批,合格3721批,合格率96.4%;兽药跟踪抽检315批,合格296批,合格率94.0%;兽药定向抽检85批,合格82批,合格率96.5%;兽药鉴别抽检495批,合格468批,合格率94.5%。
从抽检环节看,生产环节抽检676批,合格653批,合格率96.6%,比2016年第三季度(98.0%)下降1.4个百分点;经营环节抽检3410批,合格3271批,合格率95.9%,比2016年第三季度(95.5%)提高0.4个百分点;使用环节抽检668批,合格643批,合格率96.3%,比2016年第三季度(96.4%)下降0.1个百分点。
从产品类别看,化药类产品共抽检1939批,合格1885批,合格率97.3%,比2016年第三季度(96.2%)提高1.1个百分点;抗生素类产品共抽检1698批,合格1646批,合格率96.9%,比2016年第三季度(97.3%)下降0.4个百分点;中药类产品共抽检1093批,合格1012批,合格率92.6%,比2016年第三季度(94.0%)下降1.4个百分点;其他类产品共抽检24批,合格24批,合格率100.0%。
中华人民共和国农业部公告第2503号——进口兽药注册目录正文:----------------------------------------------------------------------------------------------------------------------------------------------------中华人民共和国农业部公告第2503号根据《兽药管理条例》和《兽药注册办法》规定,经审核,批准保加利亚标伟特股份有限公司生产的黄霉素预混剂等7个兽药产品在我国再注册和变更注册,发布修订后的产品质量标准、说明书和标签,自发布之日起执行;并发布泰妙菌素的每日允许摄入量(ADI)和最高残留限量(MRLs)(试行)及其残留检测方法标准(试行),自发布之日起执行。
此前发布的同品种兽药质量标准、说明书和标签同时废止。
批准英特威国际有限公司生产的鸡新城疫、传染性法氏囊病二联灭活疫苗(Clone 30株+D78株)等7个兽药产品在我国变更注册。
特此公告。
附件:1.进口兽药注册目录2.质量标准(略)3.说明书和标签4.泰妙菌素的每日允许摄入量(ADI)和最高残留限量(MRLs)(试行)5.泰妙菌素残留检测方法标准(试行)农业部2017年3月14日进口兽药注册目录兽药名称生产厂名称国别进口兽药注册证书号有效期限备注黄霉素预混剂(100g:4g)Flavomycin Premix(100g:4g)保加利亚标伟特股份有限公司Biovet Joint Stock Company保加利亚(2017)外兽药证字12号2017.3.14-2022.3.13再注册黄霉素预混剂(100g:8g)Flavomycin Premix(100g:8g)(2017)外兽药证字13号2017.3.14-2022.3.13再注册延胡索酸泰妙菌素Tiamulin Fumarate瑞士诺华公司意大利Sandoz生产厂Sandoz Industrial Products S.P.A(2017)外兽药证字14号2017.3.14-2022.3.13变更注册:变更质量标准;再注册延胡索酸泰妙菌素可溶性粉Tiamulin Fumarate Soluble Powder奥地利Sandoz生产厂Sandoz GmbH奥地利(2017)外兽药证字15号2017.3.14-2022.3.13变更注册:变更质量标准;再注册延胡索酸泰妙菌素预混剂Tiamulin Fumarate Premix奥地利Sandoz生产厂Sandoz GmbH奥地利(2017)外兽药证字16号2017.3.14-2022.3.13变更注册:变更质量标准;再注册猪支原体肺炎复合佐剂灭活疫苗(P株)Swine Mycoplasma Hyopneumoniae Vaccine in Compound Adjuvant,Inactivated(Strain P)美国普泰克国际有限公司PROTATEK INTERNATIONAL,INC.(2017)外兽药证字17号2017.3.14-2022.3.13再注册鸡毒支原体活疫苗(MG 6/85株)Mycoplasma gallisepticum Vaccine,Live Culture(Strain MG 6/85)英特威美国分公司INTERVETINC.美国(2017)外兽药证字18号2017.3.14-2022.3.13再注册鸡新城疫、传染性法氏囊病二联灭活疫苗(Clone 30株+D78株)NewcastleDisease and Infectious Bursal Disease Vaccine, Inactivated (Strain Clone 30+Strain D78) 英特威国际有限公司Intervet International B.V.荷兰(2012)外兽药证字71号2012.12-2017.11变更注册:地址由“P.O. Box31, 5830 AA BOXMEER, The Netherlands”变更为“Wim de K?rverstraat35, 5831 AN Boxmeer, The Netherlands”鸡新城疫、传染性支气管炎二联灭活疫苗(Clone 30株+M41株)NewcastleDisease and Infectious Bronchitis Vaccine, Inactivated (Strain Clone 30+Strain M41) (2012)外兽药证字70号2012.12-2017.11鸡传染性法氏囊病灭活疫苗(D78株)Infectious Bursal Disease Vaccine, Inactivated (Strain D78)英特威国际有限公司Intervet International B.V.荷兰(2012)外兽药证字69号2012.12-2017.11变更注册:地址由“P.O. Box31, 5830 AA BOXMEER, The Netherlands”变更为“Wim de K?rverstraat35, 5831 AN Boxmeer, The Netherlands”猪萎缩性鼻炎灭活疫苗Swine Atrophic Rihitis Vaccine(2012)外兽药证字46号2012.08-2017.07猪胸膜肺炎放线杆菌亚单位灭活疫苗Porcine subunit Actinobacillus pleuropneumoniae vaccine, Inactivated(2012)外兽药证字43号2012.08-2017.07犬钩端螺旋体病(犬型、黄疸出血型)二价灭活疫苗Inactivated combined L.canicola and L.icterohaemorrhagiae Vaccine(2014)外兽药证字13号2014.03-2019.02犬、猫狂犬病灭活疫苗Canine and feline Rabies Vaccine, Inactivated (2012)外兽药证字49号2012.08-2017.07——结束——。
兽药是用于预防和治疗动物疾病的药物,其质量标准对于保障动物健康和人类食品安全具有重要意义。
2017年版的兽药质量标准生物制品卷是针对生物制品兽药的质量要求,本文将对其进行详细介绍。
一、主要内容2017年版兽药质量标准生物制品卷主要包括以下几个方面的内容:1. 通则包括了兽药生物制品的范围、应用范围、命名、分类、标志、保质期以及兽药生产企业的责任等内容。
2. 质量控制主要包括了兽药生物制品的质量要求、质量控制的一般原则、质量控制的基本要求、质量控制的技术要求、质量控制的检验方法等内容。
3. 药效学主要包括了兽药生物制品的药理学要求、药物代谢和药效动力学要求、药物致敏性评价、耐药性评价等内容。
4. 毒理学主要包括了兽药生物制品的急性毒性评价、慢性毒性评价、致突变性评价、致畸性评价、致致癌性评价等内容。
5. 病原学主要包括了兽药生物制品病原菌的鉴定、纯化、培养和保存要求、病原菌毒力评价、毒素的鉴定和纯化要求等内容。
6. 疫苗学主要包括了病原疫苗的免疫原性评价、免疫原的纯化要求、疫苗生产工艺要求等内容。
7. 血清学主要包括了兽用血清的免疫原性评价、血清的纯化要求、血清生产工艺要求等内容。
8. 分析学主要包括了兽药生物制品的分析方法、分析标准等内容。
二、更新与优化2017年版的兽药质量标准生物制品卷相较于之前的版本进行了更新与优化,主要体现在以下几个方面:1. 标准内容更加全面2017年版的标准内容更加全面,不仅对兽药生物制品的质量要求进行了详细的规定,还对质量控制、药效学、毒理学、病原学、疫苗学、血清学、分析学等方面进行了全面规定,使得标准更加完善。
2. 技术要求更加严格2017年版的标准在质量控制、药效学、毒理学、病原学、疫苗学、血清学等方面对技术要求进行了进一步严格,充分保障了兽药生物制品的质量和安全性。
3. 检验方法更加科学2017年版的标准对分析学方面的内容进行了补充和完善,对兽药生物制品的检验方法进行了进一步科学化,确保了检验结果的准确性和可靠性。
农业部办公厅关于2017年上半年畜禽及蜂产品兽药残留监控
计划检测结果的通报
【法规类别】兽医兽药
【发文字号】农办医[2017]30号
【发布部门】农业部
【发布日期】2017.09.01
【实施日期】2017.09.01
【时效性】现行有效
【效力级别】部门规范性文件
农业部办公厅关于2017年上半年畜禽及蜂产品兽药残留监控计划检测结果的通报
(农办医〔2017〕30号)
根据《兽药管理条例》规定和《农业部关于印发2017年动物及动物产品兽药残留监控计划的通知》(农医发〔2017〕1号),各地完成了2017年上半年畜禽及蜂产品兽药残留监控计划检测工作。
有关情况通报如下。
一、监控项目基本情况
2017年上半年共检测畜禽及蜂蜜产品兽药残留样品5075批,包括猪肝、猪肉、牛奶、牛肉、羊肉、鸡肝、鸡肉、鸡蛋、蜂产品,共9种;检测猪肝中的药物1类2种,猪肉8类42种,牛奶8类34种,牛肉4类10种,羊肉3类18种,鸡肝3类21种,鸡肉8类35种,鸡蛋4类13种,蜂蜜6类42种(具体兽药残留检测项目类别见附件)。
畜禽产
品采集样品来源覆盖除西藏以外的30个省、自治区、直辖市;蜂产品采集样品来源为2016年残留超标情况较为严重的四川、湖北和浙江等3个省份。
热点聚焦1一、《宠物用兽药说明书范本》(2512号公告)发布 2017年4月15日,宠物用兽药说明书范本发布,列入范本的183种兽药可以直接申报文号,取得文号的可直接生产。
缓解了我国宠物用兽药品种不足的情况。
二、《兽药质量标准(2017版)》(2513号公告)发布 新版《兽药质量标准》施行后,2010年12月31日前(含31日)各版《中国兽药典》《兽药国家标准》《兽用生物制品质量标准》《兽用生物制品规程》以及农业部公告发布的同品种兽药质量标准同时废止。
也就是说,2017年11月1日后,查看兽药标准,看2017版《兽药质量标准》和2015版《中国兽药典》就可以了。
三、《全国遏制动物源细菌耐药行动计划(2017—2020年)》发布 2017年6月22日,农业部发布《全国遏制动物源细菌耐药行动计划(2017—2020年)》。
计划提出五个目标,实施六个行动。
目标包括: 1.推进兽用抗菌药物规范化使用。
省(区、市)凭兽医处方销售兽用抗菌药物的比例达到50%。
2.推进兽用抗菌药物减量化使用。
人兽共用抗菌药物或易产生交叉耐药性的抗菌药物作为动物促生长剂逐步退出。
动物源主要细菌耐药率增长趋势得到有效控制。
3.优化兽用抗菌药物品种结构。
研发和推广安全高效低残留新兽药产品100个以上,淘汰高风险兽药产品100个以上。
畜禽水产品兽用抗菌药物残留监测合格率保持在97%以上。
4.完善兽用抗菌药物监测体系。
建立健全兽用抗菌药物应用和细菌耐药性监测技术标准和考核体系,形成覆盖全国、布局合理、运行顺畅的监测网络。
5.提升养殖环节科学用药水平。
结合大中专院校专业教育、新型职业农民培训和现代农业产业体系建设,对养殖一线兽医和养殖从业人员开展相关法律、技能宣传培训。
行动包括: “退出行动”推动促生长用抗菌药物逐步退出;“监管行动”强化兽用抗菌药物监督管理;“监测行动”健全动物源细菌耐药性监测体系;“监控行动”强化兽用抗菌药物残留监控;“示范行动”开展兽用抗菌药物使用减量化示范创建; “宣教行动”,加强从业人员培训和公众宣传教育 四、《兽用疫苗生产企业生物安全三级防护标准》发布 2017年8月31日,农业部发布《兽用疫苗生产企业生物安全三级防护标准》,自发布之日起实施。
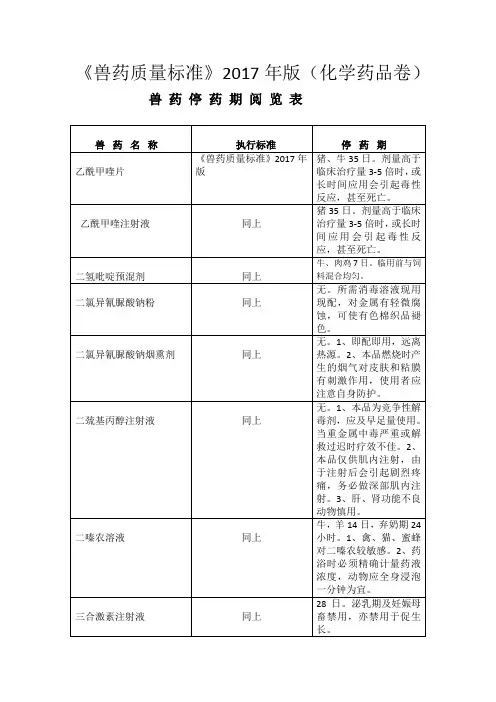
农业部公告第2513号――《兽药质量标准》(2017年版)
【法规类别】兽医兽药
【发文字号】农业部公告第2513号
【发布部门】农业部
【发布日期】2017.04.07
【实施日期】2017.11.01
【时效性】现行有效
【效力级别】部门规范性文件
农业部公告
(第2513号)
为加强兽药国家标准管理,我部对2010年12月31日前发布的、未列入《中国兽药典》(2015年版)的兽药质量标准进行了修订,编纂为《兽药质量标准》(2017年版),并制定了配套的说明书范本,现予发布,自2017年11月1日起施行。
现就有关事宜公告如下。
一、《兽药质量标准》(2017年版)包括化学药品卷、中药卷和生物制品卷等三个部分。
二、自2017年11月1日起,除《中国兽药典》(2015年版)和《兽药质量标准》(2017年版)收载品种的兽药质量标准外,2010年12月31日前(含31日)各版《中
国兽药典》《兽药国家标准》《兽用生物制品质量标准》《兽用生物制品规程》以及农业部公告发布的同品种兽药质量标准同时废止。
凡《兽药质量标准》(2017年版)品种项下未收载的制剂规格(已明令废止的除外),其质量标准按《兽药质量标准》(2017年版)同品种相关要求执行,规格项按原批准证明文件执行。
三、自2017年11月1日起,申报《兽药质量标准》(20。