[精品]2017-2018学年高中化学下学期《原电池》教学设计
- 格式:doc
- 大小:103.54 KB
- 文档页数:5

西南大学第七届师范生讲课比赛化学化工学院2014级化学师范二班黄小雪“原电池”教学设计一、教材分析本节课授课内容选自高中化学必修二第二章第二节“化学能与电能”第二课时“原电池”。
在高中化学中关于原电池的内容有两部分,分别是必修二第二章第二节(化学能与电能)以及选修四第四章第一节(原电池)。
本节课作为必修内容中的一部分,在高中的教材中具有承上启下的作用,它是对高一上册氧化还原,电子得失等知识综合运用的承接,也是对必修四中原电池,电解池知识学习的一个启发,同时为原电池的组成条件的后续学习做好铺垫。
二、学情分析本节课针对高一下册的学生,学生在必修一中已学习了氧化还原反应、电解质的基础等知识,对氧化还原反应的特征一一“反应中有电子的得失”有较好的认识;在初中物理中也学习了电学最基础的知识,在知识层次上达到了可以学习电化学的基础,在知识的理解掌握上也较容易掌握。
三、教学目标1、知识与技能:(1) 掌握原电池的本质,知道不同能量间可进行转化;(2) 初步掌握原电池工作原理;(3) 会判断原电池的正负极及原电池中电子的流向;(4) 初步掌握通过对比的方法来处理实验结果,由具体的实验现象形成抽象的结论。
2、过程与方法(1)通过回顾“火力发电”的过程,了解能量的一系列转化;⑵ 通过探究实验,模拟电池内部的工作情况,分析并归纳出原电池的工作原理;(3)通过对比实验,认识到原电池在化学能转变为电能过程中所起到的作用,加深对原电池的认识;3、情感态度与价值观(1)体会合作探究对于化学学习和进行化学科学研究的重要性;(2)充分理解“化学是一门以实验为基础的科学”,形成化学源于生活服务于生活的概念。
四、教学重难点重点:原电池的本质及工作原理难点:原电池的工作原理五、教学方法合作探究学习法讲授法实验演示法六、教学过程教学环节学生活动设计意图创设情境课程导入好了,同学们,我们准备上课了,上课前老师想问大家一个问题,同学们都有手机吧,说不定有的同学正盯着呢。

人教版高二年级化学选修4“原电池”教学设计刘勤勇学习任务3 寻找盐桥替代物评价任务3 进一步优化改进原电池,自主学习新知识,培养思维深刻性,发展诊断学生解决实际问题的能力和对化学价值的水平。
学生活动 设计意图3.练习巩固 学以致用学习任务4 完成练习,学以致用评价任务4 诊断并发展学生真实问题解决能力(孤立水平、系统水平) (2016浙江高考11题改编)金属(M )–空气电池(如图)具有原料易得、能量密度高等优点,有望成为新能源汽车和移动设备的电源。
该类电池放电的总反应方程式为:4M+nO 2 +2nH 2O=4M(OH)n 。
下列说法不正确的是____A .金属(M )电极是该电池的负极B .多孔电极上发生还原反应C .阴阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡D .在M –空气电池中,为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜4.获取信息,实践分析学习任务5 了解车用电池及工作原理,展望电池研究前景评价任务5 培养学生模型认知、科学态度与社会责任核心价值,发展科技转化为生产力的时候都会遇到问题,学生只有了解设计的前因后果,才能真正理解其中的化学原理。
学生在思考解决问题的时候体会化学是真实有用的。
小组合作,交流研讨分析寻找便捷有效的盐桥替代物,画出装置,进行分析化学学科价值的认识水平。
四、强化练习(2013江苏卷)Mg-H 2O 2电池可用于驱动无人驾驶的潜航器。
该电池以海水为电解质溶液,示意图如下。
该电池工作时,下列说法正确的是A .Mg 电极是该电池的正极B .H 2O 2在石墨电极上发生氧化反应C .石墨电极附近溶液的pH 增大D .溶液中Cl - 向正极移动八、板书设计原电池:化学能 电能低效,电流不稳 高效,电流稳定九、课后反思通过提供材料,探究实验,设计问题串、让学生实验探究、思考讨论,达到对有盐桥的原电池的工作原理的清晰的认识。
此时学生的思维活跃起来,最后再通过与单液原电池的实验现象的对比,让学生讨论两种装置的优缺点,这样也就让学生明白双液原电池的核心理念就是要让还原剂和氧化剂分开以提高能量转换效率。
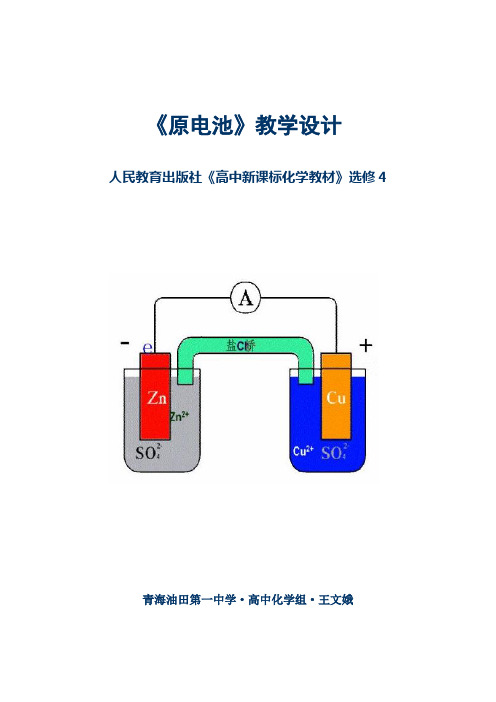
《原电池》教学设计人民教育出版社《高中新课标化学教材》选修4青海油田第一中学·高中化学组·王文娥《原电池》教学设计根据:人民教育出版社《高中新课标化学教材》选修4设计思想从“以学科为中心”向“以学习者为中心”转变,从“知识系统”向“多元能力”转化,鼓励学生在科学探究中提高能力,这是化学课程改革的趋势。
如何既能使学生成为学习的主体、课堂的主人,又能提高课堂教学的有效性和实效性?为了解决这些问题,本堂课我尝试采用布鲁纳的“发现--学习模式”。
首先围绕主干知识设计问题情境,在这个过程中发现问题,并提出解决问题的设想,再用实验进行验证,在这个过程中让学生产生问题体验过程。
最后对所学知识进行整合、应用。
在整个过程中激发学生思考的积极性,培养学生的情感,并内化为分析问题、解决问题的能力。
在教学内容的安排上,按照从易到难,从理论到实践再理论再进行实践的顺序,根据学生的知识结构、心理特点和教学内容的实际需要,采取了合作探究等教学方法,并采用多媒体进行教学。
教材分析1、教材内容:这节内容是以必修2第二章第二节《化学能与电能》为基础,是对必修2的加深与提高,在必修2中学生对原电池已有一定的了解,但很浅显,而选修4中则应使学生从微观层面对原电池和其原理有更深的认识和理解。
本节内容在必修2原电池的基础上新加入了盐桥,在原有知识的基础上起到一个承前启后的作用,盐桥不仅仅是普通实验技术的改进,而是对旧的思维模式的质的突破,这也为原电池原理的实用性开发奠定了理论基础。
2、教材前后联系:本节内容以化学必修2第二章第二节“化学能与电能”为基础,同时借助于氧化还原的知识进行学习,此乃承上。
作为第四章——电化学基础第一节的内容,原电池的原理在学生认识化学能与电能的转换以及了解电解池的知识的过程中起到了重要的引领作用。
此乃启下。
学情分析1、学生已有知识分析:学生在必修2中已经学习了化学能与热能的知识,对于把化学能转变为电能的原电池组成、原理等知识已非常熟悉。

-===Zn2+ 2e -===Cu 装置举例 第四章电化学基础第 一 节 原 电 池【教学目标】 1、理解原电池的工作原理和构成原电池的条件。
(重点)2、掌握原电池正、负极的判断及电极反应式的书写。
(难点)3、原电池原理的应用。
(重点)【教学重点、难点】1. 通过设计铜锌原电池两种方案的对比,加深原电池原理的理解。
(重点)2. 正确书写电极反应与电池反应方程式。
(难点)3. 会设计简单原电池。
(重点)【教学设计过程】一、单液原电池提问 1:复习原电池的定义。
提问 2:以铜、锌原电池为例,练习电极反应式书写和原电池的工作原理。
二、双液原电池提问 3:双液原电池的定义,原电池的构成条件。
1. 原理(以铜、锌原电池为例)原电池是利用氧化还原反应原理将化学能转化为电能的装置。
2. 电极反应锌片负极,发生氧化反应电极反应式:Zn -2e铜片正极,发生还原反应电极反应式:Cu2++ 总电极反应式为:Cu2++Zn===Cu +Zn2+3. 构成条件条件两个活泼性不同的电极,较活泼的做负极电解质溶液形成闭合回路能自发地发生氧化还原反应【思考与交流】:对比单液原电池和双液原电池的原理和优缺点。
三 原电池正、负极的判断方法 【问题导思】①原电池中,电子流出的极是正极还是负极?②若某电极在反应过程中增重,是原电池的正极还是负极?【小结】原电池正、负极的判断方法有哪些?1.由组成原电池的两极材料判断较活泼的金属为负极,较不活泼的金属或能导电的非金属为正极。
2.根据电流方向或电子流向判断外电路中,电流由正极流向负极,电子由负极流向正极。
3.根据原电池电解质溶液中离子的移动方向判断在原电池电解质溶液中,阳离子移向正极,阴离子移向负极。
4.根据原电池中两极发生的反应判断原电池中,负极总是发生氧化反应,正极总是发生还原反应。
若给出一个总方程式,则可根据化合价升降来判断。
5.根据电极质量的变化判断原电池工作后,某一电极质量增加,说明溶液中的阳离子在该电极上放电,该极为正极,活泼性较弱;反之,如果某一电极质量减轻,则该电极溶解,为负极,活泼性较强。

-===Zn2+ 2e -===Cu 装置举例 第四章电化学基础第 一 节 原 电 池【教学目标】 1、理解原电池的工作原理和构成原电池的条件。
(重点)2、掌握原电池正、负极的判断及电极反应式的书写。
(难点)3、原电池原理的应用。
(重点)【教学重点、难点】1. 通过设计铜锌原电池两种方案的对比,加深原电池原理的理解。
(重点)2. 正确书写电极反应与电池反应方程式。
(难点)3. 会设计简单原电池。
(重点)【教学设计过程】一、单液原电池提问 1:复习原电池的定义。
提问 2:以铜、锌原电池为例,练习电极反应式书写和原电池的工作原理。
二、双液原电池提问 3:双液原电池的定义,原电池的构成条件。
1. 原理(以铜、锌原电池为例)原电池是利用氧化还原反应原理将化学能转化为电能的装置。
2. 电极反应锌片负极,发生氧化反应电极反应式:Zn -2e铜片正极,发生还原反应电极反应式:Cu2++ 总电极反应式为:Cu2++Zn===Cu +Zn2+3. 构成条件条件两个活泼性不同的电极,较活泼的做负极电解质溶液形成闭合回路能自发地发生氧化还原反应【思考与交流】:对比单液原电池和双液原电池的原理和优缺点。
三 原电池正、负极的判断方法 【问题导思】①原电池中,电子流出的极是正极还是负极?②若某电极在反应过程中增重,是原电池的正极还是负极?【小结】原电池正、负极的判断方法有哪些?1.由组成原电池的两极材料判断较活泼的金属为负极,较不活泼的金属或能导电的非金属为正极。
2.根据电流方向或电子流向判断外电路中,电流由正极流向负极,电子由负极流向正极。
3.根据原电池电解质溶液中离子的移动方向判断在原电池电解质溶液中,阳离子移向正极,阴离子移向负极。
4.根据原电池中两极发生的反应判断原电池中,负极总是发生氧化反应,正极总是发生还原反应。
若给出一个总方程式,则可根据化合价升降来判断。
5.根据电极质量的变化判断原电池工作后,某一电极质量增加,说明溶液中的阳离子在该电极上放电,该极为正极,活泼性较弱;反之,如果某一电极质量减轻,则该电极溶解,为负极,活泼性较强。

高中化学必修二《原电池》教案一、探究目标体验化学能与电能相互转化的探究过程二、探究重点初步认识原电池概念、原理、组成及应用。
三、探究难点通过对原电池实验的研究,引导学生从电子转移角度理解化学能向电能转化的本质,以及这种转化的综合利用价值。
四、教学过程【引入】电能是现代社会中应用最广泛,使用最方便、污染最小的一种二次能源,又称电力。
例如,日常生活中使用的手提电脑、手机、相机、摄像机……这一切都依赖于电池的应用。
那么,电池是怎样把化学能转变为电能的呢?我们这节课来一起复习一下有关原电池的相关内容。
【板书】4.1原电池一、原电池实验探究讲:铜片、锌片、硫*都是同学们很熟悉的物质,利用这三种物质我们再现了1799年意大利物理学家----伏打留给我们的历史闪光点!【实验探究】(铜锌原电池)实验步骤现象1、锌片*入稀硫*2、铜片*入稀硫*3、锌片和铜片上端连接在一起*入稀硫*【问题探究】1、锌片和铜片分别*入稀硫*中有什么现象发生?2、锌片和铜片用导线连接后*入稀硫*中,现象又怎样?为什么?3、锌片的质量有无变化?溶液中c(H+)如何变化?4、锌片和铜片上变化的反应式怎样书写?5、电子流动的方向如何?讲:我们发现检流计指针偏转,说明产生了电流,这样的装置架起了化学能转化为电能的桥梁,这就是生活中提供电能的所有电池的开山鼻祖----原电池。
【板书】(1)原电池概念:学能转化为电能的装置叫做原电池。
问:在原电池装置中只能发生怎样的化学变化?学生:Zn+2H+=Zn2++H2↑讲:为什么会产生电流呢?答:其实锌和稀硫*反应是氧化还原反应,有电子的转移,但氧化剂和还原剂热运动相遇发生有效碰撞电子转移时,由于分子热运动无一定的方向,因此电子转移不会形成电流,而通常以热能的形式表现出来,激烈的时候还伴随有光、声等其他的形式的能量。
显然从理论上讲,一个能自发进行的氧化还原反应,若能设法使氧化与还原分开进行,让电子的不规则转移变成定向移动,便能形成电流。
原电池教案(优秀3篇)(经典版)编制人:__________________审核人:__________________审批人:__________________编制单位:__________________编制时间:____年____月____日序言下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!并且,本店铺为大家提供各种类型的经典范文,如工作资料、求职资料、报告大全、方案大全、合同协议、条据文书、教学资料、教案设计、作文大全、其他范文等等,想了解不同范文格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor. I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you!In addition, this shop provides you with various types of classic model essays, such as work materials, job search materials, report encyclopedia, scheme encyclopedia, contract agreements, documents, teaching materials, teaching plan design, composition encyclopedia, other model essays, etc. if you want to understand different model essay formats and writing methods, please pay attention!原电池教案(优秀3篇)在教学工作者开展教学活动前,就不得不需要编写教学设计,借助教学设计可以更好地组织教学活动。
原电池教案(优秀6篇)高中化学必修二《原电池》教案篇一【教学目标】1、掌握原电池的构成条件,理解原电池的原理,能正确判断原电池的正负极,正确书写电极反应式、电池反应式,能根据氧化还原原理设计简单的原电池。
2、通过实验探究,体验科学探究的方法,学会分析和设计典型的原电池,提高实验设计、搜索信息、分析现象、发现本质和总结规律的。
3、在自主探究、合作交流中感受学习快乐和喜悦,增强学习的反思和自我评价能力,激发科学探索,培养科学态度和创新精神,强化环境保护意识以及事物间普遍联系、辨证统一的哲学观念。
【教学重点】原电池的构成条件【教学难点】原电池原理的理解;电极反应式的书写【教学手段】多媒体教学,学生实验与演示实验相结合【教学方法】实验探究教学法【课前准备】将学生分成几个实验小组,准备原电池实验仪器及用品。
实验用品有:金属丝、电流表、金属片、水果。
先将各组水果处理:A组:未成熟的橘子(瓣膜较厚),B组:成熟的橘子(将瓣膜、液泡搅碎),C组:准备两种相同金属片,D组:准备两种不同金属片。
【教学过程】[师]:课前我们先作个有趣的实验。
请大家根据实验台上的仪器和药品组装:将金属片用导线连接后插入水果中,将电流表串联入线路中,观察会有什么现象发生?(巡视各组实验情况)。
[师]:请大家总结:有什么现象发生?[生]:总结:出现两种结果:①电流表指针偏转②电流表指针不发生偏转[师]:电流表指针偏转说明什么?为什么会发生偏转?[生]:说明有电流产生。
[师]:这个装置就叫做原电池。
这节课我们共同研究原电池。
请大家列举日常使用的原电池都有哪些?[展示干电池]:我们日常使用的电池有下面几种,大家请看:[播放幻灯片]:化学电池按工作性质可分为:一次电池(原电池);二次电池(可充电电池)铅酸蓄电池。
其中:一次电池可分为:糊式锌锰电池、纸板锌锰电池、碱性锌锰电池、扣式锌银电池、扣式锂锰电池、扣式锌锰电池、锌空气电池、一次锂锰电池等。
《原电池》教学设计(节选自必修二第二章第二节:化学能与电能)教学流程图:演示实验讲解原电池工作原理演示实验判断原电池正负极方法教学过程:教师活动学生活动设计意图【引入】通过格林太太的故事,病症,引出原电池课题。
问题与思考:格林太太的病因是什么能为她开个处方吗引入课题,激发学生学习的兴趣。
【实验探究一】将一锌片、铜片平行插入稀硫酸中。
【问题讨论一】我们可观察到什么现象说明了什么问题Zn + 2H+ = Zn2+ H2↑【实验探究二】在实验一的基础上用一根导线将铜片和锌片连接起来【问题讨论二】我们又观察到什么现象铜片上的气泡可能是什么气体H元素原来是以什么形式存在的从氢离子到氢气,氢离子是得到电子还是失去电子得到的电子是谁失去的锌失去的电子是怎样转移到铜片上去的怎么验证你的猜想观察实验现象,回答问题。
仔细观察实验现象,回答问题。
通过实验,观察,思考,发现问题,解决问题。
锻炼学生的分析推理能力。
【实验探究三】在实验二的基础上,在导线中接入一电流计【问题讨论三】仔细观察电流计指针有什么变化探究问题的过程:发现问题提出猜想验证猜想得出结论观察实验现象,得出实验结论。
H2SO4通过实验验证理论猜测。
CuZnH2SO4新课导入(故事导入)学生分组实验探究原电池构成条件单点学生回答是否构成原电池练习两名学生上台设计简单原电池分小组讨论设计水果电池两名学生上台制作水果电池下台展示成果课堂练习小结布置作业板书设计:原电池1、原电池的定义:将化学能转变为电能的装置叫做原电池。
装置图:电极电极反应反应类型正极Cu 2H++2e-= H2↑ 还原反应负极Zn Zn-2e-= Zn2+氧化反应2、原电池的构成条件:①有两种活动性不同的金属(或一种是非金属导体)作电极②电极材料均插入电解质溶液中(能自发进行氧化还原反应)③两极相连形成闭合电路教学设计反思:1、课堂开始利用故事导入,吸引学生注意;2、录播室无投影设备,让第一排学生到讲台两边观察演示实验,并借用物理学科演示电流表,使得实验现象更好地展示出来;3、分组实验,培养学生的实验操作能力,透过实验现象分析、归纳的能力;4、分小组讨论,培养学生沟通交流的能力,让学生上台制作水果电池,培养学生动手实践能力,并将制作成果下台展示给同学观看,通过水果电池实践活动激发学生对化学学科的学习兴趣和成就感。