电镀镀锡液配制(开缸)及分析方法
- 格式:pdf
- 大小:151.86 KB
- 文档页数:3

1、目的:通过分析对电镀液中各种药水的含量检测。
规范药水分析方法并让所有相关人员了解。
2、适用范围:镀银线电镀所有药水3、相关文件:《分析补充量表》《现场药水维护》4、相关权责:镀银生产线所有人员及相关人员.5. 标准液配制5。
1 0.1N Na0H标准液:取氢氧化钠4g加纯水至1L。
5.2 0.2N Na0H标准液:取氢氧化钠8g加纯水至1L。
5.3 0。
1NAgNO3标准液:取AgNO317g加纯水至1L。
5.4 0.1M EDTA—2Na标准溶液:取乙二胺四乙酸二钠37.24g加纯水至1L。
5.5 0.1N NH4SCN标准溶液:秤取8.0g NH4SCN固体试,加纯水溶解,稀释至1L再标定之.(或购浓缩液Twenty—two points, plustriple-word-score, plus fifty points for usingall my letters。
Game's over。
I’m outta here。
标准稀释之)。
5。
6 0.1碘液:12。
69g碘(I2)+40g碘化钾(KI)+2~3滴HCL配成1L。
5.7 0。
1Na2S2O3标准液:取硫代硫酸钠24。
8g加纯水至1L.6. 指示剂配制6.1 1% pp指示剂:取1.0g pp粉末,加入99cc酒精溶解均匀.6。
2 5% K2CO4溶液:秤取5g K2CO4 粉末,加95cc纯水溶解稀释黄色.6。
3 p-sorbital C6H8 (OH)6甘露醇液:100纯水配至500m.6。
4 0.1%PNA指示剂:1-(2pyridyld-920)-2-Naphthol:秤取0。
1g PAN粉末溶解100cc酒精中.6。
5 10%碘化钾(KI)溶液:秤取10g KI固体试加纯水溶解,并稀释成100cc.6.6 1%酚钛指示剂:1gpp粉未加洒精至100ml.6。
7 1%甲基橙指示剂:取1g甲基橙加洒精至100 cc .6.8 10%碘化钾(KI)溶液:秤取10g KI固体试加纯水溶解,并稀释成100cc。

电镀液配方分析电镀液配方分析密度包括质量密度和相对密度。
质量密度是指物质单位体积的质量。
它与物体的体积和质量之间的关系可以用下式表示:Ρ=(2-3-1)式中ρ—质量密度(g/cm3或kg/dm3)m—物质的质量(g或kg)v—物质的体积(cm3或dm3,其单位与质量单位相对应)。
相对密度是指在共同的特定条件下,第一物质的质量密度ρ1与第二物质的质量密度ρ2之比,常用d表示:d=(2-3-2)因此,只要知道了物质的质量密度就可根据式(2-3-2)求得。
同时,也可根据式(2-3-1),求算物质的质量或体积。
这样对一些液体试剂,尤其是有腐蚀性的试剂,如在电镀中常用的浓硝酸、浓硫酸、浓盐酸等,因称量的质量和起质量密度,计算出相应体积,然后再量取一定体积的该试剂。
这样操作简捷快速,可减少对设备的腐蚀。
[例1]要配制25g/L的硫酸溶液50L,问应量取质量密度为1.84g/cm3、质量分数浓度为98%的浓硫酸多少体积?解:要求欲量取的体积,首先计算所需浓硫酸的质量m,m=25g/L×50L×1/0.98=1275.5g 根据式(2-3-1),v===693.2cm3l只要用量筒量取693.2ml浓硫酸,用水稀释至50L即可。
由上可知,要进行质量与体积的折算,首先需知液体的质量密度,而液体的质量密度可以由密度计直接测得。
质量密度测量密度计是一个封闭严密的玻璃管,管的上端一段细长,中间一段胶粗,下端有一个装着水银或者铅粒的玻璃泡。
因为其重心靠近下端,所以能竖直地浮在液体内。
上部的细长筒内附有纸做的刻度尺,液面所对应的标尺上的数字就是该溶液的质量密度和相应的波美度值。
把密度计放在密度不同的液体内,它沉入的深度不同。
液体的密度越大,密度计沉入的深度越小,这种下沉深度的大小与密度有一定的反比关系,因而密度计上的刻度可直接指示液体密度,使用起来很方便。
在生产中,有时用波美度(O Be’)来表示密度。

钯水(PdCl2,SnCl2,HCl)PdCl2用分光光度计进行分析参比液:取300ml 浓盐酸加3g 氯化亚锡,摇匀,用水定容至1L待测液:缸液波长:440NM浓度:参照化验室“钯水浓度与吸光度对照图”SnCl2准确移取5ml 缸液于250ml 锥形瓶中,再加100ml 水摇匀,再加1:1 盐酸50ml,1%淀粉指示剂约2ml,用0.1N I2 标准溶液滴定至蓝色为终点(蓝色半分钟内不消失)SnCl2(g/L)=2.256VHCl准确移取缸液1ml 于250ml 锥形瓶中,加纯水50ml,加酚酞指示剂2-3滴,以0.2N 标准氢氧化钠溶液滴定至溶液呈红色即终点。
HCl(g/L)=16.73V活化硫酸(H2SO4)准确移取缸液2ml 于250ml 锥形瓶中,加纯水50ml,加酚酞指示剂2-3滴,以0.2N 标准氢氧化钠溶液滴定至溶液呈红色即终点H2SO4(g/L)=4.9V化学镍(NiSO4 NaH2PO2 Na3Cit<柠檬酸钠> NH4Cl NaHPO3)NiSO4准确移取缸液5ml 于250ml 锥形瓶中,加纯水50ml,加1:1 氨水,紫尿酸胺少许,以0.05M 标准EDTA 溶液滴定至溶液呈兰紫色即为终点NiSO4(g/L)=2.6275VNaH2PO2移取缸液2ml 于250ml 碘量瓶中,加12N 硫酸10ml,0.1N 标准碘溶液25ml,盖上瓶塞,放暗处3min,以0.1N 标准硫代硫酸钠溶液滴定至溶液呈淡蓝色,加1%淀粉指示剂2-3ml,继续滴定至溶液淡蓝色消失1min即终点H2PO2(g/L)=26.5(25N1-N2V2)N1=标准碘溶液的当量浓度N2=标准硫代硫酸钠溶液的当量浓度Na3Cit<柠檬酸钠>准确移取缸液2ml 于250ml 容量瓶中,定容,取此溶液10ml 与250ml锥形瓶中,加纯水50ml,12N 硫酸5ml,硫酸锰1g,加热至70℃,搅拌下缓缓加入0.1N 标准高锰酸钾溶液25ml,在70℃下放置15-20min,用水冷却,加碘化钾2g,以0.1N 硫代硫酸钠溶液滴定至溶液呈淡黄色,加1%淀粉指示剂2-3ml,继续滴至蓝色消失1min 即终点Na3Cit(g/L)=5000T[25-(KV)]-0.67(NaH2PO2-15)K 值:准确移取0.1N 标准高锰酸钾溶液25ml 于250ml 锥形瓶中,加6N硫酸10ml,硫酸锰1g,碘化钾2g,摇匀,以0.1N 标准硫代硫酸钠溶液滴至淡黄色,加1%淀粉指示剂2-3ml,继续滴至蓝色消失1min 即终点。

电镀过程电镀液的配置和电镀液的简单原理
一、镀液配制
(1)分别把计算量的氰化钠和氢氧化钠溶解好。
(2)将计算量的氧化锌调成糊状,在搅拌下加人氰化钠溶液中去,待氧化锌络合溶解完全后,慢慢倒入氢氧化钠溶液中,加水至所需体积。
(3)如果不用氧化锌而用氰化锌,溶解方法一样。
然后加人计算量的光亮剂或添加剂。
把溶液搅匀,静置澄清,边电镀边试镀。
不过一般来讲深圳电镀厂都是用的氰化锌。
二、镀液简单原理
在氰化物镀液中,锌离子与氰化钠及氢氧化钠均形成络合物即锌氰化钠及锌酸钠。
电镀时发生以下反应:
1.阴极过程
锌氰化钠通过两步离解,离解出锌离子。
锌酸钠也通过两步离解,离解出锌离子。
通电时,锌离子在阴极上吸收电子而沉积出锌。
2.阳极过程
电解时,阳极上发生锌的溶解
继而生成络合盐。
阳极上也有少量氧气析出。
以上就是电镀液的原理。
(本文由立信顺电镀厂整理发布)。


电镀液配方与制作电镀液是一种用于将金属物体表面镀上一层金属膜的溶液。
电镀可以改善金属物体的外观、增加硬度、防腐蚀和提高导电性。
电镀液的配方和制作根据所需镀层的材料和要求不同而有所差异。
下面是一种常见的电镀液配方和制作过程。
配方:1.镀铬液配方:-水:1000mL-枪金属二硫代硫酸钠:40g-三氯化铬:2g-四氯化钛:0.2g-硫酸铜:0.3g-异丙醇:20mL2.镀铜液配方:-水:500mL-硫酸铜:150g-硫酸:5mL-次亚氯酸钠:25g3.镀金液配方:-水:500mL-金氯化物:0.5g-鱼鳞酸钠:1g-硫酸铜:0.5g制作过程:1.将所需的化学品准备好,并按照配方的比例称量。
2.将一定量的水倒入容器中,加热至适当的温度,通常为50-70°C。
3.将枪金属二硫代硫酸钠、三氯化铬、四氯化钛、硫酸铜等化学品分别加入水中,搅拌均匀直至化学品完全溶解。
4.在搅拌的同时,逐渐添加异丙醇,继续搅拌,直至溶液均匀。
5.镀铬液制作完成后,将溶液过滤,去除悬浮固体颗粒,保证溶液的纯净度。
6.对于镀铜液和镀金液,也是通过将化学品逐一加入水中,搅拌均匀溶解。
但是需要注意的是,在制备镀金液时,金氯化物必须小心加入,以防止氯化物的挥发和损失。
7.由于电镀液中的化学品大多具有一定的危险性,因此在制作过程中,应该遵守相关的安全操作规程,如佩戴防护手套和眼镜。
以上是一种电镀液配方和制作过程的简单介绍。
实际上,电镀液的配方非常多样化,不同的金属、不同的应用目的会使用不同的配方。
在制作电镀液时,应根据具体需求选择合适的配方,并严格按照生产操作规程进行制作。
同时,应注意安全操作,避免接触有害化学品对人身和环境造成伤害。
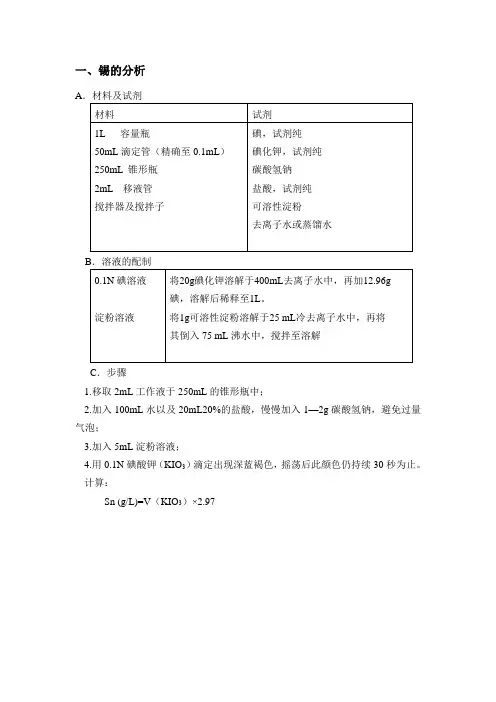
一、锡的分析AC.步骤1.移取2mL工作液于250mL的锥形瓶中;2.加入100mL水以及20mL20%的盐酸,慢慢加入1—2g碳酸氢钠,避免过量气泡;3.加入5mL淀粉溶液;4.用0.1N碘酸钾(KIO3)滴定出现深蓝褐色,摇荡后此颜色仍持续30秒为止。
计算:Sn (g/L)=V(KIO3)×2.97二、ASSB A-70 ACID CONC. 的分析用氢氧化钠滴定法分析酸浓度。
起初时pH值变化很小,当pH值约为2.2时,随着氢氧化钠溶液的滴加,pH 值将有明显的增加。
硫酸钠用于抗铅离子的干扰。
(注:建议先用此方法分析已知浓度的样品。
)A.材料及试剂B.步骤:1.移取5mL 工作液于250mL 的烧杯中,加20mL15%硫酸钠溶液,混合均匀;2.加去离子水至100 mL;3.边搅拌,边用1N 氢氧化钠标准液滴定至pH 值至1.8~2.0;4.用去离子水冲洗杯壁;5.继续以每次0.2 mL 的量追加氢氧化钠标准液,每次追加后冲洗烧杯,并记录pH 值;6.因金属含量不同,终点应在pH值为2.2~2.8之间。
取每追加0.2mL氢氧化钠标准液后pH值变化最大的点为终点。
计算:ASSB A-70 ACID CONC(mL/L)= N(NaOH)×NaOH的毫升数×20.8三、ASSB-753 R的分析ASSB-753 R是以氯甲烷萃取出镀液的润湿剂成分来进行分析的。
萃取液与水溶性络合剂反应成蓝色,测量分离出的蓝色氯甲烷层在620nm 的吸收值。
以已知浓度的镀液制出校正曲线,工作液的ASSB-753 R便可从校正曲线上确定。
该颜色有2小时的稳定期。
A.材料及试剂B.标准和空白溶液配制配制含5、7、10mL ASSB-753 R 的标准液各100mL(相当于50、70、100mL/L 的ASSB-753 R 的溶液)。
标准液中的金属浓度应与工作液中的浓度相同。
标准液成份如下:注意:硫氰化铵的溶解性极强,且会使用溶液体积增大,故最初时切忌加水过量。

金属电镀:电镀锡酸性镀锡工艺配方l 酸性光亮镀锡硫酸亚锡l8.00—35.00g/L硫酸(相对密度l.84)40.00—80.00mL酒石酸8.00—16.00g/L无机盐0.05—0.10g/L抗坏血酸l.00—2.00g/L琥珀酸0.20—0.40g/L水加至1.00L工艺条件:温度为室温,电流密度0.3∼0.5A/dm2,时间3—5min。
配方2甲酚磺酸镀锡液硫酸亚锡60g/L硫酸60g/Lβ一萘酚1g/L明胶2g/L甲酚磺酸75mL水加至1L锡是无毒金属,因此,在罐头工业用作马口铁的防腐层,而且一些盛放食品的铜制容器也常用镀锡层来保护。
锡的可焊性好,在空气中几乎不变色,几乎不与硫化物反应,因此铜引线、焊片、与火药和橡胶接触的零件常采用锡。
但在某种条件下易发生电路短路,所以电子元件使用锡镀层应十分小心,需采取必要措施。
本配方工艺成分简单,操作容易,成本低,但它的镀层粗糙、孔隙多、抗蚀性差,镀后要经过软熔处理。
本配方适用于滚镀和挂镀。
明胶应先在冷水中浸泡几小时再溶解在沸水中。
萘酚先溶解在少量硝酸中。
软熔:可用热油浸锡法,使镀层光亮致密。
油的温度应在250∼265℃。
时间2—10s。
软熔后应立即在煤油中冷却,以免产生雾状膜。
配方3氟硼酸镀锡(一)氟硼酸亚锡100(100∼400)g/LSn2+80(40∼160)g/L氟硼酸100(50∼250)g/L明胶6g/Lβ一萘酚l(0.5∼1.0)g/L工艺条件:温度20℃(15—40℃),阴极电流密度,挂镀为3A/dm2(2.5—12.5A/dm2),滚镀为lA/dm2;极限电流密度,20℃无搅拌为25A/dm2,40℃无搅拌为45A/dm2。
注:括号内数据为适用范围,括号外数据为最佳,后同。
本配方电流密度范围宽,沉积速度快,耗电量少,镀层细致、光亮,分散能力好,但成本高。
配方4氟硼酸镀锡(二)氟硼酸亚锡50(40∼60)g/LSn2+20(15∼25)g/L氟硼酸100(80∼120)g/L甲醛(37%)5(3∼8)g/L光亮剂20(15∼30)g/L分散剂(烷基酚聚氧乙烯醚)20(8∼140)g/L工艺条件:温度20℃(10—25℃),阴极电流密度,挂镀为4.2A/dm2(0.5—5.0 A/dm2),滚镀为l—10A/dm2,阴极移动速度1.5m/min(1∼2m/min)。

电镀锌镀液配制镀液的配制(以lL为例):⑴在镀槽内先加入1/3体积的纯净水;⑵用1/3的纯水溶解氢氧化钠(溶解时会发热,必须小心);⑶用少量的水将氧化锌调成糊状,然后加入较多的纯水,充分搅拌。
将搅拌好的氧化锌慢慢加入到溶解好的氢氧化钠溶液中,边加边搅拌,使其充分络合后加入到镀槽中;⑷当镀液温度降至30~C以下后,加入85g的Baser,充分搅拌;⑸将15mL BaseF溶解在15g BaseR中,然后将其混合物加入镀槽;⑹加入4mL的H—O624,充分搅拌;加水至所配体积;⑺加入光亮剂ZF-105A、ZF-105B;充分搅拌。
黑色钝化工艺流程:水洗→出光→水洗→黑色钝化→水洗→后处理→干燥。
影响因素⑴锌含量的影响锌含量太高,光亮范围窄,容易获得厚的镀层,镀层中铁含量降低;锌含量太低,光亮范围宽,要达到所需的厚度需要较长的时间,镀层中铁含量高。
⑵氢氧化钠的影响氢氧化钠含量太高时,高温操作容易烧焦;氢氧化钠含量太低时,分散能力差。
⑶铁含量的影响铁含量太高,镀层中铁含量高,钝化膜不亮;铁含量太低,镀层中铁含量低,耐蚀性降低,颜色偏橄榄色。
⑷光亮剂的影响ZF-IOOA太高,镀层脆性大;太低,低电流区域无镀层,钝化颜色不均匀;ZF一100B 太高,镀层脆性大;太低,整个镀层不亮。
⑸温度的影响温度太高,分散能力下降,镀层中铁含量高,耐蚀性降低,钝化膜颜色不均匀,发花;温度太低,高电流密度区烧焦,镀层脆性大,沉积速度慢。
⑹阴极移动的影响必须采用阴极移动。
移动太快,高电流密度区镀层粗糙;太慢,可能产生气流,局部无镀层。
电镀锌目的是为了防止钢铁类物体被腐蚀,提高钢铁的耐蚀性及使用寿命,同时也使产品增加装饰性的外观,钢铁随着时间的增长会被风化,水或泥土腐蚀。
国内每年被腐蚀的钢铁差不多占整个钢铁量的十分之一,所以,为了保护钢铁或其零件的使用寿命,一般都采用电镀锌来将钢铁加工处理。
由于锌在干燥空气中不易变化,而且在潮湿的环境下更能产生一种碱式碳酸锌薄膜,这种薄膜就能保护好内部零件而不被腐蚀损坏,即使锌层被某种因素破坏的情况下,锌和钢经过一段时间结合会形成一种微电池,而使钢基体成为阴极而受到保护。

白铜锡镀液分析方法A金属铜(Cu)分析步骤1 抽取镀液2ml于250毫升之三角锥瓶。
2 加50ml纯水,加1.5克左右过硫酸铵,后摇匀,加热至沸腾。
3 冷却后,加10ml 1:1氨水至深蓝色。
4 加100ml纯水,加PAN指示剂5滴。
5 以0.1mol EDTA标准溶液滴定,由蓝色变绿色为终点。
计算:金属铜(克/升)= 所用0.1mol EDTA滴定毫升数×3.18B金属锡(Sn)分析步骤1 取镀液1ml于250ml三角锥瓶中,加入30ml纯水。
2 加入1:1盐酸8ml加热至白色沉淀消失,并煮沸1分钟。
3 加入7~8滴浓硝酸,煮沸1分钟;4. 加8ml10%氯化钾溶液、加10ml 0.1molmolEDTA ,煮沸1分钟。
4 冷却后加入50ml 30%六次甲基四胺溶液,加入二甲酚橙指示剂5滴,此时溶液为绿色,用0.05mol硝酸铅(Pb(NO3)2)滴定至由绿色变化为蓝色或紫色,不计体积。
5 加入氟化铵(NH4F)1克,静置15分钟,此时溶液变为绿色。
用0.05mol 硝酸铅(Pb(NO3)2),滴定至由绿色变为蓝色或紫色,记录读数。
计算:金属锡(克/升)=5.935×0.05mol硝酸铅(Pb(NO3)2)所滴定的毫升数C金属锌(Zn)分析步骤1 取镀液5ml,2 加100ml纯水,10ml PH=10缓冲溶液3 加抗坏血酸0.5克4 加0.5克EBT指示剂(铬黑T)5 加15ml 10%甲醛6 以0.1mol EDTA标准溶液滴定,由红色刚呈蓝色.计算:金属锌(克/升)=0.1mol EDTA滴定毫升数а×0.65D游离氰(Free CN)---------氢氧化钾(KOH)分析步骤1 抽取1ml镀液,;2 加50ml纯水;3 加10ml 10%碘化钾;4 以0.1mol硝酸银标准溶液滴定溶液,由透明变刚呈混浊为终点,记录V1;5. 过量1ml硝酸银;6 加30%氯化钡30ml,加酚酞指示剂4滴,用0.1N盐酸滴定至蓝色消失为终点,记录体积V2。

Zhejiang Haining Rongxin Electronics Co., Ltd.地址/Add:浙江海宁对外综合开发区之江路邮编/PC:314423电话/TEL:86-573-87966368传真/FAX:86-573-87966326网址/Website: Email: rongxin@镀锡槽液配制及镀液分析化验方法一、设备:1、镀槽---PVC或PE材质2、过滤系统(耐酸材料)。
3、冷却系统(铁氟龙被覆管)。
二、槽液备制:以配制100升标准的RX-770/780光亮纯锡镀液为例:1、加入60升去离子水;2、在连续搅拌的情况下缓慢加入计量硫酸9L,注意此时有放热现象,充分搅拌均匀,注意安全;3、在连续搅拌的情况下缓慢加入计量硫酸亚锡2.5kg-3kg(建议为2.5kg,因为亚锡会随着电镀的进行而增加)。
4、冷却至室温时(30℃左右)加入RX-770开缸剂600ml,RX-780光亮剂150ml。
5、补加去离子水到所需液面高度,充分搅拌均匀后可进行试镀。
三、硫酸镀锡液分析方法1、硫酸亚锡(SnSO4)A药品:A-1.稀盐酸(6N):浓盐酸和水比例1:1。
A-2.淀粉指示剂:可溶性淀粉1g,溶解于沸腾水中至100ml。
再沸腾一分钟。
A-3.0.1N碘标准液:称取升华精制的碘12.7g。
加于少量的水,溶解。
加碘化钾40g,待溶解,再加水稀释至1L。
B 分析操作:B-1.取镀液5ml;B-2.加水100ml;B-3.加稀盐酸(6N)20mlB-4.加淀粉指示剂5mlB-5.用0.1N碘标准液滴至溶液恰变蓝紫色,记录体积。
C 计算:SnSO4(g/L)=碘滴定所耗体积乘以2.15。
2、硫酸A 药品:A-1.甲基红指示剂:0.5 g甲基红加20ml酒精溶解,再加水至100mlA-2.1N氢氧化钠标准液:称取氢氧化钠45g,加水溶解至1L。
B 分析操作:B-1.取镀液5ml;B-2.加水50ml;B-3.加1至5滴甲基红指示剂(呈玫瑰红);B-4.用1N氢氧化钠滴定至终点(呈黄色);C 计算:硫酸含量(g/L)=滴定耗用溶液体积乘以9.8。
一.氰化镀锌分析方法1.氰化钠计算:M×V×98÷2 过程:取镀液2 ml,加水50 ml,KI(10%)5-10 ml,NaOH (25%) 10 ml,用标液硝酸银滴定至开始浑浊为终点。
2.氢氧化钠计算:M×V×40 过程:取镀液1 ml,加纯水50 ml,加滴定氰化钠所消耗的硝酸银的量,加氯化钡(10%)20 ml,酚酞2滴,用标液盐酸滴至由红变白色(百里酚酞由蓝变白)为终点.3.氧化锌计算:M×V×81.4 过程:取镀液1 ml,加2:3三乙醇胺10 ml,加PH=10缓冲液15 ml,络黑T少许,加1:9甲醛10 ml.用标液EDTA滴定,由紫变兰色为终点。
二.碱性无氰镀锌分析方法1. 氧化锌计算:M×V×81.4 过程:取镀液1 ml,加2:3三乙醇胺10 ml,加PH=10缓冲液10 ml,络黑T少许,加1:9甲醛10 ml.用标液EDTA滴定,由紫变兰色为终点。
2.氢氧化钠计算:M×V×40 过程:取镀液1 ml,加水50 ml,加滴定氧化锌所消耗的EDTA 的量,加氯化钡(10%)20 ml,酚酞2滴,用标液盐酸滴至由红变白色(百里酚酞由蓝变白)为终点.三.氯化钾镀锌分析方法1.氯化钾计算:氯化钾(g/L)=(M1×V1-M2×V2)×2×74.6过程:取镀液0.5 ml,加水80ml,加饱和铬酸钾溶液5-10滴(最好用硝酸银滴定时瞬间红色较明显),用标液硝酸银滴定至白色沉淀且略带淡红色为终点。
2.氯化锌计算:M2×V2×136.3 过程:取镀液1 ml,加2:3三乙醇胺10 ml,加PH=10缓冲液15 ml,络黑T少许,加1:9甲醛10 ml.用标液EDTA滴定,由紫变兰色为终点。
计算:M×V×61.8 过程:取镀液1 ml,加水50 ml,加0.1%溴甲酚紫3-4滴,10%盐酸滴至黄色,加10%片碱滴至紫蓝色,加甘露醇少许,摇匀,此时溶液变黄,用标准氢氧化钠液滴至紫蓝色为终点。
电镀锡钝化液的配制工艺电镀锡钝化液是一种用于保护金属表面的液体溶液,主要应用于金属制品的电镀过程中。
它能够形成一层致密的、具有一定厚度的钝化膜,从而提高金属制品的抗划伤性、耐磨性和耐腐蚀性。
下面将介绍电镀锡钝化液的配制工艺。
电镀锡钝化液的配制工艺主要包括材料准备、液体配比和工艺参数控制。
首先,需要准备以下材料:硝化锡、硼酸、硫酸、稀硫酸和蒸馏水。
1. 材料准备:准备适量的硝化锡(Sn(NO3)2)和硼酸(H3BO3),其中硝化锡的浓度一般为75-100 g/L,硼酸的浓度一般为30-40 g/L。
准备适量的硫酸(H2SO4)和稀硫酸(H2SO4)作为酸性调节剂,其中硫酸的浓度一般为150-200 g/L,稀硫酸的浓度一般为10-15 g/L。
准备足够的蒸馏水作为稀释剂。
2. 液体配比:将硝化锡和硼酸按照一定比例加入容器中,搅拌溶解,使得硝化锡和硼酸均匀混合。
一般的液体配比为硝化锡:硼酸= 1:0.3-0.4。
随后,将酸性调节剂(硫酸和稀硫酸)逐渐加入容器中,搅拌均匀。
最后,用蒸馏水稀释溶液,直到所需浓度。
稀释的过程中需要保证搅拌均匀。
3. 工艺参数控制:在电镀锡钝化液的使用过程中,需要控制以下几个工艺参数:温度:一般控制在20-40的范围内,过高或过低的温度都会影响涂层的质量。
需要根据不同的金属材料和工艺要求进行调节。
时间:电镀锡的钝化时间一般为2-10分钟,具体时间根据涂层的厚度要求和金属材料的种类进行调节。
电流密度:电流密度是指单位面积上的电流值,一般控制在1-5 A/dm²的范围内。
电流密度过高会导致涂层不均匀,过低会导致涂层过薄。
PH值:PH值是指溶液的酸碱程度,一般控制在2-3的范围内。
需要通过加入适量的酸性调节剂进行调节。
总结:电镀锡钝化液的配制工艺主要包括材料准备、液体配比和工艺参数控制。
通过合理的配制和控制工艺参数,可以获得高质量的电镀锡钝化液,从而提高金属制品的性能和耐蚀性。
电镀药水分析方法1电镀液分析方法盐酸(HCl含量):试剂:1N氢氧化钠标准滴定溶液酚酞指示剂步骤:1)用移液管精确吸取5ml溶液于250ml锥形瓶中;2)加入100ml DI水;3)加入1-2滴酚酞指示剂;4)用1N NaOH滴定,溶液由无色突变为浅红色时即为终点;5)记录所消耗的NaOH溶液的体积,用下式计算盐酸(HCl)含量: HCl %(V/V)= V NaOH ×N NaOH×2.1硫酸(H2SO4含量):试剂:0.1N氢氧化钠标准滴定溶液酚酞指示剂步骤:1)用移液管精确吸取5ml溶液于250ml锥形瓶中;2)加入100ml DI水;3)加入1-2滴酚酞指示剂;4)用1N NaOH滴定,溶液由无色突变为浅红色时即为终点;5)记录所消耗的NaOH溶液的体积,用下式计算盐酸(H2SO4)含量: H2SO4 %(V/V)= V NaOH ×N NaOH×1.05盐酸(HCl含量):试剂:1N氢氧化钠标准滴定溶液酚酞指示剂步骤:1)用移液管精确吸取1ml溶液于250ml锥形瓶中;2)加入100ml DI水;3)加入1-2滴酚酞指示剂;4)用1.0N NaOH滴定,溶液由无色突变为浅红色时即为终点;5)记录所消耗的NaOH溶液的体积,用下式计算盐酸(HCl)含量: HCl %(V/V)= V NaOH ×N NaOH×10.5氨基磺酸镍镍离子试剂:0.05N EDTA 标准滴定溶液MX(紫尿酸胺)指示剂氨水步骤:1)用移液管精确吸取1ml镀液于250ml锥形瓶中;2)加入100ml DI水;3)加入10ml氨水;4)加入0.2gMX指示剂;5)用0.05N EDTA滴定,溶液由褐色至蓝紫色时即为终点;6)记录所消耗的EDTA溶液的体积,用下式计算Ni含量:Ni(g/L)= V EDTA×C EDTA×58.7H3BO3试剂:0.1N氢氧化钠标准滴定溶液甘露醇BCP(溴甲酚紫)指示剂步骤:1)用移液管精确吸取1ml镀液于250ml锥形瓶中;2)加入20ml DI水;3)加入5g甘露醇;4)加入BCP指示剂4滴;5)用0.1N NaOH滴定,溶液由黄绿色变为蓝色时即为终点;6)记录所消耗的NaOH溶液的体积,用下式计算HBO3含量;H3BO3(g/L)= V NaOH×C NaOH×61.8NiCl2·6H2O(氯化镍)试剂:0.1N硝酸银标准滴定溶液2%铬酸钾指示剂步骤:1)用移液管精确吸取2ml镀液于250ml锥形瓶中;2)加入50ml DI水;3)加入2%铬酸钾指示剂1ml;4)用0.1N AgNO3滴定,溶液由亮黄色变为土黄色时即为终点;5)记录所消耗的AgNO3溶液的体积,用下式计算阳极活化剂含量:NiCl2·6H2O(g/l)V×N×59.5(二价锡)试剂:0.1N碘酸钾标准滴定溶液淀粉指示剂浓盐酸步骤:1)用移液管精确吸取2ml电镀溶液于250ml锥形瓶中;2)加入50ml DI水;3)加入50ml浓盐酸;4)加入1-2ml淀粉指示剂;5)用0.1N碘酸钾滴定,溶液由无色突变为蓝色时即为终点;6)记录所消耗的碘酸钾溶液的体积,用下式计算二价锡含量:Sn2+(g/L )= V KIO3× N KIO3×11.9×2.5铅离子的分析方法试剂:0.05M EDTA0.05M 硫酸锌30%双氧水20%三乙醇胺缓冲溶液(54g氯化铵溶于350ml浓氨水溶液中用去离子水配成1L溶液)铬黑T指示剂(1g和400g氯化钠混合)步骤:1)用移液管精确吸取5ml电镀溶液于250ml锥形瓶中;2)加入100ml DI水;3)精确量取0.05M EDTA 25ml;4)加2ml 双氧水;5)加5ml三乙醇胺;6)加20ml 缓冲溶液;7)加少许铬黑T;8)用0.05M 硫酸锌溶液从蓝色滴定到紫色为终点Pb2+ = (25-滴定量)×2.072 g/L= (V EDTA×C EDTA)-(V Zn×C Zn)×41.44常用标准溶液配制和标定以下所用一般试剂纯度为分析纯,基准试剂要求为优级纯。
电镀镀锡液配制(开缸)及分析方法我折腾了好久电镀镀锡液配制(开缸)及分析方法,总算找到点门道。
咱先说说这镀锡液的配制吧。
这一开始啊,我真是瞎摸索。
我知道最基本的原料得有锡盐,就像盖房子得有砖头一样,当时我用硫酸亚锡这个最常见的,但是这东西容易水解啊,我开始没搞清楚,就直接弄水里,就跟沙子直接扔水里不搅拌肯定不均匀一样,结果就出现好多沉淀,这就是失败的教训啊。
后来我知道了,得把硫酸亚锡先放到稀硫酸里溶解,这个稀硫酸就像一个好的溶剂桥梁,能让硫酸亚锡乖乖地分散在溶液里。
在配制镀锡液,光亮剂也不能少。
我试过好多光亮剂,不同品牌的效果真的差别很大。
我开始的时候以为只要有就行,随便挑了一个便宜的,可是镀出来的东西表面乌漆嘛黑的,一点也不光亮。
后来我咬咬牙买了个贵点的知名品牌的光亮剂,效果就好多了。
光亮剂就像化妆抹的亮粉,能让镀出来的锡层变得特别好看。
还有啊,这镀锡液里还得有添加剂。
我不确定具体每个添加剂都起在这溶液里确切起什么作用,但我知道稳定剂是很重要的。
因为在镀锡过程中,有时候溶液会因为一些原因变得很不稳定,就像人的情绪忽上忽下一样。
我试过有一回没加稳定剂,镀着镀着就开始出问题,镀件表面这儿一块好那儿一块不好,坑坑洼洼的。
接下来再讲讲这分析方法。
分析镀锡液,我觉得最主要的就是测锡离子的浓度了。
我试过用化学滴定的方法,就像拿小勺子一勺一勺量东西一样。
我按照那种教材上的标准方法,用一种专门的试剂,一点一点地加,看颜色变化。
但是这颜色变化我老是把握不准,后来我才知道原来是光线角度的问题,就像你看东西在不同光下看起来不一样似的。
后来我就特别注意这个光线,慢慢就测准了。
这电导率我也测过,电导率就像是这镀锡液里的小电流通道是不是通畅的一个指标。
我用那个电导率仪去测,开始我的仪器没校准好,测出来的数据乱七八糟的,那数据肯定就是假的啦。
后来我认真看了说明书,把仪器校准好了,才得到了比较准确的电导率数据。
还有酸碱度的测定,我用的就是普通的pH试纸。
Zhejiang Haining Rongxin Electronics Co., Ltd.
地址/Add:浙江海宁对外综合开发区之江路邮编/PC:314423
电话/TEL:86-573-87966368传真/FAX:86-573-87966326
网址/Website: Email: rongxin@
镀锡槽液配制及镀液分析化验方法
一、设备:
1、镀槽---PVC或PE材质
2、过滤系统(耐酸材料)。
3、冷却系统(铁氟龙被覆管)。
二、槽液备制:
以配制100升标准的RX-770/780光亮纯锡镀液为例:
1、加入60升去离子水;
2、在连续搅拌的情况下缓慢加入计量硫酸9L,注意此时有放热现象,充分搅拌均匀,
注意安全;
3、在连续搅拌的情况下缓慢加入计量硫酸亚锡2.5kg-3kg(建议为2.5kg,因为亚锡
会随着电镀的进行而增加)。
4、冷却至室温时(30℃左右)加入RX-770开缸剂600ml,RX-780光亮剂150ml。
5、补加去离子水到所需液面高度,充分搅拌均匀后可进行试镀。
三、硫酸镀锡液分析方法
1、硫酸亚锡(SnSO4)
A药品:
A-1.稀盐酸(6N):浓盐酸和水比例1:1。
A-2.淀粉指示剂:可溶性淀粉1g,溶解于沸腾水中至100ml。
再沸腾一分钟。
A-3.0.1N碘标准液:称取升华精制的碘12.7g。
加于少量的水,溶解。
加碘化钾40g,待溶解,再加水稀释至1L。
B 分析操作:
B-1.取镀液5ml;
B-2.加水100ml;
B-3.加稀盐酸(6N)20ml
B-4.加淀粉指示剂5ml
B-5.用0.1N碘标准液滴至溶液恰变蓝紫色,记录体积。
C 计算:
SnSO4(g/L)=碘滴定所耗体积乘以2.15。
2、硫酸
A 药品:
A-1.甲基红指示剂:0.5 g甲基红加20ml酒精溶解,再加水至100ml
A-2.1N氢氧化钠标准液:称取氢氧化钠45g,加水溶解至1L。
B 分析操作:
B-1.取镀液5ml;
B-2.加水50ml;
B-3.加1至5滴甲基红指示剂(呈玫瑰红);
B-4.用1N氢氧化钠滴定至终点(呈黄色);
C 计算:
硫酸含量(g/L)=滴定耗用溶液体积乘以9.8。
(内部技术资料)。