旋光异构
- 格式:doc
- 大小:274.00 KB
- 文档页数:7


旋光异构名词解释旋光异构体(chiral isomer)指的是某些化合物由于电子的波函数与原来的不同,因此所呈现出来的光学性质也跟着改变,这种性质可以藉由对旋光仪器的观测而被得知。
通常情况下,异构体之间具有如下特征:(1)化学上呈现碱性或者酸性;(2)在有机化学的历程中,其分子骨架一定会使它带有正电荷;(3)在外界条件改变时,异构体都会保持异构体之间固有的形态。
旋光异构体有很多,但大多数都是碳链的异构体,例如正碳离子、碳烯、卡宾、卡拜。
基于这个概念,可以使用下列的定义来分类化合物的旋光异构体。
1.按原子中所含的电子个数不同,分为三类:(1)不等性碳正离子(含有四个电子);(2)等性碳负离子(含有三个电子);(3)四聚性碳正离子(含有两个电子)下面几个主要反应会影响到旋光性的产生。
1.水解反应。
当一个四聚体结合一个单体成为四聚体时,键结强度减弱,键长增加,从而引起了正电荷。
在正电荷和水分子的共同作用下,碳离子被拉长。
碳正离子的旋光率随着核电荷数的增加而增加,这就是旋光异构体的最初由来。
2.消去反应。
相同碳正离子的化合物在分子内形成碳正离子的过程中会发生消去反应。
由于所涉及的碳原子不能稳定地和两个水分子相连接,导致了水解反应的发生,消去反应形成两个新的正碳离子,并使碳正离子重新回到平衡状态,于是结合了一个水分子的碳离子又变成了碳正离子。
通过以上的实验,可以发现碳正离子中的每一个碳离子是以与水分子结合的碳氧双键的方式进行稳定结合的。
3.加成反应。
这种反应将会导致产生碳负离子。
由于在和四个水分子连接的碳上有一个孤对电子,可以使得碳正离子和四个水分子之间发生作用,碳负离子的存在就意味着消除了一个单体。
然后碳正离子和其他碳正离子进行结合。
4.氧化还原反应。
有些化合物可以被氧化,这样就会减弱碳正离子的作用。
同时,它们可以被还原,这样会增强碳正离子的作用。
于是结果是可以得到不同的产物。
旋光异构体有很多,但大多数都是碳链的异构体,例如正碳离子、碳烯、卡宾、卡拜。




旋光异构两个或多个分子由于构型上的差异而表现出不同旋光性能的现象。
这些分子互为旋光异构体,也称对映异构体。
导致旋光异构现象的原因有两种:①分子中含有一个或多个手性原子(见手征性)。
含有一个手性碳原子时,有两个旋光异构体,它们具有互为实物和镜像的关系,故也称对映体。
对映异构体具有相等的旋光能力,但旋转方向相反,其物理和化学性质极为相似,如甘油醛(如对图片说明中“菲舍尔投影式”有疑问,见菲舍尔投影式):甘油醛菲舍尔投影式含有两个相同手性碳原子的分子,有3个旋光异构体,如酒石酸:酒石酸菲舍尔投影式其中a和b为对映异构体,c与d也好像是对映体。
但实际上c与d是同一种分子,因为它们可以互相叠合。
只要把c以通过C(2)-C(3)键中点,与读者的显示器荧屏(设荧屏竖直)垂直的线为轴旋转180°,就可以看出来它是可以与d叠合的。
也就是说,c和d是相同的。
c的旋光能力由于分子内的两个结构相同但构型(见分子构型)相反的手性原子的存在而互相抵消,称为内消旋体。
它与a或b在分子中既有构型相同的部分,又有构型相互对映的部分,这种关系称为非对映异构。
非对映异构体不仅旋光性不同,物理和化学性质也不尽相同。
环状化合物中含有手性原子时,也可出现以上旋光异构现象。
分子中当含有几个不同的手性原子时,其旋光异构体的数目为2n,n为不同手性原子的个数。
旋光异构体可用D-、L-法标记其构型(见单糖),也可用R-、S-法标记其分子中每个原子的构型(见顺序规则)。
②某些分子虽然不含手性原子,但由于分子中的内旋转受阻碍,也可以引起旋光异构现象,例如丙二烯型或联苯型旋光化合物是通过分子中的一个轴来区别左右手征性;又如旋光性提篮型化合物分子是就一个平面来区别手征性的等。
等量互为对映异构体的旋光性物质均匀混合,所得混合物没有旋光性。
这种混合物叫做外消旋体。
旋光异构体定义在化学的广阔领域中,旋光异构体是一个颇为重要的概念。
简单来说,旋光异构体指的是那些具有相同分子式和原子连接顺序,但由于分子中的原子在空间排列方式不同,从而导致它们使平面偏振光的振动平面发生不同方向旋转的同分异构体。
为了更深入地理解旋光异构体,我们首先需要了解一下什么是平面偏振光。
想象一下,一束普通的光就像一群没有组织、四处乱跑的孩子,它们的振动方向是杂乱无章的。
而平面偏振光则像是经过训练的整齐队列,所有的“成员”(光波)都在同一个平面内振动。
当平面偏振光通过某些物质时,这些物质可能会使光的振动平面发生旋转。
如果一种物质能使平面偏振光的振动平面向右旋转,我们就称其为右旋体,通常用“+”表示;相反,如果使平面偏振光的振动平面向左旋转,那就是左旋体,用“”表示。
那么,旋光异构体是如何产生的呢?这主要归因于分子的手性。
手性就像是人的左右手,虽然看起来相似,但却不能完全重合。
在分子中,如果一个碳原子连接了四个不同的原子或基团,那么这个分子就具有手性,可能存在旋光异构体。
比如说,乳酸分子就有两种旋光异构体。
一种是从肌肉中提取出来的,能使平面偏振光向右旋转,称为右旋乳酸;另一种是通过化学合成得到的,使平面偏振光向左旋转,称为左旋乳酸。
旋光异构体在生物体内往往具有不同的生理活性和药理作用。
例如,某些药物的一种旋光异构体可能具有很好的疗效,而另一种则可能效果不佳甚至产生副作用。
这是因为生物体内的酶和受体通常具有手性识别能力,只能与特定的旋光异构体相互作用。
在化学研究和工业生产中,旋光异构体的分离和分析也是非常重要的。
常用的方法包括手性色谱法、化学拆分法等。
通过这些方法,可以得到纯净的旋光异构体,从而更好地研究它们的性质和应用。
此外,旋光异构体在农业、食品等领域也有着广泛的应用。
比如,某些农药的旋光异构体可能对害虫的杀灭效果更好,同时对环境的危害更小;在食品添加剂中,特定的旋光异构体可能具有更理想的口感和稳定性。
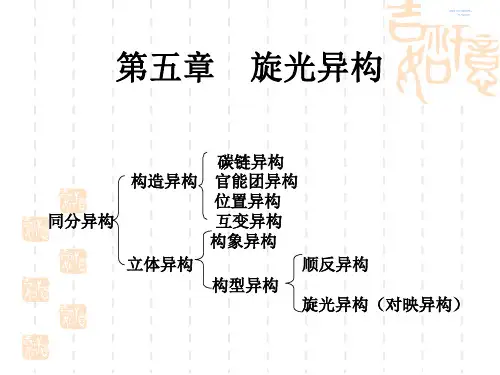
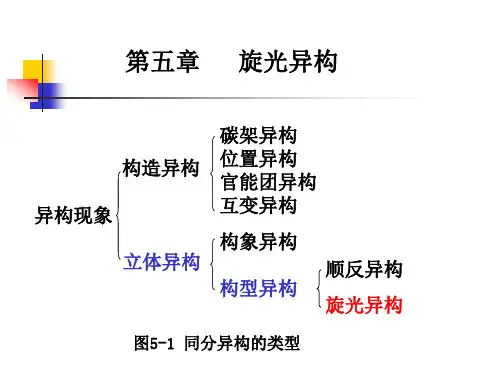
第五章:旋光异构引言有机化合物异构现象根据产生原因分类如下:碳链异构结构异构:官能团位置异构官能团互变异构同分异构:构象立体异构:顺反异构旋光异构“旋光异构”目录一.偏振光和旋光活性。
二.旋光度和比旋光度。
三.分子的对称性、手性和旋光活性。
四.含一个C*的化合物。
五.含两个不同C*的化合物。
六.含两个相同C*的化合物。
七.不含手性碳原子的化合物。
八.旋光异构体的性质。
九.练习题。
1.偏振光:通过尼可尔棱镜后只在一个平面上振动的光谓之偏振光。
镜轴镜轴偏振光普通光2.旋光活性与光学活性物质:●旋光活性:物质能够使偏振光偏离原来的振动平面振动的特性。
●光学活性物质:具有旋光活性的物质。
3.旋光方向和旋光度:①方向:②旋光度:左旋:使偏振光振动平面逆时针旋转。
用“-”表示。
右旋:使偏振光振动平面顺时针旋转。
用“+”表示。
物质使偏振光振动平面旋转的角度。
用“α”表示。
4.旋光仪:测定物质旋光度的仪器。
cba旋光仪结构示意1.影响旋光度的因素:●溶液浓度、盛液管长度、温度、光波波长、溶液的性质等。
2.比旋光度:●浓度为1g/ml的旋光活性物质的溶液放在1分米长的盛液管中所测得的旋光度,以[α]表示。
●被测物为固体:[α]λ=αC×lt C:溶液浓度,单位:g/mll:液体柱长度,单位:dm(分米)●被测物为液体:●常以钠灯为光源,波长λ=589.3nm ,记为D 。
3.表示法:•[α]D = +3.8(乳酸、H 2O 、C =0.1g /ml )•[α]D = +3.79(酒石酸、CH 3CH 2OH 、5%)•必须注明光波波长、温度、溶剂和溶液浓度。
[α]λ=αd ×ltd :液体密度,单位:g/ml20201.手性:•实物与它的镜象不能完全重合的特性。
•不能和自己的镜象完全重叠的分子谓之为手性分子。
•物质分子具有手性表现为物质具有旋光活性。
COOH COOHH HOHCH3OHCH3乳酸与其镜像模型2.手性与分子的对称性。
第五章 旋光异构Ⅰ 学习要求1. 掌握旋光性、旋光度、比旋光度、手性、手性碳原子、手性分子、对映体、非对映体、外消旋体、内消旋体等基本概念。
2. 掌握物质的旋光性与其分子构形的关系,能够正确判断一个化合物是否具有旋光性。
3. 掌握含有一个和两个手性碳原子化合物的旋光异构体Fischer 投影式的书写及相互关系的确定。
4. 熟练掌握含有一个和两个手性碳原子化合物的旋光异构体构型(D 、L 或R 、S )的标记、命名及书写。
5. 了解外消旋体拆分的一般方法。
6. 了解亲电加成反应的立体化学。
Ⅱ 内容提要一. 旋光性物质和比旋光度1. 旋光性物质:在偏振光通过某物质时,能使偏振光的振动平面发生旋转的性质称为旋光性,具有旋光性的物质称为旋光性物质。
2. 比旋光度:旋光能力的大小用旋光度α和比旋光度[]tλα表示。
旋光度是指旋光性物质使偏振光的振动平面旋转的角度;比旋光度则是规定在一定温度下,使用一定波长的光源,物质的浓度为g ·mL —1,盛液管的长度为1dm ,温度为常温时测得的旋光度。
比旋光度与旋光度的关系为:比旋光度是旋光物质的一个物理常数。
比旋光度按右旋(顺时针旋转)和左旋(反时针旋转)分别用(+)和(﹣)表示。
二. 分子的手性与旋光异构1. 手性分子:物质的分子与其镜象不能完全重叠,它们之间相当于左手和右手的关系,把这种特征称为物质的手性。
具有手性的分子称为手性分子,手性分子具有旋光性,具有旋光性的分子一定是手性分子。
2. 对称面:能将分子分成互为镜象两部分的平面称为分子的对称面。
3. 对称中心:从分子中任何一原子或原子团向分子的中心做连线,延长此连线至等距离处,若出现相同的原子或原子团,该点称为分子的对称中心。
对称面和对称中心统称对称因素。
不具有对称因素的分子是手性分子,或者说手性分子不具有对称因素。
4. 手性碳原子:连有四个不同原子或原子团的碳原子有不对称性,称为手性碳原子或不对称碳原子,用“C*”表示,是分子的不对称中心或手性中心。
手性是指整个物质的性质,手性中心是指其中某一原子的性质。
[]lC t⋅α=αλ三. 含一个手性碳原子化合物的旋光异构1. 对映体:彼此呈实物与镜象的对映关系,但又不能完全重叠的一对旋光异构体称为对映异构体,简称对映体。
分子有手性,就存在对映异构体。
对映异构体的物理性质和化学性质一般都相同,比旋光度相等,但旋光方向相反。
2. 外消旋体:等量对映体的混合物称为外消旋体,通常用“±”表示。
外消旋体无旋光性,外消旋体与其左、右旋体的物理性质有差异,但化学性质基本相同。
含有一个手性碳原子的化合物,由于不具有对称因素,所以一定具有旋光性。
有两个旋光异构体,一个左旋体,一个右旋体,为一对对映异构体。
等量混合组成一个外消旋体。
四. 旋光异构体构型的表示方法——费歇尔(E.Fischer)投影式费歇尔投影式的书写方法(略)五. 旋光异构体构型的标记方法1. D/L标记:(略)2. R/S标记:(略)D/L、R/S与(+)、(﹣)无关。
D/L、R/S是构型的标记方法,而(+)、(﹣)表示旋光方向,是通过旋光仪测出来的。
构型与旋光方向无必然联系。
六. 含两个手性碳原子化合物的旋光异构手性碳原子旋光异构体数目外消旋体数目内消旋体数目二个不相同C*2n(n=C*的数目)2n-1(n=C*的数目)二个相同C* 3 1 1 内消旋体:如果分子有二个或二个以上手性中心(手性碳原子),并有一个内在的对称面,这个分子称为内消旋体,它不具有旋光性。
同一化合物的内消旋体与其左旋体和右旋体都呈非对映体关系,它们的物理性质不同,化学性质基本相似。
七. 其他化合物的旋光异构1. 环状化合物的旋光异构:环烷烃分子中不同碳原子上的氢原子被其他原子或原子团取代后,同时又有手性碳原子存在时,就会产生顺反异构和旋光异构。
2. 丙二烯化合物的旋光异构:在丙二烯分子中,如果两端碳原子上连有不同原子或原子团时,虽然分子中不含手性碳原子,但由于整个分子没有对称因素,属于手性分子,具有旋光性。
一旦一端连有相同原子或原子团,就存在对称面,就不是手性分子,就不具有旋光性。
3. 联苯型化合物的旋光异构:在联苯分子中,两个苯环直接相连,如果两个苯环的邻位上连有较大的基团时,由于空间位阻效应使两个苯环的旋转受阻,两个苯环不能处在同一平面上。
如果每个苯环的邻位连有的两个基团都不相同,与丙二烯分子相似,虽然分子中不含手性碳原子,由于整个分子没有对称因素,属于手性分子,具有旋光性。
一旦一个苯环的邻位上连有两个相同基团,分子就有对称面,整个分子就不是手性分子,就没有旋光性。
可见,具有旋光性的物质不一定含有手性碳原子(如丙二烯和联苯型化合物);含有手性碳原子的化合物不一定具有旋光性(如内消旋酒石酸)。
所以,判定一个物质有无旋光性主要是去判断整个分子有无对称因素,整个分子有无手性,是不是手性分子。
Ⅲ例题解析例1. 命名下列化合物,并标出R、S构型。
3COOH2SHH NH23(4)(5)(6)解:(1)3R﹣2 , 3﹣二甲基﹣3﹣戊醇(2)2R﹣2﹣氨基丙酸(3)2R , 3S﹣2 , 3﹣二羟基丙醛(4)3R﹣3﹣甲基环戊烯(5)2S﹣2﹣氨基﹣3﹣巯基丙酸(6)2R﹣2﹣氯丁醇例2. 下列化合物各有多少个旋光异构体?为什么?(1) CH3CH2CH(OH)CHClCH3(2) (CH3)2CHCH2CH(CH3)COOH(3) C6H5CHBrCH2CH(OH)CH2CH(NH2)COOH(4) CH2(OH)CH(OH)CH(OH)CH(OH)CHO(5) CH3CH2CHClCHClCH2CH3解:(1)有两个不相同的手性碳原子,有4个旋光异构体(22 = 4)。
(2)有一个手性碳原子,有2个旋光异构体(21 = 2)。
(3)有三个不相同的手性碳原子,有8个旋光异构体(23 = 8)。
(4)有四个不相同的手性碳原子,有16个旋光异构体(24 = 16)。
(5)有两个完全相同的手性碳原子,有3个旋光异构体,其中一个左旋体,一个右旋体和一个内消旋体。
例3. 下列化合物是否具有旋光性?为什么?解:(1)、(2)、(4)有旋光性,因为无对称因素;(3)、(5)无旋光性,因为有对称面。
CH32H5HO CH(CH3)2COOHCH3H NH2CHOH OHHHO CH3(1)(2)(3)CH2OHH ClCH3H ClCOOHHO HH OHCOOHH OHHO HCOOHH OHCH2OHH OHHO HH OHHO HCH2OHCH3C2H5C C CCH3CH3(1)(2)(3)(4)(5)例4. 标记出下列化合物的构型是R 还是S ,并指出B ~E 的表示方法及它们与化合物A 的关系。
解:A 、C 、E 为S 构型,B 、D 为R 构型。
B 为费歇尔投影式,C 、D 为纽曼投影式,E 为一般投影式(或称锯架式)。
B 、D 是A 的对映体,C 、E 与A 的构型相同。
例5. 下列各对化合物哪些是相同的,哪些是对映体,哪些是非对映体,哪些是内消旋体?解:(1)为同一构型,(2)为对映体,(3)为同一构型,且为内消旋体,(4)为非对映体。
例6. 写出下列化合物所有的旋光异构体,并注明其相互关系(对映体,非对映体,内消旋体和外消旋体)。
(1) 1 , 3﹣二氯环戊烷 (2) 3 , 4﹣二甲基﹣3 , 4﹣二溴己烷 (3) 2﹣氯﹣3﹣溴丁烷 解:(Ⅰ)为内消旋体(有对称面),(Ⅱ)与(Ⅲ)互为对映体,等量混合组成外消旋体,(Ⅰ)与(Ⅱ),(Ⅰ)与(Ⅲ)互为非对映体。
(Ⅰ)与(Ⅱ)互为对映体,等量混合组成外消旋体,(Ⅲ)为内消旋体,(Ⅰ)与(Ⅲ),(Ⅱ)与(Ⅲ)互为非对映体。
CH 32H 5H Cl H H 3C C 2H 53H 3H 3H CH 3H H CH 3Cl A B CDE CH 32H 5BrH CH 3BrH C 2H 5COOH H Br H Br COOH Br H Br H CHO2OH H OH CHO HCH 2OH 22与与与与(1)(2)(3)(4)( )Ⅰ( )Ⅱ( )Ⅲ(1)CH 2CH 3Br CH 3CH 2CH 3H 3C BrCH 2CH 3H 3CBr 2CH 3Br CH 3CH 2CH 3H 3C Br 2CH 3H 3C Br( )Ⅰ( )Ⅱ( )Ⅲ(2)(Ⅰ)与(Ⅱ),(Ⅲ)与(Ⅳ)分别为对映体,分别等量混合组成两个外消旋体,(Ⅰ)与(Ⅲ),(Ⅰ)与(Ⅳ),(Ⅱ)与(Ⅲ),(Ⅱ)与(Ⅳ)互为非对映体。
例7. 化合物A 分子式为C 6H 11Cl ,具有旋光性,能使溴水褪色,与氢氧化钠的乙醇溶液加热反应生成B ,B 无旋光性,B 经臭氧氧化后还原水解生成的产物之一是2﹣甲基丙二醛,试推测A 、B 的构造式并写出各步反应。
解:Ⅳ 练习题一. 标出下列化合物中的手性碳原子:1. CH 3CHClCH 2CH 32. CH 3CH(NH 2)COOH3. C 6H 5CH(OH)COOH4. CH 3CHClCH(OH)CH 3二. 下列化合物哪些存在旋光异构体?1. 1﹣溴﹣2﹣丙醇2. 2﹣甲基﹣2﹣丁醇3. 3﹣甲基﹣2﹣丁醇4. 1﹣苯基﹣1﹣氯乙烷5. 1﹣苯基﹣2﹣氯乙烷6. 2﹣氨基﹣1﹣丙醇三. 用R / S 标记法,标明下列化合物中手性碳原子的构型:四. 画出2 , 3﹣二氯戊烷所有旋光异构体的Fischer 投影式,并指出它们之间的关系。
ⅣCH 3H Cl 3H Br CH 3Cl H CH 3Br HCH 3H Cl 3Br HCH 3Cl H CH 3H Br ( )( )Ⅲ( )Ⅱ( )Ⅰ(3)CH 2CHCHCH 2CH 2CH 3CH 2CHCHCH 2CH 2Cl Br 32CHCHCH CH 3CH 1) O 32OHC CH CHOCH 3(A)(B)含有C*,具有旋光性。
2C 2OCH 3H 3CH CH 3OCH3HBr 3Cl H C 2COOH H OH 2CH 3H OH3)2H 21. 2.3.4. 5.6.五. 根据R / S 标记法写出下列化合物的Fischer 投影式:1. CHClBrF (S)2. C 6H 5CHClCH 3 (S)3. CH 3CHClCHClCH 3 (2R , 3R)4. C 6H 5CH(CH 3)CH(OH)CH 3 (2S , 3R)5. HOOCCH(OH)CH(OH)COOH (2R , 3S)六. 写出3﹣甲基戊烷进行一氯代反应的可能产物,并指出哪些是对映体,哪些是非对映体,哪些不具有手性?七. 指出下列各对化合物的相互关系(相同构型,对映体,非对映体,内消旋体):八. 化合物A ,分子式为C 6H 10,具有旋光性。