【人教版】高中化学必修二:《乙酸》ppt课件
- 格式:ppt
- 大小:2.68 MB
- 文档页数:45


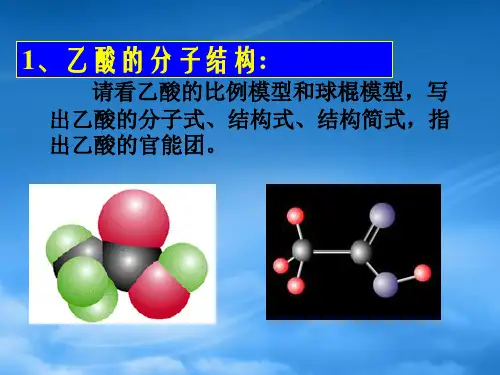
高中化学必修2乙酸ppt课件contents •乙酸概述•乙酸的分子结构和化学键•乙酸的实验室制备•乙酸的化学性质及反应•乙酸在有机合成中的应用•乙酸的安全使用与储存目录01乙酸概述无色透明液体,有刺激性气味熔点16.6℃,沸点117.9℃相对密度1.05,折射率1.3719易溶于水、乙醇、乙醚等有机溶剂01020304010204具有羧酸的通性,如与醇发生酯化反应,与碱发生中和反应等能被还原成乙醇,也能被氧化成二氧化碳和水能与金属钠、镁等活泼金属反应生成氢气和相应的盐在一定条件下,能发生脱羧反应生成甲烷和二氧化碳03用作调味品和香料,如食醋的主要成分就是乙酸用作有机溶剂和萃取剂,如从植物中提取精油时常用乙酸作为萃取剂用于合成乙酸乙酯、乙酸纤维素等有机化合物用于制造染料、农药、医药等化工产品乙酸在日常生活中的应用02乙酸的分子结构和化学键03官能团羧基(-COOH )01分子式C2H4O202结构简式CH3COOH原子间连接方式乙酸分子中,碳原子与氢原子、氧原子之间通过共价键连接。
空间构型乙酸分子为平面结构,羧基中的碳氧双键与碳氢键之间的夹角约为120°。
乙酸分子中,碳原子与氢原子、氧原子之间通过共价键连接,包括碳氢共价键、碳氧共价键和氢氧共价键。
共价键极性共价键配位键由于乙酸分子中氧原子的电负性较强,使得碳氧共价键具有一定的极性,这种极性共价键的存在使得乙酸分子具有一定的偶极矩。
在乙酸分子中,羧基上的氧原子可以与某些金属离子形成配位键,这种配位键的形成使得乙酸具有一定的络合能力。
030201乙酸的化学键类型03乙酸的实验室制备实验室制备乙酸的方法和原理方法通过乙醇的氧化反应制备乙酸。
原理乙醇在催化剂的作用下,与氧气发生氧化反应,生成乙酸和水。
准备实验器材和试剂组装实验装置加热反应收集产物烧瓶、冷凝管、酒精灯、乙醇、催化剂等。
点燃酒精灯,对烧瓶中的乙醇进行加热,使其发生氧化反应。
将烧瓶、冷凝管等实验器材按照实验要求组装好。