腐蚀 第2章 腐蚀热力学讲解
- 格式:ppt
- 大小:2.13 MB
- 文档页数:53









第2章腐蚀热力学2.1 腐蚀倾向的热力学判据在自然环境和许多腐蚀介质中,除个别贵金属(Au,Pt等)外,绝大多数金属在热力学上是不稳定的,有自动发生腐蚀的倾向。
在一定的外界条件下,这些金属从金属状态自发地转变为离子状态,生成相应的氧化物、硫化物或有关的盐类。
从这个意义上讲,金属腐蚀是冶金的逆过程。
为什么大多数金属有自发腐蚀的倾向?为什么不同金属在不同介质中的腐蚀倾向不同?如何用热力学方法判断金属的腐蚀倾向及程度呢?自然界一切自发过程都是有方向性的,都有从自由能高的状态向自由能低的状态转变的趋势。
例如,热总是从高温物体自动传向低温物体,直到两物体的温度一致;水总是从高处自动流向低处,直到水位相等;电流总是从高电位处自动流向低电位处,直到电位差为零;溶液中的溶质总是从高浓度处自动向低浓度处扩散,直到浓差为零。
对于化学反应,同样存在着自发进行的方向和限度问题。
例如,锌片浸在稀的硫酸铜溶液中,将自动发生取代反应,生成铜和硫酸锌溶液,其逆反应不能自发进行,除非用电解的方法,从外界对它做功。
可见,不管是自发的物理过程还是化学变化,它们都有一定的方向和限度。
它们都是不可逆过程。
每一自发过程都有导致其变化的原因,即自发过程的推动力。
如温差、水位差、浓度差、电位差、化学位差等。
自发过程的方向就是使这些差值减小的方向,限度就是这种差值的消失。
对于金属腐蚀和大多数化学反应来说,一般是在恒温、恒压的敞开体系条件下进行的。
这种情况下,通常用吉布斯(Gibbs)自由能判据来判断反应的方向和限度。
即在等温等压条件下:(ΔG)T,p < 0 自发过程;(ΔG)T,p = 0 平衡状态;(ΔG)T,p > 0 非自发过程。
(2-1)(ΔG)T,p表示等温等压下,过程或反应的自由能变化△G只取决于始态和终态,与过程或反应的途径无关。
用它可作为过程或反应能否自发进行的统一衡量标准。
就是说,在等温等压条件下,若体系的自由能减小,则该过程可自发进行,若体系的自由能减到了最小,则体系达到了平衡状态,若体系的自由能增大,则该过程不能自发进行。
第 2 章 腐蚀热力学2.1 腐蚀倾向的热力学判据 在自然环境和许多腐蚀介质中,除个别贵金属(Au ,Pt 等) 外,绝大多数金属在热力学上是不稳定的,有自动发生腐蚀的倾向。
在一定的外界条件下,这些金属从金属状态自发地转 变为离子状态,生成相应的氧化物、硫化物或有关的盐类。
从这个意义上讲,金属腐蚀是冶 金的逆过程。
为什么大多数金属有自发腐蚀的倾向 ?为什么不同金属在不同介质中的腐蚀倾向不同 ?如何用热力学方法判断金属的腐蚀倾向及程度呢 ?自然界一切自发过程都是有方向性的,都有从自由能高的状态向自由能低的状态转变的 趋势。
例如,热总是从高温物体自动传向低温物体,直到两物体的温度一致;水总是从高处 自动流向低处,直到水位相等;电流总是从高电位处自动流向低电位处,直到电位差为零; 溶液中的溶质总是从高浓度处自动向低浓度处扩散,直到浓差为零。
对于化学反应,同样存 在着自发进行的方向和限度问题。
例如, 锌片浸在稀的硫酸铜溶液中, 将自动发生取代反应, 生成铜和硫酸锌溶液,其逆反应不能自发进行,除非用电解的方法,从外界对它做功。
可见,不管是自发的物理过程还是化学变化,它们都有一定的方向和限度。
它们都是不 可逆过程。
每一自发过程都有导致其变化的原因,即自发过程的推动力。
如温差、水位差、 浓度差、电位差、化学位差等。
自发过程的方向就是使这些差值减小的方向,限度就是这种 差值的消失。
对于金属腐蚀和大多数化学反应来说,一般是在恒温、恒压的敞开体系条件下进行的。
这种情况下, 通常用吉布斯 (Gibbs) 自由能判据来判断反应的方向和限度。
即在等温等压条件 下:(△ G T , p 表示等温等压下,过程或反应的自由能变化△或反应的途径无关。
用它可作为过程或反应能否自发进行的统一衡量标准。
就是说,在等温 等压条件下,若体系的自由能减小,则该过程可自发进行,若体系的自由能减到了最小,则 体系达到了平衡状态,若体系的自由能增大,则该过程不能自发进行。
第二章电化学腐蚀热力学2.1金属腐蚀倾向的热力学判据自然界中绝大多数金属元素(除Au,Pt等贵金属之外)均以化合态存在。
大部分金属单质是通过外界对化合态体系提供能量(热能或者电能)还原而成的,因此,在热力学上金属单质是一个不稳定体系。
在一定的外界环境条件下,金属的单质状态可自发地转变为化合物状态,生成相应的氧化物、硫化物和相应的盐等腐蚀产物,使体系趋于稳定状态,即有自动发生腐蚀的倾向。
金属发生腐蚀的可能性和程度不仅与金属性质有关,还与腐蚀介质的特性和外界条件有关。
研究腐蚀现象需要从两个方面着手,一方面是看腐蚀的自发倾向大小。
另—方面是看腐蚀进程的快慢,前者需要用热力学原理进行分析,后者则要借助动力学理论。
金属腐蚀反应体系是一个开放体系。
在反应过程中,体系与环境既有能量的交换又有物质的交换。
金属腐蚀反应一般都是在恒温和恒压的条件下进行的,用体系的热力学状态函数吉布斯(Gibb)自由能判据来判断反应的方向和限度较为方便。
吉布斯自由能用G表示,对于等温等压并且没有非体积功的过程,腐蚀体系的平衡态或稳定态对应于古布斯自由能G为最低的状态。
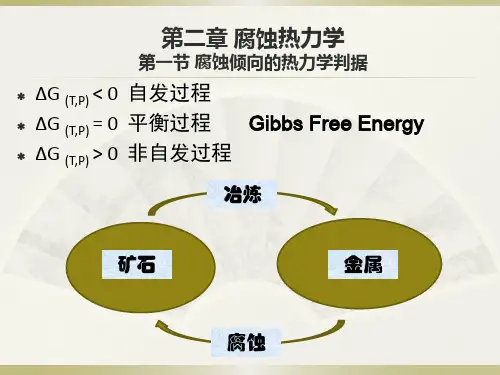
设物质系统吉布斯自由能变化为ΔG,则有<0自发过程ΔG=0平衡状态(2-1)>0非自发过程自然环境中的大多数金属的单质态和化合物状态的吉布斯自由能高低表现出如图2.1所示的状况,即腐蚀产物与矿石一样处于低能的稳定状态,金属单质处于高能的状态。
因此金属腐蚀具有自发倾向。
图2.1物质的吉布斯自由能一个腐蚀体系是由金属和外围介质组成的多组分敞开体系。
对于一个腐蚀化学反应,可用下式表示。
0iiAi(2-2)式中νi为反应式中组分i的化学计量数,反应物的计量数取负值,生成物的计量数取正值;Ai为参加腐蚀反应的物质组分。
在任意情况下,腐蚀反应体系吉布斯自由能的改变ΔG服从范特荷甫等温方程。
GGRTlnQ(2-3)式中ΔG为反应的标准吉布斯自由能的改变;R为气体常数;T为热力学温度,Q为活度商(或者逸度商)用下式表示。