细胞的破碎与分离包涵体
- 格式:ppt
- 大小:511.00 KB
- 文档页数:39

包涵体的纯化和复性总结(二)关于包涵体的纯化是一个令人头疼的问题,包涵体的复性已经成为生物制药的瓶颈,关于包涵体的处理一般包括这么几步:菌体的破碎、包涵体的洗涤、溶解、复性以及纯化,内容比较庞杂一、菌体的裂解1、怎样裂解细菌?细胞的破碎方法1.高速组织捣碎:将材料配成稀糊状液,放置于筒内约1/3体积,盖紧筒盖,将调速器先拨至最慢处,开动开关后,逐步加速至所需速度。
此法适用于动物内脏组织、植物肉质种子等。
2.玻璃匀浆器匀浆:先将剪碎的组织置于管中,再套入研杆来回研磨,上下移动,即可将细胞研碎,此法细胞破碎程度比高速组织捣碎机为高,适用于量少和动物脏器组织。
3.超声波处理法:用一定功率的超声波处理细胞悬液,使细胞急剧震荡破裂,此法多适用于微生物材料,用大肠杆菌制备各种酶,常选用50-100毫克菌体/毫升浓度,在1KG至10KG 频率下处理10-15分钟,此法的缺点是在处理过程会产生大量的热,应采取相应降温措施,时间以及超声间歇时间、超声时间可以自己调整,超声完全了菌液应该变清亮,如果不放心可以在显微镜下观察。
对超声波及热敏感的蛋白和核酸应慎用。
4.反复冻融法:将细胞在-20度以下冰冻,室温融解,反复几次,由于细胞内冰粒形成和剩余细胞液的盐浓度增高引起溶胀,使细胞结构破碎。
5.化学处理法:有些动物细胞,例如肿瘤细胞可采用十二烷基磺酸钠(SDS)、去氧胆酸钠等细胞膜破坏,细菌细胞壁较厚,可采用溶菌酶处理效果更好,我用的浓度一般为1mg/ml。
无论用哪一种方法破碎组织细胞,都会使细胞内蛋白质或核酸水解酶释放到溶液中,使大分子生物降解,导致天然物质量的减少,加入二异丙基氟磷酸(DFP)可以抑制或减慢自溶作用;加入碘乙酸可以抑制那些活性中心需要有疏基的蛋白水解酶的活性,加入苯甲磺酰氟化物(PMSF)也能清除蛋白水解酶活力,但不是全部,而且应该在破碎的同时多加几次;另外,还可通过选择pH、温度或离子强度等,使这些条件都要适合于目的物质的提取。

包涵体的复性总结关于包涵体的复性是一个令人头疼的问题,已经成为生物制药的瓶颈,包涵体的复性前期准备工作尤为重要,关于包涵体的处理一般包括这么几步:菌体的破碎、包涵体的洗涤、溶解、复性以及纯化,实验内容比较庞杂、繁琐。
一、菌体的裂解菌体的破碎方法很多:高速组织捣碎、玻璃匀浆器匀浆、超声波处理法、反复冻融法、化学处理法。
无论用哪一种方法破碎组织细胞,都会使细胞内蛋白质或核酸水解酶释放到溶液中,使大分子生物降解,导致天然物质量的减少,不同的菌体蛋白需要加入不同的抑制剂:二异丙基氟磷酸(DFP)可以抑制或减慢自溶作用;碘乙酸可以抑制那些活性中心需要有疏基的蛋白水解酶的活性,苯甲磺酰氟化物(PMSF)也能清除蛋白水解酶活力,但不是全部,而且应该在破碎的同时多加几次;另外,还可通过选择pH、温度或离子强度等,使用这些条件时都要适合于目的物质的提取。
在实验室研究多采用超声波处理法和匀浆器匀浆法。
二、包涵体的洗涤通常的洗涤方法一般是难以洗干净的,包涵体中主要含有重组蛋白,但也含有一些细菌成分,如一些外膜蛋白、质粒DNA和其它杂质。
洗涤常用1%以下的中性去垢剂,如Tween、Triton、Lubel和NP40等加EDTA反复多次进行,因去垢剂洗涤能力随溶液离子强度升高而加强,在洗涤包涵体时可加50 mM NaCL。
也可用低浓度的盐酸胍或尿素/中性去垢剂/EDTA/还原剂等洗去包涵体表面吸附的大部分不溶性杂蛋白。
洗涤液pH以与工程菌生理条件相近为宜。
根据不同的菌体选用与之相应的洗涤液,比如:2 M尿素+50mm Tris-HCl+0.2 mM NaCl +1%Triton x-100+2mmEDTA PH8.0,再用缓冲洗涤一次。
此外,刚处理完的包含体好溶解,冷冻后难溶解,且溶解时间和比例都会加大。
三、包涵体的溶解强的变性剂如尿素、盐酸胍,是通过离子间的相互作用,打断包涵体蛋白质分子内和分子间的各种化学键,使多肽伸展,SDS、正十六烷基三甲基铵氯化物等去垢剂,可以破坏蛋白内的疏水键,也可溶解一些包涵体蛋白质。
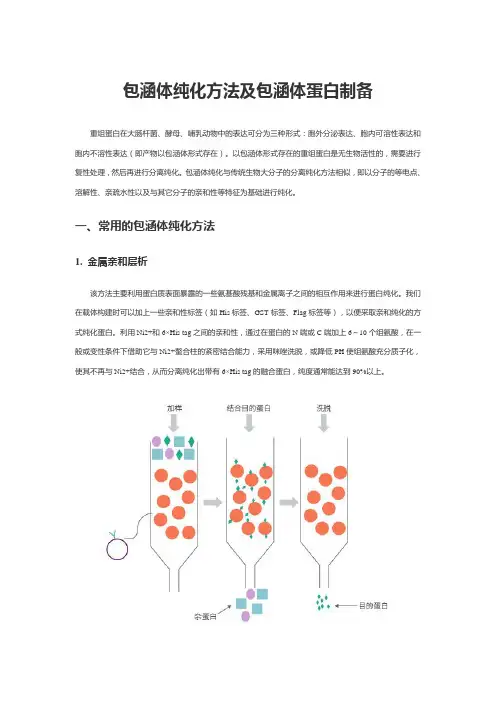
包涵体纯化方法及包涵体蛋白制备重组蛋白在大肠杆菌、酵母、哺乳动物中的表达可分为三种形式:胞外分泌表达、胞内可溶性表达和胞内不溶性表达(即产物以包涵体形式存在)。
以包涵体形式存在的重组蛋白是无生物活性的,需要进行复性处理,然后再进行分离纯化。
包涵体纯化与传统生物大分子的分离纯化方法相似,即以分子的等电点、溶解性、亲疏水性以及与其它分子的亲和性等特征为基础进行纯化。
一、常用的包涵体纯化方法1. 金属亲和层析该方法主要利用蛋白质表面暴露的一些氨基酸残基和金属离子之间的相互作用来进行蛋白纯化。
我们在载体构建时可以加上一些亲和性标签(如His标签、GST标签、Flag标签等),以便采取亲和纯化的方式纯化蛋白。
利用Ni2+和6×His tag之间的亲和性,通过在蛋白的N端或C端加上6~10个组氨酸,在一般或变性条件下借助它与Ni2+螯合柱的紧密结合能力,采用咪唑洗脱,或降低PH使组氨酸充分质子化,使其不再与Ni2+结合,从而分离纯化出带有6×His tag的融合蛋白,纯度通常能达到90%以上。
2.离子交换层析离子交换层析是根据在一定pH条件下,蛋白质所带电荷不同而进行的分离的方法。
常用的离子交换剂有羧甲基纤维素(阳离子交换剂,弱酸型)和二乙基氨基乙基纤维素(阴离子交换剂,弱碱型)。
阴离子交换基质结合带有负电荷的蛋白质,所以这类蛋白质被留在柱子上,需要通过提高洗脱液中的盐浓度等措施将其洗脱下来。
根据蛋白质结合能力不同,洗脱的速度会存在差异,通常结合较弱的蛋白质先被洗脱。
反之,阳离子交换基质会结合带有正电荷的蛋白质,可以通过提高洗脱液的PH或增加洗脱液中的盐浓度将蛋白洗脱下来。
3.凝胶过滤层析凝胶过滤层析通常又称为分子筛方法,主要是根据蛋白质的大小和形状达到分离和纯化的目的。
一般是大分子先流出来,小分子后流出来。
此方法的优点在于层析所用的凝胶属于惰性载体,不带电荷并且吸附力弱,可较广的温度范围内进行。


2 )包涵体的分离蛋白质在细菌中的高水平表达,常形成相差显微镜下可见到的细胞质颗粒,即为包涵体,经离心沉淀后可用Triton-X100/ EDTA 或尿素洗涤,若为获取可溶性的活性蛋白,须将洗涤过的包涵体重新溶解并进行重折叠。
(1)试剂与配制①洗涤液I:0.5 % Triton X -10010 mmol / L EDTA (pH 8 .0 )溶于细胞裂解液中。
②2×凝胶电泳加样缓冲液。
(2)细胞裂解混合物12 000g 离心,15 min ,4 ℃;弃上清,沉淀用9×洗涤液l 悬浮;室温放置5 min ; 12 000g 离心15 min ,4 ℃;吸出上清,用1 00 μL 水重新悬浮沉淀;分别取10 μL上清和重新悬浮的沉淀,加10 μL 2× 凝胶电泳加样缓冲液,进行SDS-PAGE 。
3 )包涵体的溶解和复性(1)试剂与配制①缓冲液I:1 mmol / L PMSF8mol /L 尿素10 mmol / L DTT溶于前述裂解缓冲液中。
②缓冲液Ⅱ:50 mmol / L KH2PO41 mmol / L EDTA (pH 8 .0 )50 mmol / L NaCI2 mmol / L 还原型谷胱甘肽1 mmol / L 氧化型谷胱甘肽③KOH 和HCI 。
④2×凝胶电泳加样缓冲液。
(2)用100 μL 缓冲液I 溶解包涵体;室温放置lh ;加9×缓冲液Ⅱ,室温放置30 min ,用KOH 调pH 到10.7 ;用HCI 调至pH 8 .0 ,在室温放置至少30 min ; 1000g 离心,15 min ,室温;吸出上清液并保留,用100 μL 2×凝胶电泳加样缓冲液溶解沉淀;取10 μL 上清,加10 μL 2× 凝胶电泳加样缓冲液,与20 μL 重新溶解的沉淀进行SDS-PAGE 。
四、注意事项(1)不同的大肠杆菌表达载体带有不同的启动子和诱导成分。

《生化分离工程》思量题及答案第一章绪论1、何为生化分离技术?其主要研究那些内容?生化分离技术是指从动植物组织培养液和微生物发酵液中分离、纯化生物产品的过程中所采用的方法和手段的总称。
2、生化分离的普通步骤包括哪些环节及技术?普通说来,生化分离过程主要包括 4 个方面:①原料液的预处理和固液分离,常用加热、调 PH、凝结和絮凝等方法;②初步纯化(提取),常用沉淀、吸附、萃取、超滤等单元操作;③高度纯化(精制),常选用色谱分离技术;④成品加工,有浓缩、结晶和干燥等技术。
3、生化分离工程有那些特点,及其重要性?特点: 1、目的产物在初始物料(发酵液)中的含量低; 2、培养液是多组分的混合物,除少量产物外,还有大量的细胞及碎片、其他代谢物(几百上千种)、培养基成份、无机盐等; 3、生化产物的稳定性低,易变质、易失活、易变性,对温度、pH 值、重金属离子、有机溶剂、剪切力、表面张力等非常敏感; 4、对最终产品的质量要求高重要性:生物技术产品普通存在于一个复杂的多相体系中。
惟有经过分离和纯化等下游加工过程,才干制得符合使用要求的产品。
因此产品的分离纯化是生物技术工业化的必需手段。
在生物产品的开发研究中,分离过程的费用占全部研究费用的 50%以上;在产品的成本构成中,分离与纯化部份占总成本的 40~80%;精细、药用产品的比例更高达 70~90%。
显然开辟新的分离和纯化工艺是提高经济效益或者减少投资的重要途径。
5、为何生物技术领域中往往浮现“丰产不丰收”的现象?第二章预处理、过滤和细胞破碎1、发酵液预处理的目的是什么?主要有那几种方法?目的:改变发酵液的物理性质,加快悬浮液中固形物沉降的速率;出去大部份可溶性杂质,并尽可能使产物转入便于以后处理的相中(多数是液相),以便于固液分离及后提取工序的顺利进行。
:①加热法。
升高温度可有效降低液体粘度,从而提高过滤速率,常用于粘度随温度变化较大的流体。
控制适当温度和受热时间,能使蛋白质凝结形成较大颗粒,进一步改善发酵液的过滤特性。

一、实验目的1. 学习包涵体蛋白的提取方法。
2. 掌握包涵体蛋白的纯化技术。
3. 了解包涵体蛋白的分离和鉴定。
二、实验原理包涵体是细菌在表达外源蛋白时,由于蛋白折叠错误而形成的无活性蛋白聚集体。
本实验通过裂解细菌细胞,提取包涵体蛋白,然后对其进行纯化、分离和鉴定。
三、实验材料与仪器1. 实验材料:(1)BL21(DE3)pLysS大肠杆菌菌株,含有待表达的外源蛋白基因。
(2)裂解缓冲液:50 mM Tris pH 8.0,100 mM NaCl,1 mM EDTA。
(3)蛋白上样缓冲液:50 mM Tris pH 6.8,2% SDS,10% β-巯基乙醇,0.1% 亮蓝R250。
(4)SDS-PAGE凝胶制备试剂:丙烯酰胺、甲叉双丙烯酰胺、Tris、SDS、甘氨酸等。
(5)电泳设备:垂直电泳仪、电泳槽、电源等。
(6)层析设备:层析柱、层析板、紫外检测仪等。
2. 实验仪器:(1)超声波破碎仪(2)离心机(3)恒温水浴锅(4)移液器(5)微量移液器(6)紫外分光光度计(7)凝胶成像系统四、实验步骤1. 菌株培养与诱导表达(1)将BL21(DE3)pLysS大肠杆菌菌株接种于LB液体培养基中,37℃培养过夜。
(2)将过夜培养的菌液按1:100比例接种于LB液体培养基中,37℃培养至OD600约为0.6。
(3)加入IPTG诱导剂,使终浓度为0.5 mM,37℃培养4小时。
2. 包涵体蛋白的提取(1)将诱导表达的菌液在冰浴中冷却30分钟。
(2)将菌液以5000 rpm离心10分钟,收集菌体。
(3)将菌体用裂解缓冲液重悬,超声破碎45秒,重复两次。
(4)以10000 rpm离心30分钟,收集上清液。
3. 包涵体蛋白的纯化(1)将上清液加入等体积的蛋白上样缓冲液,煮沸5分钟。
(2)以10000 rpm离心5分钟,收集沉淀。
(3)将沉淀用蛋白上样缓冲液重悬,加入SDS-PAGE凝胶制备试剂,混匀。
4. 包涵体蛋白的分离与鉴定(1)制备SDS-PAGE凝胶,按照分子克隆上的配方,采用变性不连续凝胶电泳。


生物分离工程:,从生物产品的生产技术来看:指生物产品的下游加工过程(Down stream processing)。
➢从生物工程的新技术看,主要指工程菌和动植物细胞产品的分离与纯化。
➢从研究对象看,主要指生物大分子产品的分离与纯化。
➢➢➢包涵体(inclusion body):外源蛋白质在大肠杆菌中高效表达时常形成不可溶、无生物活性的聚集体。
➢初级分离是指从发酵液、细胞培养液、胞内抽提液(细胞破碎液)及其他各种生物原料初步提取目标产物,使目标产物得到浓缩和初步分离的下游加工过程。
➢胶体是一种尺寸在1~100 nm以至1000 nm的分散体。
它既非大块固体,又不是分子分散的液体,而是具有两相的微不均匀分散体系。
➢沉淀定义:物理环境的变化引起溶质溶解度降低,生成固体凝聚物(aggregrates)的现象➢盐析:蛋白质在高离子强度的溶液中溶解度降低、发生沉淀的现象称为盐析。
➢利用蛋白质在pH值等于其等电点的溶液中溶解度下降的原理进行沉淀分级的方法称为等电点沉淀法➢泡沫分离:根据表面吸附的原理,利用通气鼓泡在液相中形成的气泡为载体对液相中的溶质和颗粒进行分离,又称泡沫吸附分离,泡沫分级或鼓泡分级。
➢在一种流体相间内或者两种流体相间,有一层薄的凝聚相物质,其把流体相分隔开来成为两部分,并在两部分之间进行传质作用,这一薄层物质称为膜。
➢膜分离技术➢利用膜的选择性(孔径大小),以膜的两侧存在的能量差作为推动力,由于溶液中各组分透过膜的迁移率不同而实现分离的一种技术。
➢微滤( Microfiltration ,MF):以多孔细小薄膜为过滤介质,压力差为推动力,使不溶性物质得以分离的操作,孔径分布范围在0.025~14μm之间;➢超滤( Ultrafiltration ,UF):分离介质同上,但孔径更小,为0.001~0.02 μm,分离推动力仍为压力差,适合于分离酶、蛋白质等生物大分子物质;➢反渗透(Reverse osmosis, RO):是一种以压力差为推动力,从溶液中分离出溶剂的膜分离操作,孔径范围在0.0001~0.001 μm之间;(由于分离的溶剂分子往往很小,不能忽略渗透压的作用,故而成为反渗透);➢纳滤(Nanofiltration,NF ):以压力差为推动力,从溶液中分离300~1000小分子量的膜分离过程,孔径分布在平均2nm;➢电渗析(Electrodialysis,ED):以电位差为推动力,利用离子交换膜的选择透过性,从溶液中脱除或富集电解质的膜分离操作;➢超滤:根据高分子溶质之间或高分子与小分子溶质之间分子量的差别进行分离的方法。

包涵体蛋白纯化步骤引言:包涵体蛋白纯化是生物技术和生物制药领域中重要的工艺步骤之一。
通过纯化包涵体蛋白,可以获得高纯度的目标蛋白,为后续的研究和应用提供了基础。
本文将介绍包涵体蛋白纯化的一般步骤,包括细胞破碎、包涵体回收、包涵体溶解、亲和层析和蛋白质再折叠等。
一、细胞破碎:细胞破碎是包涵体蛋白纯化的第一步。
通常使用机械方法(如超声波破碎或高压均质)或化学方法(如洗涤剂破碎)来破碎细胞,释放包涵体蛋白。
需要注意的是,破碎条件应该使得包涵体蛋白能够充分溶解而不会发生蛋白质降解。
二、包涵体回收:包涵体蛋白通常以包涵体的形式存在于细胞裂解液中。
包涵体回收是将包涵体从其他细胞成分中分离出来的过程。
一种常用的方法是通过离心将细胞碎片和其他细胞成分与包涵体分离。
此外,还可以使用过滤、沉淀或超滤等技术来实现包涵体的回收。
三、包涵体溶解:包涵体蛋白在还原条件下通常以不溶性的形式存在。
为了使包涵体蛋白能够溶解,通常需要添加变性剂(如尿素或胍氯酸)和还原剂(如二硫醇)。
通过调节溶解条件,可以使得包涵体蛋白迅速溶解为可溶性蛋白。
四、亲和层析:亲和层析是包涵体蛋白纯化的关键步骤之一。
通过将目标蛋白与亲和层析介质上的亲和配体结合,可以实现目标蛋白的富集和纯化。
亲和配体可以是金属离子、抗体或亲和标签等。
在亲和层析过程中,需要注意选择合适的亲和配体和适宜的洗脱条件,以实现对目标蛋白的高效纯化。
五、蛋白质再折叠:由于包涵体蛋白在还原条件下溶解,其折叠状态通常不完整。
为了使得目标蛋白具有正确的结构和功能,需要对其进行再折叠。
常用的再折叠方法包括逐渐降低变性剂浓度、添加折叠辅助剂和调节pH 值等。
通过适当的再折叠条件,可以使得目标蛋白恢复到天然的折叠状态。
结论:包涵体蛋白纯化是一项复杂的工艺步骤,需要经过细胞破碎、包涵体回收、包涵体溶解、亲和层析和蛋白质再折叠等步骤。
通过这些步骤的有序进行,可以得到高纯度和高活性的包涵体蛋白。
随着生物技术和生物制药的不断发展,对包涵体蛋白纯化技术的要求也越来越高,希望通过不断的研究和创新,能够进一步提高包涵体蛋白纯化的效率和纯度,为生物医药领域的研究和应用提供更好的支持。

一、菌体的裂解1、怎样裂解细菌?细胞的破碎方法1.高速组织捣碎:将材料配成稀糊状液,放置于筒约1/3体积,盖紧筒盖,将调速器先拨至最慢处,开动开关后,逐步加速至所需速度。
此法适用于动物脏组织、植物肉质种子等。
2.玻璃匀浆器匀浆:先将剪碎的组织置于管中,再套入研杆来回研磨,上下移动,即可将细胞研碎,此法细胞破碎程度比高速组织捣碎机为高,适用于量少和动物脏器组织。
3.超声波处理法:用一定功率的超声波处理细胞悬液,使细胞急剧震荡破裂,此法多适用于微生物材料,用大肠杆菌制备各种酶,常选用50-100毫克菌体/毫升浓度,在1KG至10KG 频率下处理10-15分钟,此法的缺点是在处理过程会产生大量的热,应采取相应降温措施,时间以及超声间歇时间、超声时间可以自己调整,超声完全了菌液应该变清亮,如果不放心可以在显微镜下观察。
对超声波及热敏感的蛋白和核酸应慎用。
4.反复冻融法:将细胞在-20度以下冰冻,室温融解,反复几次,由于细胞冰粒形成和剩余细胞液的盐浓度增高引起溶胀,使细胞结构破碎。
5.化学处理法:有些动物细胞,例如肿瘤细胞可采用十二烷基磺酸钠(SDS)、去氧胆酸钠等细胞膜破坏,细菌细胞壁较厚,可采用溶菌酶处理效果更好,我用的浓度一般为1mg/ml。
无论用哪一种方法破碎组织细胞,都会使细胞蛋白质或核酸水解酶释放到溶液中,使大分子生物降解,导致天然物质量的减少,加入二异丙基氟磷酸(DFP)可以抑制或减慢自溶作用;加入碘乙酸可以抑制那些活性中心需要有疏基的蛋白水解酶的活性,加入苯甲磺酰氟化物(PMSF)也能清除蛋白水解酶活力,但不是全部,而且应该在破碎的同时多加几次;另外,还可通过选择pH、温度或离子强度等,使这些条件都要适合于目的物质的提取。
这是标准配方:裂解液:50mM Tris-HCl(pH8.5~9.0),2mM EDTA,100mM NaCl,0.5%Triton X-100,1mg/ml溶菌酶。
(溶菌酶在这个pH围比较好发挥作用)但我个人的经验是:如果你裂解细菌是为了提取蛋白的话,而且蛋白的分子量又小于20kd的话,尽量减少溶菌酶的用量,会引入溶菌酶这种杂蛋白.一般配60ml裂解液用药匙匙柄盛一点就够.判断裂解好坏的标准是,溶液很粘.protocol是10ml-50ml缓冲液(菌体洗涤液,裂解液等)/1g湿菌体.如果只做一个鉴定,我觉得100-200ml菌就够了.但凡超声,我都用60ml裂解液,因为我们的超声仪(现代分子生物学实验技术录象里的那种)很适合用100ml小烧杯,装60ml裂解液,这样能让超声头离液面不高不低,不会冒泡泡,也不会洒出来.菌多我就延长超声时间.沉淀,也就是包涵体沉淀了,如果要上柱纯化,一定要先用4M尿素洗涤一下再用8M尿素溶解.如果不上柱,只是跑跑电泳,可以直接用8M尿素溶解以后,离心取上清,加入适量体积的loading buffer.loading buffer对于包涵体的溶解能力是较弱的."取200微升菌液,离心后直接加上样buffer,100度3分钟后上样,然后SDSPAGE.这个方法到底能不能溶解细菌中的包涵体?"而楼主的问题,虽然loading buffer对于包涵体的溶解能力是较弱的,但是我觉得你的做法只是在鉴定有无表达,用loading buffer是没有问题的.2、表达重组蛋白时,细菌裂解方法都有哪些?在表达重组蛋白时,诱导以后跑SDS-PAGE发现表达都很好,但是在裂解细胞时遇到问题。
题型:问答简答综合内容1.固液分离(沉降、离心、过滤、膜分离)比较,适用对象2.液-液传质分离(萃取、双水相、反胶束、超临界、泡沫分离)3.如何减少,避免失活问题双水相反胶束4.分离原理适用对象特点5.细胞破碎特点3.发酵液的预处理和菌体的回收(为什么进行预处理;预处理方法;过滤器的主要特点)3.2悬浮液的预处理(原因)原因:1.产品在培养液或菌体中浓度低2.产品与许多杂质混在一起3.非牛顿型流体目的:1.改变发酵液的物理性质,提高从悬浮液中分离固形物的速率,提高固液分离器的效率。
2.尽可能使产物转入便于后处理的某一相中(多数是液相)。
3.去除发酵液中部分杂质,以利于后续各步操作。
方法:1.加热法:①降低粘度②提供能量,促进细胞聚集③破坏凝胶结构——利于细胞聚集2.调节pH:①细胞聚集与pH值有关②简便,降低粘度③如何保持pH局部值不过高/低3.凝聚:(无机类电解质或高分子物质)表面电荷的简单中和,消除双电层,产生氢键结合。
4.絮凝:使用絮凝剂(天然或者合成的大分子量聚电解质以及生物絮凝剂)将胶体粒子联网,絮凝剂起架桥作用。
5.使用惰性助滤剂:一种颗粒均匀质地坚硬不可压缩的粒状物质,用于扩大过滤表面的适用范围。
3.4过滤法(主要特点型号)定义:过滤是迫使液体通过固体支撑物或过滤介质,把固体截留,从而达到固液分离的目的。
常用新型过滤器:1.真空过滤器:转鼓(优点:用于大规模生物分离的主要过滤设备,可以分离较难过滤的悬浮固粒,劳动强度小;缺点:表面利用率低,洗涤效果差,滤饼卸料时易剥落;滤布更换困难,不便观察)水平带式(优点:处理量大,操作灵活,洗涤效果好;占地面积大;缺点:有效过滤面积小,投资较高)水平圆盘(大型化,洗涤效果好)水平回转翻盘(大型化,适用于过滤密度大,浓度高的粗颗粒悬浮液)2.压滤器(适用于固含量高难处理的细颗粒料液):板框压滤器加压叶滤器气压罐式连续压滤器带式压滤器3.错流过滤:料液给过滤介质表面一个平行的大流量的冲刷,则过滤介质表面积累的滤饼就会减少到可以忽略的程度,而通过过滤介质的流速则比较小。
包涵体名词解释
包涵体是外源基因在原核细胞中表达时,尤其在大肠杆菌中高效表达时,形成的由膜包裹的高密度、不溶性蛋白质颗粒,在显微镜下观察时为高折射区,与胞质中其他成分有明显区别。
简介
与一般微生物细胞相比,基因工程菌的细胞破碎要复杂得多。
基因工程菌新合成的重组蛋白,是没有活性的、折叠构型有误的蛋白质,叫包涵体。
细胞破碎后先分离出包涵体,将包涵体溶解在变性剂中。
再加入还原剂,还原蛋白质中的半胱氨酸,使二硫键断裂,得到单体肽链再复性重新折叠。
特性
一般含有50%以上的重组蛋白,其余为核糖体元件、RNA聚合酶、外膜蛋白ompC、ompF和ompA等,环状或缺口的质粒DNA,以及脂体、脂多糖等,大小为0.5-1um,难溶于水,只溶于变性剂如尿素、盐酸胍等。
病毒包涵体
包涵体有的位于细胞质中(如天花病毒包涵体)。
有的包涵体还具有特殊名称,如天花病毒包涵体叫顾氏(Guarnieri)小体,狂犬病毒包涵体叫内基氏(Vegri)小体。
版权声明:本站几乎所有资源 搜集于网络,仅供学习参考,不得进行任何商业用途,否则产生的一切后 果将由使用者本人承担! 本站仅仅提供一个观摩学习与交流的平台, 将不保证所提供资源的完 整性,也不对任何资源负法律责任。
所有资源请在下载后 24 小时内删除。
如果您觉得满意, 请购买正版,以便更好支持您所喜欢的软件或书籍!☆☆☆☆☆生物秀[]☆☆☆☆☆中国生物科学论 [/bbs/]☆☆☆☆☆生物秀下载频道[/Soft/]生物秀——倾力打造最大最专业的生物资源下载平台!■■■ 选择生物秀,我秀我精彩!!■■■欢迎到生物秀论 (中国生物科学论 )的相关资源、软件版 参与讨论,共享您的资源,获 取更多资源或帮助。
二、Hela细胞核提取物的Sephacry S-300 HR柱层析98实验3 序列特异性DNA亲和层析101一、用制备凝胶电泳纯化寡核苷酸 105二、DNA亲和介质的制备107三、亲和层析中非特异性竞争DNA的正确使用112四、亲和层析的操作 113实验4 DNA酶I足迹分析117一、DNA酶I足迹探针的制备118二、DNA酶I足迹分析122实验5 凝胶迁移变动分析126实验6 肝素-Sepharose CL-2B的制备129试剂的配制 131参考文献 138第3单元 大肠杆菌中过表达重组蛋白的纯化 Richard R. Burgess和Mark W. Knuth141实验1 大肠杆菌细胞的破碎和包涵体的配制144实验2 包涵体沉淀的溶解、重折叠和离子交换层析148 实验3 可溶性提取物(核心RNA聚合酶-复合物)的聚乙烯亚胺沉淀和免疫亲和层 152 析一、PEI沉淀法分级分离可溶性提取物153二、免疫亲和层析 154实验4 定量测定与制备小结158一、蛋白质的定量测定 158二、定量SDS凝胶染色与扫描159三、定量蛋白质斑点印迹 160四、酶测定法 163五、纯化记录表 164六、蛋白质纯化总结表与主要组分的总电泳照片 165实验5 蛋白质的鉴定167一、纯蛋白质的紫外光谱——A280mm/A260nm167二、消光系数的测定(Scopes法)167三、过载染色SDS凝胶扫描法估测纯度169四、由非变性凝胶电泳迁移率法评估均一性 169方案补充实验:从过表达细菌提纯 172一、快速蛋白质斑点印迹试验 172二、是可溶的还是不溶的? 173三、溶解包涵体沉淀需多少N-十二烷基肌氨酸钠? 173四、沉淀和RNA聚合酶需多少聚乙烯亚胺?174五、从PEI沉淀洗脱和RNA聚合酶需多少盐?175六、透析法除N-十二烷基肌氨酸钠需多少时间? 176五、胰岛素受体对胰岛素亲和性的测定 202实验2 膜胰岛素受体的溶解205一、胰岛素受体的溶解及活性测定 211二、溶解膜蛋白用的去垢剂的筛选 213实验3 溶解受体的凝集素亲和层析215实验4 部分纯化受体的胰岛素亲和层析219一、胰岛素亲和层析 220二、配体与活化介质的偶联 221实验5 胰岛素受体与胰岛素的交联223实验6 胰岛素激素的胰岛素受体自磷酸化226实验7 胰岛素受体糖基化的分析229试剂的配制 234参考文献 240附录 243附录1 pH的测量243附录2 缓冲液的配制245附录3 电导率的测量247附录4 固态硫酸铵法分级分离248附录5 蛋白质的SDS-PAGE电泳249一、电泳 251二、凝胶染色 256三、样品制备(沉淀法) 259附录6 蛋白质的过甲酸氧化263附录7 用亚氨基二乙酸Sepharose 6B分离磷酸肽265附录8 蛋白质内序分析用肽段的分离与纯化267附录9 推荐读物269技术索引 271主题索引 273。