2010版《中国药典》纯化水标准及检测项目
- 格式:doc
- 大小:34.50 KB
- 文档页数:3
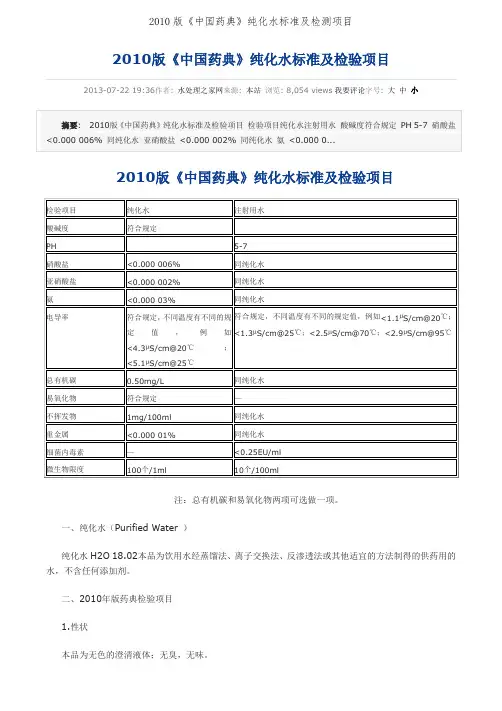
2010版《中国药典》纯化水标准及检验项目2013-07-22 19:36作者: 水处理之家网来源: 本站浏览: 8,054 views我要评论字号: 大中小注:总有机碳和易氧化物两项可选做一项。
一、纯化水(Purified Water )纯化水H2O 18.02本品为饮用水经蒸馏法、离子交换法、反渗透法或其他适宜的方法制得的供药用的水,不含任何添加剂。
二、2010年版药典检验项目1.性状本品为无色的澄清液体;无臭,无味。
取本品10ml,加甲基红指示液2滴,不得显红色;另取10ml,加溴麝香草酚蓝指示液5滴,不得显蓝色。
3.硝酸盐取本品5ml置试管中,于冰浴中冷却,加10%氯化钾溶液0.4ml与0.1%二苯胺硫酸溶液0.1ml,摇匀,缓缓滴加硫酸5ml,摇匀,将试管于50℃水浴中放置15分钟,溶液产生的蓝色与标准硝酸盐溶液[取硝酸钾0.163g,加水溶解并稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,再精密量取10ml,加水稀释成100ml,摇匀,即得(每1ml相当于1μgNO3)]0.3ml,加无硝酸盐的水4.7ml,用同一方法处理后的颜色比较,不得更深(0.000 006%)。
4.亚硝酸盐取本品10ml,置纳氏管中,加对氨基苯磺酰胺的稀盐酸溶液(1→100)1ml及盐酸萘乙二胺溶液(0.1→100)1ml,产生的粉红色,与标准亚硝酸盐溶液[取亚硝酸钠0.750g(按干燥品计算),加水溶解,稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,摇匀,再精密量取1ml,加水稀释成50ml,摇匀,即得(每1ml相当于1μgNO2))0.2ml,加无亚硝酸盐的水9.8ml,用同一方法处理后的颜色比较,不得更深(.0000 02%)。
5.氨取本品50ml,加碱性碘化汞钾试液2ml,放置15分钟;如显色,与氯化铵溶液(取氯化铵31.5mg,加无氨水适量使溶解并稀释成1000ml)1.5ml,加无氨水48ml与碱性碘化汞钾试液2ml制成的对照液比较,不得更深(0.000 03%)。
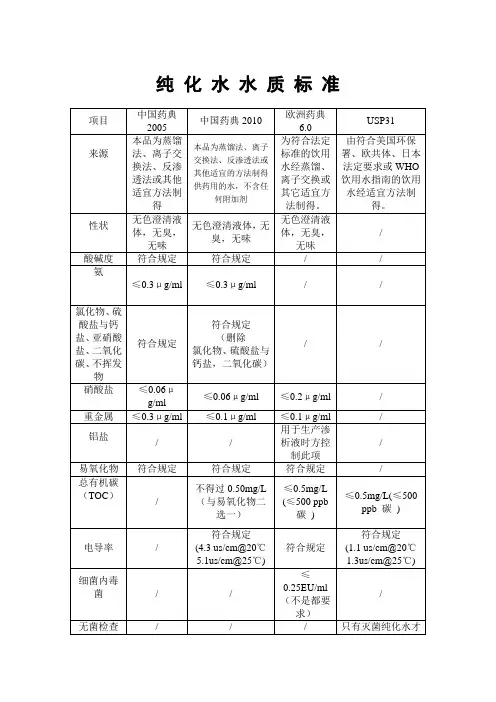
纯化水水质标准
注射用水水质标准
解读2010年版《中国药典》(八)新版药典对纯化水、注射用水和灭菌注射用水检验新增电导率和总有机碳两个检查项目
制药企业的生产工艺用水,涉及到制剂生产过程当中容器清洗、配液及原料药精制纯化等所需要使用的水,此类用水一般分成纯化水和注射用水两大类。
2010年版《中国药典》对纯化水、注射用水和灭菌注射用水的检验项目作了修订。
特别值得关注的是新增了电导率和总有机碳两个检查项目。
电导率和总有机碳的指标在一定意义上说明的是对水污染的监控。
当水中含有无机酸、碱、盐或有机带电胶体时,电导率就增加。
检查制药用水的电导率可在一定程度上控制水中电解质总量。
而各种有机污染物,微生物及细菌内毒素经过催化氧化后变成二氧化碳,进而改变水的电导,电导的数据又转换成总有机碳的量。
如果总有机碳控制在一个较低的水平上,意味着水中有机物、微生物及细菌内毒素的污染处于较好的受控状态。
没有检测电导率和总有机碳可能会有什么后果?1, 不知道药品已受污染,以及不知道什么原因和什么时候受到污染;2, 纯水系统的过滤装置需要更换而不知道;3, 管路设计上存在死角滋长微生物而不知道;4,引入新杂质不能通过验证。
这也是将这两项指标作为检查项目的重要原因。
这两项指标的增订使得我国药品标准进一步与国际接轨,对制药企业和监督检验部门都提出了更高的要求。

水系统1、概述水在制药工业中是应用最广泛的工艺原料,用做药品的成份、溶剂、稀释剂等。
制药用水作为制药原料,各国药典定义了不同质量标准和使用用途的工艺用水,并要求定期检测。
水极易滋生微生物并助其生长,微生物指标是其最重要的质量指标,在水系统设计,安装,验证,运行和维护中需采取各种措施抑制其生长。
水是良好的溶剂、尤其是与自然界失去平衡的纯化水和注射用水,具有极强的溶解能力和极少的杂质,广泛用于制药设备和系统的清洗。
鉴于水在制药工业中的既作为原料又作为清洗剂,各国药典对制药用水的质量标准,用途都有明确的定义和要求;各个国家和组织的GMP将制药用水的生产和储存分配系统视为制药生产的关键系统,对其设计,安装,验证,运行和维护等提出明确要求。
在指南第二章将具体介绍我国和其他国家药典和GMP对制药用水的要求。
我国幅员辽阔,各地水质不同,季节的变化也会导致水质的巨大变化,我国制药企业使用的最初原料水未必常年符合饮用水的标准要求,需将其依次处理成饮用水,纯化水,注射用水等制药用水,适合不同的工艺需求。
在指南第三章中将介绍制药用水处理的各种技术,工艺和设备。
制药生产中其它原料、辅料、包装材料是按批检验和释放的,而作为原料的制药用水(饮用水,纯化水或注射用水)通常是通过管道连续流出的,随时取用的,其微生物属性等质量指标通常无法连续地实时检测到。
通常是先使用到产品中,若干天后才能知道其微生物指标是否合格,为保证制药用水系统生产出的水在任何时候是好的,即水系统生产质量的稳定性和一致性是各国药品监管部门和制药企业共同关注的重大问题。
各国GMP对水系统的设计和验证有严格要求,第四章将介绍水系统的设计和验证。
在水系统的设计、验证和运行过程中,制药企业、药监部门都遇到各种各样的疑问、问题和争议,我们参照国际组织尤其是ISPE(国际制药工程协会)的指南和工程实践,在第五章对常见问题进行了讨论。
第六章介绍一些关于水的化学和微生物知识以及水系统的钝化技术。

水系统1、概述水在制药工业中是应用最广泛的工艺原料,用做药品的成份、溶剂、稀释剂等。
制药用水作为制药原料,各国药典定义了不同质量标准和使用用途的工艺用水,并要求定期检测。
水极易滋生微生物并助其生长,微生物指标是其最重要的质量指标,在水系统设计,安装,验证,运行和维护中需采取各种措施抑制其生长。
水是良好的溶剂、尤其是与自然界失去平衡的纯化水和注射用水,具有极强的溶解能力和极少的杂质,广泛用于制药设备和系统的清洗。
鉴于水在制药工业中的既作为原料又作为清洗剂,各国药典对制药用水的质量标准,用途都有明确的定义和要求;各个国家和组织的GMP将制药用水的生产和储存分配系统视为制药生产的关键系统,对其设计,安装,验证,运行和维护等提出明确要求。
在指南第二章将具体介绍我国和其他国家药典和GMP对制药用水的要求。
我国幅员辽阔,各地水质不同,季节的变化也会导致水质的巨大变化,我国制药企业使用的最初原料水未必常年符合饮用水的标准要求,需将其依次处理成饮用水,纯化水,注射用水等制药用水,适合不同的工艺需求。
在指南第三章中将介绍制药用水处理的各种技术,工艺和设备。
制药生产中其它原料、辅料、包装材料是按批检验和释放的,而作为原料的制药用水(饮用水,纯化水或注射用水)通常是通过管道连续流出的,随时取用的,其微生物属性等质量指标通常无法连续地实时检测到。
通常是先使用到产品中,若干天后才能知道其微生物指标是否合格,为保证制药用水系统生产出的水在任何时候是好的,即水系统生产质量的稳定性和一致性是各国药品监管部门和制药企业共同关注的重大问题。
各国GMP对水系统的设计和验证有严格要求,第四章将介绍水系统的设计和验证。
在水系统的设计、验证和运行过程中,制药企业、药监部门都遇到各种各样的疑问、问题和争议,我们参照国际组织尤其是ISPE(国际制药工程协会)的指南和工程实践,在第五章对常见问题进行了讨论。
第六章介绍一些关于水的化学和微生物知识以及水系统的钝化技术。

中国药典纯化水检验标准一、酸碱度按照中国药典规定,纯化水的酸碱度应该符合以下要求:pH值在5.0-7.0之间,以保证其符合药典规定的范围。
测试酸碱度的样品应该在使用之前进行取样,并且使用酸碱度试纸进行检测。
二、硝酸盐硝酸盐是纯化水中常见的污染物之一,其含量过高会对药品的质量产生影响。
因此,中国药典规定纯化水中的硝酸盐含量不得超过0.00005%。
测试硝酸盐的样品应该在使用之前进行取样,并且使用硝酸盐试纸进行检测。
三、亚硝酸盐亚硝酸盐也是纯化水中常见的污染物之一,其含量过高会对人体健康产生影响。
因此,中国药典规定纯化水中的亚硝酸盐含量不得超过0.00001%。
测试亚硝酸盐的样品应该在使用之前进行取样,并且使用亚硝酸盐试纸进行检测。
四、氨氨是一种有毒物质,其含量过高会对人体健康产生影响。
因此,中国药典规定纯化水中的氨含量不得超过0.00005%。
测试氨的样品应该在使用之前进行取样,并且使用氨试纸进行检测。
五、氯化物氯化物是纯化水中常见的污染物之一,其含量过高会对药品的质量产生影响。
因此,中国药典规定纯化水中的氯化物含量不得超过0.001%。
测试氯化物的样品应该在使用之前进行取样,并且使用氯化物试纸进行检测。
六、硫酸盐硫酸盐是纯化水中常见的污染物之一,其含量过高会对药品的质量产生影响。
因此,中国药典规定纯化水中的硫酸盐含量不得超过0.001%。
测试硫酸盐的样品应该在使用之前进行取样,并且使用硫酸盐试纸进行检测。
七、钙钙是纯化水中常见的污染物之一,其含量过高会对药品的质量产生影响。
因此,中国药典规定纯化水中的钙含量不得超过0.002%。
测试钙的样品应该在使用之前进行取样,并且使用钙试纸进行检测。
八、镁镁是纯化水中常见的污染物之一,其含量过高会对药品的质量产生影响。
因此,中国药典规定纯化水中的镁含量不得超过0.002%。
测试镁的样品应该在使用之前进行取样,并且使用镁试纸进行检测。

纯化水检验规范1目的:为纯化水日常监测和周期检测制定依据,以便有效控制纯化水质量;2范围:适用于纯化水日常监测和周期检测管理。
3日常监测3.1正常取水时,操作人员观察纯水机电导率、水温、TOC等数据显示,每班记录一次,并依据《中国药典》纯化水相关规定(附件1),判定结果;3.2如果操作过程中出现指标不合格等异常状况,应协同相关技术或负责人员,参阅《使用说明书》等资料,及时处理和维修,难以解决的疑难问题,联系厂家来完成;4周期检测4.1每周检验人员,在正常使用情况下,出水口和蓄水处取样一次,对电导率进行离线检测,并依据《中国药典》纯化水相关规定(附件1),判定结果,出具报告;4.2在经过必要验证确认的前提下,每年至少按照《中国药典》纯化水相关规定(附件1),做一次全项检测,并依据《中国药典》纯化水相关规定(附件1),判定结果,出具报告;附件12010版《中国药典》纯化水质量标准本品为饮用水经蒸馏法、离子交换法、反渗透法或其他适宜的方法制得的制药用水,不含任何添加剂。
【性状】本品为无色的澄清液体;无臭,无味。
【检查】酸碱度取本品10ml,加甲基红指示液2滴,不得显红色;另取10ml,加溴麝香草酚蓝指示液5滴,不得显蓝色。
硝酸盐取本品5ml置试管中,于水浴中冷却,加10%氯化钾溶液0.4ml与0.1%二苯胺硫酸溶液0.1ml,摇匀,缓缓滴加硫酸5ml,摇匀,将试管于50℃水浴中放置15分钟,溶液产生的蓝色与标准硝酸盐溶液[取硝酸钾0.163g,加水溶解并稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,再精密量取10ml,加水稀释成100ml,摇匀,即得(每1ml相当于1ugNO3)]0.3ml,加无硝酸盐的水4.7ml,用同一方法处理后的颜色比较,不得更深(0.000006%)。
亚硝酸盐取本品10ml,置纳氏管中,对氨基苯磺酰胺的稀盐酸溶液(1→100)1ml与盐酸萘乙二胺溶液(0.1→100)1ml,产生粉红色,与标准亚硝酸盐溶液[取亚硝酸钠0.75g(按干燥品计算),加水溶解,稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,摇匀,再精密量取1ml,加水稀释成50ml,摇匀,即得(每1ml相当于1ugNO2)]0.2ml,加无亚硝酸盐的水9.8ml,用同一方法处理后的颜色比较,不得更深(0.000002%)。


中国药典纯化水标准
中国药典纯化水,是指符合中国药典规定的水质标准,用于药品生产中的洁净
生产环境和药品生产中的洗涤、溶解、稀释等工艺过程。
中国药典纯化水标准的制定,旨在保障药品生产过程中水质的安全、纯净、稳定,确保药品质量的稳定和安全。
中国药典纯化水标准主要包括外观、物理性质、化学性质、微生物限度等多个
方面的指标。
在外观方面,要求水质清澈透明,无悬浮物和沉淀物。
在物理性质方面,要求水质无色无味,不含有害物质,电导率低,矿化度低。
在化学性质方面,要求水质无重金属、无机盐、有机物质等有害成分。
在微生物限度方面,要求水质无细菌、霉菌和其他微生物。
中国药典纯化水标准的制定,是为了保障药品生产过程中水质的安全和稳定。
水作为药品生产过程中的重要原料,其质量直接影响药品的质量和安全,因此,严格执行中国药典纯化水标准,对于保障药品质量和安全具有重要意义。
在实际生产中,要严格按照中国药典纯化水标准执行,建立健全水质管理体系,加强水质监测和检验,确保生产用水符合标准要求。
同时,加强设备维护和清洁,确保生产设备和管道不会对水质造成污染。
加强员工培训,提高操作技能,做好生产过程中的水质控制和管理。
总之,中国药典纯化水标准的制定和执行,对于保障药品生产过程中水质的安
全和稳定具有重要意义。
只有严格执行标准要求,加强水质管理,才能确保药品质量和安全,保障人民群众的用药安全。
希望各药品生产企业能够重视中国药典纯化水标准,切实加强水质管理,提高药品质量,为人民群众的健康保驾护航。


2010版药典纯化水设备制作要求及标准1purpose目的本URS文件规定了纯化水系统的用户需求,总括了用户对该设备的功能、性能、制造及标准等方面的要求。
本URS文件是构建起项目和系统的文件体系的基础,同时也是验收的主要依据。
2scope范围本URS文件的范围自原水进水阀开始至纯水灭菌后输出的整个纯水制备系统。
包括设备配电控制柜、电仪系统、原水进水自动阀、纯化水泵、臭氧灭菌器等。
3responsibility职责质量部质量工程师负责编写和发行本URS文件。
设备部厂务工程师负责按本URS文件确认和验收纯化水系统。
4referencedocuments参考文件《中华人民共和国药典》2010年版《中华人民共和国药品质量管理规范(2010年版)》《钢制件焊接常压容器》JB/T4735-95GB/T19249-2003反渗透水处理设备GB/T《机械产品电气安全要求通用要求》5Procedure程序使用要求URSNo: 需求编号Requirements需求Require/Expect必须/期望URS001 纯化储罐水量:吨必须URS002 制水机产水量:吨/小时必须URS003 纯化水指标:符合中国药典(2010版)纯化水指标必须URS004 生产出水点:5个(生产洁净区3个,实验室2个)必须技术要求工艺技术总要求URSNo: 需求编号Requirements需求Require/Expect必须/期望URS005 纯化水质符合《中华人民共和国药典》2010年版要求电导率小于2μS/cm(25℃,在线控制),TOC控制在L内(离线控制),不挥发物小于1mg/100ml,微生物限度100个/1ml,pH5-7,硝酸盐<006%,亚硝酸盐<002%,氨<03%,重金属<01%必须URS006 纯化水制备系统的设计基于如下原水数据:按城市饮用水供水水质进行设计必须URS007 系统设计应最大限度地减少微生物生长的可能,应最大限度地减少系统死点必须URS008 任何与纯化水接触的材料必须满足GMP的要求,所用钢材必须是304L以上不锈钢必须/304卫生级管件URS009 整个系统必须具备可靠的消毒功能必须URS010 为了控制纯化水产品的质量,必须控制总送水、原水储罐和总回水。

制药用水检测项目及注意事项第一部分、制药用水所检项目有哪些?制药用水根据不同的使用范围分为饮用水、纯化水、注射用水和灭菌注射用水。
这里我们只针对纯化水(PW)和注射用水(WFI)进行分析讨论。
根据中国药典规定,PW需检验项目为:性状、酸碱度、氨、硝酸盐、亚硝酸盐、电导率、总有机碳(TOC)、不挥发物、重金属、微生物限度。
WFI所需检验项目与PW相比,将酸碱度更换为pH值,增加了细菌内毒素控制,其余检验项目与PW基本相同,但是微生物的控制标准要严于PW的标准。
第二部分、微生物限度检测方法的确认根据非无菌产品微生物限度检测方法的要求,应进行培养基适用性检查和计数方法适用性试验。
纯化水培养基适用性检查方面,相应进行R2A琼脂培养基的适用性检查,菌株为铜绿假单胞菌和枯草芽孢杆菌。
以及无菌培养试验。
方法:取不大于100cfu菌液,于购买的R2A琼脂培养基,快速涂布,每一菌株平行2个平板。
同样操作涂布与中检院购买的对照培养基,培养5天。
无菌培养试验:取2平皿,作为阴性对照培养。
标准:被测培养基上的菌落平均数与对照培养基上的菌落平均数比值应在0.5-2之间,菌落形态、大小一致。
无菌培养,培养基上无微生物生长。
纯化水计数方法适用性方面,水作为无抑菌作用的溶剂,进行微生物回收试验意义不大,因此,应不进行计数方法适用性试验。
R2A培养基,营养欠丰富,有利于损伤微生物的回收,培养时间不低于5天。
第三部分、准备工作注意哪些?(1)仪器设备及耗材:检测前要根据所要检测的项目,检查所用仪器/设备(如天平、pH计、电导率仪、培养箱等)是否经过了校准,是否在校准效期内,有些仪器还需要使用前校准或日校,比如天平,pH计。
微生物限度检验所用的生物安全柜(或超净工作台)、微生物过滤系统和培养箱应保证在确认效期内。
用到的关键耗材,如微孔滤膜及滤杯等物料应保证其无菌性,可购买一次性无菌过滤器,也可在经验证的灭菌程序下灭菌,并在经验证的有效期内使用,但微孔滤膜不建议用户自行湿热灭菌,因为湿热灭菌可能会引起滤膜孔径的改变,除非有充分的证据证明灭菌后的滤膜仍满足使用需求。
纯化水纯化水:本品为饮用水经蒸馏法、离子交换法、反渗透法或其他适宜的方法制得的制药用水,不含任何添加剂。
(药典411页)取样:微生物监测放水至少3分钟以上,理化检测放水20秒。
按干燥品计算:取未经干燥的供试品进行试验,并将计算中的取用量按检查项下测得的干燥失重(或水分或溶剂)扣除。
【检查】(1)酸碱度A、试剂的配制①甲基红指示液:取甲基红0.1g,加L氢氧化钠溶液使溶解,再加水稀释至200ml,即得。
变色范围(红→黄)。
(药典附录177)L氢氧化钠溶液:取固体氢氧化钠0.2g,加水稀释至100ml,即得。
水:试验用水,除另有规定外,均系指纯化水。
酸碱度检查所用的水,均系指新沸并放冷至室温的水。
(药典凡例三十二)②溴麝香草酚蓝指示液:取溴麝香草酚蓝,加L氢氧化钠溶液使溶解,再加水稀释至200ml,即得。
变色范围(黄→蓝)。
(药典附录178)B、检验方法:取本品10ml,加甲基红指示液2滴,不得显红色;另取10ml,加溴麝香草酚蓝指示液5滴,不得显蓝色。
(药典411页)(2)硝酸盐原理:二苯胺在酸性条件下被硝酸根离子氧化,生成蓝色的醌式联二苯。
A、试剂的配制①10%氯化钾溶液:称取氯化钾10.0g,加水使溶解成100ml,即得。
②%二苯胺硫酸溶液:称取二苯胺0.10g,加硫酸100ml使溶解,即得。
二苯胺试液:取二苯胺1g,加硫酸100ml使溶解,即得。
(药典附录170)③标准硝酸盐溶液:取硝酸钾,加水溶解并稀释至100ml,精密量取1ml,加水稀释成100ml,再精密量取10ml,加水稀释成100ml,摇匀,即得(每1ml相当于1μg NO3)。
(药典411页)④无硝酸盐与无亚硝酸盐的水:取无氨水或去离子水即得(检查:取本品50ml,加碱性碘化汞钾1ml,不得显色。
)(附录151)无氨水:取纯化水1000ml,加稀硫酸1ml与高锰酸钾试液1ml,蒸馏即得。
(附录151)(注意:在水中加入几滴浓硝酸pH<2使得各种形态的氨氮转化为不挥发的铵盐再进行蒸馏,前后200ml流出液都应弃去,只保留中间蒸出液。
《中国药典》(2010年版)规定:“纯化水为采用蒸馏法、离子交换法、反渗透法,EDI法或其他适宜的方法制得供药用的水。
”而不再仅局限于“蒸馏”这一种工艺。
药典这一改变是我国制药用水生产发展史上的一大进步,与世界先进国家的药典实现了接轨。
药典将注射用水规定为“纯化水经蒸馏所得的水”。
而USP已连续在7个版本中明确规定反渗透(reverse osmosis,RO)法可以作为制取注射用水的法定方法,显示了人们对采用膜技术生产制药用水的信心。
膜分离法生产制药用水是制药用水技术发展的必然趋势。
目前,国内、外多数制药企业采用离子交换及反渗透、离子交换联合等方法制得纯化水,再经蒸馏的方法制取注射用水。
上述制药用水生产工艺中,离子交换技术作为深度除盐手段仍被普遍采用。
但离子交换树脂再生时会产生大量废酸、废碱,严重污染环境,发展受到制约。
反渗透膜对水中的细菌、热原、病毒及有机物的去除率达到100%。
二级反渗透虽可以免除使用离子交换树脂,但对原水的含盐量要求极高,因为目前反渗透装置的系统脱盐率为98%左右,如果原水含盐量高,则产水电导率就会超过控制指标。
医药用纯水对水质要求相对来说更加严格,更加高。
常要求超纯水的电阻值应高于15兆以上。
为保证医药用超纯水的用水安全,超纯水的处理设备整个系统也都由全不锈钢材质组合而成,而且在用水点之前都必须装备杀菌装置。
我们公司从整个医药行业用超纯水的特点出发,针对不同用户对高纯水的不同要求,采用反渗透,EDI等最新工艺,比较有针对性地设计出成套高纯水处理工艺,以满足药厂、医院的纯化水制取、大输液制取的用水要求。
[编辑本段]分类制药用水(工艺用水:药品生产工艺中使用的水,包括饮用水、纯化水、注射用水)分类1)饮用水(Potable-Water):通常为自来水公司供应的自来水或深井水,又称原水,其质量必须符合国家标准GB 5749 -2006《生活饮用水卫生标准》。
按2010中国药典规定,饮用水不能直接用作制剂的制备或试验用水。
2010版《中国药典》纯化水标准及检验项目2013-07-22 19:36作者: 水处理之家网来源: 本站浏览: 8,054 views我要评论字号: 大中小注:总有机碳和易氧化物两项可选做一项。
一、纯化水(Purified Water )纯化水H2O 18.02本品为饮用水经蒸馏法、离子交换法、反渗透法或其他适宜的方法制得的供药用的水,不含任何添加剂。
二、2010年版药典检验项目1.性状本品为无色的澄清液体;无臭,无味。
取本品10ml,加甲基红指示液2滴,不得显红色;另取10ml,加溴麝香草酚蓝指示液5滴,不得显蓝色。
3.硝酸盐取本品5ml置试管中,于冰浴中冷却,加10%氯化钾溶液0.4ml与0.1%二苯胺硫酸溶液0.1ml,摇匀,缓缓滴加硫酸5ml,摇匀,将试管于50℃水浴中放置15分钟,溶液产生的蓝色与标准硝酸盐溶液[取硝酸钾0.163g,加水溶解并稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,再精密量取10ml,加水稀释成100ml,摇匀,即得(每1ml相当于1μgNO3)]0.3ml,加无硝酸盐的水4.7ml,用同一方法处理后的颜色比较,不得更深(0.000 006%)。
4.亚硝酸盐取本品10ml,置纳氏管中,加对氨基苯磺酰胺的稀盐酸溶液(1→100)1ml及盐酸萘乙二胺溶液(0.1→100)1ml,产生的粉红色,与标准亚硝酸盐溶液[取亚硝酸钠0.750g(按干燥品计算),加水溶解,稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,摇匀,再精密量取1ml,加水稀释成50ml,摇匀,即得(每1ml相当于1μgNO2))0.2ml,加无亚硝酸盐的水9.8ml,用同一方法处理后的颜色比较,不得更深(.0000 02%)。
5.氨取本品50ml,加碱性碘化汞钾试液2ml,放置15分钟;如显色,与氯化铵溶液(取氯化铵31.5mg,加无氨水适量使溶解并稀释成1000ml)1.5ml,加无氨水48ml与碱性碘化汞钾试液2ml制成的对照液比较,不得更深(0.000 03%)。
2010版《中国药典》纯化水标准及检验项目
2013-07-22 19:36作者: 水处理之家网来源: 本站浏览: 8,054 views我要评论字号: 大中小
注:总有机碳和易氧化物两项可选做一项。
一、纯化水(Purified Water )
纯化水H2O 18.02本品为饮用水经蒸馏法、离子交换法、反渗透法或其他适宜的方法制得的供药用的水,不含任何添加剂。
二、2010年版药典检验项目
1.性状
本品为无色的澄清液体;无臭,无味。
取本品10ml,加甲基红指示液2滴,不得显红色;另取10ml,加溴麝香草酚蓝指示液5滴,不得显蓝色。
3.硝酸盐
取本品5ml置试管中,于冰浴中冷却,加10%氯化钾溶液0.4ml与0.1%二苯胺硫酸溶液0.1ml,摇匀,缓缓滴加硫酸5ml,摇匀,将试管于50℃水浴中放置15分钟,溶液产生的蓝色与标准硝酸盐溶液[取硝酸钾0.163g,加水溶解并稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,再精密量取10ml,加水稀释成100ml,摇匀,即得(每1ml相当于1μgNO3)]0.3ml,加无硝酸盐的水4.7ml,用同一方法处理后的颜色比较,不得更深(0.000 006%)。
4.亚硝酸盐
取本品10ml,置纳氏管中,加对氨基苯磺酰胺的稀盐酸溶液(1→100)1ml及盐酸萘乙二胺溶液(0.1→100)1ml,产生的粉红色,与标准亚硝酸盐溶液[取亚硝酸钠0.750g(按干燥品计算),加水溶解,稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,摇匀,再精密量取1ml,加水稀释成50ml,摇匀,即得(每1ml相当于1μgNO2))0.2ml,加无亚硝酸盐的水9.8ml,用同一方法处理后的颜色比较,不得更深(.0000 02%)。
5.氨
取本品50ml,加碱性碘化汞钾试液2ml,放置15分钟;如显色,与氯化铵溶液(取氯化铵31.5mg,加无氨水适量使溶解并稀释成1000ml)1.5ml,加无氨水48ml与碱性碘化汞钾试液2ml制成的对照液比较,不得更深(0.000 03%)。
6.电导率
电导率≤2μS/cm (电阻率≥0.5 MΩ.CM)
7.总有机碳
不得过0.50mg/L(附录VIII R)。
8.易氧化物
取本品100ml,加稀硫酸10ml,煮沸后,加高锰酸钾滴定液(0.02mol/L)0.10ml,再煮沸10分钟,粉红色不得完全消失。
9.不挥发物
取本品100ml,置105℃恒重的蒸发皿中,在水浴上蒸干,并在105℃干燥至恒重,遗留残渣不得过1mg。
取本品100ml,加水19ml,蒸发至20ml,放冷,加醋酸盐缓冲液(pH3.5)2ml与水适量使成25ml,加硫代乙酰胺试液2ml,摇匀,放置2分钟,与标准铅溶液1.0ml加水19ml用同一方法处理后的颜色比较,不得更深(0.000 01%)。
11.微生物限度
取本品,采用薄膜过滤法处理后,依法检查(附录XIJ),细菌、霉菌和酵母菌总数每1ml不得超过100个。