以重晶石为原料制取高纯碳酸钡的工艺流程和工艺条件探讨_图文_(精)
- 格式:doc
- 大小:313.00 KB
- 文档页数:2
![一种以毒重石为原料生产氯化钡的工艺[发明专利]](https://uimg.taocdn.com/459c741e7275a417866fb84ae45c3b3567ecdd8f.webp)
(10)申请公布号(43)申请公布日 (21)申请号 201510226848.0(22)申请日 2015.05.06C01F 11/24(2006.01)(71)申请人四川理工学院地址643000 四川省自贡市汇兴路学苑街180号(72)发明人刘勇 杨虎 潘中才 刘建容王学娟 徐飞 李伟 罗家文(74)专利代理机构北京国智京通知识产权代理有限公司 11501代理人张瑜(54)发明名称一种以毒重石为原料生产氯化钡的工艺(57)摘要本发明属于化工技术领域,具体公开了一种以毒重石为原料生产氯化钡的工艺。
主要由下列步骤实现:将原料毒重石与水混合磨碎并加酸进行酸解、加盐及石灰乳除杂、降膜预浓缩、蒸发结晶得到二水氯化钡晶体;将晶浆进行降温重结晶,进一步回收热溶液中的二水氯化钡晶体;合并二水氯化钡晶体用饱和食盐水洗涤,再次重结晶提纯并干燥得到产品氯化钡。
本发明对毒重石的品种不限制,降低了对原料的要求;无传统生产过程中的除杂步骤,流程简单,易操作;整个流程无废气、废渣及废液排放,符合绿色化工要求且制得的氯化钡晶体收率高、纯度高、成本低,适合大规模工业化生产需要。
(51)Int.Cl.(19)中华人民共和国国家知识产权局(12)发明专利申请权利要求书1页 说明书4页 附图1页(10)申请公布号CN 104891549 A (43)申请公布日2015.09.09C N 104891549A1.一种以毒重石为原料生产氯化钡的工艺,其特征在于,包括如下步骤:步骤1:将原料毒重石与水混合磨碎作为矿浆,向矿浆中加入30%的盐酸并加热到一定温度,在反应釜中反应一定时间,回收二氧化碳气体;步骤2:向步骤1得到的浆料中加入石灰乳及与浆料同温度的氯化钠饱和溶液,调节pH 为碱性,以去除Mg2+、Fe3+、Al3+杂质离子;步骤3:将步骤2得到的浆料离心过滤,过滤后得到的滤渣通过水洗后做水泥,过滤后得到的净化液为BaCl2-NaCl-H2O三元体系溶液;步骤4:将步骤3中得到的BaCl2-NaCl-H2O三元体系溶液送入降膜式升温蒸发器中升温至一定温度后对料液进行预浓缩;步骤5:将步骤4中得到的浓缩液泵入真空式循环蒸发结晶器中结晶一段时间;步骤6:将步骤5中得到的浆料离心分离得到二水氯化钡晶体,用等温度的饱和食盐水洗涤所述二水氯化钡晶体后,干燥得到氯化钡,洗涤滤饼的滤液循环回到真空式循环蒸发结晶器中结晶并保存晶浆;步骤7:将步骤6中离心分离得到的晶浆泵入釜式降温结晶器中重结晶,进一步回收热溶液中的二水氯化钡晶体;步骤8:将步骤7得到的浆料离心分离后,用与离心后浆料等温度的饱和食盐水洗涤,滤液及洗水为钙水溶液,所得二水氯化钡晶体返回循环结晶器中重结晶以提高纯度。

高中工艺流程题的解题思路及方法高中工艺流程题解题思路及方法。
一、解题思路。
1. 浏览题目,明确目的:首先快速浏览工艺流程题,了解题目要求和目的,是制备某种物质、提纯某种物质还是分析某个过程中的化学反应等。
2. 分析流程,理解原理:仔细分析工艺流程的各个步骤,理解每个操作的目的和原理,包括原料的预处理、反应的条件控制、物质的分离和提纯等。
3. 关注信息,提取关键:注意题目中给出的文字信息、图表数据等,提取关键的化学知识和信息,如物质的性质、化学反应方程式、溶解度等。
4. 联系知识,解决问题:运用所学的化学知识,如元素化合物、化学反应原理、化学实验等,解决工艺流程中提出的问题,如判断反应类型、计算物质的产量或纯度等。
二、解题方法。
1. 箭头分析法:顺着工艺流程的箭头方向,逐步分析每个步骤的反应物、生成物和反应条件,理解物质的转化和流向。
2. 元素守恒法:根据化学反应前后元素的种类和质量守恒,计算物质的含量、转化率等。
3. 对比分析法:对比不同工艺路线或操作条件,分析其优缺点,选择最优方案。
4. 数据分析法:利用题目中给出的数据,如溶解度、浓度、产量等,进行计算和推理。
三、例题解析。
例题 1:(人教版)从海水中提取镁的工艺流程如下:海水ce{->[加入石灰乳]}氢氧化镁ce{->[加盐酸]}氯化镁溶液ce{->[蒸发浓缩、冷却结晶]}氯化镁晶体ce{->[在氯化氢气流中加热脱水]}无水氯化镁ce{->[电解]}镁。
步骤中加入石灰乳的作用是______。
步骤中发生反应的化学方程式为______。
步骤④中在氯化氢气流中加热脱水的目的是______。
解析:石灰乳中的氢氧化钙能与海水中的镁离子反应生成氢氧化镁沉淀,从而将镁离子从海水中分离出来。
步骤中发生的反应是氢氧化镁与盐酸反应生成氯化镁和水,化学方程式为:ce{Mg(OH)2 + 2HCl = MgCl2 + 2H2O}。
氯化镁在加热脱水过程中会发生水解生成氢氧化镁和氯化氢,如果在氯化氢气流中加热,可以抑制氯化镁的水解,得到无水氯化镁。

2024成都中考化学复习第二部分 重难题型分类练 题型四 流程图题 类型1 制备与生产流程考向1 金属及金属氧化物的制备流程1.(中华优秀传统文化) (2023岳阳)《梦溪笔谈》中记载了用“苦泉水”制取铜的方法:“挹其水熬之,则成胆矾,烹胆矾则成铜;熬胆矾铁釜,久之亦化为铜”。
此文记录了两种冶铜工艺,主要流程如图所示。
资料:“熬成胆矾”是将硫酸铜溶液蒸发制得硫酸铜晶体,该化学反应为:CuSO 4+5H 2O =====加热CuSO 4·5H 2O 。
(1)写出“铁釜”中发生反应的化学方程式________________________________。
(2)上述生产过程中,没有涉及到的化学反应类型是________(填字母)。
A.化合反应B.分解反应C.置换反应D.复分解反应(3)实验室从硫酸铜溶液中分离出硫酸铜晶体的操作过程为:①加热蒸发到饱和;②降温析出晶体;③______(填操作名称)。
(4)生产生活中铁釜(铁锅)易锈蚀,请写出一种金属防锈的方法_____________。
2.(2022江西改编)某化工厂以生产钛白粉的主要副产物(含硫酸亚铁)为原料,制取含高纯度氧化铁的氧化铁红,其工业流程如下:(1)操作1能得到硫酸亚铁晶体,说明硫酸亚铁的溶解度随温度的升高而________。
(2)实验室中完成操作2时,玻璃棒的作用是________。
(3)操作3中,硫酸亚铁在空气中煅烧得到氧化铁和三氧化硫的化学方程式为___________。
(4)操作4吸收三氧化硫时水由顶端喷洒的目的是_____。
3.(2023昆明)铬是一种用途广泛的金属。
工业上以铬铁矿[主要成分Fe(CrO2)2]为原料冶炼铬,流程如下:回答下列问题:(1)操作a的名称是________。
(2)反应Ⅱ的化学方程式为8Na2CrO4+3X+20H2O=== 8Y↓+3Na2SO4+16NaOH,X、Y表示两种物质,Y的化学式为________________________________________________。

重晶石一、矿产名称重晶石(Barite)二、矿床类型我国重晶石矿床可分为四种类型,即沉积型矿床、火山沉积型矿床、热液型矿床和残坡积型矿床。
矿产的分布情况:全世界重晶石资源比较丰富,主要分布在美国、苏联、中国、秘鲁、印度等国,世界重晶石储量为20亿吨。
我国重晶石资源丰富,全国26个省,市自治区均有分布,主要集中在南方,贵州省占全国总储量三分之一,湖南、广西分别居全国第二、第三位,我国重晶石不但储量大,而且品位高,BaSO4>92.8%。
富矿储量占全国富矿总量的99.4%,大中型矿储量占全国总量88.4%,截止95年底,我国已探明重晶石储量4.6亿吨。
三、矿床主要工业指标边界品位:硫酸钡(BaSO4)10%工业品位:硫酸钡(BaSO4)30%可采厚度:原生矿床0.25米,风化粘土质矿床1米。
表1 重晶石的矿石类型和特点矿石类型矿石特点主要矿物及伴生矿物沉积型块状或条纹和豆粒状构造重晶石、石英、粘土矿物、黄铁矿等热液型致密、灰至白色重晶石、黄铁矿、黄铜矿、方铅矿、闪锌矿、赤铁矿、萤石、毒重石等火山沉积型重晶石、菱铁矿、镜铁矿等残坡积型易选、品位较高重晶石、萤石、方解石、石英等重晶石矿物的矿物特征重晶石是最普通的富含钡矿物,其要性质列于表2表2 重晶石矿物的主要性质矿物名称化学式化学组成%密度g/cm莫氏硬度晶系形状颜色重晶石BaSO4BaO,65.7SO3,34.34.52.5~3.5斜方板状柱状灰白此外,重晶石难容于水和酸、无毒、无磁性,能吸收X-射线及伽玛射线等特性。
五、工艺特性及主要用途重晶石是一种重要的含钡矿物,具有比重大(4.3—4.7)、硬度低(3—3.5)化学性质稳定、不溶于水和酸,重晶石粉主要用于石油、化工、油漆、填料等工业部门,其中80%—90%用作石油钻井中的泥浆加重剂。
表3列出了它的主要用途。
表3 重晶石的主要用途应用领域主要用途备注石油钻探油气井旋转钻探中的环流泥浆加重剂冷却钻头,带走切削下来的碎屑物,润滑钻杆,封闭孔壁,控制油气压力,防止油井自喷化工生产碳酸钡、氯化钡、硫酸钡、锌钡白、氢氧化钡、氧化钡等各种钡化合物这些钡化合物广泛应用于试剂、催化剂、糖的精制、纺织、防火、各种焰火、合成橡胶的凝结剂、塑料、杀虫剂、钢的表面淬火、荧光粉、荧光灯、焊药、油脂添加剂等玻璃去氧剂、澄清剂、助熔剂增加玻璃的光学稳定性、光泽和强度橡胶、塑料油漆填料、增光剂、加重剂建筑混凝土骨料、铺路材料重压沼泽地区埋藏的管道,代替铅板用于核设施,原子能工厂、X光实验室等的屏蔽,延长路面的寿命六、产品质量标准重晶石产品根据其用途,有不同的规格及质量要求。


高考化学复习专题复习---无机化工流程试题(一)专题复习---无机化工流程试题(一)例题1.稀土元素是周期表中IIIB族钪、钇和镧系元素的总称,它们都是很活泼的金属,性质极为相似,常见化合价为+3。
我国蕴藏着丰富的钇矿石(Y2FeBe2Si2O10),以此矿石为原料生产氧化钇(Y2O3)的主要流程如下:已知:①有关金属离子形成氢氧化物沉淀时的pH如下表:开始沉淀时的pH 完全沉淀时的pHFe3+ 2.7 3.7Y3+ 6.0 8.2②在周期表中,铍、铝元素处于第二周期和第三周期的对角线位置,化学性质相似。
(1)钇矿石(Y2FeBe2Si2O10)的组成用氧化物的形式可表示为。
(2)欲从Na2SiO3和Na2BeO2的混合溶液中制得Be(OH)2沉淀。
则①最好选用盐酸、(填字母)两种试剂,再通过必要的操作即可实现。
a.NaOH溶液 b.氨水 c.CO2气 d.HNO3②写出Na2BeO2与足量盐酸发生反应的离子方程式:。
(3)沉淀A为(填化学式);为使Fe3+沉淀完全,须用氨水调节pH =a,则a应控制在的范围内;检验Fe3+是否沉淀完全的操作方法是。
例题2.工业上制取CuCl2的生产流程如下:(1)写出下列主要离子方程式:A→B;B→C+D 。
(2)溶液A中加入NaClO的目的是。
(3)在溶液B中加入CuO的作用是。
(4)操作①应控制的pH 范围是:;操作②的目的是。
(5)由Cu(OH)2加入盐酸使Cu(OH)2转变为CuCl 2。
采用“稍多量盐酸”和“低温蒸干”的目的是。
例题3.二氧化锰是制造锌锰干电池的基本材料。
工业上以软锰矿为原料,利用硫酸亚铁制备高纯二氧化锰的流程如下:某软锰矿的主要成分为MnO 2,还含有Si (16.72%)、Fe (5.86%)、Al (3.42%)、Zn (2.68%)和Cu (0.86%)等元素的化合物。
部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH(124式为(2)滤渣A 的主要成分是。

利用回转窑煅烧重晶石生产碳酸钡的工艺过程碳酸钡是较为重要的无机盐产品之一,广发应用于无线电、光学玻璃、油漆、建筑等行业。
其生产方法大都是重晶石经煅烧生成硫化钡,再经碳化、烘干制得。
硫化钡(俗称粗钡)工序是生产中的一个重要的操作单元,目前国内钡盐生产厂家重晶石还原大都是在回转窑中进行的。
回转窑是整个碳酸钡生产的龙头设备,其开车率直接影响整条生产线的产量。
重晶石回转窑的生产工艺过程原料煤和重晶石按一定的比例通过提升机、下料管进入到回转窑中,由罗茨风机吧燃料煤吹入回转窑中燃烧,提供反应能量。
随后经过沉降室除掉部分灰尘,在经预热锅炉降温,水膜除尘彻底处理,最后经引风机进入烟囱排放。
回转窑的前部和后部都是由耐火水泥浇筑而成,中间由耐火砖砌成。
外部由托辊作为支撑,不同长度的回转窑支撑托辊的数量也不同,一般是3~4道。
回转窑是通过拖动电机经减速机齿圈产生转动的。
燃烧器河南宏科重工专业提供回转窑专用燃烧器的设计、制作、安装、调试和维护!四通道粉煤燃烧器结构及原理:多通道粉煤燃烧器的结构如图下图所示,它是有管路、阀门、补偿器、测量仪器、喷嘴和耐火浇注保护层等构成。
管路由外到内分别为外轴流风管、煤风管、旋流风管、中心风管和燃油管组装而成。
喷嘴采用新研制的特殊材料加工。
原理如下图所示,粉煤由气流携带,从煤风通道按设定的扩散角由外喷出,由内邻的旋流风传给相当高的动量和动量矩,以高速度螺旋前进,并继续径向扩散,与高速射出的轴流风束相遇。
轴流风束的插入进一步增强了煤、风的混合,改善了原形环形风周围屏蔽的不良作用,产生较强的热回流,使入窑的二次风及窑内的高温气体快速卷吸到燃烧器的出口,强化粉煤燃烧,缩短粉煤燃烧时间。
并可通过阀门调节风量和调节丝杆(出口截面积),来调节火焰的发散程度,可按需要调节火焰的长短、粗细,达到良好的火焰形状。
中心风的作用是促使中心部位少量煤粉及Co燃烧,使煤粉燃烧更为充分,并起稳流作用。
由这样的燃烧机理所产生的速度差、压力差、方向差,燃烧非常安全。

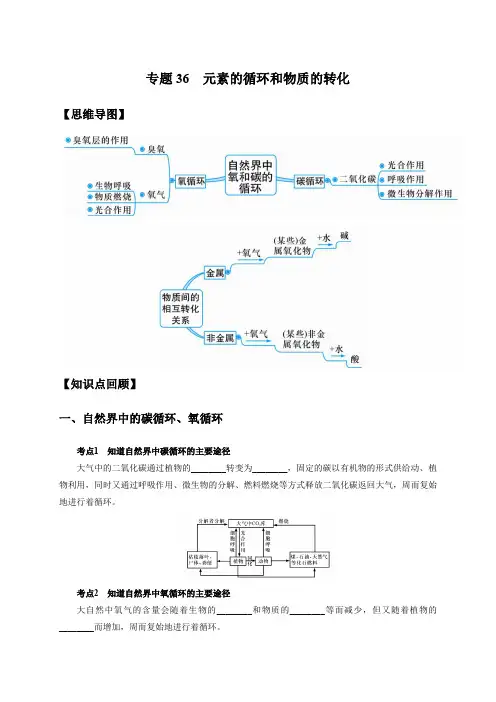
专题36元素的循环和物质的转化【思维导图】【知识点回顾】一、自然界中的碳循环、氧循环考点1知道自然界中碳循环的主要途径大气中的二氧化碳通过植物的________转变为________,固定的碳以有机物的形式供给动、植物利用,同时又通过呼吸作用、微生物的分解、燃料燃烧等方式释放二氧化碳返回大气,周而复始地进行着循环。
考点2知道自然界中氧循环的主要途径大自然中氧气的含量会随着生物的________和物质的________等而减少,但又随着植物的________而增加,周而复始地进行着循环。
产生氧气的主要途径:________。
消耗氧气的主要途径:①动、植物的呼吸作用;①燃料燃烧;①微生物分解动、植物遗体;①其他氧化反应(如:生锈、食物腐败)。
二、物质间的相互转化考点3说明金属、金属氧化物、碱之间的转化关系;说明非金属、非金属氧化物、酸之间的转化关系1.金属→________→碱,如:Ca→CaO→Ca(OH)2。
2.非金属→________→酸,如:C→CO2→H2CO3。
3.物质间的相互转化注意:(1)极少数非金属氧化物不与碱起反应,如CO等。
(2)根据物质之间的相互转化关系图可查找各类物质的主要化学性质。
(3)根据物质之间的相互转化关系图可查找各类物质的可能制法。
【例题精析】例1.(2021•杭州)二氧化碳的资源化利用是实现碳减排的重要途径。
如图是一种实现二氧化碳转化为重要原料二甲醚(化学式为C2H6O)的途径:(1)转化①是二氧化碳与一种常见单质反应生成甲醇和水,这种单质的化学式为。
(2)转化②是甲醇发生分解反应生成二甲醚和水,反应中生成二甲醚和水的分子数之比为。
例2.(2020•宁波)铁的化合物有广泛用途,如碳酸亚铁(FeCO3)可作补血剂。
某硫酸厂产生的炉渣中除了有Fe2O3、FeO,还有一定量的SiO2.兴趣小组利用炉渣尝试制备FeCO3,其流程如图:【已知:Fe+Fe2(SO4)3═3FeSO4;SiO2不溶于水,也不与稀硫酸反应】(1)操作①的名称是。

年产十万吨碳酸钡碳化法工艺设计碳酸钡(BaCO3)是一种重要的化学原料,被广泛应用于电子、光电、陶瓷、橡胶、塑料和玻璃制造等工业领域。
随着市场需求的不断增长,对碳酸钡的年产量也有着更高的要求。
本文将介绍一种年产十万吨碳酸钡的碳化法工艺设计。
碳化法工艺是一种常用的生产碳酸钡的方法。
它的主要步骤包括:制备碳酸钡母液、净化、过滤、碳化、高压过滤、干燥和精制等。
下面将逐步介绍每个步骤的详细设计。
首先是制备碳酸钡母液。
碳酸钡母液的主要原料是重铁矿和石灰石,在反应器中加入适量的重铁矿和石灰石,加入足够的水,并进行搅拌,使其充分反应。
反应产物通过过滤分离得到碳酸钡母液。
接下来是净化步骤。
为了确保生产的碳酸钡的纯度,需要进行净化处理。
将碳酸钡母液中不纯物质去除,可采用沉淀法、溶剂法或离子交换法等方式进行净化。
然后是过滤步骤。
净化后的碳酸钡母液需要进行过滤,去除其中的固体杂质。
过滤器的选择应考虑流量大、过滤效果好、操作简便等因素。
然后是碳化步骤。
将过滤后的碳酸钡母液加入碳化反应器中,控制温度、压力和时间等参数,使得碳酸钡和二氧化碳充分反应生成碳酸钡颗粒。
反应完成后,通过过滤分离得到碳酸钡颗粒。
接着是高压过滤步骤。
将碳酸钡颗粒进行高压过滤,去除过滤液中的水分和其他杂质。
选择高压过滤器应考虑设备的稳定性和过滤效果等因素。
然后是干燥步骤。
将过滤后的碳酸钡颗粒进行干燥,去除水分,得到干燥的碳酸钡产品。
干燥的方法可以采用气流干燥、真空干燥或喷雾干燥等方式。
最后是精制步骤。
对干燥的碳酸钡产品进行精制处理,提高其纯度和质量。
精制方法可以采用洗涤、萃取、结晶等工艺。
综上所述,年产十万吨碳酸钡碳化法工艺设计包括碳酸钡母液制备、净化、过滤、碳化、高压过滤、干燥和精制等步骤。
通过合理的设计和控制参数,能够实现高效、稳定地生产出高质量的碳酸钡产品,满足市场需求。
为了实现年产十万吨碳酸钡碳化法工艺的设计,需要对每个步骤进行进一步详细设计和优化。

钡产业链一、钡生产及加工现状钡是一种银白色的金属元素,燃烧时发出黄绿色火焰。
和其它碱土金属一样,在地球上到处都有分布:在地壳上部的含量是0.026%,而在地壳中的平均值是0.022%。
钡主要以重晶石形式存在,以硫酸盐或碳酸盐形式存在。
我国钡资源是从硫酸钡和碳酸钡矿中提取的。
我国有着丰富的重晶石资源,分布在湖南、广西、山东等省区,其中湖南衡南县的重晶石储量非常丰富。
我国重晶石的开发,因缺乏深度加工的配套设备及经济效益不理想,发展速度缓慢,还不能满足国民经济发展的需要。
工业上制取金属钡分为制取氧化钡和金属热还原(铝热还原)两个步骤。
在1000~1200℃,用金属铝还原氧化钡,可制得金属钡,再用真空蒸馏法提纯。
金属钡主要用作消气剂,以除去真空管和电视显像管内的痕量气体。
在蓄电池极板的铅合金中加入少量的钡,可以改善性能。
钡可做球化剂和脱气合金,用于制造球墨铸铁和精炼金属。
钡的化合物用途广泛,重晶石可做钻探用的泥浆。
锌钡白俗称立德粉,是一种常用的白色颜料。
钛酸钡压电陶瓷广泛用作仪器中的换能器。
硝酸钡燃烧时,呈明亮的绿黄色,大量用于制造焰火和信号弹。
硫酸钡常用于医学X 射线肠胃诊察,俗称“钡餐造影”。
二、钡产业发展趋势钡是无机盐行业的主要产品,钡盐行业的主要产品有碳酸钡、硫酸钡、氢氧化钡、氯化钡、硝酸钡、钛酸钡等。
(一)碳酸钡碳酸钡产品主要用于电子行业,是彩色显像管、磁性材料的重要添加剂。
随着电子工业的迅速发展,我国碳酸钡向精细化、功能化方向发展。
目前,我国碳酸钡产品生产规模已超过60 万吨/年,产量达50 万吨/年,全世界碳酸钡产量为70 万吨/年左右,我国产量占世界产量的77%。
我国碳酸钡的主要生产企业有青岛红星集团公司和河北辛集化工集团有限公司,生产工艺以传统的碳化法为主,技术进步主要表现在微机配料、余热利用及新型造粒技术方面。
产品有粉状BaCO3、粒状BaCO3(干法与湿法)产品,我国碳酸钡产品长期以来大量出口,已成为世界第一大碳酸钡出口国,在国际市场上占有重要地位。
高中化学工业流程100题1.以黄铜矿(主要成分是CuFeS₂)为原料冶炼铜的流程如下:黄铜矿→焙烧→浸出→除杂→精炼→铜。
请写出焙烧过程中主要反应的化学方程式。
2.工业上利用软锰矿(主要成分MnO₂)制备高锰酸钾的流程如下:软锰矿与氢氧化钾在空气中加热熔融反应后,再进行一系列操作得到高锰酸钾。
写出软锰矿与氢氧化钾反应的化学方程式。
3.从海水中提取镁的工业流程中,贝壳(主要成分CaCO₃)经过煅烧后用于制取氢氧化镁。
写出贝壳煅烧的化学方程式以及制取氢氧化镁的反应原理。
4.工业上用铝土矿(主要成分Al₂O₃,含Fe₂O₃、SiO₂等杂质)为原料冶炼铝的工艺流程中,首先用氢氧化钠溶液溶解铝土矿。
写出铝土矿中氧化铝与氢氧化钠反应的化学方程式。
5.工业上以铬铁矿(主要成分FeCr₂O₄)为原料制备重铬酸钾(K₂Cr₂O₇)的流程如下:铬铁矿与碳酸钠在空气中煅烧后,经过一系列反应得到重铬酸钾。
写出铬铁矿与碳酸钠在空气中煅烧的主要反应方程式。
6.某工厂利用废旧电池中的锌皮制取硫酸锌晶体的流程为:锌皮→酸溶→除杂→结晶→硫酸锌晶体。
写出酸溶过程中发生反应的化学方程式(假设用稀硫酸溶解锌皮)。
7.工业上从废定影液(主要含有[Ag(S₂O₃)₂]³⁻)中回收银的流程如下:先向废定影液中加入硫化钠溶液,再进行后续处理。
写出加入硫化钠溶液时发生反应的离子方程式。
8.以萤石(CaF₂)为原料制备氟化氢的工业流程中,萤石先与浓硫酸反应。
写出该反应的化学方程式。
9.工业上利用磷矿石(主要成分Ca₅(PO₄)₃F)生产磷酸的流程中,磷矿石与硫酸反应。
写出该反应的化学方程式。
10.从某含有金、银、铜的废旧合金中回收金、银、铜的工业流程为:废旧合金→预处理→分金→分银→分铜。
写出分金过程中可能用到的一种化学试剂及对应的反应原理。
11.工业上从铝土矿中提取氧化铝的流程如下:铝土矿→粉碎→碱浸→过滤→酸化→煅烧→氧化铝。
写出碱浸过程中主要反应的离子方程式(假设杂质只有SiO₂)。
钡盐产品特性及制作工艺简述氢氧化钡产品简介性质:八水氢氧化钡为白色结晶体.相对密度,微溶于水,其溶解度受温度影响较大,溶于酸.在空气中吸收二氧化碳生成碳酸钡,加热至100℃开始缓慢失去结晶水变为一水氢氧化钡,一水氢氧化钡407℃失去结晶水变为无水氢氧化钡.有毒用途:生产钡盐产品的原料,润滑油及润滑油脂的添加剂.产品特征商标仙峰规格主含量98%min产量300吨-400吨/月价格吨公司名称氯化钡高纯,无水,二水产品简介工业二水氯化钡产品说明书产品名称:工业氯化钡Barium chloride分子式:BaCl2·2H2O分子量:按1985年国际原子量密度:/cm3外观:白色片状或粉状结晶包装:内塑外编,每袋净重50kg、25kg.性质:白色单斜结晶体,冷结晶体为扁平菱形,热结晶为无定形.通常含有二个分子结晶水,结晶水在空气中稳定不风化.溶于水,水溶液具有苦味和咸凉味,有毒危险有害性:有毒、不易燃、不易爆.应急措施:产品有一定毒性,摄入产品会出现呕吐、腹痛、腹泻等症状,立即就医治疗;吸入产品时,刺激鼻腔、支气管、肺部等粘膜,立即擤鼻涕、漱口:附在皮肤上时,立即用水清洗.用途:氯化钡用途广泛,主要用于化学工业、机械制造、金属加工等.储运注意事项:氯化钡应贮存在清洁、阴凉通风处,在贮存和运输过程中应做到防潮、防雨、防破损,不得与其他物品混存.环境保护:无三废污染.危险货物类别:六类联合国编号:1564注册商标:“昱胜”牌编号:1969768质量体系:ISO9001—2000执行标准:GB1617—2002技术指标:注:主含≥100%以上,为不含游离水商标昱胜产量1000吨/月价格面议公司名称其它产品、、碳酸钡产品简介碳酸钡BaCO3为白色斜方结晶体,属无机盐能溶于稀酸,也可溶于氯化铵溶液和硝酸铵溶液,几乎不溶于水,约1300℃时分解.我公司主要产品包括:重质粉状碳酸钡、轻质粉状碳酸钡、干粒状碳酸钡和湿状粒碳酸钡. 碳酸钡是生产显像管、计算机显示器、工业监视器、电子元器件的重要原料,还广泛用于磁性材料、陶瓷、涂料的制造,产品用途涉及电子信息、化工、轻工、陶瓷、冶金等十多个行业.包装规格为25kg、50kg或吨袋.产品特征型号50、25公斤塑编规格99%产量6000吨/月价格1550元/吨公司名称其它产品、、、硫酸钡bsp-l产品简介BLANC FINE BSP系采用高纯钡盐和硫酸钠溶液作为原料,加上特殊的制备工艺精制而成,其粒径得到很好的控制,且杂质含量被降至极低范围,再加之多级后期处理合成的硫酸钡产品BLANC FIXE.具有比重小、狭窄的粒径分布、极其良好的耐晒性、耐候性等优秀的化学性能.BLANC FINE BSP独特的D97<完整球形或近似球形的超细硫酸钡晶体,具备了庞大的比表面积和较少的基料用量,可有效增加或放大涂层中光源的反射面积,而被广泛推荐应用于高光泽产品的配方体系之中.Baso4含量,.>%平均粒径D97吸油量,15g/100g干亮白度>95PH值,7-9105℃挥发份,<产品特征海关编码2833327商标Gemme型号bsp-l规格ISO9001产量50,000 pcs/year源产地china包装25kg/bags最小起订量20tons公司名称沉淀硫酸钡产品简介沉淀硫酸钡分子式:BaSO4、分子量、233、10.我公司生产了浆水牌硫酸钡,是将的重晶石、芒硝经过煅烧——合成——洗滤——烘干——粉碎等化学反应和物理处理,最终产品为无定型白色粉末.应用范围:油漆、油墨、颜料、橡胶、蓄电池、塑料和铜板纸等工业.沉淀硫酸钡技术指标:执行GB/T、2899——1996国家标准.硝酸钡产品简介中文名称:硝酸钡化学式:BaNO32相对分子质量:性状:无色结晶或白色结晶性粉末.微有吸湿性.在高于熔点时分解.易溶于水,极微溶于乙醇和丙酮,几乎不溶于浓酸.盐酸和硝酸能降低其水中溶解度.相对密度.熔点约590℃.折光率.有强氧化性.中等毒,半数致死量大鼠,经口355mG/kG. 储存:密封干燥保存. 用途:硫酸和铬酸的定性.制造过氧化钡.绿光焰火.真空管工业. 安全措施:贮于低温通风处,远离火种、热源.与食用化学品、酸碱类、易燃物、还原剂等分储.严禁身体直接接触;误食,饮温水,催吐.海关编码01产量5000吨/年品质工程级处理方法提纯外观粉末状类别硝酸盐粉末100目公司名称重晶石粉200-1250目产品简介重晶石粉重晶石化学组成为BaSO4,晶体属正交斜方晶系的硫酸盐矿物.摩氏硬度,比重重晶石化学性质稳定,不溶水和盐酸.1、钻井泥浆加重剂:在一些油井、气井钻探时,一般使用的钻井泥浆、粘土比重为25左右,水的比重为1,因此泥浆比重较低,有时泥浆重量不能与地下油、气压力平衡,则造成井喷事故.在地下压力较高的情况下,就需要增加泥浆比重,往泥浆中加入重晶石粉是增加泥浆比重的有效措施.做钻井泥浆用的重晶石一般细度要达到325目以上,如重晶石细度不够则易发生沉淀.钻井泥浆用重晶石要求比重大于,BaSO4含量不低于95%,可溶性盐类小于1%.2、锌钡白颜料:锌钡白是一种常用的优质白色颜料,可作为油漆、绘画颜料的原料.将硫酸钡加热重晶石,使用还原剂就可还原成硫化钡BaS,然后与硫酸锌ZnSO4反应得到的硫酸钡和硫化锌的混合物BaSO4占70%,ZnS占30%即为锌钡白颜料.制取锌钡白的重晶石要求BaSO4含量大于95%,同时应不含有可见的有色杂物.3、各种钡化合物:以重晶石为原料可以制造氧化钡、碳酸钡、氯化钡、硝酸钡、沉淀硫酸钡、氢氧化钡等化工原料.化学纯的硫酸钡是测量白度的标准;碳酸钡是光学玻璃的重要原料,它向玻璃中引入BaO,从而增大玻璃的折光率,并改善其它光学性能;在陶瓷中用来配制釉料;氯化钡是一种农用杀虫剂;硝酸钡用于焰火和玻璃工业中;高锰酸钡是一种绿色颜料.4、填料工业用重晶石:在油漆工业中,重晶石粉填料可以增加漆膜厚度、强度及耐久性.锌钡白颜料也用于制造白色油漆,在室内使用比铅白、镁白具有更多的优点.油漆工业用重晶石要求有足够的细度和较高的白度.造纸工业、橡胶和塑料工业也用重晶石作填料,这种填料能提高橡胶和塑料的硬度、耐磨性及耐老化性.橡胶、造纸用重晶石填料一般要求BaSO4大于98%,CaO 小于%,不许含有氧化镁、铅等成分.5、水泥工业用矿化剂:在水泥生产中采用重晶石、萤石复合矿化剂掺入对促进C3S形成、活化C3S具有明显的效果,熟料质量得到了改善,水泥早期强度大约可提高20~25%,后期强度约提高10%,熟料烧成温度由1450℃降低到1300±50℃.重晶石掺量为~%时,效果最好.在白水泥生产中,采用重晶石、萤石复合矿化剂后,烧成温度从1500℃降至1400℃,游离CaO含量低,强度和白度都有所提高.在以煤矸石为原料的水泥生料中加入适量的重晶石,可使熟料饱和比低的水泥强度,特别是早期强度得到大幅度的提高,这就为煤矸石的综合利用,为生产低钙、节能、早强和高强水泥提供了一条有益途径.6、防射线水泥、砂浆及混凝土:利用重晶石具有吸收X 射线的性能,用重晶石制做钡水泥、重晶石砂浆和重晶石混凝土,用以代替金属铅板屏蔽核反应堆和建造科研、医院防X 射线的建筑物.钡水泥是以重晶石和粘土为主要原料,经烧结得到以硅酸二钡为主要矿物组成的熟料,再加适量石膏,共同磨细而成.比重较一般硅酸盐水泥高,可达~.强度标号为325~425.由于钡水泥比重大,可与重质集料如重晶石配制成均匀、密实的防X射线混凝土.重晶石砂浆是一种容重较大、对X射线有阻隔作用的砂浆,一般要求采用水化热低的硅酸盐水泥,通常用的水泥∶重晶石粉∶重晶石砂∶粗砂配合比为1∶025∶25∶1.重晶石混凝土是一种容重较大,对X射线具有屏蔽能力的混凝土,胶凝材料一般采用水化热低的硅酸盐水泥或高铝水泥、钡水泥、锶水泥等特种水泥.硅酸盐水泥应用最广.常用的水泥∶重晶石碎石重晶石砂∶水的配合比为1∶454∶34∶05;1∶544∶446∶06;1∶5∶38∶02三种做防射线砂浆及混凝土的重晶石,BaSO4含量应不低于80%,其中含有的石膏、黄铁矿、硫化物和硫酸盐等杂质不得超过7%.7、道路建设:橡胶和含约10%重晶石的柏油混合物已成功地用于停车场,是一种耐久的铺路材料.目前,重型道路建设设备的轮胎已部分地填充有重晶石,以增加重量,利于填方地区的夯实. 8、其它:重晶石和油料调和后涂于布基上制造油布;重晶石粉用来精制煤油;在医药工业中做消化道造影剂;还可制农药、制革、制焰火等.此外,重晶石还用作提取金属钡,用作电视和其它真空管的吸气剂、粘结剂.钡与其它金属铝、镁、铅、钙制成合金,用于轴承制造.于水和盐酸,无磁性和毒性.商标安泰型号200-1250目产量3000吨/月价格电议包装500公斤,1000公斤最小起订量1吨运输方式汽运外观粉末类型增塑剂尺寸200-1250目颜色白色含量90min比重白度90min公司名称。
重晶石深加工应用概述
重晶石主要成分是硫酸钡,莫氏硬度较高,一般为3-3.5。
重晶石是最重要的钡盐制品生产原料。
就目前的重晶石行业应用而言,重晶石粉末加工还是一个比较粗放的状态。
在实际生产中,重晶石被磨至100-600目之间即可,超细加工需求并不迫切。
所用粉碎设备主要为球磨机,雷蒙磨(含改进型的超细雷蒙机)。
然而重晶石粉末的应用,并非仅限于直接使用重晶石粉末。
很多情况下是利用提纯后的重晶石粉(硫酸钡含量超过98%)生产各类钡盐制品。
重晶石的主要成分是硫酸钡,但是原生的重晶石矿由于比重或品位难以达到理想的要求而必须首先进行选矿,筛选出较为纯净的重晶石后再进行磨粉,也就是说重晶石粉加工过程的第一个流程实际上是选矿流程,要通过选矿的作用将废石抛弃掉,然后把选矿所得的优质重晶石矿磨成粉。
重晶石晶体一、重晶石选矿
重晶石的选矿提纯所用方法主要是重选法,通过重力选矿的方法从重晶石矿中提取优质的重晶石,抛弃比重较小的脉石和废石,以提高重晶石矿的比重或品位,然后经过脱水处理即可进入磨粉流程。
重晶石的重选所用设备是跳汰机,跳汰机可以有效抛弃重晶石矿中的脉石和废石,恢复重晶石矿的地址品位,提高重晶石比重,常用的重晶石选矿跳汰机为AM30跳汰机和梯形跳汰机。
二、重晶石深加工概述
1、生产高白度重晶石粉末。
2020届届届届届届届届届——届届届届届届届19届届届IIA届届届届届届届一、单选题(本大题共2小题,共4分)1.钛酸钡(BaTiO3)在电工、陶瓷等行业有广泛用途。
实验室以工业碳酸钡(主要成分BaCO3,含少量MgO、SiO2杂质)为原料制备BaTiO3的一种工艺流程如下:下列说法错误的是()A. 滤渣1可用于制备光导纤维B. “调pH”的主要目的是沉淀Mg2+C. “混合”时加入盐酸是防止Ba2+沉淀D. “煅烧”反应属于氧化还原反应【答案】C【解析】【分析】本题以钛酸钡的制备过程考查了物质分离和提纯的综合应用,理解流程中每一步的含义是解题的关键。
【解答】A.由工业碳酸钡成分和流程中信息知,SiO2不溶于盐酸,滤渣1为SiO2,该物质可用于制备光导纤维、玻璃等,故A正确;B.“调pH”的主要目的是将Mg2+转化为沉淀除去,故B正确;C.“混合”时加入盐酸防止TiCl4水解,故C错误;D.由信息知,“煅烧”反应中碳元素的化合价升高,属于氧化还原反应,故D正确。
故选C。
2.钡盐生产中排出大量的钡泥[主要含有BaCO3、BaCO3、BaSO3、Ba(FeO2)2],某主要生产BaCl2、BaCO3、BaSO4的化工厂,利用钡泥制取Ba(NO3)2,其部分工艺流程如下:已知:①Fe(OH)3和Fe(OH)2完全沉淀时溶液的pH分别为3.2和9.7②Ba(NO3)2在热水中的溶解度大,在冷水中的溶解度小下列有关说法不正确的是:A. 过滤2后滤液中含有硝酸,操作Ⅱ加入氢氧化钡中和得到硝酸钡溶液B. X试剂应选过量的H2O2,目的是为了是溶液中的Fe2+转化为Fe3+,最终转化为Fe(OH)3沉淀C. 操作Ⅲ蒸发浓缩、冷却结晶D. 此工艺流程生产流程会有氮的氧化物造成大气污染【答案】B【解析】【分析】本题是以工艺流程形式考查物质的分离提纯,注意除铁一般是转化为铁离子后通过调节pH使其沉淀。
【解答】钡泥主要含有BaCO3、BaCO3、BaSO3、Ba(FeO2)2,加入硝酸,在容器中充分溶解,可生成硝酸钡、硫酸钡,过滤后滤渣1含有硫酸钡,滤液中含有铁离子、钡离子等,且溶液呈酸性,可加入碳酸钡,调节PH=4∼5,使铁离子水解生成Fe(OH)3沉淀,过滤后废渣为Fe(OH)3,滤液中含有硝酸、硝酸钡等,加入氢氧化钡中和得到硝酸钡溶液,经蒸发、浓缩、过滤可得硝酸钡晶体,母液中含有硝酸钡,过滤得到的固体洗涤后出去废渣,滤液重新加入酸溶步骤充分利用。