烯烃和炔烃 (定稿 带答案)
- 格式:doc
- 大小:683.50 KB
- 文档页数:14

第三章单烯烃炔烃和二烯烃习题答案第三章单烯烃、炔烃和二烯烃习题答案第三章单烯烃、炔烃和二烯烃3.1用系统命名法命名以下化合物a.c.(ch3ch2)2c=ch2ch3c=chchch2ch3b.d.ch3ch2ch2cch2(ch2)2ch3ch2(ch3)2chch2ch=c( ch3)2c2h5ch3答案:a.2-乙基-1-丁烯2-ethyl-1-buteneb.2-丙基-1-己烯2-propyl-1-hexenec.3,5-二甲基-3-庚烯3,5-dimethyl-3-heptened.2,5-二甲基-2-己烯2,5-dimethyl-2-hexene3.2写出下列化合物的结构式或构型式,如命名有误,予以更正。
a.2,4-二甲基-2-戊烯b.3-丁烯c.3,3,5-三甲基-1-庚烯d.2-乙基-1-戊烯e.异丁烯f.3,4-二甲基-4-戊烯g.反华-3,4-二甲基-3-己烯h.2-甲基-3-丙基-2-戊烯答案:a.b.错,应属1-丁烯c.d.e.h.f.错,应属2,3-二甲基-1-戊烯g.错,应属2-甲基-3-乙基-2-己烯3.4以下烯烃哪个存有承、反异构?写下顺、反异构体的构型,并命名。
ch3a.ch3ch2c=cch2ch3c2h5b.ch2=c(cl)ch3ch3ch=chch=chc.c2h5ch=chch2ich3ch=chch=c hc2h5d.ch3ch=chch(ch3)2答案:c,d,e,f有顺反异构c.c2h5hch2icchhcc2h5ce.2f.ch2ihd.h3cchcch(ch3)2hh3chhccch(ch3)2(z)-1-碘-2-戊烯(e)-1-碘-2-戊烯e.hch3cchchch2h3cchchch(z)-4-甲基-2-戊烯(e)-4-甲基-2-戊烯hhch3chcccc2h5hf.ch2(z)-1,3-戊二烯hch3chchhccc2h5(e)-1,3-戊二烯h3cchhchccc2h5h(2z,4z)-2,4-庚二烯h3cchhchhccc2h5(2z,4e)-2,4-庚二烯(2e,4z)-2,4-庚二烯(2e,4e)-2,4-庚二烯3.5顺利完成以下反应式,写下产物或所需试剂.a.b.c.d.e.ch3ch2ch=ch2(ch3)2c=chch3ch3ch2ch=ch2ch3ch2ch=ch2(ch3)2c=chch2ch3ch2 =chch2ohh2so4hbrch3ch2ch2ch2ohch3ch2ch-ch3o3zn,h2oclch2ch-ch2ohohohf.答案:a.ch3ch2ch=ch2h2so4ch3ch2chch3oso2ohb.(ch3)2c=chch3hbr(ch3)2c-ch2ch3brc.ch3ch2ch=ch21).bh32).h2o2,oh-h2o/h+ch3ch2ch2ch2ohd.ch3ch2ch=ch2ch3ch2ch-ch3ohe.(ch3)2c=chch2ch3ch2=chch2oh1).o32).zn,h2och3coch3cl2/h2o+ch3ch2chof.clc h2ch-ch2ohoh3.6两瓶没有标签的无色液体,一瓶是正己烷,另一瓶是1-己烯,用什么简单方法可以给它们张贴上恰当的标签?答案:1-己烯正己烷无反应br2/ccl4orkmno4褪色1-己烯正己烷3.7有两种互为同分异构体的丁烯,它们与溴化氢加成得到同一种溴代丁烷,写出这两个丁烯的结构式。

第二节烯烃炔烃第1课时烯烃跟踪训练(有答案和详细解析)1.下列各组有机物中,能形成顺反异构的是()A.1,2-二氯丙烯B.2-氯丙烯C.1,1-二氯丙烯D.1-丁烯答案A解析有机物必须具备以下两个条件才能存在顺反异构:一是要含有碳碳双键;二是两个不饱和碳原子上一定分别连有不同的原子或原子团,若同一个不饱和双键碳原子上连有相同原子或原子团,则不存在顺反异构。
A存在顺反异构体和。
2.下列说法不正确的是()A.可用溴水鉴别乙烯和乙烷B.SO2与乙烯使酸性KMnO4溶液褪色的原理相同C.X气体通入溴水中,溴水褪色,则X气体一定为乙烯D.可用酸性KMnO4溶液区别甲烷和乙烯,因为二者结构不同答案C解析能使溴水褪色的气体有乙烯、二氧化硫、丙烯等,所以X气体不一定是乙烯,C项错误。
3.由乙烯推测丙烯的结构或性质正确的是()A.分子中3个碳原子在同一直线上B.分子中所有原子在同一平面上C.与HCl加成只生成一种产物D.能使酸性KMnO4溶液褪色答案D解析4.某烃的结构式用键线式可表示为,则该烃与Br2加成时(物质的量之比为1∶1)所得产物有()A.3种B.4种C.5种D.6种答案C解析如图,给双键碳原子进行编号,与溴按物质的量之比为1∶1发生加成反应时,可以是1,2-加成,3,4-加成,5,6-加成,还可以是1,4-加成,4,6-加成,所得产物有5种。
5.现有两种烯烃:CH2==CH2和。
它们的混合物进行聚合反应,则聚合反应的产物中含有如下四种物质中的()①CH2—CH2②③④A.①④B.③C.②D.①②④答案D解析烯烃的重要性质之一是发生加成聚合反应,当两种烯烃混合后,一定会有两种烯烃自身的加聚反应,得到①④;另外两种烯烃的共聚,得到②,所以D正确。
6.下列现象中,是因为发生加成反应而产生的现象是()A.乙烯使酸性高锰酸钾溶液褪色B.将苯滴入溴水中,振荡后水层接近无色C.乙烯使溴的四氯化碳溶液褪色D.甲烷与氯气混合,光照一段时间后黄绿色消失答案C解析乙烯使酸性高锰酸钾溶液褪色,是乙烯被酸性高锰酸钾溶液氧化而褪色,发生的是氧化还原反应;溴在苯中的溶解度远远大于其在水中的溶解度,苯能萃取溴水中的溴而使水层接近无色,此过程为物理过程;乙烯含有碳碳双键,与溴发生加成反应使溴的四氯化碳溶液褪色;甲烷和氯气混合,光照一段时间后黄绿色消失,是因为发生了取代反应。

第6章 炔烃和二烯烃问题参考答案1.炔烃没有顺反异构体。
因为三键碳是sp 杂化,为直线形构型,故无顺反异构现象。
2.HC CCH 2CH 2CH 2CH 3H 3CC CCH 2CH 2CH 3H 3CH 2CC CCH 2CH 2CH 3HCCCHCH 2CH 3HCCCH 2CHCH 3HCCCCH 3H 3CC CCHCH 3CH 3CH 3CH 3CH 3CH 31-己炔2-己炔3-己炔3-甲基-1-戊炔4-甲基-1-戊炔3,3-二甲基-1-丁炔4-甲基-2-戊炔3.化)4. 表面上看来,碳碳三键更具不饱和性,那末怎样来理解这些事实呢? 解释烯烃比炔烃更容易亲电加成的原因,有以下三点:(1).由于三键和双键的碳原子的杂化状态不同三键碳原子的杂化状态为sp ,较双键(sp 2)的s 成份为多,由于s 成份的增加,使sp 杂化轨道比sp 2杂化轨道的直径短,因而造成碳碳三键较双键为短。
所以在炔烃中形成π键的两个p 轨道的重叠程度较烯烃为大,使炔烃中的π键更强些。
而且由于不同杂化状态的电负 性为sp >sp 2>sp 3,炔烃分子中的sp 碳原子和外层电子(π电子)结合得更加紧密,使其不易给出电子,因而使快烃不易发生亲电加成反应。
(2).由于电子的屏蔽效应不同炔烃和烯烃分子中,都存在着σ电子和π电子,可以近似地看成π电子是在σ电子的外围。
σ电子受原子核的吸引而π电子除受原子核的吸引外还受内层电子的排斥作用,因而就减弱了受核的束缚力,即为电子的屏蔽效应。
乙烯分子中有五个σ键,即有五对σ电子,而乙炔分子中只有三个σ键即只有三对σ电子,因而乙烯分子中的电子的屏蔽效应大于乙炔分子,所以乙烯分子中的π电子受原子核的吸引力小,易给出电子,也就容易发生亲电加成反心,而乙炔则较难。
(3).炔烃比烯烃的加成较难的原因,还可以从形成的中间体碳正离子的稳定性不同来说明:R CH CH 2+E+R +H C H 2C E RCCH+E +RC +C HE由于烷基正离了要比烯基正离子稳定些,所以烯烃的亲电加成较易。

第二节烯烃炔烃第1课时烯烃课后训练巩固提升基础巩固1.甲烷中混有乙烯,欲除去乙烯得到纯净的甲烷,最好依次通过盛有下列哪些试剂的洗气瓶( )。
A.溴水,烧碱溶液,浓硫酸B.酸性KMnO4溶液,浓硫酸C.澄清石灰水,浓硫酸D.浓硫酸,酸性KMnO4溶液答案:A解析:乙烯能与溴发生加成反应而被除去,烧碱溶液能吸收挥发出来的溴蒸气,浓硫酸能吸收水蒸气。
2.下列现象中,不是因为发生化学反应而产生褪色现象的是( )。
A.乙烯使酸性KMnO4溶液褪色B.将直馏汽油滴入溴水中,振荡后水层接近无色C.乙烯使溴的四氯化碳溶液褪色D.甲烷与氯气混合,光照一段时间后黄绿色消失答案:B解析:溴在直馏汽油中的溶解度大于在水中的溶解度。
直馏汽油滴入溴水中,振荡后水层褪色,褪色的原因是发生了萃取,不是发生了化学反应。
3.有关烯烃的下列说法中,正确的是( )。
A.烯烃分子中所有的原子都采取sp2杂化B.烯烃在适宜的条件下只能发生加成反应,不能发生取代反应C.分子式是C4H8的烃分子中一定含有碳碳双键D.烯烃既能使溴水褪色也能使酸性KMnO4溶液褪色答案:D解析:烯烃分子中,双键碳原子采取的是sp2杂化,其他饱和碳原子采取的是sp3杂化;加成反应是不饱和键的特征反应,但若烯烃中还含有烷基等其他原子团时,一定条件下也可发生取代反应;分子式为C4H8的烃可以是烯烃,也可以是环烷烃,而环烷烃中并不含碳碳双键;烯烃中的碳碳双键既可以与Br2加成而使溴水褪色,也可以被酸性KMnO4溶液氧化而使酸性KMnO4溶液褪色。
4.由乙烯推测丙烯的结构或性质正确的是( )。
A.分子中所有原子在同一平面上B.与HCl加成只生成一种产物C.能使酸性KMnO4溶液褪色D.能与溴水发生取代反应而使溴水褪色答案:C解析:丙烯分子结构中含有—CH3,由甲烷的空间结构可知,丙烯分子中所有原子一定不在同一平面上;丙烯分子中含有,能与Br2发生加成反应,能被酸性KMnO4溶液氧化;丙烯与HCl发生加成反应的产物可能为CH3CH2CH2Cl或。

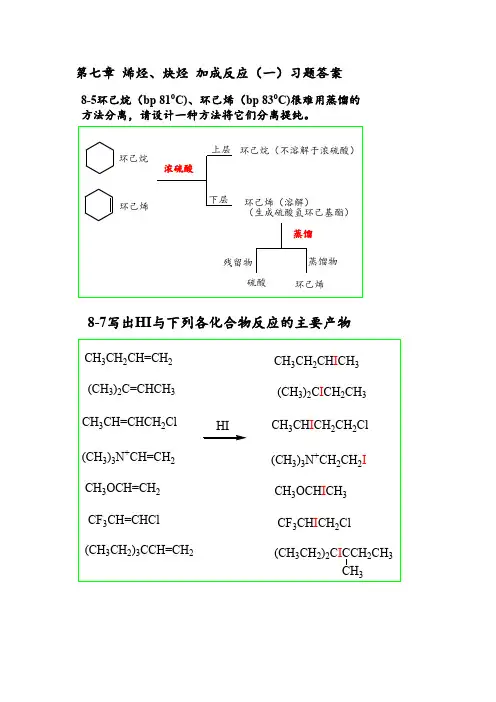
第七章烯烃、炔烃加成反应(一)习题答案8-5环己烷(bp 81o C)、环己烯(bp 83o C)很难用蒸馏的方法分离,请设计一种方法将它们分离提纯。
环己烷环己烯浓硫酸上层下层环己烷(不溶解于浓硫酸)环己烯(溶解)(生成硫酸氢环己基酯)蒸馏残留物蒸馏物硫酸环己烯8-7写出HI与下列各化合物反应的主要产物8-13苯乙烯在甲醇溶液中溴化,得到1-苯基-1,2-二溴乙烷和1-苯基-1-甲氧基-2-溴乙烷。
写出反应机理8-20A, B两个化合物,分子式均为C7H14。
A和KMnO4溶液加热反应生成4-甲基戊酸,并有一种气体逸出;B与KMnO4溶液或Br2/CCl4溶液都不发生反应,B分子中有二级8-21完成下列反应,写出主要产物8-23有A,B两个化合物,其化学式都是C6H12。
A经臭氧化,并经锌和酸处理得到乙醛和甲乙酮;B经高锰酸钾氧化只得到丙酸。
请写出A,B的构造式。
8-24完成下列反应,写出主要产物8-27完成下列反应,写出主要产物(反应物物质的量比为1:1)8-37化合物A 和B ,相对分子质量均为54,含碳88.8%,含氢11.1%,都能使溴的四氯化碳溶液褪色。
A 与Ag(NH 3)2+溶液反应产生沉淀,A 经KMnO 4热溶液氧化得CO 2和CH 3CH 2COOH ;B 不与银氨溶液反应,用热的KMnO 4溶液氧化得CO 2和HOOCCOOH 。
写出A 和B 的构造式及有关反应的化学式。
8-38用化学方法鉴别下列化合物CH 3CH 2CH 2CH 3CH 3CH 2CH=CH 2CH 3CH 2C ≡CH CH 3CH 2CH 2CH 2I CH 3CH 2CH 2CH 2ClAg(NH 3)2+(+)(+)(+)(-)(-)(-)(-)(-)(-)(-)AgNO 3/C 2H 5OH(+)(-)Br 2/CCl 4加热后白色沉淀方式(一)8-49完成下列反应,写出主要产物。

第1章第3节第2课时1.制取较纯净的一氯乙烷最好采用的方法是( )A.乙烷和氯气反应B.乙烯和氯气反应C.乙烯和氯化氢反应D.乙烷通入浓盐酸解析:乙烷和氯气发生取代反应生成一氯乙烷、二氯乙烷等多种有机产物,不纯,A错;乙烯和氯气发生加成反应生成,B错;乙烯和氯化氢加成生成CH3CH2Cl,C正确;乙烷通入浓盐酸不反应,D错。
答案: C2.由乙炔制CHClBr—CH2Br,下列方法中最可行的是( )A.先与HBr加成后再与HCl加成B.先与H2完全加成后再与Cl2、Br2发生取代反应C.先与HCl加成后再与Br2加成D.先与Cl2加成后再与HBr加成解析:A、D两项不可能得到产物CHClBr—CH2Br;B可能得到产物CHClBr—CH2Br,但生成的是含产物在内的多种物质,B方法不可行。
答案: C3.有八种物质:①甲烷、②苯、③聚丙烯、④聚1,3丁二烯,⑤2丁炔、⑥环己烷、⑦乙烯,既能使酸性KMnO4溶液褪色,又能使溴的CCl4溶液褪色的是( )A.③④⑤⑥⑦ B.④⑤⑥C.④⑤⑦D.③④⑤解析:下表中用“√”表示褪色,用“×”表示不褪色答案: C4.由乙烯推测丙烯的结构或性质正确的是( )A.分子中3个碳原子在同一直线上B.分子中所有原子在同一平面上C.与HCl加成只生成一种产物D.能使酸性高锰酸钾溶液褪色解析:答案: D5.某种烯烃与H2加成后的产物是CHCH3CH3CHCH3C(CH3)3,则该烯烃的结构可能有( )A.1种B.2种C.3种D.4种解析:加成前若有双键,加成后的碳上应有氢,则该烯烃的结构可能有:答案: C6.下列各选项能说明分子式为C4H6的某烃是CH≡C—CH2—CH3,而不是CH2===CH—CH ===CH3的事实是(双选)( )A.燃烧时有浓烟B.能使酸性KMnO4溶液褪色C.所有原子一定不在同一平面上D.与足量溴水反应,生成物中只有2个碳原子上有溴原子解析:由于分子式相同,燃烧时火焰的明亮程度及产烟程度相同,且C元素质量分数较高,燃烧时均有浓烟,A项不符合题意;二者均使酸性KMnO4溶液褪色,B项不符合题意;HC≡C—CH2—CH3分子中含有饱和碳原子,所有原子肯定不在同一平面上,CHCH2===CH—CH===CH2分子中所有原子有可能共平面,C项符合题意;CH2===CH—CH===CH3与足量溴水反应,只有1、2号碳原子上有溴原子,而CH2==CH—CH==CH2与足量溴水反应后所有碳原子上均有溴原子,D项符合题意。

第5章炔烃二烯烃思考题答案思考题5-1写出C6H14的炔烃异构体,并用系统命名法命名。
答案:思考题5-2用化学方法鉴别己烷、己烯和己炔。
答案:或思考题5-3判断2-戊炔与下列试剂有无反应,如有反应,写出主要产物的结构式。
1.Br2(1mol)2.HCl(1mol)3.H3O+4.AgNO3,NH4OH5.CH3CH2MgBr6.1)B2H6;2)H2O2,OH7.H2/Lindlar Pd 8.Na+NH3(l) 答案:1. 2.3. 4. ×5. ×6.7. 8.思考题5-4完成下列转换。
1.2.3.4..思考题5-5 用IUPAC 规则命名下列化合物答案:(2E,4E)-2,4-己二烯 (2Z,4E)-2,4-己二烯思考题5-6 在分子C CH C CH 3CH 3CH 3CH 3中存在哪些类型的共轭?答:σ-π共轭,ρ-π共轭,ρ-σ共轭思考题5-7写出下列反应式的主要产物 (1)答案:以1,2-加成产物为主(动力学控制)(2)答案:以1,4-加成产物 为主(热力学控制)思考题5-8 用化学方法鉴别1,5-庚二烯,1,3-庚二烯,1-庚炔 答案:习题答案习题5-1答案:(1) 2,2-二甲基-3-己炔 (2) 1-己烯-5-炔 (3) 4-乙烯基-4-庚烯-2-炔(4) (3E)-1,3-己二烯 (5) (2Z,4E)-2,4-己二烯 (6) 5-氯-1,3-戊二烯(7) 1,3,5-己三烯习题5-2 写出下列化合物的构造式。
(1)4-苯基-1-戊炔 (2)3-甲基-3-戊烯-1-炔 (3)乙基叔丁基乙炔(4)3-仲丁基-4-己烯-1-炔 (5)异戊二烯 (6)(2E,4E)2,4-己二烯 (7)丁苯橡胶答案:(1) (2) (3) (4)(5) (6) (7)习题5-3答案: (1) CH3CH2COOH,CO2 (2)(3) (4)(5)(6)(7)习题5-4 用反应式表示以丙炔为原料并选用必要的无机试剂合成下列化合物。

烯烃和炔烃(定稿带答案)第X课时烯烃和炔烃⾼考⽬标与要求1.以烷、烯、炔的代表物为例,⽐较它们在组成、结构、性质上的差异。
2.根据有机化合物组成和结构的特点,认识加成、取代反应。
3.举例说明烃类物质在有机合成和有机化⼯中的重要作⽤。
知识梳理1.烷烃、烯烃、炔烃的组成、结构特点和通式2.物理性质(1)随着分⼦中碳原⼦数的递增,烃的物理性质呈现规律性的变化。
C n H 2n +2+3n +12O 2――→点燃n CO 2+(n +1)H 2O(2)甲烷、⼄烯、⼄炔的结构和物理性质⽐较烃类甲烷⼄烯⼄炔分⼦式 CH 4 C 2H 4 C 2H 2 结构简式CH 2==CH 2CH ≡CH 分⼦结构特点正四⾯体结构,键⾓为 109°28′ ,由极性键形成的⾮极性分⼦平⾯结构,键⾓为 120°,所有原⼦处于同⼀平⾯内,⾮极性分⼦ H —C ≡C —H直线型结构,键⾓为 180°,分⼦中所有的原⼦均处于同⼀直线上,⾮极性分⼦物理性质⽆⾊、⽆味⽓体,极难溶于⽔,密度⽐空⽓⼩⽆⾊、稍有⽓味的⽓体,难溶于⽔,密度⽐空⽓略⼩纯⼄炔是⽆⾊、⽆味的⽓体,密度⽐空⽓⼩,微溶于⽔碳的质量分数75% 85.7%92.3%3.甲烷、烷烃的化学性质 (1)甲烷的化学性质①通常状况下,甲烷的性质稳定 ,与强氧化剂(如KMnO4)、强酸、强碱等均不能发⽣化学反应。
但在⼀定条件下可以燃烧,可以发⽣取代反应。
②取代反应:有机物分⼦⾥的某些原⼦或原⼦团被其他原⼦或原⼦团所替代的反应。
甲烷与Cl2发⽣取代反应的化学⽅程式:(2)烷烃的化学性质和甲烷类似,通常较稳定,在空⽓中能点燃,在光照条件下能与氯⽓发⽣取代反应。
①稳定性:通常情况下,与强氧化剂、强酸及强碱都不发⽣反应,也难与其他物质化合。
②可燃性:③取代反应:与⽓态卤素单质在光照条件下发⽣取代反应。
如⼄烷和氯⽓⽣成⼀氯⼄烷: CH 3CH 3+Cl 2――→光 CH 3CH 2Cl +HCl ④⾼温裂解:如重油裂化过程: C 8H 18―――→⾼温C 4H 10+C 4H 84.⼄烯、烯烃的化学性质 (1)⼄烯的化学性质①氧化反应a.⼄烯在空⽓中能燃烧,⽕焰明亮带有⿊烟。
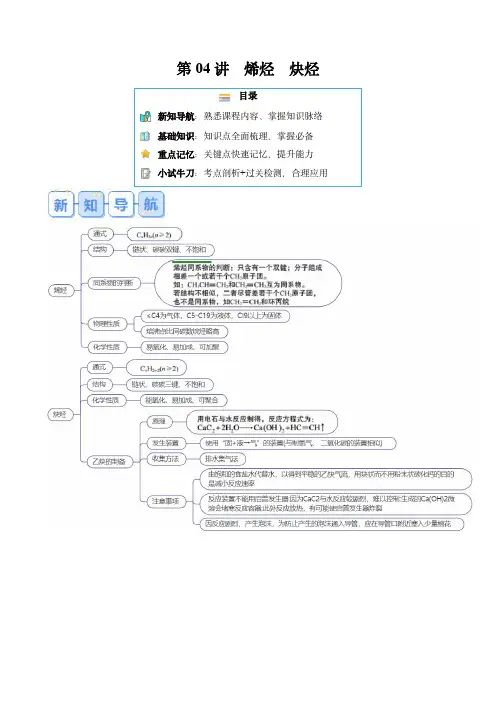
第04讲烯烃炔烃目录新知导航:熟悉课程内容、掌握知识脉络基础知识:知识点全面梳理,掌握必备重点记忆:关键点快速记忆,提升能力小试牛刀:考点剖析+过关检测,合理应用课时1烯烃一.烯烃的结构和性质1.烯烃及其结构(1)烯烃:含有碳碳双键的烃类化合物。
(2)官能团:名称为碳碳双键,结构简式为。
(3)通式:烯烃只含有一个碳碳双键时,其通式一般表示为C n H 2n (n ≥2)。
(4)乙烯的结构特点分子中碳原子采取sp 2杂化,碳原子与氢原子间均形成单键(σ键),碳原子与碳原子间以双键相连(1个σ键,1个π键),键角约为120°,分子中所有原子都处于同一平面内。
2.烯烃的物理性质(1)沸点:随碳原子数的递增而逐渐升高。
(2)状态:常温下由气态逐渐过渡到液态、固态,当烯烃分子中碳原子数≤4时,常温下呈气态。
(3)溶解性和密度:难溶于水,易溶于有机溶剂,密度比水小。
3.烯烃的化学性质——与乙烯相似(1)氧化反应①烯烃能使酸性高锰酸钾溶液褪色。
②可燃性燃烧通式为C n H 2n +3n 2O 2――→点燃n CO 2+n H 2O 。
(2)加成反应①烯烃能与H 2、X 2、HX 、H 2O 等发生加成反应,写出下列有关反应的化学方程式:a .丙烯与溴的四氯化碳溶液反应生成1,2-二溴丙烷:CH 2==CHCH 3+Br 2―→。
b .乙烯制乙醇:CH 2==CH 2+H 2O――→催化剂△CH 3CH 2OH 。
c .乙烯制氯乙烷:CH 2==CH 2+HCl――→催化剂△CH 3CH 2Cl 。
d .丙烯转化为丙烷:CH 2==CHCH 3+H 2――→催化剂△CH 3CH 2CH 3。
(3)加聚反应丙烯发生加聚反应的化学方程式:n CH 2==CHCH 3――→催化剂。
4.二烯烃的加成反应(1)定义:分子中含有两个碳碳双键的烯烃称为二烯烃,如1,3-丁二烯的结构简式为CH 2==CH—CH==CH 2。
第十三章 第二节第2节 烯烃炔烃解析 人教版本栏目内容在学生用书中以活页形式单独装订成册!一、选择题1.下列物质不能使KMnO 4酸性溶液褪色的是( )A .丙烷B .乙烯C .乙苯D .二氧化硫【解析】 乙烯和乙苯能被KMnO 4酸性溶液氧化,SO 2具有还原性,能与具有强氧化性的KMnO 4酸性溶液反应;丙烷不与KMnO 4酸性溶液反应。
【答案】 A2.下列关于乙炔性质的叙述中,既不同于乙烯又不同于乙烷的是( )A .能燃烧生成二氧化碳和水B .能发生加成反应C .能与高锰酸钾溶液发生氧化反应D .能与氯化氢反应生成氯乙烯【解析】 C 2H 2、C 2H 4、C 2H 6均能燃烧(生成CO 2和H 2O),C 2H 2和C 2H 4均能发生加成反应,均能与KMnO 4发生氧化反应。
C 2H 6不与HCl 反应,C 2H 4与HCl 反应生成C 2H 5Cl(氯乙烷),只有C 2H 2与HCl 反应生成CH 2=CHCl(氯乙烯)。
【答案】 D3.甲烷中混有乙烯,欲除去乙烯得到纯净的甲烷,最好依次通过盛有什么试剂的洗气瓶( )A .澄清石灰水、浓硫酸B .KMnO 4酸性溶液、浓硫酸C .溴水、浓硫酸D .浓硫酸、KMnO 4酸性溶液【解析】 除去CH 4中混有的C 2H 4必须满足试剂只能吸收C 2H 4而不能吸收CH 4,且最后CH 4中不能含有H 2O ,KMnO 4酸性溶液氧化C 2H 4生成CO 2,CO 2不能被浓硫酸吸收,故只能选C 。
【答案】 C4.在120 ℃时,装有等物质的量CO 和某烯烃的密闭容器中,充入足量O 2点燃,充分燃烧,当恢复到原条件时,测知容器内反应前后压强相等,此烯烃是( )A .乙烯B .丙烯C .丁烯D .戊烯【解析】 设烯烃的分子式为C n H 2nCO +C n H 2n +3n +12O 2――→点燃(n +1)CO 2+n H 2O 由题意可得:1+1+3n +12=n +1+n n =3。
第2课时烯烃、炔烃和苯及其同系物的性质 [课标要求]1.掌握烷烃、烯烃、炔烃、苯及其同系物的化学性质。
2.能从结构的角度分析烷烃、烯烃和炔烃化学性质的不同及烯烃与炔烃化学性质相似的原因。
,1.烯烃、炔烃分子中含有不饱和的双键、叁键,容易与卤素单质、卤化氢、H 2、H 2O 等发生加成反应,易被酸性高锰酸钾溶液氧化,能发生加聚反应生成高分子化合物。
2.苯及其同系物的分子式通式为C n H 2n -6(n ≥6),易发生取代反应,难发生加成反应,在苯的同系物中,若连接苯环烷基的碳原子上有氢原子,也被酸性高锰酸钾溶液氧化。
烯烃、炔烃的化学性质1.化学性质 (1)可燃性C 2H 4+3O 2――→点燃2CO 2+2H 2O 2C 2H 2+5O 2――→点燃4CO 2+2H 2O (2)与卤素单质、氢气、氢卤酸等的反应 ①与卤素单质发生加成反应 CH CH +Br 2―→CHBr===CHBr CHBr===CHBr +Br 2―→CHBr 2—CHBr 2 CH 3—CH===CH 2+Br 2―→CH 3—CHBr —CH 2Br ②与氢气发生加成反应CH 3—CH===CH 2+H 2――→催化剂CH 3—CH 2—CH 3 CH CH +2H 2――→催化剂CH 3CH 3③与氢卤酸发生加成反应烯烃、炔烃与氢卤酸发生加成反应生成卤代烃。
CH CH +HCl ――→催化剂△CH 2===CHCl ④加成聚合反应n CH 3—CH===CH 2――→引发剂n HC CH ――→引发剂(3)与酸性KMnO 4溶液的反应 ①烯烃被酸性高锰酸钾溶液氧化氧化产物与不饱和键在碳链中的位置有关,如下表②乙炔被酸性高锰酸钾溶液氧化 CH CH ――――――――→酸性KMnO 4溶液CO 2+H 2O③利用酸性KMnO 4溶液可以鉴别烷烃与烯烃或烷烃与炔烃。
2.应用在有机合成中,通过这些反应可以得到含有卤原子、氰基、羰基、羧基等官能团的化合物。
第2课时炔烃课后·训练提升基础巩固1.某炔烃与氢气加成后得到,该炔烃可能有的结构式有( )。
A.1种B.2种C.3种D.4种答案:B解析:给2-甲基戊烷中各碳原子编号可得:,其中2号C上只含有1个氢原子,无法添加碳碳三键,能够添加碳碳三键的碳原子为3、4和4、5两个位置,所以满足炔烃的结构有2种。
2.由两种气态烃组成的混合气体完全燃烧后所得到的CO2和H2O的物质的量随混合烃的总物质的量的变化如图所示,则下列对混合烃的判断正确的是( )。
A.混合气体一定是甲烷和乙烯B.混合气体中可能含有C3H4C.混合气体中可能有乙烷D.混合气体中一定有乙炔(CH≡CH)答案:B解析:由图可知两种气态烃的平均组成为C1.6H4,根据碳原子平均数可知,混合气体一定含有CH4,由氢原子平均数可知,另一气态烃中氢原子数目为4,碳原子数目大于1.6,且为气体,可能含有C3H4(丙炔)、乙烯,一定没有乙烷、丙烷。
3.下列说法中正确的是( )。
①丙炔分子中三个碳原子有可能位于同一直线上②乙炔分子中碳碳间的三个共价键性质完全相同③分子组成符合C n H2n-2通式的链烃一定是炔烃④乙炔及其同系物中,乙炔的含碳量最大A.①②B.②③C.③④D.①④答案:D解析:由乙炔的分子结构可推知丙炔中的三个碳原子应在同一直线上;碳碳三键中有一个共价键与其余两个共价键不同;符合C n H 2n -2通式的链烃还可以是二烯烃;乙炔同系物C n H 2n -2中碳的质量分数为12n 14n -2×100%=1214-2n×100%,n 增大时,14-2n增大,含碳量减小,故n =2时含碳量最大。
4.块状固体电石遇水会剧烈反应生成乙炔气体。
实验室若用此法制取乙炔,选择的装置最好是图中的( )。
答案:B5.两分子乙炔在一定条件下可生成乙烯基乙炔(),下列关于乙烯基乙炔的说法错误的是( )。
A.能使酸性高锰酸钾溶液褪色 B.能发生加聚反应生成高分子 C.分子中所有碳原子都在一条直线上 D.没有顺反异构现象 答案:C解析:乙烯基乙炔为,分子中含有一个碳碳双键、一个碳碳三键,都能使酸性高锰酸钾溶液褪色,所以A 项正确;乙烯基乙炔为,分子中含有不饱和键,能发生加聚反应生成高分子,所以B 项正确;乙烯是平面结构,乙炔是直线形分子,乙烯基乙炔分子中的所有原子一定都共平面,但不是所有碳原子都在一条直线上,故C 项错误;乙烯基乙炔为,其中连接相同的H 原子,不具有顺反异构,所以D 项正确。
烯烃炔烃基础一、单选题1.下列烃中不是饱和烃的是()A.CH4B.C2H4C.C2H6D.C4H102.下列关于乙烷(CH3—CH3)和乙烯(CH2===CH2)的说法中不正确的是()A.乙烷和乙烯都是由碳、氢两种元素组成B.乙烷属于饱和烃,乙烯属于不饱和烃C.乙烷和乙烯分子中碳原子形成的共价键相同D.乙烯分子中的碳原子还能结合氢原子3.某烯烃的相对分子质量为84,该烯烃的分子式是()A.C4H10B.C5H10C.C6H12D.C6H144.据报道,科学家合成了一种分子式为C200H300含多个碳碳双键的链状烃,其分子中所含碳碳双键最多是()A.48个B.49个C.50个D.51个5.某混合气体由两种气态烃组成。
2.24 L该混合气体完全燃烧后,得到4.48 L二氧化碳(气体已折算成标准状况)和3.6 g水。
则这两种气体可能是()A.CH4和C3H8B.CH4和C3H4C.C2H4和C3H4D.C2H4和C2H66.乙烷和乙烯的混合气体200 mL,在催化剂的作用下与氢气发生加成反应,最多消耗氢气100 mL,则原混合气体中乙烷和乙烯的体积比是()A.2∶1B.3∶1C.1∶1D.1∶37.一种气态烷烃和气态烯烃组成的混合物共10 g,混合气体的密度是相同状况下氢气密度的12.5倍,该混合气体通过装有溴水的试剂瓶时,试剂瓶总质量增加了8.4 g,该混合气体的组分可能是() A.乙烯和乙烷B.乙烷和丙烯C.甲烷和乙烯D.丙烯和丙烷8.下列有关乙炔的说法不正确的是()A.燃烧时有浓厚的黑烟B.实验室制乙炔时可用CuSO4除杂质气体C.为了减缓电石和水的反应速率,可用饱和食盐水来代替D.乙炔的收集方法可用排空气法收集9.下列有关烃说法叙述正确的是()A.通式为C n H2n+2的烃一定是烷烃B.通式为C n H2n的烃一定是烯烃C.通式为C4H6的烃一定是炔烃D.相对分子质量为128的烃一定是烷烃10.已知Mg2C3的结构与CaC2相似,由此可断定Mg2C3与水反应的产物是()A.Mg(OH)2和CH≡CH B.MgO和CH≡CHC.Mg(OH)2和CH3CH=CH2D.Mg(OH)2和CH3C≡CH11.下列烯烃中存在顺反异构体的是()A.丙烯B.1-丁烯C.3-己烯D.2-甲基-2-丁烯二、填空题13.已知碳原子数小于或等于8的某单烯烃与HBr反应,其加成产物只有一种结构。
烯烃和炔烃2 2014.12.201.下列加成反应违反马氏加成规则的是A .CH 3CH=CH 2+HBrB .CH 2=C(CH 3)CH 3+HClC .CH 3CH=CH 2+HBrD .CH 2=C(CH 3)CH 3+HOCl2.实验室可用来制取乙烯的装置是A .B .C .D .3.下列物质中,与1-丁烯互为同系物的是A.丙炔 B.2-丁炔 C.4-甲基-1-丁炔 D.2-戊烯 4.室温下,下列物质分别与硝酸银氨溶液作用,能立即产生沉淀的是A.乙烯 B.2-丁炔 C.2-戊烯 D.3-甲基-1-丁炔 5.能使Br 2-CCl 4溶液褪色的物质是 A .乙烷 B .乙烯 C .乙苯 D .乙醇6.某气态烃含碳85.7%,氢14.3%,标准状况下密度是2.5g/L ,则此烃的化学式是 A. C 3H 6 B. C 3H 8 C. C 4H 8 D. C 4H 10 7.在下列烯烃中,用作水果催熟剂的是A 、乙烯B 、丙烯C 、丁烯D 、异丁烯8.炔银和炔亚铜干态时受撞击易爆炸,处理试验中炔银和炔亚铜的试剂是 A .盐酸 B .氢氧化钠溶液 C .水 D .丙酮溶液 9.分离1-戊炔和2-戊炔的试剂是A .溴的四氯化碳溶液B .硝酸银氨溶液、稀盐酸C .高锰酸钾溶液D .浓硫酸 10.制取较纯的氯乙烷,下列合成路线最佳的是 A .乙烷与氯气在光照下发生取代反应 B .乙烯与氯气加成 C .乙烯与HCl 加成 D .乙炔在Pt 催化下加氢,再与HCl 加成11.欲除去甲烷中混有的乙烯并检验得到的甲烷是否纯净,依次通过的试剂洗气瓶为 A .澄清的石灰水,浓H 2SO 4B .浓H 2SO 4,硝酸银氨溶液C .溴水,浓H 2SO 4D .浓H 2SO 4,酸性KMnO 4溶液 12.制取氯乙醇的正确做法是A .乙烯与氯水反应B .乙烯与氯气反应C .乙炔与氯水反应D .乙烷与氯水反应 13.实验室制取乙炔的方法是A .甲烷瞬间高温脱氢B .石油中短链烃的裂解C .电石与水反应D .植物秸秆发酵 14.分离1-戊炔和2-戊炔的试剂是A .溴的四氯化碳溶液B .硝酸银氨溶液、稀盐酸C .高锰酸钾溶液D .浓硫酸 15. 下列物质中与2—戊烯互为同系物的是 A .1—戊烯 B .2—甲基—1—丁烯 C .2—甲基—2—丁烯 D .4—甲基—1—戊烯 16.化合物C 5H 10经酸性高锰酸钾氧化后产物是乙酸和丙酮,该化合物是 ( )A .2-甲基-1-戊烯B .3-甲基-1-戊烯C .2-甲基-2-丁烯D .3-甲基-1-丁烯 17. 下列反应中,属于加成反应的是A. 乙烯与酸性高锰配钾溶液反应,使KMnO4褪色B. 乙烯与溴的CCl4溶液反应使溴褪色C. 乙炔通入硝酸银的氨溶液中有白色沉淀D.苯在加热及FeCl3催化下与溴反应,使溴褪色 18.2-甲基-2-丁烯与HBr 在冰醋酸作用下反应的主要产物是 A .2-甲基-1-溴丁烷 B .2-甲基-2-溴丁烷 C .3-甲基-1-溴丁烷 D .3-甲基-2-溴丁烷 19.同温同压下,燃烧相同质量的体积的下列气体,产生CO 2体积最多的是 A .CH 4 B .C 2H 6 C .C 2H 4 D .C 2H 2 20.在下列烯烃中,最易与浓硫酸反应的是 A .乙烯 B .丙烯 C .1—丁烯 D .异丁烯1、除去乙烷中乙烯的简便方法是()A.通入氢气加成制成烷烃B.通过浓硫酸C.通入水D.通入溴的四氯化碳溶液 2、下列气态烃充分燃烧后生成的二氧化碳和水的物质的量之比为4:3的是() A.C4H10 B.C4H8 C.C4H6 D.C3H43、石油裂解气净化过程中,将乙炔转化为乙烯选用的催化剂是() A.兰尼镍催化剂 B.齐格勒催化剂 C.林德拉催化剂 D.银催化剂4、分子式为C 6H 12的分子结构中含三个甲基的烯烃共有()过氧化物过氧化物A.2种B.3种C.4种D.5种5、使酸性高锰酸钾溶液和溴的四氯化碳溶液都褪色且氯化亚铜氨溶液生成红色沉淀的是()A.1-丁烯B.1-丁炔C.乙醇D.乙醛6、含一个三键的炔烃,氢化后产物的结构简式为CH3CH2CH(CH3)CH2CH(C2H5)2,此炔烃可能有的结构有()A.1种B.2种C.3种D.4种7、下列化合物中既能使溴的四氯化碳溶液褪色,又能在高温下与溴发生取代反应的是()A.甲苯B.乙醇C.丙烯D.乙烯8、某链状烯烃(C5H10)分子中含三个甲基且无顺反异构体,其构造简式为()A.CH2=CHCH2CH2CH3B.CH3CH=CHCH2CH3C.CH2=CHCH(CH3)2D.CH3CH=C(CH3)29、与乙炔具有相同的碳、氢百分含量,但既不是同系物又不是同分异构体的是()A.丙炔B.环丁烷C.甲苯D.苯(C6H6)10、下列气态物质不能用浓硫酸干燥的是()A.乙烷B.乙炔C.乙烯D.氯乙烷11、下列关于塑料王的叙述中,正确的是()A.其聚合单体为四氟乙烯B.其聚合单体为四氯乙烯C.易老化产生有毒气体D.紫外线照射下可分解产生氯原子12、既可鉴别1-丁炔和2-丁炔又可除去2-丁炔中少量1-丁炔的试剂是()A.溴的四氯化碳溶液B.酸性高锰酸钾溶液C.硝酸银的氨溶液D.硝酸银的乙醇溶液13、当有过氧化物存在时,丙炔与两分子氢溴酸加成反应生成()A.1,2-二溴丙烷B.1,1-二溴丙烷C.2,2-二溴丙烷D.1,3-二溴丙烷14、从某有机物燃烧后生成的CO2和H2O中可计算出它含碳80%,含氢20%,实验测定它的分子量为30,其分子式应是()A.C2H6B.C2H8C.CH6ND.CH4O15、分子式为C5H10的烯烃,其同分异构体的数目是()A.3B.4C.5D.616、在适当条件下,1mol丙炔与1mol溴化氢有过氧化物存在时加成的主要产物是()A.CH3CH2CHBr2B.CH3CBr2CH3C.CH3CH=CHBrD.CH2CBr=CH217、现阶段普遍使用的能源材料中最为清洁的是()A.用木材作燃料B.天然气C.煤炭D.汽油18、科学家发现C60后,近年又合成了许多球形分子(富勒烯),如C50、C70、C120、C540等以下叙述正确的是()A.属于同系物B.属于同分异构体C.化合价均为0 D.属于化合物19、某烯烃与氯化氢加成后得到2,2-二甲基-3-氯丁烷,则该烯烃的名称是()A.2,2-二甲基-3-丁烯B.2,2-二甲基-2-丁烯C.2,2-二甲基-1-丁烯D.3,3-二甲基-1-丁烯20、下列关于聚乙烯的说法中正确的是()A.纯净物B.混合物C.不易燃烧D.其产品不能制作食品包装袋21、分子式为C4H6的烃经高锰酸钾溶液氧化后产物是乙二酸和CO2,此烃是()A.1-丁烯B.2-丁烯C.1,3-丁二烯D.1-丁炔22、使裂化汽油中有少量烯烃转化为烷烃的方法是()A.催化加氢B.与HBr发生加成反应C.加入浓硫酸洗涤,再分离D.与氯气发生加成反应23、在加热条件下,可与溴化氢反应主要生成2-甲基-3-氯戊烷是()A.4-甲基-2-戊烯B.2-甲基-2-戊烯C.2-甲基-3-戊烯D.2-甲基-3-戊烯24、下列物质中与2-戊烯互为同分异构体的是()A.1,3-戊二烯B.2-甲基-1-丁烯C.2-甲基-2-戊烯D.4-甲基-1-戊烯25、在适当条件下1mol丙炔与1mol溴加成的主要产物是()A.CH3CH2CHBr2B.CH3CBr2CH3C.CH3CBr=CHBrD.CH2BrCHBr=CH226、下列分子中,所有原子都处在同一直线的是()A、环乙烯B.丙炔 C.乙炔 D.乙烯27、当有过氧化物存在时,氢溴酸与丙烯加成反应生成A.1-溴丙烯B.1-溴丙烷C.2-溴丙烯D.2-溴丙烷28、下图是无水醋酸钠和碱石灰反应制取CH4的装置,正确的是棉花DCBA。
第X课时烯烃和炔烃高考目标与要求1.以烷、烯、炔的代表物为例,比较它们在组成、结构、性质上的差异。
2.根据有机化合物组成和结构的特点,认识加成、取代反应。
3.举例说明烃类物质在有机合成和有机化工中的重要作用。
知识梳理1.烷烃、烯烃、炔烃的组成、结构特点和通式2.物理性质(1)随着分子中碳原子数的递增,烃的物理性质呈现规律性的变化。
性质变化规律状态常温下含有1~4个碳原子的烃都是气态,随着碳原子数的增多,逐渐过渡到液态、固态沸点随着碳原子数的增多,沸点逐渐升高;同分异构体之间,支链越多,沸点越低相对密度随着碳原子数的增多,相对密度逐渐增大,密度均比水小水溶性均难溶于水(2)甲烷、乙烯、乙炔的结构和物理性质比较烃类甲烷乙烯乙炔分子式CH4C2H4C2H2结构简式CH2==CH2CH≡CH分子结构特点正四面体结构,键角为109°28′ ,由极性键形成的非极性分子平面结构,键角为120°,所有原子处于同一平面内,非极性分子H—C≡C—H直线型结构,键角为180°,分子中所有的原子均处于同一直线上,非极性分子物理性质无色、无味气体,极难溶于水,密度比空气小无色、稍有气味的气体,难溶于水,密度比空气略小纯乙炔是无色、无味的气体,密度比空气小,微溶于水碳的质量分数75% 85.7% 92.3%3.甲烷、烷烃的化学性质(1)甲烷的化学性质①通常状况下,甲烷的性质稳定 ,与强氧化剂(如KMnO4)、强酸、强碱等均不能发生化学反应。
但在一定条件下可以燃烧,可以发生取代反应。
②取代反应:有机物分子里的某些原子或原子团被其他原子或原子团所替代的反应。
甲烷与Cl2发生取代反应的化学方程式:C n H 2n +2+3n+12O 2――→点燃n CO 2+(n +1)H 2O (2)烷烃的化学性质和甲烷类似,通常较稳定,在空气中能点燃,在光照条件下能与氯气发生取代反应。
① 稳定性:通常情况下,与 强氧化剂 、 强酸 及 强碱 都不发生反应,也难与其他物质化合。
② 可燃性: ③ 取代反应:与气态卤素单质在光照条件下发生取代反应。
如乙烷和氯气生成一氯乙烷: CH 3CH 3+Cl 2――→光 CH 3CH 2Cl +HCl ④ 高温裂解:如重油裂化过程: C 8H 18―――→高温C 4H 10+C 4H 84.乙烯、烯烃的化学性质 (1)乙烯的化学性质 ①氧化反应a.乙烯在空气中能燃烧,火焰明亮带有黑烟。
燃烧的化学方程式为: C 2H 4+3O 2―――→点燃2CO 2+2H 2Ob.乙烯通入酸性KMnO4溶液中,现象为KMnO4溶液的紫红色褪去 。
②加成反应a.定义:有机物分子中的 双键或三键断裂,两端 碳原子与其他原子或原子团直接结合生成新的化合物的反应。
b .乙烯与溴水、H2、HCl 、H2O 反应的化学方程式分别为。
③加聚反应合成聚乙烯塑料的化学方程式为n CH 2==CH 2――――――→一定条件CH 2CH 2(2)烯烃的化学性质①与酸性KMnO 4溶液的反应能使酸性KMnO 4溶液 褪色 ,发生 氧化 反应。
②燃烧燃烧通式为 C n H 2n +3n 2O 2――→点燃n CO 2+n H 2O。
③加成反应CH 2==CH —CH 3+Br 2―→CH 2==CH —CH 3+H 2O ―――→催化剂△④加聚反应nCH 2==CH —CH 3――――→催化剂。
5.炔烃的化学性质 (1)与酸性KMnO 4溶液的反应能使酸性KMnO 4溶液 褪色 ,如:CH≡CH――――→KMnO 4H 2SO 4 CO2 (主要产物)。
(2)燃烧燃烧通式为 C n H 2n -2+3n -12O 2――→点燃n CO 2+(n -1)H 2O。
(3)加成反应CH≡CH+H 2―――→催化剂△CH≡CH+2H 2――――→催化剂△(4)加聚反应nC H≡CH ―――→引发剂CH 2==CH 2CH 3—CH 3 CH==CH6.乙烯实验室制法实验室制备乙烯时的注意事项①用量:浓硫酸作催化剂和脱水剂,乙醇和浓硫酸的体积比约为1∶3。
②顺序:反应物进行混合时,应把浓硫酸慢慢注入酒精中。
③温度:140 ℃时生成乙醚,所以温度要迅速升高到170 ℃。
④干扰:浓硫酸使乙醇脱水生成碳而使混合液变黑,碳与浓硫酸反应会生成二氧化硫。
由于二氧化硫能使溴水和高锰酸钾溶液褪色,在验证乙烯的性质时必须把二氧化硫除去以排除干扰。
⑤实验装置:⑥实验原理: 方法点拨一是必须熟悉不饱和烃的代表物乙烯和乙炔的结构特点:①乙烯分子中的所有原子都在同一平面内,键角为120°,如。
当乙烯分子中某氢原子被其他原子或原子团取代时,则代替该氢原子的原子一定在乙烯的平面内。
②乙炔分子中的2个碳原子和2个氢原子一定在一条直线上,键角为180°,如。
当乙炔分子中的一个氢原子被其他原子或原子团取代时,代替该氢原子的原子一定和乙炔分子中的其他原子共线。
二是必须掌握不饱和烃如烯烃、炔烃和二烯烃的性质,它们均具有不饱和键,化学性质也类似,均可发生以下反应:①加成反应:分子中的碳碳双键或碳碳三键断裂,双键或三键两端的原子可与其他原子或原子团结合。
②加聚反应:实质上是加成反应,与普通加成反应有所不同的是生成的产物一般为高分子化合物。
③氧化反应:可以燃烧,也可以被酸性高锰酸钾溶液氧化。
温度计:控制温度水银球位置:混合溶液中,但不接触器壁 碎瓷片:防爆沸CH 3CH 2OH CH 2=CH 2↑+H 2O ―――→浓流酸170℃典型考题回放1.(11全国卷一)金刚烷是一种重要的化工原料,工业上可通过下列途径制备:请回答下列问题:(1)环戊二烯分子中最多有____________个原子共平面;(2)金刚烷的分子式为_______________,其分子中的CH2基团有_____________个;(3)下面是以环戊烷为原料制备环戊二烯的合成路线:其中,反应①的产物名称是______________________,反应②的反应试剂和反应条件是______________________________,反应③的反应类型是_______________;(4)已知烯烃能发生如下反应:请写出下列反应产物的结构简式:(5) A是二聚环戊二烯的同分异构体,能使溴的四氯化碳溶液褪色,A经高锰酸钾酸性溶液加热氧化可以得到对苯二甲酸【提示:苯环上的烷基(一CH3,一CH2R,一CHR2)或烯基侧链经高锰酸钾酸性溶液氧化得羧基】,写出A所有可能的结构简式(不考虑立体异构):答案:(1)9(2)C10H16;6(3)氯代环戊烷;氢氧化钠乙醇溶液,加热;加成反应(4)(5)巩固练习1.有机化学中的反应类型较多,将下列反应归类。
(填写序号)①由乙烯制氯乙烷②乙烷在氧气中燃烧③乙烯使溴的四氯化碳溶液褪色④乙烯使酸性高锰酸钾溶液褪色⑤由乙烯制聚乙烯⑥甲烷与氯气在光照的条件下反应其中属于取代反应的是__________;属于氧化反应的是__________;属于加成反应的是____________;属于聚合反应的是__________。
2.判断正误(1)聚乙烯可发生加成反应( )(2)乙烯和甲烷可用酸性高锰酸钾溶液鉴别( )(3)乙烯和苯都能与溴水反应( )(4)乙烯和乙烷都能发生加聚反应( )(5)苯不能使溴的四氯化碳溶液褪色,说明苯分子中没有与乙烯分子中类似的碳碳双键( )(6)甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应( ) 3.1 mol乙烷和1 mol氯气混合,在紫外线作用下可以发生反应,则生成的含氯有机物是() A.只有CH3CH2Cl B.只有CH2ClCH2ClC.只有CH2Cl2 D.多种氯代物4.下列过程与加成反应有关的是 ( ) A.苯与溴水混合振荡,水层颜色变浅B.乙烯与溴水混合振荡,水层颜色变浅C.乙烯与高锰酸钾溶液混合振荡,溶液颜色变浅D.甲烷与氯气混合光照,气体颜色变浅5. “不粘锅”炊具是在金属锅的内壁上涂一薄层聚四氟乙烯制成,下列各项对聚四氟乙烯的叙述中正确的是()A. 在聚四氟乙烯的单体中不含有碳碳双键B. 聚四氟乙烯在高温时容易燃烧C. 聚四氟乙烯的化学性质很稳定,正常使用时不会发生化学变化D. 聚四氟乙烯的分子内支链很多,且彼此缠绕,不会污染食物6.下列各组物质在一定条件下反应,可以制得较纯净的1,2-二氯乙烷的是()A.乙烷与氯气混合B.乙烯与氯化氢气体混合C.乙烯与氯气混合D.乙烯通入浓盐酸7.实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4反应生成少量的二氧化硫,有人设计下列实验以确认上述混合气体中有乙烯和二氧化硫。
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ装置可盛放的试剂是:Ⅰ___________;Ⅱ___________;Ⅲ___________;Ⅳ___________(将下列有关试剂的序号填入空格内)。
A.品红溶液B.NaOH(aq)C.浓H2SO4D.酸性KMnO4(aq)(2)能说明二氧化硫气体存在的现象是_______________________________。
(3)使用装置Ⅱ的目的是___________________________________________。
(4)使用装置Ⅲ的目的是___________________________________________。
(5)确证含有乙烯的现象是_________________________________________。
答案:1、6; 2,4; 1,3; 52、(1)错(2)对(3)错(4)错(5)对(6)错3、D4、B5、C6、C7、(1)A B A D(2)装置Ⅰ中品红溶液褪色气体,以免干扰乙烯实验(3)除去SO2是否除尽(4)检查SO2(5)装置Ⅲ中的品红溶液不褪色,装置Ⅳ中的高锰酸钾酸性溶液褪色有机综合练习(标题设为黑体三号)(练习时间60分钟,满分100分)一、选择题(每小题5分,共60分。
每小题有1个选项符合题意)1.下列说法中的各项性质,属于CH4、C2H4、C2H2共性的是() A.常温常压下是无色无味气体 B.在通常状况下,密度比空气小C.能使酸性KMnO4溶液褪色 D.在一定条件下能发生加聚反应2.实现下列变化的有机反应的类型,不正确的是() A.CH3CH3―→CH3CH2Cl取代反应B.CH2=CH2―→CH2BrCH2Br加成反应C.CH2=CH2―→CH3CH2OH取代反应D. CH CH―→CHBr=CHBr加成反应3.下列对乙烯和聚乙烯的描述不正确的是() A.乙烯是纯净物,常温下为气态,聚乙烯为固态,是混合物B.乙烯比聚乙烯易发生氧化反应C.取等质量乙烯和聚乙烯完全燃烧后,生成的CO2和H2O的质量分别相等D. 取等物质的量的乙烯和聚乙烯,完全燃烧后生成的CO2和H2O的物质的量分别相等4.既可以用来鉴别乙烯和甲烷,又可用来除去甲烷中混有乙烯的方法是()A.通入足量的溴水B.与足量液溴反应反应C.在导管口点燃D.一定条件下与H25.质量相同的乙烯和一氧化碳具有相同的()A.物质的量B.原子个数C.体积和密度D.燃烧产物6. 由A、B两种烃组成的混合物,当混合物质量一定时,无论A、B以何种比例混合,完全燃烧消耗氧气的质量为一恒量。