驱动基因详解
- 格式:doc
- 大小:31.50 KB
- 文档页数:3

最新:晚期驱动基因阳性非小细胞肺癌免疫治疗专家共识(全文)一、EGFR突变EGFR基因突变是非鳞状NSC1C最常见的突变类型之一,EGFR突变阳性率在高加索人群中约为10%,在东亚人群中约为50%o对于伴有EGFR敏感突变的晚期NSC1C患者,一线标准治疗方案为EGFRTKIs,包括第一代EGFRTKIs(吉非替尼、厄洛替尼和埃克替尼\第二代EGFRTKIs(阿法替尼和达可替尼)和第三代EGFRTKIs(奥希替尼、阿美替尼和伏美替尼入研究证实,与传统化疗相比,EGFRTKIs显著改善了ORR和PFS o但随着治疗的推进,不可避免的面临耐药问题。
免疫治疗可以通过激活免疫系统发挥肿瘤杀伤作用,并可获得持续的疾病控制。
共识意见1不推荐ICIs用于晚期初治EGFR敏感突变NSC1C患者(推荐程度:一致不推荐IEGFR突变与肿瘤免疫原性低及非炎症性微环境有关,且早期临床研究表明,IQs单药或ICIs联合化疗治疗初治EGFR敏感突变患者疗效远不及标准EGFRTKIs靶向治疗,然而,在EGFRTKIs基础上联合ICIs的疗效提升有限,且存在较大安全性风险。
共识意见2推荐耐药的EGFR突变患者再次活检,同时检测肿瘤耐药基因和免疫微环境相关的生物标志物(推荐程度:一致推荐工基于EGFRTKIs治疗会影响肿瘤特征和及肿瘤微环境(TME),建议条件允许的情况下应再次活检,为后续精准治疗提供依据。
检测标本优选肿瘤组织,组织标本无法获得时可以采用其他类型标本替代;检测范围优选高通量检测以获得全面的耐药信息,包括肿瘤相关和免疫微环境相关的生物标志物。
共识意见3对于EGFRTKIs耐药后发生广泛进展的患者,且在缺乏有效靶向治疗的情况下,推荐使用ICIs(推荐程度:一致推荐\对于ICIS的方案选择,应结合患者的体能状态和疾病进展情况进行综合判断,其中IC1s+化疗+抗血管治疗方案的临床证据较为丰富(推荐程度:强推荐);IQs+含粕化疗方案在多项早期研究中均显示良好的治疗活性,且耐受性方面ICIs+含粕化疗方案较ICIs+含粕化疗+抗血管联合方案具有一定优势(推荐程度:强推荐);ICIs联合抗血管治疗(推荐程度:弱推荐)的证据主要针对多线耐药的患者或体力状况较差不耐受高强度治疗的患者,疗效获益有限。

肿瘤驱动基因的特征和功能研究肿瘤驱动基因是引发癌症的一类基因,它们可以在细胞内发挥重要的功能,促进癌症的发展和生长。
随着分子生物学的研究,我们已经了解了许多肿瘤驱动基因的特征和功能。
本文将探究肿瘤驱动基因的定义、特征及其功能,以期更好地理解肿瘤病理生理学。
1. 肿瘤驱动基因的定义肿瘤驱动基因,即促进细胞癌变和肿瘤形成的基因,这些基因有不同的作用,但它们的共同点是能够通过突变、拷贝数增加等方式对细胞的生长和分裂产生重要影响。
肿瘤驱动基因的存在是一个重要的发现,它引起了关于癌症起源和发展的许多理论。
2. 肿瘤驱动基因的特征肿瘤驱动基因的特征主要体现在以下几个方面:(1)拷贝数变异:肿瘤驱动基因的拷贝数改变可以是整倍体增加也可以是基因座突变。
这种变异可能唤起肿瘤形成。
(2)突变:某些突变会导致肿瘤抑制基因失去了正常功能,同时肿瘤驱动基因的突变往往会导致基因失去控制。
(3)化学修饰:一些化学修饰如DNA甲基化、羟甲基化等也可能影响肿瘤驱动基因的功能。
3. 肿瘤驱动基因的功能肿瘤驱动基因可以对细胞的正常生理功能产生影响,并促进癌症的发展。
其主要功能体现在三个方面:(1)参与细胞生长和分裂的调节:肿瘤驱动基因可以促进或抑制细胞的生长和分裂,这是它们的基本功能。
突变或拷贝数增加等变异可能导致基因失去对生长和分裂的正常调节作用,从而引起癌细胞的不受限制生长。
(2)细胞信号通路的激活:细胞通路是细胞间通信网络的重要组成部分,肿瘤驱动基因可以通过激活信号通路的某些分子来参与信号传递。
这些分子可能是细胞内的激活酶、受体或转录因子等,在突变时导致某些分子一直处于激活状态。
(3)参与细胞程序化死亡调节:细胞程序性死亡(apoptosis)是细胞生命周期的一个重要环节,避免细胞癌变的发生。
但在某些情况下,肿瘤驱动基因可以抑制细胞凋亡的发生,从而促进持续的生长。
这种抑制可能与直接抑制凋亡信号通路的分子有关,或者与促进细胞生长和分裂的信号通路紊乱有关。

驱动基因算法-概述说明以及解释1.引言1.1 概述概述部分的内容可以类似如下所示:概述:驱动基因算法是一种基于自然界进化理论和遗传学原理的优化算法。
它模拟了生物进化中的基因变异、选择和遗传传递的过程,通过对解空间中个体的适应度评估和优胜劣汰的操作,不断演化、优化搜索过程中的解策略。
相比于其他优化算法,驱动基因算法具有较强的全局搜索能力和较高的收敛速度。
在驱动基因算法中,通过定义适应度函数来度量每个个体与目标解的接近程度,进而决定个体的生存或淘汰。
同时,算法通过遗传操作(交叉、变异等)不断改变个体基因的组合,使得个体能在搜索空间中发现更优的解。
这种基于遗传变异和自然选择的进化模拟,使得驱动基因算法能够在复杂的优化问题中寻找到较优的解。
驱动基因算法广泛应用于各个领域,例如组合优化、图像处理、机器学习等。
其灵活的算法框架和自适应性能使其在实际问题中展现出很好的性能和应用前景。
同时,驱动基因算法也具有一定的局限性,比如对于高维、非线性、多模态的问题,算法的搜索性能可能较差。
此外,算法的参数设置和收敛性分析也是需要进一步研究和改进的方向。
本文将围绕着驱动基因算法的定义和原理、应用领域、优势与局限性以及未来发展方向展开深入探讨。
通过系统的整理和总结,我们将更好地理解驱动基因算法,并为其在实际问题中的应用提供一定的指导和借鉴。
接下来,我们将首先从驱动基因算法的定义和原理入手,为读者呈现一个全面的概览。
1.2 文章结构文章结构部分主要描述了本文的组织结构和内容安排。
本文按照以下几个章节展开讨论。
第一章是引言部分,包括概述、文章结构和目的。
在概述中,将简要介绍驱动基因算法的背景和意义。
文章结构部分将提供一个简要的概览,向读者展示本文的章节安排。
目的部分将说明本文撰写的目的和意图,明确阐述本文对驱动基因算法的研究和应用的贡献。
第二章是正文部分,主要探讨驱动基因算法的定义和原理,以及它的应用领域。
在2.1节中,将详细介绍驱动基因算法的定义和原理,包括算法的基本概念、工作原理和核心思想。

乳腺癌的基因组学和突变负荷乳腺癌是女性最常见的恶性肿瘤之一,也可发生在男性身上。
对于乳腺癌的研究和治疗,基因组学和突变负荷是两个重要的方面。
本文将探讨乳腺癌的基因组学研究以及突变负荷的意义。
一、乳腺癌的基因组学研究乳腺癌的基因组学研究旨在揭示肿瘤细胞的遗传背景以及肿瘤发展的分子机制。
通过对乳腺癌组织样本的基因测序和表达谱分析,可以找到与乳腺癌发生和发展相关的基因突变和基因表达异常。
这些基因的突变可以分为两类:驱动基因突变和副作用基因突变。
驱动基因突变是指那些直接推动癌症发展的突变,这些基因的突变会使肿瘤细胞获得增殖和转移的能力。
乳腺癌中最常见的驱动基因突变包括TP53、PIK3CA、PTEN和BRCA1/2等。
这些基因的突变与乳腺癌的病理特征和预后密切相关。
副作用基因突变是指那些在癌症发展中起到辅助作用的突变。
这些突变不直接推动癌症的发展,但是会增加癌症细胞在进化过程中的适应能力。
乳腺癌中常见的副作用基因突变包括CCND1、CDH1和MAPK等。
这些基因的突变会影响肿瘤的微环境以及治疗的反应性。
乳腺癌的基因组学研究为临床提供了诊断和治疗的新选择。
通过分析肿瘤细胞的基因突变情况,可以为患者提供个体化的治疗方案,包括靶向治疗和免疫疗法。
二、乳腺癌的突变负荷突变负荷是指肿瘤细胞在基因组水平上发生的突变数量和频率。
乳腺癌的突变负荷与肿瘤的遗传稳定性和免疫系统的活性密切相关。
高突变负荷的肿瘤通常具有更高的抗原负荷,即更多的新抗原表达,这使得肿瘤细胞更容易被免疫系统识别和攻击。
突变负荷的高低与肿瘤的治疗反应性和预后有密切关系。
高突变负荷的乳腺癌往往对免疫疗法的治疗反应更好。
通过抑制肿瘤细胞的逃逸机制,免疫疗法可以激活免疫系统对肿瘤的攻击,从而达到抑制肿瘤发展的效果。
因此,突变负荷的评估可以为临床提供指导,选择合适的治疗策略。
三、结论乳腺癌的基因组学和突变负荷对于研究乳腺癌的发病机制、诊断和治疗具有重要意义。


人类基因驱动技术的原理和应用前景随着科技的迅猛发展,人们对于基因科学的研究日益深入,而基因编辑技术作为其中的重要一环也逐渐受到广泛关注。
近年来,人类基因驱动技术作为一种崭新的基因编辑技术受到了越来越多的关注,其应用前景备受瞩目。
那么,什么是人类基因驱动技术?它的原理和应用前景是什么?一、人类基因驱动技术的原理人类基因驱动技术源于昆虫基因驱动技术。
昆虫基因驱动技术最早源于20世纪50年代,主要应用于虫类的控制。
20世纪80年代,科学家们开始研究昆虫基因驱动技术在哺乳动物身上的应用,但由于哺乳动物基因编辑技术的难度较大,一直没有取得明显的进展。
直到20世纪90年代末,科学家们发现了全新的基因驱动技术——CRISPR/Cas9,才使得人类基因驱动技术得以迎来发展的机遇。
CRISPR/Cas9是一种基因编辑技术,利用它可以在细胞内精确地修建、插入或删除基因。
人类基因驱动技术利用CRISPR/Cas9的原理,将一种自然存在的基因驱动系统——基因驱动元件(Gene drive)与之结合,形成一种全新的基因编辑技术。
基因驱动元件是一种特殊的DNA序列,可以通过基因编辑技术被嵌入到受控动物或植物的基因组中,从而实现对该物种的基因传递方式进行控制。
其中,基因驱动元件的特殊性在于:在杂合状态下,它能够被强制“遗传到”下一代子孙中的每一个个体,从而最终影响到物种整个种群的基因传递方式。
二、人类基因驱动技术的应用前景目前,人类基因驱动技术在科学界已经备受关注,主要有以下几个方面的应用前景:1. 疾病控制人类基因驱动技术可以被用来控制某些疾病的传播。
例如,可以使用人类基因驱动技术来控制某些病毒或病菌在蚊子等害虫群体中的传播。
这种应用前景相当广阔,可望为人们减轻某些疾病的压力和痛苦。
2. 美化城市环境城市环境中的生物多样性一直受到人类活动的干扰。
人类基因驱动技术可以通过控制害虫或者有害植物的繁殖和生长来优化城市环境,使城市更加安全、宜居。
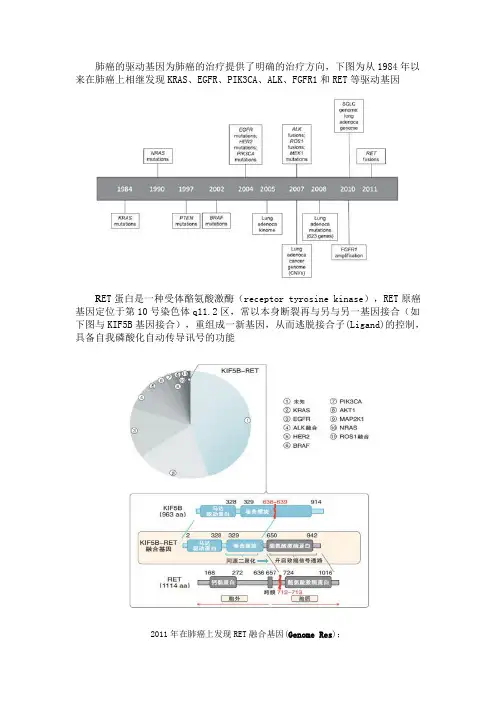
肺癌的驱动基因为肺癌的治疗提供了明确的治疗方向,下图为从1984年以来在肺癌上相继发现KRAS、EGFR、PIK3CA、ALK、FGFR1和RET等驱动基因R ET蛋白是一种受体酪氨酸激酶(receptor tyrosine kinase),RET原癌基因定位于第10号染色体q11.2区,常以本身断裂再与另与另一基因接合(如下图与KIF5B基因接合),重组成一新基因,从而逃脱接合子(Ligand)的控制,具备自我磷酸化自动传导讯号的功能2011年在肺癌上发现RET融合基因(Genome Res);2012年初,Dana-Farber等癌症中心,在24位NSCLC上发现1例RET融合基因,扩大到561位肺腺癌上后,又发现11位RET融合基因(2%),(Nature medicine);2012年初,日本学者在319为肺腺癌上发现9位发生RET融合基因(2.8%),并且发现含该驱动基因的肺癌细胞可被vandetanib抑制,(Nature medicine);2012年初,日本学者在1529例肺癌患者上发现44例ALK融合基因,14例RET融合基因,13例ROS1融合基因,共71例(均为肺腺癌),(Nature medicine);2012年11月,中国学者在936位发现13位RET融合基因,11位为肺腺癌,2位为腺鳞癌(JCO)。
2012年7月,斯隆凯瑟琳癌症中心,启动II期临床试验:Cabozantinib in Patients With KIF5B/RET Positive Advanced NSCLC。
Cabozantinib可同时 MET, VEGFR, and RET。
一些医学平台目前已开展临床认可的ALK、ROS1等融合基因商业化检测(FISH方法);一些EGFR突变阴性的晚期NSCLC患者,在化疗耐药或耐受不了化疗时,可根据ALK或ROS1融合基因的结果选择Crizotinib药物治疗;相信不久的未来,将有更多的驱动基因被发现后相应的药物也会随即得到FDA的批准,如RET融合基因和Cabozantinib。

非小细胞肺癌驱动基因在最新一期的《Cancer cell》杂志上来自麻省总医院的Rebecca S. Heist 和Jeffrey A. Engelman发表了一篇题为“SnapShot: Non-Small Cell Lung Cancer”的文章。
文章以概略图加上主题内容简介及推荐了10篇文献,简明扼要地归纳了非小细胞性肺癌(NSCLC)当前临床前景、肺癌的体细胞“驱动”基因突变图谱,为广大研究人员提供了重要的资料。
通过开发靶向癌症特异基因突变的药物,近年来非小细胞肺癌(NSCLC)的诊断和治疗发生了重大的变革。
对肺癌活检组织的体细胞突变常规基因测试正成为提供最佳患者医疗护理的标准。
确定特异的突变例如EGFR和ALK为使用FDA批准的靶向治疗提供指导,有可能使临床获益。
发现其他的基因突变也可以引导患者和医生往新靶向药物的临床试验做出努力。
许多目前还正在开发当中的治疗方案主要是靶向激活的受体酪氨酸激酶(PTKs)或相关下游信号通路,尤其是RAS-RAF-MAPK和PI3K-AKT信号通路。
还有大量的临床试验目前正在开展,评估包含特异突变的癌症最佳特异靶向信号通路(单独或联合)。
NSCLC驱动基因:EGFR活化EGFR突变位于酪氨酸激酶域,可导致组成性的EGFR信号。
EGFR突变激活的PI3K-AKT 和RAS-MEK-ERK信号对癌细胞的生长、生存和迁移起至关重要的作用。
最常见的激活突变是19号外显子的框内缺失(in-frame deletion)同突变和858密码子的一个错义突变(导致精氨酸被亮氨酸取代,L858R)。
带有EGFR突变的肺癌EGFR酪氨酸激酶抑制剂(TKIs)高度敏感。
当前,EGFR突变的基因型筛查常被用于筛选患有IV期NSCLC、一线治疗方案为接受EGFR—TKIs治疗的患者。
目前的研究重点集中在延长反应持续时间,找到有效的途径靶向在疾病进程中形成的耐药机制。
最常见的耐药机制就是EGFR T790M突变,存在约50%的耐药肿瘤中。

驱动基因型
基因是生命的基础,它决定了我们的身体构造、性格特点、智力水
平等方面。
而基因型则是指一个人所拥有的全部基因的组合。
基因型
的不同,决定了人们在生理、心理、行为等方面的差异。
而驱动基因
型则是指通过一定的方式,来影响和改变基因型,从而达到某种目的
的行为。
驱动基因型的方式有很多种,下面我们将按照类别进行介绍。
1. 饮食类
饮食是影响基因型的重要因素之一。
科学研究表明,一些食物中含有
的营养物质可以影响基因的表达,从而改变基因型。
例如,富含维生
素C的食物可以促进基因的修复和更新,从而延缓衰老;而富含蛋白
质的食物则可以促进肌肉生长,改善身体素质。
2. 运动类
运动是另一个可以影响基因型的重要因素。
适当的运动可以促进基因
的表达,从而改变基因型。
例如,有氧运动可以促进心肺功能的提高,增强身体的耐力和抵抗力;而力量训练则可以促进肌肉生长,改善身
体素质。
3. 心理类
心理因素也可以影响基因型。
例如,压力和焦虑会导致基因的表达发生变化,从而影响身体的健康;而积极的心态和乐观的情绪则可以促进基因的表达,从而改善身体的健康。
4. 环境类
环境因素也可以影响基因型。
例如,空气污染、辐射等环境污染物会导致基因的突变,从而影响身体的健康;而良好的环境则可以促进基因的表达,从而改善身体的健康。
总之,驱动基因型是一种可以通过改变生活方式和环境来影响基因型的行为。
通过科学的饮食、适当的运动、积极的心态和良好的环境,我们可以改变自己的基因型,从而达到健康、长寿、美丽等目的。


驱动基因阳性非小细胞肺癌脑转移的个体化综合治疗王克万;杨开军;欧阳辉;龙浩;钱大棣;王洪筱;漆松涛【摘要】驱动基因阳性的非小细胞肺癌(NSCLC)脑转移的治疗已取得很大进展, 随着分子生物学技术的进步, NSCLC新的基因突变位点不断被发现, 新一代靶向药物研发及临床应用速度加快, 并取得显著疗效.目前采用EGFR-TKI及ALK抑制剂靶向药物一线治疗驱动基因阳性NSCLC脑转移已形成共识, 但是一线靶向药物获得性耐药和治疗后进展仍是临床面临的主要问题.脑脊液的液体活检可对脑转移瘤基因异质性及突变进行监测.靶向药物治疗联合放射治疗可使患者最大获益, 尤其是立体定向放射治疗联合靶向药物治疗, 可显著增加NSCLC脑转移颅内缓解率, 无进展生存期及总生存期显著增加, 值得进一步进行临床随机对照研究.【期刊名称】《广东医学》【年(卷),期】2019(040)001【总页数】5页(P41-45)【关键词】驱动基因阳性;非小细胞肺癌;脑转移;靶向治疗;放射治疗【作者】王克万;杨开军;欧阳辉;龙浩;钱大棣;王洪筱;漆松涛【作者单位】南方医科大学南方医院神经外科, 广东广州 510515;南方医科大学南方医院神经外科, 广东广州 510515;南方医科大学南方医院神经外科, 广东广州510515;南方医科大学南方医院神经外科, 广东广州 510515;南方医科大学南方医院神经外科, 广东广州 510515;南方医科大学南方医院神经外科, 广东广州 510515;南方医科大学南方医院神经外科, 广东广州 510515【正文语种】中文【中图分类】R739.41原发性肺癌是我国发病率及病死率最高的恶性肿瘤[1]。
近年来,随着基因突变检测进展及相应靶向药物的研发,肺癌患者生存期明显延长,在疾病进程中30%~50%肺癌患者出现脑部转移[2],10%~15%的肺癌患者初诊时即伴有脑转移。
脑转移瘤患者常伴有严重神经功能障碍,生活质量显著降低,未经治疗平均生存期仅2个月左右。
基因驱动的概念基因驱动是指通过干预特定基因的功能或表达来驱动遗传物质在种群中的传播。
它是一项新兴的基因技术,可以被用来改变或控制一种生物种群的遗传特征。
基因驱动技术可以用于传统农业、人类健康、生态保护以及控制害虫和传染病等多个领域。
基因驱动的核心原理是利用基因编辑工具,如CRISPR-Cas9,去修改生物个体的遗传信息,使其在繁殖中对后代产生影响,进而快速扩散和固定特定基因。
这种驱动效应可以通过几种方式产生:一是通过引入一种新的遗传修复机制,例如选择性杀死不持有驱动基因的个体;二是通过引入压制自然选择的功能,如性选择;三是通过增加基因的拷贝数来增加驱动的效率。
基因驱动技术的潜在应用非常广泛。
在农业领域,基因驱动可以用于改良作物的遗传特性,如使作物对抗虫害和病害的能力增强,提高产量和耐受性。
在人类健康领域,基因驱动可以用于治疗遗传疾病,如通过修复有缺陷的基因来治疗遗传性肿瘤和单基因病。
在生态保护领域,基因驱动可以用于恢复濒危物种的数量,如通过驱动传染病抵抗基因传播到濒危物种中,以提高其生存能力。
此外,基因驱动还可用于控制害虫和传染病的传播,从而减少对农作物和人类健康的危害。
虽然基因驱动技术有巨大的潜力,但也存在一些潜在的风险和挑战。
首先,基因驱动技术的安全性和效果需要进行严格的评估和监管,以确保其对环境和生态系统的潜在影响最小化。
其次,基因驱动可能引发道德、社会和法律问题,如物种改变的风险、人类干预自然生态系统的争议等。
此外,技术的可逆性也是一个重要问题,一旦基因驱动释放到环境中,是否能够控制其传播和影响是需要深入研究的。
总的来说,基因驱动是一项有巨大潜力的基因技术,它可以用于改良作物、治疗遗传疾病、恢复物种数量以及控制害虫和传染病等领域。
然而,对于基因驱动的研究和应用需要充分考虑风险和挑战,并制定相应的监管和伦理标准,以确保其安全性和可持续性。
未来,随着技术的进一步发展和研究的深入,基因驱动将在各个领域发挥重要作用,为人类带来更大的福祉。
基因驱动基因适应序列依赖属性讨论深层揭示在过去的几十年里,基因编辑技术已经取得了巨大的突破,为人类治疗疾病、改善农作物等方面带来了巨大的潜力。
然而,近年来又出现了一种相对新颖的基因编辑技术,即基因驱动(gene drive)。
基因驱动技术具有潜在的广泛应用领域,可以彻底改变自然界和人类社会的生态系统。
基因驱动是一种具有自我复制功能的基因,可以通过转录自身并将自己复制到其他染色体上,以实现在物种中快速传播和扩散的目的。
这使得基因驱动成为一种强有力的工具,可以促使特定基因在整个物种中迅速传播,而不仅仅是在一代中传递。
基因驱动技术的一个重要应用是控制疾病传播媒介,如蚊子和啮齿动物。
例如,通过将一种抗病毒基因驱动到蚊子的基因组中,可以有效控制蚊子传播疟疾的能力。
这种应用有望大幅度降低疟疾在全球的传播,对全球公共卫生具有重要意义。
另一个潜在的应用领域是农业。
基因驱动技术可以被用来改变农作物的性状,提高产量和抗病性。
例如,通过驱动一种特定基因到作物中,可以使其抵抗特定的病原体,减少病害的发生,提高作物的生长和产量。
然而,基因驱动技术也存在一些潜在的风险和问题,需要深入讨论和研究。
首先,基因驱动技术的广泛应用可能会导致生态系统的不可逆转变。
由于基因驱动具有高效的传播能力,一旦在自然环境中释放,可能导致潜在的生态灾难。
因此,在使用基因驱动技术之前,必须进行充分的风险评估和适应性研究。
其次,基因驱动技术引发了伦理和道德的争议。
对于一些人来说,修改自然界的基因组可能会被视为干涉自然选择的过程。
此外,还存在着对基因驱动技术可能在物种中强制传播的影响的担忧。
这些担忧需要考虑并解决,以确保基因驱动技术的可行性和安全性。
基于上述问题,科学界和政府机构已经开始呼吁对基因驱动技术进行严格的监管和监控。
需要建立相关的法律法规和政策框架,确保基因驱动技术在合适的条件下进行,同时保护生态系统和人类社会的利益。
此外,基因驱动技术的发展和应用还需要更多的研究来解决技术本身的局限性。
驱动基因和乘客基因一、什么是基因?基因是生物体内的遗传物质,可以决定生物的性状和特征。
它们是由DNA分子编码的,可以传递给后代,影响他们的表现形式。
二、驱动基因和乘客基因1.驱动基因驱动基因是一类具有特殊功能和重要表达的基因,它们对生物体的生存、繁殖和适应环境等方面起着关键作用。
驱动基因负责控制和调节其他基因的表达,决定了生物体的发育过程和个体特征。
驱动基因具有高度保守性和稳定性,它们在进化过程中很少发生变异。
驱动基因可以通过突变和基因重组来产生新的表达方式,进而推动物种的进化。
2.乘客基因乘客基因是相对于驱动基因而言的。
它们是在基因组中存在,但对生物体的生存和适应性没有直接影响的基因。
乘客基因不会独立地实现某个重要的功能,它们在基因组中的存在可能是因为基因组重组、基因复制、转座子等过程的结果。
乘客基因在进化过程中可能会发生变异和丢失,因为它们对生物个体的生存和繁殖没有显著影响。
然而,乘客基因在基因组中的存在可能对其他基因的表达产生间接的影响。
三、驱动基因的重要性1.驱动物种进化驱动基因是物种进化的推动力,它们通过控制和调节其他基因的表达,决定了物种的适应性和生存能力。
驱动基因的重要改变可以导致物种的分化和新的适应策略的产生。
2.驱动个体发育驱动基因在个体发育过程中起着重要作用,它们控制和调节细胞分化、器官发育和身体形态等方面。
驱动基因的表达异常或突变可以导致个体发育异常和功能缺陷。
3.驱动基因治疗驱动基因的突变和异常表达与许多遗传性疾病和肿瘤的发生有关。
通过对驱动基因进行研究,可以发现并开发新的治疗方法、药物和基因治疗技术。
四、乘客基因的潜力1.功能转化乘客基因在进化过程中可能会发生功能转化,即原本无功能的基因在一些特定环境下获得了新的功能。
这些乘客基因的功能转化对物种的进化和适应性产生了重要影响。
2.调控基因表达乘客基因虽然不直接参与物种适应环境的过程,但它们在基因组中的存在可能通过调控其他基因的表达,间接影响生物体的表型。
癌细胞十周年特刊快照:非小细胞肺癌来源: 作者:admin非小细胞肺癌易瑞沙21世纪肺癌治疗新方中医如何治疗非小细肺癌转移怎么治疗?影响肺癌早期治愈率肺癌晚期骨转移吃瑶早期小细胞肺癌怎样肿瘤医乱没无“单方晚期肺癌如何提高生小细胞肺癌的早期症什么是非小细胞肺癌印刷非法刊物药品国际抗癌联盟公布:专家告诉您:肺癌脑CLS自体细胞治疗小在最新一期(3月20日)的《癌细胞》(Cancercell)上来自麻省总医院的RebeccaS.Heist 和JeffreyA.Engelman发表了一篇题为“SnapShot:Non-SmallCellLungCancer”的文章。
文章以概略图加上主题内容简介及推荐了10篇文献,简明扼要地归纳了非小细胞性肺癌(NSCLC)当前临床前景、肺癌的体细胞“驱动”基因突变图谱,为广大研究人员提供了重要的资料。
FGFR1是一个潜在的肺鳞状上皮细胞癌靶标。
FGFR1是RTKs家族FGFR。
FGFR1激活可导致通过PI3K-AKT和RAS-MEK-MAPK的下游信号。
在大约20%的鳞状细胞癌中发现有FGFR1扩增。
在实验室研究中,包含FGFR1的癌细胞系和小鼠模型中的FGFR1可导致生长和凋亡。
多种FGFR剂正在临床研发阶段,其中许多剂除了FGFR1还可多种酪氨酸激酶。
在1.5%的肺腺癌中存在有包含ROS1基因的染色体重排。
与ALK阳性癌症相似,ROS1阳性癌症患者往往都比较年轻,无吸烟史,并患有腺癌。
包含ROS1易位的癌症患者对于crizotinib的反应已经获得确定。
当前针对转移性的活IV期肺癌的靶向治疗正在研发当中。
对转移性肺癌,通常不主张手术和放射治疗,而主要采用治疗。
因为这些新型药物在用于治疗带有基因突变的癌症时显示了对转移性癌症的前景,今后的研究方向可能包括实施这些策略,辅助治疗以提高患者的治愈率。
对于ALK剂crizotinib的大型I期研究在包含ALK易位的癌症患者中整体反应率为57%,疾病控制率为90%,由此获得了FDA的批准。
基因驱动进化基因驱动是一种科学家们利用基因工程技术来改变物种的传递基因的方法。
这种技术的应用给生物学研究和资源保护带来了新的突破。
基因驱动进化是指通过这种技术所引发的物种进化过程。
本文将探讨基因驱动进化的原理、应用及其对生态系统的影响。
一、基因驱动进化的原理基因驱动进化是通过改变生物个体的遗传信息,使其在繁殖过程中具有更高的遗传优势,从而传递给下一代的一种方法。
其原理是通过人为设计的基因改造技术,使得改造后的基因在自然繁殖中能够更快速地传递并取代自然种群中的野生型基因。
这种传递方式不依赖于自然选择,而是通过技术手段直接改变物种的遗传构成。
二、基因驱动进化的应用1. 病虫害防治基因驱动进化可用于病虫害的生物防治。
通过将含有具有特定抗虫抗病基因的驱动基因导入特定物种中,可以使得这些物种在繁殖过程中将抗虫抗病基因传递给后代,从而实现对病虫害的防治目的。
2. 物种保护与恢复一些濒危物种的保护与恢复常常面临遗传多样性不足的问题。
基因驱动进化可以通过引入更多的遗传信息来增强物种的适应性和生存能力,从而促进物种的保护与恢复。
3. 农业生产基因驱动技术可以用于改良农作物,提高其产量和抗逆性。
通过引入具有高产量或抗逆性的基因,可以使得农作物在繁殖过程中快速遗传这些有益基因,从而提高农作物的经济产量和质量。
三、基因驱动进化对生态系统的影响虽然基因驱动进化在许多方面都有着积极的应用潜力,但是其对生态系统的影响也不能忽视。
由于基因驱动进化可以改变物种的遗传构成,可能导致基因污染或遗传多样性的丧失。
此外,在引入驱动基因的过程中,也需要注意对于非目标物种的影响评估,防止引发意想不到的生态效应。
四、基因驱动进化技术的挑战和展望基因驱动进化技术的开发和应用还面临着许多技术和伦理上的挑战。
技术上,如何确保驱动基因的稳定性和有效性,以及防止其在目标物种以外的物种中传播,都是需要解决的问题。
伦理上,如何平衡科学家的责任与对生物多样性和生态系统的尊重也是一个需要深入讨论的问题。
mf 驱动基因MF驱动基因(MF Driver Gene)我还记得那个晴朗的早晨,当我第一次听说MF驱动基因的时候,我的内心充满了无尽的好奇和兴奋。
这个被誉为基因科学的突破,让我对未来的世界充满了无限的遐想。
MF驱动基因是一种新型的基因技术,它被用来改变人类身体的特征和能力。
通过操控基因序列,科学家们可以为人类注入各种超凡的能力,如超强的力量、超快的反应速度以及超强的智力。
这种基因技术的问世,无疑让人类迈入了一个新的时代。
在MF驱动基因的研究中,科学家们首先通过大量的实验和数据分析,确定了一系列与特殊能力相关的基因。
这些基因被称为MF基因,它们是人类基因组中的一部分,但却具有特殊的功能。
通过激活这些MF基因,科学家们可以让人类具备超越常人的能力。
然而,MF驱动基因并非一蹴而就的技术。
在研究的过程中,科学家们要面对无数的困难和挑战。
他们需要克服基因序列的复杂性,解决基因操控的精确性和安全性等问题。
更重要的是,科学家们还需要细致地考虑伦理和道德的问题,确保这项技术的安全和合法。
尽管MF驱动基因有着巨大的潜力,但我们必须谨慎对待。
这项技术的应用必须建立在科学、伦理和法律的基础之上。
我们不能为了个人的私利而滥用这项技术,更不能让它成为分裂社会的工具。
我们应该将其用于造福人类,推动社会的进步和发展。
在未来的世界中,MF驱动基因可能会成为人类生活的常态。
但我们不能忘记,人类的特殊能力并不仅仅是靠基因来决定的。
我们每个人都有潜力成为更好的自己,而不仅仅是依赖基因的改造。
我们应该努力发掘自身的潜力,并用智慧和勤奋去追求自己的梦想和目标。
MF驱动基因是人类科技发展的产物,它为我们带来了无限的可能。
但我们不能忽视人类的内心世界和情感需求。
无论我们拥有多强大的能力,我们都需要保持对人类情感的关怀和理解。
只有这样,我们才能真正实现人类的进步和发展。
MF驱动基因,是一个令人兴奋又充满挑战的领域。
在未来的岁月里,我相信科学家们会继续努力,将这项技术推向更高的层次。
癌细胞十周年特刊快照:非小细胞肺癌来源: 作者:admin非小细胞肺癌易瑞沙21世纪肺癌治疗新方中医如何治疗非小细肺癌转移怎么治疗?影响肺癌早期治愈率肺癌晚期骨转移吃瑶早期小细胞肺癌怎样肿瘤医乱没无“单方晚期肺癌如何提高生小细胞肺癌的早期症什么是非小细胞肺癌印刷非法刊物药品国际抗癌联盟公布:专家告诉您:肺癌脑CLS自体细胞治疗小
在最新一期(3月20日)的《癌细胞》(Cancercell)上来自麻省总医院的RebeccaS.Heist 和JeffreyA.Engelman发表了一篇题为“SnapShot:Non-SmallCellLungCancer”的文章。
文章以概略图加上主题内容简介及推荐了10篇文献,简明扼要地归纳了非小细胞性肺癌(NSCLC)当前临床前景、肺癌的体细胞“驱动”基因突变图谱,为广大研究人员提供了重要的资料。
FGFR1是一个潜在的肺鳞状上皮细胞癌靶标。
FGFR1是RTKs家族FGFR。
FGFR1激活可导致通过PI3K-AKT和RAS-MEK-MAPK的下游信号。
在大约20%的鳞状细胞癌中发现有FGFR1扩增。
在实验室研究中,包含FGFR1的癌细胞系和小鼠模型中的FGFR1可导致生长和凋亡。
多种FGFR剂正在临床研发阶段,其中许多剂除了FGFR1还可多种酪氨酸激酶。
在1.5%的肺腺癌中存在有包含ROS1基因的染色体重排。
与ALK阳性癌症相似,ROS1阳性癌症患者往往都比较年轻,无吸烟史,并患有腺癌。
包含ROS1易位的癌症患者对于crizotinib的反应已经获得确定。
当前针对转移性的活IV期肺癌的靶向治疗正在研发当中。
对转移性肺癌,通常不主张手术和放射治疗,而主要采用治疗。
因为这些新型药物在用于治疗带有基因突变的癌症时显示了对转移性癌症的前景,今后的研究方向可能包括实施这些策略,辅助治疗以提高患者的治愈率。
对于ALK剂crizotinib的大型I期研究在包含ALK易位的癌症患者中整体反应率为57%,疾病控制率为90%,由此获得了FDA的批准。
更有效的ALK剂和靶向获得性耐药的策略目前还正在研发当中。
肿瘤基因PTEN编码的脂质磷酸酯酶对PI3K-AKT信号起负调控作用,PTEN可导致组成性PI3K-AKT信号。
PTEN在大量癌症中可通过多种机制失活。
相比于腺癌,PTEN在鳞状细胞癌中更常见。
癌细胞》十周年特刊快照:非小细胞肺癌临床试验正在评估PI3K剂在PTEN缺失癌症中的效应。
小细胞肺癌能活多久在肺鳞状细胞癌中发现有PDGFRA的扩增。
通过shRNA敲除或小PDGFRA可损害细胞存活和贴壁非依赖性的生长,表明PDGFRA可能是带有PDGFRA扩增的癌症的一种驱动癌基因。
多种PDGFR剂目前在临床开发中。
与FGFR1剂相似,大量的药物都能多种激酶。
PIK3CA突变集中在两个热区,第9号和20号外显子,分别编码蛋白的螺旋域和激酶域。
这些突变导致了脂质激酶活性增强,以及组成性的PI3K-AKT信号通。
目前有多个PI3K 剂正在研发中,其范围涵盖双PI3K/MTOR,泛PI3K以及亚型选择性PI3K剂。
临床前数据表明包含PIK3CA激活突变的癌症对单剂PI3K信号剂最,目前正在肺癌中开展临床试验验
证这一推测。
许多目前还正在开发当中的治疗方案主要是靶向激活的受体酪氨酸激酶(PTKs)或相关下游信号通,尤其是RAS-RAF-MAPK和PI3K-AKT信号通。
在这篇文章中附列的信号通图解汇集了当前NSCLC中的靶向蛋白,所附图表列出了已获FDA批准或正在积极开发的靶向治疗方案。
还有大量的临床试验目前正在开展,评估包含突变的癌症最佳靶向信号通(单独或联合)。
文献全文下载
活化EGFR突变位于酪氨酸激酶域,可导致组成性的EGFR信号。
EGFR突变激活的PI3K-AKT和RAS-MEK-ERK信号对癌细胞的生长、和迁移起至关重要的作用。
最常见的激活突变是19号外显子的框内缺失(in-framedeletion)同突变和858密码子的一个错义突变(导致精氨酸被亮氨酸取代,L858R)。
带有EGFR突变的肺癌EGFR酪氨酸激酶剂(TKIs)高度。
当前,EGFR突变的基因型筛查常被用于筛选患有IV期NSCLC、一线治疗方案为接受EGFRTKIs治疗的患者。
目前的研究重点集中在延长反应持续时间,找到有效的途径靶向在疾病进程中形成的耐药机制。
最常见的耐药机制就是EGFRT790M突变,存在约50%的耐药肿瘤中。
此外还有一些其他的例如MET扩增,PIK3CA突变以及向SCLC也曾得到描述。
通过开发靶向癌症基因突变的药物,近年来非小细胞肺癌(NSCLC)的诊断和治疗发生了重大的变革。
对肺癌活检组织的体细胞突变常规基因测试正成为提供最佳患者医疗护理的标准。
确定的突变例如EGFR和ALK为使用FDA批准的靶向治疗提供指导,有可能使临床获益。
发现其他的基因突变也可以引导患者和医生朝新靶向药物的临床试验做出努力。
DDR2是一种可与胶原蛋白结合的受体酪氨酸激酶(PTK),可促进细胞迁移、增殖和存活。
DDR2突变存在于肺鳞状细胞癌和细胞系中。
在DDR2突变细胞系中,DDR2活性可导致增殖。
异位表达突变DDR2可导致细胞,而不同的突变导致的水平有所差异。
这些结果表明DDR2突变可能是致癌性的,带有这些突变的癌症可能会对DDR2激酶剂。
KRAS是肺癌中一种最常见的突变基因,发生在大约25%的腺癌细胞》十周年特刊快照:非小细胞肺癌癌中。
肺癌KRAS突变主要定位在第12和13号密码子。
肺癌中的KRAS突变似乎与EGFR和ALK易位互不相容,而患者通常都有吸烟史。
KRAS突变通常耐受EGFRTKI治疗。
尽管目前尚没有直接靶向突变KRAS的药物得到开发,利用更新的靶向治疗联合化疗,或联合PI3K及MEK等其他靶向治疗的策略现在正在临床研发中。
BRAF突变存在于1%–3%的非小细胞肺癌中。
V600E是最常见的突变,在肺癌中也有多种其他类型的BRAF突变被报道,包括G469A和D594G。
尽管性药物例如vemurafenib 在包含BRAFV600E突变的黑色素瘤中高度有效,但这些药物在BRAF突变肺癌中的活性还需评估。
多项评估BRAF和MEK剂活性的试验正在BRAF突变的癌症中开展。
2号染色体的倒位导致生成了EML4-ALK融合基因,其编码的融合蛋白形成非配体依赖性二聚体引起组成性的ALK激活。
ALK信号可通过激活RAS-MEK-ERK,JAK3-STAT3和PI3K-AKT信号通导致细胞增殖和生成。
在NSCLC中ALK易位与腺癌组织学、印戒细
胞形态学、年轻患者及非吸烟史相关。
今年是《癌细胞》创刊10周年,最新一期(3月20日)为纪念这一重要时刻,特免费。
这一期《癌细胞》包含有三篇综述,四篇评论性文章,八篇研究进展,以及一篇快照文章,其中综述文章主要聚焦于癌症干细胞、代谢以及微。
文章来自:/html/xiaoxibaofeiai/20120401/67129.html。