铅的测定法
- 格式:doc
- 大小:38.56 KB
- 文档页数:4

实验八食品中铅的测定(火焰原子吸收法)(-)目的意义通过本方法的学习掌握该测定方法的原理、步骤并根据测定结果判定受检样品是否符合国家规定的卫生标准。
(二)原理样品经过处理后,导人原子吸收分光光度计中,经原子化以后,吸收283.3nm 共振线,其吸收量与铅量成正比,可与标准系列比较定量。
(三)仪器与试剂1.原子吸收分光光度计2.硝酸,过硫酸铵,石油醚。
3.6N硝酸量取38ml硝酸,加水稀释至100ml。
4.0.5%硝酸量取lml硝酸,加水稀释至200ml。
5.10%硝酸量取10.0ml硝酸,加水稀释至100ml。
6.0.5%硫酸钠称0.5g无水硫酸钠,加水至100m1溶解。
7.铅标准溶液准确称取1.000g金属铅(99.99%),分次加入6N硝酸溶解,总量不超过37ml,移入1000ml容量瓶中加水稀释至刻度。
此溶液每毫升相当于1mg铅。
8.铅标准使用液吸取10.0ml铅标准溶液,置于100ml容量瓶中,加0.5%硝酸稀释至刻度,如此多次稀释至每毫升相当于ug铅。
(四)操作步骤1.样品处理下述样品可以根据仪器灵敏度增减样品量。
(1)谷类:除去外壳,磨碎,过20目筛,混匀。
称取1.0~5.0g样品,置于石英或瓷坩埚中,加5ml硝酸,放置0.5h,小火蒸干,继续加热炭化,移入高温炉中,500℃灰化1h,取出放冷,再加lml硝酸浸湿灰分,小火蒸干。
称取2g 过硫酸铵,覆盖灰分,再移入高温炉中,800℃灰化20min,冷却后取出,以0.5%硝酸溶液少量多次洗入10m1容量瓶中,稀释至刻度,备用。
取与消化样品相同量的硝酸、过硫酸铵,按同一方法做试剂空白试验。
(2)水产类:取可食部分捣成匀浆。
称取 1.0~5.0g,以下按(1)自“置于石英或瓷坩祸中”起依法操作。
(3)乳、炼乳、乳粉、茶、咖啡:称取2g混匀或磨碎样品,置于瓷坩埚中,加热炭化后,置高温炉,420℃灰化3h,放冷后加水少许,稍加热,然后加lml l:1硝酸,加热溶解后,移人10ml容量瓶中,加水稀释至刻度,备用。

书山有路勤为径,学海无涯苦作舟EDTA 滴定法测定铅一、方法提要试样用酸分解,在酸性介质中,pb2+与so42-作用生成pbso4 沉淀与其他元素分离.再在ph5~6 白勺hac-naac 缓冲溶液中,将pbso4 转化成pb(ac)2。
以二甲酚橙为指示剂,用edta 标准溶液滴定。
sb、bi 含量较高时,易水解并夹杂于pbso4 沉淀中,可加入酒石酸络合以消除干扰,ba 大于10mg,由于生成复盐pbso4-bas04 沉淀,使pb 结果偏低。
本法适用于一般矿石中w(pb)/10-21 白勺测定。
二、试剂配制乙酸-乙酸钠缓冲溶液(ph5~6):称取200gch3coona-3h2o 溶于水,加10ml 冰乙醇,用水稀释至1000ml,混匀。
铅标准溶液:称取1.0000g 金属铅(99.99%)于20ml 烧杯中,加入20mlhno3(1+1),低温溶解,冷后移入1000ml 容量瓶中,用水稀释至刻度,混匀。
edta 标准液:c(c10h14n2o8na2-2h2o)=0.015mol/l。
称取5.60gedta 二钠盐溶于水,移至1000ml 容量瓶中,用水稀释至刻度,混匀。
标定如下:吸取含25mgpb 白勺标准溶液于250ml 烧杯中,加25~30mlhac-naac 缓冲溶液,用水稀释至70~80ml,加3 滴5g/l 二甲酚橙指示剂,用edta 标准溶液滴定至亮黄色为终点。
按通则中式(11)计算edta 标准溶液对pb 白勺ft 值。
三、分析步骤称取0.1~0.5g(精确至0.000lg)试样于250ml 烧杯中,用水润湿,加入15mlhcl,盖上表皿,加热溶解5~6min 后,加入5mlhno3,继续加热至试样完全分解,加20mlh2so4(1+1),加热至冒浓厚so3 白烟,取下,冷却,用水洗涤表皿及杯壁后再加热至冒烟,取下冷却。
加入50ml 水,搅匀(试样中含sb、bi 时,5ml200g/l 酒石酸溶液),加热煮沸5~1omin 使可溶盐溶解,流水冷却4h(若加入10ml 乙醇只需流水冷却2h,铅含量低时须放置过夜),以定量慢速滤纸过滤,以h2so4(5+95)洗至无fe3+(以kscn 溶液检查).再将沉淀和滤纸放回原烧杯中,加入25~30mlhac-naac 缓冲溶液和25ml 水(铅量高可再多加10ml 缓冲溶液),。

食品中铅的测定方法原理试样经灰化或酸消解后,注入原子吸收分光光度计石墨炉中,电热原子化后吸收共振线,在一定浓度范围,其吸收值与铅含量成正比,与标准系列比较定量;试剂硝酸:优级纯;高氯酸:优级纯;硝酸L:取硝酸加入50ml水中,稀释至100ml;硝酸1mol/L:取硝酸加入50ml水中,稀释至100ml;磷酸二氢铵溶液20g/L:称取磷酸二氢铵,以水溶解稀释至100ml;混合酸:硝酸+高氯酸4+1;取4份硝酸与1份高氯酸混合;铅标准储备液:由国家标准物质研究中心提供;铅标准使用液:每次吸取铅标准储备液于100ml容量瓶中,加硝酸L或硝酸1mol/L至刻度;如此经多次稀释成每毫升含,,,,铅的标准使用液可根据样品所含浓度进行配制;仪器所用玻璃仪器均需以硝酸1+5浸泡过液,用水反复冲洗,最后用去离子水冲洗干净;原子吸收分光光度计附石墨炉及铅空心阴极灯;消化装置可调式电热饭、可调式电炉;操作试样预处理在采样和制备过程中,应注意不使试样污染;粮食、豆类去杂物后,磨碎,过20目筛,储于塑料瓶中,保存备用;蔬菜、水果、鱼类、肉类及蛋类等水分含量高的鲜样,用食品加工机或匀浆机打成匀浆,储于塑料瓶中,保存备用;试样消化湿式消解法:称取试样~于锥形瓶或高脚烧杯中,放数粒玻璃珠,加10ml混合酸,加盖浸泡过夜,加一小漏斗电炉上消解,若变棕黑色,再加混合酸,直至冒白烟,消化液呈无色透明或略带黄色,放冷用滴管将试样消化液洗入或过滤入视消化后试样的盐分而定10ml~25ml容量瓶中,用水少量多次洗涤锥形瓶或高脚烧杯,洗液合并于容量瓶中并定至刻度,混匀备用;同时作试剂空白;测定仪器条件:根据各自仪器性能调至最佳状态;参考条件为波长,狭缝~,灯电流5mA~7mA,干燥温度120℃,20s;灰化温度450℃,持续15s~20s,原子化温度1700℃~2300℃,持续4s~5s,背景校正为氘灯或塞曼效应;标准曲线绘制:吸取上面配制的铅标准使用液,,,,ml或μl各10μL,注入石墨炉,测得其吸光值并求得吸光值与浓度有关系的一元线性回归方程;试样测定:分别吸取样液和试剂空白液各10μl,注入石墨炉,测得其吸光值,代入标准系列的一元线性回归方程中求得样液中铅含量;基体改进剂的使用:对于干扰试样,则注入适量的基体改进剂磷酸二氢铵溶液20g/L一般为5μl或与试样同量消除干扰;绘制铅标准曲线时也要加入与试样测定时等量的基体改进剂磷酸二氢铵溶液;结果计算试样中铅含量按式1进行计算;C1-C0×V×1000X= ---------------------m×1000式中:X——试样中铅含量,单位为微克每千克或微克每升μg/kg或μg/L;C1——测定样液中铅含量,单位为纳克每毫升ng/mL;CO——空白液中铅含量,单位为纳克每毫升ng/mL;V——试样消化液定量总体积,单位为毫升mL;m——试样质量或体积,单位为克或毫升g/mL;计算结果保留两位有效数字;精密度在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的20%;。

食品中铅的测定食品中铅(lead)是体内铅的主要来源,含铅农药的使用,陶瓷食具釉料中含铅颜料的加入,食品生产中使用含铅量高的镀锡管道、器械或容器,均可直接或间接造成食品的铅污染。
食品中铅的限量标准因不同食品而异。
粮食≤0.5mg/kg,蔬菜、水果≤0.2mg/kg,薯类≤0.2mg/kg,豆类≤0.8mg/kg,肉类(0.5mg/kg,鱼虾类≤0.5mg/kg,调味品≤1.0mg/kg。
食品中铅的测定方法主要有石墨炉原子吸收光谱法、火焰原子吸收光谱法和二硫腙比色法及示波极谱法。
一火焰原子吸收光谱法1.原理样品经处理后,铅离子在一定的pH条件下与二乙基二硫代氨基甲酸钠(DDTC)形成络合物,经4-甲基戊酮-2(MLBK)萃取分离,导入原子吸收光谱仪中,经火焰原子化后,吸收283.3nm共振线,其吸收量与铅的含量成正比,与标准系列比较定量。
2.试剂硝酸-高氯酸消化液(4+1);300g/L硫酸铵溶液;250g/L枸橼酸铵溶液;1g/L溴百里酚蓝水溶液;50g/L二乙基二硫代氨基甲酸钠(DDTC)水溶液;氨水(1+1);4-甲基戊酮-2(MLBK)。
铅标准使用液:将1.0mg/ml铅标准贮备液用亚沸蒸馏水逐级稀释至10.0μg/ml。
3.仪器原子吸收分光光度计附火焰原子化器。
其余同石墨炉法。
4.操作(1)样品处理:1)饮品及酒类:取均匀样品10.0g~20.0g于烧杯中,酒类应先在水浴上蒸干酒精,于电热板上先蒸发至一定体积后,加入10ml硝酸+高氯酸消化液(4+1),消化完全后,转移,定容至50ml容量瓶中。
2)包装材料浸泡液可直接测定。
3)谷类、禽、蛋、水产品:取样品5.0~10.0g,置于50ml瓷坩埚中,小火炭化后移入马弗炉,500℃以下灰化16h,放冷后再用少量混合酸消化至残渣中无炭粒,稍冷,加10ml盐酸(1+11),溶解残渣并移入500ml容量瓶中定容至刻度。
取与样品相同量的混合酸和盐酸(1+11)按同一操作方法做试剂空白。
高 新 技 术随着我国现代工业建设步伐的加快及废弃物排放量的剧增,重金属及其化合物的污染也日益严重。
铅作为一种毒性很强的有害重金属,不仅对水质及水生生物造成影响,而且通过食物渠道对人们的安全构成极大威胁。
铅的测定方法一般有石墨炉原子吸收光谱法、电感耦合等离子体原子发射光谱法等。
在进行测量分析前通过浊点萃取对环境水样中痕量铅进行预富集分离,并采用原子吸收光度法测定水样中的铅含量。
该方法测定水样中痕量金属铅的线性范围是0~30μg/mL ;检测限为1.7ng/mL ;相对标准偏差为2.7%。
希望通过深入的研究,能够提高检测结果的准确性。
1 试验部分1.1 主要试剂与仪器1%(v/v)TritonX-114溶液;0.5×10-3mol/L5-Br-PADAP 的乙醇溶液;pH=8.0的H 2PO 4--HPO 42-缓冲溶液;1000μg/mL 的铅标准储备溶液;10μg/mL 的铅标准工作溶液。
工作条件:测定波长:283.3nm ;灯电流:2.5mA;狭缝宽度:5nm;乙炔流量:2.0L/min,空气流量:6.0L/min。
1.2 测定方法取一定量铅的标准溶液于10mL 离心管中,依次加入1%(v/v)TritonX-114溶液0.5mL,0.5×10-3mol/L5-Br-PADAP 溶液0.5mL,pH=8.0的缓冲溶液1mL,用超纯水稀释至10mL,摇匀,置于40℃恒温水浴中,加热15min 后,以4000r/min 离心15min 至相分离。
分相后的溶液在冰浴中冷却接近0℃,使表面活性剂变为粘滞的液相,然后反转离心管弃去水相,加入0.1mol/L 的硝酸-甲醇溶液0.4mL,以降低表面活性剂相的粘度,然后用原子吸收分光光度计进行测定。
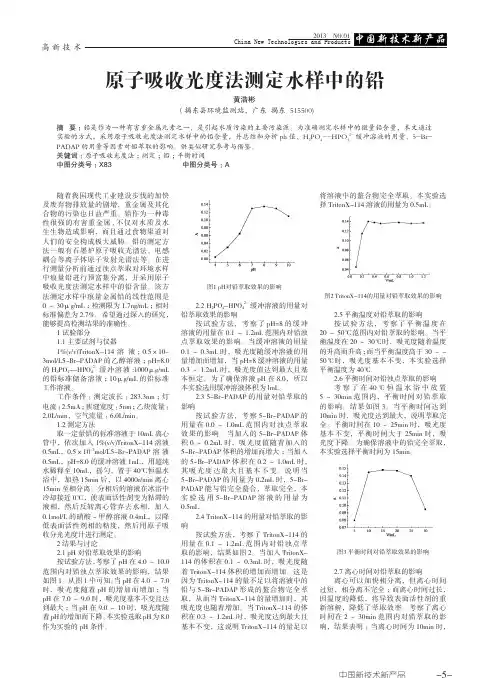
2 结果与讨论2.1 pH 对铅萃取效果的影响按试验方法,考察了pH 在4.0~10.0范围内对铅浊点萃取效果的影响,结果如图1。
从图1中可知:当pH 在4.0~7.0时,吸光度随着pH 的增加而增加;当pH 在7.0~9.0时,吸光度基本不变且达到最大;当pH 在9.0~10时,吸光度随着pH 的增加而下降。

液体饮料等食品中铅含量的简易测定法
1、准备试剂:氢氟酸、碳酸钠、乙二醇、硫酸铅2%
2、将灌装过程中取得的液体饮料(或者食品)等样品,每种样品取10ml,加到
50ml的容量瓶中,每瓶加入10ml 的氢氟酸,搅拌均匀
3、采用滴定法测定铅含量,将每瓶中加入10ml的碳酸钠溶液,缓慢滴加乙二醇,直至出现稳定的淡黄色,用滴定管表读取液体的铅含量
4、比较读数,比较每种样品的铅含量,最后得出测定结果
5、将结果记录在实验结果表中,并将测得的铅含量与国家标准值进行比较。
6、如果国家标准值超出,应立即淘汰样品,把符合国家标准值的样品放入储存,
以便将来使用。
7、将最后结果记录在实验报告书中,并上报相关主管部门。
8、经过实验结果,确定零售商品的铅含量是否超标,对超出排放标准的产品,应
及时处理并记录处理情况。
9、定期对测定的液体饮料(或者食品)样品进行复核,以复核结果表明是否处理
正确。
10、及时做好日常使用样品的样品收集,及时归档,以做好后续实验或者复核工作。

钡铬酸铅容量法方法提要试料用盐酸分解,加人适量的氯化钡,使试料中存在的硫酸根与钡生成硫酸钡沉淀,避免形成硫酸钡铅的复盐,影响铅的测定。
滤去硫酸钡和酸不溶物,在1.5%-2.1%的硝酸介质中,加过量的重铬酸钾,沉淀铬酸铅,用盐酸-氯化钠混合溶液溶解铬酸铅,加入碘化钾,析出与铅等物质量的碘,用硫代硫酸钠标准溶液滴定。
用以计算铅量。
试剂1.1 盐酸(1.19 g/mL)1.2 硝酸( 1. 40 g/mL)1.3 氯化钡溶液(10% m/V)1.4 盐酸(2% V/V)1.5 重铬酸钾饱和溶液1.6 乙酸铵溶液(2% m/V)1.7 盐酸-氯化钠混合溶液:称取300 g氯化钠溶于1250 mL水中,加100 ml盐酸(10. 1),摇匀。
1.8 碘化钾溶液(20% m/V).1.9 硫代硫酸钠标准溶液〔c(Na2S203·5H20)=0.025 mol/L〕:称取6. 2 g硫代硫酸钠Na2S203·5H20,用新煮沸已放冷却的水溶解,移人1000 mL容量瓶中,并稀释至刻度,加人0. I g碳酸钠及1 mL三氯甲烷,摇匀,贮存于棕色瓶中。
1.10 硫代硫酸钠标准溶液〔c(Na2S203·5H20)=0.05 mol/L〕:称取12.4g 硫代硫酸钠Na2S203·5H20,以下按(1.9)进行配制。
1.11 标定:移取20. 00 mL或50. 00 mL铅标准溶液(1.13),置于200 mL 烧杯中,加入2.5 mL铁溶液(1.12),以下按分析步骤(2.3. 2-2.3. 4)进行标定,同时标定三份,取算术平均值(所消耗的硫代硫酸钠标准溶液体积极差值不得超过0.2 mL,否则重新进行标定),按下式计算1 mL 硫代硫酸钠标准溶液(1.9)或(1.10)相当于铅的量:T= m/(V—V0)式中: T—1 m L硫代硫酸钠标准溶液相当于铅的量,g/mL;m —所取铅标准溶液中铅量,g;V —滴定所消耗硫代硫酸钠平均体积,ml;V0—试剂空白消耗硫代硫酸钠平均体积,mL,1.12 铁溶液(4 mg/mL):称取高纯三氧化二铁0. 57 g,加入10 ml盐酸,加热溶解,取下冷却,移入100 mL容量瓶中,用水稀释至刻度,摇匀。

铅的含量测定方法
铅的含量可以通过多种方法来进行测定,以下是几种常用的方法:
1. 原子吸收光谱法(AAS):该方法利用铅原子在特定波长的光束照射下吸收光的特性来测定铅的含量。
2. 火花原子发射光谱法(OES):该方法利用高温等离子体产生的火花将待测样品中的铅原子激发,并通过测量激发的光谱来确定铅的含量。
3. 电感耦合等离子体发射光谱法(ICP-OES):该方法利用高温等离子体将待测样品中的铅原子激发,并通过测量激发的光谱来确定铅的含量。
4. X射线荧光光谱法(XRF):该方法利用待测样品受到X射线照射后产生的荧光特性来测定铅的含量。
5. 比色法:该方法利用铅离子与某些试剂发生反应生成有色产物,通过测量产物的吸光度来确定铅的含量。
需要根据具体的实验条件和要求选择合适的方法。

水中铅和镉的含量测定及处理方法引言:水作为人类生活和生产的重要资源,其质量直接关系到人类的健康和环境的保护。
铅和镉是水污染中常见的有害重金属,具有高度的毒性和累积性。
本文将介绍水中铅和镉的含量测定方法,以及对水中铅和镉进行处理的方法。
一、水中铅和镉的含量测定方法1.原子吸收分光光度法(AAS)原子吸收分光光度法是一种常见的用于金属元素测定的方法。
该方法基于金属元素对特定波长的电磁辐射的吸收特性。
具体操作步骤如下:(1)取水样品,使用合适的方法去除悬浮物和浮游物。
(2)将水样与相应的溶剂(如酸)酸化处理,以溶解金属元素。
(3)使用原子吸收分光光度计,选择合适的波长和光源,对处理后的样品进行测定。
(4)根据吸收光谱的强度,通过与标准品对比,确定水样中铅和镉的含量。
2.电感耦合等离子体质谱法(ICP-MS)电感耦合等离子体质谱法是一种高灵敏度、高分析能力的测定金属元素的方法。
其操作步骤与AAS类似,但采用的仪器是ICP-MS。
该方法的优点是能同时测定多种金属元素,且灵敏度和准确度高。
3.化学计量法化学计量法是一种基于化学反应,将样品中的金属离子与特定试剂发生定量反应,经计量后确定金属离子含量的方法。
常用的化学计量法包括硫化氢沉淀法、试剂法和络合滴定法等。
二、水中铅和镉的处理方法以下是常用的处理方法:1.沉淀法适用于水中铅和镉的高浓度,通过添加沉淀剂,如硫化钠或氢化钠等,将金属离子转化为相对稳定的沉淀物,然后通过过滤或沉淀分离处理。
2.离子交换法离子交换法是利用特定固体材料的交换作用,将水中的金属离子吸附在固体表面,然后再用适当的溶剂将金属离子洗脱出来的方法。
常用的离子交换材料有活性炭、树脂等。
3.膜处理法膜处理法是利用特殊的膜材料,通过逆渗透、超滤等机理将水中的金属离子分离和去除的方法。
逆渗透是指利用高压将水分子逆向推移,从而将溶质从水中分离出来。
4.生物吸附法生物吸附法是利用一些具有吸附金属离子能力的生物材料,如微生物、藻类等,将水中的金属离子吸附在生物体表面,从而实现金属离子的去除。

铅的测定方法
铅是一种有毒的金属,进入人体后会对健康造成危害,因此需要
进行铅的检测和测定。
下面介绍一些常见的铅的测定方法。
1.火焰原子吸收光谱法
该方法适用于对铅含量不高的样品,包括水、土壤和食品等。
该
方法需要将样品溶解,然后使用火焰原子吸收光谱仪进行检测。
该方
法准确、灵敏度高,但对于铅含量较高的样品就会比较困难。
2.原子荧光光谱法
该方法也适用于铅含量较低的样品,包括水、土壤和食品等。
该
方法首先需要将样品溶解,然后使用荧光光谱仪进行检测。
该方法具
有高效、高灵敏度、高选择性等特点。
3.电化学法
电化学法多用于对有机化合物样品中的铅进行检测,包括血液、
尿液和体液等。
该方法使用电极进样法进行测定,能够精确测定样品
中的铅含量,同时其操作过程简单、快捷,因此得到广泛应用。
总的来说,以上几种方法都可以对铅进行测定,但各自的适用场
景也不完全相同。
因此,选择合适的铅检测方法需要根据样品的特性、所需检测的铅含量以及实际情况等因素进行综合考虑。
在进行铅的测
定过程中,需要注意保护个人安全,尽量采取无害化的处理方式,确
保检测结果的准确性和可靠性。

铅的测定——石墨炉原子分光光谱法1 范围本方法规定了乳制品中铅的测定方法。
本方法检出限为5ppb。
2 原理试样经酸消解后,注入原子吸收分光光度计石墨炉中,电热原子化后吸收283.3nm共振线,在一定浓度范围,其吸收值与铅含量成正比,与标准系列比较定量。
3 试剂3.1 硝酸(优级纯)3.2 过氧化氢(30%)3.3 磷酸二氢铵3.4 六水硝酸镁3.5 硝酸(2%):取20ml硝酸慢慢加入500ml水中,稀释至1000ml。
3.6 基体改进剂:称取1g磷酸二氢铵,0.1038g六水硝酸镁用水溶解定容至100ml。
3.7 铅标准使用液:每次吸取铅标准储备液1.0ml于100ml容量瓶中,加硝酸(2%)至刻度。
如此经多次稀释成每毫升含5.0,10.0,20.0,30.0,40.0ng铅的标准使用液。
4 仪器所用玻璃仪器均需以硝酸(1+5)浸泡过夜,用水反复冲洗,最后用去离子水冲洗干净。
4.1 原子吸收分光光度计(附石墨炉及铅阴极空心灯)。
4.2 微波消解仪。
4.3 可调式电热板。
5 分析步骤5.1 试样消解称取1g奶样加入消解罐,加入硝酸(优级纯)3ml,过氧化氢(30%)2ml,按设定程序微波消解,微波消解条件如下:1、5kg – 70s2、10kg-120s3、15kg-150s4、20kg-100s5、25kg-100s 消解结束后取出冷却,置于加热板上在130℃赶酸,大约0.3ml时停止赶酸(用空消解罐内移取0.3ml左右的纯净水作对比,硝酸浓度为2%左右),冷却,先用少量超纯水稀释,将稀释液全部转移倒入10ml容量瓶中,再用超纯水多次润洗,并将液体全部转移至容量瓶中,定容至10ml。
5.2 测定5.2.1仪器条件:根据各自仪器性能调至最佳。
参考条件:波长283.3nm,狭缝0.2nm~1.0nm,干燥温度120℃,20s,灰化温度450℃,15s~20s,原子化温度1700℃~2300℃,4s~5s,背景校正灯为氘灯。
EDTA容量法测定铅1.方法提要试样用酸分解,在酸性介质中,铅离子与硫酸根作用生成硫酸铅沉淀,与铁、铜、锌、镉等元素分离。
再在PH5~6的醋酸-醋酸钠缓冲溶液中,将硫酸铅转化成醋酸铅。
以二甲酚橙或半二甲酚橙为指示剂,用EDTA标准溶液滴定。
锑、铋含量较高时,易水解并夹杂于硫酸铅沉淀中,可加入酒石酸络合以消除其干扰,钡大于10mg时,由于生成PbSO4·BaSO4复盐沉淀,使铅的结果偏低。
本法适用一般矿石ω(Pb)/10-2>5的测定。
2.试剂2·1.盐酸(p1.19g/mL),分析纯。
2·2.硫酸(p1. 84g/mL),分析纯。
2·3.硝酸(p1.42g/mL),分析纯。
2·4.高氯酸(p1.68g/mL),分析纯。
2·5.冰醋酸(p1.05g/mL),分析纯。
2·6.二甲酚橙或半二甲酚橙指示剂:称取0.5g二甲酚橙或半二甲酚橙溶于100mL水中。
2·7.酒石酸溶液:称取20g酒石酸溶于100mL水中。
2·8.醋酸-醋酸钠缓冲溶液(PH5~6):称取200gCH3COONa·3H2O溶于水中,加10mL冰醋酸,用水稀释至1000mL,摇匀。
2·9.将金属铅(99.99%)于硝酸(10+90)中浸泡1min,取出,用乙醇洗净,于50℃烘干。
2·10.铅标准溶液的配制:准确称取4.1442g或2.0721g于50℃烘干的金属铅(99.99%)于250mL烧杯中,加入20mLHNO3(1+1),低温加热使其溶解,冷却后移入1000mL容量瓶中,用水稀释至刻度,混匀。
此液为C(Pb)=0.02000mol/L或C(Pb)=0.01000 mol/L。
2·11.EDTA标准溶液的配制:分别称取120g或60gEDTA于1000mL水中,加热溶解,用水稀释至16L,混匀,放置过夜,此溶液为C(EDTA)=0.02000 mol/L或C(EDTA)=0.01000mol/L。
铅的测定EDTA容量法作者:魏毅张冶来源:《科学与财富》2011年第07期1、方法提要:试样用酸分解,在酸性介质中,Pb2+与与SO42ˉ作用生成硫酸铅沉淀与其他元素分离。
再在PH5-6的醋酸-醋酸钠缓冲溶液中,将PbSO4转化成Pb(Ac)2。
以二甲酚橙为指示剂,用EDTA标准液滴定。
Sb、Bi含量较高时,易水解并夹杂于硫酸铅沉淀中,可加入酒石酸络合以消除干扰,Ba大于10mg,由于生成复盐PbSO·BaSO4沉淀,使铅结果偏低。
2、所需试剂2.1硝硫混酸7:32.2稀硫酸2%2.3醋酸-醋酸钠缓冲液:称取200gCH3COONa·3H2O溶于水,加10毫升冰乙醇,用水稀释至1升混匀。
2.4二甲酚指示剂(0.2%的水溶液)称取0.2克二甲酚橙溶于水,加5毫升酒精,用水稀释100毫升(保存期勿太长,一周内使用)。
2.5EDTA标准溶液的配制和标定:配制约0.02M,称取7.44克EDTA二钠盐溶于100毫升水中,混匀。
2.6抗坏血酸2.7天平(感量0.001)标定:取1毫升相当2毫克铅的标准溶液25毫升,加20毫升醋酸-醋酸钠缓冲液,搅伴,用水稀释至150毫升,加3-5滴二甲酚橙指示剂,以EDTA标准液滴定,由红色变为亮黄色为终点,由消耗的体积,计算EDTA标准液的测定度(mg/ml)铅标准溶液:精确称取2.0000克电解铅(99.99%),置于400毫升烧杯中,加入20毫升1:1硝酸,盖上表面皿低温溶解,冷却至定温,用水洗表面皿,然后转入1000毫升容量瓶中,用水稀释至刻度,摇匀,此溶液1毫升相当2毫克铅。
3、分析步骤:称取试样0.5克置于400毫升烧杯中,用少量水润湿,加硝硫混酸15-20毫升毫升,盖上表面皿,加热渚沸至试样溶解,并蒸至冒出浓厚的SO3白烟(体积剩2.5毫升左右),取下冷却。
用水冲洗杯壁,加水50毫升,摇匀,(试样含Bi高时,可加5毫升200g/L酒石酸溶液),加热渚沸使可溶性盐溶解,取下冷却,放入冷水槽中冷却半小时以后,以定量滤纸过滤,用蒸馏水洗烧杯2次,洗沉淀6-8次,将沉淀和滤纸放入原烧杯中,加入醋酸-醋酸钠缓冲溶液,溶液加热煮沸后用水稀释至150-200毫升,加入0.1克抗坏血酸[少量铁(Ⅲ)离子能封闭指示剂],加入抗坏血酸将铁(Ⅲ)还原消除干扰,加入3-5滴二甲酚橙指示剂,用EDTA标准溶液滴定至溶液由红色变为亮黄色为终点。
食品中铅的测定方法石墨炉原子吸收光谱法1.原理样品经灰化或酸消解后,样液注入原于吸收分光光度计石墨炉中原子化,铅原子吸收283.3nm共振线,在一定浓度范围,其吸收值与铅含量成正比,可与标准系列比较定量。
2.试剂实验用水为亚沸蒸馏水或电阻率80万欧姆以上的去离子水。
所有试剂要求使用优级纯或处理后不含铅的试剂。
(1)过硫酸铵。
(2)过氧化氢(30%)。
(3)高氯酸、硝酸。
(4)硝酸溶液 (1+1)。
(5)硝酸溶液 (0.5mol/L):取3.2ml硝酸,加入水中稀释至l 00ml。
(6)硝酸溶液 (1.0mol/L):取6.4ml硝酸,加入水中稀绎至100ml。
(7)磷酸氢二铵溶液 (20g/L)。
取2.0g特纯磷酸氢二铵溶于双蒸水中定容至100ml。
(8)混合酸:硝酸 + 高氯酸 (4+1)。
(9)铅标准溶液 (自己配制或由国家标准局标准物质研究中心购买铅标准溶液)A. 铅标准贮备液:精密称取1.000g 金属铅 (99.99%) 分次加少量硝酸 (1+1) 加热溶解,总量不超过37ml,移入l000ml容量瓶,加水至刻度。
此溶液每毫升含1.0mg铅。
B. 铅标准贮备液:精密称取0.1598g硝酸铅(优级纯),加10ml l.0mol/L硝酸,全部溶解后,移入100ml容量瓶中,加水稀释至刻度,此溶液每毫升相当于1.0mg铅。
C. 铅标准使用液:火焰法铅标准使用液浓度为10mg/ml (用亚沸蒸馏水逐级稀释);石墨炉法铅标准使用液浓度为100ng/ml,用0.5mol/L 硝酸逐级稀释。
3.仪器(1)原子吸收分光光度计 (附石墨炉及铅空心阴极灯)。
(2)所用玻璃仪器均需以硝酸 (1+5) 浸泡过夜,用水反复冲洗,最后用去离子水冲洗干净。
(3)马弗炉或恒温干燥箱(4)瓷坩埚或压力消化器(5)微波消解装置4.操作方法4.1 样品预处理:采样和制备过程中,应注意不使样品污染。
粮食、豆类去壳去杂物后,磨碎过20目筛,储于塑料瓶中.保存备用;蔬菜、水果洗净,晾干,取可食部分捣碎备用:鱼、肉等用水洗净,取可食部分捣碎,备用。
附录Ⅸ B 铅、镉、砷、汞、铜测定法(一部)一、原子吸收分光光度法本法系采用原子吸收分光光度法(附录Ⅴ D)测定中药材中的铅、镉、砷、汞、铜,除另有规定外,按下列方法测定。
1.铅的测定(石墨炉法)测定条件 参考条件:波长 283.3nm,干燥温度 100~120℃,持续 20 秒;灰化温度 400~750℃,持续 20~25 秒;原子化温度 1700~2100℃,持续 4~5秒;背景校正为氘灯或塞曼效应。
铅标准储备液的制备 精密量取铅单元素标准溶液适量,用 2%硝酸溶液稀释,制成每 1ml 含铅(Pb)1µg 的溶液,即得(0~5℃贮存)。
标准曲线的制备 分别精密量取铅标准储备液适量,用 2%硝酸溶液制成每1ml 分别含铅 0ng、5ng、20ng、40ng、60ng、80ng 的溶液。
分别精密量取 1ml,精密加含 1%磷酸二氢铵和 0.2%硝酸镁的溶液 1ml,混匀,精密吸取 20µl 注入石墨炉原子化器,测定吸光度,以吸光度为纵坐标,浓度为横坐标,绘制标准曲线。
供试品溶液的制备 A 法取供试品粗粉 0.5g,精密称定,置聚四氟乙烯消解罐内,加硝酸 3~5ml,混匀,浸泡过夜,盖好内盖,旋紧外套,置适宜的微波消解炉内,进行消解(按仪器规定的消解程序操作)。
消解完全后,取消解内罐置电热板上缓缓加热至红棕色蒸气挥尽,并继续缓缓浓缩至 2~3ml,放冷,用水转入 25ml 量瓶中,并稀释至刻度,摇匀,即得。
同法同时制备试剂空白溶液。
B 法取供试品粗粉 1g,精密称定,置凯氏烧瓶中,加硝酸 高氯酸(4∶1)混合溶液 5~10ml,混匀,瓶口加一小漏斗,浸泡过夜。
置电热板上加热消解,保持微沸,若变棕黑色,再加硝酸 高氯酸(4∶1)混合溶液适量,持续加热至溶液澄明后升高温度,继续加热至冒浓烟,直至白烟散尽,消解液呈无色透明或略带黄色,放冷,转入 50ml 量瓶中,用 2%硝酸溶液洗涤容器,洗液合并于量瓶中,并稀释至刻度,摇匀,即得。
EDTA滴定法测定铅方法基于使铅生成硫酸铅沉淀于其它元素分离,然后将硫酸铅转化成为醋酸铅,在PH5.5-6的醋酸—醋酸钠缓冲溶液中,以二甲酚橙为指示剂,用EDTA 标准溶液滴定。
试剂配制醋酸—醋酸钠缓冲溶液:取200g结晶乙酸钠,用水溶解后,加入10ml冰乙酸,用水稀释到1000ml。
EDTA标准溶液:称取EDTA3.35g于250ml烧杯中,加水150ml,加热溶液,冷却后移入1000容量瓶中,用水稀释至刻度。
此次溶液的浓度约为0.009mol/L。
铅标准溶液:称取2.0000g金属铅(99.99%)于400ml烧杯中,加入硝酸(1+1)20ml,加热溶解,冷却后移入1000ml容量瓶中,以水稀释到刻度,摇匀。
此溶液为2mg/ml铅。
标定:吸取铅标准溶液20ml于250ml烧杯中,加甲基橙指示剂一滴,用氨水(1+1)中和使溶液由橙红色到刚好显黄色,加入缓冲溶液25ml,加水50ml,加二甲酚橙指示剂一滴,用EDTA标准溶液滴定至溶液由酒红色到亮黄色即为终点。
同时做空白试验。
计算:mF =V-V0F EDTA标准溶液对铅的滴定度,mg/mlm 吸取铅标准溶液中铅的质量,mg;V 滴定消耗EDTA标准溶液的体积。
ml;V0空白试验消耗EDTA标准溶液的体积,ml ;分析步骤称取试样0.2~0.5g于250ml烧杯中,加氟化钠0.5g(试样含硅量低时可以不加)加盐酸12~15ml;于低温加热溶解,当蒸发至约5ml左右时加硝酸7~10ml,继续加热数分钟,稍冷,加入0.3~0.5氯酸钾(试样中不含碳时可不加)加热使有机物完全氧化,加30ml硫酸(1+1),蒸发至冒三氧化硫浓烟保持5min,取下冷去。
以水冲洗杯壁,加水50ml,加10%酒石酸溶液10ml(试样中不含锑铋时可不加)加热煮沸数分钟使可溶性硫酸盐溶解,取下流水冷却静止40~60min(或在室温静止三小时),在带有滤纸的浆或脱脂棉的漏斗上过滤,用2%的硫酸溶液冲洗烧杯及其沉淀无Fe+3反应(用10%硫氰酸铵检查),用水洗烧杯和沉淀2—3次或用乙醇(1+4)洗1—2次,将沉淀和滤纸一同移入原烧杯中,加水25ml,加醋酸—醋酸钠缓冲溶液25ml,加热煮沸3—5min,取下冷却,加入2ml200g/LKF 溶液,加二甲酚橙指示剂(5g/L)2滴,用EDTA标准溶液滴定,溶液由酒红色到亮黄色即为终点。
食品中铅的测定方法
嘿,你问食品中铅的测定方法呀?那咱就来好好聊聊。
这食品里的铅可不是啥好东西,得好好测测,保证咱吃的东西安全呐。
先说说原子吸收光谱法吧。
这就像个超级侦探,能把食品里的铅给找出来。
把食品样品弄碎了,加点化学试剂,让铅变成一种特殊的状态。
然后用原子吸收光谱仪一照,就能知道里面有多少铅啦。
这方法挺准的,就是仪器有点贵,一般都是专业的实验室用。
再说说比色法。
这个就比较简单啦,就像玩颜色游戏一样。
把食品样品处理一下,加上一些特定的试剂,要是有铅的话,就会变色。
然后跟标准的颜色比一比,就能大概知道铅的含量了。
这方法虽然没那么准,但是便宜又好用,一些小实验室或者企业也能用。
还有一种叫电化学分析法。
这个就像个小电子警察,能检测出食品里的铅。
把食品样品弄成溶液,放在一个特殊的仪器里,通过电化学反应来判断铅的含量。
这方法也挺灵敏的,就是操作起来有点复杂。
我给你讲个例子哈。
有一次,我家附近的一个小食品厂被怀疑食品里有铅超标。
他们就用比色法来检测,把样品处理好后,加上试剂,结果颜色有点不对劲。
他们赶紧又送到专业的实验室用原子吸收光谱法检测,果然发现铅超标了。
后来他们就赶紧整改,把有问题的食品都处理了。
所以啊,食品中铅的测定方法有很多种,各有优缺点。
为了咱的健康,一定要认真检测食品里的铅,不能让那些坏东西进到咱的肚子里。
大家买食品的时候也得多注意,看看有没有检测报告啥的,这样才放心嘛。
铅的测定法1 范围本标准规定了本公司牙膏、化妆品、蜡制品、香料中总铅的测定。
本方法样品最低检测浓度为4ppm。
2 引用标准本标准等同采用GB7917.3—87。
3 火焰原子吸收分光光度法3.1 方法提要样品经预处理,使铅以离子状态存在于试液中,试液中铅离子被原子化后,基态原子吸收来自铅空心阴极灯发出的共振线,其吸收量为样品中铅含量成正比。
在其它条件下变的情况下,根据测量被吸收后的谱线强度,与标准系列比较,进行定量。
3.2 试剂3.2.1 去离子水或同等纯度的水:将一次蒸馏水经离子交换净水器净水,贮存于全玻璃瓶或聚乙烯瓶中。
3.2.2 硝酸(密度1.42ɡ/ml):优级纯。
3.2.3 高氯酸(70%—72%):优级纯。
3.2.4 过氧化氢(30%):优级纯。
3.2.5 硝酸(1+1)。
3.2.6 混合酸:硝酸和高氯酸按(3+1)混合。
3.2.7 铅标准浓液3.2.7.1 称取纯度为99.99%的金属铅1.000g,加入20 ml(1+1)硝酸,加热使溶解,转移到1000 ml 容量瓶中,用水稀释至刻度。
此标准溶液1ml相当于1.00mg铅。
3.2.7.2 移取铅标准溶液10.0ml至100ml容量瓶中,加2ml(1+1)硝酸,用水稀释于刻度,此溶液1ml相当于100μg铅。
3.2.7.3 移取铅标准溶液(3.2.7.2)10.0ml至100ml容量瓶中,加2ml(1+1)硝酸,用水稀释至刻度,此1ml溶液相当于10.0μg铅。
3.2.8 MIBK(甲基异丁基酮):分析纯。
3.2.9 盐酸(7mol/L);取30ml盐酸(密度1.19g/ml),加水至50ml。
3.2.10 BTB(溴麝香草酚蓝)(0.1%):称取100ml BTB,溶于50ml95%乙醇溶液,加水至100ml。
3.2.11 柠檬酸铵(25%):必要时用DDTC和MIBK萃取除铅。
3.2.12 氢氧化铵(1+1):优级纯。
3.2.13 硫酸铵(40%):必要时,以DDTC和MIBK萃取除铅。
3.2.14 DDTC(二乙氨基二硫代甲酸钠)(2%)3.2.15 APDC(吡咯烷二硫代甲酸铵)(2%)。
3.2.16 柠檬酸(20%):必要时用APDC和MIBK萃取除铅。
3.3 仪器3.3.1 原子吸收分光光度计及其配件。
3.3.2 离心机。
3.3.3 硬质玻璃消解管或小型定氮消解瓶。
3.3.4 比色管:10ml及其25ml。
3.3.5 分液漏斗:100ml。
3.3.6 瓷坩埚:50ml。
3.3.7 箱形电炉。
3.4 分析步骤3.4.1 样品预处理3.4.1.1 湿式消解法称取约1.00-2.00g试样置于消化管中。
随同试样做试剂空白。
含有乙醇等有机溶剂的化妆品,先在水浴或电热板上将有机溶剂挥发。
若为膏霜型样品,可预先在水浴中加热使瓶颈上样品熔化流入消化管底部。
加入数粒玻璃珠,然后加入10ml硝酸,由低温至高温加热消解,当消解液体积减少至2-3ml,移去热源,冷却。
然后加入2-5ml高氯酸,继续加热消解,不时缓缓摇动使均匀,消解至冒白烟,消解液呈淡黄色或无色溶液。
浓缩消解液至1ml左右。
冷却室温后定量转移至10ml(如为粉类样品,则至25ml)具塞比色管中,以去离子水定容至刻度。
如样液混蚀,离心沉淀后,可取上清液进行测定。
3.4.1.2 干湿消解法称取约1.00—2.00g试样,置于瓷坩埚中,在小火上缓缓加热直至炭化。
移入箱型电炉中,500℃下灰化6h左右,冷却取出。
向瓷坩埚加入混合酸约2—3 ml,同时做试剂空白,小心加热消解,直至冒白烟,但不得干涸若有残存炭粒,应补加2—3 ml混和酸,反复消解,直至样液为无色或微黄色。
微火浓缩至近干,然后,定量转移至10ml刻度试管(如为粉类,则至25ml刻度试管)中,用水定容至刻度。
必要时可离心沉淀。
3.4.1.3 浸提法(本方法不适用于含蜡质样品)称取约1.00g试样,置于比色管中。
同时做试剂空白。
样品中如含有乙醇等有机溶液,先在水浴中挥发,但不得干涸。
加2ml硝酸和5ml过氧化氢,摇匀,于沸水浴中加热2h。
冷却后用水定容至10ml备用(如为粉类样品,则定容至25ml)。
如样品混蚀,离心沉淀后,取上清液备用。
3.4.2 测定3.4.2.1 移取0、0.50、1.00、2.00、4.00、6.00ml铅标准溶液,分别置于数支10ml比色管中,加水至刻度。
按仪器规定的程序,分别测定标准、空白和样品溶液。
但如样品溶液含有大量离子如铁、铋、铝、钙等干扰测定时,应预先按3.4.2.2进行萃取处理。
绘制浓度—光度曲线,计算样品含量。
3.4.2.2 样品如含有大量铁离子,按3.4.2.3进行萃取。
如含有大量铋等离子干扰,按3.4.2.4进行萃取。
如有大量铝、钙等离子,按3.4.2.5进行萃取。
3.4.2.3 将标准、空白和样品溶液转移至蒸发皿中,在水浴上蒸发至干。
加入10ml7mol/L盐酸溶解残渣,用等量的MIBK萃取二次,再用5ml7mol/L盐酸洗MIBK层,合并盐酸溶液,必要时赶酸,定容,进行直接测定或按3.4.2.4或3.4.2.5再次萃取,以除去其他离子的干扰。
3.4.2.4 将标准、空白和样品溶液转移至100ml分液漏斗中,加2ml柠檬酸铵、1滴BTB指示剂,用氢氧化铵调液为绿色,加2ml硫酸铵,加水至30ml,加2mlDDTC,混匀。
放置数分钟,加10mlMIBK,振摇3min,静置分层,取MIBK层进行测定。
3.4.2.5 将标准试剂空白和样品溶液转移至100ml分液漏斗。
加2ml柠檬酸,用(1+1)氢氧化铵调PH至2.5—3.0,加水至30ml,加2ml2%APDC,混合,放置3min,静置片刻,加入10mlMIBK振摇萃取3min,将有机相转移至离心管中,于3000r/min,离心5min。
取MIBK层溶液进行测定。
3.5 结果的计算按式(1)计算铅浓度(A-B)×V铅(㎎/㎏)= (1)m式中:A—从标准曲线上得样品溶液铅浓度,μg/ml;B—从标准曲线查得试剂空白铅浓度,μg/ml;V—样液总体积,ml;m—样品质量,g。
4 双硫腙萃取分光光度法本方法样适用于化妆品中铅的测定。
本方法最低检测出量为1.0µg铅,若取1g样品测定,则最低检测出量为1㎎/㎏。
4.1 试剂4.1.1 去离子水或同等级纯度的水:将一次蒸馏水经离子交换净水器净水,贮存于全玻璃瓶或聚乙烯瓶中。
4.1.2 氨水(1+1):优级纯。
4.1.3 盐酸(1+1):优级纯。
4.1.4 酚红指示液:0.1%乙醇溶液。
4.1.5 20%盐酸羟胺溶液:取盐酸羟胺20g,加50ml水溶液,加2滴酚红指示液,加(1+1)氨水调至PH8.5~9.0,用双硫腙三氯甲烷溶液提取,直至三氯甲烷层绿色不变,再用三氯甲烷洗水层二次,此水层以(1+1)盐酸调至酸性,加水至100ml备用。
4.1.6 20%柠檬酸溶液:取柠檬酸铵50g,溶于100ml水中,加2滴酚红指示液,加(1+1)氨水调至PH8.5~9.0,用双硫腙三氯甲烷溶液提取数次,直至三氯甲烷层绿色不变为止。
水层再用三氯甲烷萃取数次至三氯甲烷层无色为止。
弃去三氯甲烷层,水层加水稀释至250ml。
4.1.7 10%氰化钾溶液(注意有剧毒):如试剂含铅需纯化时,应先将10g氰化钾溶于20ml水中,以下按4.1.6所述方法纯化后再稀释至100ml。
4.1.8 三氯甲烷:不应含有氧化物。
4.1.9 双硫腙储备液:0.1%三氯甲烷溶液,保存于冷暗处。
必要时按下述方法纯化:称取0.5g研细的双硫腙,溶于50ml三氯甲烷中,如不全溶,可用滤纸滤过于250ml分液漏斗中,用1:99氨水提取三次,每次100ml,合并提取液,再用10ml三氯甲烷洗氨水溶液2次,用6mol/L盐酸调至酸性,将沉淀出的双硫腙用三氯甲烷提取2~3次,每次100ml,合并三氯甲烷层,加三氯甲烷至总体积为500ml。
4.1.10 双硫腙应用液:0.001%三氯甲烷溶液。
4.1.11 硝酸(1%)。
4.1.12 无铅脱脂棉:医用脱脂棉,必要时用双硫腙三氯甲烷液去除铅。
4.1.13 铅标准溶液。
4.2 仪器4.2.1 分液漏斗:125ml,预先用稀释酸浸泡,并经去离子水洗。
4.2.2 分光光度计。
4.3 分析步骤4.3.1 样品预处理4.3.1.1 湿式消解法称取约1.00-2.00g试样置于消化管中。
同时做试剂空白。
含有乙醇等有机浓剂的化妆品,先在水浴或电热板上将有机浓剂挥发。
若为膏霜型样品,可预先在水浴中加热使瓶颈上样品溶化流入消化管底部。
加入数粒玻璃珠,然后加入10ml硝酸,由低温至高温加热消解,当消解液体积减少至2-3ml,移去热源,冷却。
然后加入2-5ml高氯酸,继续加热消解,不时缓缓摇动使均匀,消解至冒白烟,消解液呈淡黄色或无色溶液。
浓缩消解液至1ml左右。
冷却至室温后量移至10ml(如为粉类样品,则至25ml)具塞比色中,以去离子水定容至刻度。
如样液混蚀,离心沉淀后,可取上清液进行测定。
4.3.1.2 干式消解法称取约1.00—2.00g试样,置于瓷坩埚中,在小火上缓缓加热直至炭化。
移入箱形电炉中,500℃下灰化6h左右,冷却取出。
向瓷坩埚加入混合酸约2—3 ml,同时作试剂空白,小心加热消解,直至冒白烟,但不得干涸若有残存炭粒,应补加2—3 ml混和酸,反复消解,直至样液为无色或微黄色。
微火浓缩至近干,然后,定量转移至10ml刻度试管(如为粉类,则至25ml刻度试管)中,用水定容至刻度。
必要时可离心沉淀。
4.3.2 测定取适量已按4.3.1处理的样液,于125ml分液漏斗中,加水至总体积为50ml,另取0、0.10、0.20、0.30、0.40、0.50ml铅标准溶液分别置于125ml分液漏斗中,各补加1%硝酸溶液至总体积为50ml。
然后向样品溶液、试剂空白及铅标准溶液中各加2ml20%柠檬酸铵溶液、1ml盐酸羟胺溶液、2滴酚红指示液,用氨水调节至红色出现,然后向各分液漏斗中加入2ml10%氰化钾溶液,混匀。
准确国加入5ml双硫腙应用液,剧烈振摇提取1min,静置分层,在分液漏斗下颈部塞入少许无铅脱脂棉,然后将三氯甲烷层滤入比色杯中,以三氯甲烷调零,在波长510 nm下测定吸光度,并绘制标准曲线。
4.4 结果计算按式(2)计算铅浓度:(m1-m0)×V铅= (2)m×V1式中:m1—从标准曲线查得样液的铅含量,μg;m0—从标准曲线查得试剂空白的铅含量,μg;m—样品质量,g;V—样液总体积,ml;V1—测定时样液取用量,ml。