【名师一号】2015高考化学大一轮复习 专题1 第一单元 物质的分类和转化精讲课件(含14年新题)苏教版
- 格式:ppt
- 大小:1.21 MB
- 文档页数:32

第01讲物质的分类及转化知识体系逻辑和学习要求核心逻辑:物质根据性质或组成进行分类,同类物质转化为其他物质的规律相似化学中有很多种物质,根据组成或性质将其进行归类并且命名,每个类别的物质在组成或性质上相似(纯净物),如果存在差异则会进一步细分(单质、化合物),直至同一类别的物质组成/性质十分接近(化合物→氧化物→酸性氧化物)。
不同类别的物质之间可以通过反应实现转化,对于同一类元素(金属/非金属),转化路径基本一致。
学习要求:1、理解物质分类的依据2、判断常见物质所属的具体类别及其性质a)熟记各类常见物质(特别是各类氧化物、六大强酸、四大强碱)b)熟记容易分类错误的物质c)熟记各类物质的性质(酸、碱、酸式盐和各类氧化物的性质)3、区分树状分类法和交叉分类法4、掌握金属元素和非金属元素从单质→盐的转化路径5、判断物理变化和化学变化知识梳理一一、物质的分类1、根据物质的组成和性质分类任何物质都是有元素组成的,根据元素组成对物质进行分类是常用的方法。
)和红磷、(1)同素异形体:由一种元素形成的几种性质不同的单质。
如:金刚石和石墨、白磷(P4氧气和臭氧【注】①同素异形体之间的转换是化学变化。
②同素异形体之间由于结构不同,物理性质有差异,但由于同种元素组成,化学性质相似或略有差异。
③由一种元素组成的物质不一定是纯净物。
如氧气和臭氧。
树状分类:对同类事物进行再分类的方法。
单质:O2、Fe、He等纯净物有机化合物:CH4、葡萄糖、酒精(乙醇)等酸:电离出的阳离子全部是氢离子无机化合物碱:电离出的阴离子全部是氢氧根盐:由金属阳离子或NH4+与酸根离子结合氧化物:只含两种元素,其中一种是氧元素溶液:NaCl溶液、稀硫酸等混合物胶体:Fe(OH)3胶体、淀粉胶体等浊液:泥水【注】冰水混合物、胆矾、明矾、水银等并非混合物,均为纯净物。
①酸的分类:酸可依据电离出氢离子的个数,将酸分为一元酸、二元酸、多元酸。
也可按照酸分子中是否含氧元素,将酸分为含氧酸和无氧酸。




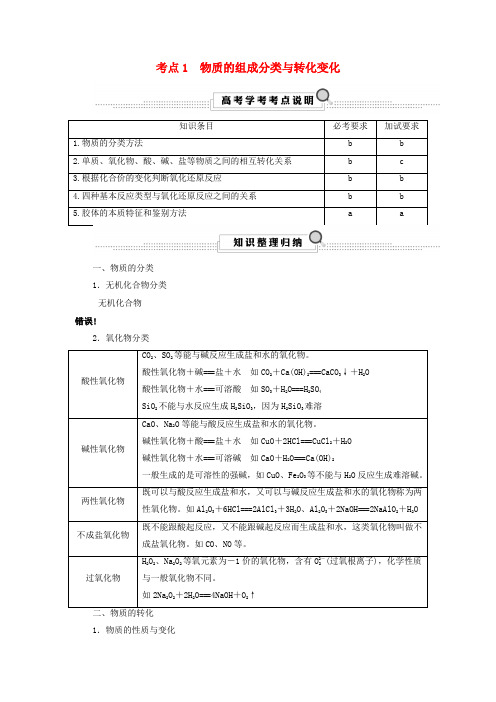
考点1 物质的组成分类与转化变化一、物质的分类1.无机化合物分类无机化合物错误!2.氧化物分类1.物质的性质与变化根据是否有新物质生成分为物理变化和化学变化。
应注意:升华、萃取、分液、蒸馏、吸附、盐析、金属导电、焰色反应、电离等都归为物理变化;脱水、蛋白质变性、水解、同素异形体互变、电解、熔融盐导电、电解质溶液导电等都是化学变化。
2.化学反应的分类四、胶体的性质与应用1.丁达尔效应可见光束通过胶体时,在与入射光垂直的角度可看见明亮的光路,可用此性质来鉴别溶液和胶体。
2.吸附性自来水含有铝和铁的化合物时,溶于水产生氢氧化铝胶体或氢氧化铁胶体,吸附水中的悬浮颗粒并沉降,从而达到净水的目的。
【例1】下列属于氧化物的是( )A.Na2OB.Ca(OH)2C.HClOD.K2CO3【解析】Na2O属于氧化物,则A选项正确;Ca(OH)2属于碱,不是氧化物,则B选项错误;HClO属于酸,则C选项错误;K2CO3属于盐,并非氧化物,则D选项错误。
【答案】 A【提炼】本题考查酸、碱、盐和氧化物的分类,难度不大。
如果再细分,要注意氧化物还可以分成酸性氧化物、碱性氧化物、过氧化物和不成盐氧化物等,要注意区别。
【例2】下列关于化学反应类型的叙述中,正确的是( )A.凡是生成盐和水的反应都是中和反应B.复分解反应一定没有单质参加C.生成一种单质和一种化合物的反应一定是置换反应D.分解反应的生成物一定有单质【解析】酸性氧化物与碱反应、碱性氧化物与酸反应也能生成盐和水,因此产物是盐和水的反应并不一定是中和反应,则A选项错误;复分解反应是指两种化合物互相交换成分,生成另外两种化合物的反应,复分解反应一定没有单质参加,则B选项正确;已知SO2+2H2S===3S↓+2H2O,该反应的产物也是单质和化合物,但并非置换反应,则C选项错误;已知Ca(OH)2===CaO+H2O,该反应属于分解反应,但是产物中没有单质,则D选项错误。
第1讲 物质的分类与转化 物质的分散系[考纲要求] 1.了解分类法在化学科学研究和化学学习中的重要作用,能根据物质的组成和性质对物质进行分类。
2.了解分散系的概念、分类方法,掌握胶体的概念、重要性质及应用,掌握Fe(OH)3胶体的制备方法。
3.理解混合物和纯净物、单质和化合物的概念,理解酸、碱、盐、氧化物的概念及其相互关系。
考点一 物质的组成1.元素、物质及微粒间的关系(1)宏观上物质是由元素组成的,微观上物质是由分子、原子或离子构成的。
(2)元素:具有相同核电荷数的一类原子的总称。
(3)元素与物质的关系元素――→组成⎩⎪⎨⎪⎧单质:只由一种元素组成的纯净物。
化合物:由多种元素组成的纯净物。
(4)元素在物质中的存在形态①游离态:元素以单质形式存在的状态。
②化合态:元素以化合物形式存在的状态。
(5)元素、微粒及物质间的关系图2.同素异形体(1)同种元素形成的不同单质叫同素异形体。
同素异形体的形成有两种方式:①原子个数不同,如O2和O3;②原子排列方式不同,如金刚石和石墨。
(2)同素异形体之间的性质差异主要体现在物理性质上,同素异形体之间的转化属于化学变化。
3.混合物和纯净物(1)纯净物:由同种单质或化合物组成的物质。
(2)混合物:由几种不同的单质或化合物组成的物质。
深度思考1.下列元素①Na②Mg③Al④Fe⑤Cu⑥C⑦Si⑧O⑨S⑩N⑪P⑫Cl ⑬H⑭He在自然界中,(1)只以化合态存在的是__________________。
(2)只以游离态存在的是__________________。
(3)既以化合态存在又以游离态存在的是_________________。
答案(1)①②③④⑤⑦⑫⑬(2)⑭(3)⑥⑧⑨⑩⑪2.判断下列说法是否正确?若不正确,说出理由。
①元素在自然界中的存在形式有原子、分子或离子②在化学变化中,分子可以再分,离子和原子不可以再分③同一种元素可能有多种不同原子,同一种原子也可能形成不同的离子④原子与该原子形成的离子相对原子质量几乎相等⑤由同一种元素组成的物质一定是同一种物质⑥物质的化学性质一定是由分子保持的⑦质子数、中子数和电子数都相同的粒子一定是同一种粒子答案①正确;②错误,在化学变化中复合离子如NH+4等可以再分;③正确;④正确;⑤错误,金刚石、石墨均是由C元素组成,但不是同一种物质,互为同素异形体;⑥错误,如Fe是由原子构成的,化学性质由铁原子保持;⑦错误,如N2和CO。