巯基化HA中巯基的取代度Ellman法详细步骤
- 格式:docx
- 大小:1.00 MB
- 文档页数:2

5,5-二硫二硝基苯甲酸 DTNB 现货供应产品描述:DTNB为Ellman试剂。
它用于比色法测定生物样品中巯基。
它易溶于水。
在巯基化合物的存在下,无色的DTNB将被转变成黄色的5-巯基-2-硝基苯甲酸。
由于5-巯基-2-硝基苯甲酸在412 nm处具有最大吸收,DTNB的吸收光谱并不干扰巯基的测定。
配置方法:准确称取0.198gDTNB用50mMNa2HPO4(pH=7.0)配制成50ml溶液,存放于棕色瓶中,于暗处低温保存备用。
应该注意的是配置缓冲、浓度,储存时要避免见光。
应用举例:半胱氨酸中自由巯基的定量检测方法一、试剂的配制:1、Tris-HCL缓冲液(0.25M):DDW准确配制后,用盐酸调节pH=8.3;2、半胱氨酸标准溶液(1mM):准确称取0.017563gL-半胱氨酸(175.63),用1ml甲酸溶解,以DDW定容至100ml;3、DTNB(分子量:396.35)标准溶液(10mM):准确称取0.198175gDTNB用50mMNa2HPO4(pH=7.0)配制成50ml溶液,存放于棕色瓶中,于暗处低温保存备用4、DTNB分析溶液(0.1mM):由1体积10mMDTNB标准液加99体积0.25M的Tris缓冲液配制而成,现用现配。
二、标准曲线的制作;1、25℃条件下,用Tris缓冲液稀释半胱氨酸标准液配成梯度的稀释液(5.0ml),其浓度分别为:0.00mM、0.025mM、0.05mM、0.1mM、0.15mM、0.2mM;2、取上述各浓度溶液1ml分别加入到5ml预先恒温于25℃水中的DTNB分析溶液,摇匀,准确静止10min,立即于波长412nm处测定吸光度值(A)。
根据目的蛋白的吸光度在标准曲线上读出对应的浓度即可Product Name:DTNBProduct Number:D8130Product Brand:SigmaCAS Number:69-78-3Molecular Formula:[-SC6H3(NO2)CO2H]2 Molecular Weight:396.35Ordering Information。

埃尔曼的试剂,5,5'二硫代双-(二硝基苯甲酸),5克分子量:396.35CAS号:69-78-3使用半胱氨酸标准精确量化巯基程序材料的制备1 反应缓冲液:0.1M的磷酸钠,pH 8.0,含有1 mM的EDTA半胱氨酸标准品,分子量136.2 :配成一定浓度梯度3 Ellman试剂溶液:1mL反应缓冲液4毫克溶解DTNB程序3在各试管中加入250μL各浓度的标准工作液或待测物溶液注:对于未知的样品需要稀释,以便使其浓度标准曲线的工作范围之内(理想的浓度为0.1-1.0)。
4在室温混合和反应15分钟。
在412 nm处测量吸光度。
根据得到数值生成一个标准曲线,测定待测样品由标准曲线计算SH含量摩尔吸光系数的程序精确量化的巯基的材料的制备1 反应缓冲液:0.1M的磷酸钠,pH 8.0,含有1 mM的EDTAEllman试剂溶液:1mL反应缓冲液4毫克溶解DTNB测量吸光度去若干试管,每管加入50μL的Ellman试剂溶液和2.5mL反应缓冲液。
加入250μL待测样品,空白添加250μL反应缓冲液在室温混合和反应15分钟。
分光光度计412nm测定吸光度。
根据TNB的摩尔消光系数(14,150)计算巯基含量该国能在412nm的合成,有一个相对比较激烈的吸光度同时二硫化物。
由于蛋白质的巯基,以国能形成化学计量为1:1,国能形成可以用来评估硫醇数目。
在变性剂的情况下,唯一能够找到的硫醇的反应,而残留的chaotropic代理人在场的总数减少胱氨酸目前可以衡量的。
经处理后减少的蛋白质与chaotropes及DTNB能够产生的半胱氨酸总数(半胱氨酸巯基加半胱氨酸-β-半胱氨酸)。
- -反应是敏感的碱性pH值(俄亥俄州)与RS竞争),酸性pH值(二硫化物可以打破),氧(R的巯基再氧化),以及温度(热致变色)。
因此,通常的反应是进行了过多的DTNB的蛋白质,在中性pH值固定的温度,erature,有时在厌氧条件。

E L L M A N试剂法测定自由巯基和二硫键This manuscript was revised by the office on December 22, 2012E L L M A N试剂测定自由巯基试验基于的原理:5,5’-dithiobis-2-nitrobenzoicacid(DTNB)5,5-二硫基-双(2-硝基苯甲酸)5,5-二硫基-双(2-硝基苯甲酸)(DTNB)在412nm没有吸收,与巯基反应后,生成2-硝基-5-巯基苯甲酸(TNB)[1]。
TNB2-在412nm有很强的吸收,可以用于对肽段的自由巯基进行定量分析[2]。
DTNBTNB2-根据文献记载,TNB的吸光系数在13.6*103M-cm-~14.25*103M-cm-之间[3,4]。
吸光度测量的最灵敏范围在0.2-0.7之间。
A=εbc,其中A为吸光度,ε是摩尔吸收光系数或消光系数,ε单位为升/(摩尔·厘米)[L/(mol·cm)]。
以吸光度下限0.2来计算(吸光系数取14.15*103M-cm-),需要TNB的浓度为c=0.2/(14.15*103LM-cm-*1cm)=1.4*10-5mol/L(1.4*10-8mol/ml),需要蛋白浓度为1.4*10-5mol/L*18790g/mol=0.2631g/L=0.2631mg/ml.我们的条件可以达到这个检测限度。
ELLMAN试剂法测定自由巯基主要的影响因素有:1.EDTA的适量加入有助于TNB显色的稳定和成梯度线性关系[5]。
2.在不同缓冲液中,TNB的最大吸收波长略微不同,所以它们在412nm的吸收也不3.同,要根据选择的缓冲液来确定[5]。
另外,TNB的分光光度法分析对SDS很敏感[6]。
4.DTNB随着pH的升高,降解速度加快。
在pH7.0,其降解速度为0.02%/h,在5.pH值8.0,其降解速度为0.2%/h,随着pH值得升高,降解速度加快,在pH12时,15min之内会完全降解[7,8]。
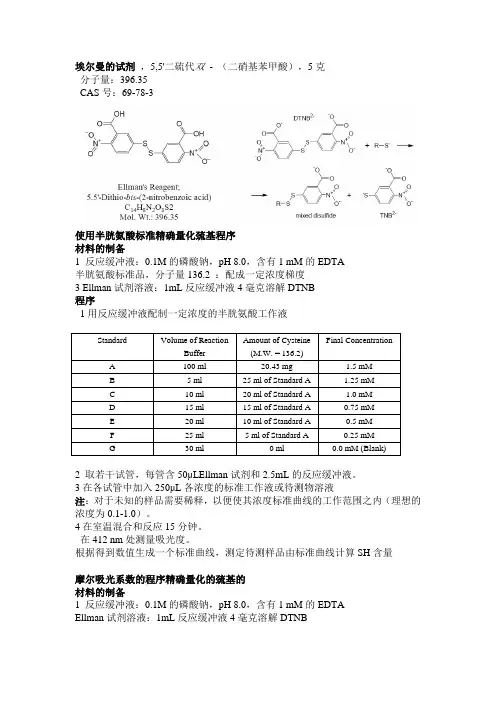
埃尔曼的试剂,5,5'二硫代双- (二硝基苯甲酸),5克分子量:396.35CAS号:69-78-3使用半胱氨酸标准精确量化巯基程序材料的制备1 反应缓冲液:0.1M的磷酸钠,pH 8.0,含有1 mM的EDTA半胱氨酸标准品,分子量136.2 :配成一定浓度梯度3 Ellman试剂溶液:1mL反应缓冲液4毫克溶解DTNB程序1用反应缓冲液配制一定浓度的半胱氨酸工作液2 取若干试管,每管含50μL Ellman试剂和2.5mL的反应缓冲液。
3在各试管中加入250μL各浓度的标准工作液或待测物溶液注:对于未知的样品需要稀释,以便使其浓度标准曲线的工作范围之内(理想的浓度为0.1-1.0)。
4在室温混合和反应15分钟。
在412 nm处测量吸光度。
根据得到数值生成一个标准曲线,测定待测样品由标准曲线计算SH含量摩尔吸光系数的程序精确量化的巯基的材料的制备1 反应缓冲液:0.1M的磷酸钠,pH 8.0,含有1 mM的EDTAEllman试剂溶液:1mL反应缓冲液4毫克溶解DTNB测量吸光度去若干试管,每管加入50μL的Ellman试剂溶液和2.5mL反应缓冲液。
加入250μL待测样品,空白添加250μL反应缓冲液在室温混合和反应15分钟。
分光光度计412nm测定吸光度。
根据TNB的摩尔消光系数(14,150)计算巯基含量该国能在412nm的合成,有一个相对比较激烈的吸光度同时二硫化物。
由于蛋白质的巯基,以国能形成化学计量为1:1,国能形成可以用来评估硫醇数目。
在变性剂的情况下,唯一能够找到的硫醇的反应,而残留的chaotropic代理人在场的总数减少胱氨酸目前可以衡量的。
经处理后减少的蛋白质与chaotropes及DTNB能够产生的半胱氨酸总数(半胱氨酸巯基加半胱氨酸-β-半胱氨酸)。
- -反应是敏感的碱性pH值(俄亥俄州)与RS竞争),酸性pH值(二硫化物可以打破),氧(R的巯基再氧化),以及温度(热致变色)。

E L L M试剂法测定自由巯基和二硫键Prepared on 22 November 2020ELLMAN试剂测定自由巯基试验基于的原理:5,5’-dithiobis-2-nitrobenzoicacid(DTNB)5,5-二硫基-双(2-硝基苯甲酸)5,5-二硫基-双(2-硝基苯甲酸)(DTNB)在412nm没有吸收,与巯基反应后,生成2-硝基-5-巯基苯甲酸(TNB)[1]。
TNB2-在412nm有很强的吸收,可以用于对肽段的自由巯基进行定量分析[2]。
DTNBTNB2-根据文献记载,TNB的吸光系数在*103M-cm-~*103M-cm-之间[3,4]。
吸光度测量的最灵敏范围在之间。
A=εbc,其中A为吸光度,ε是摩尔吸收光系数或消光系数,ε单位为升/(摩尔·厘米)[L/(mol·cm)]。
以吸光度下限来计算(吸光系数取*103M-cm-),需要TNB的浓度为c=(*103LM-cm-*1cm)=*10-5mol/L*10-8mol/ml),需要蛋白浓度为*10-5mol/L*18790g/mol=L=ml.我们的条件可以达到这个检测限度。
ELLMAN试剂法测定自由巯基主要的影响因素有:1.EDTA的适量加入有助于TNB显色的稳定和成梯度线性关系[5]。
2.在不同缓冲液中,TNB的最大吸收波长略微不同,所以它们在412nm的吸收也不3.同,要根据选择的缓冲液来确定[5]。
另外,TNB的分光光度法分析对SDS很敏感[6]。
4.DTNB随着pH的升高,降解速度加快。
在,其降解速度为%/h,在5.pH值,其降解速度为%/h,随着pH值得升高,降解速度加快,在pH12时,15min之内会完全降解[7,8]。
6.摩尔吸收光系数在不同的温度下不同,随温度的升高而下降[4].试验方案主要材料:1.材料PEG-G-CSF批号:080229浓度mlG-CSF批号:080126浓度ml10k超滤膜PALL2.试剂SequencingGradeModifiedTrypsin,Promega,lot#237826。

ELLMAN试剂测定自由巯基试验基于的原理:5,5’-dithiobis-2-nitrobenzoic acid (DTNB) 5,5-二硫基-双(2-硝基苯甲酸) 5,5-二硫基-双(2-硝基苯甲酸)(DTNB)在412nm没有吸收,与巯基反应后,生成2-硝基-5-巯基苯甲酸(TNB)[1]。
TNB2-在412nm有很强的吸收,可以用于对肽段的自2-吸光度0.2来计算-*1cm)1.4*101.2.不3.同,要根据选择的缓冲液来确定[5]。
另外,TNB的分光光度法分析对SDS很敏感[6]。
4.DTNB随着pH的升高,降解速度加快。
在pH7.0,其降解速度为0.02%/h,在5.pH值8.0,其降解速度为0.2%/h,随着pH值得升高,降解速度加快,在pH 12时,15min之内会完全降解[7,8]。
6.摩尔吸收光系数在不同的温度下不同,随温度的升高而下降[4].试验方案主要材料:1.材料PEG-G-CSF 批号:080229 浓度4.32mg/mlG-CSF 批号:080126 浓度6.9mg/ml小瓶。
NOB液:0.1%TFA/90%乙腈/H2O3.仪器质谱仪:BRUKER DALTONICS MALTI-TOF-TOF autoflexⅢ(厂内编号KC2007-011)Beckman 22R台式离心机(厂内编号AM-039)Beckman DU-800 紫外分光光度计(厂内编号KC2007-005)恒温循环仪:JULABO F12-ED(厂内编号KC2008-003)反相柱:Symmetry C18 5um 300à高压液相仪器:,(UV/Visible Detector)试验过程:一、缓冲液替换PEG-G-CSF和G-CSF进行缓冲液替换,超滤替换缓冲液为50mM NH4HCO3,稀释中加入G-CSF+DTT相分离收样:SF+DTT相分离集到之间的交由崔文喜冻干四、ELLMAN试剂测定自由巯基由于收集到的PEG肽段已经是自由巯基,所以可以跳过还原二硫键这一步。

E L L M A N试剂法测定自由巯基和二硫键标准化工作室编码[XX968T-XX89628-XJ668-XT689N]E L L M A N试剂测定自由巯基试验基于的原理:5,5’-dithiobis-2-nitrobenzoicacid(DTNB)5,5-二硫基-双(2-硝基苯甲酸)5,5-二硫基-双(2-硝基苯甲酸)(DTNB)在412nm没有吸收,与巯基反应后,生成2-硝基-5-巯基苯甲酸(TNB)[1]。
TNB2-在412nm有很强的吸收,可以用于对肽段的自由巯基进行定量分析[2]。
DTNBTNB2-根据文献记载,TNB的吸光系数在13.6*103M-cm-~14.25*103M-cm-之间[3,4]。
吸光度测量的最灵敏范围在0.2-0.7之间。
A=εbc,其中A为吸光度,ε是摩尔吸收光系数或消光系数,ε单位为升/(摩尔·厘米)[L/(mol·cm)]。
以吸光度下限0.2来计算(吸光系数取14.15*103M-cm-),需要TNB的浓度为c=0.2/(14.15*103LM-cm-*1cm)=1.4*10-5mol/L(1.4*10-8mol/ml),需要蛋白浓度为1.4*10-5mol/L*18790g/mol=0.2631g/L=0.2631mg/ml.我们的条件可以达到这个检测限度。
ELLMAN试剂法测定自由巯基主要的影响因素有:1.EDTA的适量加入有助于TNB显色的稳定和成梯度线性关系[5]。
2.在不同缓冲液中,TNB的最大吸收波长略微不同,所以它们在412nm的吸收也不3.同,要根据选择的缓冲液来确定[5]。
另外,TNB的分光光度法分析对SDS很敏感[6]。
4.DTNB随着pH的升高,降解速度加快。
在pH7.0,其降解速度为0.02%/h,在5.pH值8.0,其降解速度为0.2%/h,随着pH值得升高,降解速度加快,在pH12时,15min之内会完全降解[7,8]。

埃尔曼的试剂,5,5'二硫代双-(二硝基苯甲酸),5克分子量:CAS号:69-78-3使用半胱氨酸标准精确量化巯基程序材料的制备1 反应缓冲液:0.1M的磷酸钠,pH ,含有1 mM的EDTA半胱氨酸标准品,分子量:配成一定浓度梯度3 Ellman试剂溶液:1mL反应缓冲液4毫克溶解DTNB程序3在各试管中加入250μL各浓度的标准工作液或待测物溶液注:对于未知的样品需要稀释,以便使其浓度标准曲线的工作范围之内(理想的浓度为)。
4在室温混合和反应15分钟。
在412 nm处测量吸光度。
根据得到数值生成一个标准曲线,测定待测样品由标准曲线计算SH含量摩尔吸光系数的程序精确量化的巯基的材料的制备1 反应缓冲液:0.1M的磷酸钠,pH ,含有1 mM的EDTAEllman试剂溶液:1mL反应缓冲液4毫克溶解DTNB测量吸光度去若干试管,每管加入50μL的Ellman试剂溶液和反应缓冲液。
加入250μL待测样品,空白添加250μL反应缓冲液在室温混合和反应15分钟。
分光光度计412nm测定吸光度。
根据TNB的摩尔消光系数(14,150)计算巯基含量该国能在412nm的合成,有一个相对比较激烈的吸光度同时二硫化物。
由于蛋白质的巯基,以国能形成化学计量为1:1,国能形成可以用来评估硫醇数目。
在变性剂的情况下,唯一能够找到的硫醇的反应,而残留的chaotropic代理人在场的总数减少胱氨酸目前可以衡量的。
经处理后减少的蛋白质与chaotropes及DTNB能够产生的半胱氨酸总数(半胱氨酸巯基加半胱氨酸-β-半胱氨酸)。
- -反应是敏感的碱性pH值(俄亥俄州)与RS竞争),酸性pH值(二硫化物可以打破),氧(R的巯基再氧化),以及温度(热致变色)。
因此,通常的反应是进行了过多的DTNB的蛋白质,在中性pH值固定的温度,erature,有时在厌氧条件。
此外,国能是敏感的各种离子的缓冲,所以采用消光系数硫醇数量计算必须正确匹配的反应条件。
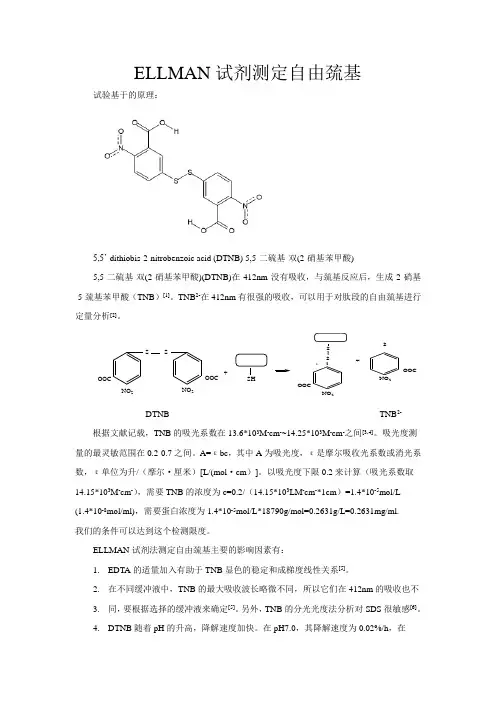
ELLMAN 试剂测定自由巯基试验基于的原理:5,5’-dithiobis-2-nitrobenzoic acid (DTNB) 5,5-二硫基-双(2-硝基苯甲酸)5,5-二硫基-双(2-硝基苯甲酸)(DTNB)在412nm 没有吸收,与巯基反应后,生成2-硝基-5-巯基苯甲酸(TNB )[1]。
TNB 2-在412nm 有很强的吸收,可以用于对肽段的自由巯基进行定量分析[2]。
SS NO 2NO 2-OOC-OOC+SH S -SNO 2NO 2-OOC-OOC+SDTNB TNB 2- 根据文献记载,TNB 的吸光系数在13.6*103M -cm -~14.25*103M -cm -之间[3,4]。
吸光度测量的最灵敏范围在0.2-0.7之间。
A=εbc ,其中A 为吸光度,ε是摩尔吸收光系数或消光系数,ε单位为升/(摩尔·厘米)[L/(mol ·cm )]。
以吸光度下限0.2来计算(吸光系数取14.15*103M -cm -),需要TNB 的浓度为c=0.2/(14.15*103LM -cm -*1cm )=1.4*10-5mol/L (1.4*10-8mol/ml),需要蛋白浓度为1.4*10-5mol/L*18790g/mol=0.2631g/L=0.2631mg/ml. 我们的条件可以达到这个检测限度。
ELLMAN 试剂法测定自由巯基主要的影响因素有:1. EDTA 的适量加入有助于TNB 显色的稳定和成梯度线性关系[5]。
2. 在不同缓冲液中,TNB 的最大吸收波长略微不同,所以它们在412nm 的吸收也不3. 同,要根据选择的缓冲液来确定[5]。
另外,TNB 的分光光度法分析对SDS 很敏感[6]。
4. DTNB 随着pH 的升高,降解速度加快。
在pH7.0,其降解速度为0.02%/h ,在5.pH值8.0,其降解速度为0.2%/h,随着pH值得升高,降解速度加快,在pH 12时,15min之内会完全降解[7,8]。
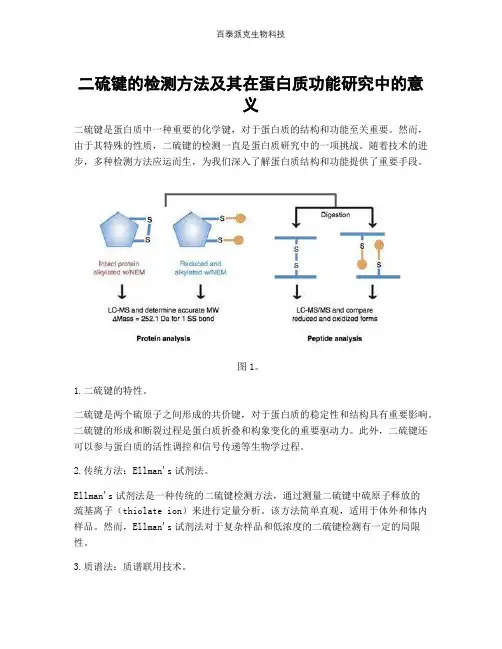
二硫键的检测方法及其在蛋白质功能研究中的意义二硫键是蛋白质中一种重要的化学键,对于蛋白质的结构和功能至关重要。
然而,由于其特殊的性质,二硫键的检测一直是蛋白质研究中的一项挑战。
随着技术的进步,多种检测方法应运而生,为我们深入了解蛋白质结构和功能提供了重要手段。
图1。
1.二硫键的特性。
二硫键是两个硫原子之间形成的共价键,对于蛋白质的稳定性和结构具有重要影响。
二硫键的形成和断裂过程是蛋白质折叠和构象变化的重要驱动力。
此外,二硫键还可以参与蛋白质的活性调控和信号传递等生物学过程。
2.传统方法:Ellman's试剂法。
Ellman's试剂法是一种传统的二硫键检测方法,通过测量二硫键中硫原子释放的巯基离子(thiolate ion)来进行定量分析。
该方法简单直观,适用于体外和体内样品。
然而,Ellman's试剂法对于复杂样品和低浓度的二硫键检测有一定的局限性。
3.质谱法:质谱联用技术。
质谱联用技术(MS)在二硫键检测中发挥着重要作用。
通过将质谱与色谱等分离技术联用,可以实现对蛋白质样品中二硫键的鉴定和定量分析。
质谱法具有高灵敏度、高分辨率和高准确性的优势,可以应用于复杂样品和低浓度的二硫键检测。
4.分子探针法:缺硫共轭体探针。
缺硫共轭体探针是一种基于分子探针的二硫键检测方法。
该方法利用硫醚键的反应特性,通过缺硫共轭体探针与二硫键发生反应产生荧光信号来实现二硫键的定量分析。
这种方法对于体内的二硫键检测具有优势,并且可以应用于活细胞和动物模型中的研究。
5.二硫键在蛋白质功能研究中的意义。
二硫键在蛋白质功能研究中具有重要意义。
通过揭示二硫键的形成、断裂和调控机制,我们可以深入了解蛋白质折叠和构象变化的过程,以及蛋白质的功能调控。
此外,二硫键还与一些蛋白质疾病的发生和药物开发密切相关,为相关疾病的诊断和治疗提供了新的思路和靶点。
二硫键的检测方法为我们深入了解蛋白质结构和功能提供了重要的工具和手段。

E L L M A N试剂测定自由巯基试验基于的原理:5,5’-dithiobis-2-nitrobenzoicacid(DTNB)5,5-二硫基-双(2-硝基苯甲酸)5,5-二硫基-双(2-硝基苯甲酸)(DTNB)在412nm没有吸收,与巯基反应后,生成2-硝基-5-巯基苯甲酸(TNB)[1]。
TNB2-在412nm有很强的吸收,可以用于对肽段的自由巯基进行定量分析[2]。
DTNBTNB2-根据文献记载,TNB的吸光系数在13.6*103M-cm-~14.25*103M-cm-之间[3,4]。
吸光度测量的最灵敏范围在0.2-0.7之间。
A=εbc,其中A为吸光度,ε是摩尔吸收光系数或消光系数,ε单位为升/(摩尔·厘米)[L/(mol·cm)]。
以吸光度下限0.2来计算(吸光系数取14.15*103M-cm-),需要TNB的浓度为c=0.2/(14.15*103LM-cm-*1cm)=1.4*10-5mol/L(1.4*10-8mol/ml),需要蛋白浓度为1.4*10-5mol/L*18790g/mol=0.2631g/L=0.2631mg/ml.我们的条件可以达到这个检测限度。
ELLMAN试剂法测定自由巯基主要的影响因素有:1.EDTA的适量加入有助于TNB显色的稳定和成梯度线性关系[5]。
2.在不同缓冲液中,TNB的最大吸收波长略微不同,所以它们在412nm的吸收也不3.同,要根据选择的缓冲液来确定[5]。
另外,TNB的分光光度法分析对SDS很敏感[6]。
4.DTNB随着pH的升高,降解速度加快。
在pH7.0,其降解速度为0.02%/h,在5.pH值8.0,其降解速度为0.2%/h,随着pH值得升高,降解速度加快,在pH12时,15min之内会完全降解[7,8]。
6.摩尔吸收光系数在不同的温度下不同,随温度的升高而下降[4].试验方案主要材料:1.材料PEG-G-CSF批号:080229浓度4.32mg/mlG-CSF批号:080126浓度6.9mg/ml10k超滤膜PALL2.试剂SequencingGradeModifiedTrypsin,Promega,lot#237826。
首先制作半胱氨酸标准曲线,再用紫外分光光度法测定样品吸光度,计算出疏基含量,最终得出修饰率。
1、制作标准曲线:
缓冲液的配制:称取0.254gNaH2PO4与10.162gNa2HPO4于500ml容量瓶中,用
超纯水溶解,加入148.896mg的EDTA(乙二胺四乙酸),使其完全溶解,定容成500ml。
Ellman试剂的配制:称取4mgDTNB溶解在1ml缓冲液中。
取7只试管,分别在每只试管内加入50μL Ellman试剂与2.5ml磷酸钠缓冲溶液,混匀后,再在各试管内加入50μL标准溶液,混合均匀,在室温放置15min,以溶液G为空白,于波长412nm处测定半胱氨酸标准液的吸光度值(A),如表9所示:
制作标准曲线如图10所示。
得标准曲线方程为y=0.1692x-0.0001,R2=09994,满足要求。
2、测量半胱氨酸透明质酸结合物的修饰率:
配制样品溶液:称取10.5mg半胱氨酸透明质酸结合物(含0.0274mmol伯醇羟基)用缓冲液溶解并定容至5ml;
配制空白对照溶液:称取10.5mg透明质酸(含0.0274mmol伯醇羟基)用缓冲液溶解并定容至5ml;
取2只试管,分别在每支试管内加入50μL Ellman试剂与2.5ml磷酸钠缓冲溶液,混匀后,再在各试管内加入50μL待测样品,混合均匀,在室温放置15min,以透明质酸溶液做空白,于波长412nm处测定待测样品的吸光度值(A),如表10所示:
利用标准曲线和测得的样品溶液吸光度,计算样品中巯基的含量。
带入标准曲线计算:0.0385=0.1692x-0.0001,得出修饰率为3.5%(巯基数相对于透明质酸的双糖单位数)。
6-氮杂-2-硫代胸腺嘧啶(Ellman's reagent)是一种常用的生物化学试剂,广泛用于蛋白质还原和巯基含量的测定。
它的分子式为C9H9N3O2S,具有类似于Elliott's reagent B的结构。
在生物化学实验中,Ellman's reagent可用于测定蛋白质中的巯基含量,也可以作为生物分子的还原剂。
本文将对Ellman's reagent的化学性质、用途、合成方法以及注意事项进行系统总结。
1. 化学性质Ellman's reagent,又称5,5'-二硫代二硫代酸戊二醛(5,5'-dithiobis(2-nitrobenzoic acid),DTNB)是一种黄色晶体,不溶于水,但溶于乙醇和氢氧化钠溶液。
它在乙醇中呈现出橙黄色,而在碱性条件下呈现出明显的红色。
Ellman's reagent具有很强的吸光性,其在pH8.0条件下的吸光峰为412nm。
2. 用途Ellman's reagent主要用于测定蛋白质中的巯基含量。
在这种测定方法中,Ellman's reagent与蛋白质中的巯基反应生成硫醇盐,从而产生黄色溶液。
通过测定溶液的吸光度,可以计算出蛋白质中巯基的含量。
Ellman's reagent还可作为生物分子的还原剂,参与生物化学实验中的还原反应。
3. 合成方法Ellman's reagent的合成方法相对简单,通常采用以下步骤:- 将硝基苯酚和二氯丙酮反应制备二硝基二苯醚;- 将二硝基二苯醚与硫化氢反应,生成芳香二硫醚;- 将芳香二硫醚与溴乙酸酰乙酯反应,生成Ellman's reagent。
4. 注意事项在使用Ellman's reagent进行巯基含量测定时,需注意以下事项:- 操作需在洁净的实验室条件下进行,避免其受到杂质的污染;- 测定过程中需控制好pH值,否则可能影响测定结果的准确性;- 暴露于光线下会导致Ellman's reagent失去活性,使用过程中需避光保存。
gattermann法-回复Gattermann法,是一种有机合成方法,主要用于合成含有卤素取代基的芳香化合物。
其基本原理是通过在芳香化合物上引入卤素取代基,从而实现目标分子的合成。
Gattermann法的步骤分为以下几个部分。
首先,准备好所需的原料和试剂。
Gattermann法所需的原料主要包括芳香化合物、卤代物和酰基化试剂。
芳香化合物可以是苯或其它含有芳环的化合物。
卤代物可以是卤代烷或卤代酰基。
酰基化试剂常用的有氯化亚铁(FeCl3)和氯甲酸(声明:该化合物属于乙酸类)。
确保所有试剂和溶剂均为干燥的,以避免不必要的副反应。
接下来,准备反应体系。
首先,在干燥的环境中,将芳香化合物、卤代物和酰基化试剂放入干燥的圆底烧瓶中。
这一步骤需要仔细控制实验室的温度和湿度,避免试剂受到空气中的水分和杂质影响。
然后,加入适量的干燥剂,如氯化钙或氯化钠,以吸收反应中产生的水分。
最后,将烧瓶与冷凝管连接起来,以防止反应物的挥发。
然后,进行反应。
首先,将烧瓶放入加热设备中,加热到适当的温度,一般在60-70摄氏度。
同时,冷却冷凝管,以保证反应产生的气体能够冷凝并回流到烧瓶中。
随着反应进行,可以观察到烧瓶中气泡的产生,表明反应正在进行中。
当反应结束后,停止加热并冷却烧瓶。
然后,将反应混合物转移到一个试剂瓶中,并对其进行抽滤,以去除产生的沉淀物。
抽滤过程可以使用玻璃吸滤漏斗和适当大小的滤纸进行。
接下来,对产物进行分离和提纯。
通常,产物可以通过蒸馏、结晶或柱层析等分离方法进行提纯。
蒸馏是其中常用的方法,通过控制温度和压力,将反应产物从混合物中分离出来。
结晶则是通过溶剂的添加或温度的改变,使反应产物从溶液中结晶出来。
而柱层析则是通过反应物在固定相和流动相之间的分配系数不同,从而实现分离。
选择合适的方法进行分离和提纯,可以得到纯度较高的目标产物。
最后,对产物进行表征和鉴定。
利用各种分析技术,如核磁共振(NMR)、红外光谱(FT-IR)和质谱(MS)等,对合成的产物进行表征和鉴定。
首先制作半胱氨酸标准曲线,再用紫外分光光度法测定样品吸光度,计算出疏基含量,最终得出修饰率。
1、制作标准曲线:
缓冲液的配制:称取0.254gNaH2PO4与10.162gNa2HPO4于500ml容量瓶中,用
超纯水溶解,加入148.896mg的EDTA(乙二胺四乙酸),使其完全溶解,定容成500ml。
Ellman试剂的配制:称取4mgDTNB溶解在1ml缓冲液中。
取7只试管,分别在每只试管内加入50μL Ellman试剂与2.5ml磷酸钠缓冲溶液,混匀后,再在各试管内加入50μL标准溶液,混合均匀,在室温放置15min,以溶液G为空白,于波长412nm处测定半胱氨酸标准液的吸光度值(A),如表9所示:
制作标准曲线如图10所示。
得标准曲线方程为y=0.1692x-0.0001,R2=09994,满足要求。
2、测量半胱氨酸透明质酸结合物的修饰率:
配制样品溶液:称取10.5mg半胱氨酸透明质酸结合物(含0.0274mmol伯醇羟基)用缓冲液溶解并定容至5ml;
配制空白对照溶液:称取10.5mg透明质酸(含0.0274mmol伯醇羟基)用缓冲液溶解并定容至5ml;
取2只试管,分别在每支试管内加入50μL Ellman试剂与2.5ml磷酸钠缓冲溶液,混匀后,再在各试管内加入50μL待测样品,混合均匀,在室温放置15min,以透明质酸溶液做空白,于波长412nm处测定待测样品的吸光度值(A),如表10所示:
利用标准曲线和测得的样品溶液吸光度,计算样品中巯基的含量。
带入标准曲线计算:0.0385=0.1692x-0.0001,得出修饰率为3.5%(巯基数相对于透明质酸的双糖单位数)。