镁的制取制作
- 格式:ppt
- 大小:5.11 MB
- 文档页数:26


皮江法炼镁的工艺流程及其优缺点(来源:全球五金网日期:2010-6-9 点击:95 )镁的冶炼方法总体上可分成三种:一种是电解法;一种是硅热法(皮江法);另一种是碳热法。
皮江法炼镁的主要工艺流程是:白云石在回转窑或立窑中煅烧成煅白,经破碎后与硅铁粉(含硅75%)和萤石粉(含GaF2)=95%)混合均匀制团,装入耐热不锈钢还原罐内,置于还原炉中,在1200-1250℃及真空的1.33Pa 真空度下还原制取粗镁,经过熔剂精制、铸锭、表面处理得到成品镁锭。
皮江法炼镁是中国现行普遍应用的一种方法:其优点是:1、规模能大能小,原材料可就地取材;2、成本相对电解法较低;3、技术不难掌握;4、在九十年代经济效益可观;5、镁的等级质量略高于电解镁等。
皮江法炼镁缺点:生产1 吨金属镁锭需要有消耗白云石12-14吨;无烟煤及烟煤8-10吨;副产还原渣5-6吨,这些还原渣目前还没有发现更好的用途,污染环境;劳动强度大,原料车间粉尘污染严重。
镍含量太低,如要回收用浮选法,但杂质镁可能不易控制。
一般工厂用什么冶炼镁,对人体有害吗?答:有害。
镁是在自然界中分布最广的十个元素之一,但由于它不易从化合物中还原成单质状态,所以迟迟未被发现。
长时期里,化学家们将从含碳酸镁的菱镁矿焙烧获得的镁的氧化物苦土当作是不可再分割的物质。
在1789年拉瓦锡发表的元素表中就列有它。
1808年,戴维在成功制得钙以后,使用同样的办法又成功的制得了金属镁。
从此镁被确定为元素,并被命名为magnesium,元素符号是Mg。
镁是一种参与生物体正常生命活动及新陈代谢过程必不可少的元素。
镁影响细胞的多种生物功能:影响钾离子和钙离子的转运,调控信号的传递,参与能量代谢、蛋白质和核酸的合成;可以通过络合负电荷基团,尤其核苷酸中的磷酸基团来发挥维持物质的结构和功能;催化酶的激活和抑制及对细胞周期、细胞增殖及细胞分化的调控;镁还参与维持基因组的稳定性,并且还与机体氧化应激和肿瘤发生有关。


工业上制取镁单质的方法-概述说明以及解释1.引言1.1 概述概述:镁是一种轻质金属,具有良好的机械性能和热传导性能,因此在航天、汽车和电子等领域具有重要的应用价值。
镁单质是镁的一种基本形态,其制备方法对镁材料的质量和性能具有重要影响。
本文将介绍工业上制取镁单质的方法,并探讨其在工业应用中的重要性。
部分的内容1.2 文章结构文章结构包括引言、正文和结论三部分。
引言部分主要是对文章的主题进行概述,介绍文章的目的和意义,引出文章要讨论的内容,为读者提供一个整体的了解和预期。
正文部分是文章的主体,包括镁单质的重要性、制取镁单质的方法和工业应用等内容,详细介绍了镁单质的相关知识和制备方法,以及其在工业上的具体应用和意义。
结论部分对全文进行总结,展望未来的发展方向并给出具体的结论,对全文进行一个概括性的总结和升华,为读者留下深刻的印象。
1.3 目的本文旨在探讨工业上制取镁单质的方法,并对其重要性和工业应用进行深入分析。
通过对制取镁单质的方法进行全面介绍,可以帮助读者了解镁单质在工业生产中的关键作用,以及如何高效地制取镁单质。
同时,本文也旨在展望镁单质在未来工业应用中的潜力,为读者提供对镁单质制取方法的深入了解和未来发展的展望。
通过本文的阐述,读者可以更加全面地了解镁单质的制取方法,以及其在工业中的重要性和应用前景。
2.正文2.1 镁单质的重要性镁是一种轻质金属,具有很高的比强度和耐蚀性,是工业上使用最广泛的金属之一。
镁单质在工业生产中具有重要的作用,主要体现在以下几个方面:首先,镁单质在航空航天领域有着重要的应用。
由于镁的密度只有铝的2/3,而且具有很高的强度和刚度,因此在航空航天领域被广泛应用于制造飞机、火箭和航天器的结构材料。
其次,镁单质在汽车工业中也有着重要的地位。
镁合金由于其优异的加工性能、抗冲击性和轻质化特性,被广泛应用于汽车发动机、变速箱、车身结构和其他部件的制造中,有助于提高汽车的燃油经济性和减轻整车此外,镁单质还被广泛用于电子设备、高铁和轻型化设备的制造中,其特殊的物理和化学性质使得其在这些领域具有独特的优势。

镁的冶炼方法
镁是一种轻质金属,具有良好的机械性能和耐腐蚀性能,因此在航空航天、汽车制造、电子产品等领域有着广泛的应用。
镁的冶炼方法主要包括熔炼法、电解法和气相法等多种方式。
首先,熔炼法是镁的传统冶炼方法之一。
这种方法是将镁矿石与还原剂(通常是焦炭)放入电炉或熔炼炉中进行高温熔炼,通过还原反应将镁矿石中的氧化镁还原成金属镁。
这种方法适用于镁矿石含量较高的原料,但能耗较高,同时还需处理炉渣等问题,因此在工业生产中逐渐被电解法所取代。
其次,电解法是目前镁的主要冶炼方法之一。
这种方法是将氯化镁溶解在熔融的氯化钠中,通过电解还原制取金属镁。
相比于熔炼法,电解法具有能耗低、生产效率高、产品纯度高等优点,因此在工业生产中得到广泛应用。
但是,电解法也存在着设备投资大、操作技术要求高等问题,需要在实际生产中加以克服。
另外,气相法是近年来发展起来的一种新型镁冶炼方法。
这种方法是将气态的镁化合物在高温下分解,通过化学反应制取金属镁。
气相法具有生产过程简单、能耗低、环境友好等特点,逐渐成为镁冶炼领域的研究热点。
然而,气相法在工业应用中还存在着工艺参数控制难、设备成本高等问题,需要进一步完善和改进。
总的来说,镁的冶炼方法多种多样,每种方法都有其特点和适用范围。
在实际生产中,需要根据原料资源、工艺条件、产品要求等因素选择合适的冶炼方法,并不断进行技术改进和创新,以提高生产效率、降低能耗、改善产品质量,推动镁工业的可持续发展。
在未来,随着科技的不断进步和工艺的不断完善,相信镁的冶炼方法会更加多样化和高效化,为镁材料的生产和应用开辟更广阔的空间。


镁的工艺流程
镁是一种重要的金属材料,具有较低的密度、良好的机械性能和优异的耐腐蚀性能,因此在航空航天、汽车制造、电子产品等领域有着广泛的应用。
镁的工艺流程主要包括矿石选矿、冶炼和精炼三个主要环节。
首先是矿石选矿。
镁的主要矿石有菱镁矿、莫来石、菱镁矿、白云石等。
在选矿过程中,需要将矿石进行破碎、磨矿、浮选等步骤,以提高矿石的品位和回收率。
矿石选矿的质量直接影响到后续冶炼过程的效果,因此选矿工艺的优化对于提高生产效率和降低成本非常重要。
接下来是冶炼过程。
镁的冶炼主要采用炼镁法和电解法两种工艺。
炼镁法是将镁矿石与石灰石或白云石等碱性矿石混合,在高温下还原制取金属镁。
电解法则是将氯化镁溶解在熔融的氯化钾中,通过电解制取金属镁。
两种方法各有优劣,具体选择取决于原料资源、能源成本、环保要求等因素。
最后是精炼过程。
镁的精炼主要包括真空蒸馏、电解铅法、气相炼镁等方法。
通过精炼过程可以去除镁中的杂质,提高镁的纯度
和质量。
精炼过程对于提高镁的机械性能和耐腐蚀性能起着至关重要的作用。
在镁的工艺流程中,需要注意控制生产过程中的温度、压力、气氛等参数,确保产品的质量稳定。
此外,还需要重视环保和安全生产,减少废气、废水的排放,确保生产过程安全可靠。
总的来说,镁的工艺流程是一个复杂而严谨的过程,需要多方面的技术和经验的积累。
只有不断优化工艺流程,提高生产效率和产品质量,才能更好地满足市场需求,推动镁材料产业的发展。
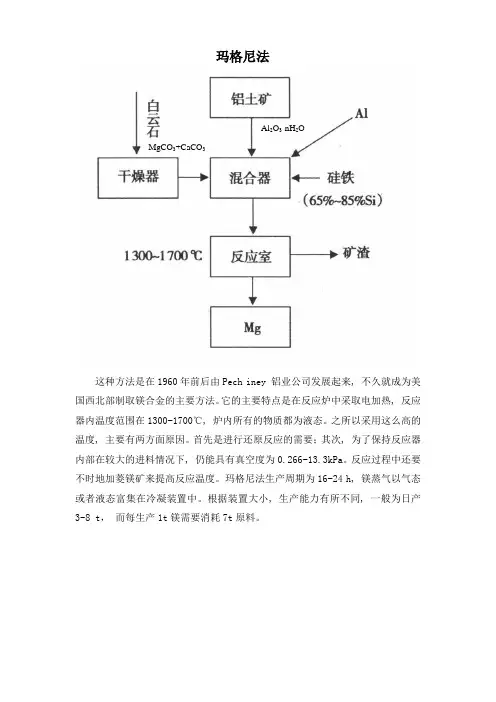
玛格尼法
Al2O3·nH2O
MgCO3+CaCO3
这种方法是在1960年前后由Pech iney 铝业公司发展起来, 不久就成为美国西北部制取镁合金的主要方法。
它的主要特点是在反应炉中采取电加热, 反应器内温度范围在1300~1700℃, 炉内所有的物质都为液态。
之所以采用这么高的温度, 主要有两方面原因。
首先是进行还原反应的需要;其次, 为了保持反应器内部在较大的进料情况下, 仍能具有真空度为0.266~13.3kPa。
反应过程中还要不时地加菱镁矿来提高反应温度。
玛格尼法生产周期为16~24 h, 镁蒸气以气态或者液态富集在冷凝装置中。
根据装置大小, 生产能力有所不同, 一般为日产3~8 t,而每生产1t镁需要消耗7t原料。

海水制镁五个化学方程式全文共四篇示例,供读者参考第一篇示例:海水中的镁是一种十分重要的元素,它不仅在海水中存在丰富,还在人类的生活中发挥着重要的作用。
制备海水中的镁元素可以通过化学方法来实现,下面我们就来看看海水制镁的五个化学方程式。
1. 氢氧化镁和氯化钠生成氯化镁和氢氧化钠这是一种常见的制备氯化镁的方法。
当氢氧化镁和氯化钠反应时,会生成氯化镁和氢氧化钠两种化合物。
化学方程式如下:Mg(OH)2 + 2NaCl → MgCl2 + 2NaOH这个方程式表示了氢氧化镁和氯化钠在一定条件下发生反应,生成氯化镁和氢氧化钠。
通过这种反应可以得到氯化镁,从而实现对海水中镁元素的提取。
除了氯化镁的制备方法外,还可以通过碳酸镁和氢氯酸的反应来制备氯化镁。
在反应条件下,碳酸镁和氢氯酸会生成氯化镁、二氧化碳和水。
化学方程式如下:海水中的镁元素可以通过多种化学方法来提取,其中包括通过氢氧化镁、碳酸镁、氯化镁等物质的反应来实现。
这些化学方程式展示了海水制镁的几种常见方法,对于研究镁元素的提取和应用具有重要的参考价值。
希望通过这些方程式的介绍,可以更深入地了解海水中镁元素的制备过程。
【结束】。
第二篇示例:海水是地球上最丰富的资源之一,其中含有大量的镁元素。
在提取海水中的镁元素时,通常会采用化学方法进行处理。
下面将介绍五个关于海水制镁的化学方程式。
1. 镁在海水中的存在形式海水中含有丰富的镁元素,一般以镁离子(Mg2+)的形式存在。
镁离子在水中是稳定的,但要提取镁元素需要将镁离子与其他物质结合形成沉淀物。
2. 镁离子与碳酸钠的反应将海水中的镁离子与碳酸钠(Na2CO3)反应,生成碳酸镁(MgCO3)沉淀。
化学方程式如下:Mg2+ + Na2CO3 → MgCO3↓ + 2Na+碳酸镁是一种不溶于水的白色沉淀物,可以通过过滤等方法分离出来。
3. 碳酸镁的热分解接下来,将碳酸镁进行热分解处理,得到氧化镁(MgO)和二氧化碳(CO2)。

电解法炼镁的各种工艺原理2008/4/14/10:06氯化熔盐电解法包括氯化镁的生产及电解制镁两大过程。
该方法又可分为以菱镁矿为原料的无水氯化镁电解法和以海水为原料制取无水氯化镁的电解法。
其中后者最大的难点是如何去除MgCl2·6H2O中的结晶水。
一般来说:采用普通的加热法可以去除部分结晶水,生成MgCl2·3/2H2O。
但MgCl2·3/2H2O在空气中加热时很容易发生水解反应,生成不利于电解过程的杂质,如Mg(OH)2。
电解法生产镁的工艺很多,但基本原理相同,其中最有代表性的有DOW工艺、I.G.Farben 工艺、Magnola工艺等。
DOW工艺1916年DOW工艺在美国Michighn的Midland首次得到应用。
当时所用的制备MgCl2的方法是将海水与煅烧白云石一起制成泥浆,与盐酸反应,生成氯化镁溶液,将其浓缩并干燥处理后生成MgCl2·3/2H20。
这种原料直接加入电解槽内进行反应,副产物氯气可以回收利用。
1941年道屋(DOW)化学公司在塔克赛斯自由港建立了一个工厂,从海水中提取镁的电解原料。
海水由引水槽引入,滤过淤泥后导人沉淀池,与石灰混合,过滤后与20%HCl反应生成MgCl2,蒸发后得到固体氯化镁,然后经干燥炉干燥得到低水合氯化镁(MgCl2·3/2H2O),成为DOW工艺电解制镁的原料。
许多生产厂家都采用与DOW工艺类似的方法电解海水来生产镁,主要差别在于提取无水氯化镁的方法不同。
DOW化学公司通过在含大量MgCl2、NaCl和CaCl2混合溶液的电解池中直接加入少量部分脱水氯化物来迅速脱水。
挪威诺斯克—海德罗(Norsk—Hydro)公司是欧洲最主要的镁生产商,通过在干燥的氯化氢气氛中加热MgCl2·6H2O来实现完全脱水。
前独联体则主要采用往电解池中加入无水光卤石来脱水。
最近,澳大利亚金属镁公司开发了一种制备无水氯化镁原料的全新工艺,在氯化镁溶液中加入一种称为Gylcol的物质,蒸馏脱水,然后喷雾氨生成六氨合氯化镁,接着焙烧制备高质量的无水氯化镁。

镁粉生产工艺镁粉是一种重要的金属粉末材料,广泛应用于冶金、化工、电子等领域。
本文将介绍镁粉的生产工艺,包括原料准备、炼制过程和产品加工等方面。
一、原料准备镁粉的主要原料是高纯度的镁锭,其纯度要求达到99.9%以上。
在生产过程中,需要将镁锭加热至高温状态,然后通过物理或化学方法将其转化为粉末状。
二、炼制过程1. 镁锭破碎:首先,将高纯度的镁锭加热至高温状态,然后通过机械设备进行破碎,将镁锭破碎成较小的块状物料。
2. 粉碎和筛分:将破碎后的镁锭块料进行粉碎和筛分处理,得到所需的镁粉颗粒。
粉碎过程中需要控制粒度大小和颗粒形状,以满足不同应用领域的需求。
3. 清洗和干燥:将粉碎和筛分后的镁粉进行清洗,去除杂质和表面氧化物。
然后将清洗后的镁粉进行干燥处理,以保证其质量和稳定性。
三、产品加工1. 球磨和混合:将干燥后的镁粉进行球磨处理,以提高其表面平整度和流动性。
同时,可以根据需求将镁粉与其他材料进行混合,以获得特定的性能和用途。
2. 包装和储存:经过球磨和混合后的镁粉进行包装,通常采用密封包装,以防止氧化和潮湿等不良影响。
然后将包装好的镁粉存放在干燥、通风的仓库中,避免受潮和污染。
四、质量控制镁粉的生产过程中需要进行严格的质量控制,以确保产品的质量稳定和可靠。
常见的质量控制指标包括镁粉的纯度、粒度分布、表面平整度等。
在生产过程中,需要进行原料、中间产品和最终产品的质量检验和测试,以及对生产设备和工艺参数的监控和调整。
总结:镁粉的生产工艺包括原料准备、炼制过程和产品加工等环节。
通过对高纯度镁锭的加热、破碎、粉碎、筛分、清洗、干燥、球磨和混合等处理,最终得到符合要求的镁粉产品。
在生产过程中需要进行质量控制,确保产品的质量稳定和可靠。
镁粉的应用广泛,可以满足冶金、化工、电子等领域的需求,具有重要的经济和社会价值。
投稿栏目:复习与练习镁及其重要化合物的制备浙江省绍兴县柯桥中学 312030 林春辉镁是一种重要的金属材料,主要用于制造镁合金。
由于镁合金密度小,但硬度和强度都较大,因此被大量用于制造火箭、导弹和飞机的部件等。
镁的重要化合物有氯化镁、硫酸镁、氧化镁、碳酸镁等,它们在生产生活中都有着重要的应用。
下面重点探讨有关镁及其化合物的制备问题。
一、从海水中提取金属镁自然界中的镁主要以化合态的形式存在于地壳和海水中。
海水中镁的总储量约为1.8×1015t 。
现代工业主要是从海水中获得金属镁。
问题1 海水的综合利用可以制备金属镁,其流程如下图所示:(1)若在空气中加热MgCl 2•6H 2O ,生成的是Mg(OH)Cl 或MgO ,写出相应反应的化学方程式用电解法制取金属镁时,需要无水氯化镁。
在干燥的HCl 气流中加热MgCl 2•6H 2O 时,能得到无水MgCl 2,其原因是(2)Mg(OH)2沉淀中混有的Ca(OH)2应怎样除去?写出实验步骤。
(3)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的:溶解时: ;过滤时: ;蒸发时: 。
解析 (1)若直接在空气中加热MgCl 2•6H 2O ,则会发生镁离子的水解,生成Mg(OH)Cl 或MgO 。
根据Cl 、H 、O 三种元素守恒可知,在空气中加热MgCl 2•6H 2O 除了生成Mg(OH)Cl 或MgO 外,还有HCl 和H 2O 生成。
为抑制加热时MgCl 2•6H 2O 的水解,并且除去在加热过程中产生的水蒸气,应将MgCl 2•6H 2O 放在干燥的HCl 气流中进行加热。
(2)由于Mg(OH)2难溶于水,Ca(OH)2微溶于水,要除去Mg(OH)2中的Ca(OH)2,可用可溶性的镁盐溶液跟Ca(OH)2作用,将Ca(OH)2转化为Mg(OH)2,这样既不会引入新杂质,又生成了提纯物质,再经搅拌、过滤、洗涤便可达到提纯的目的。
一工业如何制镁详细流程海水中镁的含量是L,仅次于氯和钠,总蕴藏量估计有2×1015t。
在陆地上,镁的矿物主要是菱镁矿(主要成分是MgCO3)。
煅烧菱镁矿可以得到氧化镁,再加工成镁。
用这种方法制得的氧化镁,纯度不高,还要消耗大量的能源,并且污染环境。
如果能从海水中提取镁,不仅可以得到高纯度的镁,而且能耗低、没有污染。
所以海水提镁在本世纪40年代开创以来,发展极快。
目前世界上生产的镁已有60%取自海水中。
那么,镁是怎样的一种金属呢怎样从海水中提取镁从海水中提镁的化学原理和方法对我们有什么启示呢镁和海水提镁镁和镁的化合物镁是现有最轻的结构金属。
它在制取高强度的轻合金中有重要的地位。
例如,一种含镁80%(还含有铝、铜、锡、锰、钛等元素)的合金,密度只有cm3,不足钢铁的1/4,却有钢铁的强度,是制造汽车、飞机、火箭的重要材料。
镁原子容易失去最外层的两个电子,变成镁离子(Mg2+)。
因此,镁的还原性较强,可以用作冶炼一些金属的还原剂。
例如,四氯化钛就是用镁来还原成钛的。
镁在空气里点燃,放出大量的热,产生耀眼的白光。
利用这个性质,镁可以用来制造照明弹等。
氧化镁是白色粉末,味苦,俗称苦土。
土壤里含有少量氧化镁,因此它有苦味。
氧化镁是离子化合物,熔点高达2800℃,在高温下仍十分稳定,因此是优良的耐火材料。
上海宝山钢铁厂所用的耐火材料,要求氧化镁的纯度在98%以上。
氧化镁在制造水泥、纸浆、医药、精炼石油和橡胶工业中也有许多用途。
镁盐的种类很多,有的很有实用价值。
例如,运动员用来擦手的白色粉末,就是有很强吸湿能力的碳酸镁。
硫酸镁是泻盐,可以医治便秘和驱除蛔虫。
海水提镁海水是含有多种离子的混合溶液,其中阳离子有钠离子、钾离子和镁离子等。
海水提镁,就是要把镁离子跟其他阳离子分离开来。
利用离子反应生成难溶物质,可以使某些离子从溶液中析出。
那么,能不能向海水中加入一种离子,使镁离子变成沉淀析出,而其他的阳离子仍留在海水中呢【实验3-1】氯化镁、氯化钠跟碱溶液的反应在两支试管里分别加入3mL氯化镁溶液和氯化钠溶液。
氯化镁制镁的化学方程式
氯化镁制镁的化学方程式如下:
2MgCl2 + 2Na → 2NaCl + 2Mg
在这个方程式中,氯化镁(MgCl2)和钠(Na)反应生成氯化钠(NaCl)和镁(Mg)。
这个反应是通过将氯化镁和钠在高温下加热进行的。
氯化镁的熔点很高,在高温下可以熔化并电离成离子态的镁离子和氯离子。
钠是用作还原剂,将镁离子还原成镁原子并释放出电子。
由于钠的化学活性很高,因此它能够与氯化镁反应,从而产生高温下的还原反应,生成镁。
生成的镁会沉积在反应器的底部,并且在反应后可以通过过滤和水洗来分离出来。