甘肃省2019年高考化学模拟试题及答案
- 格式:doc
- 大小:263.00 KB
- 文档页数:7

2019年甘肃高考《化学》模拟试题及答案1.下列几种说法中正确的是()A.摩尔是化学上常用的一个物理量B.某物质含有6.02×1023个微粒,含有这个数目微粒的物质一定是1 molC.1摩尔氢气分子可以表示为1 mol H2D.硫酸的摩尔质量为98 g答案: C2.下列叙述正确的是()A.含1 mol溶质的任何溶液,物质的量浓度一定相等B.配制1 mol·L-1 NaCl溶液1 L,其方法是:将58.5 g NaCl溶于1 L 水中即可C.体积相同、物质的量浓度相同的同种溶液所含溶质的粒子数一定相同D.1 L 0.5 mol·L-1 CaCl2溶液中,Ca2+与Cl-的物质的量浓度都是0.5 mol·L-1答案: C3.( ·山东师大附中模拟)下列有关操作或判断正确的是()A.配制一定物质的量浓度的溶液时,定容时俯视刻度线会导致所配溶液浓度偏低B.用托盘天平称取25.20 g NaClC.用100 mL的量筒量取5.2 mL的盐酸D.用浓盐酸配制一定物质的量浓度的稀盐酸,量取浓盐酸时仰视量筒的刻度线会导致所配溶液浓度偏高解析:定容时俯视刻度线会使所配溶液的体积偏小,浓度偏高,A 错;托盘天平的精确度为0.1 g,B错;用量筒量取液体时,一般来说所量取的液体体积为量筒量程的60%左右,C错;量取一定量的液体时,仰视量筒的刻度线,会使所量取的溶液的体积偏大,最终所配溶液浓度偏高,D正确。
答案: D4.( ·汕头模拟)下列有关说法正确的是()A.7.45 g NaClO中含有6.02×1022个NaClO分子B.1.00 mol NaClO中所有ClO-的电子总数为26×6.02×1023C.1 L 2 mol/L明矾经水解可得到氢氧化铝胶体粒子数目为2×6.02×1023D.将2.00 mol明矾完全溶于1.00 L水中,得到溶液的物质的量浓度为2 mol/L解析:7.45 g NaClO的物质的量为0.1 mol,但NaClO是离子化合物,不存在NaClO分子,A项错;1个ClO-含有26个电子,B项正确;水解反应为可逆反应,Al3+不可能完全转化为Al(OH)3,并且形成的氢氧化铝胶体粒子数远远小于水解生成的Al(OH)3的数目,C项错;1.00 L 水配制溶液后,溶液体积不是1.00 L,D项错。

甘肃省达标名校2019年高考一月化学模拟试卷一、单选题(本题包括15个小题,每小题4分,共60分.每小题只有一个选项符合题意)1.已知:FeCl 3(aq)+3KSCN(aq)3KCl(aq)+Fe(SCN)3(aq),平衡时Fe(SCN)3的物质的量浓度与温度T 的关系如图所示,则下列说法正确的是A.A点与B点相比,A点的c(Fe3+)大B.加入KCl固体可以使溶液由D点变到C点C.反应处于D点时,一定有υ(正)<υ(逆)D.若T1、T2温度下的平衡常数分别为K1、K2,则K1<K22.已知:CH3C≡CH+CO+CH3OH M,N+CH3OH M+H2O。
其中M的结构简式为CH2=C(CH3)COOCH3,下列说法错误的是()A.N可以使溴水褪色B.N转化为M的反应为取代反应C.M中所有碳原子可能共面D.N属于酯的同分异构体有3种3.我国科研人员研制出一种室温“可呼吸” Na-CO2电池。
放电时该电池“吸入”CO2,充电时“呼出”CO2。
吸入CO2时,其工作原理如图所示。
吸收的全部CO2中,有2/3转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面。
下列说法正确的是A.“吸入”CO2时,钠箔为正极B.“呼出”CO2时,Na+向多壁碳纳米管电极移动C.“吸入” CO2时的正极反应式为:4Na++3CO2+4e-=2Na2CO3+CD.标准状况下,每“呼出”22.4 L CO2,转移电子的物质的量为0.75 mol4.某有机物的结构为,下列说法正确的是()A.1 mol该有机物最多可以与7 mol H2发生加成反应B.该有机物可以发生取代、加成、氧化、水解等反应C.0.1 mol该有机物与足量金属钠反应最多可以生成3.36L H2D.与该有机物具有相同官能团的同分异构体共有8种(不考虑立体异构)5.下列有关物质的性质与用途具有对应关系的是()A.NH4HCO3 受热易分解,可用作化肥B.NaHCO3 溶液显碱性,可用于制胃酸中和剂C.SO2具有氧化性,可用于纸浆漂白D.Al2O3具有两性,可用于电解冶炼铝6.下列化学用语正确的是A.中子数为2的氢原子:21H B.Na+的结构示意图:C.OH-的电子式:[H]一D.N2分子的结构式:N—N7.下列关于有机化合物的说法正确的是A.除去乙醇中的少量水,方法是加入新制生石灰,经过滤后即得乙醇B.CH3CH2CH2COOH和CH3COOCH2CH3属于碳链异构C.除去乙酸乙酯中的乙酸和乙醇杂质,可加入足量烧碱溶液,通过分液即得乙酸乙酯D.一个苯环上已经连有—CH3、—CH2CH3、—OH三种基团,如果在苯环上再连接一个—CH3,其同分异构体有16种8.许多无机颜料在缤纷的世界扮演了重要角色。
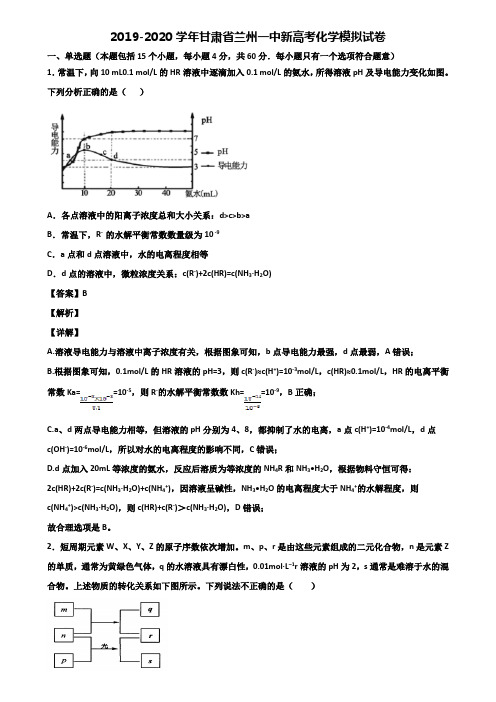
2019-2020学年甘肃省兰州一中新高考化学模拟试卷一、单选题(本题包括15个小题,每小题4分,共60分.每小题只有一个选项符合题意)1.常温下,向10 mL0.1 mol/L的HR溶液中逐滴加入0.1 mol/L的氨水,所得溶液pH及导电能力变化如图。
下列分析正确的是()A.各点溶液中的阳离子浓度总和大小关系:d>c>b>aB.常温下,R- 的水解平衡常数数量级为10 -9C.a点和d点溶液中,水的电离程度相等D.d点的溶液中,微粒浓度关系:c(R-)+2c(HR)=c(NH3∙H2O)【答案】B【解析】【详解】A.溶液导电能力与溶液中离子浓度有关,根据图象可知,b点导电能力最强,d点最弱,A错误;B.根据图象可知,0.1mol/L的HR溶液的pH=3,则c(R-)≈c(H+)=10-3mol/L,c(HR)≈0.1mol/L,HR的电离平衡常数Ka==10-5,则R-的水解平衡常数数Kh==10-9,B正确;C.a、d两点导电能力相等,但溶液的pH分别为4、8,都抑制了水的电离,a点c(H+)=10-4mol/L,d点c(OH-)=10-6mol/L,所以对水的电离程度的影响不同,C错误;D.d点加入20mL等浓度的氨水,反应后溶质为等浓度的NH4R和NH3•H2O,根据物料守恒可得:2c(HR)+2c(R-)=c(NH3∙H2O)+c(NH4+),因溶液呈碱性,NH3•H2O的电离程度大于NH4+的水解程度,则c(NH4+)>c(NH3∙H2O),则c(HR)+c(R-)>c(NH3∙H2O),D错误;故合理选项是B。
2.短周期元素W、X、Y、Z的原子序数依次增加。
m、p、r是由这些元素组成的二元化合物,n是元素Z 的单质,通常为黄绿色气体,q的水溶液具有漂白性,0.01mol·L–1r溶液的pH为2,s通常是难溶于水的混合物。
上述物质的转化关系如下图所示。

2019-2020学年甘肃省新高考化学模拟试卷一、单选题(本题包括15个小题,每小题4分,共60分.每小题只有一个选项符合题意)1.下列离子方程式书写正确的是A.食醋除水垢2H++CaCO3=Ca2++CO2↑+H2O:B.稀硝酸中加入少量亚硫酸钠:2H++SO32-=SO2↑+H2OC.处理工业废水时Cr(Ⅵ)的转化:Cr2O72-+3SO32-+8H+=3SO42-+2Cr3++4H2OD.用酸性KMnO4测定草酸溶液浓度:5C2O42-+2MnO4-+16H+=2Mn2++10CO2↑+8H2O【答案】C【解析】【详解】A.食醋的主要成分为乙酸,属于弱酸,用食醋除水垢,离子方程式:2CH3COOH+CaCO3═CO2↑+Ca2++H2O+2CH3COO-,故A错误;B.酸性条件下,亚硫酸钠被硝酸氧化生成硫酸钠,离子反应方程式为:3SO32-+2H++2NO3-=3SO42-+2NO↑+H2O,故B错误;C.Cr(Ⅵ)具有强氧化性,可以用在酸性条件下,用亚硫酸钠处理工业废水时Cr(Ⅵ),反应的离子方程式为:Cr2O72-+3SO32-+8H+=3SO42-+2Cr3++4H2O,故C正确;D.酸性高锰酸钾可氧化草酸溶液,草酸是弱酸,不能拆开,正确的的离子反应为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,故D错误;故选C。
【点睛】本题的易错点为B,要注意硝酸具有强氧化性,能够将亚硫酸根离子氧化。
2.类推是化学学习和研究中常用的思维方法.下列类推正确的是()A.CO2与SiO2化学式相似,故CO2与SiO2的晶体结构也相似B.晶体中有阴离子,必有阳离子,则晶体中有阳离子,也必有阴离子C.检验溴乙烷中的溴原子可以先加氢氧化钠水溶液再加热,充分反应后加硝酸酸化,再加硝酸银,观察是否有淡黄色沉淀,则检验四氯化碳中的氯原子也可以用该方法,观察是否产生白色沉淀D.向饱和碳酸氢钠溶液中加入氯化铵会有碳酸氢钠晶体析出,则向饱和碳酸氢钾溶液中加入氯化铵也会有碳酸氢钾晶体析出【答案】D【解析】【分析】【详解】A. 二氧化碳是分子晶体,二氧化硅是原子晶体,晶体结构不同,故A错误;B. 晶体中有阳离子,未必一定有阴离子,如:在金属晶体中,存在金属阳离子和自由移动的电子,故B 错误;C. 四氯化碳不易发生水解反应,故C错误;D. 碳酸氢钾与碳酸氢钠性质相似,可析出碳酸氢钾晶体,故D正确;答案选D。
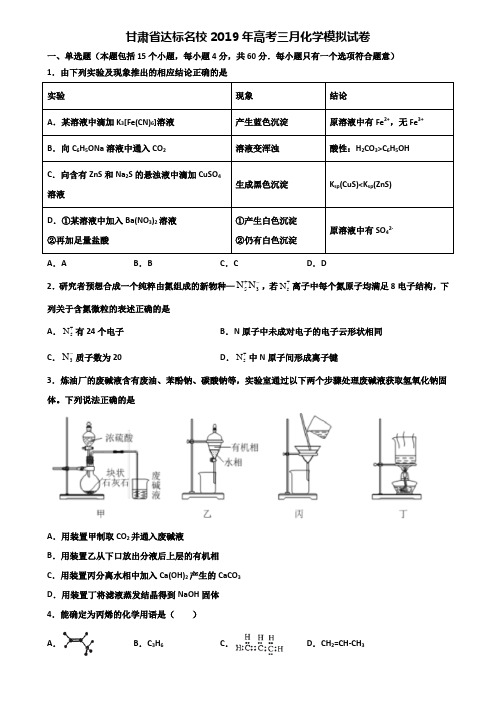
甘肃省达标名校2019年高考三月化学模拟试卷一、单选题(本题包括15个小题,每小题4分,共60分.每小题只有一个选项符合题意)1.由下列实验及现象推出的相应结论正确的是实验现象结论A.某溶液中滴加K3[Fe(CN)6]溶液产生蓝色沉淀原溶液中有Fe2+,无Fe3+ B.向C6H5ONa溶液中通入CO2溶液变浑浊酸性:H2CO3>C6H5OHC.向含有ZnS和Na2S的悬浊液中滴加CuSO4溶液生成黑色沉淀K sp(CuS)<K sp(ZnS)D.①某溶液中加入Ba(NO3)2溶液②再加足量盐酸①产生白色沉淀②仍有白色沉淀原溶液中有SO42-A.A B.B C.C D.D2.研究者预想合成一个纯粹由氮组成的新物种—+53N N-,若+5N离子中每个氮原子均满足8电子结构,下列关于含氮微粒的表述正确的是A.+5N有24个电子B.N原子中未成对电子的电子云形状相同C.3N-质子数为20 D.+5N中N原子间形成离子键3.炼油厂的废碱液含有废油、苯酚钠、碳酸钠等,实验室通过以下两个步骤处理废碱液获取氢氧化钠固体。
下列说法正确的是A.用装置甲制取CO2并通入废碱液B.用装置乙从下口放出分液后上层的有机相C.用装置丙分离水相中加入Ca(OH)2产生的CaCO3D.用装置丁将滤液蒸发结晶得到NaOH固体4.能确定为丙烯的化学用语是()A.B.C3H6C.D.CH2=CH-CH35.下列各物质或微粒性质的比较中正确的是A.碳碳键键长:乙烯>苯B.密度:一氯乙烷>一氯丁烷C.热稳定性:NaHCO3>Na2CO3>H2CO3D.沸点:H2O>H2S>H2Se6.工业上电解NaHSO4溶液制备Na2S2O8。
电解时,阴极材料为Pb;阳极(铂电极)电极反应式为2HSO4-- 2e-=S2O82-+2H+。
下列说法正确的是()A.阴极电极反应式为Pb+HSO4-- 2e-=PbSO4+H+B.阳极反应中S的化合价升高C.S2O82-中既存在非极性键又存在极性键D.可以用铜电极作阳极7.Ag+与I-既能发生沉淀反应又能发生氧化还原反应。

2019-2020学年甘肃省示范名校新高考化学模拟试卷一、单选题(本题包括15个小题,每小题4分,共60分.每小题只有一个选项符合题意)1.已知H 2S 与CO 2在高温下发生反应:H 2S(g)+CO 2(g)=COS(g)+H 2O(g)。
在610 K 时,将0.10 mol CO 2与0.40 mol H 2S 充入2.5 L 的空钢瓶中,经过4 min 达到平衡,平衡时水的物质的量分数为2%,则下列说法不正确的是( )A .CO 2的平衡转化率α=2.5%B .用H 2S 表示该反应的速率为0.001 mol·L -1·min -1C .在620 K 重复试验,平衡后水的物质的量分数为3%,说明该平衡正向移动了D .反应过程中混合气体平均摩尔质量始终不变 【答案】A 【解析】 【详解】根据题意列出三段式,如下:()()()()222(mol/L)0.160.0400(mol/L)x x x x H S g CO g CO (mol/L)0.16-x0.04-xxH O g xS g ƒ起始变化平衡++根据平衡时水的物质的量分数为2%,则2%0.2x=,故x=0.004mol/L , A 、CO 2的平衡转化率α=0.004100%0.04⨯=10%,选项A 不正确; B 、用H 2S 表示该反应的速率为0.004/4mol Lmin=0.001 mol·L -1·min -1,选项B 正确;C 、当温度升高到620K 时,平衡后水的物质的量分数为3%,可知温度升高平衡向正反应方向移动了,选项C 正确;D 、由于反应前后都为气体,且为气体体积不变的反应,反应过程中混合气体平均摩尔质量始终不变,选项D 正确。
答案选A 。
2.银精矿(其化学成分有:Ag 、Zn 、Cu 、Pb 、S 及 SiO 2 等)从其中提取银及铜和铅的工艺流程如图:回答下列问题:(1)“浸取”时,当盐酸的浓度和 KClO 3 的量一定时,为提高浸取率可采取的措施是______(请用简练语言列举一项)。
甘肃省白银市2019届高三化学模拟试题(一)可能用到的相对原子质量:可能用到的相对原子质量:H1 8 11 C 12 N 14 0 16 Na 23 Mg 24 S 32 Fe 56一、选择题:本题共7个小题,每小题6分,共42分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
7.在日常生活中,下列做法值得提倡的是A.将生活垃圾分类处理 B.将废旧塑料深挖填埋C.选用一次性碗筷和纸杯 D.利用焚烧秸杆施肥8.某地区已探明蕴藏着丰富的赤铁矿、煤、石灰石和黏土,现拟建设大型炼铁厂和与之相关联的焦化厂、发电厂、水泥厂等。
下图中工厂名称正确的是A.焦化厂 B.炼铁厂 C.发电厂 D.水泥厂9.N A代表阿伏加德罗常数的值。
下列说法正确的是A.将0.1 mol CO2溶于适量水,溶液中CO32-、HCO3-、H2CO3粒子总数为0.1N AB.在7.8 g Na2O2与Na2S的混合物中,离子总数为0.3N AC.使0.5 mol乙烯被溴的四氯化碳溶液完全吸收,断裂的共价键总数为0.5N AD.标准状况下,2. 24 L Cl2与CH4反应完全,生成物中气体分子数目小于0.1N A10.下列实验过程可以达到实验目的的是11.降冰片二烯类化合物是一类太阳能储能材料。
降冰片二烯在紫外线照射下可以发生下列转化。
下列说法错误的是A.降冰片二烯与四环烷互为同分异构体B.降冰片二烯的同分异构体可能是苯的同系物C.四环烷的一氯代物超过三种(不考虑立体异构)D.降冰片二烯分子中位于同一平面的碳原子不超过4个12.W、X、Y和Z为原子序数依次增大的四种短周期元素。
常温常压下,Y的单质和氧化物均能与X的氢化物的水溶液反应生成一种相同的气体,该气体分子与CH4具有相同的空间结构。
Z原子最外层的电子数是W 原子的最外层电子数的2倍。
下列叙述错误的是A.元素X的氢化物比其它三种元素的氢化物更稳定B.元素Y在自然界中只以化合态形式存在C.元素Z的含氧酸只有两种D.元素W、Y位于周期表中金属与非金属分界线附近13.电渗析法淡化海水装置示意图如下,电解槽中阴离子交换膜和阳离子交换膜相间排列,将电解槽分隔成多个独立的间隔室,海水充满在各个间隔室中。
2019-2020学年甘肃省甘南新高考化学模拟试卷一、单选题(本题包括15个小题,每小题4分,共60分.每小题只有一个选项符合题意)1.工业上常用铁碳混合物处理含Cu2+废水获得金属铜。
当保持铁屑和活性炭总质量不变时,测得废水中Cu2+浓度在不同铁碳质量比(x)条件下随时间变化的曲线如下图所示。
下列推论不合理...的是A.活性炭对Cu2+具有一定的吸附作用B.铁屑和活性炭会在溶液中形成微电池,铁为负极C.增大铁碳混合物中铁碳比(x),一定会提高废水中Cu2+的去除速率D.利用铁碳混合物回收含Cu2+废水中铜的反应原理:Fe+Cu2+=Fe2++Cu【答案】C【解析】【分析】A、由图可知纯的活性炭铜离子的浓度减小;B、铁与活性炭形成原电池,铁比炭活泼;C、由图可知纯铁时去除铜离子的速率,没铁碳比为2:1时的速率快;D、利用铁碳混合物回收含Cu2+废水中铜的反应原理是铁与铜离子发生自发的氧化还原反应。
【详解】A项,活性炭具有许多细小微孔,且表面积巨大,具有很强的吸附能力,由图像可知,Cu2+在纯活性炭中浓度减小,表明活性炭对Cu2+具有一定的吸附作用,故不选A项;B项,铁屑和活性炭在溶液中形成微电池,其中铁具有较强的还原性,易失去电子形成Fe2+,发生氧化反应,因此铁作负极,故不选B项;C项,由图像可知,随着铁碳混合物中铁含量的增加至x=2:1,Cu2+的去除速率逐渐增加;但当铁碳混合物变为纯铁屑时,Cu2+的去除速率降低。
当铁碳混合物中铁的含量过大时,正极材料比例降低,铁碳在废液中形成的微电池数量减少,Cu2+的去除速率会降低,因此增大铁碳混合物中铁碳比(x),不一定会提高废水中Cu2+的去除速率,故选C项;D项,在铁碳微电池中,碳所在电极发生还原反应,Cu2+得到电子生成铜单质;因此该微电池的总反应方程式为Fe+Cu2+=Fe2++Cu,故不选D项。
综上所述,本题正确答案为C 。
【点睛】本题对电化学的原理和学生看图识的能力的考查,题目有利于培养学生的良好的科学素养,侧重于考查学生的分析、实验能力的考查,注意把握提给信息以及物质的性质,为解答该题的关键。
2019-2020学年甘肃省兰州市甘肃一中新高考化学模拟试卷一、单选题(本题包括15个小题,每小题4分,共60分.每小题只有一个选项符合题意)1.如图所示装置中不存在的仪器是()A.坩埚B.泥三角C.三脚架D.石棉网【答案】D【解析】【分析】【详解】由图示装置可知,涉及的仪器为:坩埚、泥三角、三脚架、酒精灯等,由于给坩埚加热时可以直接进行加热,不需要使用石棉网,所以该装置中没有用到石棉网,答案选D。
【点睛】注意常见的仪器干燥及正确的使用方法,明确给坩埚加热时,不需要垫上石棉网。
2.SO2能使溴水褪色,说明SO2具有()A.还原性B.漂白性C.酸性D.氧化性【答案】A【解析】【详解】溴单质与二氧化硫能发生氧化还原反应生成硫酸和HBr,溶液中溴的颜色会褪去,反应的化学方程式为:SO2+Br2+2H2O=H2SO4+2HBr,硫元素化合价升高(+4→+6),体现还原性,溴元素化合价降低,体现氧化性(0→-1),A项正确;答案选A。
【点睛】本题考查二氧化硫的化学性质,二氧化硫具有多重性质,可总结如下:1、酸性氧化物:二氧化硫是酸性氧化物,和二氧化碳相似,溶于水显酸性,可与碱等反应;2、还原性:二氧化硫可与酸性高锰酸钾、过氧化氢、氯水、溴水等强氧化性的物质反应;3、弱氧化性:二氧化硫可与硫化氢反应生成硫单质等;4、漂白性:二氧化硫的漂白性体现在可漂白品红等物质,尤其是二氧化硫的漂白性和还原性是学生们的易混点。
使酸性高锰酸钾溶液、氯水、溴水褪色体现的二氧化硫的还原性,使品红溶液褪色体现的是漂白性。
3.水果、蔬菜中含有的维生素C具有抗衰老作用,但易被氧化成脱氢维生素C。
某课外小组利用滴定法测某橙汁中维生素C的含量,其化学方程式如图所示,下列说法正确的是A .脱氢维生素C 分子式为C 6H 8O 6B .维生素C 中含有3种官能团C .该反应为氧化反应,且滴定时不可用淀粉作指示剂D .维生素C 不溶于水,易溶于有机溶剂 【答案】B 【解析】 【分析】 【详解】A. 根据物质结构简式可知脱氢维生素C 的分子式为C 6H 6O 6,A 错误;B. 根据维生素C 结构可知维生素C 含有羟基、碳碳双键、酯基三种官能团,B 正确;C. 1分子维生素C 与I 2发生反应产生1分子脱氢维生素C 和2个HI 分子,维生素C 分子失去两个H 原子生成脱氢维生素C ,失去H 原子的反应为氧化反应;碘遇淀粉变蓝,所以滴定时可用淀粉溶液作指示剂,终点时溶液由无色变蓝色,C 错误;D. 羟基属于亲水基团,维生素C 含多个羟基,故易溶于水,而在有机溶剂中溶解度比较小,D 错误; 故合理选项是B 。
甘肃省达标名校2019年高考四月仿真备考化学试题一、单选题(本题包括15个小题,每小题4分,共60分.每小题只有一个选项符合题意)1.必须随配随用,不能长期存放的试剂是()A.氢硫酸B.盐酸C.AgNO3溶液D.NaOH溶液2.下列关于有机化合物的说法正确的是A.C3H6C12有4种同分异构体B.乙烯与Br2的CC l4溶液反应后,混合液分为两层C.乙醇被氧化一定生成乙醛D.合成材料会造成巨大的环境压力,应禁止使用3.现有短周期主族元素X、Y、Z、R、T,R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T型化合物能破坏水的电离平衡,五种元素的原子半径与原子序数的关系如图所示。
下列推断正确的是()A.原子半径和离子半径均满足:Y<ZB.简单氢化物的沸点和热稳定性均满足:Y>TC.最高价氧化物对应的水化物的酸性:T<RD.常温下,0.1mol·L-1由X、Y、Z、T四种元素组成的化合物的水溶液的pH一定大于14.己知在碱性溶液中可发生如下反应:2R(OH)3+ 3C1O-+ 4OH-= 2RO4n-+3Cl-+5H2O。
则RO4n-中R的化合价是()A.+3 B.+4 C.+5 D.+65.某二元弱碱B(OH)2(K1=5.9×10-2、K2=6.4×10-5)。
向10mL稀B(OH)2溶液中滴加等浓度盐酸,B(OH)2、B(OH)+、B2+的浓度分数 随溶液pOH[pOH=-lgc(OH-)]变化的关系如图,以下说法正确的是A.交点a处对应加入的盐酸溶液的体积为5mLB.当加入的盐酸溶液的体积为10mL时存在c(Cl-)>c(B(OH)+)>c(H+)>c(OH-)>c(B2+)C.交点b处c(OH-)=6.4×l0-5D.当加入的盐酸溶液的体积为15mL时存在:c(Cl-)+c(OH-)>c(H+)>c(OH-)>c(B2+)+ c(B(OH)+)+c(H+) 6.下列有关14C60的叙述正确的是A.与12C60化学性质相同B.与12C60互为同素异形体C.属于原子晶体D.与12C60互为同位素7.下列说法正确的是()A.淀粉、纤维素、油脂都是高分子化合物B.石油分馏和煤的干馏过程,都属于物理变化C.甲烷、汽油、柴油、酒精都是碳氢化合物,都可作燃料D.聚乙烯是无毒高分子材料,可用于制作食品包装袋8.化学与生产、生活密切相关,下列叙述中正确的是A.用活性炭为糖浆脱色和用双氧水漂白纸浆,其原理相同B.铜制品在潮湿空气中生锈,其主要原因是发生析氢腐蚀C.用NaHCO3和Al2(SO4)3溶液可以制作泡沫灭火剂D.从海水中可以制取NaCl,电解饱和NaCl溶液可以制取金属Na9.下列表示对应化学反应的离子方程式正确的是( )A.常温下,由水电离的c(H+)=10-13mol·L-1的溶液中:Na+、NH4+、Cl-、HCO3-B.酸性碘化钾溶液中滴加适量双氧水:2I—+2H++H2O2=I2+2H2OC.氢氧化钡溶液与硫酸铜溶液反应:Ba2++SO42—=BaSO4D.向饱和碳酸钠溶液中通入二氧化碳:CO32—+CO2+H2O=2HCO3—10.25℃时,将浓度均为0.1 mol·L-1,体积分别为V a和V b的HA溶液与BOH溶液按不同体积比混合,保持V a+V b=100 mL,V a、V b与混合液pH的关系如图所示,下列说法正确的是A.K a(HA)=1×10-6B.b点c(B+)=c(A-)=c(OH-)=c(H+)C.a→c过程中水的电离程度始终增大D.c点时,c(A-)/[c(OH-)⋅c(HA)]随温度升高而减小11.下列关于有机物()的说法错误的是A.该分子中的5个碳原子可能共面B.与该有机物含相同官能团的同分异构体只有3种C.通过加成反应可分别制得烷烃、卤代烃D.鉴别该有机物与戊烷可用酸性高锰酸钾溶液12.温度T℃时,在初始体积为1L的两个密闭容器甲(恒容)、乙(恒压)中分别加入0.2molA和0.1molB,发生反应2A(g)+B(g)x C(g),实验测得甲、乙容器中A的转化率随时间的变化关系如图所示。
甘肃省2019年高考化学模拟试题及答案(试卷满分100分,考试时间60分钟)一、选择题(共7小题,每小题6分,共42分,每小题只有一个选项符合题意)1.设N A为阿伏加德罗常数的值。
下列说法正确的是A. 常温常压下,22.4 L乙烯中含C-H键的数目为4N AB.0.1 mol/L的NaHSO4溶液中含有阳离子的数目为0.2N AC.0. Imol Cl2与过量NaOH溶液反应,转移电子数目为0.2N AD.7.8 g Na2S与7.8 g Na2O2中含有的阴离子数目均为0.IN A2.温度和压强相同时,在体积相同的两个密闭容器甲和乙,甲中充满O2气体,乙中充满O2和O3的混合气体,下列说法正确的是A.两容器中气体的质量相等B.两容器中气体的分子数目相等C.两容器中气体的氧原子数目相等D.两容器中气体的密度相等3. 在指定条件下,下列粒子一定能大量共存的是A.使酚酞变红色的溶液中:Na+、Fe3+、SO42-、Cl-B.饱和氯水中:K+、Na+、Cl-、HSO3-C.室温下,pH=13的溶液中:Na+、K+、SiO32-、Cl-D.1.0mol/L的KNO3溶液:H+、Fe2+、Cl-、SO32-4.化学反应速率和化学反应的限度是化工生产研究的主要问题之一.下列对化学反应速率和反应限度的认识正确的是A.决定化学反应速率的主要因素是光照、超声波、压强和催化剂等B.化学反应速率理论是研究怎样提高原料转化率的C.可逆反应到一定程度时,会出现正、逆反应速率相等,各物质浓度相等的现象D.化学限度(即平衡)理论,是研究怎样改变反应条件,提高产品的产率5.某溶液中含有的离子可能是K+、Ba2+、A13+、Mg2+、A1O2-、CO32-、SiO32-、C1-中的几种,现进行如下实验:①取少量溶液加氢氧化钠溶液过程中无沉淀生成;②另取少量原溶液,逐滴加入5 mL 0.2 mol • L-1的盐酸,发生的现象是开始产生沉淀并逐渐增多,沉淀量基本不变后产生气体,最后沉淀逐渐减少至消失;③在上述②沉淀消失后的溶液中,再加入足量的硝酸银溶液可得到沉淀0.435 g。
下列说法中正确的是A.该溶液中一定不含有Ba2+、Mg2+、A13+、SiO32-、C1-B.该溶液中一定含有K+、A1O2-、CO32-、C1-C.该溶液中是否含有K+需做焰色反应(透过蓝色钴玻璃片)D.可能含有C1-6. 由下列实验及现象推出的相应结论不正确的是7. 能正确表示下列反应的离子方程式是A. 将铁粉加入稀硫酸中B. 将硫酸铜溶液和氢氧化钡溶液混合:C. 向溶液中逐滴加入溶液至中性:D. 将铜投入到氯化铁溶液中:二、非选择题(共4小题,共58分)8.(15分)亚硝酰氯(NOCl)是一种红褐色液体或黄色气体,其熔点−64.5℃,沸点−5.5℃,遇水易水解。
它是有机合成中的重要试剂,可由NO与Cl2在常温常压下合成。
(1)实验室制备原料气NO和Cl2的装置如下图所示:实验室制Cl2时,装置A中烧瓶内发生反应的化学方程式为_______。
装置B中盛放的试剂为_______,其作用为___________________。
(3分)(2)将上述收集到的Cl2充入D的集气瓶中,按图示装置制备亚硝酰氯。
①NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为_______。
(2分)②装置D中发生的反应方程式为___________________________________(2分)。
③如果不用装置E会引起什么后果_________________________________。
(2分)④某同学认为装置F不能有效吸收尾气中的某种气体,该气体为_____,为了充分吸收尾气,可将尾气与_______同时通入氢氧化钠溶液中。
(2分)(3)工业上可用间接电化学法除去NO,其原理如下图所示,吸收塔中发生的反应为:NO+S2O42−+H2O →N2+HSO3−①吸收塔内发生反应的氧化剂与还原剂物质的量之比为_________________。
(2分)②阴极的电极反应式为_________________________________________。
(2分)9.(12分)某100mL溶液中含有的部分离子浓度大小如图所示,该溶液可能还含有Fe2+、Ba2+、H+、SO42-、CO32-。
为了进一步确认,对该溶液进行实验检测:步骤一; 仔细观察,该溶液呈无色、透明、均一状态。
步骤二: 加入足量BaCl2溶液,生成23.3g 白色沉淀,再加稀硝酸,沉淀不消失。
(1)原溶液中除上图中的离子以外,肯定还含有的离子是________,(2分)肯定不含有的离子是________。
(2分)(2)实验操作的步骤二中称量沉淀前的实验操作步骤有: 过滤、洗涤、干燥、检验沉淀已洗干净的方法是____________。
(2分)(3)原溶液中H+物质的量浓度为_________mol/L。
(2分)(4)向原溶液中加入NaHCO3溶液,反应的离子方程式为:______ _______。
(2分)(5)若向100 mL 原溶液中加入1mo/L 的Ba(OH)2溶液,当生成的沉淀质量刚好最大时,则加入的Ba(OH)2溶液体积为___________L。
(2分)10.(17分)碱式氯化铜[Cu x(OH)y Cl z.mH2O]是重要的农药、医药中间体,还可用作木材防腐剂、饲料添加剂等。
研究小组在实验室用某厂废铜渣(主要成分Cu、CuO,含少量Fe3O4、Ni、A12O3)制备碱式氯化铜的流程如下:回答下列问题:(l)“研磨”的目的为___________________________ 。
(2分)(2)“碱溶”的目的为 ________________________________ 。
(2分)(3)“酸溶”时生成Fe3+反应的离子方程式为 ______________________________;生成的Fe3+对Cu 发生的氧化反应的催化原理如图所示。
N的化学式为________________________________。
(4分)(4)“酸溶”时温度不能过高的理由为_______________________________________。
(3分)(5)若滤液2中c(Fe3+)=4×10-8 mol/L,pH=4,则Ksp[Fe(OH)3]=_________________。
(2分)(6)为测定Cu x (OH)y Cl z.mH2O的组成,进行如下操作:取样品2.232 g,用适量酸溶解后配成100 mL 溶液;取25. 00 mL溶液加入足量AgNO3溶液,生成0.3444 g沉淀;另取25. 00 mL溶液,用0.1600 mol.L-1的EDTA标准液滴定Cu2+(Cu2+与EDTA以物质的量之比1:1反应),滴定至终点时消耗标准液体积为30. 00 mL。
①溶解样品所用酸的化学式为 _____________________________________。
(2分)②该样品的化学式为__________________________________。
(2分)11.(14分)G是药物合成中的一种重要中间体,下面是G的一种合成路线:回答下列问题:(1)B的结构简式为__________,其中所含官能团的名称为__________;B生成C的反应类型为__________。
(4分)(2)D的名称是__________。
(2分)(3)由C和E合成F的化学方程式为________________________________________。
(2分)(4)D的同分异构体中,能发生银镜反应且分子结构中含苯环的还有__________种,其中核磁共振氢谱上有6组峰,峰面积之比为1∶1∶1∶1∶1∶1的同分异构体的结构简式为______________________ (一种即可)。
(2分)(5)参照上述合成路线,以CH3CH2Cl为原料(其他试剂任选),设计制备巴豆醛(CH3CH=CHCHO)的合成路线。
_______________(4分)参考答案一、选择题(共7小题,每小题6分,共42分,每小题只有一个选项符合题意)1.D2.B3.C4.D5.B6.D7.C二、非选择题(共4小题,共58分)8.(15分)⑴ MnO2 + 4HCl MnCl2+Cl2↑+H2O 饱和食盐水除去 Cl2 中HCl 气体⑵①②2NO + Cl2 = 2NOCl③F中的水蒸气进入 D 装置中,会导致产品水解④ NO O2⑶① 1:1 ② 2HSO3−+ 2H+ + 2e−= S2O42−+ 2H2O9.(12分)(1)、SO42-、H+(2分); Fe3+、Ba2+、CO32-(2分)(2)取最后一次洗涤液少量于试管中,加入硝酸银溶液,若无白色沉淀生成,证明已洗涤干净(2分)(3) 3 (2分)(4) H++HCO3-=H2O +CO2↑(2分)(5)0.2(2分)10. (19分) (1)加快化学反应速率,使反应充分(2)将Al2O3转化为NaAlO2而分离除去(3) 4Fe3O4 + O2 + 36H+ = 12Fe3+ + 18H2O Fe2+(或FeCl2)(4)温度升高,盐酸挥发,空气溶解度减小,会导致反应速率降低,“酸溶”不充分(5)4×10-38(6) HNO3 Cu2(OH)3Cl·H2O11.(14分) (1) 羟基、羰基取代反应(2) 对羟基苯甲醛(3)(4) 3 或(5)。