第六章 燃烧与燃料知识点总结
- 格式:docx
- 大小:120.43 KB
- 文档页数:5


第六章 燃烧与燃料第一节 燃烧与灭火一.燃烧的条件(重点)1.燃烧:是可燃物跟氧气发生的剧烈的发光、发热的氧化反应。
(1)燃烧的现象:发光、发热,反应剧烈。
(2)燃烧的反应类型:氧化反应,不一定是化合反应。
(3)燃烧的反应物:常见的燃烧都是可燃物跟氧气发生反应,但是,不是所有的燃烧都一定有氧气参加。
例如,镁就能在二氧化碳中燃烧:2Mg+CO 2点燃C+2MgO ;钠能在氯气中燃烧:2Na +Cl 2点燃2NaCl(4)燃烧的反应条件:点燃 (5)燃烧的分类及燃烧的产物注意:① “完全燃烧”和“不完全燃烧”又叫“充分燃烧”和“不充分燃烧” ② 要掌握含C 、H 、O 等元素的燃料完全燃烧的化学方程式: 2.燃烧的条件:①物质具有可燃性 ②可燃物要与氧气接触;③可燃物的温度达到其自身的着火点(即可燃物燃烧所需要的最低温度) 燃烧必须要同时满足三个条件,才能发生燃烧的现象。
二.灭火的原理:①.移走可燃物可燃物 ②.隔绝氧气③.使温度降到着火点以下1.灭火原理实质就是破坏物质燃烧的条件,三者破坏其一即可灭火。
2.几种常见的灭火方法:(1) 移走可燃物可燃物:森林火灾开辟隔离带,管道煤气着火先关掉阀门,釜底抽薪等; (2)隔绝氧气:酒精灯用等冒盖灭,油锅着火用用锅盖盖灭,向着火的木柴上覆盖沙子,少量酒精燃烧用湿抹布盖灭等;(3)使温度降到着火点以下:用水等大量的冷却剂灭火,用嘴将灯吹熄,(4)用灭火器灭火:①泡沫灭火器:可用于扑灭木材、棉布等燃烧而引起的一般火灾,不能用于扑灭电器火灾;②干粉灭火器:除了用来扑灭一般火灾外,还用于扑灭电器、油、气等燃烧引起的火灾;③液态二氧化碳灭火器:用于扑灭图书档案、贵重设备、精密仪器的火灾。
3.二氧化碳与灭火(1)原理:二氧化碳不能燃烧也不能支持燃烧,且密度比空气大。
(2)灭火器主要是用二氧化碳灭火,二氧化碳不能扑灭所有的火灾:如镁带燃烧就不能用二氧化碳扑灭。
4火灾处置、自救 (1)火警电话:119(2)电器、管道煤气、天然气着火,首先要关闭电源或气阀。

第六单元:《燃烧与燃料》知识汇总精讲【考点精讲】考点一、燃烧与灭火(1)定义:可燃物跟氧气发生的剧烈的发光、发热的氧化反应。
(2)条件:①物质具有可燃性; ②可燃物跟氧气充分接触;③可燃物的温度达到着火点以上(着火点:可燃物燃烧所需要的最低温度,是物质的固有属性,不能改变;着火点越低,越易燃烧);三者同时具备才可以燃烧。
(3)促进燃烧的方法:①增大氧气的浓度;②增大可燃物与氧气的接触面积; 燃烧分类:①充分燃烧:氧气充足;②不充分燃烧:氧气不足。
例如:(1)乙炔:(2)碳:氧气充足,化学方程式:C+O 2CO 2 ;氧气不充足2C+O 22CO ;(CO 中毒:与血红蛋白结合,失去运氧能力)2、灭火原理:破坏燃烧所需的条件,(只要破坏其中一个燃烧条件,就可灭火)。
方法:①隔绝氧气(如沙土覆盖); ②移走可燃物(如关闭煤气阀门); ③降低温度到着火点以下(如用水灭火)。
3、爆炸(1)分类:①物理爆炸:如气球吹爆、爆胎、锅炉爆炸等;②化学爆炸:燃放鞭炮、甲烷爆炸等。
(2)化学爆炸的条件:①可燃性气体或粉尘在空气中的含量达到爆炸极限; ②遇明火燃烧;③气体体积在有限的空间内急剧膨胀。
典例1 【2020云南】下列有关燃烧和灭火的说法正确的是( )乙炔 充分燃烧不充分燃烧 条件 氧气充足 氧气不充足现象 蓝色火焰、放热 黄色火焰、放热、浓烈黑烟 生成物 二氧化碳和水 一氧化碳(或炭黑)、水 方程式2C 2H 2+5O 22H 2O+4CO 2 2C 2H 2+3O 22H 2O+4COA.熄灭酒精灯时,用嘴吹灭B.通电的电热毯着火时,用水浇灭C.篝火晚会时,把木柴架空,有利于木柴充分燃烧D.只要可燃物的温度达到着火点,可燃物就能燃烧【答案】C【解析】A、熄灭酒精灯时,不能用嘴吹灭,应用灯帽盖灭,错误,不符合题意。
B、通电的电热毯着火时,不能用水浇灭,用水浇灭,会有触电的危险,错误,不符合题意。
C、篝火晚会时,把木柴架空,使木柴与空气充分接触,有利于木柴充分燃烧,正确,符合题意。


第六单元《燃烧与燃料》知识提纲一、燃烧与灭火1.燃烧定义:可燃物与发生的剧烈的发光放热的反应。
2.燃烧的条件:①;②;③。
三者缺一不可。
3.灭火的原理:①;②;③。
灭火的实质其实就是破坏燃烧的条件,只需破坏条即可达到灭火目的。
4.促进燃烧的方法:;。
5.着火点:可燃物燃烧所需的温度。
着火点是物质的一种性质,改变。
(填“能”或“否”)6.爆炸的条件:①;②;③;④如果可燃物是气体,需要达到爆炸极限范围内。
7.爆炸极限:爆炸上限:可燃性气体浓度高到不能爆炸的限度。
爆炸下限:可燃性气体浓度低到不能爆炸的限度。
8.含碳元素的物质在氧气时发生充分燃烧,生成;含碳元素的物质在氧气时发生不充分燃烧,生成。
9.检验氢气纯度的方法:收集一试管氢气,用拇指堵住试管口,移近酒精灯火焰,松开拇指,若,证明氢气不纯净;若,证明氢气纯净。
二、化石燃料的利用1.三大化石燃料分别是、、。
2.石油的分馏原理:利用石油中各成分的不同,将其分离出来。
该变化属于变化。
3.被称作“工业的血液”的是,被称作“工业的粮食”的是。
三、大自然中的二氧化碳1、二氧化碳的物理性质:常温下,为色味的体,溶于水,密度比空气,在降温加压的条件下,会变成固态,称作。
2.二氧化碳的实验室制法:①实验室制二氧化碳的两种药品为和(写出其主要成分的化学式)其反应的化学方程式为。
②实验室制取二氧化碳的装置为装置,因为反应物的状态分别为和,而反应的条件不需要。
3.以下是几种固液制气装置A B C D E①试写出这几种装置各自的优点A: B:C: D:E:其中,装置D控制反应停止的原理是使和分离。
②装置A在制取气体时,长颈漏斗下端应,原因是;检验装置A气密性的方法是:4.收集二氧化碳时,应采用法,原因是二氧化碳溶于水,且密度比空气。
若用右图装置收集二氧化碳,应从端进气。
5.检验一瓶气体是否为二氧化碳的方法:6.收集二氧化碳时验满的方法:7.制取二氧化碳时,不用粉末状石灰石的原因是:;不用浓盐酸的原因是:;不用稀硫酸的原因是:。
第六单元燃烧与燃料一、燃烧条件和灭火原理1. 燃烧(1)定义:通常情况下,可燃物与氧气发生的一种发光、放热的剧烈的氧化反应。
(2)燃烧需满足的条件:①可燃物②与空气(或氧气)接触③达到可燃物的着火点可燃物要想燃烧需要同时满足上述3个条件,缺一不可【特别提醒】a. 着火点是可燃物固有的一种属性,与本身的性质有关,一般不会随外界条件的改变而改变,灭火只能降低温度至着火点以下,不能降低着火点。
b. 不是所有的燃烧都有氧气参加,如H2在Cl2中能够燃烧。
(3)促进燃烧的方法及意义①需要足够的空气或氧气,如架空木材,火燃烧更旺。
②增大燃料与空气的接触面积,如工业燃煤时,常将块煤磨成煤粉。
意义:节约能源,减少环境污染。
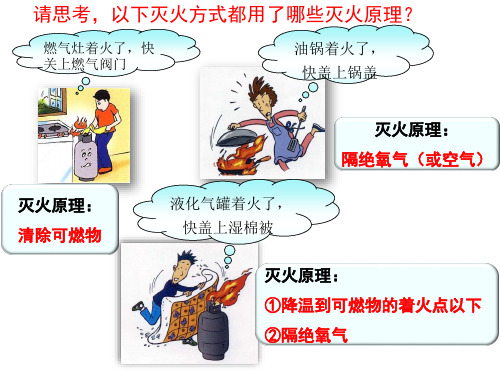
1.灭火原理灭火原理→①清除可燃物(或使可燃物与其他物品隔离);如美国森林大火砍伐出隔离带。
②隔绝氧气(或空气);如做饭油锅起火,用锅盖盖灭。
③使可燃物的温度降低到可燃物的着火点以下。
用水灭火、用嘴吹灭燃烧的火柴。
如果想灭火,只需要满足上述3个条件之一即可灭火二、燃烧条件的探究注意:红磷的着火点为240℃,白磷的着火点为40℃。
(1)铜片的作用:导热。
(2)水的作用:热源、隔绝空气(或氧气)。
2. 实验设计中运用的实验方法(1)对比实验法:铜片上的白磷与红磷对比;铜片上的白磷与水中的白磷对比。
(2)条件控制法:把白磷放入热水中液封隔绝空气(或氧气)。
3.实验设计铜。
4. 实验结论燃烧需要的条件是:可燃物、与氧气(或空气)接触、温度达到可燃物的着火点,三者缺一不可。
5. 装置的评价与改进白磷在空气中燃烧生成的五氧化二磷有毒,会造成空气污染三、易燃易爆物的安全常识1. 爆炸:可燃物在有限的空间内急剧地燃烧,就会在短时间内聚积大量的热,使气体的体积迅速膨胀而引起爆炸。
2. 一些与燃烧和爆炸有关的图标3. 日常生活中的安全常识(1)家用天然气、煤气或液化石油气等泄漏,切不可开灯检查,应关闭阀门并开窗通风。
第六单元燃烧与燃料知识点整理1、燃烧的概念与条件(1)概念:可燃物与________发生的剧烈的_______ 、________的______________。
(2)条件:①物质具有__________②可燃物与__________接触;③可燃物温度达到自身的____________。
(3)注意:着火点指的是可燃物燃烧所需要的最低温度,是物质的一种固有属性,一般情况下不会改变。
2、灭火的原理和方法(1)原理:破坏燃烧的三个条件中的任何一个都可达到灭火的目的即:①清除________或隔离_________;②隔绝_________;③使可燃物温度降到___________以下。
(2)注意:燃烧必须要同时满足三个条件,而灭火只需要破坏燃烧的任何一个条件即可。
3、促进燃烧的方法(1)硫粉燃烧:①在空气中燃烧现象:________________________________;②在氧气中燃烧现象:_______________________________。
③反应的化学方程式为:_______________________。
(2)促进燃烧的方法:①__________________________;②_____________________________。
写出甲烷燃烧的化学方程式:__________________________酒精燃烧的化学方程式___________________________ 4、充分燃烧与不充分燃烧燃烧产物:常用燃料主要组成元素是碳,当氧气充足时,燃料充分燃烧,生成 ________ ,当氧气不足时,燃料不充分燃烧,生成____________。
以碳燃烧为例写化学方程式:____________________、 ______________________5、爆炸:可燃性气体或易燃物粉尘在空气中的_________________ 时,在_______________ 内遇____________,就会发生爆炸。
第六章燃烧与燃料
第一节燃烧与灭火
一.燃烧的条件(重点)
1.燃烧:是可燃物跟氧气发生的剧烈的发光、发热的氧化反应。
(1)燃烧的现象:发光、发热,反应剧烈。
(2)燃烧的反应类型:氧化反应,不一定是化合反应。
(3)燃烧的反应物:常见的燃烧都是可燃物跟氧气发生反应,但是,不是所有的燃烧都一定有氧气参加。
例如,镁就能在二氧化碳中燃烧:2Mg+CO点燃C+2MgO;钠能在氯气中燃烧:2Na+Cl2点燃2NaCl (4)燃烧的反应条件:点燃
(5)燃烧的分类及燃烧的产物
注意:
①“完全燃烧”和“不完全燃烧”又叫“充分燃烧”和“不充分燃烧”
②要掌握含C、H、O等元素的燃料完全燃烧的化学方程式:
2.燃烧的条件:
①物质具有可燃性
②可燃物要与氧气接触;
③温度达到可燃物其自身的着火点(即可燃物燃烧所需要的最低温度)
燃烧必须要同时满足三个条件,才能发生燃烧的现象。
二.灭火的原理:
①.移走可燃物
②.隔绝氧气
③.使温度降到着火点以下
1.灭火原理实质就是破坏物质燃烧的条件,三者破坏其一即可灭火。
2.几种常见的灭火方法:
(1)移走可燃物:森林火灾开辟隔离带,管道煤气着火先关掉阀门,釜底抽薪等;
(2)隔绝氧气:酒精灯用灯冒盖灭,油锅着火用用锅盖盖灭,向着火的木柴上覆盖沙子,少量酒精燃烧用湿抹布盖灭等;
(3)使温度降到着火点以下:用水等大量的冷却剂灭火,用嘴将灯吹熄,
(4)用灭火器灭火:①泡沫灭火器:可用于扑灭木材、棉布等燃烧而引起的一般火灾,不能用于扑灭电器火灾;②干粉灭火器:除了用来扑灭一般火灾外,还用于扑灭电器、油、气等燃烧引起的火灾;③液态二氧化碳灭火器:用于扑灭图书档案、贵重设备、精密仪器的火灾。
3.二氧化碳与灭火
(1)原理:二氧化碳不能燃烧也不能支持燃烧,且密度比空气大。
(2)灭火器主要是用二氧化碳灭火,二氧化碳不能扑灭所有的火灾:如镁带燃烧就不能用二氧化碳扑灭。
4火灾处置、自救
(1)火警电话:119
(2)电器、管道煤气、天然气着火,首先要关闭电源或气阀。
(3)楼层着火,人应用湿毛巾捂住口鼻,沿墙壁匍匐前进,脱离火灾区。
(4)室内火灾,不能打开门窗。
空气流通会让火势更旺。
(5)森林火灾,应从逆风方向逃离。
三.促进可燃物燃烧的方法:
1.增大氧气的浓度:木炭燃烧:C+O2(氧气充足)点燃 CO2 ;2C+O2(氧气不足)点燃 2CO;给锅炉鼓风,增加空气供给量。
2.增大可燃物与氧气的接触面积:煤制成蜂窝煤、粉成煤粉;柴油机把柴油喷成雾状燃烧等。
四.爆炸及易燃物、易爆物的安全知识
1.爆炸:可燃物在有限的空间内迅速发生反应,瞬间放出大量的热;气体的体积急剧膨胀,就产生了爆炸。
2.易发生爆炸的物质:可燃性气体、粉尘。
3.爆炸的条件:与氧气或空气充分接触;遇到高温、明火或撞击。
4.爆炸极限:可燃气体与空气形成混合气体,遇明火发生爆炸的浓度范围(即可燃气体占混合气体的体积分数范围)。
可燃性气体浓度低到不能发生爆炸的限度,称为爆炸下限;可燃性气体浓度高到不能发生爆炸的限度,叫爆炸上限。
5.与燃烧、爆炸有关的消防标识
燃烧爆炸缓慢氧化自然
概念可燃物跟氧气发生的剧烈的
发光、发热的氧化反应
在有限的空间内
发生的急速燃烧
缓慢进行的氧化
反应
由缓慢氧化引起
的自发的燃烧
温度达到了着火点达到了着火点没有达到着火点达到了着火点
现象发热、发光发热、发光只放热、不发光发热、发光
联系都是氧化反应,都有热量放出,只是反应的剧烈程度不同。
六.一氧化碳的性质
1.物理性质:无色,无味,难溶于水,密度比空气略小。
2.化学性质:
(1)可燃性:2CO+O2点燃2CO2
燃烧时,有淡蓝色火焰,常用作燃料。
煤气主要成分是CO、H2O(制取方法:C+H2O高温CO+H2)
(2)还原性:3CO+Fe2O高温2Fe+3CO2;加热Cu+CO2
常用于冶炼金属
(3)毒性:CO和人体血红蛋白的结合,使血液失去了输氧能力,导致CO中毒。
吸入较多会缺氧而窒息死亡。
所以应注意:①点燃CO前,要检验CO的纯度,以防CO中混有空气、氧气,而发生爆炸。
②冬天用煤炉取暖时,要保持良好的的通风和有效的排气通道,以确保安全。
③在作有关CO的试验时,要做好尾气处理,以防污染环境。
第二节化石燃料及其应用
一.化石燃料
化石燃料是由古代动植物埋在地层下,经过漫长的、一系列非常复杂的变化而逐渐形成的混合物。
属不可再生资源。
三大化石燃料的比较:。