离子色谱法测定水果中氟离子
- 格式:doc
- 大小:82.00 KB
- 文档页数:3

水中氟化物的测定方法一、离子选择电极法离子选择电极法是一种常用的测定水中氟化物含量的方法。
该方法利用离子选择电极对水中的氟离子进行选择性测定,通过测量电极的电位变化来确定氟化物的浓度。
该方法操作简便、快速,且具有较高的准确性和灵敏度,适用于水质监测和环境分析等领域。
二、离子色谱法离子色谱法是一种常用的测定水中氟化物含量的方法。
该方法利用离子交换柱将样品中的氟离子与其他离子分离,再通过色谱柱分离和检测,最终得到氟化物的浓度。
离子色谱法具有高分辨率、高灵敏度和高选择性的特点,适用于各种水样的氟化物测定。
三、离子选择电极与离子色谱法相结合离子选择电极与离子色谱法相结合是一种常用的测定水中氟化物含量的方法。
该方法先利用离子选择电极对水样中的氟离子进行快速筛选,然后再使用离子色谱法对筛选出的样品进行精确测定。
这种组合方法兼具快速筛选和准确测定的优点,能够满足不同场合对氟化物测定的需求。
四、紫外分光光度法紫外分光光度法是一种常用的测定水中氟化物含量的方法。
该方法利用氟化物与酸性溴酸钾反应生成溴离子,溴离子在紫外光的照射下产生吸收,通过测量吸收光强的变化来确定氟化物的浓度。
紫外分光光度法具有简单、快速、灵敏度高的特点,适用于水质监测和环境分析等领域。
五、电化学法电化学法是一种常用的测定水中氟化物含量的方法。
该方法利用电极与水样中的氟离子发生氧化还原反应,通过测量电流或电位的变化来确定氟化物的浓度。
电化学法具有灵敏度高、准确性好的特点,适用于水质监测和环境分析等领域。
六、离子交换法离子交换法是一种常用的测定水中氟化物含量的方法。
该方法利用具有特定功能基团的离子交换树脂与水样中的氟离子进行吸附和解吸,通过测定解吸液中氟离子的浓度来确定氟化物的含量。
离子交换法具有操作简便、准确性高的特点,适用于水质监测和环境分析等领域。
水中氟化物的测定方法有离子选择电极法、离子色谱法、离子选择电极与离子色谱法相结合、紫外分光光度法、电化学法和离子交换法等。

离子色谱法测定水中氟化物的方法分析与探讨[摘要] 氟广泛存在于自然水体中,人体各组织中都含有氟,但主要积聚在牙齿和骨筋中。
适当的氟是人体所必需的,过量的氟对人体有危害,氟化钠对人的致死量为6-12克,饮用水含2.4-5毫克/升则可出现氟骨症。
因此,为了能够准确测定水中氟化物的含量,本文采用了离子色谱法对水中氟化物的方法进行了分析与探讨。
通过空白试验、方差分析、加标回收试验、标准差检验以及质量控制图等方式,对实验室环境和分析人员技术水平进行检验和评价。
经试验表明,实验测定检出限低于标准方法检出限;批内和批间变异不显著;总标准差结果均小于指标检出限;加标回收率均值为101.7%;质量控制图分布在合理范围之内。
[关键词] 氟化物;离子色谱法;精密度;分析1 引言氟化物存在于整个地壳之中,在自然界广泛分布。
某些食物和水含有氟化物。
饮用水中经常添加氟化物,以减少牙齿龋坏。
20世纪30年代,研究人员发现长期饮用氟化水的人群患龋齿的几率比不含氟化水地区的人群要少三分之二。
往美国牙医协会、世界卫生组织和美国医学协会,以及其他组织都认可在饮用水中添加氟化物有助于减少牙齿龋坏。
适当的氟是人体所必需的,过量的氟对人体有危害,主要使骨骼受害,表现肢体活动障碍,重者骨质疏散或变形,易于自发性骨折。
其次是牙齿脆弱,出现斑点、损害皮肤,出现疼痛、湿疹及各种皮炎。
氟化氢对呼吸器官有刺激作用,引起鼻炎、气管炎,使肺部纤维组织增生。
氟会影响肝脏的新陈代谢,降低肝脏解毒功能,使血浆白蛋白降低;过多的氟化物也会沉积在骨骼中导致骨头硬化,影响骨髓的造血功能。
氟化钠对人的致死量为6-12克,饮用水含2.4-5毫克/升则可出现氟骨症。
2017年10月27日,世界卫生组织国际癌症研究机构公布的致癌物清单初步整理参考中,将氟化物(饮用水中添加的无机物)确定为3类致癌物。
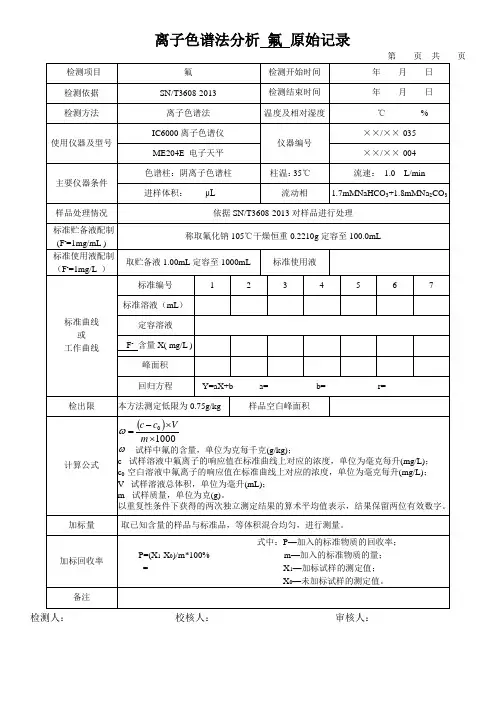
2 方法内容2.1 方法原理水质样品中的阴离子,经阴离子色谱柱交换分离,抑制型电导检测器检测,根据保留时间定性,峰高或峰面积定量。

苹果与梨中的氟食品中痕量级金属和其它元素比色法A原理14-17A中用HCl淋洗和酸化制备的苹果与梨的溶出液可被用于此。
取一份滤液,用KMnO4氧化至无色后再用H2NOH还原,并取出一小份溶液于Nessler管中,以红紫素〔1,2,4-三羟基蒽醌〕为指示剂,用Zr(NO3)4反滴定之。
在此,反滴定的原理与常用方法中Th(NO3)4滴定茜素类似。
采取措施除去干扰性阴离子,并采用高酸度的滴定条件,以减少能引起指示剂色淀的金属离子的干扰。
B仪器B.1奈斯勒比色管50ml,带玻塞,高型,且每组管的高度刻度与颜色要一致。
C试剂C.a混合硝酸盐溶液将3.0gBa(NO3)2与2.0gTh(NO3)4·4H2O溶于H2O并稀释至100ml。
C.b高锰酸钾溶液饱和,约6%。
C.c盐酸羟氨溶液5%。
C.d氯化亚铁溶液将大约1.0g的铁粉或铁丝溶于50mlHCl(1+1)中,稀释,过滤到500ml容量瓶中,加入几毫升5%H2NOH·HCl溶液并稀释至刻度。
必要时可于使用前进一步稀释。
C.e红紫素指示剂0.01%乙醇溶液。
溶解25mg纯1,2,4-三羟基蒽醌于乙醇中,必要时可适当加热,并以乙醇稀释至250ml。
每星期重新配制。
C.f硝酸锆溶液将1.50gZr(NO3)4·5H2O溶于H2O,加20mlHCl酸化后稀释至1L。
若溶液不澄清则应过滤。
C.g氟标准溶液54.5μgF/ml。
将0.1464gNaF溶于H2O并稀释至1L。
D测定取20ml混合均匀的酸性溶出滤液,14-17A,于50ml容量瓶中,加入2.0ml混合硝酸盐溶液和4.0mlKMnO4溶液,用少量H2O冲洗瓶颈内壁,放入蒸汽浴中5min。
取出容量瓶,趁热转动容量瓶边用滴定管慢慢加入5%的H2NOH·HCl溶液,直至MnO2溶解,溶液无色,然后再多加0.5ml过量的H2NOH·HCl。
〔可以明显地看到磷酸盐转化成絮状Th3(PO4)4沉淀,硫酸盐转化成BaSO4沉淀。

投稿邮箱:sjzxyx88@世界最新医学信息文摘 2018年第18卷第57期155·医学检验·0 引言根据《生活饮用水卫生标准GB5749-2006》里106项水质检测项目中,氟化物、氯化物、硝酸盐、硫酸盐均为水质常规指标[1],都为必检项目,本实验室为了提高工作效率,现采用离子色谱法对生活饮用水中上述各离子一次性同时测定,现将实验方法报告如下。
1 材料与方法1.1 原理水样中的待测阴离子随氢氧化钾(或氢氧化钠)淋洗液进入阴离子交换分离系统(由保护柱和分离柱组成),根据分析柱对各种离子的亲和力不同进行分离,已分离的阴离子流经阴离子抑制系统转化成具有高电导率的强酸,而淋洗液则转化成低电导率的水,由电导检测器测量各种阴离子组分的电导率,以保留时间定性,峰高或峰面积定量[2]。
1.2 仪器北京历元EP2000型离子色谱仪,Dionex IonPac AG11(4×50mm)阴离子保护住,Dionex IonPac AS11(4×250mm)阴离子分析柱,MES-100型阴离子抑制器,LX-50A 自动淋洗液发生器,24位自动进样器,电导检测器,EASY-2016AIO 色谱工作站,北京爱斯泰克CSR-1-30(Ⅱ)超纯水处理器。
1.3 试剂实验用水均为18.2MΩ·cm 的二次去离子水;1000mg/L的F -、Cl -、NO 3-、SO 42-标准贮备液,由坛墨质检标准物质中心提供;优级纯KOH,来自天津市科密欧化学试剂有限公司;扎鲁特旗疾病预防控制中心提供的自来水样品。
1.4 色谱条件淋洗液:8.5mmol/L KOH,等度淋洗;流速:1.1mL/min;柱温:30℃;进样量:50.0μL。
1.5 样品处理将水样经过0.22μm 水系微孔滤膜过滤除去悬浮颗粒,直接进样分析。
1.6 标准系列的配置(1)分别准确吸取F -、Cl -、NO 3-、SO 42-标准贮备液2.50mL、15.00mL、20.00mL、30.00mL 于500mL 容量瓶中,用二次去离子水稀释到标线,成混合标准使用液Ⅰ,F -、Cl -、NO 3-、SO 42-标准浓度分别为5.00、30.00、40.00、60.00mg/L。

离子色谱法测定氯离子、氟离子、溴离子、硝酸根和硫酸根1. 适用范围本方法适用于地下水中氯离子,氟离子,溴离子,硝酸根和硫酸根的测定。
进样100μL时,本方法的最低检测浓度为:Cl-0.1mol/L,SO42-0.2mol/L,NO3-0.02 mol/L,F-0.006mol/L,Br-0.03mol/L。
检测上限为:Cl-12.0mg/L,SO42-12.0 mg/L,NO3-10.0 mg/L,F-1.0 mg/L,Br-1.6 mg/L。
2. 原理水样注入仪器后,在淋洗液的携带下,流经填充了低容量阴离子交换树脂的分离柱。
由于待测离子的离子半径大小,电荷多少和其它性质的不同,它们对阴离子交换树脂的亲合力各异,故在淋洗液和交换树脂之间的分配系数也不相同。
在分离柱中,经过多次洗脱与交换后,按F-,Cl-,Br-,NO3-,SO42-的顺序依次被分离开来,然后流过阴离子抑制柱以降低溶液的背景电导,最后通过电导检测器,依次对它们进行测量。
从同样条件下绘制的标准曲线上,即可求出水样中F-,Cl-,Br-,NO3-,SO42-的含量。
3. 试剂除非另有说明,本方法所用试剂均为分析纯,水为电导率<1μs/cm的重蒸馏水或去离子水。
3.1 淋洗液:称取2.5203g碳酸氢钠(NaHCO3)溶于适量水中,另称取2.6498 g无水碳酸钠(Na2CO3)溶于适量水中,将上述两种溶液倒入10L塑料桶中(事先在10L 处作好标记),以重蒸馏水冲稀至标线。
注:增加淋洗液的浓度,能缩短各离子的保留时间,但对每种离子的影响程度不同。
保留时间长的SO42-,缩短时间的幅度较大;而保留时间短的F-,缩短的幅度就比较小,增加淋洗液的流量,也会产生上述情况,但变化程度较小。
因此,通过改变淋洗液的浓度和流量,可以改变色谱图形,从而选择灵敏度高,分辨率好,速度快的最佳分析条件。
但应注意不同的柱子对淋洗液的组成和浓度有不同的要求。


离子色谱法测定造纸废水中的氟离子浓度
一、标线的绘制
氟离子标准贮备液,1000mg/l:称取2.2323g氟化钠(纯度99%)(105℃烘干2h)溶于水,移入1000ml容量瓶中,加入10ml淋洗贮备液,用水稀释到标线。
利用F-标准储备溶液稀释成浓度为0.10、0.20、0.50、1.00、2.00、5.00 mg/L系列标准溶液,进样分析。
以浓度(c)为横坐标,以峰面积(A)为纵坐标进行线性回归,得到线性方程。
二、样品预处理
样品采集后立即经0.45um微孔滤膜过滤,可直接放入聚乙烯样品瓶,压上瓶盖放入进样器中进行分析。
如不能马上分析,密封放入冰箱4℃保存,保存时间不超过24h。
三、色谱条件
色谱柱:MetrsepA supp5-150/4.0阴离子分离柱;
检测器:CD心A电导率检测器;
淋洗液:3.2mM Na2C03/1.0mM NaHC03;
流速:2.0ml/min;
再生液:1moL/L HN03;
进样量:2ml。
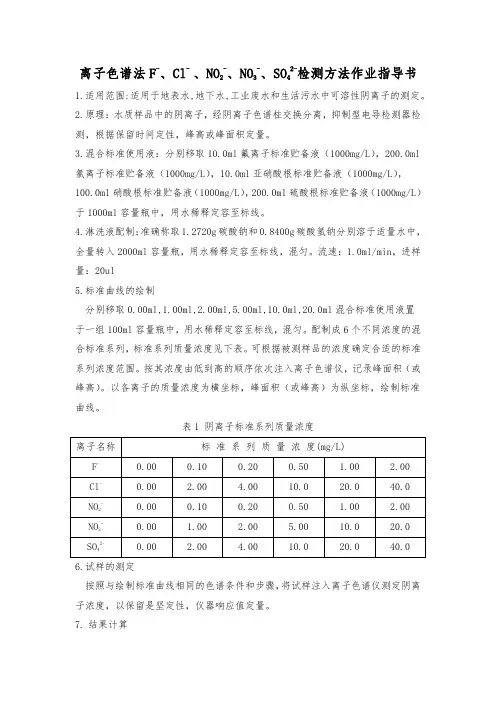
离子色谱法F-、Cl-、NO2-、NO3-、SO42-检测方法作业指导书1.适用范围:适用于地表水,地下水,工业废水和生活污水中可溶性阴离子的测定。
2.原理:水质样品中的阴离子,经阴离子色谱柱交换分离,抑制型电导检测器检测,根据保留时间定性,峰高或峰面积定量。
3.混合标准使用液:分别移取10.0ml氟离子标准贮备液(1000mg/L),200.0ml 氯离子标准贮备液(1000mg/L),10.0ml亚硝酸根标准贮备液(1000mg/L),100.0ml硝酸根标准贮备液(1000mg/L),200.0ml硫酸根标准贮备液(1000mg/L)于1000ml容量瓶中,用水稀释定容至标线。
4.淋洗液配制:准确称取1.2720g碳酸钠和0.8400g碳酸氢钠分别溶于适量水中,全量转入2000ml容量瓶,用水稀释定容至标线,混匀。
流速:1.0ml/min,进样量:20ul5.标准曲线的绘制分别移取0.00ml,1.00ml,2.00ml,5.00ml,10.0ml,20.0ml混合标准使用液置于一组100ml容量瓶中,用水稀释定容至标线,混匀。
配制成6个不同浓度的混合标准系列,标准系列质量浓度见下表。
可根据被测样品的浓度确定合适的标准系列浓度范围。
按其浓度由低到高的顺序依次注入离子色谱仪,记录峰面积(或峰高)。
以各离子的质量浓度为横坐标,峰面积(或峰高)为纵坐标,绘制标准曲线。
表1阴离子标准系列质量浓度离子名称标准系列质量浓度(mg/L)F-0.000.100.200.50 1.00 2.00 Cl-0.00 2.00 4.0010.020.040.0 NO2-0.000.100.200.50 1.00 2.00NO3-0.00 1.00 2.00 5.0010.020.0SO42-0.00 2.00 4.0010.020.040.06.试样的测定按照与绘制标准曲线相同的色谱条件和步骤,将试样注入离子色谱仪测定阴离子浓度,以保留是坚定性,仪器响应值定量。

2011年12月December2011岩 矿 测 试ROCKANDMINERALANALYSISVol.30,No.6761~767收稿日期:2010-11-02;接受日期:2010-12-27基金项目:国土资源地质大调查项目(1212010916020)作者简介:赵怀颖,助理研究员,从事化学分析测试方法研究。
E mail:rainnowying@gmail.com。
文章编号:02545357(2011)06076107高温燃烧水解-离子色谱法测定植物样品中的氟赵怀颖,孙德忠,曹亚萍,郭 琳,胡明月(国家地质实验测试中心,北京 100037)摘要:建立了高温燃烧水解-离子色谱测定植物样品中不同含量范围氟的分析方法,色谱条件为DionexIonPacAS18分离柱(4mm×250mm),DionexIonPacAG18保护柱(4mm×50mm),ASRSULTRAⅡ自动再生微膜抑制器,电导检测器。
采用纯水作为吸收介质,使样品溶液与标准溶液基体一致,过滤后可直接测定。
样品溶液中常见的Cl-、NO-3、SO2-4、PO3-4、CO2-3、HCO-3等阴离子不干扰F-的测定。
为消除样品热解过程中产生的乙酸干扰,对氟含量较高(xx~xxxμg/g)的样品,采用20mmol/L的NaOH淋洗液等度淋洗,进样体积为25μL;对氟含量较低的样品(0.x~xμg/g),进样体积为100μL。
方法具有较宽的线性范围和较好的稳定性,检出限为0.5mg/kg,适用于痕量分析;应用于灌木枝叶和茶叶等4个氟含量较高(xx~xxxμg/g)的植物标准物质的测定,相对标准偏差(RSD)<6%(n=6);应用于低氟的小麦粉和大米粉样品测定,加标回收率为90%~110%,可以满足不同氟含量植物样品中氟测定的需要,具有自动化程度高、操作简单、对环境友好等特点。
关键词:高温燃烧水解;离子色谱法;氟;水吸收;氢氧化钠淋洗QuantificationofFluorineinPlantsbyHighTemperatureCombustionHydrolysis IonChromatographyZHAOHuai ying,SUNDe zhong,CAOYa ping,GUOLin,HUMing yue(NationalResearchCenterforGeoanalysis,Beijing 100037,China)Abstract:Anewmethodforthedeterminationoffluorineinplantswasdevelopedbyhightemperaturecombustionhydrolysis IonChromatography.ChromatographicconditionswereselectedasDionexIonPacAS18separationcolumn(4mm×250mm),DionexIonPacAG18protectcolumn(4mm×50mm),ASRSULTRAⅡsuppressor(4mm)andconductivitydetection.Thefluorineionwasabsorbedbypurewater,whichprovidedthesamematrixbetweenthesamplesolutionandthestandardsolution.ThesamplesolutionwasanalyzeddirectlybyIonChromatographywithasimpleprocedureandlowcostafterfiltration.TheanionssuchasCl-,NO-3,SO2-4,PO3-4,CO2-3,HCO-3havenointerferenceswithF-,excepttheaceticacidproducedintheprocessofpyrolysis.Inordertoeliminatetheinterferencefromaceticacid,20mmol/LNaOHsolutionwasusedasequaleluentforhigherfluorinesample(xx-xxxμg/g)withthe25μLsamplevolume,whileforlowerfluorinesample(0.x-xμg/g)withthe100μLsamplevolume.Thenewmethodhaswidelinearrange,highstabilityandalowdetectionlimitasof0.5mg/kg.Fourplantreferencematerialsofshrubandteawithhigherfluorinecontents(xx-xxxμg/g)werestudiedastherelativeerrorislowerthan10%andtherelativestandarddeviationislowerthan6%.Forwheatandricesampleswhichhavelowerfluorinecontent,therecoverybystandardadditionis90%-110%.Comparedwithionselectiveelectrodeandspectrophotometry,IonChromatographycanbeusedforsampleswithalargerrangeoffluorineconcentration,andhastheadvantagesofhighautomation,easyoperationandisenvironmentallyfriendly.Keywords:hightemperaturecombustionhydrolysis;ionchromatography;fluorine;absorptionwithwater;NaOHeluting—167—Copyright ©博看网. All Rights Reserved.生物样品中的氟是生态地球化学调查的必测元素,其含量很低[1-2]。

包装工程第44卷第23期·26·PACKAGING ENGINEERING2023年12月氧弹燃烧-离子色谱法测定一次性食品接触用生物基塑料中氟含量陈杰,姚皓程,刘斌,董犇,陈燕芬,李丹*,钟怀宁(广州海关技术中心,广州510623)摘要:目的建立并优化氧弹燃烧-离子色谱法测定一次性食品接触用生物基塑料(下文简称生物基塑料)中氟含量的检测方法,分析市售生物基塑料产品中氟含量情况。
方法生物基塑料经氧弹燃烧发生高温氧化分解,氟化物转化为游离态氟离子,被吸收或溶解在吸收液中,以5.0 mmol/L碳酸氢钠和1.0 mmol/L 无水碳酸钠溶液作为流动相进行等度洗脱,进样量为20 μL,流速为0.8 mL/min;采用Metrosep A Supp 7色谱柱(250 mm×4.0 mm, 5.0 μm)和Metrosep A Supp 5 Guard保护柱(50 mm×4.0 mm, 5.0 μm),柱温为45 ℃;以电导检测器进行测定,外标法定量。
结果氧弹燃烧-离子色谱法测定生物基塑料中氟含量的相关系数R2>0.995,检出限为5.0 mg/kg,定量限为10 mg/kg,线性关系良好,加标回收率为93.8%~98.4%,精密度为2.9%~6.8%(n=6)。
通过对119款实际样品中氟含量进行定量分析,总体检出率为94.11%,总体不合格率为15.94%;PLA吸管、PLA+PBAT吸管和PLA+PBS吸管的检出率均为100%,不合格率分别为45.16%、30.77%和5.88%。
结论该方法可靠、方便、灵敏,分离效果好,适用于生物基塑料中氟含量的检测。
关键词:氟;离子色谱法;氧弹燃烧;食品接触材料;生物基塑料中图分类号:TB484;O657.7 文献标识码:A 文章编号:1001-3563(2023)23-0026-10DOI:10.19554/ki.1001-3563.2023.23.004Determination of Fluorine in Disposable Food-contact Bio-based Plastics byOxygen Bomb Combustion-ion ChromatographyCHEN Jie, YAO Hao-cheng, LIU Bin, DONG Ben, CHEN Yan-fen,LI Dan*, ZHONG Huai-ning(Guangzhou Customs Technology Center, Guangzhou 510623, China)ABSTRACT: The work aims to establish and optimize a method for the determination of fluorine in disposable food-contact bio-based plastics (hereinafter referred to as bio-based plastics) by oxygen bomb combustion-ion chroma-tography, and analyze the fluorine content of commercially available bio-based plastic products. The oxidative decom-position of bio-based plastics occurred at high temperature by oxygen bomb combustion, and the fluoride was converted into free fluoride ions, which were absorbed or dissolved in the absorbent solution, and then eluted with 5.0 mmol/L sodium bicarbonate and 1.0 mmol/L anhydrous sodium carbonate solution as the mobile phases, with an injection volume of 20 μL and a flow rate of 0.8 mL/min. The determination was carried out on a Metrosep A Supp 7 column (250 mm×4.0 mm, 5.0 μm) and Metrosep A Supp 5 Guard column (50 mm×4.0 mm, 5.0 μm) at a column temperature of收稿日期:2023-10-09基金项目:国家重点研发计划项目(2022YFF0607202);国家自然科学基金青年基金项目(42207550)*通信作者第44卷第23期陈杰,等:氧弹燃烧-离子色谱法测定一次性食品接触用生物基塑料中氟含量·27·45 ℃ with a conductivity detector, and was quantified by external standard method. The correlation coefficient for thedetermination of fluorine content in bio-based plastics by oxygen bomb combustion-ion chromatography R2 >0.995, the limit of detection (LOD) was 5.0 mg/kg, and the limit of quantification (LOQ) was 10 mg/kg, with good linearity, the spiked recoveries were in the range of 93.8%-98.4%, and the precision ranged from 2.9 to 6.8% (n=6). By quantitatively analyzing the fluorine content in 119 actual samples, the overall detection rate was 94.11%, and the overall failure rate was 15.94%. The detection rate in PLA straws, PLA+PBAT straws and PLA+PBS straws was 100%, and the failure rate was 45.16%, 30.77% and 5.88%, respectively. The method is reliable, convenient, sensitive, with good separation effect, and suitable for the determination of fluorine content in bio-based plastics.KEY WORDS: fluorine; ion chromatography; oxygen bomb combustion; food-contact materials; bio-based plastics随着人们对环境保护和可持续发展的日益关注,生物基塑料作为替代传统塑料的新型材料逐渐受到广泛应用[1-2],如聚乳酸(PLA)、聚丁二酸丁二酯(PBS)和聚己二酸对苯二甲酸丁二醇(PBAT)等[3-7]。
离子色谱法测定水果中阳离子Na+、NH4+、K+、Mg2+、Ca2+的含量刘玉芬;夏海涛;连桂香【期刊名称】《食品科学》【年(卷),期】2005(026)012【摘要】利用离子色谱法测定了五种水果(苹果、梨、橙子、菠萝、草莓)中的阳离子Na+、NH4+、K+、Mg2+、Ca2+,色谱柱为IonPAC CS12A阳离子交换柱,淋洗液为硫酸,ECD-40电导检测器检测,外标法定量.分析结果表明,五种常见阳离子的线性关系良好,它们的检出限为0.01~0.1mg/L,回收率为93.2%~102.7%,相对标准偏差在0.72%~3.92%之间.该方法具有简单、快速、准确等优点,为检测其它食品中Na+、NH4+、K+、Mg2+、Ca2+的含量提供了一种有效的方法.【总页数】3页(P182-184)【作者】刘玉芬;夏海涛;连桂香【作者单位】淮海工学院化学工程系,江苏,连云港,222005;淮海工学院化学工程系,江苏,连云港,222005;齐齐哈尔大学生命科学学院,黑龙江,齐齐哈尔,16l006【正文语种】中文【中图分类】O657【相关文献】1.离子色谱法同时测定烟叶中的K+、Na+、Ca2+、Mg2+和NH4+ [J], 郭紫明;庹苏行;吴名剑;李辉2.离子色谱法测定水果和饮料中Na+、NH4+、K+、Mg2+、Ca2+、Zn2+的含量 [J], 王宇昕;于泓3.工业循环冷却水中Na+,NH4+,k+,Mg2+,Ca2+的测定———离子色谱法[J], 蒋仁依;邵维仁4.离子色谱法测定矿泉水中K+、Ca2+、Na+、Mg2+、Cl-、SO2-4 [J], 刘耀华;杨文武5.离子色谱法测定饮用水中的Li+、Na+、NH4+、F+、Mg2+、Ca2+ [J], 李晓莲;杜苏趁因版权原因,仅展示原文概要,查看原文内容请购买。
中疾控职业卫生所氟的离子色谱
在职业卫生领域,氟的离子色谱通常用于监测工作场所中氟化物的浓度。
氟化物是一种常见的化学物质,它在许多工业过程中都有使用,但高浓度的氟化物对工人的健康可能会造成危害。
因此,利用离子色谱技术监测工作场所中氟化物的浓度对于评估工作环境的安全性非常重要。
除了在工作场所监测中的应用,氟的离子色谱也可以用于环境监测和食品安全等领域。
通过对水、土壤、空气中的氟化物进行监测,可以评估环境中的氟化物污染情况,从而采取相应的环境保护措施。
在食品安全方面,离子色谱技术也可以用于检测食品中的氟化物残留,确保食品安全。
总的来说,中疾控职业卫生所使用氟的离子色谱技术是为了监测和评估工作场所和环境中氟化物的浓度,以保障工人和公众的健康安全。
这种分析技术的应用有助于及时发现潜在的健康风险,并采取相应的控制措施,从而保障职业卫生和环境安全。
离子色谱法测定地表水中氟化物含量的不确定度评价离子色谱法是一种常用的测定地表水中氟化物含量的方法。
该方法使用高效离子交换柱进行分离,并通过离子色谱仪测定样品中氟化物的浓度。
无论使用何种分析方法,都会存在一定的不确定度。
评价不确定度对于确定测定结果的可靠性至关重要。
本文将对离子色谱法测定地表水中氟化物含量的不确定度进行评价和讨论。
我们需要确定离子色谱法测定地表水中氟化物含量的主要不确定度来源。
在离子色谱法中,可能的不确定度来源包括但不限于:仪器本身的误差、环境条件的影响、标准溶液的准确度、样品制备的影响等。
接下来,我们将对这些不确定度来源进行定量评价。
对于仪器本身的误差,我们可以通过仪器的校准和稳定性测试来确定其误差范围。
通常情况下,离子色谱仪具有较高的准确度和稳定性,因此其对测定结果的影响较小。
仪器的精度和重复性仍然需要进行定量评价。
环境条件的影响是另一个重要的不确定度来源。
温度、湿度等环境条件的变化可能会影响离子色谱分析的结果。
我们需要对环境条件的影响进行定量评价,并将其考虑在测定结果的不确定度中。
标准溶液的准确度也会对测定结果产生影响。
通常情况下,我们会使用一系列不同浓度的标准溶液来建立标准曲线,并根据标准曲线来计算样品中氟化物的浓度。
标准溶液的准确度对测定结果的不确定度有着重要的影响。
样品制备的影响也需要进行定量评价。
样品制备的不当可能会导致样品中氟化物含量的误差。
我们需要对样品制备的影响进行定量评价,并将其考虑在测定结果的不确定度中。
在对这些不确定度来源进行定量评价后,我们可以计算出离子色谱法测定地表水中氟化物含量的整体不确定度。
这种不确定度的计算可以采用“合成不确定度”的方法,即将各个不确定度来源的贡献相加得出整体不确定度。
最终,我们可以得出离子色谱法测定地表水中氟化物含量的不确定度范围,并对其进行评价和讨论。
在评价和讨论不确定度时,我们需要考虑到实际情况中可能存在的一些特殊因素。
如果某些不确定度来源的影响较小,我们可以对其进行适当的简化处理;如果某些不确定度来源的影响较大,我们需要对其进行更为详细的定量评价。
浅析氟化物的几种检测方法氟化物是一种常见的无机化合物,广泛存在于自然环境中,也是许多工业生产过程中的重要原料。
然而,尽管有其重要的应用价值,氟化物对人体和环境都具有一定的危害性。
因此,对于氟化物的准确检测和监测就显得非常重要。
本文将对氟化物的几种常用检测方法进行浅析。
1.离子选择电极(ISE)法离子选择电极法是一种简便、快速、准确的氟化物检测方法。
该方法主要是利用氟化物和可溶性氟化物电极间的电势差测定氟化物的浓度。
这种电极由一种特殊的离子选择膜构成,能够选择性地吸附氟离子,从而使电极的电位发生变化。
正是这种特殊性能使得电极能够快速准确地检测氟化物的浓度。
2.离子色谱法离子色谱法是一种高灵敏度的氟化物检测方法,它基于溶液中离子的分离和检测原理。
该方法通过将氟化物样品溶液注入色谱柱中,利用特定的分离柱分离出溶液中的氟化物离子,然后通过检测器对其进行定量分析。
离子色谱法具有高精度、高选择性和高灵敏度的特点,广泛应用于水质检测、环境监测和食品安全等领域。
3.光度法光度法是一种通过测量氟离子或其与其他物质产生的化学反应产物对可见光的吸光度来确定氟化物浓度的方法。
它通常通过在氟化物样品中添加其中一种试剂,使其与氟化物发生特定反应产生有色的产物,再通过测量产物对可见光的吸光度来确定氟化物浓度。
光度法操作简单、灵敏度高,特别适合于氟化物浓度较低的情况下进行分析。
4.电极化学法电极化学法是利用电化学技术进行氟化物浓度测定的方法。
常用的有极谱法和阻抗法。
极谱法是通过测定电极表面氟化物在电势控制下产生的氧化或还原电流来确定氟化物浓度。
阻抗法是通过测定电极表面氟化物与试剂产生的反应导致电极界面上电荷传递过程的电阻变化来测定氟化物浓度。
电极化学法具有灵敏度高、选择性好等优点,适用于低浓度氟化物的分析。
综上所述,氟化物的几种常用检测方法各有优劣,根据实际需要选择合适的方法进行分析。
离子选择电极法和离子色谱法适用于氟化物浓度较高的情况,操作简单,灵敏度高。
离子色谱法同时测定附子理中丸中9种无机阴离子含量谢玉惠;龙兴浩【期刊名称】《安徽医药》【年(卷),期】2016(020)008【摘要】目的:建立同时测定附子理中丸中9种无机阴离子(氟离子、甲酸根离子、氯离子、亚硝酸根离子、溴离子、硝酸根离子、硫酸根离子、草酸根离子和磷酸根离子)含量的离子色谱法。
方法采用 Ion Pac AS11-HC 阴离子交换分析色谱柱,ASRS 300(250 mm ×4 mm)阴离子抑制型电导检测器检测,7~40 mmol·L -1氢氧化钾溶液梯度淋洗20 min,平衡5 min,流速为1.0 mL ·min -1,柱温为35℃,进样量为20μL。
结果9种无机阴离子达到良好分离,0.1~10 mg·L -1的线性关系良好,相关系数为0.9990~0.9998,精密度的 RSD 为0.5%~1.7%,重复性的 RSD 为0.8%~2.7%,稳定性的 RSD 为1.1%~2.9%,平均加样回收率为89.18%~106.81%间,RSD 为0.51%~2.73%(n =6),检测限为0.004~0.023 mg·L -1,定量限为0.015~0.018 mg·L -1。
结论该方法快速简单,选择性好,灵敏度高,适用于附子理中丸中9种无机阴离子的含量测定。
【总页数】5页(P1490-1493,1494)【作者】谢玉惠;龙兴浩【作者单位】重庆市沙坪坝区陈家桥医院药剂科,重庆 401331;重庆市沙坪坝区陈家桥医院药剂科,重庆 401331【正文语种】中文【相关文献】1.离子色谱法同时测定大蒜鳞茎中7种无机阴离子含量 [J], 尚云涛;陈奕霖;曹佳蕊;任春雪;范宝莉;刘晓颖;王振英2.离子色谱法测定啤酒中6种无机阴离子的含量 [J], 刘珍珠;张辉珍;崔鹤;赵海峰;邱阿敏3.离子色谱法测定艾附暖宫丸中9种无机阴离子含量 [J], 吴卫东4.抽提-离子色谱法测定原油中无机阴离子含量 [J], 刘丽;张谋真;任树林;刘启瑞;贺靖江;梁真;田涛;李浩然;李斌5.离子色谱法测定车用汽油燃烧产物中8种无机阴离子的含量 [J], 鹿燕;孙宵欢;廖上富因版权原因,仅展示原文概要,查看原文内容请购买。
离子色谱法测定水果中氟离子
王雨,李静
戴安中国有限公司应用研究中心, 北京,100085,wangyu@
摘要:本文使用IonPac AS15中高疏水性高容量阴离子交换色谱柱,使氟离子与高浓度有机酸高效分离,配合大体积进样方式,成功分析了水果样品中的痕量氟离子。
氟离子标准曲线线性关系良好,相关系数为99.94%,氟离子的最低检出限为1.8μg/L。
该方法前处理简单,分离效果好,灵敏度高,基体干扰小,方法高效准确。
关键词:氟离子;离子色谱;水果;
氟是人类生命活动所必需的微量元素之一,但氟对人体健康的作用取决于剂量,摄入氟过多或过少都会给人体健康带来不利的影响。
由于人体对氟含量极为敏感,因此氟的安全范围比其他微量元素窄得多[1]。
适量的氟可以促进人体骨骼和牙齿的钙化,增强骨骼的强度。
但是长期摄人过量氟化物会引起氟中毒,如由于氟摄入过多可引起牙齿、骨骼等组织的病理改变,也可引起肾脏、肝脏等器官的组织病变等。
世界上大多数国家均制定了人体每日氟摄入量标准。
世界卫生组(WHO)规定,人均每天适宜的氟摄人量为2.5~4.0 mg[2]。
国标GB4809-84 《食品中氟允许量标准》
对多种食品中氟的含量有限制要求[3]。
本文利用离子色谱梯度淋洗的方法,成功分析了多种水果中的氟离子含量,通过IonPac AS15高效阴离子交换色谱柱分离,有效避免了样品中大量有机酸对氟离子测定干扰,该方法前处理简单,分析速度快,灵敏度高,分析干扰少,结果准确可靠。
1、实验部分
1.1仪器与试剂
仪器:ICS-3000型离子色谱仪(Dionex,美国)
试剂和样品:氟离子标准溶液(1000mg/L);甲醇(色谱纯,百灵威公司);超纯水(Millipore,电阻率为18.2MΩ/cm);OnGuard RP(1.0cc)前处理柱;0.22μm尼龙滤膜;市售水果。
1.2 色谱条件
色谱柱:IonPac AS15阴离子交换分析柱,250*4mm;IonPac AG15保护柱,50*4mm 淋洗液:KOH,0-17 min 3 mM, 17.1-27 min 60 mM , 27.1-31 min 3 mM;
淋洗液流速:1.2ml/min;
抑制器:ASRS 300型抑制器4mm,外接水抑制模式,抑制电流为150mA;
进样量:200μL;/Shop/product.asp?id=15599&cid=&s=&page=2
1.3 溶液配制
1.3.1标准溶液的配制
将1000mg/L氟离子标准溶液进行稀释,配制浓度分别为0.002、0.005、0.01、0.05、0.1mg/L 的系列标准溶液。
1.3.2样品溶液的制备
水果样品充分捣碎,取果汁1g稀释到10ml,分别通过0.22 μm尼龙过滤膜和OnGuard RP前处理柱,弃去前面3ml流出液,收集后面溶液进样。
/Shop/product.asp?id=15599&cid=&s=&page=1
2、结果与讨论
2.1 色谱柱的选择和色谱条件优化
IonPac AS15是疏水性中高的氢氧根体系色谱柱[4],对低分子量有机酸的分析非常出色,较高的色谱柱柱容量,配合大体积进样方式,适合复杂基质中痕量阴离子的分析。
水果中一般含有高含量有机酸,小分子的有机酸由于离子化程度弱,与色谱柱上离子交换基团的亲和力弱,出峰时间较快,IonPac AS15色谱柱的中高疏水性特点,使得小分子的有机酸保留增强,从而与氟离子获得了更大的分离度。
本文采用IonPac AS15色谱柱,一步梯度淋洗,成功实现了水果基体中氟离子的测定。
本方法灵敏度高,高效准确。
采用淋洗液自动发生装置进行梯度淋洗,可在31分钟内完成测定,低浓度淋洗部分,可使氟离子与干扰峰获得足够的分离度,高浓度淋洗部分使样品中其余阴离子快速冲出色谱柱,产生的浓度梯度准确,分析重现性好,操作非常简便。
图1和图2分别是苹果和梨的实际样品分离谱图,由色谱图可见,氟离子与高浓度有机酸实现了有效分离。
2.2 线性范围、相关系数、最小检出限
考察氟离子在0.002~0.1mg/L范围内浓度与峰面积的标准曲线,曲线方程为y= 1.9626x+0.001 ,相关系数为99.94%,线性关系良好。
以3倍基线噪音为检出限,10倍基线噪音为定量限,本检测方法的仪器检出限为1.8μg/L,仪器定量限为6.0μg/L。
按照本文
中采用的样品前处理方法,对水果中氟的最低方法检出限为0.018mg/kg,远低于国标中规定的限量浓度。
2.3 样品分析
检测的苹果和梨两种水果中氟离子含量见下表,
表1 样品检测结果
国标对水果中氟的限量为0.5 mg/kg。
所测定的水果中氟离子的含量均在限量范围内。
3 结论
本文使用IonPac AS15中高疏水性阴离子交换色谱柱,成功分析了水果样品中的氟离子含量,前处理方法中用OnGuard RP前处理柱除去水果中高分子有机成分,所得样品溶液直接进样分析。
前处理简单,分离效果好,灵敏度高,基体干扰小,方法高效准确。
参考文献:
[1] 贾丽,谷学新,张经华,现代仪器,2006,6:6-8
[2] 张楠,张凌云,茶叶,2009,35(1):3-6
[3] GB4809-84 食品中氟允许量标准
[4] 牟世芬,刘克纳,丁晓静,北京:化学工业出版社,2005.。