药物涂层支架
- 格式:ppt
- 大小:7.09 MB
- 文档页数:36

心脏支架的材料心脏支架是一种用于治疗心脏血管疾病的医疗器械,它可以帮助扩张狭窄的血管,恢复血液流通。
而心脏支架的材料选择对于支架的性能和效果有着至关重要的影响。
目前,主要的心脏支架材料包括金属支架和药物涂层支架两种类型。
金属支架是最早被使用的一种心脏支架材料,主要由不锈钢、钛合金或铬钴合金制成。
这些金属具有良好的机械性能和生物相容性,能够提供足够的支撑力和稳定性,但是金属支架在植入后容易导致血管内皮细胞增生,形成新的狭窄,从而影响了支架的长期效果。
为了解决这一问题,药物涂层支架应运而生。
药物涂层支架是在金属支架的基础上,表面涂覆一层药物,通过缓释药物来抑制血管内皮细胞的增生,减少新的狭窄形成。
目前,药物涂层支架的材料主要包括生物可降解聚合物和药物载体。
生物可降解聚合物材料可以在体内逐渐降解,减少对血管的刺激和损伤,但是其力学性能和稳定性相对较差。
而药物载体则是将药物包裹在载体材料中,通过控制药物的释放速度来达到抑制血管内皮细胞增生的目的。
除了金属支架和药物涂层支架,近年来还出现了生物可降解支架。
生物可降解支架是一种新型的支架材料,它可以在体内逐渐降解,不会对血管造成持久性刺激和损伤,从而有望降低新的狭窄形成的风险。
目前,生物可降解支架的材料主要包括聚乳酸、聚羟基烷酸和聚己内酯等生物可降解聚合物。
综上所述,心脏支架的材料选择对于支架的性能和效果有着至关重要的影响。
金属支架具有良好的机械性能和稳定性,但容易导致新的狭窄形成;药物涂层支架通过药物缓释来抑制血管内皮细胞增生,但需要注意药物的选择和释放速度控制;生物可降解支架可以在体内逐渐降解,减少对血管的刺激和损伤,有望降低新的狭窄形成的风险。
随着科学技术的不断进步,相信心脏支架的材料选择会越来越趋向于完美,为患者带来更好的治疗效果。

药物涂层支架机制
药物涂层支架(Drug-coated stent)是一种用于治疗冠状动脉
疾病的组织支架。
其机制是在金属支架表面涂覆一层药物,常用的药物包括利巴韦林(sirolimus)和雷帕霉素(paclitaxel)等。
药物的涂层主要是为了预防血管狭窄的再发。
血管狭窄是由于冠状动脉血管内壁产生斑块,阻塞了血液的正常流动,引发心绞痛和心肌梗塞等疾病。
药物涂层支架通过放置在狭窄的血管内,可以扩张血管并保持血流的通畅。
同时,药物的涂层可以释放药物进入血管壁,以抑制狭窄复发。
具体机制如下:
1. 血管扩张:支架可以通过物理力学作用将狭窄的血管扩张开,增加血流通畅度。
2. 药物释放:药物涂层中的药物可以缓慢释放,进入血管壁直到血液中,以起到治疗和预防血管狭窄的作用。
这些药物可以抑制血管内皮细胞的增殖和炎症反应,减少斑块的形成。
3. 促进血管内皮细胞再生:支架上的药物涂层可以促进血管内皮细胞的再生,帮助修复受损的血管内膜。
这种再生也可以减少血管狭窄的发生。
药物涂层支架相对于普通的金属支架,具有更低的复发率和再手术率。
然而,长期使用药物涂层支架可能会引发血管内再狭
窄、血栓形成等并发症,因此使用药物涂层支架需要谨慎评估患者的风险和益处。

新一代药物涂层支架(EXCEL)带给我们的是什么?药物洗脱支架(DES)的问世被誉为介入心脏病学领域的又一个里程碑。
它的神奇充分体现在它能够显著降低再狭窄率方面。
然而,随着时间的延长,植入DES后晚期支架贴壁不良(LSM)和晚期支架内血栓(LST)发生率增加,尤其是LST的明显增加以及由此造成的严重后果,引起了心脏介入医生和病理学家的广泛关注,使人们从短暂的欣喜和兴奋中对DES产生了质疑。
目前,对植入DES后发生LSM、LST和再狭窄(RS)的原因和机制仍知之甚少。
Hong、Virmani、Kuchulakanti和Guagliumi等人对部分植入CypherTM和TAXUSTM后死亡的病例进行病理学分析发现:药物所致的内皮愈合延迟、不可降解聚合物永久残留导致的局部血管壁炎症反应和纤维素沉积可能是LSM 、LST和RS的主要原因。
瑞士巴塞尔大学的Matthias Pfisterer教授设计了BASKET-LATE试验,目的是评价“支架成本-疗效-晚期血栓事件”的情况,试验结果在2006年ACC年会上公布:植入DES的病人在停用氯吡格雷1年内发生心源性死亡和心肌梗死(MI)事件的风险明显高于植入裸金属支架(BMS)的病人(4.9% vs. 1.3%, P=0.01);LST事件的发生率是BMS 病人的2倍(2.6% vs. 1.3%);非致命性心脏不良事件的发生率也显著高于BMS病人(4.1% vs. 1.3%, P=0.04)。
在“真实世界”中,每100个使用DES的病人,每6个月可避免5 次TVR,而付出的代价是3.3个人死亡或非致死性MI 事件。
因此,Pfisterer教授强调:DES会增加LST风险是无可争议的事实,应该采取新的策略来预防LST的发生。
但是在短期内,延长双重抗血小板治疗的时间可能是最好的选择,而最终的解决之道还得等待新型生物可降解支架平台、新技术或新药物的问世。
于是,研究者尝试从支架材料、药物载体、药物和支架涂层工艺等多方面进行改进,希望这些融入新理念的支架能够克服DES 的缺点,从根本上改变冠心病(CAD)介入治疗的远期效果。

药物涂层球囊与新一代药物洗脱支架治疗冠脉支架内再狭窄临床疗效对比研究随着冠心病患者数量的增加,冠状动脉支架植入术(PCI)成为了治疗冠状动脉疾病的常见手术方式。
由于支架内再狭窄的发生率较高,需要进行二次介入治疗。
在冠状动脉支架内再狭窄的治疗中,药物涂层球囊(DCB)和新一代药物洗脱支架(DES)成为了主要的治疗选择。
两者的临床疗效一直备受关注,本研究旨在比较这两种治疗方式在冠状动脉支架内再狭窄患者中的临床疗效。
一、研究背景冠状动脉支架内再狭窄是指在冠状动脉支架植入术后,支架周围血管再次出现狭窄的情况。
这种情况可能会导致患者的心绞痛加重甚至心肌梗塞,因此需要进行再次介入治疗。
目前,DCB和DES是两种主要的再次介入治疗方式。
DCB是一种在球囊表面涂覆了药物的球囊,通过球囊膨胀释放药物来抑制血管平滑肌增生,减少内膜增生和狭窄的发生。
而DES则是一种在支架表面涂覆了药物的支架,可以持续释放药物来抑制内膜增生,预防再狭窄的发生。
目前关于这两种治疗方式的临床疗效对比研究较少,因此有必要开展本研究来比较它们在冠状动脉支架内再狭窄患者中的疗效差异。
二、研究方法1. 研究对象选取了2016年1月至2021年1月在本医院接受再次介入治疗的冠状动脉支架内再狭窄患者为研究对象,根据治疗方式的不同分为DCB组和DES组。
2. 研究设计采用回顾性队列研究设计,对患者的临床资料进行收集和整理,包括基本资料、手术信息、随访情况等。
3. 疗效评估主要观察指标包括再次介入率、术后6个月内的主要不良心血管事件(MACE)发生率、引流率等。
还对患者进行一年内的随访,观察患者的临床症状和心电图变化等。
三、研究结果经过数据的收集和整理,最终纳入了DCB组和DES组各100例患者。
两组患者的基本资料、手术信息等临床特征均无显著差异。
在疗效评估方面,结果显示,DCB组的再次介入率为10%,而DES组的再次介入率为8%,差异无显著性(P>0.05)。

雷帕霉素药物涂层支架体外释放实验
1.原理
模拟药物洗脱支架体外加速释放情况、采用HPLC测定药物含量以及释放速度。
2.药物洗脱支架体外释放方法
在溶出杯中加入100mlPBS溶液,在溶出仪内37±0.5℃环境中预热约30分钟,然后将扩张后的药物洗脱支架固定在溶出仪挂钩上,浸入烧杯内的PBS溶液中。
保持温度为37±0.5℃,震荡频次为30次/分。
到达对应时间点后,迅速(半分钟内)取出支架,用纯净水清洗干净后,洗脱支架,用HPLC分析药物在涂层支架中的残余量。
3.药物洗脱支架药物总量测定方法
将支架扩张后压扁折叠,置入10ml容量瓶,加入0.3ml丙酮将支架完全淹没,浸泡十分钟后,用无水甲醇定容到10ml。
4.HPLC测定药物含量方法
1)实验条件
色谱柱:Agilent Zorbax SB C-18 150*2.1mm ID
检测波长:277nm;
流动相:甲醇:乙腈:水=40:36:24
流速:0.5 ml/min;
柱温:40℃
进样量:10ul
2)内标法测定药物含量
用微量电子天平精密称取雷帕霉素标准品0.5~4mg至50ml容量瓶中,分别加入1.5ml丙酮后用无水甲醇定容,配制成五个不同浓度的标准品溶液。
分别精密取10ul注入仪器,根据不同的浓度对应不同峰面积作标准曲线。
将药品洗脱液取定量注入仪器,记录峰面积。
依据标准曲线公式计算药物含量。

三氧化二砷药物涂层支架输送系统特点
1、中国第一个自主原创的药物支架:三氧化二砷药物涂层支架输送系统(商品
名:AVI)是复旦大学附属中山医院葛均波院士耗时6年研发的一个突破了世界的传统、创新型的药物支架。
为中国第一个自主原创的药物支架,对于中国急性冠脉综合征、心脏冠心病介入治疗具有里程碑的意义。
目前国内其他厂家的冠脉药物支架都是采用雷帕霉素及其衍生物或者紫杉醇,都是属于国外产品的仿制品。
2、AVI的经济性、安全性:AVI的不仅药物是创新的,作为药物的涂层载体同样
也有重大的创新。
一个药物支架植入人体后是否会在病变部位发生晚期血栓,和药物涂层是否能够完全降解有很大关系。
AVI采用的是3个月就可以完全降解的丙交酯和天冬氨酸衍生物聚合物,该聚合物是世界公认的生物相容性很好,在人体能够完全降解成无任何副作用的水、二氧化碳和氨基酸。
而以往无论是进口的支架(例如退市的强生CYPHER支架)还是国产的支架(例如上海微创的火鸟2等)采用是不可以完全降解的涂层载体,从而导致支架植入者为了防止晚期血栓的发生,需要长时间服用双联抗血栓药物(氯吡格雷和阿司匹林),而AVI支架植入后,昂贵的抗凝药物氯吡格雷只需要服用6个月(参见药监局审定的AVI产品说明书),而后单用廉价的阿司匹林。
意味着能节省AVI支架植入患者远期药品费用同时也降低因为需要长期服用双联抗凝剂带来的风险(例如脑出血等)。
每个支架三氧化二砷平均载药50ug,基本相当美国饮用水标准每公升的允许含量的限值,十分安全。

韩雅玲陈兵本文作者韩雅玲女士,沈阳军区总医院副院长、全军心血管内外科研究所所长兼心血管内科主任、主任医师、博士研究生导师; 陈兵先生,器材科主任、高级工程师、全国卫生装备协会常务理事、全军医学工程专业委员会常委。
关键词: 药物涂层支架冠心病再狭小血运重建术经皮经腔冠状动脉内支架植入术是冠状动脉介入医治(PCI)的要紧手腕,约占全世界PCI总例数的70%以上。
尽管冠脉内支架术能够有效降低经皮腔内冠状动脉成形术(PTCA)后再狭小率,但仍有20%~30%的病例会发生支架内再狭小(ISR),在糖尿病、小血管病变、长病变、慢性完全闭塞病变及分叉病变病人中,ISR发生率可高达30%~70%。
因此,ISR已成为阻碍PCI长期疗效的最要紧的缘故。
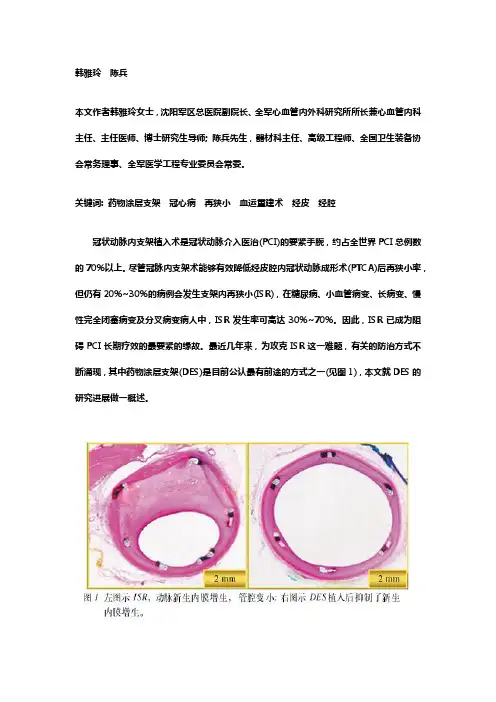
最近几年来,为攻克ISR这一难题,有关的防治方式不断涌现,其中药物涂层支架(DES)是目前公认最有前途的方式之一(见图1),本文就DES的研究进展做一概述。
一DES的概念DES又称药物释放支架或药物洗脱支架,顾名思义,确实是将药物通过适当的方式涂布于支架表面,使之形成一个药物池,在血液的冲洗和溶解作用下,药物不断从支架表面洗脱,并在局部发挥作用,因此,DES具有靶向性好、药物在局部组织中浓度高、全身副作用小的特点。
与支架内放射医治、切割球囊、定向旋切等医治ISR的方式相较,DES兼顾了ISR的预防和医治,因此具有更高的效费比。
二DES的设计DES是支架、药物载体和涂层药物三者结合应用的产物(见图2),在设计上融合了材料学、工艺学、药理学、药代动力学等诸多学科的先进技术,与一般支架相较,预防ISR的设计思想更为合理,工艺更为精细、复杂。
1. 支架设计DES的支架设计多以一般金属支架为基础,而一般金属支架在技术上已经比较成熟。
部份支架通过设计上的改良,使之能够携带更多的药物。
例如,Conor支架采纳激光切割打孔技术,使每一个支架上的激光镂孔数量达到588个之多,极大地增大了支架的表面积,同时增加了支架的带药量(图3a)。

冠脉支架的分类
冠脉支架的分类如下:
1. 金属支架:金属支架是最常用的冠脉支架,其中最早使用的是金属裸支架。
金属裸支架存在再狭窄的问题,因此后来研发出了药物涂层支架,用以减少再狭窄问题。
2. 药物涂层支架:药物涂层支架通过药物处理,可以减少支架内的再狭窄问题。
然而,早期药物涂层支架易形成血栓,目前随着技术的不断改进,支架内血栓的问题正在逐步解决。
3. 可降解的支架:可降解的支架理论上植入到血管内后可以自行降解,恢复血管通畅。
目前这类支架正在开展中,但存在一系列问题,需在临床使用中不断改良和完善。
冠脉支架的选择需根据患者的具体病情和医生的建议进行决定。
如需了解更多关于冠脉支架分类的信息,建议咨询专业医生或查阅相关医学资料。

对第一代DES安全性的担忧以及不同DES之间临床表现的差异促进了DES设计上的不断改进。
决大部分DES包括三个要素——支架架构和传送系统、支架药物、药物载体。
所有支架改良和设计均基于上述三个方面。
支架设计和传送系统是DES的基石。
支架设计要求支架壁要薄,减少血管金属负荷,并且支架要有较小的外径、良好的柔顺性、通过性和较小的管壁损伤特性。
DES第二要素为药物载体。
多聚物涂层是当前应用主流。
Virmani等研究显示长期存在的多聚物涂层是导致支架内晚期血栓形成的重要原因之一。
它可以引发血管壁表面炎症和高敏反应,从而影响支架表面内皮化进程。
多聚涂层的成分、完整性、粘性及厚度均是生物组织反应性的决定因素。
此外,支架输送和释放过程中,操作不当容易导致多聚涂层剥脱碎裂;多聚涂层裂损部位血栓形成;脱落的涂层碎片造成冠状动脉微栓塞;过度慢性炎症反应。
基于上述原因,生物可降解多聚物涂层是研发热点。
生物可降解多聚物涂层有如下优点:减少涂层长期高敏性;涂层在6月内降解吸收;携带药物在涂层降解前药物释放完毕;缩短双联抗血小板药物服用时间。
但是可降解生物涂层也有其缺点:炎症反应;在涂层降解同时很难保证平稳的药物释放曲线。
目前市场上有多种类型以可降解多聚物涂层为载体的DES,如Nobori,Biomatrix,国产的EXCEL等。
EXCEL支架以聚乳酸为载体,3~6月内降解为二氧化碳和水。
Nobori随访结果显示术后二年内无支架血栓事件发生。
药物为药物支架最为关键一部分。
目前认为较为理想药物应具备如下特征:在保证支架疗效情况下,支架携带药物量要尽量小;合理的药物动力学;为了延长药物组织内滞留时间,更倾向选择疏水性药物;促内皮愈合药物,如VEGF、eNOS、estradiols等,但这些药物一般不单独应用,通常要联合低剂量抗增生药物,采用双重DES系统。
2008年TCT会议上公布的ISAR-TEST2研究结果初步验证了双重DES安全性和有效性。

可能为紫杉醇药物涂层而引起的特有副作用紫杉醇是一种常用的抗肿瘤药物,通常用于治疗多种恶性肿瘤,如乳腺癌、卵巢癌、非小细胞肺癌等。
在临床上,紫杉醇可通过静脉注射给药,也可以通过药物涂层的方式给药,其中包括使用药物涂层的支架进行治疗。
尽管药物涂层有助于减少毒副作用的发生,但仍然可能引起一些特有的副作用。
首先,紫杉醇药物涂层可能引起血栓形成。
紫杉醇是一种微管靶向抗癌药物,通过阻断肿瘤细胞的有丝分裂,从而抑制癌细胞的生长。
然而,紫杉醇也可能对血管内皮细胞产生不良影响,导致血管损伤和血栓形成。
这种现象在放置药物涂层支架时尤为常见,因为支架接触到血管壁会引起一定程度的炎症反应,从而增加血栓形成的风险。
其次,紫杉醇药物涂层可能引起局部反应。
在药物涂层支架的表面涂覆有紫杉醇药物,这种药物在血管内释放出来后可能对周围组织产生一定程度的刺激,引起炎症反应和局部过敏反应。
患者可能出现血管狭窄、红肿、疼痛等症状。
在严重的情况下,局部反应还可能引起血栓形成和支架再狭窄。
此外,紫杉醇药物涂层还可能引起全身毒性反应。
尽管药物涂层可以减少紫杉醇的全身暴露,但仍有可能导致全身毒性反应,如低血压、呼吸困难、心律失常等。
部分患者可能还会出现恶心、呕吐、腹泻等消化道不良反应,以及头痛、眩晕、皮疹等过敏反应。
总的来说,紫杉醇药物涂层在治疗恶性肿瘤时具有一定的疗效,但也存在一些特有的副作用。
为了减少这些副作用的发生,医生在选择治疗方案时需要综合考虑患者的病情和身体状况,严格掌握用药适应症和用药方法,监测患者的治疗反应和不良反应,及时调整治疗方案。
同时,患者在接受治疗时要密切配合医生的指导,尽量避免不良的生活习惯和环境因素,以提高治疗的效果和减少副作用的发生。
气管支架的种类气管支架是一种医疗器械,用于治疗气管狭窄或阻塞等气道疾病。
根据不同的设计和材料,气管支架可以分为多种类型。
本文将介绍几种常见的气管支架种类。
1. 金属气管支架金属气管支架是最早应用的一种气管支架。
它通常由不锈钢或钛合金制成,具有较高的强度和刚度,可以提供稳定的支撑力。
金属气管支架的优点是耐久性强,可以长期留置在患者体内。
然而,金属气管支架也存在一些缺点,如可能引起组织反应和梗死等并发症。
2. 可吸收气管支架可吸收气管支架是一种新型的气管支架,它由生物可降解材料制成,如聚乳酸或聚己内酯。
这种支架可以在体内逐渐吸收,不需要进一步的手术去除。
可吸收气管支架适用于治疗短期气道狭窄,如手术后的气管狭窄。
然而,由于吸收速度和力学性能的限制,可吸收气管支架在长期留置和治疗气道疾病方面的应用还面临一些挑战。
3. 药物涂层气管支架药物涂层气管支架是一种将药物涂覆在气管支架表面的特殊设计。
这种气管支架可以在患者体内释放药物,以达到治疗目的。
常用的药物涂层包括抗生素、抗炎药物和免疫抑制剂等。
药物涂层气管支架可以减少感染和炎症等并发症的发生,提高治疗效果。
然而,药物涂层气管支架的药物释放速率和持续时间需要进行精确控制,以避免药物过量或不足的问题。
4. 膨胀式气管支架膨胀式气管支架是一种可以通过气囊或球囊进行膨胀的支架。
它通常由硅胶或聚乙烯等材料制成。
膨胀式气管支架可以在患者体内膨胀,提供稳定的支撑力。
这种支架适用于治疗短期气道狭窄或进行支气管镜检查等操作。
膨胀式气管支架的优点是可以根据患者的具体情况进行调整和取出,较为灵活。
然而,膨胀式气管支架也存在一些不适应症和并发症,如支气管损伤和气道出血等。
5. 双腔管气管支架双腔管气管支架是一种具有两个独立腔室的支架。
这种支架可以分别通气和引流,适用于治疗气道狭窄伴有分泌物潴留的患者。
双腔管气管支架可以通过分离气道和引流道,减少感染和梗阻等并发症的发生。
然而,双腔管气管支架的设计和使用需要一定的技术和经验,操作复杂度较高。
心脏支架的材料
心脏支架是一种用于治疗冠状动脉疾病的医疗设备,它可以帮助扩张狭窄的血管,恢复血液流通。
而心脏支架的材料选择对于其性能和效果有着至关重要的影响。
目前市面上主要有金属支架和药物涂层支架两种类型,它们的材料也各有特点。
金属支架主要采用的材料是不锈钢、钛合金和铬钴合金。
不锈钢支架具有较高
的强度和硬度,能够提供良好的支撑力,但由于其较大的弹性模量,容易导致支架内部应力集中,增加了血管壁的应力,可能引发再狭窄。
钛合金支架具有较好的生物相容性和较低的弹性模量,对血管壁的刺激较小,但相对不锈钢支架而言,其强度和硬度较低,可能导致支架变形或断裂。
铬钴合金支架综合了不锈钢和钛合金的优点,具有良好的强度、硬度和生物相容性,是目前应用较为广泛的金属支架材料。
药物涂层支架是在金属支架的基础上,通过药物涂层技术,将药物包裹在支架
表面,用于预防血管再狭窄和血栓形成。
药物涂层支架的材料选择更加注重生物相容性和药物释放性能。
目前常用的药物涂层支架材料包括聚合物和生物可降解材料。
聚合物材料具有良好的可塑性和药物释放性能,但可能引起过敏反应和慢性炎症反应。
生物可降解材料具有较好的生物相容性和降解性能,能够逐渐降解并释放药物,减少对血管的刺激,但其力学性能和稳定性仍存在一定挑战。
总的来说,心脏支架的材料选择需要综合考虑其力学性能、生物相容性和药物
释放性能。
未来随着材料科学和生物医学工程的发展,心脏支架的材料可能会朝着更加生物相容、稳定可靠和个性化定制的方向发展。
这将为心脏病患者带来更加安全有效的治疗方案,为心脏病的治疗注入新的活力。
心脏支架是什么材料做的心脏支架是一种用于治疗心脏血管疾病的医疗器械,它可以帮助扩张狭窄或堵塞的血管,恢复血液流通。
而心脏支架是由什么材料制成的呢?下面我们就来详细了解一下。
首先,心脏支架的材料主要有两种,金属支架和药物涂层支架。
金属支架通常由不锈钢、铬钴合金或镍钛合金制成。
这些金属具有良好的机械性能和生物相容性,能够在血管内部长期稳定地支撑血管壁,同时不会对人体产生不良反应。
而药物涂层支架则是在金属支架表面覆盖一层药物,这些药物可以抑制血管再狭窄的过程,减少血管内部的血栓形成,提高手术成功率和患者的生存率。
其次,金属支架的材料选择非常重要。
不锈钢是最早被使用的心脏支架材料,它具有良好的机械性能和耐蚀性,但是由于不锈钢支架的弹性模量较大,可能会导致支架植入后血管壁的损伤。
铬钴合金和镍钛合金则是近年来发展起来的新型材料,它们具有更好的生物相容性和弹性模量,能够更好地适应血管的形态,降低术后并发症的风险。
再次,药物涂层支架的材料选择也至关重要。
药物涂层支架的药物一般是通过聚合物载体覆盖在金属支架表面的,这些聚合物要求具有良好的附着力和稳定性,同时要能够释放药物并保持药物的活性。
目前常用的聚合物材料有聚乳酸、聚己内酯、聚乳酸-羟基乙酸共聚物等,它们都具有良好的生物相容性和可降解性,能够在血管内部起到良好的治疗效果。
最后,无论是金属支架还是药物涂层支架,其材料的选择都是在考虑了材料的生物相容性、机械性能、可加工性、药物释放性等多方面因素后做出的。
未来随着材料科学和医疗技术的不断发展,心脏支架的材料将会越来越多样化,能够更好地适应不同患者的需求,为心脏病患者带来更好的治疗效果。
总之,心脏支架的材料选择是非常重要的,它直接关系到手术的成功率和患者的生存质量。
目前金属支架和药物涂层支架是主流的心脏支架类型,它们都具有良好的材料性能和治疗效果。
未来随着科技的不断进步,心脏支架的材料将会更加多样化,为心脏病患者带来更好的治疗选择。
药物涂层球囊与新一代药物洗脱支架治疗冠脉支架内再狭窄临床疗效对比研究1. 引言1.1 背景在冠脉支架植入术后,有一定比例的患者会出现支架内再狭窄的情况,导致血液流动受阻,进而引发心绞痛、心肌梗死等危险情况。
为了解决此类问题,药物涂层球囊和新一代药物洗脱支架作为治疗手段应运而生。
药物涂层球囊通过在球囊表面涂覆药物,使药物得以释放到血管壁内,抑制内膜增生,从而减少再狭窄的发生。
而新一代药物洗脱支架相比传统支架更具生物相容性和可塑性,能更好地适应血管形态,减少支架内再狭窄的可能性。
目前,药物涂层球囊和新一代药物洗脱支架在治疗冠脉支架内再狭窄方面都取得了一定的临床疗效。
两种治疗手段的优劣仍有待深入研究和对比。
本研究旨在通过对两种治疗手段的临床疗效进行对比研究,为临床医生提供更准确的治疗选择,以提高患者治疗效果和生存质量。
1.2 研究目的本研究旨在比较药物涂层球囊与新一代药物洗脱支架治疗冠状动脉支架内再狭窄的临床疗效,探讨两种治疗方式在临床应用中的优劣势。
具体目的包括以下几个方面:2. 系统评估药物涂层球囊和新一代药物洗脱支架在治疗冠脉支架内再狭窄时的药效特点,分析其在延迟血管再狭窄和血栓形成等方面的表现。
3. 探讨药物涂层球囊和新一代药物洗脱支架治疗冠脉支架内再狭窄对心脏功能及预后的影响,为临床医生提供更为科学的治疗选择。
2. 正文2.1 药物涂层球囊的原理药物涂层球囊是一种具有药物释放功能的球囊导管,可以在冠脉支架内再狭窄的部位释放药物,达到预防再次狭窄的效果。
其原理是通过球囊外层的药物涂层,在球囊膨胀时释放药物,同时通过球囊的压力将药物推送到狭窄部位,以达到药物治疗的效果。
药物涂层球囊可以选择不同的药物涂层,例如沙利度胺、依罗司他和西替利嗪等,根据具体病情选择不同功效的药物。
药物涂层球囊的原理主要包括两个方面,一是通过药物的直接释放作用达到阻塞血管内膜增生的效果,减少再次狭窄的可能性;二是通过球囊的压力作用将药物推送至狭窄部位,提高药物在局部的浓度,增强治疗效果。