初中常见物质的化学式
- 格式:doc
- 大小:68.00 KB
- 文档页数:7

初中常见物质化学公式一、离子、原子式1. 氯气:Cl₂2. 水:H₂O3. 硫酸:H₂SO₄4. 纯碱:NaOH5. 硝酸:HNO₃6. 氨气:NH₃7. 氧气:O₂8. 氢气:H₂9. 氮气:N₂10. 二氧化碳:CO₂11. 亚硫酸:H₂SO₃12. 硝酸银:AgNO₃13. 碳酸氢钠:NaHCO₃14. 氯化钠:NaCl15. 硫化氢:H₂S二、摩尔比1. 摩尔质量:M = n/m,其中n为物质的物质量,单位为mol;m为物质的质量,单位为g。
2. 摩尔占比:X = n/M,其中n为物质的物质量,单位为mol;M为物质的摩尔质量,单位为g/mol。
三、反应式1. 酸和碱的中和反应:酸 + 碱→ 盐 + 水2. 碳酸酸解反应:碳酸 + 酸→ 盐 + 水 + 二氧化碳3. 金属与酸反应:金属 + 酸→ 盐 + 氢气4. 物质燃烧反应:物质 + 氧气→ 二氧化物5. 物质与酸和金属反应:物质 + 金属→ 盐 + 氢气6. 物质与氢气反应:物质 + 氢气→ 化合物7. 燃烧反应:物质 + 氧气→ 二氧化物四、质量关系1. 反应质量平衡法则:质量守恒定律,反应前后质量不变。
2. 物质质量比:m₁:n₁ = m₂:n₂3. 反应的最大产物质量:从化学方程式知道反应物的物质量,按照化学比转换成制造物的物质量,取最小者即为反应的最大产物质量。
五、分子式1. 分子式表示分子中元素的种类和数目。
2. 示例如下:- 水的分子式为H₂O,表示一个水分子中有2个氢原子和1个氧原子。
- 二氧化碳的分子式为CO₂,表示一个二氧化碳分子中有1个碳原子和2个氧原子。
六、离子式1. 离子式用来表示离子的种类。
2. 示例如下:- 氯离子的离子式为Cl⁻,表示一个氯离子带有1个负电荷。
- 钠离子的离子式为Na⁺,表示一个钠离子带有1个正电荷。
七、化学方程式的平衡1. 化学反应的配平:通过调整反应物和生成物的系数,使得化学方程式中的原子数目相等。

初中常见物质的化学式(大全)1、非金属单质氢气碳氮气氧气磷硫氯气H2CN2O2PSCl22、金属单质钠镁铝钾钙铁锌铜NaMgAlKCaFeZnCu汞钡钨HgBaW3、常见氧化物水一氧化碳二氧化碳五氧化二磷二氧化锰二氧化氮二氧化硅H2OCOCO2P2O5MnO2NO2SiO2二氧化硫三氧化硫一氧化氮氧化镁氧化铜氧化钡氧化亚铜SO2SO3NOMgOCuOBaOCu2O氧化亚铁三氧化二铁四氧化三铁三氧化二铝FeOFe2O3Fe3O4Al2O34、氯化物/盐酸盐氯化钾氯化钠氯化镁氯化钙氯化铜氯化锌氯化钡氯化铝氯化银KClNaClMgCl2CaCl2CuCl2ZnCl2BaCl2AlCl3AgCl氯化铁氯化亚铁FeCl3FeCl25、常见的酸硫酸亚硫酸盐酸硝酸碳酸硫化氢H2SO4H2SO3HClHNO3H2CO3H2S6、常见的盐硫酸铜硫酸钡硫酸钙硫酸钾硫酸镁硫酸亚铁硫酸铁CuSO4BaSO4CaSO4K2SO4MgSO4FeSO4Fe2(SO4)3硫酸铝硫酸钠硫酸钾亚硫酸钠硝酸钠硝酸钾硝酸银Al2(SO4)3Na2SO4K2SO4Na2SO3NaNO3KNO3AgNO3硝酸镁硝酸铜硝酸钙亚硝酸钠碳酸钠碳酸钙碳酸镁MgNO3Cu(NO3)2Ca(NO3)2NaNO3Na2CO3CaCO3MgCO3碳酸钾K2CO37、常见的碱氢氧化钠氢氧化钙氢氧化钡氢氧化镁氢氧化铜氢氧化钾氢氧化铝NaOHCa(OH)2Ba(OH)2Mg(OH)2Cu(OH)2KOHAl(OH)3氢氧化铁氢氧化亚铁Fe(OH)3Fe(OH)28、常见有机物甲烷乙炔甲醇乙醇【酒精】乙酸【醋酸】CH4C2H2CH3OHC2H5OHCH3COOH9、常见结晶水合物碱式碳酸铜石膏蓝矾明矾绿矾Cu2(OH)2CO3CaSO4•2H2OCuSO4•5H2OKAl(SO4)2•12H2OFeSO4•7 H2O10、常见化肥尿素硝酸铵硫酸铵碳酸氢铵磷酸二氢钾CO(NH2)2NH4NO3(NH4)2SO4NH4HCO3KH2PO411、沉淀微溶于水淡黄色沉淀浅绿色沉淀红褐色絮状沉淀蓝色絮状沉淀Ca(OH)2,CaSO4SFe(OH)2Fe(OH)3Cu(OH)2白色沉淀Mg(OH)2、CaCO3、BaCO3、AgCl、BaSO4 (其中BaSO4、AgCl是不溶于HNO3的白色沉淀, Mg(OH)2、CaCO3 、BaCO3是溶于HNO3的白色沉淀)当我们难以前进的时候,不要忘记先退一步,再往前闯,或者变更方法前进。

初中常见物质基础的化学式
一、单质
1、金属单质:Mg镁、Fe铁、Al铝、Zn锌、Cu铜、Ag银、
2、非金属单质:常见气体:O2氧气、H2氢气、N2氮气
固体非金属单质:S硫、P磷(红磷、白磷)、C碳(木炭、石墨、金刚石)稀有气体:He氦气、Ne氖气等、
二、氧化物:
Na2O氧化钠、CO一氧化碳、CO2二氧化碳、SO2二氧化硫、P2O5五氧化二磷、Fe3O4四氧化三铁、Fe2O3氧化铁(三氧化二铁)MnO2二氧化锰、H2O水、CaO氧化钙(俗称生石灰)、CuO氧化铜、H2O2过氧化氢(俗称双氧水)三、酸
H2CO3碳酸、HCl氯化氢(又称氢氯酸,水溶液俗称盐酸)、H2SO4硫酸、
HNO3硝酸、CH3COOH醋酸、
四、碱
NaOH氢氧化钠(俗称火碱、烧碱、苛性钠)、
Ca(OH) 2氢氧化钙(俗称熟石灰、消石灰、是石灰水的主要成分)
KOH氢氧化钾、NH3·H2O一水合氨(俗称氨水)
五、盐: Na2CO3碳酸钠(俗称纯碱、苏打)、K2MnO4锰酸钾、
CaCO3碳酸钙(石灰石、大理石的主要成分)、KMnO4高锰酸钾、
NaHCO3碳酸氢钠(俗称小苏打、是发酵粉的主要成分)、KCl氯化钾
CuSO4硫酸铜、CuSO4·H2O五水硫酸铜(俗称胆矾、蓝矾)
NH4HCO3碳酸氢铵、NH4Cl氯化铵、NaCl氯化钠(食盐的主要成分)
NH4NO3硝酸铵、KAl(SO4) 2·12H2O十二水合硫酸铝钾(俗称明矾)。
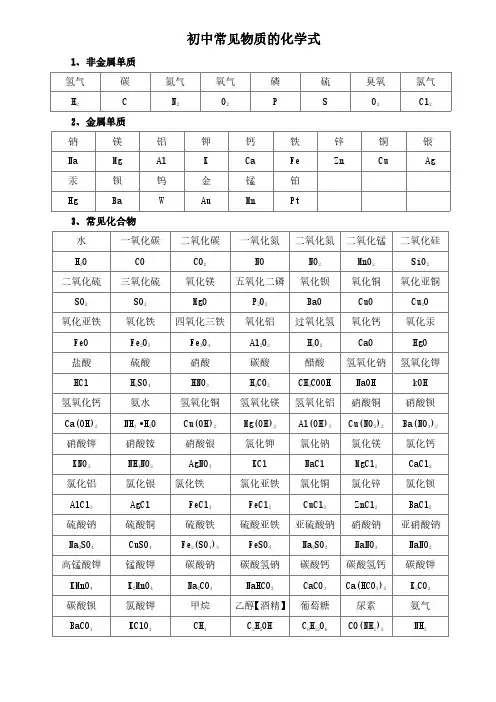
初中常见物质的化学式1、非金属单质氢气碳氮气氧气磷硫臭氧氯气H2C N2O2P S O3Cl22、金属单质钠镁铝钾钙铁锌铜银Na Mg Al K Ca Fe Zn Cu Ag 汞钡钨金锰铂Hg Ba W Au Mn Pt3、常见化合物水一氧化碳二氧化碳一氧化氮二氧化氮二氧化锰二氧化硅H2O CO CO2NO NO2MnO2SiO2二氧化硫三氧化硫氧化镁五氧化二磷氧化钡氧化铜氧化亚铜SO2SO3MgO P2O5BaO CuO Cu2O氧化亚铁氧化铁四氧化三铁氧化铝过氧化氢氧化钙氧化汞FeO Fe2O3Fe3O4Al2O3H2O2CaO HgO盐酸硫酸硝酸碳酸醋酸氢氧化钠氢氧化钾HCl H2SO4HNO3H2CO3CH3COOH NaOH kOH氢氧化钙氨水氢氧化铜氢氧化镁氢氧化铝硝酸铜硝酸钡Ca(OH)2NH3•H2O Cu(OH)2Mg(OH)2Al(OH)3Cu(NO3)2Ba(NO3)2硝酸钾硝酸铵硝酸银氯化钾氯化钠氯化镁氯化钙KNO3NH4NO3AgNO3KCl NaCl MgCl2CaCl2氯化铝氯化银氯化铁氯化亚铁氯化铜氯化锌氯化钡AlCl3AgCl FeCl3FeCl2CuCl2ZnCl2BaCl2硫酸钠硫酸铜硫酸铁硫酸亚铁亚硫酸钠硝酸钠亚硝酸钠Na2SO4CuSO4Fe2(SO4)3FeSO4Na2SO3NaNO3NaNO2高锰酸钾锰酸钾碳酸钠碳酸氢钠碳酸钙碳酸氢钙碳酸钾KMnO4K2MnO4Na2CO3NaHCO3CaCO3Ca(HCO3)2K2CO3碳酸钡氯酸钾甲烷乙醇【酒精】葡萄糖尿素氨气BaCO3KClO3CH4C2H5OH C6H12O6CO(NH2)2NH3。
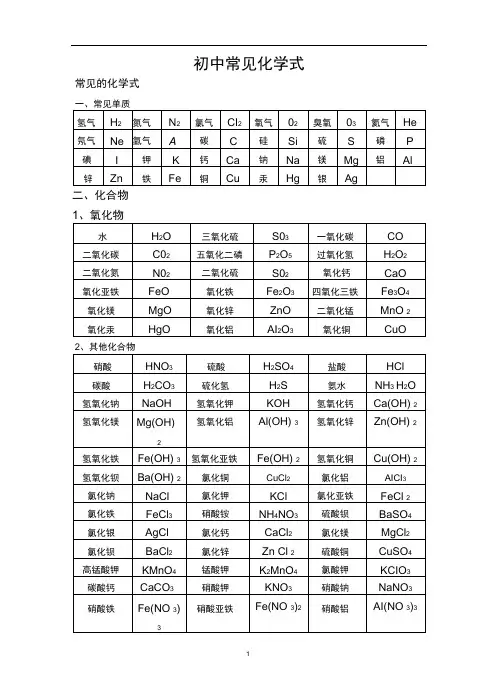
初中常见化学式常见的化学式二、化合物常见的盐硝酸镁 Mg(NO3)2、硝酸铜Cu(NO3)2、 硝酸钙Ca(NO3)2、 亚硝酸钠 NaN03、碳酸钠Na2CO3、碳酸钙 CaCO3、碳酸镁MgC03、碳酸钾K2CO3 氢氧化钠NaOH 、氢氧化钙Ca(OH)2、 氢氧化钡Ba(OH)2、氢氧化镁Mg(OH)2、氢氧化铜Cu(OH)2、 氢氧化钾KOH 、氢氧化铝Al(OH)3 (常见的碱) 氢氧化铁氢氧化亚铁Fe(OH)3、Fe(OH)2 (常见有机物) 甲烷 乙炔 甲醇乙醇碱式碳酸铜 石膏熟石膏Cu2(OH)2CO3 、 CaSO4・2H2O 、 CaSO4・H2O 明矶、KAl(SO4)2.12H2O 、绿矶 FeSO4・7H2O(常见结晶水合物)蓝矶 CuSO4.5H2O 、碳酸钠晶体 Na2CO3.10H2O(常见化肥)尿素 CO(NH2)2、硝酸铵 NH4NO3、硫酸铵(NH4)2SO4、 碳酸氢铵NH4HCO3、磷酸二氢钾KH2PO4、 硝酸钾KNO3 沉淀: 红褐色沉淀 ---- Fe(OH)3 浅绿色沉淀 ----- F e(OH)2蓝色沉淀 ----- Cu(0H)2乙酸甲醛CH4 、C2H2 、 CH3OH 、C2H5OH 、CH3COOH 、CH2O白色沉淀 -------- C aC03 、BaC03、Mg(0H)2、AI(0H)3、Zn(0H)2、AgCI、BaS04(其中仅BaS04、AgCI 是不溶于HN03的白色沉淀).淡黄色沉淀(水溶液中)----S微溶于水 ------- C a(0H)2 、CaS04、Ag2S04物质的学名、俗名及化学式⑴金刚石、石墨:C ⑵水银、汞:Hg (3)生石灰、氧化钙:Ca0(4)干冰(固体二氧化碳):C02 (5)盐酸、氢氯酸:HCI⑹亚硫酸:H2S03 (7)氢硫酸:H2S(8) 熟石灰、消石灰:Ca(0H)2(9) 苛性钠、火碱、烧碱:Na0H(10) 纯碱、苏打:Na2C03碳酸钠晶体、纯碱晶体:Na2CO3.10H2O(11) 碳酸氢钠、酸式碳酸钠:NaHC03 (也叫小苏打)(12) 胆矶、蓝矶、硫酸铜晶体:CuS04.5H2O(13) 铜绿、孔雀石:Cu2(OH)2CO3 (分解生成三种氧化物的物质)(14) 甲醇:CH30H 有毒、失明、死亡(15)酒精、乙醇:C2H5OH(16)醋酸、乙酸(16・6C冰醋酸)CH3C00H (CH3C00-醋酸根离子)具有酸的通性(17) 氨气:NH3 (碱性气体)(18) 氨水、一水合氨:NH3・H20 (为常见的碱,具有碱的通性,是一种不含金属离子的碱)(19) 亚硝酸钠:NaN02 (工业用盐、有毒)常见物质的颜色的状态1、白色固体:MgO、P2O5、CaO、NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;铁、镁为银白色(汞为银白色液态)2、黑色固体:石墨、炭粉、铁粉、CuO、MnO2、Fe3O4A KMnO4 为紫黑色3、红色固体:Cu、Fe2O3、HgO、红磷硫:淡黄色Cu2(OH)2CO3为绿色4、溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色; 凡含Fe3+的溶液呈棕黄色,其余溶液一般不无色。

初中常见物质的化学式和化学方程式关键信息:1、常见金属单质的化学式铁:Fe铜:Cu铝:Al锌:Zn镁:Mg钠:Na钾:K钙:Ca汞:Hg银:Ag2、常见非金属单质的化学式氢气:H₂氧气:O₂氮气:N₂氯气:Cl₂碳:C磷:P硫:S3、常见氧化物的化学式水:H₂O二氧化碳:CO₂一氧化碳:CO二氧化硫:SO₂三氧化硫:SO₃氧化铜:CuO氧化铁:Fe₂O₃四氧化三铁:Fe₃O₄氧化铝:Al₂O₃氧化钙:CaO氧化镁:MgO二氧化锰:MnO₂4、常见酸的化学式盐酸:HCl硫酸:H₂SO₄硝酸:HNO₃碳酸:H₂CO₃5、常见碱的化学式氢氧化钠:NaOH氢氧化钾:KOH氢氧化钙:Ca(OH)₂氢氧化镁:Mg(OH)₂氢氧化铝:Al(OH)₃氢氧化铜:Cu(OH)₂6、常见盐的化学式氯化钠:NaCl碳酸钠:Na₂CO₃碳酸氢钠:NaHCO₃碳酸钙:CaCO₃硫酸铜:CuSO₄硫酸亚铁:FeSO₄硫酸铁:Fe₂(SO₄)₃氯化亚铁:FeCl₂氯化铁:FeCl₃11 常见金属单质的化学式及相关化学方程式111 铁(Fe)铁在氧气中燃烧:3Fe + 2O₂点燃 Fe₃O₄铁与稀硫酸反应:Fe + H₂SO₄= FeSO₄+ H₂↑铁与硫酸铜溶液反应:Fe + CuSO₄= FeSO₄+ Cu112 铜(Cu)铜在空气中加热:2Cu + O₂加热 2CuO铜与硝酸银溶液反应:Cu + 2AgNO₃= Cu(NO₃)₂+ 2Ag 113 铝(Al)铝在空气中形成氧化膜:4Al + 3O₂= 2Al₂O₃铝与稀盐酸反应:2Al + 6HCl = 2AlCl₃+ 3H₂↑114 锌(Zn)锌与稀硫酸反应:Zn + H₂SO₄= ZnSO₄+ H₂↑锌与硫酸铜溶液反应:Zn + CuSO₄= ZnSO₄+ Cu 115 镁(Mg)镁在空气中燃烧:2Mg + O₂点燃 2MgO镁与稀盐酸反应:Mg + 2HCl = MgCl₂+ H₂↑116 钠(Na)钠在空气中燃烧:2Na + O₂点燃 Na₂O₂钠与水反应:2Na + 2H₂O = 2NaOH + H₂↑117 钾(K)钾在空气中燃烧:2K + O₂点燃 KO₂钾与水反应:2K + 2H₂O = 2KOH + H₂↑118 钙(Ca)钙与水反应:Ca + 2H₂O = Ca(OH)₂+ H₂↑碳酸钙高温分解:CaCO₃高温 CaO + CO₂↑12 常见非金属单质的化学式及相关化学方程式121 氢气(H₂)氢气在空气中燃烧:2H₂+ O₂点燃 2H₂O氢气还原氧化铜:H₂+ CuO 加热 Cu + H₂O122 氧气(O₂)木炭在氧气中燃烧:C + O₂点燃 CO₂硫在氧气中燃烧:S + O₂点燃 SO₂红磷在氧气中燃烧:4P + 5O₂点燃 2P₂O₅123 氮气(N₂)氮气和氢气合成氨气:N₂+ 3H₂催化剂高温高压 2NH₃124 氯气(Cl₂)氢气在氯气中燃烧:H₂+ Cl₂点燃 2HCl125 碳(C)碳在氧气中充分燃烧:C + O₂点燃 CO₂碳在氧气中不充分燃烧:2C + O₂点燃 2CO碳还原氧化铜:C + 2CuO 高温 2Cu + CO₂↑126 磷(P)磷在氧气中燃烧:4P + 5O₂点燃 2P₂O₅127 硫(S)硫在氧气中燃烧:S + O₂点燃 SO₂13 常见氧化物的化学式及相关化学方程式131 水(H₂O)电解水:2H₂O 通电 2H₂↑ + O₂↑二氧化碳与水反应:CO₂+ H₂O = H₂CO₃132 二氧化碳(CO₂)二氧化碳与澄清石灰水反应:CO₂+ Ca(OH)₂= CaCO₃↓ +H₂O碳酸钙与稀盐酸反应生成二氧化碳:CaCO₃+ 2HCl = CaCl₂+H₂O + CO₂↑133 一氧化碳(CO)一氧化碳燃烧:2CO + O₂点燃 2CO₂一氧化碳还原氧化铜:CO + CuO 加热 Cu + CO₂134 二氧化硫(SO₂)二氧化硫与水反应:SO₂+ H₂O = H₂SO₃二氧化硫与氢氧化钠溶液反应:SO₂+ 2NaOH = Na₂SO₃+H₂O135 三氧化硫(SO₃)三氧化硫与水反应:SO₃+ H₂O = H₂SO₄三氧化硫与氢氧化钠溶液反应:SO₃+ 2NaOH = Na₂SO₄+H₂O136 氧化铜(CuO)氢气还原氧化铜:H₂+ CuO 加热 Cu + H₂O一氧化碳还原氧化铜:CO + CuO 加热 Cu + CO₂137 氧化铁(Fe₂O₃)一氧化碳还原氧化铁:3CO + Fe₂O₃高温 2Fe + 3CO₂138 四氧化三铁(Fe₃O₄)一氧化碳还原四氧化三铁:4CO + Fe₃O₄高温 3Fe + 4CO₂139 氧化铝(Al₂O₃)氧化铝与盐酸反应:Al₂O₃+ 6HCl = 2AlCl₃+ 3H₂O氧化铝与氢氧化钠溶液反应:Al₂O₃+ 2NaOH = 2NaAlO₂+H₂O1310 氧化钙(CaO)氧化钙与水反应:CaO + H₂O = Ca(OH)₂1311 氧化镁(MgO)氧化镁与盐酸反应:MgO + 2HCl = MgCl₂+ H₂O1312 二氧化锰(MnO₂)过氧化氢在二氧化锰催化下分解:2H₂O₂二氧化锰 2H₂O +O₂↑氯酸钾在二氧化锰催化和加热条件下分解:2KClO₃二氧化锰加热 2KCl + 3O₂↑14 常见酸的化学式及相关化学方程式141 盐酸(HCl)盐酸与氢氧化钠反应:HCl + NaOH = NaCl + H₂O盐酸与碳酸钠反应:2HCl + Na₂CO₃= 2NaCl + H₂O + CO₂↑盐酸与碳酸钙反应:2HCl + CaCO₃= CaCl₂+ H₂O + CO₂↑142 硫酸(H₂SO₄)硫酸与氢氧化钠反应:H₂SO₄+ 2NaOH = Na₂SO₄+ 2H₂O 硫酸与锌反应:H₂SO₄+ Zn = ZnSO₄+ H₂↑硫酸与氧化铜反应:H₂SO₄+ CuO = CuSO₄+ H₂O143 硝酸(HNO₃)硝酸与氢氧化钠反应:HNO₃+ NaOH = NaNO₃+ H₂O硝酸与碳酸钙反应:2HNO₃+ CaCO₃= Ca(NO₃)₂+ H₂O +CO₂↑144 碳酸(H₂CO₃)碳酸分解:H₂CO₃= H₂O + CO₂↑15 常见碱的化学式及相关化学方程式151 氢氧化钠(NaOH)氢氧化钠与二氧化碳反应:2NaOH + CO₂= Na₂CO₃+ H₂O 氢氧化钠与硫酸反应:2NaOH + H₂SO₄= Na₂SO₄+ 2H₂O 氢氧化钠与硫酸铜溶液反应:2NaOH + CuSO₄= Cu(OH)₂↓ +Na₂SO₄152 氢氧化钾(KOH)氢氧化钾与盐酸反应:KOH + HCl = KCl + H₂O氢氧化钾与二氧化碳反应:2KOH + CO₂= K₂CO₃+ H₂O 153 氢氧化钙(Ca(OH)₂)氢氧化钙与二氧化碳反应:Ca(OH)₂+ CO₂= CaCO₃↓ + H₂O 氢氧化钙与碳酸钠溶液反应:Ca(OH)₂+ Na₂CO₃= CaCO₃↓ + 2NaOH154 氢氧化镁(Mg(OH)₂)氢氧化镁与盐酸反应:Mg(OH)₂+ 2HCl = MgCl₂+ 2H₂O155 氢氧化铝(Al(OH)₃)氢氧化铝与盐酸反应:Al(OH)₃+ 3HCl = AlCl₃+ 3H₂O氢氧化铝与氢氧化钠溶液反应:Al(OH)₃+ NaOH = NaAlO₂+2H₂O156 氢氧化铜(Cu(OH)₂)氢氧化铜受热分解:Cu(OH)₂加热 CuO + H₂O氢氧化铜与硫酸反应:Cu(OH)₂+ H₂SO₄= CuSO₄+ 2H₂O16 常见盐的化学式及相关化学方程式161 氯化钠(NaCl)氯化钠与硝酸银溶液反应:NaCl + AgNO₃=AgCl↓ + NaNO₃162 碳酸钠(Na₂CO₃)碳酸钠与盐酸反应:Na₂CO₃+ 2HCl = 2NaCl + H₂O + CO₂↑碳酸钠与氢氧化钙溶液反应:Na₂CO₃+ Ca(OH)₂= CaCO₃↓ + 2NaOH163 碳酸氢钠(NaHCO₃)碳酸氢钠受热分解:2NaHCO₃加热 Na₂CO₃+ H₂O + CO₂↑碳酸氢钠与盐酸反应:NaHCO₃+ HCl = NaCl + H₂O + CO₂↑164 碳酸钙(CaCO₃)碳酸钙与盐酸反应:CaCO₃+ 2HCl = CaCl₂+ H₂O + CO₂↑高温煅烧碳酸钙:CaCO₃高温 CaO + CO₂↑165 硫酸铜(CuSO₄)硫酸铜与铁反应:CuSO₄+ Fe = FeSO₄+ Cu硫酸铜与氢氧化钠溶液反应:CuSO₄+ 2NaOH = Cu(OH)₂↓ +Na₂SO₄166 硫酸亚铁(FeSO₄)硫酸亚铁与氢氧化钠溶液反应:FeSO₄+ 2NaOH = Fe(OH)₂↓ +Na₂SO₄167 硫酸铁(Fe₂(SO₄)₃)硫酸铁与氢氧化钠溶液反应:Fe₂(SO₄)₃+ 6NaOH =2Fe(OH)₃↓ + 3Na₂SO₄168 氯化亚铁(FeCl₂)氯化亚铁与氢氧化钠溶液反应:FeCl₂+ 2NaOH = Fe(OH)₂↓ +2NaCl169 氯化铁(FeCl₃)氯化铁与氢氧化钠溶液反应:FeCl₃+ 3NaOH = Fe(OH)₃↓ +3NaCl以上内容涵盖了初中常见物质的化学式和部分相关化学方程式,您可以根据实际需求进行调整和补充。

初中常见物质化学式一、单质1.非金属单质:(1)气体单质:O 2氧气 H 2氢气 N 2氮气 Cl 2氯气 O 3臭氧(2)固体单质:C 碳 S 硫 P 磷(红磷、白磷 ) Si 硅C 60 碳六十或足球稀2.稀有气体单质:He 氦气 Ne 氖气 Ar 氩气3.金属单质:Fe 铁 Cu 铜 Al 铝 Zn 锌 Ag 银 Mg 镁Hg 汞 K 钾 Ca 钙 Na 钠二、化合物1.氧化物:(1)非金属氧化物 (液体): H 2O 水 H 2O 2过氧化氢 (气体):CO 一氧化碳 SO 2 二氧化硫 NO 2二氧化氮 CO 2二氧化碳 SO 3三氧化硫 (固体):P 2O 5五氧化二磷 (2)金属氧化物(固体):CaO 氧化钙 Al 2O 3氧化铝 MnO 2二氧化锰 CuO 氧化铜FeO 氧化亚铁 Fe 2O 3氧化铁 Fe 3O 4四氧化三铁Na 2O 氧化钠 MgO 氧化镁 ZnO 氧化锌 HgO 氧化汞 2.酸:(液体)HCl 盐酸 H 2SO 4 硫酸 HNO 3 硝酸 H 2CO 3 碳酸 CH 3COOH 乙酸3.碱:(固体)NaOH 氢氧化钠 NH 3 .H 2O 氨水B a (O H )2氢氧化钡C a (O H )2氢氧化钙A l (O H )3氢氧化铝 F e (O H )2氢氧化亚铁 F e (O H )3氢氧化铁 C u (O H )2氢氧化铜 4.盐(固体):NaCl 氯化钠 KCl 氯化钾 CaCl 2氯化钙 ZnCl 2氯化锌 BaCl 2氯化钡 FeCl 2氯化亚铁 Fe Cl 3氯化铁 AgCl 氯化银 -----盐酸盐CuSO 4硫酸铜 ZnSO 4 硫酸锌 CaSO 4 硫酸钙 MgSO 4硫酸镁 FeSO 4硫酸亚铁 Fe 2(SO4)3 硫酸铁 BaSO 4硫酸钡 -----硫酸盐 Na 2CO 3碳酸钠 CaCO 3碳酸钙 NaHCO 3碳酸氢钠 K 2CO 3 碳酸钾 ------碳酸盐 KNO 3 硝酸钾 C u (N O 3)2硝酸铜 AgNO 3硝酸银 B a (N O 3)2 硝酸钡 -------硝酸盐 KClO 3 氯酸钾 KMnO 4高锰酸钾 K 2MnO 4锰酸钾 --------其他盐 化学肥料常见氮肥 :CO(NH 2)2尿素(有机物) NH 4NO 3硝酸铵 NH 4HCO 3碳酸氢氨 NH 4Cl 氯化铵 常见钾肥 :KCI 氯化钾 K 2CO 3 碳酸钾常见磷肥:C a (H 2P O 4)2 磷酸二氢钙 CaHPO 4磷酸氢钙 常见复合肥:KNO 3 硝酸钾 KH 2PO 4 磷酸二氢钾常见有机物CH 4甲烷 C 2H 5OH 乙醇 C 6H 12O 6 葡萄糖 C 12H 22O 11 蔗糖 CH 3COOH 醋酸初中化学方程式全(已配平). 一、化合反应1、镁在空气中燃烧:2Mg+ O 2 点燃 2MgO2、铁在氧气中燃烧:3Fe +2O 2 点燃 Fe 3O 43、铝在空气中燃烧:4Al+ 3O 2 点燃 2Al 2O 34、氢气在空气中燃烧:2H 2 +O 2 点燃 2H 2O6、硫粉在空气中燃烧: S+ O2点燃 SO27、碳在氧气中充分燃烧:C +O2 点燃 CO28、碳在氧气中不充分燃烧:2点燃 2CO9、二氧化碳通过灼热碳层:2高温 2CO10、一氧化碳在氧气中燃烧:2CO +O2 点燃 2CO211:CO2 +H2O === H2CO312、生石灰溶于水:CaO+ H2O === Ca(OH)213、无水硫酸铜作干燥剂:CuSO4 +5H2O ==== CuSO4·5H2O14、钠在氯气中燃烧:2Na+ Cl2点燃 2NaCl 二、分解反应15、实验室用双氧水制氧气:2H2O2MnO22H2O +O2↑16、加热高锰酸钾:2KMnO4 加热 K22+O2↑172通电 2H2↑+O2↑1823 === H2O +CO2↑19、高温煅烧石灰石(二氧化碳工业制法):CaCO3高温 CaO+ CO2↑三、置换反应20、铁和硫酸铜溶液反应:Fe+ CuSO4 == FeSO4+Cu21、锌和稀硫酸反应(实验室制氢气):Zn+ H2SO4== ZnSO4+H2↑22、镁和稀盐酸反应:Mg +2HCl === MgCl2 +H2↑23、氢气还原氧化铜:H2 +CuO 加热 Cu +H2O24、木炭还原氧化铜:C+ 2CuO 高温 2Cu +CO2↑25、甲烷在空气中燃烧:CH4点燃 CO2+2H2O26、水蒸气通过灼热碳层:H2O +C 高温 H2+CO27、焦炭还原氧化铁:3C +2Fe2O3高温 4Fe +3CO2↑其他28、氢氧化钠溶液与硫酸铜溶液反应:2NaOH+ CuSO4 == Cu(OH)2↓+ Na2SO429、甲烷在空气中燃烧:CH4 +2O2点燃 CO2+2H2O30、酒精在空气中燃烧:C2H52点燃 2CO2+3H2O31、一氧化碳还原氧化铜:CO +CuO 加热 Cu+ CO232、一氧化碳还原氧化铁:23高温 2Fe+ 3CO233:Ca(OH)2+ CO2==== CaCO3↓+ H2O34、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH+ CO2 ==== Na2CO3+H2O35、石灰石(或小学音乐教案大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO3 +2HCl === CaCl2+H2O +CO2↑36、碳酸钠与浓盐酸反应(泡沫灭火器的原理): Na2CO3+ 2HCl === 2NaCl +H2O+CO2↑一.物质与氧气的反应:(1)单质与氧气的反应:1. 镁在空气中燃烧:2Mg+ O2点燃 2MgO2. 铁在氧气中燃烧:3Fe+ 2O2点燃 Fe3O43. 铜在空气中受热:2Cu+ O2加热 2CuO4. 铝在空气中燃烧:4Al +3O2 点燃 2Al2O35. 氢气中空气中燃烧:2H22点燃 2H2O7. 硫粉在空气中燃烧: S +O2 点燃 SO28. 碳在氧气中充分燃烧:2点燃 CO29. 碳在氧气中不充分燃烧:2点燃 2CO (2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO+ O2点燃 2CO211. 甲烷在空气中燃烧:CH4 +2O2点燃 CO22O12. 酒精在空气中燃烧:C2H52点燃 2CO2+3H2O二.几个分解反应:13. 水在直流电的作用下分新概念英语第一册解:2H2O 通电 2H2↑+ O2↑14. 加热碱式碳酸铜:Cu2(OH)2CO3加热 2CuO +H2O +CO2↑15.3 ==== 2KCl+ 3O2↑16. 加热高锰酸钾:2KMnO4 加热 K2MnO4+MnO2+O2↑17. 碳酸不稳定而分解:H232O +CO2↑18. 高温煅烧石灰石:CaCO3 高温 CaO +CO2↑三.几个氧化还原反应:19. 氢气还原氧化铜:H2+ CuO 加热 Cu+ H2O20. 木炭还原氧化铜:C+ 2CuO 高温 2Cu +CO2↑ 2 初三化学方程式大合集21. 焦炭还原氧化铁:3C+ 2Fe2O3高温 4Fe+ 3CO2↑22. 焦炭还原四氧化三铁:2C +Fe3O4高温 3Fe+ 2CO2↑23. 一氧化碳还原氧化铜:CO +CuO 加热 Cu+ CO224. 一氧化碳还原氧化铁:3CO+ Fe23高温 2Fe +3CO225. 一氧化碳还原四氧化三铁:34高温 3Fe+ 4CO2(1)金属单质+酸 -------- 盐+氢气(置换反应)26. 锌和稀硫酸Zn+ H2SO4= ZnSO4+ H2↑27. 铁和稀硫酸Fe +H2SO4= FeSO4+ H2↑28. 镁和稀硫酸Mg +H2SO4= MgSO4+H2↑29. 铝和稀硫酸2Al+ 3H2SO4= Al2(SO4)3+3H2↑30. 锌和稀盐酸Zn +2HCl === ZnCl2+ H2↑31. 铁和稀盐酸Fe+ 2HCl === FeCl2+ H2↑32. 镁和语文教案格式稀盐酸Mg 2HCl === MgCl2+ H2↑33. 铝和稀盐酸2Al+ 6HCl == 2AlCl3 +3H2↑(2)金属单质+ 盐(溶液) ------- 另一种金属+另一种盐34. 铁和硫酸铜溶液反应:Fe+ CuSO4 === FeSO4+ Cu35. 锌和硫酸铜溶液反应:Zn+ CuSO4 === ZnSO4+ Cu36. 铜和硝酸汞溶液反应:Cu +Hg(NO3)2=== Cu(NO3)2+Hg(3)碱性氧化物+酸 -------- 盐+ 水37. 氧化铁和稀盐酸反应:Fe2O3+ 6HCl === 2FeCl3+ 3H2O38. 氧化铁和稀硫酸反应:Fe2O3+3H2SO4=== Fe2(SO4)3+ 3H2O39. 氧化铜和稀盐酸反应:CuO +2HCl ==== CuCl2 +H2O40. 氧化铜和稀硫酸反应:CuO +H2SO4==== CuSO4+ H2O41. 氧化镁和稀硫酸反应:MgO+ H2SO4==== MgSO4+ H2O42. 氧化钙和稀盐酸反应:CaO +2HCl ==== CaCl2 +H2O(4)酸性氧化物+碱 -------- 盐+水43.苛性钠暴露在空气中变质:2NaOH +CO2 ==== Na2CO3+H2O44.苛性钠吸收二氧化硫气体:2NaOH +SO2 ==== Na2SO3+H2O45.苛性钠吸收三氧化硫气体:2NaOH+ SO3 ==== Na2SO4+ H2O46.消石灰放在空气中变质:Ca(OH)2+ CO2==== CaCO3↓+ H2O47. 消石灰吸收二氧化硫:Ca(OH)2 +SO2==== CaSO3↓+H2O(5)酸+碱 -------- 盐+水48.盐酸和烧碱起反应:HCl+ NaOH ==== NaCl+ H2O49. 盐酸和氢氧化钾反应:HCl+ KOH ==== KCl+H2O50.盐酸和氢氧化初中家长会课件铜反应:2HCl+ Cu(OH)2 ==== CuCl2+2H2O51. 盐酸和氢氧化钙反应:2HCl+ Ca(OH)2 ==== CaCl2+2H2O52. 盐酸和氢氧化铁反应:3HCl+ Fe(OH)3 ==== FeCl3+3H2O53.氢氧化铝药物治疗胃酸过多:3HCl +Al(OH)3 ==== AlCl3+3H2O54.硫酸和烧碱反应:H2SO4 +2NaOH ==== Na2SO4+2H2O55.硫酸和氢氧化钾反应:H2SO4 +2KOH ==== K2SO4+2H2O56.硫酸和氢氧化铜反应:H2SO4 +Cu(OH)2==== CuSO4+2H2O57. 硫酸和氢氧化铁反应:3H2SO4+2Fe(OH)3==== Fe2(SO4)3+ 6H2O58. 硝酸和烧碱反应:HNO3+ NaOH ==== NaNO3 +H2O(6)酸+盐 -------- 另一种酸+另一种盐59.大理石与稀盐酸反应:CaCO3 +2HCl === CaCl2H2O +CO2↑60.碳酸钠与稀盐酸反应: Na2CO3+2HCl === 2NaCl +H2O+ CO2↑61.碳酸镁与稀盐酸反应: MgCO3 +2HCl === MgCl2+H2O+CO2↑62.盐酸和硝酸银溶液反应:HCl+ AgNO3=== AgCl↓+ HNO363.硫酸和碳酸钠反应:Na2CO3+H2SO4=== Na2SO4+H2O +CO2↑64.硫酸和氯化钡溶液反应:H2S O4+BaCl2==== BaSO4↓+ 2HCl(7)碱+盐 -------- 另一种碱+另一种盐65.氢氧化钠与硫酸铜:2NaOH CuSO4 ==== Cu(OH)2↓ Na2SO466.氢氧化钠与氯化铁:3NaOH FeCl3 ==== Fe(OH)3↓ 3NaCl67.氢氧化钠与氯化镁:2NaOH MgCl2 ==== Mg(OH)2↓ 2NaCl68. 氢氧化钠与氯化铜:2NaOH CuCl2 ==== Cu(OH)2↓ 2NaCl69. 氢氧化钙与碳酸钠:Ca(OH)2 Na2CO3=== CaCO3↓ 2NaOH(8)盐+ 盐 ----- 两种新盐70.氯化钠溶液新概念英语第二册和硝酸银溶液:NaCl +AgNO3==== AgCl↓+NaNO371.硫酸钠和氯化钡:Na2SO4+ BaCl2==== BaSO4↓+ 2NaCl五.其它反应:72.二氧化碳溶解于水:CO2+ H2O === H2CO373.生石灰溶于水:CaO+ H2O === Ca(OH)274.氧化钠溶于水:Na2O +H2O ==== 2NaOH75.三氧化硫溶于水:SO3 +H2O ==== H2SO476.硫酸铜晶体受热分解:CuSO4·5H2O 加热 CuSO45H2O77.无水硫酸铜作干燥剂:CuSO4+ 5H24·5H2化学方程式反应现象应用2Mg+ O 2点燃或Δ2MgO 剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟 2Hg +O 点燃或Δ2HgO 银白液体、生成红色固体 拉瓦锡实验 2Cu+ O 点燃或Δ2CuO 红色金属变为黑色固体 2点燃或Δ2Al 2O 3 银白金属变为白色固体 3Fe+ 2O 点燃Fe3O4 剧烈燃烧、火星四射、生成黑色固体、放热 4Fe +3O2高温2Fe 2O 3C+ O 2 点燃CO 2 剧烈燃烧、白光、放热、使石灰水变浑浊 S +O 2 点燃SO 2 剧大学英语四级烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.2H 2 O 2 点燃2H 2O 淡蓝火焰、放热、生成使无水CuSO 4变蓝的液体(水) 高能燃料4P +5O2 点燃2P 2O 5 剧烈燃烧、大量白烟、放热、生成白色固体 证明空气中氧气含量CH 4+ 2O 2点燃2H 2O+ CO 2 蓝色火焰、放热、生成使石灰水变浑浊气体和使无水CuSO 4变蓝的液体(水) 甲烷和天然气的燃烧2C 2H 2+ 5O 点燃2H 2O +4CO 2 蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体和使无水4 氧炔焰、焊接切割金属2KClO 3MnO2、Δ2KCl +3O 2↑ 生成使带火星的木条复燃的气体 实验室制备氧气 2KMnO 4Δ K2MnO 4 MnO 2 +O 2↑ 紫色变为黑色、生成使带火星木条复燃的气体 实验室制备氧论文气2HgO Δ2Hg+ O 2↑ 红色变为银白、生成使带火星木条复燃的气体 拉瓦锡实验 通电2H 2↑+ O 2↑ 水通电分解为氢气和氧气 电解水Cu 223Δ2CuO +H 2O+ CO 2↑ 绿色变黑色、试管壁有液体、使石灰水变浑浊气体 NH 4HCO 3ΔNH 3↑+ H 2O+ CO 2↑ 白色固体消失、管壁有液体、使石灰水变浑浊气体 碳Zn+ H 2SO 4=ZnSO 4 +H 2↑ 有大量气泡产生、锌粒逐渐溶解 实验室制备氢气 Fe +H 2SO 4=FeSO 4 +H 2↑ 有大量气泡产生、金属颗粒逐渐溶解 Mg +H 2SO 4 =MgSO 4 +H 2↑ 有大量气泡产生、金属颗粒逐渐溶解2Al+ 3H 2SO 4=Al 2(SO4)3+ 3H 2↑ 有大量气泡产生、金属颗粒逐渐溶解Fe 2O 3+3H 2 Δ 2Fe +3H 2O 红色逐渐变为银白色、试管壁有液体 冶炼金属、利用 Fe 3O 4 +4H 2 Δ3Fe+ 4H 2O 黑色逐渐变为银白色英语翻译、试管壁有液体 冶炼金属、WO 3 +3H 2Δ W +3H 2O 冶炼金属钨、利用氢气的还原性 MoO 32 ΔMo +3H 2O 冶炼金属钼、利用氢气的还原性2Na+ Cl 2Δ或点燃2NaCl 剧烈燃烧、黄色火焰 离子化合物的形成、H 2 +Cl 2点燃或光照 2HCl 点燃苍白色火焰、瓶口白雾 共价化合物的形成、制备盐酸CuSO 4 +2NaOH=Cu(OH)2↓+ Na 2SO 4 蓝色沉淀生成、上部为澄清溶液 质量守恒定律实验2C +O 点燃2CO 煤炉中常见反应、空气污染物之一、煤气中毒原因 点燃2CO 2 蓝色火焰 煤气燃烧C+ CuO 高温2Cu+ CO2↑ 黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体冶炼金属2Fe2O3+ 3C 高温4Fe+ 3CO2↑ 冶炼金属Fe3O4+2C高温3Fe+ 2CO2↑ 冶炼金属C+ CO2 高温2COCO2+H2O = H2CO3碳酸使石蕊变红证明碳酸的酸性小学三语文教学论文H2CO3ΔCO2↑+ H2O 石蕊红色褪去2+CO2= CaCO3↓+ H2O 澄清石灰水变浑浊应用CO2检验和石灰浆粉刷墙壁CaCO3 +H2O+ CO2= Ca(HCO3)2白色沉淀逐渐溶解溶洞的形成,石头的风化Ca(HCO3)2ΔCaCO3↓+ H2O +CO2↑ 白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成.钟乳石的形成2NaHCO3ΔNa2CO3+ H2O +CO2↑ 产生使澄清石灰水变浑浊的气体小苏打蒸馒头CaCO3 高温 CaO +CO2↑ 工业制备二氧化碳和生石灰CaCO3 2+ H2O +CO2↑ 固体逐渐溶解、有使澄清石灰水变浑浊的气体实验室制备二氧化碳、除水垢初中化学方程式汇总一、氧气的性质:(1)单质与氧气的反应:(化合反应)1. 镁在空气中燃烧:2Mg+ O2点燃 2MgO2. 铁在氧气中燃烧:3Fe+ 2O2点燃 Fe3O43. 铜在空气中受热:2Cu+ O2加热 2CuO4. 铝在空气中燃烧:4Al +3O2 点燃2Al2O 35. 氢气中空气中燃烧:2H2 +O2点燃 2H2O6. :4P +5O2点燃 2P2O57. 硫粉在空气中燃烧: S +O2 点燃 SO28. 碳在氧气中充分燃烧:2点燃 CO29. 碳在氧气中不充分燃烧:2点燃 2CO (2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO+O2点燃 2CO211. 甲烷在空气中燃烧:CH4 +2O2点燃 CO2+2H2O12. 酒精在空气中燃烧:C2H52点燃 2CO2+3H2O(3)氧气的来源:13.玻义耳研究空气的成分实验 2HgO 加热 Hg +O2↑14.加热高锰酸钾:2KMnO4加热 K242+O2↑(实验室制氧气原理1)15 H2O2MnO22H2O+ O2↑(实验室制氧气原理2)二、自然界中的水:16.水在直流电的作用下分解(研究水的组成实验):2H2O 通电 2H2↑+O2↑17.生石灰溶于水英语六级作文:CaO +H2O == Ca(OH)218.二氧化碳可溶于水: H2O+CO2==H2CO3三、质量守恒定律:19.镁在空气中燃烧:2Mg+ O2点燃 2MgO20.铁和硫酸铜溶液反应:44+ Cu21.氢气还原氧化铜:H2 +CuO 加热 Cu +H2O22. 镁还原氧化铜:Mg+ CuO 加热 Cu +MgO四、碳和碳的氧化物:(1)碳的化学性质23. 碳在氧气中充分燃烧:C + O2点燃 CO224.木炭还原氧化铜:C + 2CuO 高温 2Cu+ CO2↑25.焦炭还原氧化铁:3C + 2Fe2O3高温 4Fe + 3CO2↑(2)煤炉中发生的三个反应:26.煤炉的底层:C +O点燃 CO2 27.煤炉的中层:CO2+ C 高温 2CO282CO +O2点燃 2CO2(3)二氧化碳的制法与性质:29.大理石与稀盐酸反应(实验室制二氧化碳):CaCO3+ 2HCl == CaCl2+ H2O +CO2↑30.碳酸不稳定而分解:H2CO3== H2O +CO2↑31.二氧化碳可溶于水: H2O +CO2== H2CO332.高温煅烧石灰石(工业制二氧化碳):CaCO3高温 CaO+ CO2↑33:Ca(OH)2 +CO2=== CaCO3↓+H2O(4)一氧化碳的性质:34.一氧化碳还原氧化铜:CO+ CuO 加热 Cu +CO235.一氧化碳的可燃性:2CO +O2点燃 2CO2其它反应:36.碳酸钠与稀盐酸反应(灭火器的原理):Na2CO32HCl == 2NaCl+ H2O +CO2↑五、燃料及其利用:37.甲烷在空气中燃烧:CH4 +2O2点燃 CO2+2H2O38.酒精在空气中燃烧:C2H5OH +3O2 点燃 2CO2+3H2O39.氢气中空气中燃烧:2H2+ O2点燃 2H2六、金属(1)金属与氧气反应:40.镁在空气中燃烧:2Mg+ O2点燃 2MgO41.铁在氧气中燃烧:3Fe +2O2点燃 Fe3O442. 铜在空气中受热:2Cu +O2加热 2CuO43. 铝在空气中形成氧化膜:2 = 2Al2O3(2)金属单质酸 -------- 盐氢气(置换反应)44. 锌和稀硫酸Zn+ H2SO4= ZnSO4+ H2↑45. 铁和稀硫酸Fe +H2SO4= FeSO4+H2↑46. 镁和稀硫酸Mg +H2SO4= MgSO4+ H2↑47. 铝和稀硫酸2Al+ 3H2SO4= Al2(SO4)3+3H2↑48. 锌和稀盐酸Zn+ 2HCl == ZnCl2+ H2↑49. 铁和稀盐酸Fe +2HCl == FeCl2 +H2↑50. 镁和稀盐酸Mg +2HCl == MgCl2+ H2↑51.铝和稀盐酸2Al+ 6HCl == 2AlCl3 +3H2↑(3)金属单质盐怎样学好高中物理(溶液) ------- 新金属新盐52. 铁和硫酸铜溶液反应:Fe +CuSO4 == FeSO4+Cu53. 锌和硫酸铜溶液反应:Zn +CuSO4 ==ZnSO4+Cu54. 铜和硝酸汞溶液反应:Cu +Hg(NO3)2== Cu(NO3)2+Hg(3)金属铁的治炼原理:55.3CO +2Fe2O3高温 4Fe +3CO2↑七、酸、碱、盐1、酸的化学性质(1)酸金属 -------- 盐氢气(见上)(2)酸金属氧化物-------- 盐水56. 氧化铁和稀盐酸反应:Fe2O3+6HCl ==2FeCl3+3H2O57. 氧化铁和稀硫酸反应:Fe2O3+3H2SO4 == Fe2(SO4)3+3H2O58. 氧化铜和稀盐酸反应:CuO +2HCl ==CuCl2+H2O59. 氧化铜和稀硫酸反应:CuO+ H2SO4 == CuSO4+ H2O(3)酸碱 -------- 盐水(中和反应)60.盐酸和烧碱起反应:HCl +NaOH == NaCl+H2O61. 盐酸和氢氧化钙反应:2HCl+ Ca(OH)2 == CaCl2+2H2O62. 氢氧化铝药物治疗胃酸过多:3HCl +Al(OH)3 == AlCl3+3H2O63. 硫酸和烧碱反应:H2SO4+ 2NaOH == Na2SO4+2H2O(4)酸盐 -------- 另一种酸另一种盐64.大理石与稀盐酸反应:CaCO3+2HCl == CaCl2+H2O+ CO2↑65.碳酸钠与稀盐酸反应: Na2CO3+2HCl == 2NaCl+ H2O+ CO2↑66.碳酸氢钠与稀盐酸反应:NaHCO3 +HCl== NaCl+H2O+ CO2↑67. 硫酸和氯化钡溶液反应:H 2SO 4 +BaCl 2 == BaSO 4↓+2HCl 2、碱的幼儿园小班音乐教案化学性质 (1) 碱 非金属氧化物 -------- 盐 水68.苛性钠暴露在空气中变质:2NaOH+CO 2 == Na 2CO 3+ H 2O 69.苛性钠吸收二氧化硫气体:2NaOH +SO 2 == Na 2SO 3 +H 2O 70.苛性钠吸收三氧化硫气体:2NaOH+ SO 3 == Na 2SO 4 +H 2O 71.消石灰放在空气中变质:Ca(OH)2+ CO 2 == CaCO 3↓+H 2O 72. 消石灰吸收二氧化硫:Ca(OH)2 +SO 2 == CaSO 3↓+ H 2O (2)碱 酸-------- 盐 水(中和反应,方程式见上) (3)碱 盐 -------- 另一种碱 另一种盐73. 氢氧化钙与碳酸钠:Ca(OH)2 +Na 2CO 3 == CaCO 3↓+ 2NaOH 3、盐的化学性质(1)盐(溶液) 金属单质------- 另一种金属 另一种盐 74. 铁和硫酸铜溶液反应:Fe+ CuSO 4 == FeSO 4 +Cu (2)盐 酸-------- 另一种酸 另一种盐75.碳酸钠与稀盐酸反应: Na 2CO 3 +2HCl == 2NaCl +H 2O+ CO 2↑ 碳酸氢钠与稀盐酸反应:NaHCO 3 +HCl== NaCl+ H 2O +CO 2↑ (3)盐 碱 -------- 另一种碱 另一种盐76. 氢氧化钙与碳酸钠:Ca(OH)2 +Na 2CO 3 == CaCO 3↓+ 2NaOH (4)盐 盐 ----- 两种新盐77.氯化钠溶液和硝酸银溶液:NaCl +AgNO 3 == AgCl↓+NaNO 3 78.硫酸钠和氯化钡:Na 2SO 4 +BaCl 2 == BaSO4↓+2NaCl 一、其他反应类型1、二氧化碳通入澄清石灰水中:CO 2 + Ca(OH)2 == CaCO 3↓+ H 2O2、氢氧化钠在空气中变质:CO 2+ 2NaOH = Na 2CO 3 + H 2O3、氢氧化钠溶液吸收二氧化硫:SO 2 + 2NaOH ==Na 2SO 3+ H 2O4、一氧化碳还原氧化铜:CO + CuO Cu + CO 25、酒精燃烧:C 2H 5OH + 3O 2 2CO 2 + 3H 2O6、甲烷燃烧:CH 4 + 2O 2 CO 2 + 2H 2O△点燃 点燃。
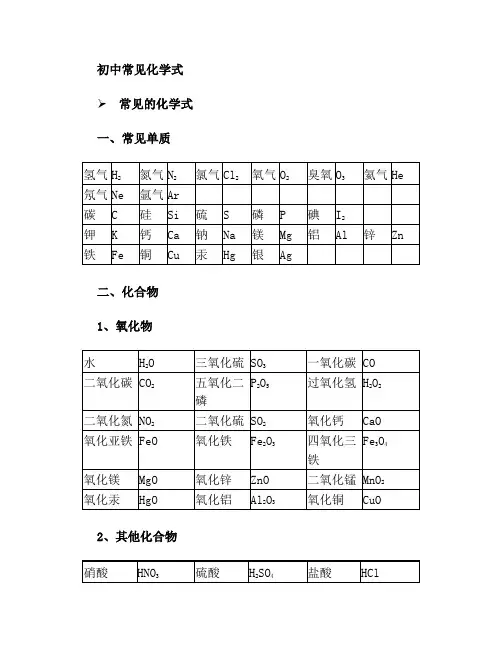
初中常见化学式➢ 常见的化学式一、常见单质二、化合物1、氧化物2、其他化合物3、常见有机化合物初中化学方程式全(已配平).一、化合反应1、镁在空气中燃烧:2Mg O2点燃 2MgO2、铁在氧气中燃烧:3Fe 2O2点燃 Fe3O43、铝在空气中燃烧:4Al 3O2点燃 2Al2O34、氢气在空气中燃烧:2H2 O2点燃 2H2O5、红磷在空气中燃烧:4P 5O2点燃 2P2O56、硫粉在空气中燃烧: S O2点燃 SO27、碳在氧气中充分燃烧:C O2 点燃CO28、碳在氧气中不充分燃烧:2C O2点燃 2CO9、二氧化碳通过灼热碳层: C CO2高温 2CO10、一氧化碳在氧气中燃烧:2CO O2 点燃 2CO211、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2 H2O === H2CO312、生石灰溶于水:CaO H2O === Ca(OH)213、无水硫酸铜作干燥剂:CuSO4 5H2O ==== CuSO4·5H2O14、钠在氯气中燃烧:2Na Cl2点燃 2NaCl二、分解反应15、实验室用双氧水制氧气:2H2O2MnO2 2H2O O2↑16、加热高锰酸钾:2KMnO4 加热 K2MnO4 MnO2 O2↑17、水在直流电的作用下分解:2H2O 通电 2H2↑ O2↑18、碳酸化学物理学报不稳定而分解:H2CO3 === H2O CO2↑19、高温煅烧石灰石(二氧化碳工业制法):CaCO3高温 CaO CO2↑三、置换反应20、铁和硫酸铜溶液反应:Fe CuSO4 == FeSO4 Cu21、锌和稀硫酸反应(实验室制氢气):Zn H2SO4 == ZnSO4H2↑22、镁和稀盐酸反应:Mg 2HCl === MgCl2 H2↑23、氢气还原氧化铜:H2 CuO 加热 Cu H2O24、木炭还原氧化铜:C 2CuO 高温2Cu CO2↑25、甲烷在空气中燃烧:CH4 2O2 点燃 CO2 2H2O26、水蒸气通过灼热碳层:H2O C 高温H2 CO27、焦炭还原氧化铁:3C 2Fe2O3高温4Fe 3CO2↑其他28、氢氧化钠溶液与硫酸铜溶液反应:2NaOH CuSO4 == Cu(OH)2↓ Na2SO429、甲烷在空气中燃烧:CH4 2O2点燃CO2 2H2O30、酒精在空气中燃烧:C2H5OH 3O2点燃 2CO2 3H2O31、一氧化碳还原氧化铜:CO CuO加热Cu CO232、一氧化碳还原氧化铁:3CO Fe2O3高温2Fe 3CO233、二氧化碳通过澄清石灰水(检验二氧化碳):Ca(OH)2 CO2==== CaCO3 ↓ H2O34、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH CO2 ==== Na2CO3 H2O35、石灰石(或小学音乐教案大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO3 2HCl === CaCl2 H2O CO2↑36、碳酸钠与浓盐酸反应(泡沫灭火器的原理): Na2CO3 2HCl=== 2NaCl H2O CO2↑一.物质与氧气的反应:(1)单质与氧气的反应:1. 镁在空气中燃烧:2Mg O2点燃 2MgO2. 铁在氧气中燃烧:3Fe 2O2点燃 Fe3O43. 铜在空气中受热:2Cu O2加热 2CuO4. 铝在空气中燃烧:4Al 3O2点燃 2Al2O35. 氢气中空气中燃烧:2H2 O2点燃 2H2O6. 红磷在空气中燃烧:4P 5O2点燃 2P2O57. 硫粉在空气中燃烧: S O2 点燃 SO28. 碳在氧气中充分燃烧:C O2点燃CO29. 碳在氧气中不充分燃烧:2C O2点燃 2CO(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO O2点燃 2CO211. 甲烷在空气中燃烧:CH4 2O2点燃 CO2 2H2O12. 酒精在空气中燃烧:C2H5OH 3O2点燃2CO23H2O二.几个分解反应:13. 水在直流电的作用下分新概念英语第一册解:2H2O 通电2H2↑ O2↑14. 加热碱式碳酸铜:Cu2(OH)2CO3加热2CuO H2O CO2↑15. 加热氯酸钾(有少量的二氧化锰):2KClO3 ==== 2KCl 3O2↑16. 加热高锰酸钾:2KMnO4 加热 K2MnO4 MnO2 O2↑17. 碳酸不稳定而分解:H2CO3 === H2O CO2↑18. 高温煅烧石灰石:CaCO3 高温 CaO CO2↑三.几个氧化还原反应:19. 氢气还原氧化铜:H2 CuO 加热Cu H2O20. 木炭还原氧化铜:C 2CuO 高温2Cu CO2↑2 初三化学方程式大合集21. 焦炭还原氧化铁:3C 2Fe2O3 高温4Fe 3CO2↑22. 焦炭还原四氧化三铁:2C Fe3O4高温 3Fe 2CO2↑23. 一氧化碳还原氧化铜:CO CuO 加热 Cu CO224. 一氧化碳还原氧化铁:3CO Fe2O3高温2Fe 3CO225. 一氧化碳还原四氧化三铁:4CO Fe3O4高温 3Fe 4CO2四.单质、氧化物、酸、碱、盐的相互关系(1)金属单质酸 -------- 盐氢气(置换反应)26. 锌和稀硫酸Zn H2SO4 = ZnSO4 H2↑27. 铁和稀硫酸Fe H2SO4 = FeSO4 H2↑28. 镁和稀硫酸Mg H2SO4 = MgSO4 H2↑29. 铝和稀硫酸2Al 3H2SO4 = Al2(SO4)3 3H2↑30. 锌和稀盐酸Zn 2HCl === ZnCl2 H2↑31. 铁和稀盐酸Fe 2HCl === FeCl2 H2↑32. 镁和语文教案格式稀盐酸Mg 2HCl === MgCl2 H2↑33. 铝和稀盐酸2Al 6HCl == 2AlCl3 3H2↑(2)金属单质盐(溶液) ------- 另一种金属另一种盐34. 铁和硫酸铜溶液反应:Fe CuSO4 === FeSO4 Cu35. 锌和硫酸铜溶液反应:Zn CuSO4 === ZnSO4 Cu36. 铜和硝酸汞溶液反应:Cu Hg(NO3)2 === Cu(NO3)2 Hg(3)碱性氧化物酸 -------- 盐水37. 氧化铁和稀盐酸反应:Fe2O3 6HCl === 2FeCl3 3H2O38. 氧化铁和稀硫酸反应:Fe2O3 3H2SO4 === Fe2(SO4)3 3H2O39. 氧化铜和稀盐酸反应:CuO 2HCl ==== CuCl2 H2O40. 氧化铜和稀硫酸反应:CuO H2SO4 ==== CuSO4 H2O41. 氧化镁和稀硫酸反应:MgO H2SO4 ==== MgSO4 H2O42. 氧化钙和稀盐酸反应:CaO 2HCl ==== CaCl2 H2O(4)酸性氧化物碱 -------- 盐水43.苛性钠暴露在空气中变质:2NaOH CO2 ==== Na2CO3 H2O 44.苛性钠吸收二氧化硫气体:2NaOH SO2 ==== Na2SO3 H2O 45.苛性钠吸收三氧化硫气体:2NaOH SO3 ==== Na2SO4 H2O 46.消石灰放在空气中变质:Ca(OH)2 CO2 ==== CaCO3 ↓ H2O 47. 消石灰吸收二氧化硫:Ca(OH)2 SO2 ==== CaSO3↓ H2O(5)酸碱 -------- 盐水48.盐酸和烧碱起反应:HCl NaOH ==== NaCl H2O49. 盐酸和氢氧化钾反应:HCl KOH ==== KCl H2O50.盐酸和氢氧化初中家长会课件铜反应:2HCl Cu(OH)2 ==== CuCl2 2H2O51. 盐酸和氢氧化钙反应:2HCl Ca(OH)2 ==== CaCl2 2H2O52. 盐酸和氢氧化铁反应:3HCl Fe(OH)3 ==== FeCl3 3H2O53.氢氧化铝药物治疗胃酸过多:3HCl Al(OH)3 ==== AlCl3 3H2O54.硫酸和烧碱反应:H2SO4 2NaOH ==== Na2SO4 2H2O55.硫酸和氢氧化钾反应:H2SO4 2KOH ==== K2SO4 2H2O56.硫酸和氢氧化铜反应:H2SO4 Cu(OH)2 ==== CuSO4 2H2O57. 硫酸和氢氧化铁反应:3H2SO4 2Fe(OH)3==== Fe2(SO4)3 6H2O58. 硝酸和烧碱反应:HNO3 NaOH ==== NaNO3 H2O(6)酸盐 -------- 另一种酸另一种盐59.大理石与稀盐酸反应:CaCO3 2HCl === CaCl2 H2O CO2↑60.碳酸钠与稀盐酸反应: Na2CO3 2HCl === 2NaCl H2O CO2↑61.碳酸镁与稀盐酸反应: MgCO3 2HCl === MgCl2 H2O CO2↑62.盐酸和硝酸银溶液反应:HCl AgNO3=== AgCl↓ HNO363.硫酸和碳酸钠反应:Na2CO3 H2SO4 === Na2SO4 H2O CO2↑64.硫酸和氯化钡溶液反应:H2S O4 BaCl2 ==== BaSO4↓ 2HCl (7)碱盐 -------- 另一种碱另一种盐65.氢氧化钠与硫酸铜:2NaOH CuSO4 ==== Cu(OH)2↓ Na2SO4 66.氢氧化钠与氯化铁:3NaOH FeCl3 ==== Fe(OH)3↓ 3NaCl 67.氢氧化钠与氯化镁:2NaOH MgCl2 ==== Mg(OH)2↓ 2NaCl68. 氢氧化钠与氯化铜:2NaOH CuCl2 ==== Cu(OH)2↓ 2NaCl69. 氢氧化钙与碳酸钠:Ca(OH)2 Na2CO3 === CaCO3↓ 2NaOH (8)盐盐 ----- 两种新盐70.氯化钠溶液新概念英语第二册和硝酸银溶液:NaCl AgNO3==== AgCl↓ NaNO371.硫酸钠和氯化钡:Na2SO4 BaCl2 ==== BaSO4↓ 2NaCl五.其它反应:72.二氧化碳溶解于水:CO2 H2O === H2CO373.生石灰溶于水:CaO H2O === Ca(OH)274.氧化钠溶于水:Na2O H2O ==== 2NaOH75.三氧化硫溶于水:SO3 H2O ==== H2SO476.硫酸铜晶体受热分解:CuSO4·5H2O 加热 CuSO4 5H2O 77.无水硫酸铜作干燥剂:CuSO4 5H2O ==== CuSO4·5H2化学方程式反应现象应用2Mg O2点燃或Δ2MgO 剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟白色信号弹2Hg O2点燃或Δ2HgO 银白液体、生成红色固体拉瓦锡实验2Cu O2点燃或Δ2CuO 红色金属变为黑色固体4Al 3O2点燃或Δ2Al2O3银白金属变为白色固体3Fe 2O2点燃Fe3O4 剧烈燃烧、火星四射、生成黑色固体、放热4Fe 3O2高温2Fe2O3C O2点燃CO2剧烈燃烧、白光、放热、使石灰水变浑浊S O2点燃SO2剧大学英语四级烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.氧气中蓝紫色火焰2H2 O2点燃2H2O 淡蓝火焰、放热、生成使无水CuSO4变蓝的液体(水)高能燃料4P 5O2 点燃2P2O5剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量CH42O2点燃2H2O CO2蓝色火焰、放热、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)甲烷和天然气的燃烧2C2H2 5O2点燃2H2O 4CO2 蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)氧炔焰、焊接切割金属2KClO3MnO2、Δ2KCl 3O2↑生成使带火星的木条复燃的气体实验室制备氧气2KMnO4Δ K2MnO4 MnO2 O2↑紫色变为黑色、生成使带火星木条复燃的气体实验室制备氧论文气2HgOΔ2Hg O2↑红色变为银白、生成使带火星木条复燃的气体拉瓦锡实验2H2O通电2H2↑ O2↑水通电分解为氢气和氧气电解水Cu2(OH)2CO3Δ2CuO H2O CO2↑绿色变黑色、试管壁有液体、使石灰水变浑浊气体铜绿加热NH4HCO3ΔNH3↑ H2O CO2↑白色固体消失、管壁有液体、使石灰水变浑浊气体碳酸氢铵长期暴露空气中会消失Zn H2SO4=ZnSO4 H2↑有大量气泡产生、锌粒逐渐溶解实验室制备氢气Fe H2SO4=FeSO4 H2↑有大量气泡产生、金属颗粒逐渐溶解Mg H2SO4 =MgSO4 H2↑有大量气泡产生、金属颗粒逐渐溶解2Al 3H2SO4=Al2(SO4)3 3H2↑有大量气泡产生、金属颗粒逐渐溶解Fe2O3 3H2Δ 2Fe 3H2O 红色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性Fe3O4 4H2 Δ3Fe 4H2O 黑色逐渐变为银白色英语翻译、试管壁有液体冶炼金属、利用氢气的还原性WO3 3H2Δ W 3H2O 冶炼金属钨、利用氢气的还原性MoO3 3H2ΔMo 3H2O 冶炼金属钼、利用氢气的还原性2Na Cl2Δ或点燃2NaCl 剧烈燃烧、黄色火焰离子化合物的形成、H2 Cl2点燃或光照 2HCl 点燃苍白色火焰、瓶口白雾共价化合物的形成、制备盐酸CuSO4 2NaOH=Cu(OH)2↓ Na2SO4蓝色沉淀生成、上部为澄清溶液质量守恒定律实验2C O2点燃2CO 煤炉中常见反应、空气污染物之一、煤气中毒原因2CO O2点燃2CO2蓝色火焰煤气燃烧C CuO 高温2Cu CO2↑黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体冶炼金属2Fe2O3 3C高温4Fe 3CO2↑冶炼金属Fe3O4 2C高温3Fe 2CO2↑冶炼金属C CO2 高温2COCO2H2O = H2CO3碳酸使石蕊变红证明碳酸的酸性小学三语文教学论文H2CO3 ΔCO2↑ H2O 石蕊红色褪去Ca(OH)2 CO2= CaCO3↓ H2O 澄清石灰水变浑浊应用CO2检验和石灰浆粉刷墙壁CaCO3 H2O CO2 = Ca(HCO3)2 白色沉淀逐渐溶解溶洞的形成,石头的风化Ca(HCO3)2Δ CaCO3↓ H2O CO2↑白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成.钟乳石的形成2NaHCO3ΔNa2CO3 H2O CO2↑产生使澄清石灰水变浑浊的气体小苏打蒸馒头CaCO3 高温 CaO CO2↑工业制备二氧化碳和生石灰CaCO3 2HCl=CaCl2 H2O CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体实验室制备二氧化碳、除水垢初中化学方程式汇总一、氧气的性质:(1)单质与氧气的反应:(化合反应)1. 镁在空气中燃烧:2Mg O2点燃2MgO2. 铁在氧气中燃烧:3Fe 2O2点燃 Fe3O43. 铜在空气中受热:2Cu O2加热 2CuO4. 铝在空气中燃烧:4Al 3O2 点燃2Al2O35. 氢气中空气中燃烧:2H2 O2 点燃 2H2O6. 红磷在空气中燃烧(研究空气组成的实验):4P 5O2点燃2P2O57. 硫粉在空气中燃烧: S O2 点燃SO28. 碳在氧气中充分燃烧:C O2点燃 CO29. 碳在氧气中不充分燃烧:2C O2点燃2CO(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO O2点燃 2CO211. 甲烷在空气中燃烧:CH4 2O2点燃 CO2 2H2O12. 酒精在空气中燃烧:C2H5OH 3O2点燃 2CO2 3H2O(3)氧气的来源:13.玻义耳研究空气的成分实验 2HgO 加热 Hg O2 ↑14.加热高锰酸钾:2KMnO4加热K2MnO4 MnO2 O2↑(实验室制氧气原理1)15.过氧化氢在二氧化锰作催化剂条件下分解反应: H2O2MnO22H2O O2↑(实验室制氧气原理2)二、自然界中的水:16.水在直流电的作用下分解(研究水的组成实验):2H2O 通电2H2↑ O2 ↑17.生石灰溶于水英语六级作文:CaO H2O == Ca(OH)218.二氧化碳可溶于水: H2O CO2==H2CO3三、质量守恒定律:19.镁在空气中燃烧:2Mg O2点燃2MgO20.铁和硫酸铜溶液反应:Fe CuSO4 === FeSO4 Cu21.氢气还原氧化铜:H2 CuO 加热 Cu H2O22. 镁还原氧化铜:Mg CuO 加热 Cu MgO四、碳和碳的氧化物:(1)碳的化学性质23. 碳在氧气中充分燃烧:C O2点燃 CO224.木炭还原氧化铜:C 2CuO 高温2Cu CO2↑25.焦炭还原氧化铁:3C 2Fe2O3高温4Fe 3CO2↑(2)煤炉中发生的三个反应:(几个化合反应)26.煤炉的底层:C O2 点燃 CO227.煤炉的中层:CO2 C 高温 2CO28.煤炉的上部蓝色火焰的产生:2CO O2点燃 2CO2(3)二氧化碳的制法与性质:29.大理石与稀盐酸反应(实验室制二氧化碳):CaCO3 2HCl == CaCl2 H2O CO2↑30.碳酸不稳定而分解:H2CO3 == H2O CO2↑31.二氧化碳可溶于水: H2O CO2== H2CO332.高温煅烧石灰石(工业制二氧化碳):CaCO3高温 CaO CO2↑33.石灰水与中学历史教学园地二氧化碳反应(鉴别二氧化碳):Ca(OH)2 CO2 === CaCO3↓ H2O(4)一氧化碳的性质:34.一氧化碳还原氧化铜:CO CuO 加热 Cu CO235.一氧化碳的可燃性:2CO O2点燃2CO2其它反应:36.碳酸钠与稀盐酸反应(灭火器的原理):Na2CO3 2HCl == 2NaCl H2O CO2↑五、燃料及其利用:37.甲烷在空气中燃烧:CH4 2O2点燃 CO2 2H2O38.酒精在空气中燃烧:C2H5OH 3O2 点燃2CO2 3H2O39.氢气中空气中燃烧:2H2 O2点燃 2H2O六、金属(1)金属与氧气反应:40.镁在空气中燃烧:2Mg O2点燃2MgO41.铁在氧气中燃烧:3Fe 2O2点燃 Fe3O442. 铜在空气中受热:2Cu O2加热2CuO43. 铝在空气中形成氧化膜:4Al 3O2 = 2Al2O3(2)金属单质酸 -------- 盐氢气(置换反应)44. 锌和稀硫酸Zn H2SO4 = ZnSO4 H2↑45. 铁和稀硫酸Fe H2SO4 = FeSO4 H2↑46. 镁和稀硫酸Mg H2SO4 = MgSO4 H2↑47. 铝和稀硫酸2Al 3H2SO4 = Al2(SO4)3 3H2↑48. 锌和稀盐酸Zn 2HCl == ZnCl2 H2↑49. 铁和稀盐酸Fe 2HCl == FeCl2 H2↑50. 镁和稀盐酸Mg 2HCl == MgCl2 H2↑51.铝和稀盐酸2Al 6HCl == 2AlCl3 3H2↑(3)金属单质盐怎样学好高中物理(溶液) ------- 新金属新盐52. 铁和硫酸铜溶液反应:Fe CuSO4 == FeSO4 Cu53. 锌和硫酸铜溶液反应:Zn CuSO4 ==ZnSO4 Cu54. 铜和硝酸汞溶液反应:Cu Hg(NO3)2 == Cu(NO3)2 Hg(3)金属铁的治炼原理:55.3CO 2Fe2O3 高温 4Fe 3CO2↑七、酸、碱、盐1、酸的化学性质(1)酸金属 -------- 盐氢气(见上)(2)酸金属氧化物-------- 盐水56. 氧化铁和稀盐酸反应:Fe2O3 6HCl ==2FeCl3 3H2O57. 氧化铁和稀硫酸反应:Fe2O3 3H2SO4 == Fe2(SO4)3 3H2O58. 氧化铜和稀盐酸反应:CuO 2HCl ==CuCl2 H2O59. 氧化铜和稀硫酸反应:CuO H2SO4 == CuSO4 H2O(3)酸碱 -------- 盐水(中和反应)60.盐酸和烧碱起反应:HCl NaOH == NaCl H2O61. 盐酸和氢氧化钙反应:2HCl Ca(OH)2 == CaCl2 2H2O62. 氢氧化铝药物治疗胃酸过多:3HCl Al(OH)3 == AlCl3 3H2O63. 硫酸和烧碱反应:H2SO4 2NaOH == Na2SO4 2H2O(4)酸盐 -------- 另一种酸另一种盐64.大理石与稀盐酸反应:CaCO32HCl == CaCl2 H2O CO2↑65.碳酸钠与稀盐酸反应: Na2CO3 2HCl == 2NaCl H2O CO2↑66.碳酸氢钠与稀盐酸反应:NaHCO3 HCl== NaCl H2O CO2↑67. 硫酸和氯化钡溶液反应:H2SO4 BaCl2 == BaSO4↓ 2HCl 2、碱的幼儿园小班音乐教案化学性质(1)碱非金属氧化物 -------- 盐水68.苛性钠暴露在空气中变质:2NaOH CO2 == Na2CO3 H2O 69.苛性钠吸收二氧化硫气体:2NaOH SO2 == Na2SO3 H2O 70.苛性钠吸收三氧化硫气体:2NaOH SO3 == Na2SO4 H2O 71.消石灰放在空气中变质:Ca(OH)2 CO2 == CaCO3↓ H2O 72. 消石灰吸收二氧化硫:Ca(OH)2 SO2 == CaSO3↓ H2O(2)碱酸-------- 盐水(中和反应,方程式见上)(3)碱盐 -------- 另一种碱另一种盐73. 氢氧化钙与碳酸钠:Ca(OH)2 Na2CO3 == CaCO3↓ 2NaOH3、盐的化学性质(1)盐(溶液)金属单质------- 另一种金属另一种盐74. 铁和硫酸铜溶液反应:Fe CuSO4 == FeSO4 Cu(2)盐酸-------- 另一种酸另一种盐75.碳酸钠与稀盐酸反应: Na2CO3 2HCl == 2NaCl H2O CO2↑碳酸氢钠与稀盐酸反应:NaHCO3 HCl== NaCl H2O CO2↑(3)盐碱 -------- 另一种碱另一种盐76. 氢氧化钙与碳酸钠:Ca(OH)2 Na2CO3 == CaCO3↓ 2NaOH (4)盐盐 ----- 两种新盐77.氯化钠溶液和硝酸银溶液:NaCl AgNO3== AgCl↓ NaNO3 78.硫酸钠和氯化钡:Na2SO4 BaCl2== BaSO4↓ 2NaCl一、其他反应类型1、二氧化碳通入澄清石灰水中:CO2 Ca(OH)2 == CaCO3↓ H2O2、氢氧化钠在空气中变质:CO2 2NaOH = Na2CO3 H2O3、氢氧化钠溶液吸收二氧化硫:SO2 2NaOH==Na2SO3 H2O4、一氧化碳还原氧化铜:CO CuO Cu CO25、酒精燃烧:C2H5OH 3O2 2CO2 3H2O6、甲烷燃烧:CH4 2O2 CO2 2H2O。
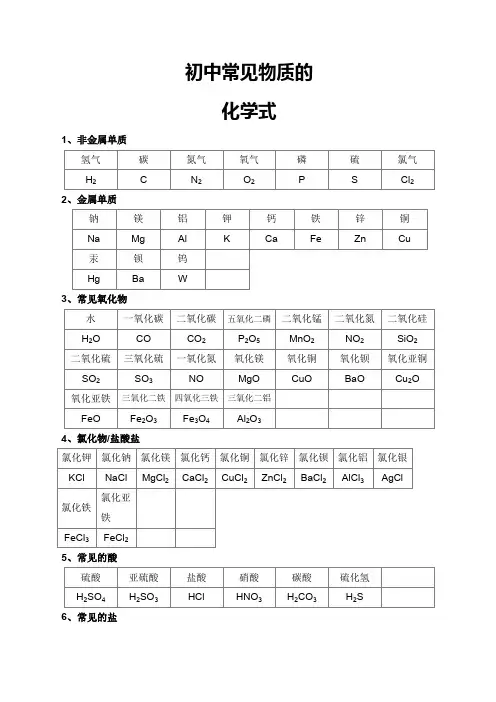

初中必背100个化学式初中常见的化学式一、常见单质氢气 H2 氮气 N2 氯气 Cl2 碘 I2 氧气 O2 臭氧 O3氦气 He 氖气 Ne 氩气 Ar碳 C 硅 Si 硫 S 磷 P钾 K 钙 Ca 钠 Na 镁 Mg 铝 Al锌 Zn 铁 Fe 铜 Cu 汞 Hg 银 Ag二、化合物1、氧化物水 H2O 过氧化氢 H2O2二氧化硫 SO2 三氧化硫 SO3一氧化碳 CO 二氧化碳 CO2一氧化氮 NO 二氧化氮 NO2五氧化二磷 P2O5氧化亚铁 FeO 氧化铁 Fe2O3 四氧化三铁 Fe3O4氧化钙 CaO 氧化镁 MgO 氧化锌 ZnO 二氧化锰 MnO2氧化汞 HgO 氧化铝 Al2O3 氧化铜 CuO2、其他化合物硝酸 HNO3 硫酸 H2SO4 盐酸 HCl碳酸 H2CO3 磷酸 H3PO4硫化氢 H2S 硫化钠 Na2S氢氧化钠 NaOH 氢氧化钾 KOH 氢氧化钙 Ca(OH)2氢氧化镁 Mg(OH)2 氢氧化铝 Al(OH)3 氢氧化锌 Zn(OH)2氢氧化铁 Fe(OH)3 氢氧化亚铁 Fe(OH)2 氢氧化铜 Cu(OH)2氢氧化钡 Ba(OH)2 氨水 NH3•H2O氯化钠 NaCl 氯化铜 CuCl2 氯化铝 AlCl3氯化钾 KCl 氯化亚铁 FeCl2 氯化铁 FeCl3氯化银 AgCl 氯化钙 CaCl2 氯化镁 MgCl2氯化钡 BaCl2 氯化锌 ZnCl2高锰酸钾 KMnO4 锰酸钾 K2MnO4 氯酸钾 KClO3硝酸钾 KNO3 硝酸钠 NaNO3 硝酸铵 NH4NO3硝酸铁 Fe(NO3)3 硝酸亚铁 Fe(NO3)2 硝酸铝 Al(NO3)3硝酸银 AgNO3 硝酸钡 Ba(NO3)2碳酸钠 Na2CO3 碳酸氢钠 NaHCO3 碳酸铵 (NH4)2CO3碳酸钙 CaCO3 碳酸氢钙 Ca(HCO3)2硫酸铁 Fe2(SO4)3 硫酸亚铁 FeSO4硫酸铝 Al2(SO4)3 硫酸铜 CuSO4 硫酸钡 BaSO4碱式碳酸铜 Cu2(OH)2CO3磷酸二氢钙 Ca(H2PO4)2 硫酸铵 (NH4)2SO4硝酸铵 NH4NO3 碳酸氢铵 NH4HCO3氯化铵 NH4Cl 氨水NH3·H2O磷矿粉 Ca3(PO4)2 磷酸二氢氨 NH4H2PO4 磷酸氢二氨(NH4)2HPO4磷酸二氢钾 KH2PO4氨气 NH3碳酸钠晶体Na2CO3·10H2O 硫酸铜晶体CuSO4·5H2O3、常见有机化合物甲烷CH4 乙醇 C2H5OH 葡萄糖 C6H12O6尿素CO(NH2)2 醋酸CH3COOH 淀粉 (C6H10O5)n中考常用30个化学方程式1.镁在空气中燃烧:2Mg + O2点燃2MgO2.铁在氧气中燃烧:3Fe + 2O2点燃Fe3O43.铜在空气中受热:2Cu + O2 2CuO4.铝在空气中燃烧:4Al + 3O2点燃2Al2O35.氢气中空气中燃烧:2H2 + O2点燃2H2O6.红磷在空气中燃烧(研究空气组成的实验):4P + 5O2点燃2P2O57.硫粉在空气中燃烧:S + O2点燃SO28.碳在氧气中充分燃烧:C + O2点燃CO29.碳在氧气中不充分燃烧:2C + O2点燃2CO10.一氧化碳在氧气中燃烧:2CO + O2点燃2CO211.甲烷在空气中燃烧:CH4 + 2O2点燃CO2 + 2H2O12.酒精在空气中燃烧:C2H5OH + 3O2点燃2CO2 + 3H2O13.碳在氧气中充分燃烧:C + O2点燃CO214.玻义耳研究空气的成分实验2HgO Hg+ O2↑15.加热高锰酸钾:2KMnO4 K2MnO4 + MnO2 + O2↑(实验室制氧气原理1)16.双氧水制氧气:2H2O2 MnO22H2O+ O2↑(实验室制氧气原理2)17.加热氯酸钾(二氧化锰):2KCl3 MnO2 2KCl+3O2↑18.水在直流电的作用下分解(研究水的组成实验):2H2O通电2H2↑+O2↑19.生石灰溶于水:CaO + H2O === Ca(OH)220.氧化钾溶于水:K2O+H2O===2KOH21.氧化钠溶于水:Na2O+H2O===2NaOH22.氧化钡溶于水:BaO + H2O === Ba(OH)223.二氧化碳可溶于水:CO2+H2O === H2CO324.二氧化硫可溶于水:SO2+H2O === H2SO325.三氧化硫可溶于水:SO3+H2O === H2SO426.碱式碳酸铜(孔雀石)热分解:Cu2(OH)2CO3Cuo+CO2↑+H2O27.加热碳酸氢铵:NH4HNO3H2O + CO2↑+NH3↑28.镁在空气中燃烧:2Mg + O2点燃2MgO29.铁和硫酸铜溶液反应:Fe + CuSO4 === FeSO4 + Cu30.木炭还原氧化铜(置换反应)C + 2CuO =2Cu + CO2↑化学方程式100个常用的化合反应1、镁在空气中燃烧:2Mg + O2 点燃 2MgO2、铁在氧气中燃烧:3Fe + 2O2 点燃 Fe3O43、铝在空气中燃烧:4Al + 3O2 点燃 2Al2O34、氢气在空气中燃烧:2H2 + O2 点燃 2H2O5、红磷在空气中燃烧:4P + 5O2 点燃 2P2O56、硫粉在空气中燃烧: S + O2 点燃 SO27、碳在氧气中充分燃烧:C + O2 点燃 CO28、碳在氧气中不充分燃烧:2C + O2 点燃 2CO9、二氧化碳通过灼热碳层: C + CO2 高温 2CO10、一氧化碳在氧气中燃烧:2CO + O2 点燃 2CO211、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2 + H2O === H2CO312、生石灰溶于水:CaO + H2O === Ca(OH)213、无水硫酸铜作干燥剂:CuSO4 + 5H2O ==== CuSO4·5H2O14、钠在氯气中燃烧:2Na + Cl2点燃 2NaCl分解反应15、实验室用双氧水制氧气:2H2O2 MnO2 2H2O+ O2↑16、加热高锰酸钾:2KMnO4 加热K2MnO4 + MnO2 + O2↑17、水在直流电的作用下分解:2H2O 通电2H2↑+ O2 ↑18、碳酸不稳定而分解:H2CO3 === H2O + CO2↑19、高温煅烧石灰石(二氧化碳工业制法):CaCO3 高温 CaO + CO2↑置换反应20、铁和硫酸铜溶液反应:Fe + CuSO4 == FeSO4 + Cu21、锌和稀硫酸反应(实验室制氢气):Zn + H2SO4 == ZnSO4 + H2↑22、镁和稀盐酸反应:Mg+ 2HCl === MgCl2 + H2↑23、氢气还原氧化铜:H2 + CuO 加热 Cu + H2O24、木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑25、甲烷在空气中燃烧:CH4 + 2O2 点燃 CO2 + 2H2O26、水蒸气通过灼热碳层:H2O + C 高温 H2 + CO27、焦炭还原氧化铁:3C+ 2Fe2O3 高温4Fe + 3CO2↑其他28、氢氧化钠溶液与硫酸铜溶液反应:2NaOH + CuSO4 == Cu(OH)2↓ + Na2SO429、甲烷在空气中燃烧:CH4 + 2O2 点燃 CO2 + 2H2O30、酒精在空气中燃烧:C2H5OH + 3O2 点燃 2CO2 + 3H2O31、一氧化碳还原氧化铜:CO+ CuO 加热 Cu + CO232、一氧化碳还原氧化铁:3CO+ Fe2O3 高温 2Fe + 3CO233、二氧化碳通过澄清石灰水(检验二氧化碳):Ca(OH)2 + CO2 ==== CaCO3 ↓+ H2O34、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH + CO2 ==== Na2CO3 + H2O35、石灰石(或大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO3 + 2HCl === CaCl2 + H2O + CO2↑36、碳酸钠与浓盐酸反应(泡沫灭火器的原理): Na2CO3 +2HCl === 2NaCl + H2O + CO2↑一. 物质与氧气的反应:(1)单质与氧气的反应:1. 镁在空气中燃烧:2Mg + O2 点燃 2MgO2. 铁在氧气中燃烧:3Fe + 2O2 点燃 Fe3O43. 铜在空气中受热:2Cu + O2 加热 2CuO4. 铝在空气中燃烧:4Al + 3O2 点燃 2Al2O35. 氢气中空气中燃烧:2H2 + O2 点燃 2H2O6. 红磷在空气中燃烧:4P + 5O2 点燃 2P2O57. 硫粉在空气中燃烧: S + O2 点燃 SO28. 碳在氧气中充分燃烧:C + O2 点燃 CO29. 碳在氧气中不充分燃烧:2C + O2 点燃 2CO(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO + O2 点燃 2CO211. 甲烷在空气中燃烧:CH4 + 2O2 点燃 CO2 + 2H2O12. 酒精在空气中燃烧:C2H5OH + 3O2 点燃 2CO2 + 3H2O二.几个分解反应:13. 水在直流电的作用下分解:2H2O 通电2H2↑+ O2 ↑14. 加热碱式碳酸铜:Cu2(OH)2CO3 加热 2CuO + H2O + CO2↑15. 加热氯酸钾(有少量的二氧化锰):2KClO3 ==== 2KCl + 3O2 ↑16. 加热高锰酸钾:2KMnO4 加热K2MnO4 + MnO2 + O2↑17. 碳酸不稳定而分解:H2CO3 === H2O + CO2↑18. 高温煅烧石灰石:CaCO3 高温CaO + CO2↑三.几个氧化还原反应:19. 氢气还原氧化铜:H2 + CuO 加热 Cu + H2O20. 木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑21. 焦炭还原氧化铁:3C+ 2Fe2O3 高温4Fe + 3CO2↑22. 焦炭还原四氧化三铁:2C+ Fe3O4 高温3Fe + 2CO2↑23. 一氧化碳还原氧化铜:CO+ CuO 加热 Cu + CO224. 一氧化碳还原氧化铁:3CO+ Fe2O3 高温 2Fe + 3CO225. 一氧化碳还原四氧化三铁:4CO+ Fe3O4 高温 3Fe + 4CO2四.单质、氧化物、酸、碱、盐的相互关系(1)金属单质 + 酸 -------- 盐 + 氢气 (置换反应)26. 锌和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑27. 铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑28. 镁和稀硫酸Mg + H2SO4 = MgSO4 + H2↑29. 铝和稀硫酸2Al +3H2SO4 = Al2(SO4)3 +3H2↑30. 锌和稀盐酸Zn + 2HCl === ZnCl2 + H2↑31. 铁和稀盐酸Fe + 2HCl === FeCl2 + H2↑32. 镁和稀盐酸Mg+ 2HCl === MgCl2 + H2↑33. 铝和稀盐酸2Al + 6HCl == 2AlCl3 + 3H2↑(2)金属单质 + 盐(溶液) ------- 另一种金属 + 另一种盐34. 铁和硫酸铜溶液反应:Fe + CuSO4 === FeSO4 + Cu35. 锌和硫酸铜溶液反应:Zn + CuSO4 === ZnSO4 + Cu36. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2 === Cu(NO3)2 + Hg(3)碱性氧化物 +酸 -------- 盐 + 水37. 氧化铁和稀盐酸反应:Fe2O3 + 6HCl === 2FeCl3 + 3H2O38. 氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 === Fe2(SO4)3 + 3H2O39. 氧化铜和稀盐酸反应:CuO + 2HCl ==== CuCl2 + H2O40. 氧化铜和稀硫酸反应:CuO + H2SO4 ==== CuSO4 + H2O41. 氧化镁和稀硫酸反应:MgO + H2SO4 ==== MgSO4 + H2O42. 氧化钙和稀盐酸反应:CaO + 2HCl ==== CaCl2 + H2O(4)酸性氧化物 +碱 -------- 盐 + 水43.苛性钠暴露在空气中变质:2NaOH + CO2 ==== Na2CO3 + H2O44.苛性钠吸收二氧化硫气体:2NaOH + SO2 ==== Na2SO3 + H2O45.苛性钠吸收三氧化硫气体:2NaOH + SO3 ==== Na2SO4 + H2O46.消石灰放在空气中变质:Ca(OH)2 + CO2 ==== CaCO3 ↓+ H2O47. 消石灰吸收二氧化硫:Ca(OH)2 + SO2 ==== CaSO3 ↓+ H2O(5)酸 + 碱 -------- 盐 + 水48.盐酸和烧碱起反应:HCl + NaOH ==== NaCl +H2O49. 盐酸和氢氧化钾反应:HCl + KOH ==== KCl +H2O50.盐酸和氢氧化铜反应:2HCl + Cu(OH)2 ==== CuCl2 +2H2O51. 盐酸和氢氧化钙反应:2HCl + Ca(OH)2 ==== CaCl2 +2H2O52. 盐酸和氢氧化铁反应:3HCl + Fe(OH)3 ==== FeCl3 +3H2O53.氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 ==== AlCl3 + 3H2O54.硫酸和烧碱反应:H2SO4 + 2NaOH ==== Na2SO4 + 2H2O55.硫酸和氢氧化钾反应:H2SO4 + 2KOH ==== K2SO4 + 2H2O56.硫酸和氢氧化铜反应:H2SO4 + Cu(OH)2 ==== CuSO4 +2H2O57. 硫酸和氢氧化铁反应:3H2SO4 + 2Fe(OH)3====Fe2(SO4)3 + 6H2O58. 硝酸和烧碱反应:HNO3+ NaOH ==== NaNO3 +H2O(6)酸 + 盐 -------- 另一种酸 + 另一种盐59.大理石与稀盐酸反应:CaCO3 + 2HCl === CaCl2 + H2O + CO2↑60.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑61.碳酸镁与稀盐酸反应: MgCO3 + 2HCl === MgCl2 + H2O + CO2↑62.盐酸和硝酸银溶液反应:HCl + AgNO3 === AgCl↓ + HNO363.硫酸和碳酸钠反应:Na2CO3 + H2SO4 === Na2SO4 + H2O + CO2↑64.硫酸和氯化钡溶液反应:H2SO4 + BaCl2 ==== BaSO4 ↓+ 2HCl(7)碱 + 盐 -------- 另一种碱 + 另一种盐65.氢氧化钠与硫酸铜:2NaOH + CuSO4 ==== Cu(OH)2↓ + Na2SO466.氢氧化钠与氯化铁:3NaOH + FeCl3 ==== Fe(OH)3↓ +3NaCl67.氢氧化钠与氯化镁:2NaOH + MgCl2 ==== Mg(OH)2↓ +2NaCl68. 氢氧化钠与氯化铜:2NaOH + CuCl2 ==== Cu(OH)2↓ + 2NaCl关键词: 初中化学式中考常用30个化学方程式初三化学必背化学式化学方程式100个常用的。
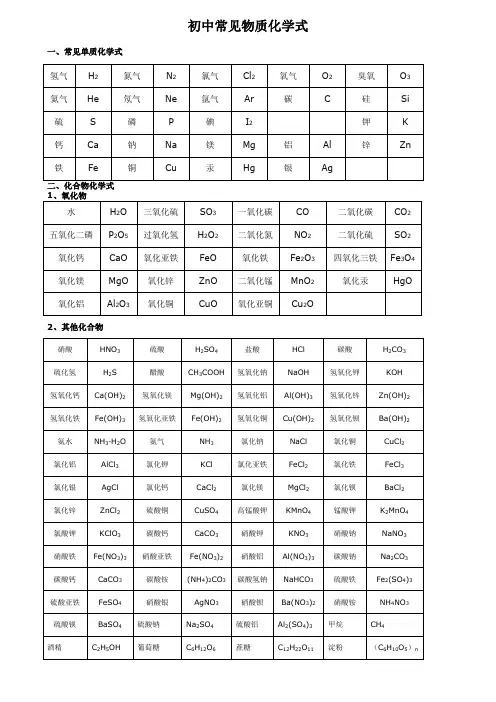
初中要求掌握的常见物质的化学式:金属单质: K Ca Na Mg Al Zn Fe Cu Ag Au Hg稀有气体: He Ne Ar Kr其它非金属单质:C S P Si O2H2N2Cl2阴离子阳离子OH-NO3-Cl-SO42-CO32-O2-H+H2O水HNO3硝酸HCl(盐酸)H2SO4硫酸H2CO3碳酸H2O(水)NH4+NH4OH氢氧化铵(氨水)NH4NO3硝酸铵NH4Cl氯化铵(NH4)2SO4硫酸铵(NH4)2CO3碳酸铵K+KOH氢氧化钾KNO3硝酸钾KCl氯化钾K2SO4硫酸钾K2CO3碳酸钾K2O氧化钾Na+NaOH氢氧化钠NaNO3硝酸钠NaCl氯化钠Na2SO4硫酸钠Na2CO3碳酸钠Na2O氧化钠Ba2+Ba(OH)2氢氧化钡Ba(NO3)2硝酸钡BaCl2氯化钡BaSO4硫酸钡BaCO3碳酸钡BaO氧化钡Ca2+Ca(OH)2氢氧化钙Ca(NO3)2硝酸钙CaCl2氯化钙CaSO4硫酸钙CaCO3碳酸钙CaO氧化钙Mg2+Mg(OH)2氢氧化镁Mg(NO3)2硝酸镁MgCl2氯化镁MgSO4硫酸镁MgCO3碳酸镁MgO氧化镁Zn2+Zn(OH)2氢氧化锌Zn(NO3)2硝酸锌ZnCl2氯化锌ZnSO4硫酸锌ZnCO3碳酸锌ZnO氧化锌Cu2+Cu(OH)2氢氧化铜Cu(NO3)2硝酸铜CuCl2氯化铜CuSO4硫酸铜CuO氧化铜Fe2+Fe(OH)2氢氧化亚铁Fe(NO3)2硝酸亚铁FeCl2氯化亚铁FeSO4硫酸亚铁FeCO3碳酸亚铁FeO氧化亚铁Fe3+Fe(OH)3氢氧化铁Fe(NO3)3硝酸铁FeCl3氯化铁Fe2(SO4)3硫酸铁Fe2O3氧化铁Al3+Al(OH)3氢氧化铝Al(NO3)3硝酸铝AlCl3氯化铝Al2(SO4)3硫酸铝Al2O3氧化铝Ag+AgNO3硝酸银AgCl氯化银Ag2SO4硫酸银Ag2CO3碳酸银Ag2O氧化银其它:CO一氧化碳CO2二氧化碳SO2二氧化硫NO2二氧化氮P2O5五氧化二磷Fe3O4四氧化三铁MnO2二氧化锰KMnO4高锰酸钾K2MnO4锰酸钾KClO3氯酸钾H2O2过氧化氢NH4HCO3碳酸氢铵NaHCO3碳酸氢钠CH4甲烷C2H5OH乙醇(酒精)CH3COOH醋酸NH3氨气化合价口诀一价铵钠钾银氢;二价汞钙钡镁锌。
初中化学常见的化学式一、单质的化学式1、金属单质:由于金属内部结构复杂,化学式一般直接用元素符号表示1、镁带Mg2、铁丝Fe3、铜Cu4、锌Zn5、金Au6、银Ag7、水银/汞Hg8、铂Pt9、钠Na 10、钙Ca11、钡Ba 12、铝 Al 13、钾K 14、铅Pb2、非金属单质①由分子构成的物质,一般用分子式表示化学式15、氧气O216、氢气H217、氮气N2 18、液氧O2 19、氯气Cl2 20、氟气F2 21、碘I2②固态非金属单质一般直接用元素符号表示化学式22、木炭 C 23、金刚石C 24、活性炭 C25、硫磺S 26、硅Si 27、红/白磷P③稀有气体:稀有气体由原子构成,故直接用其元素符号表示化学式28、氦气He 29、氖气Ne 30、氩气Ar二、化合物的化学式1、氧化某、几氧化几某类31、氧化铜CuO 32、氧化镁MgO 33、氧化汞HgO 34、氧化铁Fe2O335、氧化亚铁FeO36 氧化铝Al2O3 37、水H2O 38 氧化钙CaO39、四氧化三铁Fe3O440、二氧化碳CO2 41、一氧化碳CO42、二氧化硫SO2 43、三氧化硫SO3 44、五氧化二磷P2O545、过氧化氢H2O2 46、二氧化氮NO247、二氧化锰MnO22、某化某类48、氯化钠NaCl 49、氯化氢HCl 50、氯化镁MgCl251、氯化铜CuCl252、氯化铁FeCl353、氯化亚铁FeCl254、氯化铝AlCl355、氯化锌ZnCl2 56、氯化钙CaCl23、某酸类57、盐酸HCl58、硫酸H2SO459、硝酸HNO3 60、碳酸H2CO34、硫酸某类61、硫酸钠N a2SO4 62、硫酸钡BaSO463、硫酸钙CaSO464、硫酸镁MgSO465、硫酸铝Al2(SO4)3 66、硫酸锌ZnSO467、硫酸亚铁FeSO468、硫酸铁Fe2(SO4)3 69、硫酸铜CuSO45、硝酸某类70 硝酸亚铁Fe(NO3)2 71、硝酸铁Fe(NO3)3 72、硝酸铜Cu(NO3)273、硝酸银AgNO36、碳酸某类74、碳酸钠Na2CO3 75、碳酸钙CaCO3 76、碳酸钡BaCO37、氢氧化某类77、氨水NH3•H2O 78氢氧化钠NaOH 79、氢氧化钙Ca(OH)280、氢氧化铜Cu(OH)28、其它81、碳酸氢铵NH4HCO382、氨气NH3 83、铜绿(碱式碳酸铜)Cu2(OH)2CO384、胆矾CuSO4•5H2O 85、高锰酸钾KMnO4 86、氯酸钾KClO3 87锰酸钾K2MnO488、甲烷CH4。
初中化学常见物质名称、化学式、俗称
1、食盐:主要成分:氯化钠,化学式nacl
2、二氧化碳固体:化学式co2,俗称干冰
3、氧化钙:化学式cao,俗称生石灰
4、氢氧化钙:化学式ca(oh)2,俗称熟石灰、消石灰、石灰浆
氢氧化钙溶液:俗称石灰水,主要成分ca(oh)2
5、甲烷:化学式ch4,俗称天然气,瓦斯气、、坑气、沼气的主要成分
6、乙醇:化学式c2h5oh ,俗称酒精
7、汞:化学式hg,俗称水银
8、过氧化氢:化学式h2o2,俗称双氧水
9、硫酸铜晶体:化学式cuso4·5h2o,俗称胆矾、蓝矾
10、氢氧化钠:化学式naoh,俗称火碱、烧碱、苛性钠
11、大理石、石灰石、水垢、锅垢的主要成分:caco3
12、氢氯酸(hcl):盐酸(氯化氢气体溶于水所得的溶液),学名:氢氯酸
14、碳酸钠:化学式:na2co3,俗称纯碱、苏打
15、碳酸氢钠:化学式:nahco3,俗称小苏打
16、铁锈主要成分:氧化铁;化学式:fe2o3。
初中常见物质的名称和化学式1、单质(1)、气态非金属单质的化学式:氢气 H 2氮气 N2 氧气 O2臭氧 O3氯气Cl2氟气F2(2)、固态非金属单质一般用元素符号代表化学式:磷 P 硫 S 碳C 硅 Si 硼 B (碘I2 )(3)、金属单质用元素符号表示化学式:钠 Na 镁 Mg 铝Al 钾K 钙Ga 铁Fe 锌Zn 铜Cu 钡Ba 钨W 汞Hg 锂 Li 铍Be(4)、稀有气体是单原子分子,用元素符号表示化学式。
氦 He 氖 Ne 氩Ar 氪Kr 氙Xe 氡Rn2、氧化物(1)、非金属氧化物:水H2O 过氧化氢H2O2 一氧化碳CO 二氧化碳CO2五氧化二磷P2O5 一氧化氮NO 二氧化氮NO2二氧化硅SiO2二氧化硫SO2 三氧化硫SO3(2)、金属氧化物:氧化钠Na2O 氧化镁MgO 氧化铜CuO 氧化亚铜Cu2O 氧化钡BaO 氧化亚铁FeO 氧化铁Fe2O3 三氧化二铁(铁红)Fe2O3四氧化三铁Fe3O4 氧化铝 Al2O3 三氧化二铝 Al2O3三氧化钨WO3 二氧化锰MnO2 氧化钙 CaO3、常见的酸盐酸 HCl 硫酸 H2SO4 亚硫酸 H2SO3 硝酸 HNO3碳酸 H2CO3 磷酸 H3PO4 醋酸 CH3COOH 氢硫酸 H2S4、常见的碱:氢氧化钠NaOH 苛性钠NaOH 火碱NaOH 烧碱NaOH氢氧化钙Ca(OH) 2熟石灰Ca(OH) 2消石灰Ca(OH) 2氢氧化钡Ba(OH) 2氢氧化镁Mg(OH) 2氢氧化铜Cu(OH) 2氢氧化钾 KOH 氢氧化铁Fe(OH) 3氢氧化亚铁Fe(OH) 2氢氧化铝Al(OH) 3氨水NH3 H2O5、常见的盐:(1)、盐酸盐(氯化物):氯化钾 KCl 氯化钠(食盐) NaCl 氯化镁MgCl2 氯化钙CaCl2 氯化铜CuCl 2 氯化锌ZnCl2氯化钡BaCl2氯化铝AlCl3氯化亚铁FeCl2氯化铁FeCl3氯化银AgCl(2)、硫酸盐:硫酸铜CuSO4硫酸钡BaSO4 硫酸钙CaSO4硫酸钾K2 SO4硫酸镁MgSO4 硫酸亚铁FeSO4硫酸铁Fe2 (SO4) 3硫酸铝Al2 (SO4) 3 硫酸钠Na2 SO4(3)、硝酸盐:硝酸钠NaNO3硝酸钾KNO3硝酸银AgNO3 硝酸镁Mg(NO3)2硝酸铜Cu(NO3) 2硝酸钙Ca(NO3) 2硝酸钡 Ba(NO3)2(4)、碳酸盐:碳酸钠Na2CO3 纯碱Na2CO3 碳酸钙CaCO3碳酸镁MgCO3 碳酸钾K2CO3碳酸钡BaCO3(5)、酸式盐(了解):碳酸氢钠NaHCO3 碳酸氢钙Ca(HCO3)2 硫酸氢钠NaHSO4 (6)、碱式盐(了解):碱式碳酸铜 Cu2(OH) 2CO36、常见的化肥:尿素 CO(NH2) 2氯化铵NH4Cl 硝酸铵 NH4NO3硝酸钠 NaNO3硫酸铵(NH4) 2SO4 碳酸氢铵NH4HCO3磷酸钙Ca 3(PO4)2磷酸二氢钙Ca(H2PO4)2硫酸钾K2SO4 氯化钾 KCl氨水NH 3 H2O 磷酸二氢钾 KH2PO4 磷酸二氢铵NH4H2PO4磷酸氢二铵(NH4)2HPO4磷酸二氢钾 NH4H2PO47、常用到的几种化合物:高锰酸钾 KMnO4锰酸钾 K2MnO4氯酸钾 KClO3 氯化氢 HCl硫化氢H2S 氨气NH 3亚硫酸钠Na2 SO3亚硝酸钠NaNO28、常见有机物:甲烷CH4乙炔C2H2甲醇CH3OH 乙醇C2H5OH 乙酸 CH3COOH 9、常见结晶水合物(了解):蓝矾CuSO4•5H2O 明矾KAl(SO4) 212H2O绿矾FeSO4•7H2O 碳酸钠晶体Na2CO3•10H2O9、常用的沉淀:红褐色絮状沉淀--------Fe(OH) 3蓝色絮状沉淀--------- Cu(OH) 2白色沉淀----------- CaCO3 、 BaCO3 、 AgCl 、 BaSO4,(其中BaSO4、AgCl是不溶于 HNO3的白色沉淀,CaCO3 、 BaCO3是溶于HNO3的白色沉淀), Mg(OH) 2 、 Fe(OH) 2 .淡黄色沉淀(水溶液中)----S微溶于水----------- Ca(OH) 2 ,CaSO4。
初中常见物质的化学式氢气碳氮气氧气磷硫氯气(非金属单质)钠镁铝钾钙铁锌铜钡钨汞(金属单质)水一氧化碳二氧化碳五氧化二磷氧化钠二氧化氮二氧化硅二氧化硫三氧化硫一氧化氮氧化镁氧化铜氧化钡氧化亚铜氧化亚铁三氧化二铁(铁红)四氧化三铁三氧化二铝氧化银二氧化锰(常见氧化物)氯化钾氯化钠(食盐) 氯化镁氯化钙氯化铜氯化锌氯化钡氯化铝氯化亚铁氯化铁氯化银(氯化物/盐酸盐)硫酸盐酸硝酸碳酸(常见的酸)硫酸铜硫酸钡硫酸钙硫酸钾硫酸镁硫酸亚铁硫酸铁硫酸铝硫酸氢钠硫酸氢钾亚硫酸钠硝酸钠硝酸钾硝酸银硝酸镁硝酸铜硝酸钙亚硝酸钠碳酸钠碳酸钙碳酸镁碳酸钾(常见的盐)氢氧化钠氢氧化钙氢氧化钡氢氧化镁氢氧化铜氢氧化钾氢氧化铝氢氧化铁氢氧化亚铁(常见的碱)沉淀:红褐色絮状沉淀--------Fe(OH)3 浅绿色沉淀------------Fe(OH)2蓝色絮状沉淀----------Cu(OH)2白色沉淀--------------CaCO3,BaCO3,AgCl,BaSO4,(其中AgCl,BaSO4是不溶于HNO3的白色沉淀,CaCO3 BaCO3是溶于HNO3的白色沉淀),Mg(OH)2.淡黄色沉淀(水溶液中)----S 微溶于水------------Ca(OH)2,CaSO4初中化学方程式汇总一、氧气的性质:(1)单质与氧气的反应:(化合反应)1. 镁在空气中燃烧:2. 铁在氧气中燃烧:3. 铜在空气中受热:4. 铝在空气中燃烧:5. 氢气中空气中燃烧:6. 红磷在空气中燃烧(研究空气组成的实验):7. 硫粉在空气中燃烧:8. 碳在氧气中充分燃烧:9. 碳在氧气中不充分燃烧:(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:11. 甲烷在空气中燃烧:(3)氧气的来源:14.加热高锰酸钾:(实验室制氧气原理1)15.过氧化氢在二氧化锰作催化剂条件下分解反应:(实验室制氧气原理2)二、自然界中的水:16.水在直流电的作用下分解(研究水的组成实验):17.生石灰溶于水:18.二氧化碳可溶于水:三、质量守恒定律:19.镁在空气中燃烧:20.铁和硫酸铜溶液反应:21.氢气还原氧化铜:22. 镁还原氧化铜:四、碳和碳的氧化物:(1)碳的化学性质23. 碳在氧气中充分燃烧:24.木炭还原氧化铜:25.焦炭还原氧化铁:(2)煤炉中发生的三个反应:(几个化合反应)26.煤炉的底层:27.煤炉的中层:28.煤炉的上部蓝色火焰的产生:(3)二氧化碳的制法与性质:29.大理石与稀盐酸反应(实验室制二氧化碳):30.碳酸不稳定而分解:31.二氧化碳可溶于水:32.高温煅烧石灰石(工业制二氧化碳):33.石灰水与二氧化碳反应(鉴别二氧化碳):(4)一氧化碳的性质:34.一氧化碳还原氧化铜:35.一氧化碳的可燃性:其它反应:36.碳酸钠与稀盐酸反应(灭火器的原理):(2)金属单质+ 酸-------- 盐+ 氢气(置换反应)44. 锌和稀硫酸45. 铁和稀硫酸46. 镁和稀硫酸47. 铝和稀硫酸48. 锌和稀盐酸49. 铁和稀盐酸50. 镁和稀盐酸51.铝和稀盐酸(3)金属单质+ 盐(溶液)------- 新金属+ 新盐52. 铁和硫酸铜溶液反应:53. 锌和硫酸铜溶液反应:(3)金属铁的治炼原理:七、酸、碱、盐1、酸的化学性质(1)酸+ 金属-------- 盐+ 氢气(见上)(2)酸+ 金属氧化物-------- 盐+ 水56. 氧化铁和稀盐酸反应:57. 氧化铁和稀硫酸反应:58. 氧化铜和稀盐酸反应:59. 氧化铜和稀硫酸反应:(3)酸+ 碱-------- 盐+ 水(中和反应)60.盐酸和烧碱起反应:61. 盐酸和氢氧化钙反应:62. 氢氧化铝药物治疗胃酸过多:63. 硫酸和烧碱反应:(4)酸+ 盐-------- 另一种酸+ 另一种盐64.大理石与稀盐酸反应:65.碳酸钠与稀盐酸反应:66.碳酸氢钠与稀盐酸反应:67. 硫酸和氯化钡溶液反应:2、碱的化学性质(1)碱+ 非金属氧化物-------- 盐+ 水71.消石灰放在空气中变质:(2)碱+ 酸-------- 盐+ 水(中和反应,方程式见上)(3)碱+ 盐-------- 另一种碱+ 另一种盐73. 氢氧化钙与碳酸钠:3、盐的化学性质(1)盐(溶液)+ 金属单质------- 另一种金属+ 另一种盐74. 铁和硫酸铜溶液反应:(2)盐+ 酸-------- 另一种酸+ 另一种盐75.碳酸钠与稀盐酸反应:碳酸氢钠与稀盐酸反应:(3)盐+ 碱-------- 另一种碱+ 另一种盐76. 氢氧化钙与碳酸钠:(4)盐+ 盐----- 两种新盐77.氯化钠溶液和硝酸银溶液:78.硫酸钠和氯化钡:一、物质的学名、俗名及化学式⑴金刚石、石墨:C ⑵水银、汞:Hg (3)生石灰、氧化钙:CaO (4)干冰(固体二氧化碳):CO2(5)盐酸、氢氯酸:HCl (6)亚硫酸:H2SO3 (7)氢硫酸:H2S (8)熟石灰、消石灰:Ca(OH)2 (9)苛性钠、火碱、烧碱:NaOH (10)纯碱:Na2CO3 (11)碳酸氢钠、酸式碳酸钠:NaHCO3 (也叫小苏打)(12)胆矾、蓝矾、硫酸铜晶体:CuSO4•5H2O (14)甲醇:CH3OH 有毒、失明、死亡(15)酒精、乙醇:C2H5OH (16)醋酸、乙酸(16.6℃冰醋酸)CH3COOH(CH3COO- 醋酸根离子)具有酸的通性(17)氨气:NH3 (碱性气体)(18)氨水、一水合氨:NH3•H2O(为常见的碱,具有碱的通性,是一种不含金属离子的碱)(19)亚硝酸钠:NaNO2 (工业用盐、有毒)二、常见物质的颜色的状态1、白色固体:MgO、P2O5、CaO、NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;铁、镁为银白色(汞为银白色液态)2、黑色固体:石墨、炭粉、铁粉、CuO、MnO2、Fe3O4▲KMnO4为紫黑色3、红色固体:Cu、Fe2O3 、HgO、红磷▲硫:淡黄色▲Cu2(OH)2CO3为绿色4、溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色;凡含Fe3+的溶液呈棕黄色,其余溶液一般不无色。
(高锰酸钾溶液为紫红色)5、沉淀(即不溶于水的盐和碱):①盐:白色↓:CaCO3、BaCO3(溶于酸)AgCl、BaSO4(也不溶于稀HNO3) 等②碱:蓝色↓:Cu(OH)2 红褐色↓:Fe(OH)3白色↓:其余碱。
6、(1)具有刺激性气体的气体:NH3、SO2、HCl(皆为无色)(2)无色无味的气体:O2、H2、N2、CO2、CH4、CO(剧毒)▲注意:具有刺激性气味的液体:盐酸、硝酸、醋酸。
酒精为有特殊气体的液体。
7、有毒的,气体:CO 液体:CH3OH 固体:NaNO2 CuSO4(可作杀菌剂,与熟石灰混合配成天蓝色的粘稠状物质——波尔多液)三、物质的溶解性1、盐的溶解性含有钾、钠、硝酸根、铵根的物质都溶于水含Cl的化合物只有AgCl不溶于水,其他都溶于水;含SO42-的化合物只有BaSO4 不溶于水,其他都溶于水。
含CO32-的物质只有K2CO3、Na2CO3、(NH4)2CO3溶于水,其他都不溶于水2、碱的溶解性溶于水的碱有:氢氧化钡、氢氧化钾、氢氧化钙、氢氧化钠和氨水,其他碱不溶于水。
难溶性碱中Fe(OH)3是红褐色沉淀,Cu(OH)2是蓝色沉淀,其他难溶性碱为白色。
(包括Fe (OH)2)注意:沉淀物中AgCl和BaSO4 不溶于稀硝酸,其他沉淀物能溶于酸。
如:Mg(OH)2 CaCO3 BaCO3 Ag2 CO3 等3、大部分酸及酸性氧化物能溶于水,(酸性氧化物+水→酸)大部分碱性氧化物不溶于水,能溶的有:氧化钡、氧化钾、氧化钙、氧化钠(碱性氧化物+水→碱)四、化学之最1、地壳中含量最多的金属元素是铝。
2、地壳中含量最多的非金属元素是氧。
3、空气中含量最多的物质是氮气。
4、天然存在最硬的物质是金刚石。
5、最简单的有机物是甲烷。
6、金属活动顺序表中活动性最强的金属是钾。
7、相对分子质量最小的氧化物是水。
最简单的有机化合物CH48、相同条件下密度最小的气体是氢气。
9、导电性最强的金属是银。
10、相对原子质量最小的原子是氢。
11、熔点最小的金属是汞。
12、人体中含量最多的元素是氧。
13、组成化合物种类最多的元素是碳。
14、日常生活中应用最广泛的金属是铁。
15、最早利用天然气的是中国;中国最大煤炭基地在:山西省;最早运用湿法炼铜的是中国(西汉发现[刘安《淮南万毕术》“曾青得铁则化为铜”]、宋朝应用);最早发现电子的是英国的汤姆生;最早得出空气是由N2和O2组成的是法国的拉瓦锡。
五、初中化学中的“三”1、构成物质的三种微粒是分子、原子、离子。
2、还原氧化铜常用的三种还原剂氢气、一氧化碳、碳。
3、氢气作为燃料有三大优点:资源丰富、发热量高、燃烧后的产物是水不污染环境。
4、构成原子一般有三种微粒:质子、中子、电子。
5、黑色金属只有三种:铁、锰、铬。
6、构成物质的元素可分为三类即(1)金属元素、(2)非金属元素、(3)稀有气体元素。
7,铁的氧化物有三种,其化学式为(1)FeO、(2)Fe2O3、(3) Fe3O4。
8、溶液的特征有三个(1)均一性;(2)稳定性;(3)混合物。
9、化学方程式有三个意义:(1)表示什么物质参加反应,结果生成什么物质;(2)表示反应物、生成物各物质问的分子或原子的微粒数比;(3)表示各反应物、生成物之间的质量比。
化学方程式有两个原则:以客观事实为依据;遵循质量守恒定律。
10、生铁一般分为三种:白口铁、灰口铁、球墨铸铁。
11、碳素钢可分为三种:高碳钢、中碳钢、低碳钢。
12、常用于炼铁的铁矿石有三种:(1)赤铁矿(主要成分为Fe2O3);(2)磁铁矿(Fe3O4);(3)菱铁矿(FeCO3)。
13、炼钢的主要设备有三种:转炉、电炉、平炉。
14、常与温度有关的三个反应条件是点燃、加热、高温。
15、饱和溶液变不饱和溶液有两种方法:(1)升温、(2)加溶剂;不饱和溶液变饱和溶液有三种方法:降温、加溶质、恒温蒸发溶剂。
(注意:溶解度随温度而变小的物质如:氢氧化钙溶液由饱和溶液变不饱和溶液:降温、加溶剂;不饱和溶液变饱和溶液有三种方法:升温、加溶质、恒温蒸发溶剂)。
16、收集气体一般有三种方法:排水法、向上排空法、向下排空法。
17、水污染的三个主要原因:(1)工业生产中的废渣、废气、废水;(2)生活污水的任意排放;(3)农业生产中施用的农药、化肥随雨水流入河中。
18、通常使用的灭火器有三种:泡沫灭火器;干粉灭火器;液态二氧化碳灭火器。
19、固体物质的溶解度随温度变化的情况可分为三类:(1)大部分固体物质溶解度随温度的升高而增大;(2)少数物质溶解度受温度的影响很小;(3)极少数物质溶解度随温度的升高而减小。