碱金属和卤素的化学方程式
- 格式:doc
- 大小:29.50 KB
- 文档页数:2

高中化学方程式大全和重要离子方程式高中化学方程式总结高考总复习之高中化学方程式总结化学第一册第一章卤素第一节氯气1、2 Na Cl 2 点燃 2 NaCl2、Cu Cl 2 点燃CuCl 23、 2 Fe 3Cl 2 点燃 2 FeCl 34、H2 Cl 2 点燃(光照) 2 HCl5、 2P 3Cl 点燃 2 PCl 326、PCl 3 Cl 2 PCl 57、 Cl 2 H 2 O HCl HClO8、 2 Ca ( OH )2 2 Cl 2 Ca ( ClO )2 CaCl 2 2H 2O9、Ca(ClO)2 CO 2 H 2 O CaCO 3 2 HClO10、2 NaOH Cl 2 NaClO NaCl H 2 O11、4HCl MnO 2 MnCl 2 2H 2O Cl 212、2 KMnO 4 16 HCl (浓)2MnCl 2 2 KCl 5Cl 28 H 2 O13、2 HClO 见光O 22 HCl第二节氯化氢14、NaCl H 2 SO (浓)4 NaHSO 4 HCl15、NaHSO 4 NaCl Na 2 SO 4 HCl17、 HCl AgNO3AgCl HNO318、 NaClAgNO3AgClNaNO 319、 KClAgNO3AgCl KNO320、 2 HCl CaCO 3CaCl2H 2 O CO 2 第三节氧化还原反应21、 CuOH 2 Cu H 2 O22、 C4HNO 3CO 24NO 2 2H 2O23、 4 Zn10 HNO (极稀) 4 Zn () NH 4NO 3 3H 2O 3NO 3 224、 11 P 15 CuSO 424H 2O5 Cu 3 P 6H 3PO 415H 2SO 425、 KClO36HCl (浓)3 Cl 2KCl3H 2O26、 4 Mg10 HNO(极稀)4Mg ( NO )NH 4NO 33H 2O33 227、 K 2Cr 2O76 Fe 3 O4 31 H 2SO4 Cr ( SO ) 9 Fe (SO ) K 2SO4 31 H 2O24 324 328、 2 KNO 33C SK 2 S N 2 3CO 2第四节卤族元素29、 H30、 H2F 2 2HF2 Br 2 2 HBr31、H 2I 22 HI32、 2 NaBr Cl 22 NaCl Br 233、 2KI Cl 2 2 KCl I 234、 2 KI Br 22 KBrI 235、 NaBrAgNO3AgBrNaNO 336、 KI AgNO 3AgIKNO337、 2 AgBr 光照2 Ag Br 2第二章摩尔反应热第一节摩尔38、 C O 2 CO 239、Mg 2 HCl MgCl 2 H 2第二节气体摩尔体积40、 Zn 2HCl ZnCl 2 H 2第三节物质的量浓度41、 2 NaOH H2SO4 Na 2 SO 4 2 H 2 O第四节反应热42、C(固)O (气)2 点燃CO (气)2 393 .5kJ43、 2 H (气)2 O (气)2 2H 2 O(气)483 .6 kJ44、 2 H (气)2 O (气)2 2H 2 O(液)571 .6 kJ45、C(固)H 2O(气)CO (气)H (2气)131 .3kJ第三章硫硫酸第一节硫46、2Cu S Cu 2 S47、Fe S FeS48、S H 2 H 2S49、S高温CS 2 C50、S点燃O 2 SO 251、3S 6 KOH 2K 2S K2SO4 3H2O 第二节硫的氢化物和氧化物52、H2S H 2 S53、2H2S 3O2(足)点燃2SO 22H 2O54、2H2S O 2 (不足)点燃2 S2H 2O点燃2H 2O 3S 55、2H2S SO256、H 2S Br2 S2 HBr57、FeS 2 HCl FeCl 2 H 2 S58、CuSO 4 H 2 S CuS H2SO459、PbAc 2 H 2 S PbS 2 HAc60、 H 2S NaOH NaHS H 2 O61、 NaHS NaOH Na 2 S H 2 O62、 H 2S 2 NaOH Na 2 S 2H 2O (60、61 结合)63、H2S 2 FeCl 3 S 2 FeCl 2 2 HCl64、H2SO(4 稀)FeS FeSO 4 H 2 S65、SO2 H 2 O H2SO366、 2SO 2 O 2 V2O5 2SO 367、SO3 H 2 O H2SO468、Na2SO3H2SO4 Na 2 SO 4 H2O SO269、SO2 2 NaOH Na 2 SO 3 H 2 O70、SO2 CaO CaSO 371、SO2 2Ca ( OH )2 CaSO 3 H 2 O72、SO73、SO74、 SO75、 SO 2CaSO 3 H 2 O Ca ( HSO 3)2 22H 2S 3S 2H 2O2Cl 2 2H 2O 2 HCl H2SO4 2Br 2 2H 2O 2 HBr H2SO476、 5SO 2 2 H 2 O 2 KMnO 4MnSO 4 K 2 SO 4 2 H 2 SO 4 第三节硫酸的工业制法高温78、2SO2 O2 V2O5 2SO 379、H2O SO3 H2SO4第四节硫酸硫酸盐80、C 2H 2SO (4浓)CO81、S 2H 2SO (4浓)3SO 2 2SO 2 2H 2O 22 H 2 O82、P H(浓)H3PO4 SO 2 2H 2O 2SO483、H2S H 2SO (4 浓)S SO2 2H 2O84、Cu 2H 2SO (4 浓)CuSO 4 SO 2 2H 2O85、BaCl86、BaCl87、BaCl 2H2SO4 BaSO 4 2 HCl2Na 2SO 4 BaSO 4 2 NaCl 2 Na 2CO3 BaCO 3 2 NaCl88、BaCO 3 2 HCl BaCl 2 H 2 O CO 289、BaCO 3 2 HNO 3 Ba ( NO 3)2 H 2 O CO 290、Na2CO3 H2SO3 Na 2 S H 2 O CO 291、2H2SO3 O 2 2H 2SO 492、2 Na2SO3O2 2Na 2 SO 493、2CaSO 3 O 2 2 CaSO 494、2 Fe 6 H(浓)()3SO 2 6H 2O 2SO4 Fe 2 SO 4 395、2 NaBr 2H 2SO (4浓)Br 2 SO 2 Na 2 SO 4 H 2 O96、2 NaCl H 2SO (4浓)Na 2 SO 4 2 HCl浓H2SO 412 C 11H 2O97、C11H22O11第四章碱金属第一节钠98、 4 Na O 2 Na O99、 2 NaO 2Na 2 O 2100、 2 Na点燃2 NaClCl 2101、 2 Na S 研磨Na 2 S102、 2 Na 2H 2O 2 NaOH H 2103、 2 Na 2H 2OCuSO 4Cu ( OH )2 Na 2 SO 4 H 2第二节钠的氧化物104、 Na 2OH 2 O2 NaOH105、 2 Na 2 O 22H 2O 4 NaOH O 2106、 Na2OCO 2 Na 2 CO 3107、 2 Na 2 O 22CO 2 2 Na 2 CO 3 O 2108、 Na 2 O2HCl2 NaClH 2 O109、 Na2O24 HCl 4 NaCl 2H 2O O 2 110、 Na 2 CO 3 2 HCl2 NaClCO 2 H 2 O 111、 NaHCO 3 HCl NaCl CO 2 H 2 O 112、 2 NaHCO3Na 2 CO 3CO 2H 2 O113、 NaHCO114、 2 NaHCO3NaOH Na 2 CO 3 H 2 O3 Ca ( OH )(少量)CaCO3Na 2CO3 2 H 2O2115、 NaHCO3Ca ( OH )(足量)CaCO3NaOHH 2O2116、 Na 2 CO 3 117、 Na 2 CO 3 BaClCaCl22BaCOCaCO332 NaCl2 NaCl118、 Ca ( HCO 3)22 HCl CaCl 2 2 CO 22H 2O119、 Ca ( HCO3)22NaOHCaCO 3 Na 2 CO 3 2H 2 O 120、 NaHSO HClNaClSO H O第三节碱金属元素121、4 Li点燃O 2 2Li 2 O122、K点燃KO 2 O 2123、2 M X 2 2 MX ( M 表示氧族元素, X 代表卤族元素)124、2 M H 2 2 MH125、2 M 2H2O 2MOHH 2第五章物质结构元素周期律本章内容、性质特殊,所有化学反应方程式均融在其他章节中。

高中化学必修一二化学方程式汇总一、必修一化学方程式1. 钠及其化合物- 钠与氧气常温反应:4Na + O_{2}=2Na_{2}O- 钠在氧气中燃烧:2Na + O_{2}{点燃}{=!=!=}Na_{2}O_{2}- 钠与水反应:2Na + 2H_{2}O = 2NaOH+ H_{2}↑- 过氧化钠与水反应:2Na_{2}O_{2}+2H_{2}O = 4NaOH + O_{2}↑- 过氧化钠与二氧化碳反应:2Na_{2}O_{2}+2CO_{2}=2Na_{2}CO_{3}+O_{2} - 向碳酸钠溶液中滴加少量盐酸:Na_{2}CO_{3}+HCl = NaHCO_{3}+NaCl - 向碳酸钠溶液中滴加过量盐酸:Na_{2}CO_{3}+2HCl = 2NaCl +H_{2}O+CO_{2}↑- 碳酸氢钠受热分解:2NaHCO_{3}{}{=!=!=}Na_{2}CO_{3}+H_{2}O + CO_{2}↑- 碳酸氢钠与氢氧化钠反应:NaHCO_{3}+NaOH = Na_{2}CO_{3}+H_{2}O2. 铝及其化合物- 铝与氧气反应:4Al + 3O_{2}=2Al_{2}O_{3}- 铝与盐酸反应:2Al+6HCl = 2AlCl_{3}+3H_{2}↑- 铝与氢氧化钠溶液反应:2Al + 2NaOH+2H_{2}O = 2NaAlO_{2}+3H_{2}↑ - 氧化铝与盐酸反应:Al_{2}O_{3}+6HCl = 2AlCl_{3}+3H_{2}O- 氧化铝与氢氧化钠溶液反应:Al_{2}O_{3}+2NaOH = 2NaAlO_{2}+H_{2}O - 氢氧化铝的制备(向氯化铝溶液中滴加氨水):AlCl_{3}+3NH_{3}· H_{2}O = Al(OH)_{3}↓+3NH_{4}Cl- 氢氧化铝与盐酸反应:Al(OH)_{3}+3HCl = AlCl_{3}+3H_{2}O- 氢氧化铝与氢氧化钠溶液反应:Al(OH)_{3}+NaOH = NaAlO_{2}+2H_{2}O3. 铁及其化合物- 铁与氧气反应:3Fe + 2O_{2}{点燃}{=!=!=}Fe_{3}O_{4}- 铁与氯气反应:2Fe+3Cl_{2}{点燃}{=!=!=}2FeCl_{3}- 铁与盐酸反应:Fe + 2HCl = FeCl_{2}+H_{2}↑- 铁与硫酸铜溶液反应:Fe + CuSO_{4}=FeSO_{4}+Cu- 氯化亚铁与氯气反应:2FeCl_{2}+Cl_{2}=2FeCl_{3}- 氯化铁与铁反应:2FeCl_{3}+Fe = 3FeCl_{2}- 氯化铁与铜反应:2FeCl_{3}+Cu = 2FeCl_{2}+CuCl_{2}4. 硅及其化合物- 硅与氧气反应:Si + O_{2}{}{=!=!=}SiO_{2}- 硅与氢氧化钠溶液反应:Si + 2NaOH + H_{2}O=Na_{2}SiO_{3}+2H_{2}↑ - 二氧化硅与氢氧化钠溶液反应:SiO_{2}+2NaOH = Na_{2}SiO_{3}+H_{2}O - 二氧化硅与氢氟酸反应:SiO_{2}+4HF = SiF_{4}↑+2H_{2}O- 硅酸的制备(硅酸钠溶液与盐酸反应):Na_{2}SiO_{3}+2HCl =H_{2}SiO_{3}↓+2NaCl5. 氯及其化合物- 氯气与金属铁反应:2Fe + 3Cl_{2}{点燃}{=!=!=}2FeCl_{3}- 氯气与金属铜反应:Cu+Cl_{2}{点燃}{=!=!=}CuCl_{2}- 氯气与氢气反应:H_{2}+Cl_{2}{点燃}{=!=!=}2HCl- 氯气与水反应:Cl_{2}+H_{2}O = HCl + HClO- 次氯酸光照分解:2HClO{光照}{=!=!=}2HCl+O_{2}↑- 氯气与氢氧化钠溶液反应:Cl_{2}+2NaOH = NaCl + NaClO + H_{2}O- 氯气与氢氧化钙反应制漂白粉:2Cl_{2}+2Ca(OH)_{2}=CaCl_{2}+Ca(ClO)_{2}+2H_{2}O6. 硫及其化合物- 硫与氧气反应:S+O_{2}{点燃}{=!=!=}SO_{2}- 二氧化硫与水反应:SO_{2}+H_{2}O = H_{2}SO_{3}- 二氧化硫与氧气反应:2SO_{2}+O_{2}{催化剂}{underset{}{⇌}}2SO_{3} - 三氧化硫与水反应:SO_{3}+H_{2}O = H_{2}SO_{4}- 铜与浓硫酸反应:Cu + 2H_{2}SO_{4}(浓){}{=!=!=}CuSO_{4}+SO_{2}↑+2H_{2}O- 碳与浓硫酸反应:C + 2H_{2}SO_{4}(浓){}{=!=!=}CO_{2}↑+2SO_{2}↑+2H_{2}O7. 氮及其化合物- 氮气与氧气反应:N_{2}+O_{2}{放电或高温}{=!=!=}2NO- 一氧化氮与氧气反应:2NO+O_{2}=2NO_{2}- 二氧化氮与水反应:3NO_{2}+H_{2}O = 2HNO_{3}+NO- 工业合成氨:N_{2}+3H_{2}{催化剂}{underset{高温高压}{⇌}}2NH_{3}- 氨气与水反应:NH_{3}+H_{2}O = NH_{3}· H_{2}O- 氨气与氯化氢反应:NH_{3}+HCl = NH_{4}Cl- 氯化铵受热分解:NH_{4}Cl{}{=!=!=}NH_{3}↑+HCl↑- 碳酸氢铵受热分解:NH_{4}HCO_{3}{}{=!=!=}NH_{3}↑+H_{2}O↑+CO_{2}↑- 硝酸铵与氢氧化钠反应:NH_{4}NO_{3}+NaOH{}{=!=!=}NH_{3}↑+NaNO_{3}+H_{2}O- 铜与稀硝酸反应:3Cu + 8HNO_{3}(稀)=3Cu(NO_{3})_{2}+2NO↑+4H_{2}O- 铜与浓硝酸反应:Cu + 4HNO_{3}(浓)=Cu(NO_{3})_{2}+2NO_{2}↑+2H_{2}O二、必修二化学方程式1. 元素周期律相关反应(以碱金属和卤素为例)- 锂与氧气反应:4Li + O_{2}=2Li_{2}O- 钾与水反应:2K+2H_{2}O = 2KOH + H_{2}↑- 氯气与溴化钠溶液反应:Cl_{2}+2NaBr = 2NaCl+Br_{2}- 溴与碘化钾溶液反应:Br_{2}+2KI = 2KBr+I_{2}2. 化学反应与能量- 氢气燃烧:2H_{2}+O_{2}{点燃}{=!=!=}2H_{2}O(放热反应)- 碳酸钙受热分解:CaCO_{3}{}{=!=!=}CaO + CO_{2}↑(吸热反应)3. 有机化学基础(必修部分)- 甲烷燃烧:CH_{4}+2O_{2}{点燃}{=!=!=}CO_{2}+2H_{2}O- 甲烷与氯气发生取代反应(以一氯取代为例):CH_{4}+Cl_{2}{光照}{=!=!=}CH_{3}Cl+HCl- 乙烯燃烧:C_{2}H_{4}+3O_{2}{点燃}{=!=!=}2CO_{2}+2H_{2}O- 乙烯与溴水反应:C_{2}H_{4}+Br_{2}to C_{2}H_{4}Br_{2}- 乙烯与水加成反应:C_{2}H_{4}+H_{2}O{催化剂}{to}C_{2}H_{5}OH- 苯燃烧:2C_{6}H_{6}+15O_{2}{点燃}{=!=!=}12CO_{2}+6H_{2}O- 苯与液溴反应:C_{6}H_{6}+Br_{2}{FeBr_{3}}{=!=!=}C_{6}H_{5}Br+HBr - 乙醇燃烧:C_{2}H_{5}OH + 3O_{2}{点燃}{=!=!=}2CO_{2}+3H_{2}O - 乙醇与钠反应:2C_{2}H_{5}OH + 2Nato 2C_{2}H_{5}ONa+H_{2}↑- 乙醇的催化氧化:2C_{2}H_{5}OH + O_{2}{Cu或Ag}{underset{}{to}}2CH_{3}CHO + 2H_{2}O- 乙酸与乙醇的酯化反应:CH_{3}COOH+C_{2}H_{5}OH{浓硫酸}{underset{}{⇌}}CH_{3}COOC_{2}H_{5}+H_{2}O。

卤素化学方程式及性质1、与非金属反应(HX:卤化氢/氢卤酸)F 2 + H 2 ====2HF Cl 2+H 2====2HCl Br 2+H 2 ====2HBr I 2+H 2垐垎?噲垐?加热2HI 反应条件越来越苛刻,且HX 稳定性降低,HI 在加热下易分解4HF+SiO 2===SiF 4↑+2H 2O(HF 保存在塑料瓶的原因,此反应广泛应用于测定矿样或钢样中SiO 2的含量)HF 为弱酸,酸性比较:HF<HCl<HBr<HI (写出6大强酸)3Cl 2+2P===2PCl 3 PCl 3+Cl 2===PCl 52、与金属反应3Cl 2+2Fe===2FeCl 3 (棕色烟) 3Br 2+2Fe===2FeBr 3 I 2+Fe===FeI 2Cl 2+Cu===CuCl 2(棕黄色烟,浓溶液为绿色,稀溶液为蓝色)Br 2+Cu===CuBr 2 I 2+2Cu===2CuI总结:1、F 2、Cl 2可与任何金属化合,Br 2、I 2与大多数金属化合(除Au 、Pt 外)。
2、对于变价金属,如Fe 、Cu,Cl 2、Br 2将金属氧化到最高价,I 2将金属氧化到较低价。
Zn+I 2==ZnI 2(H 2O 为催化剂) 滴水生紫烟,放热反应3、与水反应(X 2+H 2O 垐?噲?HX+HXO 除F 2外)Cl 2+H 2O 垐?噲?HCl+HClO Br 2+H 2O 垐?噲?HBr+HBrO I 2+H 2O 垐?噲?HI+HIO反应程度减弱2F 2 +2H 2O===4HF+O 2(氧化性:F 2>O 2,置换反应)4、与碱反应(以NaOH 为例)X 2+2NaOH===NaX+NaXO+H 2OCl 2+2NaOH===NaCl+NaClO+H 2O 3Cl 2+6NaOH===5NaCl+NaClO 3+3H 2OBr 2+2NaOH===NaBr+NaBrO+H 2O 3Br 2+6NaOH===5NaBr+NaBrO 3+3H 2OI 2+2NaOH===NaI+NaIO+H 2O 3I 2+6NaOH===5NaI+NaIO 3+3H 2O3Na 2CO 3+3Br 2==5NaBr +NaBrO 3+3CO 2↑以上均为歧化反应。

主族元素(碱金属碱土金属硼族碳族氮族氧族卤素)化学方程式大全目录第12章碱金属和碱土金属(锂钠钾铍镁钙钡) (2)锂 (2)钠 (2)钾 (3)铍 (3)镁 (3)钙 (4)钡 (4)第13章硼族元素(硼铝镓铟铊) (4)硼 (4)铝 (5)镓 (6)铟 (6)铊 (6)第14章碳族元素(碳硅锗锡铅) (6)碳 (6)硅 (8)锗 (9)锡 (9)铅 (10)第15章氮族元素(氮磷砷锑铋) (10)氮 (10)磷 (14)砷 (15)锑 (16)铋 (16)第16章氧族元素(氧硫硒碲) (17)氧 (17)硫 (18)硒 (22)碲 (22)第17章卤素(氟氯溴碘) (22)氟 (23)氯 (23)溴 (27)碘 (28)第12章碱金属和碱土金属(锂钠钾铍镁钙钡)锂 1. 锂与氧气:4Li+O2=2Li2O2. 硝酸锂受热分解:4LiNO3 △2Li2O+4NO2↑+O2↑3. 氢氧化锂受热分解:2LiOH △Li2O+H2O4. 碳酸锂受热分解:Li2CO△Li2O+CO2↑5. 锂与氧气加热:4Li+O2 △2Li2O6. 锂与氮气:6Li+N△2Li3N7. 锂与过氧化氢:2Li+2H2O2=Li2O2+2H2O钠 1. 过氧化钠与水:Na2O2+2H2O=2NaOH+H2O22. 过氧化钠与二氧化碳:2Na2O2+2 CO2=2Na2CO3+O23. 钠与过氧化钠:2Na+Na2O真空2Na2O4. 叠氮化钠与硝酸钠:3NaN3+NaNO真空2NaO+5N2↑5. 硝酸钠受热分解:2NaNO△2NaNO2+O2↑6. 钠与水:2Na+2H2O=2NaOH+H2↑7. 钠与液氨:Na+2NH3(l)=Na+(NH3)+e-(NH3)8. 钠与液氨长久放置:2Na+2NH3(l)=2NaNH2+H2↑9. 电解氯化钠:2NaCl(l) 电解2Na(l)+Cl2(g)10. 钠与氯化钾:Na(l)+KCl(l) 850℃NaCl(l)+K(g)11. 钠与氧气:4Na+O2 180~200℃2Na2O12. 过氧化钠与硫酸:Na2O2+H2SO4=H2O2+Na2SO413. 过氧化钠与三氧化二铁:Fe2O3+3Na2O熔融2Na2FeO4+Na2O14. 过氧化钠与三氧化二铬:Cr2O3+3Na2O熔融2Na2CrO4+Na2O15. 5Na2O2+2MnO4-+16H+=5O2↑+2Mn2++10Na++8H2O16. 硝酸钠500℃分解:2NaNO3 500℃2NaNO2+O2↑17. 硝酸钠800℃分解:4NaNO3 800℃2Na2O+2N2↑+5O2↑18. 氯化钠与碳酸氢铵:NaCl+NH4HCO3=NaHCO3+NH4Cl19. 碳酸氢钠受热分解:2NaHCO△Na2CO3+CO2↑+H2O20. 氯化钠与浓硫酸:NaCl+H2SO4(浓)=NaHSO4+HCl↑21. 亚硫酸钠与硫酸:Na2SO3+H2SO4=Na2SO4+H2O+SO2↑钾 1. 超氧化钾与水:4KO3+2H2O=4KOH+5O2↑2. 过氧化钾与二氧化碳:4KO2+2CO2=2K2CO3+3O23. 氢氧化钾与臭氧:6KOH+4O3=4KO3+2KOH·H2O+O24. 钾与硝酸钾:10K+2KNO真空6K2O+N2↑5. 氯化钾与钠:Na(l)+KCl(l) 850℃NaCl(l)+K(g)6. 过氧化钾高温分解:4KO2 高温2K2O+3O2↑7. 超氧化钾分解:2KO3=2KO2+O2↑8. 过氧化钾与水:2KO2+2H2O=H2O2+O2↑+2KOH9. 氢氧化钾与臭氧:7O3+9KOH=6KO3+3KOH·H2O+3O2铍 1. 铍与氢氧化钠:Be+2NaOH+2H2O=Na2[Be(OH)4]+H2↑2. 氢氧化铍与氢氧化钠:Be(OH)2+2NaOH=Na2[Be(OH)4]镁 1. 镁与四氯化钛:2Mg+TiCl4=Ti+2MgCl22. 碳酸镁受热分解:MgCO△MgO+CO2↑3. 六水氯化镁受热分解:MgCl2·6H2O △Mg(OH)Cl+5H2O+HCl↑4. Mg(OH)Cl △MgO+ HCl↑5. 硝酸镁受热分解:2Mg(NO3)2△2Mg+4NO2+O26. 镁与氧气:2Mg+O2=2MgO7. 氢氧化镁受热分解:Mg(OH)△MgO+H2O8. 镁与二氧化碳:2Mg+CO2=2MgO+C9. 镁与氮气:3Mg+N△Mg3N210. 镁与沸水:Mg+2H2O 沸水Mg(OH)2+H2↑钙 1. 钙与水:Ca+2H2O=Ca(OH)2+H2↑2. 钙与氢气:H2+Ca 423~573K CaH23. 氧化钙与水:CaO(s)+H2O(l)=Ca(OH)2(s)4. 六水氯化钙受热分解:CaCl2·6H2O △CaCl2+6H2O5. 碳酸氢钙与盐酸:Ca(HCO3)2+2HCl=CaCl2+2CO2↑+2H2O6. 碳酸氢钙与氢氧化钠:Ca(HCO3)2+2NaOH=CaCO3↓+Na2CO3+2H2O7. 磷酸钙与浓硫酸:Ca3(PO4)2+3H2SO4(浓) △2H3PO4+3CaSO4↓8. 磷酸钙与浓硫酸:Ca3(PO4)2+2H2SO4(浓) △Ca(H2PO4)2+2CaSO4↓9. 磷酸钙与浓硫酸:Ca3(PO4)2+4H3PO4(浓)=3Ca(H2PO4)210. 碳酸钙与二氧化硅:CaCO3+SiO2 高温CaSiO3+CO2↑11. 碳酸钙与二氧化碳与水:CaCO3+CO2+H2O=Ca(HCO3)212. 碳酸氢钙受热分解:Ca(HCO3)△CaCO3↓+CO2↑+H2O钡 1. 碳酸钡与硝酸:BaCO3+2HNO3=Ba(NO3)2+H2O+CO2↑2. 硫酸钡与碳:BaSO4+4C 高温BaS+4CO↑3. 硫化钡与盐酸:BaS+2HCl=BaCl2+H2S↑4. 二氧化钡与硫酸:BaO2+H2SO4=BaSO4+H2O2第13章硼族元素(硼铝镓铟铊)硼 1. 硼与氮气:2B+N高温2BN2. 硼与浓硫酸:2B+3H2SO4(浓) △2B(OH)3+3SO2↑3. 碘化硼分解:2BI31000K Ta2B+3I24. 乙硼烷与氧气:B2H6+3O自然B2O3+3H2O5. LiBH4+2H2O=LiBO2+4H2↑6. 三氧化二硼与水:3B2O3+3H2O(g)=2B3O3(OH)3(g)7. 氟化硼与水:BF3+3H2O=B(OH)3+3HF氟化硼与氟化氢:BF3+HF=H[BF4]8. 硼与硫:2B+3S高温B2S39. 硼与氯气:2B+3Cl高温2BCl310. 硼与水:2B+6H2O(g)=2B(OH)3+3H211. Na2B4O7+H2SO4+5H2O=4H3BO3+Na2SO412. 硼酸受热分解:2H3BO3△B2O3+3H2O13. 三氧化二硼与镁:B2O3+3Mg高温2B+3MgO14. 硼与浓硝酸:B+3HNO3(浓) △B(OH)3+3NO2↑15. 硼与浓硫酸:2B+3H2SO4(浓) △2B(OH)3+3SO2↑16. 硼与氢氧化钠:2B+2NaOH+3KNO熔融2NaBO2+3KNO2+H2O17. 三氯化硼与氢气:2BCl3+6H无声放电B2H6+6HCl18. 3LiAlH4+4BCl乙醚中2B2H6+3LICl+3AlCl319. 乙硼烷与氯气:B2H6(g)+6Cl2(g)=2BCl3(l)+6HCl(g)20. 乙硼烷与甲醇:B2H6+6CH3OH=2B(OCH3)3+6H221. 4NaH+B(OCH3)3=NaBH4+3NaOCH322. 三氧化二硼与水:B2O3+3H2O=2H3BO3(aq)23. 三氧化二硼与氧化铜:B2O3+CuO熔融Cu(BO2)2(蓝色)24. 三氧化二硼与氧化铁:3B2O3+Fe2O3熔融2Fe(BO2)3(黄色)25. 硼酸与水:B(OH)3+H2O=[B(OH)4]-+H+26. 硼酸与乙醇:B(OH)3+3C2H5OH浓H2SO4(C2H5O)3B+3H2O27. [B4O5(OH)4]2-+5H2O=2H3BO3+2[B(OH)4]-28. 氟化硼与氨气:BF3(g)+NH3=H3N→BF329. 三氯化硼与水:BCl3+3H2O=B(OH)3+3HCl30. 硼与氟气:2B+3F2=2BF331. 硼酸与磷酸:B(OH)3+H3PO4=BPO4+3H2O32. 偏硼酸钠与过氧化氢:NaBO2+H2O2=NaBO3·H2O33. B2O3+8CaF2+8H2SO4(浓)+3H2O=2B(OH)3+16HF+8CaSO4铝 1. 铝与氢氧化钠:2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H22. 偏铝酸钠与氯化铵:NaAlO2+NH4Cl+H2O=Al(OH)3+NH3+NaCl3. Al2O3+2NaOH+3H2O加压煮沸2Na[Al(OH)4]4. 2Na[Al(OH)4]+CO2=2Al(OH)3↓+Na2CO3+H2O5. 氢氧化钠受热分解:2Al(OH)3△Al2O3+3H2O6. 电解三氧化二铝:2Al2O通电熔融冰晶石4Al+3O2↑7. 铝与氯气:2Al+3Cl2△2AlCl38. 六水氯化铝受热分解:AlCl3·6H2O△Al(OH)2Cl+4H2O+2HCl↑9. 铝离子与氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH4+10. Na[Al(OH)4]+NH4Cl=Al(OH)3↓+NaCl+NH3+H2O11. 铝与三氧化二铁:2Al+Fe2O3点燃镁条2Fe+Al2O312. 铝与盐酸:2Al+6HCl(aq)=2AlCl3+3H2↑13. 铝与硫单质:2Al+3S高温Al2S314. 氯化铝与氢化锂:3nLiH+nAlCl乙醚中(AlH3)n+3nLiCl15. 氢氧化铝与氢氧化钠:Al(OH)3+NaOH(aq)=Na[Al(OH)4]镓(Ga)1.镓与稀硫酸:2Ga+3H2SO4(稀)=Ga2(SO4)3+3H2↑2.镓与浓硝酸:Ga+6HNO3(浓)=Ga(NO3)3+3NO2↑+3H2O铟(In)1.铟与稀硫酸:2In+3H2SO4(稀)=In2(SO4)3+3H2↑铊(Tl)1.氢氧化铊与氯化钠:TlOH+NaCl=TlCl+NaOH2.三氯化铊与碘化钾:TlCl3+3KI=TlI+I2+3KCl3.三氯化铊与硫化钠:2TlCl3+3Na2S=Tl2S↓+2S↓+6NaCl4.氯化铊与氯气:TlCl+Cl2=TlCl35.铊与稀硫酸:2Tl+H2SO4(稀)=Tl2SO4+H2↑6.铊与稀硝酸:Tl+2HNO3(稀)=TlNO3+NO2↑+H2O7.硫酸铊与硫酸亚铁:Tl2(SO4)3+4FeSO4=Tl2SO4+2Fe2(SO4)38.硝酸铊与二氧化硫:Tl(NO3)3+SO2+2H2O=TlNO3+H2SO4+2HNO39.铊离子与硫离子:2Tl3++3S2-=Tl2S↓+2S↓第14章碳族元素(碳硅锗锡铅) 碳 1. 甲酸分解:HCOOH浓H2SO4CO↑+H2O2. 碳酸根与铁离子:3CO32-+2Fe3++3H2O=2Fe(OH)3↓+3CO2↑3. 二氧化碳与氨气:CO2+H2O+NH3=NH4HCO34. 2CO2+[Sn(OH)6]2-=Sn(OH)4↓+2HCO3-5. 碳与氧化铅:C+PbO=Pb+CO↑6. 一氧化碳与氧化铅:CO+PbO=Pb+CO2↑7. 草酸分解:H2C2O浓硫酸△CO2↑+CO↑+H2O8. 碳酸钙与盐酸:CaCO3+2HCl=2CaCl2+H2O+CO2↑9. 一氧化碳与氯化亚铜:CO+CuCl+2H2O=Cu(CO)Cl·2H2O10. CO2+K2CO3+H2O=2KHCO311. 碳酸氢钾分解:2KHCO3= CO2↑+K2CO3+H2O12. 碳酸钾与二氧化硫:K2CO3+SO2=K2SO3+CO2↑13. 碳酸钾与硫化氢:K2CO3+H2S=K2S+H2O+CO2↑14. 碳酸钠与盐酸:Na2CO3+2HCl=2NaCl+H2O+CO2↑15. 二氧化碳与氢氧化钙:CO2+Ca(OH)2=CaCO3↓+H2O16. CaCO3+CO2+H2O=Ca(HCO3)217. 碳与氧气:2C+O2=2CO18. 碳与氧气:C+O2=CO219. 一氧化碳与氧气:2CO+O2=2CO220. 碳与氧化锰:C+MnO=Mn+CO21. 一氧化碳与氧化锰:CO+MnO=Mn+CO222. 碳与氧化锌:C+ZnO高温Zn+CO23. 碳与水:C+H2O红热CO+H224. CO+PdCl2+H2O=CO2+2HCl+Pd↓25. CO+CuCl+2H2OH+Cu(CO)Cl·2H2O26. 一氧化碳与铁:5CO+Fe高温[Fe(CO)5]27. 碳酸钙分解:CaCO3煅烧CaO+CO2↑28. 2CO32-+H2O+2Mg2+=Mg2(OH)2CO3↓+CO2↑29. HCO32-+Mg2+=MgCO3↓+H+30. 2C+SiO2+2Cl2△SiCl4+2CO31. 3C+3Cl2+B2O3△2BCl3+3CO32. 碳酸钠与二氧化硅:Na2CO3+SiO共融Na2SiO3+CO2↑33. 甲烷分解:CH41000℃C+2H234. 甲烷分解1500℃:2CH41500℃C2H2+3H2硅 1. 硅酸根与铵根:SiO32-+2NH4+=H2SiO3↓+2NH32. 二氧化硅与碳酸钠:SiO2+NaCO共融Na2SiO3+CO2↑3. 二氧化硅与氟化氢:SiO2+6HF=H2[SiF6]+2H2O4. 甲硅烷分解:SiH4500℃Si+2H2↑5. SiCl4+LiAlH4乙醚SiH4↑+LiCl+AlCl36. SiF4+4H2O=H4SiO4↓+4HFSiF4+2HF=2H++[SiF6]2-7. 甲硅烷自燃:SiH4+2O自燃SiO2+2H2O8. 四氯化硅与锌:SiCl4+2Zn=Si+2ZnCl29. 硅与氟气:Si+2F2=SiF410. 硅与氢氧根:Si+4OH-=SiO44-+2H2↑11. 3Si+18HF(aq)+4HNO3(浓)=3H2[SiF6]+4NO↑+8H2O12. 二氧化硅与碳:SiO2+2C1800℃Si+2CO↑13. 硅与氯气:Si+2Cl2△SiCl414. 硅与盐酸:Si+3HCl△SiHCl3+H215. SiCl4+2Zn△Si+2ZnCl216. 四氯化硅与氢气:SiCl4+2H2>1100℃Si+4HCl17. SiHCl3+H21100℃Si+3HCl18. 二氧化硅与氟化氢:SiO2+4HF(aq)=SiF4↑+2H2O19. SiO2+6HF(aq)=H2SiF6+2H2O20. 二氧化硅与氢氧根:SiO2+2OH-△SiO32-+H2O21. SiO44-+4H+=H4SiO4↓22. 二氧化硅与镁:SiO2+4Mg高温Mg2Si+2MgO23. 硅化镁与盐酸:Mg2Si+4HCl(aq)=SiH4↑+2MgCl224. 甲硅烷分解:SiH4500℃Si+2H225. SiH4+2O自燃SiO2+2H2O26. 甲硅烷水解:SiH4+(n+2)H2O=SiO2·nH2O↓+4H227. SiH4+2KMnO4(aq)=2MnO2↓+K2SiO3+H2O+H228. 四氯化硅与水:SiCl4+4H2O=H4SiO4↓+4HCl↑29. SiO2+2C+2Cl2△SiCl4+2CO30. SiF4+4H2O=H4SiO4↓+4HFSiF4+2HF=2H++[SiF6]2-锗 1. 锗与浓硝酸:Ge+4HNO3(浓)=GeO2·H2O↓+4NO2↑+H2O2. 锗与氢气:Ge+2H2700~800℃GeH43. 二硫化锗与硫化钠:GeS2+Na2S(aq)=Na2GeS34. 锗与氢气:Ge+2H高温GeH4锡 1. 锡与浓硝酸:Sn+4HNO3(浓)=H2SnO3(β)↓+4NO2↑+H2O2. 锡与浓盐酸:Sn+2HCl(浓) △SnCl2+H2↑3. 3SnS2+6NaOH(aq)=Na2SnO3+2Na2SnS3+3H2O4. 3[Sn(OH)3]-+2Bi3++9OH-=3[Sn(OH)6]2-+2Bi↓5. 锡与氢氧根:Sn+2OH-+2H2O=[Sn(OH)4]2-+H2↑6. SnCl2+2HgCl2=SnCl4+Hg2Cl27. [Sn(OH)6]2-+2CO2=Sn(OH)4↓+2HCO3-8. 锡与氯气:Sn+2Cl2(g)=SnCl4(l)9. 四氯化锡与硫化钠:SnCl4+2Na2S=SnS2↓+4NaCl10. SnCl2+Na2S=SnS↓+2NaCl11. SnCl2+4NaOH=Na2[Sn(OH)4]+2NaCl12. 3[Sn(OH)4]2-+2Bi3++6OH-=2Bi↓+3[Sn(OH)6]2-13. Sn(OH)Cl+HCl=SnCl2+H2O14. 2Sn2++O2+4H+=2Sn4++2H2O15. Sn4++Sn=2Sn2+16. Na2SnS3+2HCl=SnS2↓+H2S↑+2NaCl17. 3Sn+8HNO3(极稀)=3Sn(NO3)2+2NO↑+4H2O铅 1. 铅与浓硝酸:Pb+4HNO3(浓)=Pb(NO3)2+2NO2↑+2H2O2. 二氧化铅与盐酸:PbO2+4HCl=PbCl2+Cl2↑+2H2O3. 5PbO2+2Mn2++4H+微热5Pb2++2MnO4-+2H2O4. PbCrO4+4NaOH=Na2[Pb(OH)4]+Na2CrO45. 硫化铅与氧气:2PbS+3O2=2PbO+2SO26. 氧化铅与氢氧化钠:PbO+2NaOH=Na2PbO2+H2O7. Na2PbO2+NaClO+H2O=PbO2+NaCl+2NaOH8. 氧化铅与碳:PbO+C=Pb+CO↑9. 氧化铅与一氧化碳:PbO+CO=Pb+CO2↑10. 铅与浓硫酸:Pb+3H2SO4(浓)=Pb(HSO4)2+SO2↑+2H2O11.. 铅与浓盐酸:Pb+3HCl(浓)=H[PbCl3]+H2↑12. 铅与硝酸:3Pb+8HNO3=3Pb(NO3)2+2NO↑+4H2O13. Pb2++CrO42-=PbCrO4↓14. 2PbCrO4+2H+=2Pb2++Cr2O72-+H2O15. PbCrO4+3OH-=CrO42-+[Pb(OH)3]-16. 铅与稀盐酸:Pb+2HCl(aq)=PbCl2+H2↑17. 铅与氢氧根:Pb+OH-+2H2O=[Pb(OH)3]-+H2↑18. 硫化铅与氧气:2PbS+3O焙烧2PbO+2SO219. 二氯化铅与氯离子:PbCl2+2Cl-=[PbCl4]2-第15章氮族元素(氮磷砷锑铋)氮 1. 铵根与亚硝酸根:NH4++NO-△N2↑+2H2O2. 亚硝酸钠与浓硝酸:NaNO2(g)+2HNO3(浓)=2NO2↑+NaNO3+H2O3. 二氧化氮与氢氧化钠:2NO2+2NaOH=NaNO2+NaNO3+H2O4. 亚硝酸钠受热分解:2NaNO2△Na2O+NO2↑+NO↑5. 氨气与氧化铜:2NH3+3CuO△N2+3Cu+3H2O6. 2NH2OH+2AgBr=N2+2Ag+2HBr+2H2O7. 叠氮化铅受热分解:Pb(N3)2△Pb+3N28. 金与王水:Au+HNO3+4HCl=HAuCl4+NO+2H2O9. 铂与王水:3Pt+4HNO3+18HCl=3H2PtCl6+4NO+8H2O10. 硝酸与磷:3P4+20HNO3+8H2O=12H3PO4+20NO11. H3PO2+4AgNO3+2H2O=4Ag↓+H3PO4+4HNO312. 2AsH3+12AgNO3+3H2O=As2O3+12HNO3+12Ag↓13. 浓硝酸与三氧化二锑:Sb2O3+4HNO3(浓)+H2O=2H3SbO4+4NO2↑14. 二氧化氮与水:3NO2+H2O=2HNO3+NO15. 二氧化氮与氢氧化钠:2NO2+2NaOH=NaNO3+NaNO2+H2O16. 亚硝酸根与高锰酸根:2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O17. 亚硝酸与碘离子:2HNO2+2I-+2H+=I2+2NO↑+2H2O18. 亚硝酸根与碘酸根:2IO3-+5NO2-+2H+=I2+5NO3-+H2O19. 硝酸与一氧化氮:2HNO3+NO=3NO2+H2O20. 一氧化氮与硫酸亚铁:NO+FeSO4=Fe(NO)SO421. 硝酸钠分解:2NaNO3△2NaNO2+O2↑22. 硝酸钾分解:2KNO3=2KNO2+O2↑23. 硝酸锂分解:4LiNO3=2Li2O+4NO2↑+O2↑24. 硝酸铅分解:2Pb(NO3)2=2PbO+4NO2↑+O2↑25. 硝酸铋分解:4Bi(NO3)3=2Bi2O3+12NO2↑+3O2↑26. 硝酸银分解:2AgNO3=2Ag+2NO2↑+O2↑27. 硝酸亚铁分解:4Fe(NO3)2=2Fe2O3+8NO2↑+O2↑28. 氮气与氢气:N2+3H高温高压催化剂2NH329. 氮气与氧气:N2+O放电2NO30. 氮气与锂:N2+6Li△2Li3N31. 氮气与镁:N2+3Mg△Mg3N232. 铬酸铵受热分解:(NH4)2Cr2O7△N2↑+Cr2O3+4H2O33. 氨气与溴:8NH3+3Br2(aq)=N2↑+6NH4Br34. 氯化铵与氢氧化钙:2NH4Cl+Ca(OH)2△CaCl2+2NH3↑+2H2O35. 氮化镁与水:Mg3N2+6H2O=3Mg(OH)2+2NH3↑36. 液氨与钠:2NH3(l)+2Na=2NaNH2+H2↑37. 氨气与硫酸:2NH3+H2SO4=(NH4)2SO438. 氨气与镁:2NH3+3Mg△Mg3N2+3H239. 氨气与光气:4NH3+COCl2=CO(NH2)2+2NH4Cl40. 氨气与亚硫酰氯:4NH3(aq)+SOCl2=SO(NH2)2+2NH4Cl41. 氨水与氯化汞:2NH3(aq)+HgCl2=Hg(NH2)Cl+NH4Cl42. 氨气与氧气:4NH3+3O点燃6H2O+2N243. 4NH3+5O2Pt 燃烧4NO+6H2O44. 亚硝酸铵分解:NH4NO2△N2↑+2H2O45. 硝酸铵受热分解:NH4NO3△N2O↑+2H2O46. 硝酸铵高温分解:2NH4NO3高温2N2↑+O2↑+4H2O47. 碳酸氢铵分解:NH4HCO3△NH3↑+CO2↑+H2O48. 氯化铵分解:NH4Cl△NH3↑+HCl↑49. 硫酸铵分解:(NH4)2SO4△2NH3↑+H2SO450. 磷酸铵分解:(NH4)3PO4△3NH3↑+H3PO451. 氨气与次氯酸跟:2NH3+ClO-=N2H4+Cl-+H2O52. 尿素与次氯酸钠:CO(NH2)2+NaClO+2NaOH=N2H4+NaCl+Na2CO3+H2O53. 联氨分解:N2H催化剂N2↑+2H2↑54. 联氨分解:3N2H催化剂N2↑+4NH3↑55. 联氨与溴化银:4AgBr+N2H4(aq)=4Ag+N2↑+4HBr56. 联氨与二氧化氮:2N2H4(aq)+2NO2=3N2+4H2O57. 联氨与过氧化氢:N2H4(aq)+2H2O2=N2↑+4H2O58. 2NH2OH(aq)+2AgBr=2Ag+N2↑+2HBr+2H2O59. 2NH2OH(aq)+4AgBr=4Ag+N2O↑+4HBr+H2O60. 联氨与亚硝酸:N2H4(aq)+HNO2=HN3+2H2O61. 硝酸钠与氨基钠:NaNO3+3NaNH2175℃NaN3+3NaOH+NH3↑62. 氧化氮与氨基钠:N2O+2NaNH2190℃NaN3+NaOH+NH3↑63. 硝酸铵受热分解:NH4NO3△N2O↑+2H2O64. 稀硝酸与铜:8HNO3+3Cu=3Cu(NO3)2+2NO↑+4H2O65. 一氧化氮与二氧化氮:NO+NO低温N2O366. 三氧化二氮分解:N2O3=NO+NO267. 硝酸与五氧化二磷:6HNO3+P2O5=3N2O5+2H3PO469. 二氧化氮与一氧化氮与水:NO2+NO+H2O冰水2HNO270. 二氧化氮与一氧化氮:NO2+NO+2OH-冰水2NO2-+H2O71. 硝酸钠与铅粉:NaNO3+Pb(粉)高温PbO+NaNO272. 亚硝酸根与氢离子:HNO2+H+=NO++H2O73. 2INO=2NO↑+I274. 亚硝酸分解:2HNO2=N2O3↑+H2O75. 亚硝酸分解:3HNO2=HNO3+2NO↑+H2O76. 硝酸银分解:AgNO2>140℃Ag+NO2↑77. 一氧化氮与氧气:2NO+O2=2NO278. 二氧化氮与水:3NO2+H2O=2HNO3+NO79. 硝酸分解:4HNO3△2H2O+4NO2↑+O2↑80. 4HNO3(浓)+Cu=Cu(NO3)2+2NO2↑+2H2O81. 4HNO3(浓)+Hg=Hg(NO3)2+2NO2↑+2H2O82. 8HNO3(稀)+6Hg=3Hg2(NO3)2+2NO↑+4H2O83. 10HNO3(较稀)+4Zn=4Zn(NO3)2+N2O↑+5H2O84. 10HNO3(极稀)+4Zn=4Zn(NO3)2+NH4NO3+3H2O85. 4HNO3(浓)+3Sn=3SnO2↓+4NO↑+2H2O86. 5HNO3+3Sb+8H2O△3H[Sb(OH)6]+5NO↑87. 浓硝酸与硫:2HNO3(浓)+S=H2SO4+2NO↑88. 浓硝酸与磷:5HNO3(浓)+3P+2H2O△3H3PO4+5NO↑89. 硝酸汞分解:Hg2(NO3)2100℃2HgO+2NO2↑90. 硝酸锰分解:Mn(NO3)2△MnO2+2NO2↑91. 硝酸铵分解:NH4NO3>200℃N2O↑+2H2O92. 2NH4NO3>300℃2N2↑+O2↑+4H2O93. 六水硝酸镁分解:Mg(NO3)2·6H2O△Mg(OH)NO3+HNO3+5H2O94. 二水硝酸铜分解:Cu(NO3)2·2H2O△Cu(OH)NO3+HNO3+H2O95. 碱式硝酸铜分解:Cu(OH)NO3△CuO+HNO396. 氯化铵与氯气:NH4Cl(aq)+3Cl2=NCl3+4HCl98. 氨气与氟气:4NH3+3F2CuNF3+3NH4F99. 三氟化氮与水:2NF3+3H2O(g)火花NO+NO2+6HF磷 1. 磷与溴:2P+3Br2+6H2O=6HBr+2H3PO32. 磷与硝酸:3P4+20HNO3+8H2O=12H3PO4+20NO3. 次磷酸与硝酸银:H3PO2+4AgNO3+2H2O=4Ag↓+H3PO4+4HNO34. 三氯化磷与氧气:2PCl3+O2=2POCl35. 次磷酸与氢氧化钠:H3PO2+NaOH=NaH2PO2+H2O6. 亚磷酸与氢氧化钠:H3PO3+2NaOH=Na2HPO3+2H2O7. 磷与氧气:P4+3O2=P4O68. 磷与水:P4+6H2OHI2H3PO3+2PH39. 磷与氯气:P4+6Cl2=4PCl310. 磷化氢与氯气:PH3+3Cl2=PCl3+3HCl11. 三氧化二磷与氧气:P4O6+2O2=P4O1012. 三氧化二磷与水:P4O6+6H2O(冷)=4H3PO313. 三氯化磷与水:PCl3+3H2O=H3PO3+3HCl↑14. 三氯化磷与氯气:PCl3+Cl2=PCl515. 亚磷酸与过氧化氢:H3PO3+H2O2=H3PO4+H2O16. 五氧化二磷与水:P4O10+6H2O=4H3PO417. 五氯化磷与水:PCl5+4H2O=H3PO4+5HCl18. 磷酸根与银离子:3Ag++PO43-=Ag3PO4↓(黄色)19. 2Ca3(PO4)2+6SiO2+10C1100~1450℃6CaSiO3+P4+10CO↑20. 磷与氢氧化钠:4P+3NaOH+3H2O△3NaH2PO2+PH3↑21. 磷与浓硝酸:3P+5HNO3(浓)+2H2O△3H3PO4+5NO↑22. 磷与硝酸铜:2P+5CuSO4+8H2O=5Cu+2H3PO4+5H2SO423. 11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO424. 磷化钙与水:Ca3P2+6H2O=3Ca(OH)2+2PH3↑25. PH4I+NaOH(aq)=NaI+H2O+PH3↑26. 磷与氯气2P+3Cl点燃2PCl327. 磷化氢与硫酸铜:8CuSO4+PH3+4H2O=H3PO4+4H2SO4+4Cu2SO428. 磷化氢与硫酸亚铜:4Cu2SO4+PH3+4H2O=H3PO4+4H2SO4+8Cu↓29. 磷化氢与硫酸亚铜:3Cu2SO4+2PH3=3H2SO4+2Cu3P↓30. 磷化氢与氧气:PH3+2O250℃H3PO431. 五氧化二磷与水:P4O10+6H2O加热HNO34H3PO432. 磷酸钙与硫酸:Ca3(PO4)2+3H2SO4=3CaSO4+2H3PO433. 2H3PO强热H2O+H4P2O7 (焦磷酸)34. 3H3PO4强热2H2O+H5P3O10 (三磷酸)35.nH3PO强热nH2O+(HPO3)n (偏磷酸)36. nH3PO4=(n-1)H2O+H n+2P n O3n+1 (链状多磷酸)37. nH3PO4=nH2O+(HPO3)n (环状多磷酸)38. 焦磷酸与水:H4P2O7+H2O=2H3PO439. 磷酸二氢钠分解:2NaH2PO4170℃H2O+Na2H2P2O740. nNa2H2P2O7625℃nH2O+Na2n(PO3)2n41. 磷酸氢二钠分解:2Na2HPO4△H2O+Na4P2O742. NaH2PO4+2Na2HPO4△2H2O+Na5P3O1043. 磷与氢氧化钠:P4+3NaOH(热浓)+3H2O=3NaH2PO2+PH3↑44. H2PO2-+2Ni2++6OH-=PO43-+2Ni↓+4H2O45. 亚磷酸分解:4H3PO3△3H3PO4+PH3↑46. 亚磷酸与热水:P4O6+6H2O(热)=PH3↑+3H3PO447. 三氯化磷与乙醇:PCl3+3C2H5OH=P(C2H5O)3+3HCl↑48. 五氯化磷与水:PCl5+H2O=POCl3+2HCl↑49. 次磷酸与氢氧化钠:H3PO2+NaOH=NaH2PO2+H2O砷 1. 砷化氢与硝酸银:2AsH3+12AgNO3+3H2O=As2O3+12HNO3+12Ag↓2. 三硫化二砷与氢氧化钠:As2S3+6NaOH=Na3AsO3+Na3AsS3+3H2O3. 三硫化二砷与硫化钠:As2S3+3Na2S=2Na3AsS34. 2Na3AsS4+6HCl=As2S5↓+3H2S+6NaCl5. 砷化氢受热分解:2AsH3△2As+3H26. 砷化钠与水:Na3As+3H2O=AsH3↑+3NaOH7. 三氧化二砷与锌:As2O3+6Zn+12HCl(aq)=2AsH3↑+6ZnCl2+3H2O8. 砷与次氯酸钠:2As+5NaClO+3H2O=2H3AsO4+5NaCl9. 砷化氢与氧气:2AsH3+3O自燃As2O3+3H2O10. NaH2AsO3+4NaOH(aq)+I2=Na2AsO4+2NaI+3H2O11. H3AsO4+2HI(aq)=H3AsO3+I2+H2O12. 三硫化二砷与硫化钠:As2S3+3Na2S(aq)=2Na3AsS313. 五硫化二砷与硫化钠:As2S5+3Na2S(aq)=2Na3AsS414. 三硫化二砷与氢氧化钠: As2S3+6NaOH(aq)=Na3AsO3+Na3AsS3+3H2O15. As2S3+2Na2S2(aq)=As2S5+2Na2S16. 2Na3AsS3+6HCl(aq)=As2S3↓+3H2S↑+6NaCl17. 砷与浓硝酸:As+5HNO3(浓)=H3AsO4+5NO2↑+H2O锑 1. 五硫化二锑与氢氧化钠:4Sb2S5+24NaOH=3Na3SbO4+5Na3SbS4+12H2O2. 三氧化二锑与浓硝酸:Sb2O3+4HNO3(浓)+H2O=2H3SbO4+4NO2↑3. 三硫化二锑与氧气:2Sb2S3+9O2△2Sb2O3+6SO24. 三硫化二锑与碳:Sb2O3+3C△2Sb(g)+3CO(g)5. 锑离子与氢氧根离子:Sb3++6OH-=SbO33-+3H2O6. 三氯化锑与水:SbCl3+H2O=SbOCl↓+2HCl7. 三硫化二锑与铁:Sb2S3+3Fe高温2Sb+3FeS8. SbO33-+3Zn+9H+=SbH3+3Zn2++3H2O9. 锑化氢分解:2SbH3=2Sb+3H210. 三硫化二锑与硫化钠:Sb2S3+3Na2S(aq)=2Na3SbS311. 五硫化二锑与硫化钠:Sb2S5+3Na2S(aq)=2Na3SbS412. 三硫化二锑与氢氧化钠:Sb2S3+6NaOH(aq)=Na3SbO3+Na3SbS3+3H2O13. 三硫化二锑与盐酸:Sb2S3+12HCl(aq)=2H3SbCl6+3H2S↑14. 2(NH4)3SbS4+6HCl(aq)=Sb2S5↓+3H2S↑+6NH4Cl15. 三硫化二锑与浓硝酸:Sb2O3+4HNO3(浓)+H2O=2H3SbO4+4NO2↑铋 1. 三氯化铋与水:BiCl3+H2O=BiOCl↓+2HCl2. 氢氧化铋与氯气:Bi(OH)3+Cl2+3NaOH(aq)=NaBiO3+2NaCl+3H2O3. 铋酸钠与锰离子:5NaBiO3+2Mn2++14H+=5Bi3++2MnO4-+5Na++7H2O4. 三硫化二铋与氧气:2Bi2S3+9O2△2Bi2O3+6SO25. 三氯化铋与氯气:BiCl3+Cl2+6NaOH(aq)=NaBiO3↓+5NaCl+3H2O6. 铋离子与氢氧根离子:Bi3++3OH-=Bi(OH)3↓7. 铋离子与锡离子:3Sn2++2Bi3++18OH-=2Bi↓+3[Sn(OH)6]2-8. 硝酸铋分解:4Bi(NO3)3=2Bi2O3+12NO2↑+3O2↑9. 硝酸铋与水:Bi(NO3)3+H2O=BiONO3↓+2HNO310. 铋与浓硝酸:Bi+6HNO3(浓)=Bi(NO3)3+3NO2↑+3H2O11. 氢氧化铋与氯气:Bi(OH)3+Cl2+3NaOH(aq)=NaBiO3+2NaCl+3H2O12. 三硫化二铋与盐酸:Bi2S3+6HCl(aq)=2BiCl3+3H2S↑第16章氧族元素(氧硫硒碲)氧 1. 氧化汞受热分解:2HgO△2Hg+O2↑2. 过氧化钡受热分解:2BaO2△2BaO+O2↑3. 硝酸钠受热分解:2NaNO3△2NaNO2+O2↑4. 氯酸钾受热分解:2KClO3MnO2△2KCl+3O2↑5. 氧气与镁:2Mg+O2点燃2MgO6. 氧气与硫:S+O点燃SO27. 氧气与硫化氢:3O2+2H2S点燃2SO2+2H2O8. 氧气与氨气:3O2+4NH点燃2N2+6H2O9. 臭氧分解:2O3=3O210. 臭氧与硫化铅:4O3+PbS=PbSO4+4O211. 臭氧与碘离子:O3+2I-+H2O=I2+O2+2OH-12. 氧气与磷:5O2+4P点燃P4O1013. 氧气与磷:3O2+4P点燃P4O614. 氢氧化铜受热分解:Cu(OH)2△CuO+H2O15. 碳酸钙分解:CaCO高温CaO+CO2↑16. 硝酸铅分解:2Pb(NO3)2△2PbO+4NO2↑+O2↑17. 氧化铜分解:4CuO高温2Cu2O+O2↑18. 五氧化二钒与氢气:V2O5+2H2△V2O3+2H2O19. 过氧化钠与硫酸:Na2O2+H2SO4+10H2O=Na2SO4·10H2O+H2O220. CH3CH(OH)CH3+O2=CH3COCH3+H2O221. 电解硫酸氢根:2HSO-通电H2+S2O82-22. (NH4)2S2O8+2H2SO4=H2S2O8+2NH4HSO423. 过二硫酸与水:H2S2O8+2H2O=H2O2+2H2SO424. 氧气与氢气:H2+O22-乙基蒽醌,钯H2O225. 过氧化氢与碘离子:H2O2+2I-+2H+=I2+2H2O26. HO2-+Mn(OH)2=MnO2+OH-+H2O27. 2[Cr(OH)4]-+3HO2-=2CrO42-+OH-+5H2O28. 过氧化氢与硫化铅:4H2O2+PbS=PbSO4+4H2O29. 过氧化氢与高锰酸根:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O30. 过氧化氢与氧化银:H2O2+Ag2O=2Ag+O2↑+H2O31. 过氧化氢与氯气:H2O2+Cl2=2Cl-+O2+2H+硫 1. 电解硫酸氢铵:2NH4HSO电解(NH4)2S2O8+H2↑2. 三氧化硫与碘化钾:SO3+2KI高温K2SO3+I23. 亚硫酸与硫化氢:H2SO3+2H2S=3S↓+3H2O4. 焦硫酸钾与三氧化二铝:3K2S2O7+Al2O共融Al2(SO4)3+3K2SO45. 2NaHSO3+H2SO3+Zn=Na2S2O4+ZnSO3+2H2O6. 硫化汞与硫化钠:HgS+Na2S=Na2[HgS2]7. 硫酸亚铁受热分解:2FeSO4△Fe2O3+SO3↑+SO2↑8. 焦硫酸钾与三氧化二铁:3K2S2O7+Fe2O共融Fe2(SO4)3+3K2SO49. 硫代硫酸钠与氯化亚铜:2Na2S2O3+CuCl=Na3[Cu(S2O3)2]+NaCl10. 焦硫酸钾分解:2K2S2O8△2K2SO4+2SO3↑+O2↑11. 亚硫酰氯与水:SOCl2+H2O=2HCl+SO2↑12. 三氧化硫与盐酸:SO3+HCl=HSO3Cl13. 硫离子与亚硫酸根离子:2S2-+SO32-+6H+=3S↓+3H2O14. 硫代硫酸钠与碘:2Na2S2O3+I2=Na2S4O6+2NaI15. 硫代硫酸根与氯气:S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+16. Na2S2+2HCl=NaCl+S↓+H2S17. H2S+6H++2[Ag(S2O3)2]3-=Ag2S↓+4S↓+4SO2+4H2O18. 硫化亚铁与稀盐酸:FeS+2HCl(稀)=FeCl2+H2S↑19. 硫代硫酸钠与盐酸:Na2SO3+2HCl=2NaCl+SO2↑+H2O20. 硫酸钙分解:CaSO4△CaO+SO3↑21. 浓硫酸与碘化钠:8NaI+9H2SO4(浓)=4I2+8NaHSO4+H2S+4H2O22. 浓硫酸与锌:Zn+2H2SO4(浓)=ZnSO4+SO2↑+2H2O23. 硫与氧气:S+O2=SO224. 4FeS2+11O2=2Fe2O3+8SO225. 二氧化硫与氧气:2SO2+O2V2O3△2SO326. 硫化钠与碳酸钠:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO227. 硫与氢氧化钙:3S+3Ca(OH)2=2CaS+CaSO3+3H2O28. 硫与硫化钙:(x-1)S+CaS=CaSx (橙色)29. 硫与亚硫酸钙:S+CaSO3=CaS2O330. 二硫化碳与氧气:CS2+3O2=CO2+2SO231. 二氧化硫与碳酸氢钠:SO2+2NaHCO3=Na2SO3+2CO2+H2O32. 三氧化硫与氢氧化钾:SO3+2KOH=K2SO4+H2O33. 电解硫酸氢钾:2KHSO电解K2S2O8+H2↑34. 过二硫酸钾与水:K2S2O8+2H2OH2SO42KHSO4+H2O235. 二氧化硫与碳酸钠:2SO2(过量)+Na2CO3+H2O=2NaHSO3+CO2↑36. 亚硫酸钠与氢氧化钠:NaHSO3+2NaOH=Na2SO4+H2O37. 亚硫酸钠与硫:Na2SO3+S=Na2S2O338. 硫代硫酸根与银离子:S2O32-+2Ag+=Ag2S2O3↓39. 硫代硫酸银与硫代硫酸根:Ag2S2O3+3S2O32-=2[Ag(S2O3)2]3-40. 亚硫酸与硫化氢:H2SO3+2H2S=3S↓+3H2O41. 亚硫酸氢钠与亚硫酸氢钠:2NaHSO3=Na2S2O5+H2O42. 3FeS2+12C+8O煅烧Fe3O4+12CO+6S43. 硫与铁:Fe+S△FeS44. 硫与汞:Hg+S△HgS45. 硫与碳:2S+C△CS246. 硫与浓硝酸:S+2HNO3(浓)=H2SO4+2NO↑47. 硫与浓硫酸:S+2H2SO4(浓) △3SO2↑+2H2O48. 硫与氢氧化钠:3S+6NaOH△2Na2S+Na2SO3+3H2O49. 硫化铁与稀硫酸:FeS+H2SO4(稀)=H2S↑+FeSO450. 硫化钠与稀硫酸:Na2S+H2SO4(稀)=H2S↑+Na2SO451. 硫化氢与碘:H2S(aq)+I2=S+2HI52. 硫化氢与铁离子:H2S(aq)+2Fe3+=2Fe2++S↓+2H+53. 硫化氢与二氧化硫:2H2S(aq)+SO2=3S+2H2O54. 硫化氢与碘:H2S(aq)+4I2+4H2O=H2SO4+8HI55. 硫化氢氧气:2H2S+3O点燃2SO2+2H2O56. 硫化氢与氧气:2H2S+O点燃2S+2H2O57. 硫化钠与水:2Na2S+2H2O=NaOH+NaOH+2NaHS58. 硫化钙与水:2CaS+2H2O=Ca(OH)2+Ca(HS)259. 硫氢化钙与水:Ca(HS)2+2H2O△Ca(OH)2+2H2S60. 三硫化二砷与硫化钠:As2S3+3Na2S(aq)=2Na2AsS361. 硫化汞与硫化钠:HgS+Na2S(aq)=Na2[HgS2]62. SnS+Na2S2(aq)=SnS2+Na2S63. SnS2+Na2S(aq)=Na2SnS364. 硫化钠与硫:Na2S(aq)+(x-1)S=Na2Sx65. As2S3+2Na2S2(aq)=As2S5+2Na2S66. M2S x+2H+=2M++(x-1)S↓+H2S67. 二氧化硫与一氧化碳:SO2+2CO铝矾土773K2CO2+S68. 二氧化硫与氯气:SO2+Cl活性炭SO2Cl269. 硫酸钙与碳:2CaSO4+C高温2CaO+2SO2↑+CO2↑70. 浓硫酸与锌:2H2SO4(浓)+Zn=ZnSO4+SO2↑+2H2O71. 三氧化硫与磷:5SO3+2P高温5SO2+P2O572. 硫与铜:S+2Cu△Cu2S73. 亚硫酸碘与水:H2SO3+I2+H2O=H2SO4+2HI74. 亚硫酸与铁离子与水:H2SO3+2Fe3++H2O=H2SO4+2Fe2++2H+75. 硫代硫酸钠与氧气:2Na2SO3+O2=2Na2SO476. 硫代硫酸钠分解:4Na2SO3(S) △3Na2SO4+Na2S77. 亚硫酸分解:3H2SO3△2H2SO4+S+H2O78. 亚硫酸氢钠分解:2NaHSO3△Na2S2O5+H2O79. 硫酸与硝酸钠:H2SO4+NaNO3(s)=NaHSO4+HNO3↑80. 硫酸与氯化钠:H2SO4+NaCl(s) △NaHSO4+HCl↑81. 浓硫酸与铜:2H2SO4(浓)+Cu=CuSO4+SO2↑+2H2O82. 浓硫酸与碘化钠:9H2SO4(浓)+8NaI=4I2+8NaHSO4+H2S↑+4H2O83. 硫酸镁分解:MgSO4△MgO+SO3↑84. 硫酸银分解:4Ag2SO4△8Ag+2SO3↑+2SO2↑+3O2↑85. 硫酸亚铁分解:2FeSO4△Fe2O3+SO3↑+SO2↑86. 过二硫酸与水反应:H2S2O7+H2O=2H2SO487. 2KHSO4△K2S2O7+H2O88. 硫代硫酸钠与盐酸:Na2S2O3+2HCl(aq)=2NaCl+S↓+SO2↑+H2O89. 硫代硫酸钠与碘:2Na2S2O3(aq)+I2(aq)=Na2S4O6+2NaI90. Na2S2O3+4Cl2+5H2O=Na2SO4+H2SO4+8HCl91. 硫代硫酸银与水:Ag2S2O3+H2O=Ag2S+H2SO492. 硫代硫酸钠与溴化银:2Na2S2O3(aq)+AgBr=Na3[Ag(S2O3)2]+NaBr93. 2Na2S2O3(aq)+CuCl=Na3[Cu(S2O3)2]+NaCl94. 2[Ag(S2O3)2]3-+4H+=Ag2S↓+SO42-+3S↓+3SO2↑+2H2O95. 过二硫酸钾与铜:K2S2O8(aq)+Cu=CuSO4+K2SO496. 5S2O82-+2Mn2++8H2OAg+2MnO4-+10SO42-+16H+97. 过二硫酸钾分解:2K2S2O8△2K2SO4+2SO3↑+O2↑98. 2K2S2O8+2H2O△4KHSO4+O2↑99. 过二硫酸铵与水:2(NH4)2S2O8+2H2O△4NH4HSO4+O2↑100. 亚硫酸与二氧化锰:2H2SO3+MnO2=H2S2O6+Mn(OH)2101. 硫代硫酸钠与过氧化氢:2Na2S2O3+4H2O2=Na2S3O6+Na2SO4+4H2O 102. H2S x+2SO乙醚H2S x+2O6 (x=3~8)103. 2NaHSO3+H2SO3+Zn=Na2S2O4+ZnSO3+2H2O104. 连二亚硫酸钠与氧气:2Na2S2O4+O2+2H2O=4NaHSO3105. 连二亚硫酸钠与氧气:Na2S2O4+O2+H2O=NaHSO3+NaHSO4 106. 连二亚硫酸与水:2H2S2O4+H2O=H2S2O3+2H2SO3107. 硫代硫酸分解:H2S2O3=S↓+H2SO3108. 加热连二亚硫酸钠:2Na2S2O4△Na2S2O3+Na2SO3+SO2↑109. 连二亚硫酸钠:2Na2S2O4+H2O△Na2S2O3+2NaHSO3110. 二氧化硫与五氯化磷:SO2+PCl5=SOCl2+POCl3111. S+Fe△FeS112. SO2Cl2+2H2O=H2SO4+2HCl↑113. 三氧化硫与盐酸:SO3+HCl=HSO3Cl114. HSO3Cl+H2O=H2SO4+HCl↑硒 1. 二氧化硒与水:SeO2+H2O=H2SeO3H2SeO3+2SO2+H2O=Se↓+2H2SO42. 硒酸与盐酸:H2SeO4+2HCl=H2SeO3+Cl2↑+H2O3. 二氧化硒与二氧化硫:SeO2+2SO2+2H2O=Se↓+2SO42-+4H+3. 硒与氢气:Se+H2673KH2Se4. 三硒化二铝与水:Al2Se3+6H2O=2Al(OH)3↓+3H2Se↑5. H2SeO3+Cl2+H2O=H2SeO4+2HCl碲 1. 三碲化二铝与氢离子:Al2Te3+6H+=2Al3++3H2Te↑2. 三氧化碲与浓氢氧化钾:TeO3+2KOH(浓)=K2TeO4+H2O3. 碲酸与盐酸:H6TeO6+2HCl(aq)=H2TeO3+Cl2↑+3H2O第17章卤素(氟氯溴碘)氟 1. 氟气与水:2F2+2H2O=4HF+O22. 氟气与氢气:F2+H2=2HF3. 2KHF电解2KF+F2↑+H2↑4. 五氟化溴分解:BrF5△BrF3+F2↑5. 2KF+10HF+3H2O2+2KMnO4=2K2[MnF6]+8H2O+3O26. 5HF+SbCl5=SbF5+5HCl7. K2[MnF6]+2SbF5423K2K[SbF6]+MnF48. 四氟化锰分解:2MnF4=2MnF3+F2↑9. 氟化钙与浓硫酸:CaF2(s)+H2SO4(浓)△CaSO4+2HF↑10. 氟气与氯气:F2+Cl2220~250℃2ClF11. 氟气与三氟化溴:F2+BrF3200℃BrF512. 三氟化氯分解:2ClF低温ClF+ClF513. 三氟化碘分解:2IF常温IF+IF514. 氟化氯与钨:6ClF+W=WF6+3Cl215. 氟化氯与硒:4ClF+Se=SeF4+2Cl216. 3ClF3+U=UF6+3ClF17. 五氟化溴与水:BrF5+3H2O=HBrO3+5HF18. 氟化铯与七氟化碘:CsF+IF7=CsIF819. 二氟化氧与碘离子:OF2+4I-+2H+=2I2+2F-+H2O20. 二氟化氧与氢氧根离子:OF2+2OH-=O2+2F-+H2O21. 三氟化溴与二氟化氧:BrF3+O2F2=BrF5+O222. 二氟化氧与四氟化硫:O2F2+SF4=SF6+O223. 二氟化氧与硫化氢:4O2F2+H2S=SF6+2HF+4O224. 氟气与氢氧化钠:2F2+2NaOH(aq)=OF2+2NaF+H2O25. 氟气与氧气:O2(g)+F2(g)低声放电O2F2(g)26. 氟气与水:F2+H2O233KHOF+HF27. 2HOF=2HF+O228. HOF+H2O=HF+H2O229. 氟气与溴酸根:BrO3-+F2+2OH-=BrO4-+2F-+H2O30. BrO3-+XeF2+H2O=BrO4-+Xe+2HF31. 氟气与氯气:F2+Cl2250℃2FCl32. 五氟化溴与水:BrF5+3H2O=HBrO3+5HF33. XeF2+BrO3-+H2O=BrO4-+Xe+2HF氯 1. 次氯酸跟与锰离子:ClO-+Mn2++2OH-=MnO2↓+Cl-+H2O2. 氯气与碳酸钠:3Cl2+3Na2CO3△NaClO3+5NaCl+3CO23. 氯气与碘离子:5Cl2+I2+6H2O=2HIO3+10HCl4. 6ClO-+2CrI3+4OH-=2CrO42-+3I2+6Cl-+2H2O5. 氯气与碘酸钾:Cl2+KIO3+2KOH=KIO4+2KCl+H2O6. 次氯酸跟与碘离子:ClO-+2I-+H2O=I2+Cl-+2OH-7. 次氯酸跟与碘:5ClO-+I2+2OH-=2IO3-+5Cl-+H2O8. 次氯酸跟与碘:10ClO-+I2+4H2O=2IO3-+5Cl2+8OH-9. 次氯酸跟与氯离子:ClO-+Cl-+2H+=Cl2+H2O10. 次氯酸跟与铅离子:ClO-+Pb2++2OH-=Cl-+PbO2+H2O11. 氯气与氨气:3Cl2+8NH3=6NH4Cl+N212. 氯气与氢氧化钠:Cl2+2NaOH=NaCl+NaClO+H2O13. 次氯酸分解:3HClO△2HCl+HClO314. 二氧化氯与氢氧根:2ClO2+2OH-=ClO2-+ClO3-+H2O15. 次氯酸与硫:3HClO+S+H2O=H2SO4+3HCl16. 氯气与溴离子:3Cl2+Br-+6OH-=6Cl-+BrO3-+3H2O17. 氯化碘与碘化钾:ICl+KI△KCl+I218. 氯气与溴化钠:Cl2+2NaBr=2NaCl+Br219. 次氯酸跟与水:ClO-+H2O=HClO+OH-20. 次氯酸跟与水:ClO-+Mn2++2OH-=MnO2↓+Cl-+H2O21. 氯酸钾与盐酸:8KClO3+24HCl=9Cl2↑+8KCl+6ClO2+12H2O22. 盐酸与二氧化锰:4HCl(浓)+MnO2△MnCl2+Cl2↑+2H2O23. 氯酸钾分解:4KClO3△3KClO4+KCl24. 高氯酸钾与硫酸:KClO4+H2SO4=KHSO4+HClO425. 氯气与氧化汞:2Cl2+2HgO+H2O=HgO·HgCl2+2HClO26. 氯气与氧化银:2Cl2+Ag2O+H2O=2AgCl+2HClO27. 氯气与碳酸钙:2Cl2+CaCO3+H2O=Ca2++2Cl-+CO2+2HClO28. 氯气与溴离子:Cl2+2Br-=2Cl-+Br229. 次氯酸钙与二氧化碳:Ca(ClO)2+CO2+H2O=CaCO3+2HClO30. 次氯酸分解:2HClO=2HCl+O231. 盐酸与次氯酸:HCl+HClO=H2O+Cl232. 次氯酸钙与二氧化碳:Ca(ClO)2+2CO2+CaCl2=2CaCO3+2Cl233. 次氯酸钾与盐酸:KClO+2HCl=KCl+Cl2+H2O34. 次氯酸与碘离子:ClO-+2I-+H2O=Cl-+I2+2OH-35. 氯酸根与碘离子:ClO3-+6I-+6H+=3I2+Cl-+3H2O36. 次氯酸与碘:2HClO+I2=2HIO+Cl2↑37. 氯气与碘离子:Cl2+2I-=I2+2Cl-38. 氯气与碘:5Cl2+I2+6H2O=10Cl-+2IO3-+12H+39. 次氯酸跟与铅离子:ClO-+Pb2++2OH-=PbO2↓+Cl-+H2O40. ClO-+2I-+H2O=Cl-+I2+2OH-41. 浓高氯酸与碘:2HClO4(浓)+I2+4H2O=2H5IO6+Cl242. 高氯酸与锌:2HClO4(稀)+Zn=Zn(ClO4)2+H2↑43. 氯酸钾分解:4KClO3△3KClO4+KCl44. 氯酸钾分解:2KClO3MnO2△2KCl+3O2↑45. 氯气与水:Cl2+H2O=HCl+HClO46. 氯气与硫:Cl2+2S=S2Cl247. 氯气与硫:Cl2(过量)+S=SCl248. 氯气与磷:3Cl2+2P=2PCl349. 氯气与磷:5Cl2(过量)+2P=2PCl550. 氯化镁分解:MgCl2电解熔融Mg+Cl2↑51. 氯化钠分解:2NaCl电解熔融2Na+Cl2↑52. 氯化氢与氧气:4HCl+O催化剂2H2O+2Cl253. 2NaCl+MnO2+3H2SO4(浓) △2NaHSO4+MnSO4+Cl2↑+2H2O54. 16HCl(浓)+2KMnO4=2KCl+2MnCl2+5Cl2↑+8H2O55. 氯化钠与浓硫酸:NaCl+H2SO4(浓)△NaHSO4+HCl↑56. 氯气与甲烷:Cl2+CH4450℃CH3Cl+HCl57. 盐酸与锌:2HCl+Zn=ZnCl2+H2↑58. 盐酸与氧化铜:2HCl+CuO=CuCl2+H2O59. 盐酸与氢氧化钠:HCl+NaOH=NaCl+H2O60. 盐酸与碳酸钙:2HCl+CaCO3=CaCl2+H2O+CO2↑61. 氯气与铝:3Cl2+2Al高温2AlCl362. 氯气与铬:3Cl2+2Cr高温2CrCl363. 氯气与二氧化钛:2Cl2+TiO2=TiCl4+O264. 氯气与二氧化钛:2Cl2+C+TiO2△TiCl4+CO265. 氯化银与盐酸:AgCl+KI=AgI+KCl66. [CuCl4]2-+4H2O=[Cu(H2O)4]2++4Cl-67. 氯化碘与水:ICl+H2O=HIO+HCl68. CsICl2△CsCl+ICl69. CsIBrCl△CsCl+IBr70. 氧化氯与水:Cl2O+H2O=2HClO71. 氧化氯与氨气:3Cl2O+10NH3=2N2+6NH4Cl+3H2O72. 二氧化氯与氢氧根:2ClO2+2OH-=ClO2-+ClO3-+H2O73. 二氧化氯与过氧化钠:2ClO2+Na2O2=2NaClO2+O274. 二氧化氯与水:6ClO2+3H2OhvHCl+5HClO375. 七氧化二氯分解:Cl2O7△ClO3+ClO476. 七氧化二氯受热分解:Cl2O7△ClO3+ClO477. 氯气与碳酸钠:2Cl2+2Na2CO3+H2O=Cl2O+2NaHCO3+2NaCl78. 氯酸根与草酸根:2ClO3-+C2O42-+4H+=2ClO2↑+2CO2↑+2H2O79. 氯酸钾与二氧化硫:2KClO3+SO2=2ClO2+K2SO480. 氯气与氧化汞:2Cl2+2HgO=HgCl2·HgO+Cl2O81. 氯气与氧化汞:2Cl2+2HgO+H2O=HgO·HgCl2+2HClO82. 氯气与氧化银与水:2Cl2+Ag2O+H2O=2AgCl+2HClO83. 次氯酸与硫:3HClO+S+H2O=H2SO4+3HCl84. 次氯酸与硫:6HClO+S△H2SO4+3Cl2↑+2H2O85. NaClO+Pb(Ac)2+2OH-△PbO2↓+2Ac-+NaCl+H2O86. 次氯酸钠与氢氧化镍:NaClO+Ni(OH)2=NiO(OH)2+NaCl87. 氯气与氢氧化钙:2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O88. 亚氯酸分解:5HClO2=4ClO2↑+HCl+2H2O89. 亚氯酸分解:3HClO2=2HClO3+HCl90. 亚氯酸分解:HClO2=HCl+O2↑91. 氯气与溴离子:3Cl2+Br-+6OH-=6Cl-+BrO3-+3H2O92. 氯气与碘:5Cl2+I2+6H2O=2HIO3+10HCl93. 浓氯酸分解:3HClO3(浓)=HClO4+2ClO2↑+H2O94. 二氧化氯受热分解:2ClO2△Cl2+2O295. 氯酸钾分解:4KClO3673KKCl+3KClO496. 氯酸钾催化分解:2KClO3MnO2△2KCl+3O2↑97. 氯酸锌分解:2Zn(ClO3)2△2ZnO+2Cl2↑+5O298. 氯离子与氯酸根:ClO3-+5Cl-+6H+=3Cl2+3H2O99. 氯酸根与亚硝酸根:ClO3-+3NO2-=Cl-+3NO3-100. 高氯酸钾与浓硫酸:KClO4+H2SO4(浓)=KHSO4+HClO4101. 氯气与碘酸根:Cl2+3OH-+IO3-=2Cl-+H3IO62-102. 高氯酸分解:4HClO4(浓)震动2Cl2↑+7O2↑+2H2O104. 浓高氯酸与碘:2HClO4(浓)+I2+4H2O=2H5IO6+Cl2↑105. 氯气与一氧化碳:Cl2+CO活性炭△COCl2106. 氯气与氨气:3Cl2+8NH3=6NH4Cl+N2107. 盐酸与氧气:4HCl+O催化剂2H2O+2Cl2溴 1. 溴化碘与碘化钾:IBr+KI△KBr+I22. 溴与碳酸钠:3Br2+3Na2CO3=5NaBr+NaBrO3+3CO2↑3. 溴化氢与溴酸:5HBr+HBrO3=3Br2+3H2O4. 溴与氢氧化钾:3Br2+6KOH=5KBr+KBrO3+3H2O5. 溴与磷:3Br2+2P=2PBr36. 溴与氢气:Br2+H2Pt,350℃2HBr7. 溴与硫化氢:Br2+H2S=2HBr+S8. 五氟化溴分解:BrF5△BrF3+F2↑9. 2NaBr+MnO2+3H2SO4=Br2+MnSO4+2NaHSO4+2H2O10. 溴化钠与浓硫酸:2NaBr+3H2SO4(浓)=Br2+2NaHSO4+SO2↑+2H2O11. 溴化钠与浓磷酸:NaBr(s)+H3PO4(浓)△NaH2PO4+HBr↑12. 溴化铯与溴化碘:CsBr+IBr=CsIBr213. 三溴化铯分解:CsBr3△CsBr+Br214. CsICl2△CsCl+ICl15. CsIBrCl△CsCl+IBr16. 溴与硫氰化银:2AgSCN+Br乙醚中2AgBr+(SCN)217. 2Br2+Ba(BrO)2+4OH-=Ba(BrO2)2·2H2O+4Br-18. 浓溴酸分解:4HBrO3(浓)△2Br2+5O2↑+2H2O19. 三氟化溴与氟气:BrF3+F2200℃BrF520. 溴酸根与氟气:BrO3-+F2+2OH-=BrO4-+2F-+H2O21. 三氟化溴与二氟化氧:BrF3+O2F2=BrF5+O222. 五氟化溴与水:BrF5+3H2O=HBrO3+5HF23. BrO3-+XeF2+H2O=BrO4-+Xe+2HF碘 1. 五氧化二碘与碘离子:I2O5+10I-+10H+=6I2+5H2O2. 碘与氯气:I2+5Cl2+6H2O=2HIO3+10HCl3. 碘化氢与氧化铜:4HI+2CuO=2CuI↓+I2+2H2O4. 五氧化二碘与氧化铜:I2O5+5CO△I2+5CO25. 正高碘酸与锰离子:5H5IO6+2Mn2+△2MnO4-+5IO3-+11H++7H2O6. 碘酸根与亚硫酸根:2IO3-+5SO32-+2H+=I2+5SO42-+H2O7. 碘与亚硫酸根:I2+SO32-+H2O=2I-+SO42-+2H+8. 碘酸根与亚硫酸根:IO3-+3SO32-=I-+3SO42-9. 碘酸根与亚硫酸根:2IO3-+5SO32-+I-+2H+=I3-+5SO42-+H2O10. IO3-+5I3-+6H+=8I2+3H2O11. 碘化钾与溴:2KI+Br2=2KBr+I212. 碘与浓高氯酸:I2+2HClO4(浓)+I2+4H2O=2H5IO6+Cl213. 碘离子与过氧化氢:3I-+H2O2+2H+=I3-+2H2O14. 2I3-+H2O2+2H+=3I2+2H2O15. 碘与氢气:I2+H催化剂,△2HI16. 碘酸根与亚硫酸氢根:2IO3-+6HSO3-=2I-+6SO42-+6H+17. 碘离子与硝酸银:I-+AgNO3=AgI↓+NO3-18. 碘化银与铁:2AgI+Fe=2Ag+FeI219. 碘化亚铁与氯气:FeI2+Cl2=FeCl2+I220. 碘离子与二氧化锰:2I-+MnO2+4H+=I2+Mn2++2H2O21. 2NaI+MnO2+3H2SO4=I2+MnSO4+2NaHSO4+2H2O。

无机化学化学方程式包括碱金属、卤族元素、硫和硫的化合物、碳族元素、氮族元素。
一、碱金属:1.新切的钠有银白色光泽,但很快发暗;方程式:4Na+O2=2Na2O;该产物不稳定。
钠在空气中燃烧时,发出黄色的火焰;同时生成淡黄色的固体,方程式:2Na+O2点燃==Na2O2。
锂燃烧方程式:4Li+O2点燃==2Li2O;钾燃烧方程式:K+O2点燃==KO2。
2.钠与氧气在不点火时平稳反应,硫的化学性质不如氧气活泼,将钠粒与硫粉混合时爆炸,方程式:2Na+S=Na2S 3.钠与水剧烈反应后滴有酚酞的水变成红色,方程式:2Na+2H2O=2NaOH+H2↑;钾与水反应更剧烈,甚至爆炸,为了安全,常在小烧杯上盖一块小玻璃片。
4.过氧化钠粉末用脱脂棉包住,①滴几滴水,脱脂棉燃烧;方程式:2Na2O2+2H2O=4NaOH+O2↑;②用玻璃管吹气,脱脂棉也燃烧;有关的方程式:2Na2O2+2CO2=2Na2CO3+O2↑;这两个反应都是放热反应,使脱脂棉达到着火点。
在过氧化钠与水或CO2反应生成O2的两个反应中,为生成1mol O2,需要的Na2O2的物质的量都为2mol,同时需要的H2O或CO2的物质的量都为2mol。
5.纯碱的化学式是Na2CO3,它不带结晶水,又俗名苏打。
碳酸钠晶体化学式是Na2CO3?10H2O,在空气中不稳定,容易失去结晶水,风化,最后的产物是粉末状,叫无水碳酸钠。
钠、氧化钠、过氧化钠、氢氧化钠等在空气中露置的最后产物都是无水碳酸钠。
6.碳酸钠和碳酸氢钠两种固体物质都可以与盐酸反应放出气体,有关离子方程式分别为:CO32-+2H+=H2O+CO2↑;HCO3-+H+=H2O+CO2↑;其中,以碳酸氢钠与盐酸的反应速度更快;如果碳酸钠和碳酸氢钠的质量相同,当它们完全反应时消耗的盐酸以碳酸钠为多。
7.碳酸钠和碳酸氢钠的热稳定性较差的是碳酸氢钠,其加热时发生分解,方程式是:2NaHCO3=Na2CO3+H2O+CO2↑。


有关卤素的化学方程式1. 氯气和金属钠反应Cl 2+2Na=====2NaCl 2. 氯气和铜反应Cu+Cl 2====CuCl 23. 氯气和铁反应2Fe+3Cl 2====2FeCl 34. 氯气和氢气反应H 2+Cl 2==========2HCl5. 氯气和水反应H 2O+Cl 2===HCl+HClO 6. 氯气和氢氧化钠反应2NaOH+Cl 2====NaCl+NaClO+H 2O7. 氯气和氢氧化钙反应2Ca(OH)2+2Cl 2===CaCl 2+Ca(ClO)2+2H 2O 8. 氯气的实验室制法MnO 2+4HCl===MnCl 2+Cl 2↑+2H 2O9. 高锰酸钾与盐酸反应2KMnO 4+16HCl===2MnCl 2+2KCl+8H 2O+5Cl 2↑10. 氯化亚铁和氯水反应2FeCl 2+Cl 2===2FeCl 3 11. 次氯酸分解2HClO===2HCl+O 2↑12. 次氯酸钙在空气中变质Ca(ClO)2+CO 2+H 2O===CaCO 3↓+2HClO13. 次氯酸钙和盐酸反应Ca(ClO)2+2HCl===CaCl 2+2HClO 14.氟气和氢气反应F 2+H 2===2HF 15. 溴和氢气反应Br 2+H 2====2HBr16. 碘和氢气反应I 2+H 2====2HI 17.氟和水反应2F 2+2H 2O==4HF+O 2 18. 溴和水反应Br 2+H 2O==HBr+HBrO19. 溴化钠和氯水反应2NaBr+Cl 2==Br 2+2NaCl20. 碘化钾和氯水反应2KI+Cl 2==2KCl+I 2 △△点燃或光照△△ △光照点燃21. 碘化钾和溴水反应2KI+Br 2==2KBr+I 2 22.溴化钠和硝酸银反应NaBr+AgNO 3==AgBr↓+NaNO 3 23. 碘化钾和硝酸银反应KI+AgNO 3==AgI↓+KNO 324. 氧化铝和盐酸反应Al 2O 3+6HCl==2AlCl 3+3H 2O25. 盐酸和锌反应2HCl+Zn==ZnCl 2+H 2↑26. 盐酸和硝酸银反应HCl+AgNO 3===AgCl↓+HNO 327. 盐酸和氨气反应HCl+NH 3===NH 4Cl28. 实验室用氯酸钾制取氧气2KClO 3=====2KCl+3O 2↑ 29. △ MnO 2。

卤素化学方程式2Na+Cl2点燃2NaCl2Fe+3Cl2点燃2FeCl3Cu+Cl2点燃CuCl2H2+Cl2点燃2HCl2P+3Cl2点燃2PCl3PCl3+Cl2=PCl52P+5Cl2点燃2PCl5Cl2+SO2+2H2O=2HCl+H2SO4Cl2+H2SO3+H2O=2HCl+H2SO4Cl2+H2S=S↓+2HClCl2+Na2S=2NaCl+S↓Cl2+2Fe2+=2Fe3++2Cl-Cl2+2I-=2Cl-+I2Cl2+2Br-=2Cl-+Br22NH3+3Cl2=N2+6HCl3Cl2+8NH3=N2+6NH4ClCl2+H2O HCl+HClO2HClO====2HCl+O2↑Cl2+2NaOH=NaCl+NaClO+H2O工业制漂白粉:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO Ca(ClO)2+2HCl=CaCl2+2HClO实验室制氯气:MnO2+4HCl(浓)△MnCl2+Cl2↑+2H2O2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2OKClO3+6HCl(浓)=KCl+3Cl2↑+3H2O氯碱工业:2NaCl+2H2O电解2NaOH+H2↑+Cl2↑2Fe+3Br2△2FeBr3Fe+I2△2H2+Br2△2HBrH2+I2△2HIX2+SO2+2H2O=2HX+H2SO4(X=Cl\Br\I)X2+H2S=2HX+S↓(X=Cl\Br\I)X2+2Fe2+=2Fe3++2X-(X=Cl\Br)Br2+2I-=2Br-+I22F2+2H2O=4HF+O2X2+H2O HX+HXO(X=Cl\Br\I)X2+2NaOH=NaX+NaXO+H2O(X=Cl\Br\I)4HF+SiO2=SiF4+2H2O2AgX======2Ag+X2(X=Cl\Br\I)碱金属化学方程式2Na+Cl2点燃2NaCl4Na+O2=2Na2O2Na+O2点燃Na2O22Na+S△Na2S2Na+2H2O=2NaOH+H2↑Na与NH4Cl溶液2Na+2NH4Cl=2NaCl+2NH3↑+H2↑Na与CuSO4溶液2Na+2H2O+CuSO4=Na2SO4+Cu(OH)2↓+H2↑Na2O+H2O=2NaOHNa2O+CO2=Na2CO3Na2O+2HCl=2NaCl+H2O2Na2O2+2H2O=4NaOH+O2↑2Na2O2+2CO2=2Na2CO3+O22Na2O2+4HCl=4NaCl+2H2O+O2↑Na2CO3+Ca(OH)2=CaCO3↓+2NaOHNa2CO3与Al2(SO4)3反应离子方程式:2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑NaHCO3与Al2(SO4)3反应离子方程式Al3++3HCO3-=Al(OH)3↓+3CO2↑Na2O2+SO2=Na2SO4Na2O2+H2S=2NaOH+S↓Na2CO3+H2O+CO2=2NaHCO32NaHCO3△Na2CO3+H2O+CO2↑NaHCO3+NaOH=Na2CO3+H2ONa2CO3中加入过量HClNa2CO3+2HCl=2NaCl+H2O+CO2↑向Na2CO3中逐滴加入HC l①Na2CO3+HCl=NaHCO3+NaCl②NaHCO3+HCl=NaCl+H2O+CO2↑工业制取钠方法2NaCl(熔融)电解2Na+Cl2↑过量Ca(OH)2与NaHCO3离子方程式Ca2++OH-+HCO3-=CaCO3↓+H2O光照或加热光照过量NaHCO3与Ca(OH)2离子方程式Ca2++2OH-+2HCO3-=CaCO3↓+2H2O+CO32-侯氏制碱法NaCl+NH3+CO2+H2O=NH4Cl+NaHCO32NaHCO3△2CO3+H2O+CO2↑镁及其化合物2Mg+O2点燃2MgO Mg+Cl2点燃MgCl2 3Mg+N2点燃Mg3N2Mg+2H2O △Mg(OH)2+H2↑Mg+2HCl=MgCl2+H2↑Mg+2NH4Cl=MgCl2+2NH3↑+H2↑2Mg+CO2点燃2MgO+CMgO+2H+=Mg2++H2OMg(OH)2+2H+=Mg2++2H2OMg(OH)2△MgO+H2OMgCO3△+CO2↑从海水中提取镁涉及的方程式①CaCO3高温CaO+CO2↑②CaO+H2O=Ca(OH)2③Mg2++2OH-=Mg(OH)2↓④Mg(OH)2+2HCl=MgCl2+2H2O⑤MgCl2.6H2O △MgCl2+6H2O⑥MgCl2电解Mg+Cl2↑铝及其化合物4Al+3O2点燃2Al2O3 2Al+3Cl2点燃2AlCl32Al+3S △2S32Al+6H+=2Al3++3H2↑2Al+2NaOH+2H2O=2NaAlO2+3H2↑2Al+3Cu2+=2Al3++3Cu2Al+Fe2O3高温Al2O3+2Fe8Al+3Fe3O4高温4Al2O3+9Fe 4Al+3MnO2高温2Al2O3+3Mn工业冶铝2Al2O3电解4Al+3O2↑Al2O3+6H+=2Al3++3H2↑Al2O3+2OH-=2AlO2-+H2O2Al(OH)3△Al2O3+3H2OAl(OH)3+3H+=Al3++3H2OAl(OH)3+OH-=AlO2-+2H2OAl3++3OH-===Al(OH)3↓H++AlO2-+H2O=Al(OH)3↓AlO2-+4H+=Al3++2H2OAl3++4OH-=AlO2-+2H2OAl3++3NH3·H2O=Al(OH)3↓+3NH4+AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-2AlO2-+CO2+3H2O=CO32-+2Al(OH)3↓AlO2-+HCO3-+H2O=CO32-+Al(OH)3↓Al3++3AlO2-+6H2O=4Al(OH)3↓Al3++3HCO3-=3CO2↑+Al(OH)3↓NH4++AlO2-+H2O=NH3↑+Al(OH)3↓KAl(SO4)2与Ba(OH)2反应当沉淀物质的量最大时:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓当SO42-恰好完全沉淀时:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O铁及其化合物3Fe+2O2点燃Fe3O42Fe+3Cl2点燃2FeCl3Fe+I2△FeI2Fe+S△FeS3Fe+4H2O(g)高温Fe3O4+4H2↑Fe+2H+=Fe2++H2↑Fe与HNO3反应当HNO3过量时:Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O当Fe过量时:3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O Fe+Cu2+=Fe2++CuFe+2Fe3+=3Fe2+HCl2Fe2++Cl2=2Fe3++2Cl-2Fe2++H2O2+2H+=2Fe3++2H2O 2Fe3++Cu=2Fe2++Cu2+4Fe(OH)2+O2+2H2O=4Fe(OH)3 Fe(OH)2+2H+=Fe2++2H2OFe2++2OH-=Fe(OH)2↓Fe(OH)3+3H+=Fe3++3H2O2Fe(OH)3△Fe2O3+3H2OFe3++3OH-=Fe(OH)3↓Fe3++3SCN-=Fe(SCN)3冶铁中涉及的方程式①C+O2点燃CO2②C+CO2高温2CO③Fe2O3+3CO高温2Fe+3CO2产生炉渣的反应④CaCO3高温CaO+CO2↑⑤CaO+SiO2高温CaSiO3铜及其化合物2Cu+O2△2CuOCu+Cl2点燃CuCl22Cu+S △2SCu+2Ag+=Cu2++2Ag Cu+2Fe3+=Cu2++2Fe2+Cu+2H2SO4(浓)△CuSO4+SO2↑+2H2OCu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O 3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O CuO+2H+=Cu2++2H2O3CuO+2NH3△3Cu+N2+3H2O 含硅矿物与信息材料工业制玻璃:①Na2CO3+SiO2高温Na2SiO3+CO2↑②CaCO3+SiO2高温CaSiO3+CO2↑Si+2F2=SiF4Si+4HF=SiF4↑+2H2↑Si+2NaOH+H2O=Na2SiO3+2H2↑Si+O2△SiO2工业制取Si的反应①SiO2+2C高温Si+2CO↑(制粗硅)②Si+2Cl2高温SiCl4③SiCl4+2H2高温Si+4HCl(②③提纯)SiO2+2NaOH=Na2SiO3+H2OSiO2+CaO高温CaSiO3SiO2+4HF=SiF4↑+2H2OSiO32-+2H+=H2SiO3↓Na2SiO3+CO2+H2O=Na2CO3+H2SiO3↓含硫化合物的性质和应用S+O2点燃SO2S+H2△H2SFe+S△FeSSO2+H2O H2SO3SO2+CaO=CaSO3SO2+2NaOH=Na2SO3+H2OSO2+Na2CO3=Na2SO3+CO22SO2+O2催化剂加热2SO3SO2+X2+2H2O=H2SO4+2HXSO2+2H2S=3S↓+2H2O形成酸雨涉及的方程式主要:①SO2+H2O H2SO3②2H2SO3+O2=2H2SO4次要:①2SO2+O2催化剂加热2SO3②SO3+H2O=H2SO4工业制硫酸方程式①4FeS2+11O2高温2Fe2O3+8SO2或:S+O2点燃SO2②2SO2+O2催化剂加热2SO3③SO3+H2O=H2SO4体现稀H2SO4酸的通性的反应:与碱、与碱性氧化物、与活泼金属、与某些盐的反应略,自己举例完成。
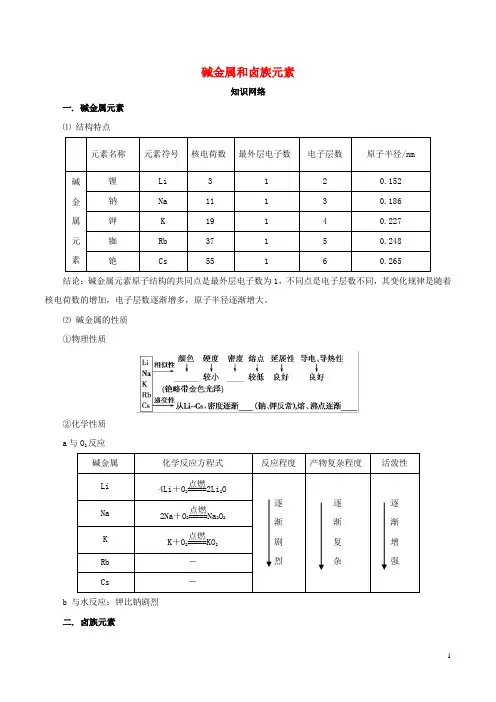
碱金属和卤族元素知识网络一. 碱金属元素 ⑴ 结构特点元素名称元素符号 核电荷数 最外层电子数电子层数原子半径/nm 碱金属 元素锂 Li 3 1 2 0.152 钠 Na 11 1 3 0.186 钾 K 19 1 4 0.227 铷 Rb 37 1 5 0.248 铯Cs55160.265结论:碱金属元素原子结构的共同点是最外层电子数为1,不同点是电子层数不同,其变化规律是随着核电荷数的增加,电子层数逐渐增多,原子半径逐渐增大。
⑵ 碱金属的性质 ①物理性质②化学性质 a 与O 2反应碱金属 化学反应方程式 反应程度产物复杂程度活泼性Li 4Li +O 2=====点燃2Li 2O 逐 渐 剧 烈逐 渐 复 杂逐 渐 增 强Na 2Na +O 2=====点燃Na 2O 2 K K +O 2=====点燃KO 2Rb - Cs-b 与水反应:钾比钠剧烈 二. 卤族元素⑴原子结构元素名称 氟(F) 氯(Cl) 溴(Br) 碘(I) 原子序数 9 17 35 53 最外层电子数 7 7 7 7 电子层数2345结论:卤族元素原子结构的共同点是最外层电子数为7,不同点是电子层数不同,其变化规律是随着原子序数增大,电子层数逐渐增多,原子半径逐渐增大。
⑵ 卤族元素单质的性质 ①物理性质F 2 Cl 2 Br 2 I 2颜色: ———————————————————→浅黄绿色 黄绿色 深红棕色 紫黑色颜色变深 熔、沸点:———————————————————→ 气体 气体 液体 固体 逐渐升高 密度:———————————————————→ 逐渐 增大 水溶性:———————————————————→反应 溶解 溶解 微溶 逐渐减小 ②化学性质 a 与H 2反应反应条件 化学方程式 产物稳定性 F 2 无 H 2+F 2=2HF 最稳定 Cl 2 光或点燃 H 2+Cl 2=2HCl 稳定 Br 2 加热 H 2+Br 2=2HBr 较稳定I 2加热H 2+I 22HI 较不稳定,可逆结论:从F 2到I 2,与H 2反应所需要的条件逐渐升高,反应剧烈程度依次减弱,生成气态氢化物的稳定性依次减弱。

高考常考的化学方程式. .. . .高考常考化学方程式(一)【说明】化学方程式是最重要的化学用语,每套高考试卷中都会考查。
本辑收录了高考无机化学方程式、离子反应方程式和有机反应方程式近300个,全面具体、书写准确、排版工整、方便记忆。
第一部分常考的无机化学方程式碱金属(钠、氧化钠、过氧化钠、氢氧化钠、钠盐)1、4Na+O2══2Na2O2、2Na + O2Na2O23、2Na+ Cl22NaCl4、2Na + S △Na2S(爆炸)5、2Na +2H2O══2NaOH + H2↑6、Na2O + H2O===2NaOH7、2Na2O +O2△2Na2O28、Na2O+ CO2══Na2CO39、Na2O+ 2HCl══2NaCl+ H2O10、2Na2O2 +2H2O══4NaOH + O2↑11、2Na2O2+2CO2══2Na2CO3+O212、2Na2O2+2H2SO4(冷、稀) ══2Na2SO4+O2↑+2H2O13、2NaHCO3△Na2CO3+CO2+H2O14、NaHCO3+ NaOH══Na2CO3+ H2O15、Na2CO3+CO2+H2O══2NaHCO316、4Na+TiCl4(熔融)=4NaCl+Ti17、2Na+2NH3=2NaNH2+H218、NaH+H2O=NaOH+H2↑NaOH19、2NaOH+Si+H2O=Na2SiO3+2H2↑20、6NaOH+3S △2Na2S+Na2SO3+3H2O21、2NaOH+2Al+2H2O=2NaAlO2+3H2↑22、2NaOH(过量)+CO2=Na2CO3+H2O23、NaOH+CO2(过量)=NaHCO324、2NaOH+SiO2=Na2SiO3+H2O(常温下强碱缓慢腐蚀玻璃)25、2NaOH+Al2O3=2NaAlO2+H2O26、2NaOH+Cl2=NaCl+NaClO+H2O27、NaOH+HCl=NaCl+H2O28、NaOH+H2S(足量)=NaHS+H2O29、2NaOH+H2S(少量)=Na2S+2H2O30、3NaOH+AlCl3=Al(OH)3↓+3NaCl31、NaOH+Al(OH)3=NaAlO2+2H2O 32、NaOH+NH4Cl△NaCl+NH3↑+H2O33、2NaOH+P2O5=2NaPO3+H2O34、6NaOH+P2O5=2Na3PO3+3H2ONaAlO235、2NaAlO2+CO2+3H2O=2Al(OH)3↓+Na2CO336、3NaAlO2+AlCl3+6H2O=4Al(OH)3↓NaCl、NaClO、NaBr、NaI37、NaCl+H2SO4(浓)△NaHSO4+HCl↑38、H2SO4(浓)+2NaCl Na2SO4+2HCl39、2NaI+Cl2=2NaCl+I240、NaBr+H3PO4(浓)=NaH2PO4+HBr41、NaI+H3PO4(浓)=NaH2PO4+HI补充:2Na2O2+2H2O=4NaOH+O2↑(此反应分两步Na2O2+2H2O=2NaOH+H2O2;2H2O2=2H2O+O2↑。

高中化学方程式总结高中化学方程式总结高中化学方程式总结第一章卤素第一节氯气1、2Na Cl2 点燃2NaCl2、Cu Cl2 点燃CuCl2点燃3、2Fe 3Cl2 2FeCl34、H2 Cl2 点燃(光照)2HCl5、2P 3Cl2 点燃2PCl36、PCl3 Cl2 PCl57、Cl2 H2O HCl HClO8、2Ca(OH)2 2Cl2 Ca(ClO)2 CaCl2 2H2O 9、Ca(ClO)2 CO2 H2O CaCO3 2HClO 10、2NaOH Cl2 NaClO NaCl H2O 11、4HCl MnO2 MnCl2 2H2O Cl212、2KMnO4 16HCl(浓)2MnCl2 2KCl 5Cl2 8H2O 13、2HClO 见光2HCl O2 第二节氯化氢14、NaCl H2SO(浓)NaHSO4 HCl 415、NaHSO4 NaCl Na2SO4 HCl16、2NaCl H2SO(浓)Na2SO4 2HCl (14、15结合)417、HCl AgNO3 AgCl HNO3 18、NaCl AgNO3 AgCl NaNO3 高中化学方程式总结19、KCl AgNO3 AgCl KNO3 20、2HCl CaCO3 CaCl2 H2OCO2 第三节氧化还原反应21、CuO H2 Cu H2O22、C 4HNO3 CO2 4NO2 2H2O23、4Zn 10HNO(极稀)4Zn(NO3)32 NH4NO3 3H2O24、11P 15CuSO4 24H2O 5Cu3P 6H3PO4 15H2SO4 25、KClO3 6HCl(浓)3Cl2 KCl 3H2O26、4Mg 10HNO(极稀)4Mg(NO3)32 NH4NO3 3H2O27、K2Cr2O7 6Fe3O4 31H2SO4 Cr(O4)O4)O4 31H2O 2S3 9Fe(2S3 K2S28、2KNO3 3C S K2S N2 3CO2 第四节卤族元素29、H2 F2 2HF 30、H2 Br2 2HBr 31、H2 I2 2HI32、2NaBr Cl2 2NaCl Br2 33、2KI Cl2 2KCl I2 34、2KI Br2 2KBr I235、NaBr AgNO3 AgBr NaNO3 36、KI AgNO3 AgI KNO3 37、2AgBr 2Ag Br2光照第二章摩尔反应热第一节摩尔38、C O2 CO2高中化学方程式总结39、Mg 2HCl MgCl2 H2 第二节气体摩尔体积40、Zn 2HCl ZnCl2 H2 第三节物质的量浓度41、2NaOH H2SO4 Na2SO4 2H2O 第四节反应热42、C(固)O(气)点燃CO(气)393.5kJ 2243、2H (气)O(气)2H2O(气)483.6kJ 2244、2H(气)O(气)2H2O(液)571.6kJ 2245、C(固)H2O(气)CO(气)H(气)131.3kJ 2第三章硫硫酸第一节硫46、2Cu S Cu2SFeS 47、Fe S48、S H2 H2S 49、S C 高温CS2 50、S O2 点燃SO251、3S 6KOH 2K2S K2SO4 3H2O 第二节硫的氢化物和氧化物52、H2S H2 S53、2H2S 3O2(足)点燃2H2O 2SO2 54、2H2S O2(不足)2H2O 2S 55、2H2S SO2 2H2O 3S 56、H2S Br2 S 2HBr 57、FeS 2HCl FeCl2 H2S点燃点燃高中化学方程式总结58、CuSO4 H2S CuS H2SO4 59、PbAc2 H2S PbS 2HAc 60、H2S NaOH NaHS H2O 61、NaHS NaOH Na2S H2O62、H2S 2NaOH Na2S 2H2O(60、61结合)63、H2S 2FeCl3 S 2FeCl2 2HCl 64、H2SO(稀)FeS FeSO4 H2S 465、SO2 H2OH2SO3252SO3 66、2SO2 O2VO67、SO3 H2O H2SO468、Na2SO3 H2SO4 Na2SO4 H2O SO2 69、SO2 2NaOH Na2SO3 H2O 70、SO2 CaO CaSO371、SO2 2Ca(OH)O3 H2O 2 CaS72、SO2 CaSO3 H2O Ca (HSO3)2 73、SO2 2H2S 3S 2H2O74、SO2 Cl2 2H2O 2HCl H2SO4 75、SO2 Br2 2H2O 2HBr H2SO476、5SO2 2H2O 2KMnO4 MnSO4 K2SO4 2H2SO4 第三节硫酸的工业制法77、4FeS2 11O2 2Fe2O3 8SO2252SO3 78、2SO2 O2高温VO79、H2O SO3 H2SO4高中化学方程式总结第四节硫酸硫酸盐80、C 2H2SO(浓)CO2 2SO2 2H2O 481、S 2H2SO(浓)3SO2 2H2O 482、P H2SO(浓)H3PO4 SO2 2H2O 483、H2S H2SO(浓)S SO2 2H2O 484、Cu 2H2SO(浓)CuSO4 SO2 2H2O 485、BaCl2 H2SO4 BaSO4 2HCl 86、BaCl2 Na2SO4 BaSO4 2NaCl 87、BaCl2 Na2CO3 BaCO3 2NaCl 88、BaCO3 2HCl BaCl2 H2O CO2 89、BaCO3 2HNO3 Ba(NO3)2 H2O CO2 90、Na2CO3 H2SO3 Na2S H2O CO2 91、2H2SO3 O2 2H2SO4 92、2Na2SO3 O2 2Na2SO4 93、2CaSO3 O2 2CaSO494、2Fe 6H2SO(浓)Fe(O4)O2 6H2O 42S3 3S95、2NaBr 2H2SO(浓)Br2 SO2 Na2SO4 H2O 496、2NaCl H2SO(浓)Na2SO4 2HCl 4497、C11H22O11 2 12C 11H2O浓HSO第四章碱金属第一节钠98、4Na O2 2Na2O 99、2Na O2 Na2O2 100、2Na Cl2 点燃2NaCl高中化学方程式总结101、2Na S 研磨Na2S103、2Na 2H2O CuSO4 Cu(OH)O4 H2 2 Na2S第二节钠的氧化物104、Na2O H2O 2NaOH105、2Na2O2 2H2O 4NaOH O2 106、Na2O CO2 Na2CO3 107、2Na2O2 2CO2 2Na2CO3 O2 108、Na2O 2HCl 2NaCl H2O109、Na2O2 4HCl 4NaCl 2H2O O2 110、Na2CO3 2HCl 2NaCl CO2 H2O 111、NaHCO3 HCl NaCl CO2 H2O 112、2NaHCO3 Na2CO3 CO2 H2O 113、NaHCO3 NaOH Na2CO3 H2O 114、2NaHCO3 Ca(OH)(少量)CaCO3 Na2CO3 2H2O 2115、NaHCO3 Ca(OH)(足量)CaCO3 NaOH H2O 2116、Na2CO3 BaCl2 BaCO3 2NaCl 117、Na2CO3 CaCl2 CaCO3 2NaCl 118、Ca(HCO3)2 2HCl CaCl2 2CO2 2H2O 119、Ca(HCO3)2 2NaOH CaCO3 Na2CO3 2H2O 120、NaHSO3 HCl NaCl SO2 H2O 第三节碱金属元素121、4Li O2 点燃2Li2O高中化学方程式总结122、K O2 点燃KO2123、2M X2 2MX(M表示氧族元素,X代表卤族元素)124、2M H2 2MH第五章物质结构元素周期律本章内容、性质特殊,所有化学反应方程式均融在其他章节中。
盘点高考化学一轮复习卤素化学方程式卤族元素指周期系ⅦA族元素。
包括氟(F)、氯(Cl)、溴(Br)、碘(I)、砹(At),简称卤素。
以下是卤素化学方程式,请考生牢记。
Cu + Cl2 == CuCl2 (点燃) H2 +Cl2 == 2HCl (点燃)Cl2 + H2O == HCl + HClO 2NaOH +Cl2== NaClO +NaCl +H2O2HClO == H2O + Cl2O(CuCl2催化) CH4 +2O2 == CO2 +2H2O (点燃)3HClO == 2HCl + HClO3(加热) 3HCl + Fe(OH)3 == FeCl3 + 3H2 O2Ca(OH)2 + 2Cl2 == Ca(ClO)2 + CaCl2 + 2H2O 工业制漂粉精Ca(ClO)2 + CO2 + H2O == CaCO3+ 2HClO 漂白粉消毒原理4HCl浓+ MnO2 == MnCl2 + 2H2O + Cl2 实验室制氯气NaCl + H2SO4(浓)== NaHSO4 + HCl(加热) 实验室制氯化氢2KMnO4 + 6HCl(浓)== 2KCl + 2MnCl2 + 5Cl2+ 8H2OH2 + F2 == 2HF H2 + Br2 == 2HBr (500℃)H2 + I2 == 2HI (加热且可逆) Cl-+ Ag+== AgCl(Br-、I-同样)2HCl + F2 == 2HF + Cl2(颜色变深)卤素化学方程式的内容确实是这些,查字典化学网期望考生能够更好的复习化学。
2021年高考第一轮复习备考专题差不多新奇出炉了,专题包含高考各科第一轮复习要点、复习方法、复习打算、复习试题,大伙儿来一起看看吧~。
金属一、碱金属 1.钠4Na+O =2Na O 2 22Na+O 2 点燃 Na 2O 2Cl 2+2Na 点燃 2NaCl 2Na+2H O =2NaOH+H ↑ 4Na+TiCl 4(熔融)=4NaCl+Ti Na O+H O =2NaOH 2 2△2 2 2 2Na O+SO =Na SO 2 3 2 4 Na O+CO =Na CO 2 2 2 3 Na O+2HCl =2NaCl+H O 2 22Na 2O 2+2H 2O = 4NaOH+O 2 ↑ ( 此 反 应 分 两 步Na 2O 2+2H 2O = 2NaOH+H 2O 2 ; 2H 2O 2 = 2H 2O+O 2 ↑。
H 2O 2 的制备可利用类似的反应)2Na O +2CO =2Na CO +O 2 2 2 2 3 2Na 2O 2+H 2SO 4(冷、稀)=Na 2SO 4+H 2O 22NaOH+Si+H O =Na SiO +2H ↑ △2 2 22NaOH+Al O =2NaAlO +H O2 3 2 2 2NaOH+Cl =NaCl+NaClO+H O 2 2 NaOH+HCl =NaCl+H O 23NaOH+AlCl 3 =Al(OH)3 ↓+3NaClNaOH+Al(OH)3=NaAlO 2+2H 2O2NaAlO 2+CO 2+3H 2O =2Al(OH)3 ↓+Na 2CO 33NaAlO +AlCl 3+6H O =4Al(OH)3 ↓Na 2CO 3+SiO 2 高温 Na 2SiO 3+CO 2Na CO +HCl =NaHCO +NaCl 2 3 3 NaHCO +HCl =NaCl+H O+CO3 2 23Na 2CO 3+2AlCl 3+3H 2O = 2Al(OH)3 ↓ +3CO 2 ↑ +6NaCl3Na 2CO 3+2FeCl 3+3H 2O = 2Fe(OH)3 ↓ +3CO 2 ↑ +6NaCl3NaHCO 3+AlCl 3 =Al(OH)3 ↓+3CO 2 ↑ 3NaHCO 3+FeCl 3 =Fe(OH)3 ↓+3CO 2 ↑ NaHCO 3+HCl =NaCl+CO 2 ↑+H 2O 2NaHCO 3△Na 2CO 3+CO 2 ↑+H 2O3Na CO +2Br +H O 2 3 2 23 23 2 2 2.钾2KOH+CO =K CO +H O 2 2 3 2 KOH+CO =KHCO 2 3K 2CO 3+2HCl =2KCl+CO 2 ↑+H 2OK 2CO 3+CaCl 2=CaCO 3 ↓+2KCK 2CO 3+2AgNO 3 =Ag 2CO 3 ↓+2KNO 3KHCO 3+HCl =KCl+CO 2 ↑+H 2O 2KHCO 3 △ K 2CO 3+CO 2 ↑+H 2O3 22KI+Cl 2=2KCl+I 2KI+AgNO 3 =AgI ↓+KNO 32KAl(SO 4)2+6NaOH = K 2SO 4+3Na 2SO 4+2Al(OH)3 ↓2KAl(SO 4)2+3Ba(OH)2 = K 2SO 4+3BaSO 4 ↓ +2Al(OH)3 ↓KAl(SO 4)2+2Ba(OH)2=KAlO 2+2BaSO 4 ↓33锂KSCN+FeCl 3 =Fe(SCN)3+3KCl Li O+CO =Li CO 2 2 2 32NaOH(过量)+CO 2=Na 2CO 3+H 2ONaOH+CO 2(过量)=NaHCO 3蚀2N 玻璃aOH SiO 2=Na 2SiO 3+H 2O (常温下强碱缓慢腐KClO 3+6HCl =KCl+3Cl 2 ↑+3H 2OKClO 3+5KCl+3H 2SO 4=3Cl 2 ↑+3K 2SO 4+3H 2O 2 2 3 22NaOH+2Al+2H O =2NaAlO +3H ↑ NaHCO +Br =NaBr+HBrO+CO ↑ 6NaOH+3S 2Na S+Na SO +3H O 2Na O+O 2Na O 2 2 3 22 2 =2NaHCO +2NaBrO+2NaBr+CO ↑ 2KClO △ 2KCl+3O ↑Li O+H O =2LiOH2 22LiOH+CO 2=Li 2CO 3 ↓+H 2OLiOH+CO =LiHCO 2 3 二、常见金属 1.镁2Mg+O 2 点燃 2MgOMg+2H 2O =2Mg(OH)2 ↓+H 2 ↑ Mg+Cl 2 点燃 MgCl 2 2Mg+CO 2 点燃 2MgO+C 3Mg+N 2 =Mg 3N 2Mg+2HCl =MgCl 2+H 2 ↑ Mg+H 2SO 4 =MgSO 4+H 2 ↑ 2Mg+TiCl 4(熔融)=Ti+2MgCl 2MgO+2HCl =MgCl 2+H 2O MgO+H 2O =Mg(OH)2 ↓Mg(OH)2+2HCl =MgCl 2+2H 2OMg(HCO 3)2+2HCl =MgCl 2+2CO 2 ↑+2H 2O 2Mg(HCO 3)2△Mg(OH)2 ↓+CO 2 ↑+H 2OMg 3N 2+8H 2O =3Mg(OH)2+2NH 3 ·H 2O2.铝Al+3O 2 点燃 2Al 2O 3△2 3 2Al+3Cl 2AlCl 2 34Al+3MnO 高温 2Al O +3Mn2 2 3高温 Al O +2Cr2 3高温 Al 2O 3+2Fe (铝热反应) Al O +3Fe 2 32Al+6HCl =2AlCl 3+3H 2t2Al+3H 2SO 4=Al 2(SO 4)3+3H 2 t2Al+6H 2SO 4(浓) △ Al 2(SO 4)3+3SO 2 t +6H 2O Al+4HNO 3(稀)=Al(NO 3)3+NO t +2H 2O (Al 、Fe 在Li 2CO 3+2HCl =2LiCl+CO 2 ↑+H 2OLiHCO 3+HCl =LiCl+CO 2 ↑+H 2O 2LiHCO 3 △ Li 2CO 3+CO 2 ↑+H 2O冷、浓的 H 2SO 4 、HNO 3中钝化)2Al+2NaOH+2H 2O =2NaAlO 2+3H 2 tAl 2O 3+3H 2SO 4=Al 2(SO 4)3+3H 2O (Al 2O 3 是两性氧Al O +2NaOH =2NaAlO +H O 2 3 2 22Al(OH)3△Al 2O 3+3H 2OAl(OH)3+3HCl =AlCl 3+3H 2O 2Al(OH)3+3H 2SO 4=Al 2(SO 4)3+6H 2O Al(OH)3+NaOH =NaAlO 2+2H 2OAlCl 3+3NaOH =Al(OH)3 ↓+3NaCl AlCl 3+3NH 3 · H 2O =Al(OH)3 ↓+3NH 4Cl2AlCl +3Na CO +3H O = 2Al(OH)3 ↓ +3CO 2 ↑AlCl 3+3NaHCO 3 =Al(OH)3 ↓+3CO 2 ↑AlCl 3+3NaAlO 2+6H 2O =4Al(OH)3 ↓Al 2(SO 4)3+3Na 2S+6H 2O =2Al(OH)3 ↓+3H 2S ↑3.铁2Fe+3Cl 点燃 2FeCl 2 33Fe+2O 点燃 Fe O2 3 4 △2Fe+3Br =2FeBr 2 3△2 2 △3Fe+4H 2O(g) 高温 Fe 3O 4+4H 2 Fe+2HCl =FeCl +H ↑Fe+CuCl =FeCl +Cu 2 2Fe+H S =FeS+H ↑ 2Fe+6H 2SO 4(浓)=Fe 2(SO 4)3+3SO 2 ↑+6H 2O Fe+H 2SO 4(稀)=FeSO 4+H 2 ↑Fe+6HNO 3 =Fe(NO 3)3+3NO 2 ↑+3H 2O2Al+Cr O 2 32Al+Fe O2 3 2Al+3FeO +6Na C 3l2 3 22Al+3S Al S Fe+S FeS Fe+S FeSFe+I FeI 2 22 2 △△ 化物)Fe+4HNO 3 =Fe(NO 3)3+NO ↑+2H 2O 8Fe+30HNO 3 =8Fe(NO 3)3+3NH 4NO 3+9H 2O Fe+(CH 3COO)2Cu =Cu+(CH 3COO)2FeFe O +2Al 高温 Al O +2Fe2 3 2 3△2 3 2Fe 2O 3+3H 2=2Fe+3H 2O (制还原铁粉)Fe O +6HCl =2FeCl +3H O 2 3 3 2Fe O +4H 3Fe+4H O 3 4 2 2Fe 3O 4+8HCl(浓) △ FeCl 2+2FeCl 3+4H 2O4Fe(OH)2+O 2+2H 2O =4Fe(OH)3 2Fe(OH)3△Fe 2O 3+3H 2O2FeCl +Cl =2FeCl 2 2 3FeCl 2+Mg =Fe+MgCl 2三、其他金属 1.锰4 2 4 2 22CuOCu S2 CuCl 2CH +4CuO =4Cu+CO +2H O 4 2 2△3 2 2CuO+2HCl =CuCl +H O 2 2CuO+H SO =CuSO +H O 2 4 4 2Cu(OH)2+2HCl =CuCl 2+2H 2OCu(OH)2+H 2SO 4=CuSO 4+2H 2O Cu(OH)2△CuO+H 2OCuCl 2+H 2S =CuS ↓+2HCl 2FeCl +Fe =3FeCl 3 22FeCl 3+Cu =2FeCl 2+CuCl 2 (用于雕刻印刷电路板)2FeCl +H SO +H O =H SO +2FeCl +2HCl 3 2 3 2 2 4 2 2FeCl +Zn =2FeCl +ZnCl 3 2 22FeCl +H S =2FeCl +2HCl+S ↓ 2FeCl +2KI =2FeCl +2KCl+I 3 2 2FeCl 3+3NH 3 ·H 2O =Fe(OH)3 ↓+3NH 4Cl2FeCl 3+3Na 2CO 3+3H 2O = 2Fe(OH)3 ↓ +3CO 2 ↑+6NaClFeCl 3+3NaHCO 3 =Fe(OH)3 ↓+3CO 2 ↑2FeCl +SO +2H O =2FeCl +H SO +2HCl 3 2 2 2 2 4BaCl 2+H 2SO 4=BaSO 4 ↓+2HClFeCl 3+3KSCN =Fe(SCN)3+3KClFe 2(SO 4)3+2Ag =FeSO 4+Ag 2SO 4 (较难反应) Fe 3C+22HNO 3 =3Fe(NO 3)3+CO 2+13NO 2+11H 2OCuSO 4+H 2S =CuS ↓+H 2SO 4CuSO 4+2NaOH =Cu(OH)2 ↓+Na 2SO 4 CuSO 4+Ba(OH)2 =Cu(OH)2 ↓+BaSO 4 ↓ 3.钙 CaO+H 2O =Ca(OH)2CaO+SiO 2 高温 CaSiO 32Ca(OH)2+2Cl 2=CaCl 2+Ca(ClO)2+2H 2OCa(OH)2+SO 3=CaSO 4+H 2O和Ca 浓CO H 3+ 3 =Ca(NO 3)2+H 2O+CO 2 ↑(用 HNO 3 CaCO 3+SiO 2 高温 CaSiO 3+CO 2 ↑ CaF 2+H 2SO 4(浓)=CaSO 4+2HF ↑ Ca 3(PO 4)2+3H 2SO 4(浓)=3CaSO 4+2H 3PO 4 Ca 3(PO 4)2+2H 2SO 4(浓)=2CaSO 4+Ca(H 2PO 4)2 Ca 3(PO 4)2+4H 3PO 4 =3Ca(H 2PO 4)2 (重钙) CaH 2+2H 2O =Ca(OH)2+2H 2 ↑CuCl 2+2NaOH =Cu(OH)2 ↓+2NaCl+8H 2O 4 2 2 2 22.铜 2KMnO 4+16HCl =2KCl+2MnCl 2+5Cl 2 ↑+8H 2O 2KMnO +5H O +6HCl = 2KCl+2MnCl +5O ↑ 2KMnO △K MnO +MnO +O ↑ 2Cu+O22Cu+SCu+Cl 23CuO+2NH 3Cu+N +3H O Fe O +3CO 2Fe+3CO 3 2 2△△ △ 性气体2)4 不能制备 H 2S 、HI 、HBr 、SO 2 等还原卤族元素、氮族元素一、卤族元素1.氟=2HF2 22F +2H O=4HF+O4HF+SiO =SiF +2H O2 4 22.氯Cl2+H2=2HCl (光照或者点燃)Cl +2Na 2NaCl23Cl +2P 2PCl2 3Cl +PCl PCl2 3 53Cl +2Fe 2FeCl2 3Cl +Cu CuCl2 2Cl +2FeCl =2FeCl2 2 32Cl +2NaBr=Cl +2KI=2KCl+I2 25Cl +I +6H O=2HIO +10HCl2 2 2 3Cl +Na S=2NaCl+S ↓2 2Cl +SO +2H O=H SO +2HCl2 2 2 2 4Cl +H SO +H O=H SO +2HCl2 23 2 2 4Cl +H O=HCl+HClO2 2Cl +H O =2HCl+O2 2 2 2Cl +2NaOH=NaCl+NaClO+H O2 22Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O3Cl2+6KOH(热、浓)=5KCl+KClO3+3H2O=2AlCl +3H ↑2HCl+Fe=FeCl +H ↑4HCl(浓)+MnO2△ MnCl2+Cl2+2H2O4HCl(g)+O2△ 2Cl2+2H2O16HCl+2KMnO =2KCl+2MnCl +5Cl +8H O4 2 2 214HCl+K Cr O =2KCl+2CrCl +3Cl +7H O2 2 73 2 2HCl+NH3=NH4Cl (白烟)2HCl+FeO=FeCl +3H O2 2二、氮族元素1.氮N +3H 2NH2 2 36HCl+Fe2O3=2FeCl3+3H2O8HCl(浓)+Fe3O4△ FeCl2+2FeCl3+4H2OHCl+Na PO =Na HPO +NaCl3 4 2 4HCl+Na HPO =NaH PO +NaCl2 4 2 4HCl+NaH PO =H PO +NaCl2 43 4HCl+Na CO =NaHCO +NaCl2 3 3HCl+NaHCO =NaCl+H O+CO3 2 2HClO=HCl+O ↑3.溴△2 2Br +Fe=FeBr2 3Br +2FeBr =2FeBr2 2 3Br +NaI=NaBr+I2 2Br +HI=HBr+I2 2Br +H O=HBr+HBrO2 2Br +NaOH=NaBr+NaBrO+H O2 2Br +SO +2H O=H SO +2HBr2 2 2 2 4Br2+H2S=S ↓+2HBr2Br +3Na CO +H O2 23 23 2HBr+NaOH=NaBr+H O22HBr+Cl =2HCl+Br2 24.碘2HII +Fe FeI2 2I +2NaOH=NaI+NaIO+H O2 2△2HI+Cl =2HCl+I2 2HI+NaOH=NaI+H O2催化剂高温、高压2NO=2 2Cl +H S=2HCl+S ↓22NaCl+Br2Br +H 2HBrI +H2 2N +O2 2H +I2 23 22HI2 222NaHCO +2NaBrO+2NaBr+CO ↑N 2+3Mg 点燃 Mg 3N 2N 2+6Na =2Na 3N2NO+O =2NO 2 2收尾NO+O 中2的+2N Na O O 和H =2 (用于制硝酸工业中吸6NO+4NH 催化剂 5N +6H O 3 2 2△O 鉴2+别2溴KI 蒸+H 气2O 和=2+2KOH (不能用淀粉 KI 溶 4NO +H S =4NO+SO +H O 2 2 3 2NO +SO =SO +NO 2 2 3 3NO +H O =2HNO +NO 2 2 3N O +H O =2HNO2 5 2 33HNO 3+Ag 3PO4=H 3PO 4+3AgNO 3Al+4HNO 3(稀)=Al(NO 3)3+NO ↑+2H 2O3As S +28HNO +4H O = 6H AsO +9H SO +28NO2 3 3 2 3 4 2 44HNO 3(浓)+C △CO 2 ↑+4NO 2 ↑+2H 2O 2HNO 3+CaCO 3 =Ca(NO 3)2+H 2O+CO 2 ↑ 6HNO 3+Fe =Fe(NO 3)3+3NO 2 ↑+3H 2O 4HNO 3+Fe =Fe(NO 3)3+NO ↑+2H 2O 30HNO 3+8Fe =8Fe(NO 3)3+3N 2O ↑+15H 2O 36HNO 3+10Fe =10Fe(NO 3)3+3N 2 ↑+18H 2O 30HNO 3+8Fe =8Fe(NO 3)3+3NH 4NO 3+9H 2O FeO+4HNO 3 =Fe(NO 3)3+NO 2 ↑+2H 2O 3H 2S+2HNO 3(稀)=3S ↓+2NO+4H 2O 4HNO 3=4NO 2+O 2+2H 2O (见光或者受热分解) H 能3+制H O H 32S =N 、H H4I 、N O Br 、白烟S 2 用HNO 3 和浓 H 2SO 43Na 2S+8HNO 3(稀)=6NaNO 3+2NO+3S ↓+4H 2O3Na 2SO 3+2HNO 3(稀)=3Na 2SO 4+2NO ↑+H 2O 3Cu 2S+22HNO 3 = 6Cu(NO 3)2+10NO ↑ +3H SO +8H O2 4 25HNO 3(浓)+P =H 3PO 4+5NO 2 ↑+H 2O P 4+20HNO 3(浓)=4H 3PO 4+20NO 2+4H 2O S+6HNO 3(浓)=H 2SO 4+6NO 2 ↑+2H 2O 3S+4HNO 3(稀)=3SO 2 ↑+4NO ↑+2H 2O碳族元素、氧族元素S+6HNO 3(浓)=H 2SO 4+6NO 2 ↑+2H 2O3As 2S 3+28HNO 3( 稀 )+4H 2O6H 3AsO 4+9H 2SO 4+28NO ↑As 2S 3+28HNO 3( 浓) =2H 3AsO 4+3H 2SO 4+28NO 2 ↑+8H 2O△3 2 22NH +3Cl =N +6HCl 3 2 2 8NH +3Cl =N +6NH Cl 3 2 2 44NH 3+3O 2(纯氧) 点燃 2N 2+6H 2O4NH +5O 催化剂 4NO+6H O 3 2 2△4NH 3+6NO 催化剂 5N 2+6HO (用氨清除 NO )△NH 3+HCl =NH 4Cl (白烟)NH 3+HNO 3=NH 4NO 3 (白烟) 2NH 3+H 2SO 4 =(NH 4)2SO 4H 法3+NaCl+H 2O+CO 2=NaHCO 3 ↓+NH 4Cl (侯氏制 2NH 3+SO 2+H 2O =(NH 4)2SO 3NH 3 ·H 2O △NH 3 ↑+H 2O NH +H O NH ·H O NH Cl =NH +HCl4 3 2NH 4Cl+Ca(OH)2 △CaCl 2+NH 3 ↑+H 2ONH 4Cl+NaOH △NaCl+NH 3 ↑+H 2ONH Cl+NaOH =NaCl+NH ·H O 2.磷P 2O 5+H 2O(冷)=2HPO 3燥+3 2 O(热)=2H 3PO 4 (P 2O 5 极易吸水、可作气P 2O 5+3H 2SO 4(浓)=2H 3PO 4+3SO 3P O +2NaOH =2NaPO +H O 2 5 3 2P O +6NaOH =2Na PO +3H O2 53 3 24H 3PO 4+Ca 3(PO 4)2 =3Ca(H 2PO 4)2 H 3PO 4(浓)+NaBr =NaH 2PO 4+HBr H 3PO 4(浓)+NaI =NaH 2PO 4+HI2NH +3CuO 3Cu+N +3H O 4 3 2NH 4++OH -3 2 3 2↑=2 2P 4S 3+38HNO 3+8H 2O =9H 2SO 4+12H 3PO 4+38NO ↑一、碳族元素 1.碳C+2F 2=CF 4C+2Cl =CCl 2 42C+O 2(少量) 点燃 2CO C+O 2(足量) 点燃 CO 2 △2C+H 2O 高温 CO+H 2 (生成水煤气)2C+SiO 2 △ Si+2CO (制得粗硅)C+Si C+2S△ △SiC (金刚砂) CS 23C+CaO 电炉CaC 2+CO ↑ 3C+SiO 电炉SiC+2CO ↑C+2H 2SO 4(浓) △ CO 2 ↑+2SO 2 ↑+2H 2O △CO 2 ↑+4NO 2 ↑+2H 2O2CO+O 点燃 2CO2 2△23CO+Fe O 2Fe+3CO 2 3 2CO+H O 催化剂 CO +H2 2 2△CO 2+2Mg 点燃 2MgO+CCO +H O =H CO 2 2 2 3CO 2+2NaOH(过量)=Na 2CO 3+H 2O CO 2(过量)+NaOH =NaHCO 3CO 2+Ca(OH)2(过量)=CaCO 3 ↓+H 2O 2CO 2(过量)+Ca(OH)2 =Ca(HCO 3)2二、氧族元素 1.氧2H O 2O +K 22O +3Fe2O +S 点燃 2 O +N 2 2KO 2点燃 Fe O3 4SO22NO 2O 3CO 2+2NaAlO 2+3H 2O =2Al(OH)3 ↓+Na 2CO 3CO +C H ONa+H O =C H OH+NaHCO 2 6 5 2 6 5 3CO +Na O =Na CO 2 2 2 32CO +2Na O =2Na CO +ONH 3 N a 2Cl+H 2 O 2=N 3aH 2CO 3 ↓+NH 4Cl (侯氏制H 2CO 3CO 2 ↑+H 2O2.硅 Si(粗)+2Cl 2 △ SiCl 4 SiCl 4+2H 2 △ Si(纯)+4HCl Si(粉)+O 2 △SiO 2Si+C△SiC (金刚砂)Si+2NaOH+H O =Na SiO +2H2 23 2△24HF+SiO =SiF +2H O 2 4 2SiO +2H2 2SiO 2+2MgSiO +CaO 2△△Si+2H O22MgO+SiCaSiO3SiO 2+2NaOH =Na 2SiO 3+H 2O (常温下强碱缓慢腐蚀玻璃) 高温SiO 2+CaCO 3 高温 CaSiO 3+CO 22NaOH+SiO =Na SiO +H O 2 2 3 24P+5O 点燃 2P O2 2 5C+O 2(足量) 点燃 CO 2△2 24Na+O =2Na O 2 2△2 2 2 22F +2H O =4HF+O 2 2 2Cl +H O =HCl+HClO 2 223C+SiO 电炉 SiC+2CO ↑ CO+CuO Cu+CO △2Mg+SiO 2点燃 2MgO+Si C+4HNO 3(浓) O +2H 2 22Na O+O 2Na O 2C+SiO Si+2CO Na SiO +CO2 3 2SiO +Na CO2 2 3C+CO 2CO Si+O SiO 3O2点燃2△高温2Na+2H O =2NaOH+H ↑ Mg+2H 2O =Mg(OH)2+H 2 ↑ 3Fe+4H 2O(g) 高温 Fe 3O 4+4H 2 2H 2O 电解 2H 2 ↑+O 2SO +H O =H SO 2 2 2 3 SO +H O =H SO 3 2 2 43NO +H O =2HNO +NO 2 2 3N O +H O =2HNO2 5 2 3P 2O 5+H 2O(冷)=2HPO 3 P 2O 5+3H 2O(热)=2H 3PO 4CO +H O =H CO 2 2 2 32 2 2 2H O +Cl =2HCl+O 2 2 2 25H O +2KMnO +6HCl = 2MnCl +2KCl+5O ↑+8H 22 O 24 2 2 2.硫S+H 22S+C S+Fe △ △△H S2CS 2FeS△3S+2Al Al S 2 3△S+O 2 点燃 SO 2S+6HNO 3(浓)=H 2SO 4+6NO 2 ↑+2H 2O3S+4HNO 3(稀)=3SO 2 ↑+4NO ↑+2H 2O△2 23 2S+2Na =Na 2S(爆炸) S+Mg =MgS△S+2H 2SO 4(浓)=3SO 2 ↑+2H 2O=3S+2H O 2 2 22SO +O △ 2SO2 2 32SO +O +2H O =2H SO 2 2 2 2 4 SO +Cl +2H O =H SO +2HCl 2 2 2 2 4 SO +Br +2H O =H SO +2HBr 2 2 2 2 4 SO +I +2H O =H SO +2HI 2 2 2 2 4 SO +NO =SO +NO 2 2 3SO +2H S =3S+2H O 2 2 2 SO +H O =H SO 2 2 2 3SO 2+2NH 3+H 2O =(NH 4)2SO 3 SO 2+(NH 4)2SO 3+H 2O =2NH 4HSO 3SO 2+Ca(OH)2=CaSO 3 ↓+H 2O不)能用澄清石灰水鉴别 SO 2 和 CO 2 .可用品红鉴2NaOH+SO 2(少量)=Na 2SO 3+H 2O NaOH+SO 2(足量)=NaHSO 3Cl +SO +2H O =H SO +2HCl 2 2 2 2 4SO +H O =H SO 3 2 2 4SO 3+MgO =MgSO 4SO 3+Ca(OH)2=CaSO 4+H 2OSO +Na O =Na SO 3 2 2 4 SO +2KI =K SO +I 3 2 3 22 2H 2S+Mg =MgS+H 22H 2S+3O 2(足量)=2SO 2+2H 2O 2H 2S+O 2(少量)=2S+2H 2O2H S+SO =3S+2H O 2 2 2H 2S+H 2SO 4(浓)=S ↓+SO 2+2H 2O△2 23H 2S+2HNO 3(稀)=3S ↓+2NO+4H 2O 5H S+2KMnO +3H SO 2 4 2 42MnSO +K SO +5S+8H O4 2 4 23H S+K Cr O +4H SO Cr 22(SO 42)3+ K 22 S 7O 4+ 32S+74H 2OH S+4Na O +2H O =Na SO +6NaOH 2 2 2 2 2 4H S+Fe =FeS+H ↑ H 2S+CuCl 2=CuS ↓+2HClH 2S+2AgNO 3 =Ag 2S ↓+2HNO 3 H 2S+HgCl 2 =HgS ↓+2HClH 2S+Pb(NO 3)2=PbS ↓+2HNO 3H S+4NO =4NO+SO +H O2 23 2H 2SO 3+X 2+H 2O =H 2SO 4+2HX (X 表示 Cl 2、Br 2、 I ) 2H SO +O =2H SO 2 3 2 2 4H SO +H O =H SO +H O 2 3 2 2 2 4 2H S+Cl =2HCl+S ↓ 2H O =2H O+O ↑ 3S+6NaOH 2Na S+Na SO +3H O S+2Cu Cu S S+Zn ZnSH S H +S S+Fe FeS2 2 2 2 △ ==225H SO +2KMnO 2 3 42MnSO +K SO +2H SO +3H O4 2 4 2 4 2H SO +2FeCl +H O =H SO +2FeCl +2HCl 2 3 3 2 2 4 2H SO =H O+SO ↑ 2H 2SO 3+2H 2S =3S ↓+2H 2O=ZnSO +H ↑ Fe+H SO =FeSO +H ↑Mg+H 22S O 44 =MgS O 44+H 22 ↑2Al+3H 2SO 4=Al 2(SO 4)3+3H 2 ↑2Al+6H 2SO 4(浓) △ Al 2(SO 4)3+3SO 2 ↑+6H 2O 2NH 3+H 2SO 4 =(NH 4)2SO 42Al+6H 2SO 4(浓) △ Al 2(SO 4)3+3SO 2 ↑+6H 2OH 2S+H 2SO 4(浓)=S ↓+SO 2+2H 2O P 2O 5+3H 2SO 4(浓)=2H 3PO 4+3SO 3 BaO 2+H 2SO 4(稀)=BaSO 4+H 2O 2) Na 2O 2+H 2SO 4(冷、稀)=Na 2SO 4+H 2O 2 离子反应(按字母顺序罗列) 2Al+6H +=2Al 3++3H 2 t2Al+2OH -+2H 2O =2 AlO +3H 2 t Al 3++3H 2O Al(OH)3 3H +Al 3++3OH - =Al(OH)3 ↓Al 3++4OH - =AlO +2H 2O3Al 3++10OH -=2A 2l(OH)3 ↓+ AlO +2H 2O (当n (AlCl 3)/n (NaOH)=3:10 时)Al 3++3NH 3 ·H 2O =Al(OH)3 ↓+3 NH 4+2Al 3++3 CO 2 +3H 2O =2Al(OH)3 ↓+3CO 2 tAl 3++3 HCO 3=Al(OH)3 ↓+3CO 2 tAl 3++3HS -+ 33H 2O =Al(OH)3 ↓+3H 2S t 2Al 3++3S 2-+6H 2O =2Al(OH)3 ↓+3H 2S t Al 3++3 AlO +6H 2O =4Al(OH)3 ↓ 2Al 3++3SiO 2 =Al 2(SiO 3)2 ↓AlO +2H 2 O 3Al(OH)3+OH - AlO +H ++H 2O =Al(OH)3 ↓ AlO +4H +=Al 3++2H 2O 9 Al O 2+30H + =2Al(OH)3 ↓+7Al 3++12H 2O (当 n (NaAlO 2)/n (HCl)=3:10 时)3 AlO +Fe 3++6H 2O =Fe(OH)3 ↓+3Al(OH)3 ↓ AlO + NH 4++H 2O =Al(OH)3 ↓+NH 3 ↑AlO + HCO +H 2O =Al(OH)3 ↓+ CO 322 AlO +CO 2+3H 2O =2Al(OH)3 ↓+ CO 32AlO +CO 2+2H 2O =Al(OH)3 ↓+ HCO Al O +6H +=2Al 3++3H O Al 2O 3+2OH -=2 AlO +H 2OAl(OH)3+3H +=Al 3++2H 2O= MgO+H 2SO 4 =MgSO 4+H 2OAl 2O 3+3H 2SO 4=Al 2(SO 4)3+3H 2O 2H 2SO 4(浓)+C △ CO 2 ↑+2SO 2 ↑+2H 2O 2H 2SO 4(浓)+S =3SO 2 ↑+2H 2O6H 2SO 4(浓)+2Fe =Fe 2(SO 4)3+3SO 2 ↑+6H 2O2H 2SO 4(浓)+Cu △ CuSO 4+SO 2 ↑+2H 2O H 2SO 4(浓)+2HBr △ SO 2+Br 2+2H 2O H 2SO 4(浓)+2HI △ SO 2+I 2+2H 2O H 2SO 4(浓)+CaF 2=CaSO 4+2HF ↑ H 2SO 4(浓)+NaCl △ NaHSO 4+HCl ↑ H 2SO 4(浓)+2NaCl Na 2SO 4+2HCl H 2SO 4(浓)+NaNO 3 △ NaHSO 4+HNO 3 ↑ 3H 2SO 4(浓)+Ca 3(PO 4)2=3CaSO 4+2H 3PO 4 2H 2SO 4(浓)+Ca 3(PO 4)2=2CaSO 4+C a (H 2PO 4)2Al(OH)3+2OH - =AlO +2H 2OAg ++H 2O AgOH+H +Ag ++NH 3 ·H 2O =AgOH ↓+ NH 4+ Ag ++2NH 3 ·H 2O = [Ag(NH 3 )2]+ +H 2OAg ++Cl - =AgCl ↓ Ag ++Br - =AgBr ↓ Ag ++I - =AgI ↓3Ag ++ PO 43=Ag 3PO 4 ↓2Ag ++ CO 2 =Ag 2CO 3 ↓Ag 2CO 3 H + =2Ag ++CO 2 ↑+H 2O Ag 3PO 4+3H + =3Ag ++H 3PO 42Ag[(NH 3)2]++2OH -+CH 3CHO CH 3COO -+ NH 4++2Ag ↓+3NH 3+H 2O2Ag[(NH 3)2]++2OH -+CH 2OH(CHOH)4CHO CH 2 OH(CHOH)4COO -+ NH 4++2Ag ↓+3NH 3+H 2OBa 2++ SO 2 =BaSO 4 ↓ Ba 2++ CO =BaCO 3 ↓3Ba 2++2 PO 43=Ba 3(PO 4)2 ↓Ba 2++2OH -+CO 2=BaCO 3 ↓+H 2OBa 2++2OH -+2H ++ SO 2 =BaSO 4 ↓+2H 2O (NaHSO 4 溶液中加 Ba(OH)2,4使溶液呈中性)Ba 2++OH -+H ++ SO 2 =BaSO 4 ↓+H 2O (NaHSO 4 溶液 中加 Ba(OH)2,使4 Ba 2+全部沉淀)BaCO 3+2H +=Ca 2++CO 2t +H 2O 2Br -+Cl =2Cl -+Br 2 22 3 2 2 4 4 22 3 2 2Br +SO +2H O =2Br -+2H ++ SO 24Br -+2Fe 2++3Cl 2=2Fe 3++2Br 2+ 64Cl - (足量 Cl 2 ) 2Br -+2Fe 2++2Cl 2=2Fe 3++Br 2+4Cl - (当 n (FeBr 2)/n (Cl 2)=1:1 时)10Br -+6Fe 2++8Cl 2=6Fe 3++5Br 2+16Cl - (当 n (FeBr 2)/n (Cl 2)=3:4 时) CO 2 +2Ag + =Ag 2CO 3 ↓CO 23+Ba 2+=BaCO 3 ↓CO 23+Ca 2+=CaCO 3 ↓CO 23+2H +=CO 2 ↑+H 2OCO 23+H 2O HCO +OH -3 C O 32 +2Al 3++3H 2O 2Al(OH)3 ↓+3CO 2 ↑3 CO 23+2Fe 3++3H 2O =2Fe(OH)3 ↓+3CO 2 ↑ CO 2 AlO +3H 2O =2Al(OH)3 ↓+CO 2CO 2+ AlO +2H 2O =Al(OH)3 ↓+ HC O 3CO +OH - =HCO CO 2+Ba 2++2OH - BaCO 3 ↓+H 2O CO 2+2OH - =CO 2 +H 2O 3CO 2+5OH -=2C 3O 2 + HCO +2H 2O (当 n (CO 2)/n (NaOH)=33:5 时) 3CO 2+ SiO 2 +2H 2O =H 4SiO 4 ↓+ CO 23 3Ca 2++2OH -+CO 2=CaCO 3 ↓+H 2O Ca 2++2OH -+SO 2=CaSO 3 ↓+H 2O Ca 2++2ClO -+SO 2+H 2O =CaSO 4 ↓+HClO+H ++Cl - (少 量 SO ) Ca 2++2ClO -+2SO 2+4H 2O = CaSO 4 ↓ +2Cl -+4H ++ SO 2 (足量 SO 2 ) Ca 2++2ClO -+C O 42+H 2O =CaCO 3 ↓+2HClO CaCO 3+2H +=Ca 2++CO 2 ↑+H 2O Cl +H O =Cl -+H ++HClOCl +2OH -=Cl -+ClO -+H O 2 2 Cl +2OH -=Cl -+ClO -+H O 2 2Cl +2I -=2Cl -+I 2 2Cl 2+H 2SO 3+H 2O =2Cl -+ SO 42+4H + Cl 2+H 2S =2Cl -+2H ++S ↓ Cl 2+2Fe 2+=2Fe 3++2Cl - (向 FeBr 2 溶液中少量 Cl 2 ) 3Cl 2+2Fe 2++4Br -=2Fe 3++2Br 2+6Cl - (足量 Cl 2 ) 2Cl 2+2Fe 2++2Br -=2Fe 3++Br 2+4Cl - (当 n (FeBr 2)/n (Cl 2)=1:1 时) 8Cl 2+6Fe 2++10Br -=6Fe 3++5Br 2+16Cl - (当n (FeBr 2)/n (Cl 2)=3:4 时) 2Cl -+4H ++MnO 2=Mn 2++Cl 2 ↑+2H 2O Cl -+Ag + =AgCl ↓ ClO -+H +=HClOClO -+SO 2+H 2O =2H ++Cl -+ SO 2ClO -+H O HClO+OH -2Cr O +6Fe 2++14H +=6Fe 3++2Cr 3++7H 2O7Cu+2Fe 3+=2Fe 2++Cu 2+3Cu+2 NO +8H +=3Cu 2++2NO t +4H 2OCu 2++2H 2 O 3Cu(OH)2+2H +Cu 2++2NH 3 ·H 2O =Cu(OH)2 ↓+2NH 4+ Cu 2++2Na+2H 2O =2Na ++Cu(OH)2 ↓+H 2 t Cu 2++H 2S =2H ++CuS ↓ Cu 2++Fe =Cu+Fe 2+Cu 2++2OH - =Cu(OH)2 ↓ CuO+2H +=Cu 2++H O Fe+2H +=Fe 2++H ↑ Fe+Cu 2+=Fe 2++CuFe+2Fe 3+=3Fe 2+ Fe 2++2OH - =Fe(OH)2 ↓ 2Fe 2++Cl 2=2Fe 3++2Cl -2Fe 2++Br 2=2Fe 3++2Br - 4Fe 2++O 2+4H +=Fe 3++2H 2O 12Fe 2++3O 2+6H 2O =8Fe 3++4Fe(OH)3 ↓ 2Fe 2++H 2O 2+2H +=2Fe 3++2H 2O 6Fe 2++ Cr O +14H +=6Fe 3++2Cr 3++7H 2O 5Fe 2++ Mn 2O +8H +=5Fe 3++Mn 2+4H 2O 3Fe 2++ NO 4H +=3Fe 3++NO ↑+2H 2OFe 2++S 2- =FeS 3↓ 2Fe 2++Cl 2=2Fe 3++2Cl - (向 FeBr 2 溶液中通入少量 Cl ) 2Fe 2++4Br -+3Cl 2=2Fe 3++2Br 2+6Cl - (足量 Cl 2) 2Fe 2++2Br -+2Cl 2=2Fe 3++Br 2+4Cl - (当 n (FeBr 2)/n (Cl 2)=1:1 时) 6Fe 2++10Br -+8Cl 2=6Fe 3++5Br 2+16Cl - (当 n (FeBr 2)/n (Cl 2)=3:4 时)2Fe 2++4I -+3Cl 2=2Fe 3++2I 2+6Cl - (向 FeI 2 溶液中足量 Cl 2 ) 2Fe 2++6I -+4Cl 2 = 2Fe 3++3I 2+8Cl - ( 当 n (FeI 2)/n (Cl 2)=3:4 时) Fe 3++3OH - =Fe(OH)3 ↓ 2Fe 3++Cu =2Fe 2++Cu 2+2Fe 3++Fe =3Fe 2+Cl 2+2I -=2Cl -+I 2 2Fe 3++Zn =2Fe 2++Zn 2+ Cl 2+2I -=I 2+2Cl - (向 FeI 2 溶液中通入少量 Cl 2 ) 2Fe 3++3Zn =2Fe+3Zn 2+3Cl 2+2Fe 2++4I -=2Fe 3++2I 2+6Cl - (足量 Cl 2 ) Fe 3++3 HCO =Fe(OH)3 ↓+3CO 2 t4Cl 2+2Fe 2++6I - =2Fe 3++3I 2+8Cl - (当 Fe 3++3 AlO +6H 2O =Fe(OH)3 ↓+3Al(OH)3 ↓n (FeI 2)/n (Cl 2)=3:4 时) 2Fe 3++3 CO 2+3H 2O =2Fe(OH)3 ↓+3CO 2 ↑2 32 2 2 2 2 22 22 242 4 2Fe 3++H 2S =2Fe 2++S ↓+2H + 2Fe 3++S 2-=2Fe 2++S ↓ 2Fe 3++2I -=2Fe 2++I 22Fe 3++SO 2+2H 2O =2Fe 2++ SO 2 +4H +Fe 3++3SCN - =Fe(SCN) (红色4溶液)Fe 3++3H 2O =Fe(OH)FeO+2H +=Fe 2++H O Fe 2O 3+6H +=Fe 3++3H 2OFe 3O 4+8H +=Fe 2++2Fe 3++4H 2O FeS+2H +=Fe 2++H 2S t H ++OH -=H 2O 2H O+2Na =2Na ++2OH -+H ↑ 2H 2O+2Na 2O 2=4Na ++4OH -+O 2 ↑ H 2O+Na 2O =2Na ++2OH - H O+Cl =Cl -+H ++HClO2 2 2 2H 2O 2+2Fe 2++2H +=2Fe 3++2H 2O5H 2O 2+2 MnO +6H +=2Mn 2++5O 2 ↑+8H 2OH 2O 2+Cl 2=2H 4++2Cl -+O 2 ↑ H 2O 2+SO 2=2H ++ SO 242 3 HCOH ++ HCO H ++ CO 233 3HCO 2O H 2C O 33+ OHHCO + OH =CO 2 +H 2O HCO +H +=CO 2 ↑2O3 HC O 3+Al 3+ =Al(OH)3 ↓+3CO 2 t3 HCO +Fe 3+ =Fe(OH)3 ↓+3CO 2 t2 HCO +Ca 2++2 OH=CaCO 3 ↓+2H 2O+ CO 2 (向NaHC O 33 溶液中加入少量澄清石灰水)3 HCO +Ca 2++ OH =CaCO 3 ↓+H 2O (足量澄清石 灰水 )3HCO +Ca 2++ OH =CaCO 3 ↓+H 2O (向 Ca(HCO 3)2溶液中3加入少量 NaOH 溶液)2 HCO +Ca 2++2 OH =CaCO3 ↓+2H 2O+ CO 2(Ca(H 3CO 3)2 溶液中加入足量 NaOH 溶液) 3 入H 少CO 量3溶=C 液O 23)+H 2O (向 NH 4HCO 3 溶液中加 HCO + NH 4 +2 OH =CO 32+H 2O+NH 3 ·H 2O (向 NH 4HCO 3 溶液中加入足量 NaOH 溶液) 2 HCO +SO 2=SO 2 +CO 2 t +H 2OHCO AlO +H 2 O 3=Al(OH)3 ↓+ CO 32H ++ H POH ++ H 2PO 244H 3PO 4+ OH =H PO +H 2OH PO + OH = HP 2O 2 +H 2O HP 2O 2 + OH = PO 3 H 2OPO 3 +H O HPO 2 + OH HP O 4 2 +H 2O H P 4O + OH H P O 4 +H 2O H 32PO 44+ OHH + P O 43 =HPO 2H ++ HP O 4 2 =H P 4OH ++ 4 =H 32PO 44H ++HS - H ++S 2-22I -+2Fe 3+=2Fe 2++I 2 2I -+Cl =2Cl -+I2 22I -+Br =2Br -+I 2 2I -+Ag + =AgI ↓2I -+H O +2H +=I +2H O 2 2I +2OH -=I -+IO -+H O 2 2I 2+5Cl 2+6H 2O =12H ++10Cl -+2 IO Mg+2H + =Mg 2++H 2 tMg 2++2OH - =Mg(OH)2 ↓ Mg 2++ CO 32=MgCO 3 ↓MgCO 3+2H + =Mg 2++CO 2 ↑+H 2O MgO+2H + =Mg 2++H 2OMg(OH)2+2H + =Mg 2++2H 2O2 2 3HS -+Al 3++3H 2O =Al(OH)3 ↓+3H 2S tH 2SO 3 H ++ HSO HSO H ++ SO 2 3HSO +H 2O H 23SO 3+OH -HSO +OH - =SO 2 +H 2O HSO +H +=SO 2 ↑3+H 2O H 2 SO 33+Cl 2+H 2O =2Cl -+ SO 42+4H +2 H 2S+Cl 2=2Cl -+2H ++S ↓ 2H 2S+SO 2=3S ↓+2H 2O 2H 2S+O 2=2S ↓+2H 2O H 2S+Cu 2+=2H ++CuS ↓ H 2S+(CH 3COO)2Pb =PbS ↓+2CH 3COOH H S+2OH -=S 2-+2H O H ++HS -=H 2S H O+S 2- HS -+OHH O +2I -+2H +=I +2H O 2 2 2 25I -+IO -+6H +=3I +3H O 2 2 H S+OH -=HS -+H O 2 2 HS -+OH -=S 2-+H O H PO3 4 H PO 2 4HPO244 42 HS -+H O H S+ OH H ++ PO 342 2H ++S 2-=HS - H S 2 HS - 233 H 2O+ CO 2 HCO +OH3MnO 2+2Cl -+4H +=Mn 2++Cl 2 t +2H 2O MnO +5Fe 2++8H +=5Fe 3++Mn 2+4H 2O2 Mn O 4+5SO 2+2H 2O =2Mn 2++5SO 2 +4H +2 MnO +5H 2O 2+6H +=2Mn 2++5O2↑4+8H 2O 12 Mn O 4+5C 2H 4+36H +=12Mn 2++10CO 2 ↑+28H 2O2 MnO C O 2 +16H +=2Mn 2++10CO 2 ↑+8H 2O4 2 42Na+2H 2O =2Na ++2OH -+H 2 ↑2Na+Cu 2++2H 2O =2Na ++Cu(OH) 2 ↓+H 2 ↑++H 2O NH 3 ·H 2O+H +2 N H 4+ +SiO 2 +H 2O =H 4SiO 4 ↓+2NH 3 ↑NH + AlO 3+H 2O =Al(OH)3 ↓+NH 3 ↑NH + HC O 2+2OH - = CO 2 +H 2O+NH 3 ·H 2O (向NH 4HCO 43 溶3液中加入足量3 NaOH 溶液)NH +H O NH ·H O NH 3 ·H 2O NH 4++OH -NH 3 ·H 2O+Ag + =AgOH ↓+NH 4+2AgOH =Ag 2O+H 2O (AgNO 3 溶液中加入少量氨水)2NH 3 ·H 2O+Ag + =[Ag(NH 3)2]++H 2O (足量氨水) 溶2N 液H 中3·加H 入2O 少量+Cu2氨水+=C u (OH)2 ↓+2 NH 4+(向 CuSO 44NH 3 ·H 2O+Cu 2+ =[Cu(NH 3)4]2++4H 2O (足量氨水) 2NH 3 ·H 2O+Zn 2+ =Zn(OH)2 ↓+2NH 4+ (向 ZnCl 2 溶液中加入少量氨水)4NH 3 ·H 2O+Zn 2+ =[Zn(NH 3)4]2++4H 2O (足量氨水) 3NH 3 ·H 2O+Al 3+ =Al(OH)3 ↓+3 NH 4+2 NO +2I -+4H +=2NO ↑+I 2+2H 2O5 NO +2 MnO +6H +=2Mn 2++5 NO +3H 2ONO 2++4H 4+=3Fe 3++NO ↑+2H 23O2 N O 3+3SO 2+2H 2O =3SO 2 +2NO ↑+4H +2 NO +3Cu+8H +=3Cu 2++ 24NO ↑+4H 2OOH +H +=H O OH +CO =HCO O 2+2H 2S =2S ↓ H 2O O 2+2S 2-+4H +=S ↓+2H 2O O 2+2HS -+2H +=S ↓+2H 2O O 2+4Fe 2++4H +=Fe 3++2H 2O3O 2+12Fe 2++6H 2O=8Fe 3++4Fe(OH)3 ↓O +2SO 2 =2SO 2 2PO 43 +3Ag + =Ag 3PO 4 ↓2 PO 43 +3Ba 2+ =Ba 3(PO 4)2 ↓2 PO 43+3Ca 2+=Ca 3(PO 4)2 ↓2 PO3 +3Mg 2+ =Mg 3(PO 4)2 ↓PO 34+H + =HPO 2PO 34 +2H + =H P 4OPO 34 +3H +=H 3PO 244Pb 2+ SO 2 =PbSO 4 ↓Pb 2++S 2- PbS ↓PbO 2+2Cl -+4H +=Pb 2++Cl 2 t +2H 2O(CH 3COO)2Pb+H 2S =PbS ↓+2CH 3COOH 3S+6OH -=2S 2-+ SO 2 +3H 2OS 2-+H O HS -+OH - 23S 2-+2Al 3++6H 2O =2Al(OH)3 ↓+3H 2S ↑ S 2-+2Fe 3+=2Fe 2++S ↓SO 2+Ca 2++2ClO -+H 2O = CaSO 4 ↓ +HClO+H ++Cl - (少量 SO 2 )2SO 2+Ca 2++2ClO -+4H 2O = CaSO 4 ↓+2Cl -+4H ++ SO 2(足量 SO 2 )SO 2+2Fe 3++2H 24O =2Fe 2++ SO 2 +4H +SO 2+2 HCO =SO 2 +CO 2 ↑ H 2O SO 2+2OH - SO 2 H 2OSO +OH -=HSO 2SO +Br +2H O =2Br -+2H ++ SO 2 2 2 2 3SO 2+2 NO +2H 2O 3SO 2 +2NO t +4H +SO 2+ClO -+H 32O =2H ++Cl - SO 2SO 2+2H 2S =3S ↓+2H 2O 4SO +H O H SO 2 2 2 35SO 2+2 MnO +2H 2O =2Mn 2++5SO 2 +4H +SO 2 +2H + = S 4O 2 t +H 2O4SO 23+H 2O HSO +OH -SO 23+Ba 2+=BaSO 4 ↓3SO 24+2H ++Ba 2++2OH -=BaSO 4 ↓+2H 2O(NaHSO 4 溶液4中加 Ba(OH)2 ,使溶液呈中性)SO 2 +H ++Ba 2++OH -=BaSO 4 ↓+H 2O (NaHSO 4 溶液中4加 Ba(OH)2 ,使 Ba 2+全部沉淀) S O +2H +=S ↓+SO 2 t +H 2O 3Si+2OH -+H 2O = SiO 2 +2H 2 ↑SiO 2+2OH - =SiO 2 +H 32O SiO 32 +2 NH 4++H 2O 3=H 4SiO 4 ↓+2NH 3 ↑SiO 32+CO 2+2H 2O =H 4SiO 4 ↓+CO 32-SiO 2 +2H ++H 2O =H 4SiO 4 ↓ 3Si O 332+2Fe 3+=Fe 2(SiO 3)2 ↓3SiO 32+2Al 3+=Al 2(SiO 3)2 ↓ Zn+2H +=Zn 2++H ↑Zn+2OH - = ZnO 2 +H 2 ↑Zn+2Fe 3+=2Fe 2+Zn 2+ (少量 Zn 片) 3Zn+2Fe 3+=2Fe+3Zn 2+ (过量 Zn 片)高中化学方程式总结,第11页,共12页SO 2+H 2O 2=2H ++ SO 2 4SO +I +2H O =2I -+2H ++ SO 23 4O +2I -+2H +=I +O +H O 3 2 3 22 2 2 2 22 4 333Zn 2++2H 2O Zn(OH)2+2H + Zn 2++2OH -=Zn(OH)2 ↓Zn 2++2NH 3 ·H 2O =Zn(OH)2 ↓+2 NH + (少量氨水)Zn 2++4NH 3 ·H 2O =[Zn(NH 3)4]2++4H 2 O 4(足量氨水)Zn(OH)2+2H +=Zn 2++2H 2OZn(OH)2+2OH =ZnO 2一 +2H 2OZnO+2H +=Zn 2++H O 2 ZnO+2OH =ZnO 2一 +H 2O高中化学方程式总结,第12页,共12页22。
二、卤族元素性质的递变规律1.卤素单质的物理性质氟、氯、溴、碘单质的颜色逐渐加深,密度逐渐加大,熔沸点逐渐升高,水溶性逐渐减小(氯除外)。
2.卤素的化学性质按氯、氯、溴、碘的顺序,元素的非金属性,单质的氧化性、与氢化合的能力、与水反应的程度均逐渐减弱。
(1)与金属反应:氟(F2)可以与所有的金属反应;氯(Cl2)可以与绝大多数金属反应;溴、碘也可以与大多数金属反应。
例如:2Fe+3Cl2== 2FeCl3而Fe+I2 == FeI2(2)与氢气反应:反应条件由易到难;反应程度由剧烈变为缓慢;卤化氢的稳定性逐渐减弱。
(3)与水反应:氟特殊,氯、溴、碘相似。
反应的剧烈程度逐渐减弱。
(4)卤素单质间的置换反应Cl2 + 2Br-= 2Cl-+ Br2氧化性:Cl2 > Br2 还原性: Br-> Cl-Cl2 + 2I-= 2Cl-+ I2氧化性:Cl2 > I2 还原性: I- > Cl-Br2 + 2I-= 2Br-+ I2氧化性:Br2 > I2 还原性: I- > Br-结论:单质氧化性:F2>CI2>Br2>I2离子还原性:F-<CI-<Br-<I-3.卤化氢的性质氢卤酸的酸性其中氢氟酸为弱酸。
、卤化氢的还原性按HF、HCl、HBr、HI的顺序依次增强,其稳定性依次减弱,4.氯的含氧酸次氯酸(HClO):仅存于溶液中,具有不稳定性,强氧化性。
其酸性比碳酸还弱。
其盐类中,次氯酸钙[Ca(ClO)2]是漂白粉中的有效成分。
高氯酸(HClO4):是已知酸中酸性最强的一种酸。
LI NA K Rb Cs 熔沸点依次降低。
1.相似性:最外层电子数为12.递变性:1.电子层数逐渐增多;2.熔点逐渐降低;3.沸点逐渐降低;4.密度呈增大趋势(但NA>K);5.金属性逐渐增强。
3.碱金属元素的主要化学性质:1.与氧气反应。
都可以与氧气反应,但Li的燃烧产物为普通氧化物Li2O,而Na的燃烧产物为过氧化物Na2O2,K,Rb,Cs的燃烧产物更复杂。
高三化学金属元素方程式总结1、碱金属(1)钠投入水中:2Na+2H2O==2NaOH+H2↑ 2Na+2H2O==2Na++2OH-+H2↑。
(2)过氧化钠与水:2Na2O2+2H2O===4NaOH+O2↑;2Na2O2+2H2O===4Na++4OH-+O2↑(转移2mole-)(3)过氧化钠与CO2: 2Na2O2+2CO2==2Na2CO3+O22、铁(1)FeCl3溶液与铁: 2Fe3++Fe=3Fe2+(2)FeCl3溶液与铜: 2Fe3++Cu=2Fe2++Cu2+ (用于雕刻铜线路版)(3)FeCl2溶液通入氯气: Cl2+2Fe2+===2Fe3++2Cl-(4)Fe3+的检验: Fe3++3SCN-===Fe(SCN)3(呈血红色)(5)氢氧化亚铁变成氢氧化铁: 4Fe(OH)2+O2+2H2O===4Fe(OH)3(6)氢氧化铁胶体的制备:FeCl3+3H2O Fe(OH)3(胶体)+3HCl3、镁(1)镁与氧气: 2Mg+O22MgO(2)镁与二氧化碳: 2Mg+CO22MgO+C(3)镁与氮气: N2+3MgMg3N2(4)海水提镁过程:CaCO3CaO+CO2↑; CaO+H2O===Ca(OH)2; Mg2++2OH-===Mg(OH)2↓;Mg(OH)2+2HCl===MgCl2+2H2O; MgCl2(熔融) Mg+Cl2↑4、铝(1)铝燃烧: 4Al+3O2 2Al2O3(2)铝热反应: 2Al+Fe2O3 Al2O3+2Fe 8Al+3Fe3O4 4Al2O3+9Fe(3)铝与强酸:2Al+6H+=2Al3++3H2↑(4)铝与强碱:2Al+2NaOH+2H2O=2NaAlO2+3H2↑ 2Al+2OH–+2H2O=2AlO2-+3H2↑(5)氧化铝与强酸: Al2O3+6H+=2Al3++3H2O(6)氧化铝与强碱: Al2O3+2OH-=2AlO2-+H2O(7)氢氧化铝与强酸: Al(OH)3+3H+===Al3++ 3H2O(8)氢氧化铝与强碱: Al(OH)3+OH–=AlO2- +2H2O(9)实验室中氢氧化铝制备:Al3++3NH3·H2O=Al(OH)3↓+3NH4+(10)向氯化铝溶液中逐滴滴加氢氧化钠至过量:Al3++3OH- ===Al(OH)3↓; Al(OH)3+OH–= AlO2- +2H2O (11)向氢氧化钠溶液中逐滴滴加氯化铝至过量:Al3++4OH-=== AlO2-+2H2O; 3 AlO2-+Al3++6H2O=4Al(OH)3↓(12)向偏铝酸钠溶液中逐滴滴加盐酸至过量:AlO2- +H++H2O===Al(OH)3↓; Al(OH)3+3H+=Al3+ +3H2O (13) 向盐酸中逐滴滴加偏铝酸钠溶液至过量:AlO2- +4H+===Al3++2H2O; 3AlO2-+Al3++6H2O=4Al(OH)3↓(14)碳酸氢钠溶液与硫酸铝溶液混合: 3HCO3-+Al3+===Al(OH)3↓+3CO2↑5、铜(1)铜绿的形成: 2Cu+O2+CO2+H2O===Cu2(OH)2CO3(2)铜与氧气: 2Cu+O2====2CuO(3)氧化铜高温分解:4CuO2Cu2O+O2↑。
点燃
1.钠在氧气中燃烧 2Na+O2=Na2O2
2.钠与氧气在常温下反应 4Na+O2=2Na2O
3.钠与水反应 2Na+2H2O=2NaOH+H2↑
4.钠与硫酸铜溶液反应 2Na+CuSO4+H2O=Na2SO4+Cu(OH)2+H2↑
5.氧化钠与水反应 Na2O+H2O==2NaOH
6.过氧化钠与水反应 2Na2O2+2H2O==4NaOH+O2↑
7.过氧化钠与二氧化碳反应 2Na2O2+2CO2==2Na2CO3+O2↑
8.碳酸钠与盐酸反应 Na2CO3+2HCl==2NaCl+CO2↑+H2O
9.碳酸氢钠与盐酸反应 NaHCO3+HCl==NaCl+CO2↑+H2O
10.碳酸氢钠与氢氧化钠反应 NaHCO3+NaOH==Na2CO3+H2O
11.碳酸氢钠加热分解 2NaHCO3加热Na2CO3+ CO2↑+H2O
12.二氧化碳通入碳酸钠溶液 CO2+ Na2CO3 +H2O ==2 NaHCO3 13.碳酸钙加盐酸 CaCO3+2HCl==CaCl2+ CO2↑+ H2O
14.碳酸氢钠加过量氢氧化钙 2NaHCO3+Ca(OH)2==Na2CO3+ CaCO3+H2O 15.碳酸氢钠加少量氢氧化钙 NaHCO3+Ca(OH)2=CaCO3+NaOH+H2O 16.氢氧化钠中通入少量的二氧化碳气体
CO2+2NaOH(过量)==Na2CO3+H2O
氢氧化钠中通入过量的二氧化碳气体 CO2(过量)+NaOH==NaHCO3 17.氢氧化钙溶液中通入过量的二氧化碳气体
2CO2(过量)+Ca(OH)2==Ca(HCO3)2
18.碳酸氢钙加过量氢氧化钠
Ca(HCO 3)2+2NaOH = CaCO 3↓+Na 2CO 3+2H 2O
19.氢氧化钠加过量碳酸氢钙 Ca(HCO 3)2+NaOH = CaCO 3↓+H 2O+NaHCO 3 20.实验室制氯气 MnO 2 + 4HCl (浓
2 + Cl 2↑+ 2H 2O 21.浓盐酸加高锰酸钾
16HCl+2KMnO 4 = 2KCl + 5Cl 2 ↑+ 8H 2O + 2MnCl 2 22.氯气与水反应 Cl 2+H 2O=HCl+HClO 23.氟气与水反应 2F 2+2H 2O===4HF+O 2
24.工业上制漂粉精(或漂白粉)2Cl 2+2Ca(OH)2=CaCl 2+Ca(ClO)2+2H 2O 25.氯气与氢氧化钠溶液反应 Cl 2+2NaOH==NaCl+NaClO+H 2O 26.氯气与铁反应 3Cl 2+2Fe== 2FeCl 3 27.氯气与铜反应 Cl 2+Cu ==CuCl 2 28.氯气与钠反应 2Na+Cl 2=2NaCl
29.氯气与溴化钠反应 Cl 2+2NaBr==2NaCl+Br 2 30.氯气与碘化氢反应 Cl 2+2HI==HClI+ HCl 31.溴与碘化钾反应 Br 2+2KI===2KBr+I 2
32.溴化银见光分解 2AgBr==2Ag+Br 2 39.卤素单质溶液X 2(X =Cl 、Br 、I )中通入SO 2 SO 2 + X 2 + 2H 2O == H 2SO 4 + 2HX 41.氯气与亚硫酸钠溶液反应 Na 2SO 3 + Cl 2 + H 2O == Na 2SO 4 + 2HCl
点燃
点燃 点燃 光照。