血清白蛋白ALB测定
- 格式:doc
- 大小:25.50 KB
- 文档页数:7

血清白蛋白(ALB)
一、检测原理
在PH4.2的缓冲液中,白蛋白分子带正电荷,与带负电荷的BCG生成蓝绿色复合物,在波长628nm处有吸收峰,吸光度与血清中ALB成正比,而求出ALB的浓度。
二、参考区间
血清:40—55g/L
三、临床意义
1、血清白蛋白也叫清蛋白,是人体血浆蛋白中最主要的组成部分,血清白蛋白作用主要有两方面,一是维持人体正常的营养状态,二是维持血浆等胶体渗透压,因为血清白蛋白对人体的正常营养状态具有非常重要的作用。
2、增高主要见于:
①白蛋白偏高主要见于血液浓缩而导致相对性的增高,比如:严重的脱水和休克,严重的烧伤、肾脏疾病、大量出血等。
②多发性骨髓瘤、巨球蛋白血症、腹泻、呕吐、高热时急剧失水也可导致血清中白蛋白浓度增高,从而引起白蛋白偏高。
③白蛋白偏高也可受到饮食中蛋白质摄入量影响。
3、血清白蛋白在肝脏合成。
临床上尚未发现单纯白蛋白浓度增高的疾病,而以白蛋白浓度降低为多见。
白蛋白浓度降低与总蛋白浓度降低的原因相同。

白蛋白(ALB)测定试剂盒(溴甲酚绿法)适用范围:本产品用于体外定量测定人血清中白蛋白的含量。
1.1规格试剂(R)5×80mL;7×60mL;5×40mL;2×100mL;3×400mL;1×20mL。
校准品(选配):1×3mL。
1.2组成1.2.1 试剂组成1.2.2校准品的组成:单个水平的液体校准品,在水基质中添加牛血清白蛋白(纯度:95%以上),稳定剂0.1%。
定值范围:(40-60)g/L。
2.1 外观液体单试剂:黄绿色液体。
校准品:无色至淡黄色澄清液体。
2.2 净含量液体试剂的净含量不得低于标示体积。
2.3 空白吸光度在37℃、(630nm±10%范围内的)波长,1cm光径条件下,试剂空白吸光度应<0.25 ABS。
2.4 分析灵敏度浓度为40g/L时,吸光度变化范围在(0.4-0.8)ABS之间。
2.5 线性范围测试血清样本,试剂线性在[10.0-60.0]g/L范围内:线性相关系数(r)≥0.990;在[20.1-60.0]g/L范围内,线性偏差应不超过±10%;[10.0-20.0]g/L范围内,线性应在±4.0g/L范围内。
2.6 精密度重复测试浓度在(40.0±5.0)g/L的控制血清,所得结果的重复性(变异系数,CV)应不大于2.0 %。
2.7 批间差测试浓度在(40.0±5.0)g/L的控制血清,批间相对极差应不大于5.0 %。
2.8 准确度相对偏差应不大于 6.0%。
2.9 稳定性2.9.1效期稳定性原包装试剂(含校准品),在(2-8)℃下有效期为18个月,取失效期的试剂盒检测其准确度和线性,试验结果满足2.5、2.8的要求。
2.9.2 开瓶稳定性试剂(含校准品)开瓶后,在(2-8)℃保存,可以稳定14天。
在第15天检测线性和准确度,试验结果满足2.5、2.8的要求。

血清白蛋白ALB溴甲酚绿BCG法测定1.实验原理在pH值4.2时,白蛋白和溴甲酚绿染料结合产生蓝绿色复合物,在630nm处比色,颜色的深度与白蛋白浓度成正比。
pH4.2白蛋白+溴甲酚绿--------------绿色化合物2. 标本采集2.1 病人准备:无特殊要求。
最好用禁食的标本以减少乳糜血的干扰。
2.2 类型:血清、肝素或EDTA血浆。
3. 标本存放留取标本后请尽快分离血清/血浆。
在室温条件下(15~25℃)可以稳定一周,在冰箱保存的条件下(2~8℃)稳定一个月,-20℃保存至少可以稳定3个月。
4. 标本运输室温条件下运输5. 标本拒收标准:细菌污染的不能做测定。
6. 实验材料:6.1 上海奥林巴斯白蛋白测定试剂盒6.1.1 试剂准备:试剂为即用式。
6.1.2 试剂稳定性与贮存:试剂避光保存于2~25℃,若无污染,可稳定至失效期。
试剂有效期为24个月。
试剂不可冰冻。
开盖后应避免污染。
6.1.3 变质指示:当试剂有浊度时,表明有细菌污染,不能继续使用。
6.1.4 注意事项:避免试剂与皮肤及粘膜接触。
6.2 校准品:参见生化检验校准品和质控品.SOP文件6.3 质控品:参见生化检验校准品和质控品.SOP文件7. 仪器:奥林巴斯AU2700生化分析仪8. 操作步骤8.1 项目基本参数:参见生化检验奥林巴斯AU2700生化分析仪项目测定参数.SOP文件8.2仪器操作步骤:参见生化检验奥林巴斯AU2700生化分析仪操作规程.SOP文件9. 检验结果的判断与分析10. 质量控制:在每一批标本中都应把非定值血清水平I 与II质控做为未知标本进行分析,以2S为质控警告限,3S为失控限,绘制质控图,判断是否在控。
质控规则参见生化室室内质控操作规程.SOP文件。
11. 计算方法:以TruCal U复合校准品白蛋白校准值或标准品标准值校准仪器后,在病人结果可报告范围内,仪器直接报告可靠的检测结果。
手工测定计算方法为:Au白蛋白(g/L)= ×校准液浓度As12. 参考值范围成人35~52g/L参考值因性别、年龄、饮食和地域的不同而有所差别。

血清白蛋白测定标准操作规程1 检验申请单独检验项目申请:血清白蛋白测定(缩写ALB);组合项目申请:血生化中肝功能测定项目组合。
临床医生根据需要提出检验申请。
2 标本采集与处理2。
1标本采集2。
1.1常规静脉采血约2ml,不抗凝,置普通试管中。
或采用含分离胶的真空采血管。
2。
1。
2检验申请单和血标本试管标上统一且唯一的标识符。
2。
1.3急诊标本采集后,在检验申请单上填写标本采集时间。
2.1.4标本采集后与检验申请单一起及时运送至检验科。
专人负责标本的接收并记录标本的状态,对不合格标本予以拒收。
2。
1。
5下列标本为不合格标本2。
1。
5.1标本量不足:少于0.3ml的全血标本,或少于0。
1ml的血清或血浆。
2。
1。
5。
2对反应吸光度有干扰的标本,包括严重溶血、严重浑浊的标本。
2。
1.5.3无法确认标本与申请单对应关系的.2。
1。
5。
4其他如标识涂改、标本试管破裂等.2。
2标本保存2.2。
1接收标本后在30min内将标本离心分离出血清.2.2.2标本保存时间:室温(15~25℃)下可稳定一周,普通冰箱中(2~8℃)稳定一个月。
为避免标本中水分挥发使血清浓缩,对保存时间超过1天的标本均加塞密闭或覆盖湿巾。
2.3标本采集的注意事项2.3。
1采血前使受检者保持平静、松弛和空腹状态。
2。
3.2不建议采集抗凝血标本,如果必须使用血浆,推荐的抗凝剂是肝素。
3 方法原理血清中的白蛋白与溴甲酚绿在PH=4.2的条件下结合生成绿色复合物,溶液由黄色变为绿色,其颜色深浅与白蛋白浓度成正比,通过在630nm处测定其吸光度可得出白蛋白的含量。
PH=4.2白蛋白 + 溴甲酚绿—-—-—-------———绿色复合物4 试剂及其他用品4.1试剂:溴甲酚绿法测定白蛋白试剂盒,由北京利德曼生化技术有限公司出品.4。
2试剂盒保存:保存于2~8℃,不开盖情况下至标签的失效期。
开盖后放于仪器的冰箱中至少稳定14天.开盖后避免污染。
变质指示:当试剂有浊度时,表明有细菌污染,不能继续使用.4.3试剂盒准备:液态单试剂型,即开即用,无特殊准备4.4试剂盒主要成分:缓冲液(pH 4.2)50 mmol/L,溴甲酚绿0.25 mmol/L,其中含有稳定剂与保护剂<0.1%。


白蛋白(ALB)测定操作规程(SOP文件)1实验原理和检验目的本试剂按WHO推荐的溴甲酚绿(BCG)法配制。
原理如下:在酸性溶液( pH4.15)中白蛋白与BCG形成绿色络合物,其色泽与白蛋白含量成正比,对照标准可测定其含量。
2标本采集和处理2.1标本种类和采集方法标本:血清,采血后应及时分离,避免溶血,血清在2~8℃稳定3天。
受检者(体检对象或病人)的准备:对于体检对象抽血前应有2周时间保持平时的饮食习惯。
静脉采血:除非是卧床的病人,一般在采血时取坐位。
体位影响水分在血管内外的分布。
2.2标本处理方法标本要放在带盖的容器内以防污染和蒸发。
样品采集后要离心标本,吸出血清。
标本应立即测定。
处理样品时要将其当成生物污染品。
3试剂3.1试剂组成3.2试剂准备试剂为液体单试剂试剂,开瓶即可使用,用后及时置于2~8℃避光保存。
3.3试剂稳定性试剂和标准液在2-8℃避光保存可稳定12个月;试剂开口稳定。
4校准4.1校准品每日进行试剂空白校准操作。
使用朗道(RONDOX)进行全点校准操作。
4.2校准品准备(RONDOX)校准物复溶30分钟,充分溶解混匀后即可使用。
4.3校准品稳定性(RONDOX)冻干校准物2~8℃密闭保存稳定至有效期,复溶后校准物15℃~25℃稳定8小时,2℃~8℃稳定2天,-15℃~-25℃稳定2周。
4.4试剂校准周期推荐校准周期为2天。
当试剂批号更换时应重新校准。
5质控5.1质控品朗道(RONDOX)血清进行室内质控。
5.2可接受性判断质控物的检测值应在给定质控范围,或可以通过参加卫生部室间质评对实验室的运作情况进行系统评估。
5.3质控操作每日进行样本检测之前首先应进行质控操作,以考察系统的在控情况。
如果检测结果符合质控要求则进行样本操作;如果不符合质控要求,则应重复质控操作,以排除可能发生的偶然误差;如果仍不符合质控要求,则应考虑质控品的重新准备、试剂的重新校准或更新、仪器的维护等。
建议在样本的检测过程中和/或结束后再次进行质控操作,以考察样本的检测全过程的在控情况。

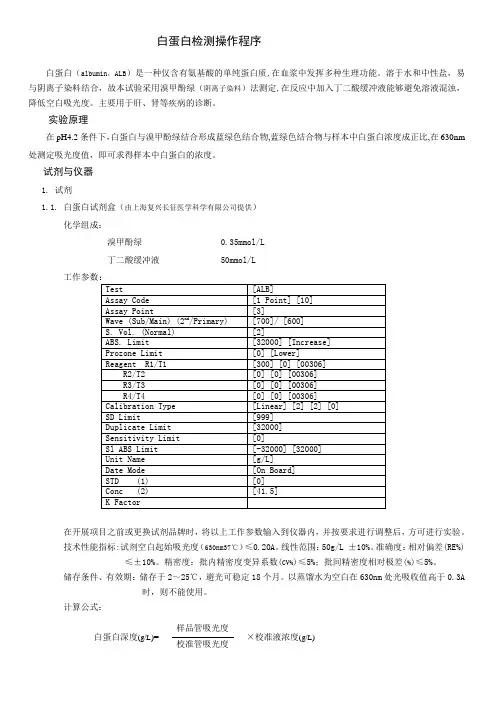
白蛋白检测操作程序白蛋白(albumin ,ALB )是一种仅含有氨基酸的单纯蛋白质,在血浆中发挥多种生理功能。
溶于水和中性盐,易与阴离子染料结合,故本试验采用溴甲酚绿(阴离子染料)法测定,在反应中加入丁二酸缓冲液能够避免溶液混浊,降低空白吸光度。
主要用于肝、肾等疾病的诊断。
实验原理在pH4.2条件下,白蛋白与溴甲酚绿结合形成蓝绿色结合物,蓝绿色结合物与样本中白蛋白浓度成正比,在630nm 处测定吸光度值,即可求得样本中白蛋白的浓度。
试剂与仪器1. 试剂1.1. 白蛋白试剂盒(由上海复兴长征医学科学有限公司提供)化学组成:溴甲酚绿0.35mmol/L 丁二酸缓冲液50mmol/L工作参数:在开展项目之前或更换试剂品牌时,将以上工作参数输入到仪器内,并按要求进行调整后,方可进行实验。
技术性能指标:试剂空白起始吸光度(630nm37℃)≤0.20A 。
线性范围:50g/L ±10%。
准确度:相对偏差(RE%)≤±10%。
精密度:批内精密度变异系数(CV%)≤5%;批间精密度相对极差(%)≤5%。
储存条件、有效期:储存于2~25℃,避光可稳定18个月。
以蒸馏水为空白在630nm 处光吸收值高于0.3A时,则不能使用。
计算公式: 白蛋白深度(g/L )= ×校准液浓度(g/L )样品管吸光度校准管吸光度以上是依据化学实验计算测试结果的公式,全自动分析时将校准液浓度值(Conc值)输入仪器即可。
1.2. 英国郎道(RANDOX)质控品,每次采用正常和异常两个水平,并参照质控品测试要求进行。
1.3. 校准液2. 仪器采用日立(HITACHI)7060型全自动生化分析仪。
选择波长340-800nm之间,能对终点、速率、两点、免疫比浊等方法的实验进行测定。
标本测定程序1. 开机:开机前要加清洗液、上打印纸、接蒸馏水等。
然后打开电源及中文计算机信息管理系统。
2. 试剂准备:开机后将所需试剂置于试剂盘相应位置。



SOP标准操作程序ALB 白蛋白(货号:OSR6102,OSR6202)实验原理:血清白蛋白可用于众多疾病的诊断。
血清白蛋白升高通常见于脱水的。
血清白蛋白降低多见于肾脏疾病,肝脏疾病,感染性疾病,严重的烧伤和癌症。
1965年,Rodkey介绍了用一种中性缓冲液溴甲酚绿(BCG)作为指示剂直接测定血清白蛋白的浓度。
1971年,Doumas等人,对以上方法进行改良,加入了非离子表面活性剂,消除浊度,改善线性与敏感度。
奥林巴斯AU640的白蛋白是Doumas和Rodkey方法的改良方法,应用的是不同的缓冲系统。
在PH值4.0,溴甲酚绿与白蛋白形成强烈的绿色复合物。
白蛋白—溴甲酚绿的复合物在双波长(600/800nm)下的吸光度与白蛋白的浓度成正比。
PH 4.2白蛋白+溴甲酚绿---------------绿色化合物标本:病人准备:无特殊要求。
最好用禁食的标本以减少乳糜血的干扰。
类型:血清、肝素或EDTA血浆,标本最好不要溶血。
留取标本后请尽快分离血清/血浆。
标本稳定性:在室温条件下(15~25℃)可以稳定一周,在冰箱保存的条件下(2~8℃)稳定一个月。
仪器与材料:仪器:奥林巴斯AU640生化分析仪材料:奥林巴斯AU640白蛋白(ALB)参与反应成份的最终浓度:琥珀酸盐缓冲液(PH 4.2)100 mmol/L溴甲酚绿0.2 mmol/L其中含有稳定剂与保护剂。
注意:1.此试剂为体外诊断用。
2.不要入口,吞下有害。
试验用试管的直径在12~16mm。
定标液:奥林巴斯定标液(Cat. No. DR0040)试剂准备:奥林巴斯AU640的ALB试剂是即开即用的。
无需特殊准备。
执行参数(性能参数):以下数据是根据奥林巴斯AU640 ALB试剂已经建立的程序。
重复性:重复性的评估是根据NCCLS推荐的典型方法,AU640批内重复性小于3%,总不精密度小于3%。
用于分析的质控血清和数据处理符合以上的NCCLS的规则。
白蛋白测定的标准程序【目的】体外检测血清白蛋白(ALB )的含量。
【职责】1.实验室工作人员均应熟知并严格遵守本SOP,室负责人监督落实。
2.本SOP的改动,可由任一使用本SOP的工作人员提出,并报经下述人员批准签字:室负责人、科主任。
【标本类型及实验前准备】1.受检者的准备病人空腹12h,不饮酒24h后采集血样。
体检对象抽血前应有两周的的正常状况。
孕妇应在产后或终止哺乳3个月后检验。
此外,有无服用影响的药物以及采血的季节都应做相关记录。
2.静脉采血除非是卧床的病人,一般在采血时取坐位。
体位影响水分在血管内外的分布,会影响测试项目的浓度。
在采血前至少应静坐5分钟,一般从肘静脉取血,使用止血带的时间不超过1分钟,穿刺成功后立即松开止血带。
【仪器设备】东芝TBA-FX8全自动生化分析仪,低速离心机一、检测原理本试剂采用澳甲酚绿染料结合法,即在PH4.2条件下,白蛋白与澳甲酚绿结合形成蓝绿色络合物。
反应形成的蓝绿色络合物与样本中白蛋白浓度成正比。
通过在630nm处测定吸光度值的变化值,即可测得样本中白蛋白的浓度。
二、试剂1.试剂本科使用上海复星长征医学科学有限公司ALB试剂盒,为液体单试剂,其各组分如下:试剂组分澳甲酚绿0.35 mmol/L丁二酸缓冲液50 mmol/L2.校准要求2.1校准品:使用与试剂配套使用的复星长征临床化学校准血清(货号:449 5 0/4 5 9 5 0对测定进行校准。
2. 2校准间隔2. 2. 1试剂批号变更时使用与试剂配套使用的复星长征临床化学校准血清对测定进行校准后再对临床病人样本进行测定。
2. 2. 2室内质量控制出现问题时使用与试剂配套使用的复星长征临床化学校准血清对测定进行校准并确认问题得到解决后方可对临床病人样本进行测定。
三、操作按生化分析仪操作要求结合长征试剂说明书输入测定参数,并按校准、质量控制、样本测定的顺序进行常规测定。
四、计算白蛋白浓度(g/L ) 五、质控程序1. 建议采用朗道水平2(正常范围质控)和 水平3 (病理范围质控)两个水平的血清进行室内质控。
血清白蛋白ALB测定
1 检验目的
指导本室工作人员规范操作本检测项目,确保检测结果的准确。
2 实验原理
在pH值4.2时,白蛋白和溴甲酚绿染料结合产生蓝绿色复合物,在630nm处比色,颜色的深度与白蛋白浓度成正比。
pH4.2
白蛋白+溴甲酚绿--------------绿色化合物
3 标本采集
3.1 病人准备:应禁食抽血.
3.2 类型:血清
3.3 标本存放:留取标本后请尽快分离血清。
在室温条件下(15~25℃)可以稳定一周,在冰箱保存的条件下(2~8℃)稳定一个月,-20℃保存至少可以稳定3个月。
3.4 标本运输:室温条件下运输
3.5 标本拒收标准:细菌污染的不能做测定。
4 实验材料
4.1 试剂:上海复星长征医学科学有限公司ALB试剂盒(沪食药监械(准)字2014第2400166号 YZB/沪 1546-40-2014)4.1.1 试剂组成
溴甲酚绿 0.35mmol/L 丁二酸缓冲液 50 mmol/L
4.1.2 试剂准备:试剂为即用式。
4.1.3 试剂稳定性与贮存:试剂避光保存于2~25℃,若无污染,可稳定至失效期。
试剂有效期为18个月。
4.1.4 变质指示:当试剂有浊度时,表明有细菌污染,不能继续使用。
4.1.5 注意事项:避免试剂与皮肤及粘膜接触。
4.2 校准品:使用上海复星长征医学科学有限公司提供的ALB校准品对自动分析仪进行校准。
4.3 质控品:使用正常值、病理值复合控制品。
5 仪器
AU2700生化分析仪,罗氏P800生化分析仪, 西门子ADVIA-2400生化分析仪,东芝TBA-120生化分析仪
6 操作步骤
6.1 样品的准备:将标好号的样品离心后放到仪器规定的位置。
6.2 试剂的检测:仪器开机后,检查各种试剂的位置,体积等确认无误后方可进行测定。
6.3 项目基本参数:参见生化检验AU2700生化分析仪,罗氏P800生化分析仪, 西门子ADVIA-2400生化分析仪,东芝TBA-120生化分析仪项目测定参数。
6.4仪器操作步骤:参见生化检验AU2700生化分析仪,罗氏P800生化分析仪, 西门子ADVIA-2400生化分析仪,东芝TBA-120生化分析仪操作规程。
7 质量控制
在每一批标本中都应把非定值血清水平I与II质控做为未知标本进行分析,以2S为质控警告限,3S为失控限,绘制质控图,判断是否在控。
8 计算方法
以ALB复合校准品校准仪器后,在病人结果可报告范围内,仪器直接报告可靠的检测结果,以g/L报告
9 参考值范围
成人 37~53g/L
参考值因性别、年龄、饮食和地域的不同而有所差别。
根据好的实验室经验,每个实验室应建立自己的参考值。
我室的参考值:40-55 g/L
10 临床意义
白蛋白是血浆中多种物质重要的结合与运输蛋白,并是维持血浆渗透压的主要组分。
血清白蛋白可用于众多疾病的诊断。
血清白蛋白升高通常见于脱水的。
血清白蛋白降低多见于营养不良、肾脏疾病,肝脏疾病,感染性疾病,严重的烧伤和癌症。
白蛋白的定量测定有助于对肝脏疾病如肝硬化的诊断与监视。
此外,白蛋白量反映了个体的健康与营养状况,因此可用于营养不良的诊断及老年住院患者的预后评估。
11 操作性能
11.1分析灵敏度:4.0g/L样本的吸光度变化率(ΔA)应不小于0.040。
11.2 线性范围:试剂(盒)线性范围应覆盖[0~50]g/L。
a) 线性相关系数(r)应不小于0.990;b) [0~10]g/L 范围内,线性偏差应不超过±4.0g/L;[11~50] U/L 范围内,线性偏差应不超过±10%。
11.3 准确度:相对偏差(B)应不大于±10%。
11.4 精密度:(1)重复性:变异系数(CV)应不大于5%;(2)批间差:相对极差(R)应不大于5%。
12 超出范围结果处理
本法线性上限为50g/L。
如样品测定值超过上限时,应将样品用0.9%氯化钠溶液作1:1稀释,重新测定,结果乘以2。
13 病危报警值的处理
无警告/危急值
14 方法局限性
14.1测定结果的准确性依赖于对所使用分析仪器校准、测定温度和测定时间的控制。
14.2高脂血清会引起测定结果假性升高,测定时应避免使用。
14.3 试剂启用后,在2~10℃避光的条件下可稳定30天。
若试剂混浊,或以水为空白在波长630nm处的吸光度大于0.30时,则不能使用。
15 补救措施
当仪器发生故障时,迅速联系仪器厂家进行维修。
16 参考文献
16.1 叶应妩,王毓山,申子瑜主编·全国临床检验操作规程·中华人民共和国卫生部医政司编·(第四版)
16.2 钱士匀主编.临床生物化学及生物化学检验实验指导.人民卫生出版社,2012年第5版
16.3 府伟灵,徐克前主编.临床生物化学检验.北京.人民卫生出版社,2012年第5版
16.4 试剂说明书。