蛋白质的基本组成单位是氨基酸
- 格式:ppt
- 大小:1.11 MB
- 文档页数:27

生命活动的主要承担者-蛋白质一、选择题(每小题5分,共60分)1. (双选)以下关于蛋白质的叙述,正确的是( )A.氨基酸是组成蛋白质的基本单位B.每种蛋白质都有20种氨基酸组成C.每种蛋白质都含有C、H、O、N、S、P、Fe等元素D.蛋白质是肽链以一定方式形成具有复杂空间结构的高分子化合物【解析】蛋白质的基本组成单位是氨基酸,A项正确;组成生物体蛋白质的氨基酸大约有20种,但每种蛋白质不一定都由20种氨基酸组成,B项错误;每种蛋白质都含有C、H、O、N四种元素,有的蛋白质还含有S或Fe等元素,C项错误;一条或几条肽链以一定方式盘曲折叠所形成的具有复杂空间结构的高分子化合物即为蛋白质,D项正确。
【答案】AD2.下列物质中哪些一定能和双缩脲试剂发生颜色反应( )①胰岛素②生长素③甲状腺激素④抗体⑤抗原⑥生长激素A.②⑤⑥B.③④⑥C.①④⑥ D.①③⑤【解析】双缩脲试剂能与分子中含有两个或两个以上肽键的化合物如多肽、蛋白质等发生紫色反应。
胰岛素、抗体、生长激素都是蛋白质,能与双缩脲试剂发生颜色反应,C正确。
【答案】 C3.下列关于蛋白质的描述,正确的是( )A.都有C、H、O、N、P五种元素B.所有的酶和激素都是蛋白质C.检测蛋白质的试剂是斐林试剂D.生物膜上的载体都是蛋白质【解析】蛋白质主要由C、H、O、N四种元素组成,很多重要的蛋白质还含有P、S两种元素,有的也含微量的Fe、Cu、Zn等元素,A项错误;绝大多数酶是蛋白质,有些激素是蛋白质如胰岛素等,但也有些激素如性激素等不是蛋白质,B项错误;检测蛋白质的试剂是双缩脲试剂,斐林试剂是用来检测还原糖的,C项错误;生物膜上的载体都是蛋白质,D项正确。
【答案】 D4.用化学分析法测得某有机物的化学元素及含量如下表所示,该物质最可能是( )A.核酸 B.脂肪C.糖类 D.蛋白质【解析】核酸由C、H、O、N、P五种元素组成,A项错误;脂肪和糖类都只含有C、H、O 三种元素,B、C项错误;所有蛋白质都含有C、H、O、N四种元素,有些蛋白质含有S、Fe 等元素,该化合物含有Fe元素,最可能是血红蛋白,D项正确。

蛋白质的基本组成单位是
氨基酸是组成蛋白质的基本单位。
蛋白质是以氨基酸为基本单位构成
的生物高分子。
蛋白质分子上氨基酸的序列和由此形成的立体结构构成了
蛋白质结构的多样性。
蛋白质具有一级、二级、三级、四级结构,蛋白质
分子的结构决定了它的功能。
氨基酸分子的羧基,脱去一分子水而连接起来,这种结合方式叫做脱
水缩合。
缩合反应在羧基和氨基之间形成的连接两个氨基酸分子的键叫做
肽键。
一个氨基酸分子的氨基和蛋白质用约20种氨基酸作原料,在细胞
质中的核糖体上,将氨基酸分子互相连接成肽链。
扩展资料
蛋白质结构:一级结构:氨基酸残基在蛋白质肽链中的排列顺序称为
蛋白质的一级结构,每种蛋白质都有唯一而确切的氨基酸序列;二级结构:蛋白质分子中肽链并非直链状,而是按一定的规律卷曲或折叠形成特定的
空间结构,这是蛋白质的二级结构;
三级结构:在二级结构的基础上,肽链还按照一定的空间结构进一步
形成更复杂的三级结构;四级结构:具有三级结构的多肽链按一定空间排
列方式结合在一起形成的聚集体结构称为蛋白质的四级结构。
如血红蛋白
由4个具有三级结构的多肽链构成。

氨基酸分子量与种类氨基酸是构成蛋白质的基本组成单位,每个氨基酸分子由一个氨基(NH2)基团和一个羧基(COOH)基团以及一个中心的碳原子连接而成。
此外,氨基酸还与一个侧链基团连在一起,侧链基团的不同决定了氨基酸的特性和性质。
目前已知的氨基酸种类有20种,它们在生物体内发挥重要的生物功能,包括构建蛋白质、参与代谢和信号传导等。
不同的氨基酸有不同的分子量,本文将对氨基酸的种类和分子量进行详细介绍。
首先是氨基酸的种类。
氨基酸可根据它们的侧链基团的特性分为两类:极性氨基酸和非极性氨基酸。
根据侧链基团是否含有电离性基团,极性氨基酸可以进一步分为两类:酸性氨基酸和碱性氨基酸。
酸性氨基酸包括谷氨酸(Glu)和天冬氨酸(Asp),它们的侧链含有羧基(COOH)基团。
碱性氨基酸包括精氨酸(Arg)、赖氨酸(Lys)和组氨酸(His),它们的侧链含有氨基(NH2)基团。
非极性氨基酸包括甘氨酸(Gly)、丙氨酸(Ala)、缬氨酸(Val)、亮氨酸(Leu)、异亮氨酸(Ile)、脯氨酸(Pro)、甲硫氨酸(Met)、苏氨酸(Ser)、色氨酸(Trp)、胱氨酸(Cys)和苯丙氨酸(Phe)等。
极性氨基酸包括丝氨酸(Ser)、苏氨酸(Thr)、天冬氨酸(Asp)、谷氨酸(Glu)、赖氨酸(Lys)、精氨酸(Arg)、酪氨酸(Tyr)和色氨酸(Trp)等。
接下来是氨基酸的分子量。
不同氨基酸的分子量不同,可以通过计算氨基酸的分子式中各元素的相对原子质量来得到。
氨基酸的分子式通常由化学符号和一个下标表示,下标表示氨基酸的位置,例如甘氨酸(Gly)的分子式为NH2CH2COOH。
根据氨基酸的分子式,可以计算出它们的分子量。
下面列举其中几种氨基酸的分子量:甘氨酸(Gly)的分子量为75.07克/摩尔。
丙氨酸(Ala)的分子量为89.09克/摩尔。
谷氨酸(Glu)的分子量为147.13克/摩尔。
天冬氨酸(Asp)的分子量为133.10克/摩尔。

生物化学思考题蛋白质1、蛋白质含量的测定方法有哪些?答:蛋白质含量的测定方法主要有:(1)凯氏定氮法:蛋白质含量=蛋白质含N量×6.25(2)紫外比色法(3)双缩脲法(4)Folin—酚法(5)考马斯亮兰G—250比色法2、蛋白质的基本组成单位是什么?蛋白质经过怎样处理才可产生这些基本组成单位?答:蛋白质的基本组成单位是氨基酸。
蛋白质经过如下三种处理均可产生氨基酸基本单位:(1)酸水解:常用 6 mol/L的盐酸或4mol/L的硫酸在105-110℃ 20小时左右。
(2)碱水解:一般用5 mol/L氢氧化钠煮沸10-20小时。
(3)酶水解:已有十多种蛋白水解酶,如胰蛋白酶、糜蛋白酶、热激蛋白酶等。
反应条件温和,酶水解时间长,反应不完全。
3、已知末端α-COOH,pK3.6,末端α-NH3+pK8.0 ε-NH+3pK10.6。
计算Ala-Ala-Lys-Ala的等电点。
4、简述蛋白质一级结构的测定顺序。
答:测定蛋白质一级结构的先后顺序为:(1)测定蛋白质分子中多肽链的数目。
(2)拆分蛋白质分子的多肽链。
(3)断开链内二硫键。
(4)分析每条多肽链的氨基酸组成比及数目。
(5)鉴定多肽链的N、C瑞残基。
(6)裂解多肽成小的肽段。
(7)测各肽段的氨基酸序列。
(8)重建完整多肽链的一级结构。
(9)确定二硫键的位置。
5、从热力学上考虑,一个多肽的片段在什么情况下容易形成α-螺旋,是完全暴露在水的环境中还是完全埋藏在蛋白质的非极性内部?为什么?答:当多肽片断完全埋藏在蛋白质的非极性内部时,容易形成氢键。
因为在水的环境中,肽键的C=O和N-H基团能和水形成氢键,亦能彼此之间形成氢键,这两种情况在自由能上没有差别。
因此相对的说,形成α-螺旋的可能性较小。
而当多肽片段在蛋白质的非极性内部时,这些极性基团除了彼此之间形成氢键外,不再和其它基团形成氢键,因此有利于α-螺旋的形成。
6、某氨基酸溶于pH7的水中,所得氨基酸溶液的pH为6,问此氨基酸的pI是大于6、等于6还是小于6?氨基酸在固体状态时以两性离子形式存在。

第一章蛋白质第一节蛋白质的基本组成单位---氨基酸(一)氨基酸的种类蛋白质是重要的生物大分子,其组成单位是氨基酸。
组成蛋白质的氨基酸有20种,均为α-氨基酸。
每个氨基酸的α-碳上连接一个羧基,一个氨基,一个氢原子和一个侧链R 基团。
20种氨基酸结构的差别就在于它们的R基团结构的不同。
根据20种氨基酸侧链R基团的极性,可将其分为四大类:非极性R基氨基酸(8种);不带电荷的极性R基氨基酸(7种);带负电荷的R基氨基酸(2种);带正电荷的R基氨基酸(3种)。
(二)氨基酸的性质氨基酸是两性电解质。
由于氨基酸含有酸性的羧基和碱性的氨基,所以既是酸又是碱,是两性电解质。
有些氨基酸的侧链还含有可解离的基团,其带电状况取决于它们的pK值。
由于不同氨基酸所带的可解离基团不同,所以等电点不同。
除甘氨酸外,其它都有不对称碳原子,所以具有D-型和L-型2种构型,具有旋光性,天然蛋白质中存在的氨基酸都是L-型的。
酪氨酸、苯丙氨酸和色氨酸具有紫外吸收特性,在280nm处有最大吸收值,大多数蛋白质都具有这些氨基酸,所以蛋白质在280nm处也有特征吸收,这是紫外吸收法定量测定蛋白质的基础。
氨基酸的α-羧基和α-氨基具有化学反应性,另外,许多氨基酸的侧链还含有羟基、氨基、羧基等可解离基团,也具有化学反应性。
较重要的化学反应有:(1)茚三酮反应,除脯氨酸外,所有的α-氨基酸都能与茚三酮发生颜色反应,生成蓝紫色化合物,脯氨酸与茚三酮生成黄色化合物。
(2)Sanger反应,α-NH2与2,4-二硝基氟苯作用产生相应的DNB-氨基酸。
(3)Edman反应,α-NH2与苯异硫氰酸酯作用产生相应的氨基酸的苯氨基硫甲酰衍生物(PIT-氨基酸)。
Sanger反应和Edmen反应均可用于蛋白质多肽链N端氨基酸的测定。
氨基酸通过肽键相互连接而成的化合物称为肽,由2个氨基酸组成的肽称为二肽,由3个氨基酸组成的肽称为三肽,少于10个氨基酸肽称为寡肽,由10个以上氨基酸组成的肽称为多肽。

名词解释氨基酸名词解释:氨基酸氨基酸是生物体内一类至关重要的有机化合物,它们既是蛋白质的基本组成单位,也是许多生物化学反应和生理功能的重要参与者。
每个氨基酸分子都包含一个中心的碳原子(称为α-碳),这个碳原子连接着四个不同的基团:一个氨基(-NH2,碱性)、一个羧基(-COOH,酸性)、一个氢原子以及一个侧链R基团。
侧链R基团使得不同类型的氨基酸具有各自独特的化学性质。
目前已知有20种常见的标准氨基酸,这些氨基酸通过肽键相互连接形成多肽链,进一步折叠成具有特定三维结构的蛋白质,执行生命体中各种复杂的生物学功能,如催化、运输、信号转导等。
拓展知识:1. 必需氨基酸与非必需氨基酸:-必需氨基酸:人体不能自身合成或合成速度不足以满足机体需求,必须从食物中摄取的氨基酸,包括亮氨酸、异亮氨酸、赖氨酸、蛋氨酸、苯丙氨酸、苏氨酸、色氨酸、缬氨酸和组氨酸(对于婴幼儿而言)。
-非必需氨基酸:人体能够在一定条件下自行合成,无需专门从食物中获取的氨基酸。
2. 条件必需氨基酸:在某些特殊情况下,如疾病状态下,有些氨基酸虽然在正常生理条件下是非必需的,但在特定时期内可能成为必需氨基酸,例如精氨酸和胱氨酸。
3. 氨基酸代谢:氨基酸不仅是构成蛋白质的原料,而且在体内参与多种代谢途径,如能量代谢、尿素循环(处理含氮废物)及作为神经递质、激素和抗氧化剂的前体物质等。
4. 氨基酸分析:在医学、营养学和生物科学领域,通过对氨基酸含量、比例和代谢状态的分析,可以评估个体营养状况、诊断遗传代谢病或研究蛋白质功能等。
5. 氨基酸序列与蛋白质功能:蛋白质的功能与其氨基酸序列密切相关,特定序列决定了蛋白质的空间构象,从而影响其生物活性。
通过基因编码的氨基酸序列变化可能导致蛋白质功能的变化,这是遗传变异和进化的重要基础。
6.氨基酸分类:与羟基酸类似,氨基酸可按照氨基连在碳链上的不同位置而分为α-,β-,γ-,w-...氨基酸,但经蛋白质水解后得到的氨基酸都是α-氨基酸或亚氨基酸,而且仅有二十二种,包括甘氨酸、丙氨酸、缬氨酸、亮氨酸、异亮氨酸、甲硫氨酸(蛋氨酸)、脯氨酸、色氨酸、丝氨酸、酪氨酸、半胱氨酸、苯丙氨酸、天门冬酰胺、谷氨酰胺、苏氨酸、天冬氨酸、谷氨酸、赖氨酸、精氨酸、组氨酸等。

氨基酸基本单位一、引言氨基酸是构成蛋白质的基本单位,具有重要的生物学功能。
本文将从氨基酸的定义、结构、分类、生理功能等多个方面进行详细介绍。
二、氨基酸定义氨基酸是由一个羧基(-COOH)和一个氨基(-NH2)组成的有机化合物,它们通过一个碳原子(C)相互连接。
这个碳原子被称为α-碳原子。
除了羧基和氨基外,α-碳原子还与一个侧链(R)相连。
三、氨基酸结构1. 羧基:羧基是由一个碳原子和两个氧原子组成的官能团。
在pH值为7.4时,羧基带负电荷。
2. 氨基:氨基是由一个氮原子和两个氢原子组成的官能团。
在pH值为7.4时,氨基带正电荷。
3. α-碳原子:α-碳原子是连接羧基和侧链的中心碳原子。
4. 侧链:侧链是与α-碳原子相连的不同官能团,不同种类的侧链决定了不同种类的氨基酸。
四、氨基酸分类1. 按侧链的性质分类:(1) 极性氨基酸:侧链中含有极性官能团,可与水分子形成氢键,如丝氨酸、谷氨酸等。
(2) 非极性氨基酸:侧链中不含有极性官能团,不能与水分子形成氢键,如甘氨酸、丙氨酸等。
(3) 硫代氨基酸:侧链中含有硫原子,如半胱氨酸、甲硫氨酸等。
2. 按人体内是否能合成分类:(1) 必需氨基酸:人体无法自行合成,必须从食物中摄入,如异亮氨酸、苯丙氨酸等。
(2) 非必需氨基酸:人体可以自行合成,不需要从食物中摄入,如天冬氨酸、谷氨酰胺等。
五、生理功能1. 构成蛋白质:多个氨基酸通过肽键连接形成多肽和蛋白质。
蛋白质是人体各种组织和器官的重要构成物质。
2. 能量来源:氨基酸可以通过脱羧反应产生能量,被身体利用。
3. 生物合成:氨基酸可以作为生物合成的原料,如谷氨酰胺可以合成核苷酸等。
4. 信号分子:一些特定的氨基酸可以作为神经递质和荷尔蒙,参与人体的调节和控制。
六、结论氨基酸是构成蛋白质的基本单位,具有多种生理功能。
不同种类的氨基酸由于侧链的差异而具有不同的性质和功能。
了解氨基酸的结构、分类和生理功能对于深入了解蛋白质及其作用机制具有重要意义。

填空题21.在各种蛋白质分子中,含量比较相近的元素是(N),测得某蛋白质样品含氮量为15.2克,该样品白质含量应为(95)克。
22.组成蛋白质的基本单位是(氨基酸),它们的结构均为(L-α-氨基酸),它们之间靠(肽)键彼此连接而形成的物质称为(肽)。
23.由于氨基酸既含有碱性的氨基和酸性的羧基,可以在酸性溶液中带(正)电荷,在碱性溶液中带(负)电荷,因此,氨基酸是(两性)电解质。
当所带的正、负电荷相等时,氨基酸成为(兼性)离子,此时溶液的pH值称为该氨基酸的(等电点(pI))。
24.决定蛋白质的空间构象和生物学功能的是蛋白质的(一)级结构,该结构是指多肽链中(氨基酸残基)的排列顺序。
25.蛋白质的二级结构是蛋白质分子中某一段肽链的(局部)构象,多肽链的折叠盘绕是以(肽键平面(肽单元))为基础的,常见的二级结构形式包括(α-螺旋),(β-折叠),(β-转角)和(无规卷曲)。
26.维持蛋白质二级结构的化学键是(氢键),它们是在肽键平面上的(-CO-)和(—NH—)之间形成。
27.稳定蛋白质三级结构的次级键包括(氢键),(离子键(盐键)),(疏水键)和(范德华力)等。
28.构成蛋白质的氨基酸有(20)种,除(甘氨酸)外都有旋光性。
其中碱性氨基酸有(精氨酸),(组氨酸),(赖氨酸)。
酸性氨基酸有(天冬氨酸),(谷氨酸)。
29.电泳法分离蛋白质主要根据在某一pH值条件下,蛋白质所带的净电荷(不同)而达到分离的目的,还和蛋白质的(形状)及(分子量大小)有一定关系。
30.蛋白质在pI时以(兼性)离子的形式存在,在pH>pI的溶液中,大部分以(负)离子形式存在,在pH<pI时,大部分以(正)离子形式存在。
31.将血浆蛋白质在pH8.6的巴比妥缓冲液中进行醋酸纤维素薄膜电泳,它们向(正)极泳动,依次分为(清蛋白),(α1-球蛋白),(α2-球蛋白),(β-球蛋白),(γ-球蛋白)。
32.在pH6.0时,将一个丙、精、谷三种氨基酸的混合液进行纸上电泳,移向正极的是(谷氨酸),移向负极的是(精氨酸),留在原点的是(丙氨酸)。
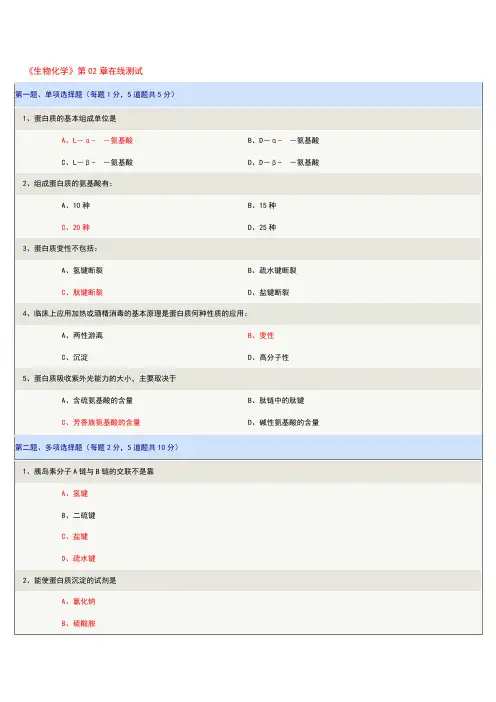
《生物化学》第02章在线测试第一题、单项选择题(每题1分,5道题共5分)1、蛋白质的基本组成单位是A、L-α--氨基酸B、D-α--氨基酸C、L-β--氨基酸D、D-β--氨基酸2、组成蛋白质的氨基酸有:A、10种B、15种C、20种D、25种3、蛋白质变性不包括:A、氢键断裂B、疏水键断裂C、肽键断裂D、盐键断裂4、临床上应用加热或酒精消毒的基本原理是蛋白质何种性质的应用:A、两性游离B、变性C、沉淀D、高分子性5、蛋白质吸收紫外光能力的大小,主要取决于A、含硫氨基酸的含量B、肽链中的肽键C、芳香族氨基酸的含量D、碱性氨基酸的含量第二题、多项选择题(每题2分,5道题共10分)1、胰岛素分子A链与B链的交联不是靠A、氢键B、二硫键C、盐键D、疏水键2、能使蛋白质沉淀的试剂是A、氯化钠B、硫酸胺C、硫酸钠D、水3、下列有关肽的叙述,正确的是A、肽是两个以上氨基酸借肽键连接而成的化合物B、组成肽的氨基酸分子都不完整C、多肽与蛋白质分子之间无明确的分界线D、氨基酸一旦生成肽,完全失去其原有的理化性质4、蛋白质分子中不含下列哪种氨基酸:A、半胱氨酸B、鸟氨酸C、丝氨酸D、瓜氨酸5、蛋白质的等电点是A、蛋白质溶液的pH等于7时溶液的pH值B、蛋白质溶液的pH等于时溶液的pHC、蛋白质的正电荷和负电荷相等时溶液的pH值D、蛋白质分子呈兼性离子状态时溶液的pH值第三题、判断题(每题1分,5道题共5分)1、变性的蛋白质一定沉淀,而沉淀的蛋白质也一定是变性的。
正确错误2、蛋白质有紫外光吸收特性。
正确错误3、氢键也是蛋白质分子的主键正确错误4、具有三级结构的蛋白质均具有生物活性正确错误《生物化学》第01章在线测试第一题、单项选择题(每题1分,5道题共5分)1、磷酸是结合在核苷酸的什么位置而形成多磷酸核甘A、5/-磷酸基B、2/-羟基C、3/-羟基D、以上都对2、不是RNA的基本组成单位的是:A、AMPB、GMPC、CMPD、cAMP3、DNA的基本组成单位下列哪个除外A、dAMPB、dCMPC、dGMPD、dUMP4、tRNA的二级结构是:A、双螺旋结构B、片状结构C、无规卷曲结构D、三叶草结构5、DNA变性后对紫外光的吸收应该是A、增加B、减少C、不受影响D、都有可能第二题、多项选择题(每题2分,5道题共10分)1、如果一DNA溶液在260nm处紫外吸收值明显增强,不能说明溶液中的DNA发生了A、复性B、变性C、杂交D、彻底分解2、关于DNA变性温度下列不正确的叙述是:A、变性温度Tm值主要与DNA分子中的A和T的含量有关B、A和T 含量高,DNA分子稳定,Tm就越高C、G和C含量高,DNA分子不稳定,Tm值就低D、G和C含量高,DNA分子稳定,Tm值就高3、核酸具有紫外吸收能力的原因是A、嘌呤环中有共轭双键B、嘧啶环中有共轭双键C、嘌呤和嘧啶中有硫原子D、嘌呤和嘧啶连接了核糖4、有关 mRNA 的不正确解释是A、大多数真核生物的 mRNA 都有 5ˊ末端的多聚腺苷酸结构B、所有生物的 mRNA 分子中都有较多的稀有碱基C、原核生物 mRNA 的 3ˊ末端是 7- 甲基鸟嘌呤D、大多数真核生物 mRNA 5ˊ端为 m7Gppp G 结构5、有关 tRNA 分子的正确解释是A、tRNA 是分子量最小的RNAB、tRNA 的功能主要在于结合蛋白质合成所需要的各种辅助因子C、tRNA 3ˊ末端有氨基酸臂D、反密码环中的反密码子的作用是结合 DNA 中相互补的碱基第三题、判断题(每题1分,5道题共5分)1、DNA都是双链结构,而RNA都是单链结构正确错误2、核小体是由DNA和组蛋白构成的正确错误3、tRNA的二级结构是三叶草结构正确错误4、即使RNA分子结构中有双链区,RAN仍是单链结构正确错误5、变性的DNA复性的标志之一是对紫外线的吸收增加正确错误《生物化学》第04章在线测试第一题、单项选择题(每题1分,5道题共5分)1、L-乳酸脱氢酶催化L-型乳酸脱氢产生丙酮酸的作用属于:A、绝对特异性B、相对特异性C、立体异构特异性D、酶的特异性2、关于酶的辅助因子错误的是:A、与酶蛋白以共价键紧密结合的称为辅基B、与酶蛋白以非共价键疏松结合的称为辅酶C、辅基和辅酶在化学本质上没有严格界限D、辅助因子的作用是在决定酶催化反应的特异性3、矩形双曲线是下列何种因素对酶催化作用的影响曲线A、酶浓度B、底物浓度C、温度D、pH4、下列关于温度对酶活性影响的说法,哪项是正确的:A、体内所有酶的最适温度均为37℃B、酶活性最大的时温度为酶的最适温度C、酶的最适温度为酶的特征性常数D、低温和高温一样都能破坏酶结构5、关于酶的抑制剂下列错误的是:A、能特异性的使酶活性降低或丧失的物质统称为抑制剂B、与酶分子的必需基团共价键结合的为不可逆抑制C、与酶分子以非共价键方式结合的为可逆性抑制剂D、酒精消毒就是对细菌酶抑制的典型例子第二题、多项选择题(每题2分,5道题共10分)1、关于同工酶是错误的是:A、分子结构相同B、理化性质相同C、免疫学特性相同D、催化功能相同2、下列酶蛋白与辅助因子的论述正确的是A、酶蛋白与辅助因子单独存在时无催化活性B、一种酶只能与一种辅助因子结合形成全酶C、一种辅助因子只能与一种酶结合成全酶D、酶蛋白决定酶促反应的特异性3、含有维生素B2的辅酶是A、NAD+B、FADC、TPPD、FMN4、下列哪些抑制作用不属于竞争性抑制作用A、砷化合物对流基酶的抑制作用B、敌敌畏对胆碱酯酶的抑制作用C、磺胺类药物对细菌二氢叶酸合成酶的抑制作用D、氰化物对细胞色素氧化酶的抑制作用5、关于酶原与酶原的激活不正确的有A、体内所有的酶在初合成时均以酶原的形式存在B、酶原的激活是酶的共价修饰过程C、酶原的激活过程也就是酶被完全水解的过程D、酶原激活过程的实质是酶的活性中心形成或暴露的过程第三题、判断题(每题1分,5道题共5分)1、乳酸脱氢酶同工酶对同一底物有不同的Km值正确错误2、有机磷中毒的机理是对胆碱酯酶活性中心中的羟基的不可逆性抑制正确错误3、酶在反应前后质量不变是酶突出的特征正确错误4、酶的必需基团都是在酶的活性中心内,所以才重要。

氨基酸与缩写氨基酸是构成蛋白质的基本组成单位,它们通过肽键连接在一起形成多肽链或蛋白质。
氨基酸的结构由一个氨基组和一个羧基组组成,其中羧基组与氨基组通过肽键连接。
氨基酸的分类可以按照它们在水溶液中的性质来划分,包括极性氨基酸、非极性氨基酸和带电氨基酸。
极性氨基酸可进一步分为带正电氨基酸、带负电氨基酸和非带电氨基酸。
以下是一些常见氨基酸及其缩写:1. 丙氨酸 (Ala):是一种非极性氨基酸,其侧链只包含一个甲基基团。
2. 谷氨酸 (Glu):是一种带负电氨基酸,其侧链包含一个羧基和一个丙二酰基。
3. 苏氨酸 (Ser):是一种极性氨基酸,其侧链包含一个羟基。
4. 苯丙氨酸 (Phe):是一种非极性氨基酸,其侧链包含一个苯环。
5. 色氨酸 (Trp):是一种非极性氨基酸,其侧链包含一个吲哚环。
6. 天冬酰胺 (Asn):是一种极性氨基酸,其侧链包含一个甲酰胺基。
7. 苏胺酸 (Thi):是一种极性氨基酸,其侧链包含一个硫基和一个羧基。
8. 缬氨酸 (Val):是一种非极性氨基酸,其侧链包含一个异戊基。
9. 虾青素基氨酸 (Ast):是一种非常罕见的氨基酸,其侧链包含一个虾青素基团。
10. 酪氨酸 (Tyr):是一种带芳香环的氨基酸,其侧链包含一个苯基和一个羟基。
以上仅是一部分常见氨基酸及其缩写,氨基酸种类繁多,每种氨基酸都对蛋白质的结构和功能起到重要作用。
它们的不同侧链特性使得蛋白质能够具有不同的功能和结构稳定性。
除了用于构建蛋白质,氨基酸还参与许多生物过程,如作为神经递质、合成抗体、体内能量的来源等。
各种氨基酸的组合和排序决定了蛋白质的特定序列和结构,进而影响蛋白质的功能和性质。
了解氨基酸的结构和性质对于理解蛋白质的组成和功能至关重要。
研究人员通过对氨基酸的改变和组合进行实验,可以深入了解蛋白质的结构与功能之间的关系。
对氨基酸的深入研究有助于发展新的药物、设计新的蛋白质工具和开发新的生物技术应用。

【高三】2021届高考生物第一轮必修一氨基酸知识点复习1.氨基酸是组成蛋白质的基本单位,大约有20种,其中必需氨基酸有8种,非必需氨基酸有12种。
2.氨基酸的结构。
至少一个氨基和一个羧基连接到同一个碳原子。
氨基酸的结构和功能不同。
21世纪教育网要点归纳1.类型构成蛋白质的氨基酸约有20种,包括必需氨基酸和非必需氨基酸。
必需氨基酸:人体内有8种(婴儿9种),必须从外界获取。
非必需氨基酸:可以通过其他化合物转化而来。
(2) 21世纪教育网的特点①氨基酸分子中的氨基和羧基数目至少一个,也可以是几个,因为r基中可能含有氨基或羧基。
② 在构成蛋白质的氨基酸中,有一个氨基和一个羧基与同一个碳原子相连,否则它们就不是构成蛋白质的氨基酸。
例如:H2NCH2CH2COOH。
③不同的氨基酸分子,具有不同的r基,这是氨基酸分类的依据。
例如甘氨酸的r基是―h,丙氨酸的r基是―ch3。
情绪膨胀基因表达时,从信使rna上的起始密码子开始,两个起始密码子分别对应甲硫氨酸和缬氨酸,即蛋白质中第一个氨基酸定为两种中其中之一,所以可以推测绝大多数蛋白质含“s”元素,但并非所有的蛋白质都含“s”,基本元素为c、h、o、n,特征元素为“s”。
经典启蒙1关于生物体内氨基酸的叙述错误的是( )a、组成蛋白质的氨基酸分子的一般结构式是b.人体内氨基酸的代谢终产物是水、二氧化碳和尿素c、人体内的所有氨基酸都可以相互转化d.两个氨基酸通过脱水缩合形成二肽分析氨基酸可分为两类:必需氨基酸(不能在体内转化,必须从食物中获得)和非必需氨基酸(可以在体内转化)。
答案c酪氨酸几乎不溶于水,精氨酸很容易溶于水。
这种差异取决于()a.两者r基团组成的不同b.两者的结构完全不同c、酪氨酸的氨基和精氨酸的羧基答案a独立梳理1.氨基酸、多肽、肽键、肽链和蛋白质的关系氨基酸是蛋白质分子的基本单位。
多个氨基酸分子脱水并缩合形成多肽。
肽键是连接多肽结构中两个氨基酸残基的化学键。
第三章蛋白质习题一、选择题1.组成蛋白质的基本单位是:a.L—α—氨基酸b.D—α—氨基酸c.L—β—氨基酸d.D—β—氨基酸e.以上都不对2.关于下列氨基酸的说明,哪个是不正确的:a.酪氨酸和苯丙氨酸都含有苯环b.苏氨酸和丝氨酸都含有羟基c.亮氨酸和缬氨酸都是分枝氨基酸d.脯氨酸和酪氨酸都是非极性氨基酸e.组氨酸和色氨酸都是杂环氨基酸3.下列哪种氨基酸溶液不能引起偏振光的旋转?a.丙氨酸b.甘氨酸c.亮氨酸d.丝氨酸e.缬氨酸4.属于亚氨基酸的是:a.组氨酸b.脯氨酸c.精氨酸d.赖氨酸e.蛋氨酸5.下列氨基酸在生理pH范围内缓冲能量最大的是:a.Gl y b Hi s c.Cys d.A sp e.Gl u 6.哪一种蛋白质组分在280nm处,具有最大的光吸收?a.色氨酸的吲哚环b.酪氨酸的苯酚基c.苯丙氨酸的苯环d.半胱氨酸的巯基e.肽链中的肽键7.有一混合蛋白质溶液,其pI值分别为4.6、5.0、5.3、6.7、7.3,电泳时欲使其中四种泳向正极,缓冲液pH应该是多少?a.4.0 h.5.0 c.6.0 d.7.0 e.8.08.与茚三酮反应呈黄色的氨基酸是:a.苯丙氨酸b.酪氨酸c.色氨酸d.αβ组氨酸e.脯氨酸9.关于蛋白质构象的下列描述,其中正确的是:a.指手性碳原子上某一原子或基团的方位b.指几何异构体中顺式或是反式c.指多肽链中一切原子(基团)随。
—碳原子旋转,盘曲面产生的空间排布d.指原子或基团改变涉及共价键的生成或断开e.不涉及蛋白质分子中次级键的断裂与生成10.维持蛋白质二级结构的主要化学键是:a.盐键b.疏水键c.二硫键d.氢键e.范德华力11.蛋白质的构象特征主要取决于:a.氨基酸的组成、顺序和数目b.氢键、盐键、范德华力和疏水力c.温度、pH和离子强度等环境条件d.肽链间及肽链内的二硫键e.各氨基酸之间的肽键12.下列哪种方法可用于测定蛋白质分子质量?a.SDS聚丙烯酰胺凝胶电泳法b.280/260nm紫外吸收比值c.凯氏定氮法d.荧光分光光度法e.Folin酚试剂法13.蛋白质的一级结构是指:a.蛋白质含氨基酸的种类和数目b.蛋白质中氨基酸的排列顺序c.蛋白质分子多肽链的折叠盘曲d.包括A、B和Ce.以上都不对14.氨基酸在等电点时,具有的特点是:a.不带正电荷b.不带负电荷c.a+bd.溶解度最大e.在电场中不泳动15.在一个肽平面中含有的原子数为:a.4 b.5 c.616.具有四级结构的蛋白质是:a.胰岛素b.核糖核酸酶 c.血红蛋白d.肌红蛋白.e.胰凝乳蛋白酶17.氨基酸与蛋白质共同的理化性质:a.胶体性质b.两性性质d.变性性质e.双缩脲反应18.具有四级结构的蛋白质特征是:a.分子中必定含有辅基b.含有两条或两条以上的多肽链c.每条多肽链都具有独立的生物:d.依靠肽键维持结构的稳定性e.以上都不是19.在具有四级结构的蛋白质分子中,每个具有三级结构的多肽链是:a.辅基b.辅酶c.亚基d.寡聚体e.肽单位20.关于蛋白质亚基的描述,其中正确的是:a.一条多肽链卷曲成螺旋结构b.两条以上多肽链卷曲成二级结构c.两条以上多肽链与辅基结合成蛋白质d.每个亚基都有各自的三级结构.e.以上都是正确的21.蛋白质一级结构与功能关系的特点是:a.相同氨基酸组成的蛋白质功能一定相同b.一级结构相近的蛋白质,其功能类似性越大c.一级结构中任何氨基酸的改变,其生物活性立即丧失d.不同生物来源的同种蛋白质,其一级结构完全相同e.一级结构中任何氨基酸残基的改变,都不会影响其功能22.蛋白质溶液的稳定因素是:a.蛋白质溶液是真溶液b.蛋白质在溶液中做布朗运动c.蛋白质分子表面带有水化膜和同性电荷d.蛋白质溶液的黏度大e.以上都不是23..关于蛋白质在等电点时的特性描述,哪项是错误的?a.导电性最小b.溶解度最小c.黏度减小d.电泳迁移率最小e.以上都不对24.令A、B、C、D四种蛋白质的混合液,等电点分别为:5.O、8.6、6.8、9.2,在pH8.6的条件下用电泳分离,四种蛋白质电泳区带自正极开始的排列顺序为:a.A、C、B\D b.A、B、C、D c.D、B、C、Ad.C、B、A、D e.B、D、C、A25.关于变性蛋白质的叙述,哪项是正确的?a.变性蛋白质,失去营养作用b.变性蛋白质的溶解度增加d.变性蛋白质旋光性增加d.变性蛋白质不能再复原e.以上都不对26.蛋白质变性不包括:a.氢键断裂b.肽键断裂 c.疏水键断裂d.盐键断裂e.范德华力破坏27.盐析法沉淀蛋白质的原理是:a.中和电荷,破坏水化膜b.与蛋白质结合成不溶性蛋白盐c.次级键断裂,蛋白质构象改变d.调节蛋白质溶液的等电点e.以上都不是二、是非题1.组成蛋白质的20种氨基酸都有一个不对称性的(1--碳原子,所以都有旋光性。
福建医科大学生物化学练习题第一章蛋白质的结构与功能一、选择题:1.蛋白质的基本组成单位是:A.L-α-氨基酸B.L-β-氨基酸 C.D-α-氨基酸D.D-β-氨基酸E.D-γ-氨基酸2.天然蛋白质分子量由多少种氨基酸组成?A.16种B.20种C.22种D.32种E.64种3.蛋白质的含氮量约为:A.16%B.6.25%C.18%D.20%E.30%4.关于蛋白分子中的肽键,下列哪项叙述是错误的?A.肽键具有部分双键的性质B.肽键及其相关的6个原子位于一个刚性平面C.肽键是连接氨基酸的主键D.与肽键相连的α-碳原子两侧的单键可以自由旋转E.肽键可以自由旋转5.蛋白质分子中α-螺旋构象的特点是:A.肽键平面呈螺旋状B.多为左手螺旋C.靠盐键(离子键)维持稳定D.螺旋方向与长轴垂直E.一般为右手螺旋6.下列哪种结构不属于蛋白质的二级结构?A.α-螺旋B.β-折叠C.β-转角D.无规卷曲E.右手双螺旋7.具有四级结构的蛋白质的特征是A.分子中必定含有辅基B.每条多肽链都具有完整的生物学活性C.由两条或两条以上具有完整三级结构的多肽链借次级键缔合而成D.四级结构的稳定性由肽键维持E.蛋白质必定经过合成后修饰8.蛋白质变性是由于A.氨基酸的组成改变B.氨基酸的排列顺序改变C.肽键的断裂D.蛋白质空间结构被破坏E.蛋白质分子的表面电荷及水化膜破坏9.有关分子伴侣的叙述正确的是A.可以促进肽链的正确折叠B.可以维持蛋白质的空间构象C.在二硫键的正确配对中不起作用D.在亚基聚合时发挥重要作用E.可以促进蛋白质的变性10.胰岛素分子中的共价键除肽键外还有?A.离子键B.二硫键C.氢键D.疏水键E.范德华引力二、名词解释:肽单元蛋白质变性三、问答1.简述蛋白质α-螺旋的特征。
2.举例说明蛋白质空间结构与功能关系。
四、参考答案(一)选择题1.A2.B3.A4.E5.E6.E7.C8.D9.A 10.B第二章核酸的结构与功能一、选择题1.遗传物质一般储存在:A.核糖核酸B.脱氧核糖核酸 C.组蛋白D.核蛋白E.非组蛋白2.碱基能较强吸收A.可见光B.540nm波长的光C.280nm的紫外光D.红外光E.260nm的紫外光3.核酸中核苷酸的连接方式为A.2′,3′-磷酸二酯键B.3′,5′-磷酸二酯键C.2′,5′-磷酸二酯键D.糖苷键E.肽键4.下列哪种碱基只存在于mRNA而不存在于DNA中A.腺嘌呤B.胞嘧啶C.鸟嘌呤D.尿嘧啶E.胸腺嘧啶5.双链DNA分子中,如果A的含量为20%,则T的含量为:A.20%B.30%C.40%D.50%E.60%6.Watson—Crick的DNA结构模型A.是一个三链结构B.双股链的走向是反向平行的C.嘌呤和嘌呤配对,嘧啶和嘧啶配对D.碱基之间共价结合E.磷酸戊糖主链位于螺旋内侧7.维持DNA双螺旋结构横向稳定的主要作用力是:A.盐键B.疏水键C.氢键D.碱基堆积力E.共价键8.核小体串珠状结构的珠状核心蛋白质是A.H2A、H2B、H3、H各一分子B.H2A、H2B、H3、H4各二分子C.H1组蛋白与140~145碱基对DNAD.非组蛋白E.H2A、H2B、H3、H4各四分子9.密码子存在于A.DNAB.rRNAC.mRNAD.hnRNAE.tRNA10.DNA变性时发生的变化A.两条单链形成右手双螺旋B.高色效应C.低色效应D.共价键断裂E.形成超螺旋二、名词解释:核小体核酸杂交三、问答题:1.试述DNA双螺旋结构模式的要点。
蛋白质基本单位结构通式蛋白质是生物体内最为重要的大分子类别之一,它在细胞内执行了多种生物学功能。
蛋白质的基本单位结构通式被称为氨基酸。
氨基酸是蛋白质的构成单体,它们由氨基羧基(酸性)和氨基(碱性)组成,而且具有一个唯一的侧链。
20种常见的氨基酸通过其侧链的差异性,分为两大类:极性氨基酸和非极性氨基酸。
极性氨基酸在水中具有亲和力,而非极性氨基酸则不具有这种特性。
氨基酸可以通过两个分子之间的酯键形成肽链。
当两个氨基酸通过酯键连接在一起时,形成了二肽。
当三个氨基酸连接在一起时,就形成了三肽,以此类推。
当氨基酸的数目超过10个时,该链被称为多肽;而当氨基酸的数目超过100个时,该链就被称为蛋白质。
具有多个肽链的复杂蛋白质被称为亚单位。
蛋白质的基本单位结构通式中,还存在着二级、三级和四级结构。
这些结构是蛋白质在氨基酸链之上的组织形式,它们的存在决定了蛋白质的功能。
以下是蛋白质的基本单位结构通式的详细解释:1.一级结构:一级结构是蛋白质最基本的结构,它由氨基酸链的线性顺序组成。
氨基酸的顺序决定了蛋白质的特定序列,这对于蛋白质的功能至关重要。
2.二级结构:二级结构是指氨基酸链上的局部区域的方式。
常见的二级结构形式有α-螺旋和β-折叠。
α-螺旋是由螺旋形状的氨基酸链组成的,而β-折叠则是由平行或反平行的氨基酸链组成的。
这些二级结构在蛋白质的稳定性和功能方面起着重要的作用。
3.三级结构:三级结构是指蛋白质中各个氨基酸链之间的空间排列方式。
这种结构是通过氨基酸间的非共价键形成的,包括疏水相互作用、静电吸引力、氢键和疏水相互作用等。
通过这些作用,蛋白质的非极性残基通常位于内部,而极性残基则位于外部。
4.四级结构:四级结构是指多肽链之间的相对排列。
一些蛋白质由多个氨基酸链组成,并通过非共价键相互结合在一起。
这些链之间的相互作用形成了蛋白质的四级结构。
蛋白质的基本单位结构通式体现了氨基酸的组合方式和各个氨基酸链之间的空间排列方式。
《蛋白质的基本组成单位是氨基酸》说课稿尊敬的各位评委老师:大家好!今天我说课的题目是《蛋白质的基本组成单位是氨基酸》。
下面我将从教材分析、学情分析、教学目标、教学重难点、教法与学法、教学过程以及教学反思这几个方面来展开我的说课。
一、教材分析本节课选自_____教材_____章节。
蛋白质作为生命活动的主要承担者,在生物学中具有极其重要的地位。
而氨基酸作为蛋白质的基本组成单位,是理解蛋白质结构和功能的基础。
教材在这部分内容的编排上,先介绍了氨基酸的结构特点,然后通过氨基酸形成蛋白质的过程,逐步深入地阐述了蛋白质的结构层次和多样性。
这一编排符合学生的认知规律,有助于学生逐步构建起关于蛋白质的知识体系。
二、学情分析授课对象为_____年级的学生,他们已经在之前的学习中积累了一定的生物学基础知识,如细胞的结构和功能等。
但是对于微观层面的分子结构和化学反应,学生的理解可能还存在一定的困难。
同时,这个阶段的学生具有较强的好奇心和求知欲,喜欢通过实验和探究活动来获取知识。
三、教学目标1、知识目标(1)学生能够说出氨基酸的结构特点,包括组成元素、基本结构等。
(2)理解氨基酸的种类,能够区分必需氨基酸和非必需氨基酸。
(3)掌握氨基酸形成蛋白质的过程,包括脱水缩合反应和肽键的形成。
2、能力目标(1)通过观察氨基酸的结构模型,培养学生的观察能力和空间想象能力。
(2)通过对氨基酸形成蛋白质过程的分析,提高学生的逻辑思维能力和分析问题的能力。
3、情感目标(1)激发学生对生物学的兴趣,培养学生探索生命奥秘的热情。
(2)让学生认识到生命的复杂性和多样性,培养学生尊重生命、热爱生命的情感。
四、教学重难点1、教学重点(1)氨基酸的结构特点。
(2)氨基酸形成蛋白质的过程。
2、教学难点(1)氨基酸结构通式的理解。
(2)脱水缩合反应的过程和肽键的形成。
五、教法与学法1、教法(1)直观演示法:通过展示氨基酸的结构模型、动画等,帮助学生直观地理解氨基酸的结构和形成蛋白质的过程。
构成蛋白质的20种氨基酸蛋白质是生物体内最基本的组成部分之一,它们在细胞中扮演着重要的角色。
构成蛋白质的基本单位是氨基酸。
目前已知有20种氨基酸参与蛋白质合成,它们分别是丙氨酸、丝氨酸、脯氨酸、天冬氨酸、谷氨酸、苏氨酸、甘氨酸、异亮氨酸、亮氨酸、酪氨酸、赖氨酸、缬氨酸、异亮氨酸、亮氨酸、酪氨酸、赖氨酸、缬氨酸、苏氨酸、甘氨酸、异亮氨酸、亮氨酸。
1. 丙氨酸:丙氨酸是一种非极性氨基酸,它在蛋白质中起到了增强结构稳定性的作用。
2. 丝氨酸:丝氨酸是一种极性氨基酸,它在蛋白质中起到了增加溶解度和稳定蛋白质结构的作用。
3. 脯氨酸:脯氨酸是一种非极性氨基酸,它在蛋白质中起到了增加溶解度和稳定蛋白质结构的作用。
4. 天冬氨酸:天冬氨酸是一种极性氨基酸,它在蛋白质中起到了增加溶解度和稳定蛋白质结构的作用。
5. 谷氨酸:谷氨酸是一种非极性氨基酸,它在蛋白质中起到了增加溶解度和稳定蛋白质结构的作用。
6. 苏氨酸:苏氨酸是一种非极性氨基酸,它在蛋白质中起到了增加溶解度和稳定蛋白质结构的作用。
7. 甘氨酸:甘氨酸是一种非极性氨基酸,它在蛋白质中起到了增加溶解度和稳定蛋白质结构的作用。
8. 异亮氨酸:异亮氨酸是一种非极性氨基酸,它在蛋白质中起到了增加溶解度和稳定蛋白质结构的作用。
9. 亮氨酸:亮氨酸是一种非极性氨基酸,它在蛋白质中起到了增加溶解度和稳定蛋白质结构的作用。
10. 酪氨酸:酪氨酸是一种非极性氨基酸,它在蛋白质中起到了增加溶解度和稳定蛋白质结构的作用。
11. 赖氨酸:赖氨酸是一种极性氨基酸,它在蛋白质中起到了增加溶解度和稳定蛋白质结构的作用。
12. 缬氨酸:缬氨酸是一种非极性氨基酸,它在蛋白质中起到了增加溶解度和稳定蛋白质结构的作用。
13. 异亮氨酸:异亮氨酸是一种非极性氨基酸,它在蛋白质中起到了增加溶解度和稳定蛋白质结构的作用。
14. 亮氨酸:亮氨酸是一种非极性氨基酸,它在蛋白质中起到了增加溶解度和稳定蛋白质结构的作用。